Настоящее изобретение относится к технике хранения газа, содержащего метан в качестве основного компонента, и касается также применения его в качестве топливного бака в автомобиле на газообразном топливе.
Для хранения газа, содержащего метан в качестве основного компонента, обычно в качестве его адсорбента предлагают использовать, главным образом, активированный уголь.
Однако активированный уголь обладает лишь ограниченной газоадсорбционной способностью по отношению к своему объему. Для повышения этой газоадсорбционной способности на единицу объема предлагалось также формовать активированный уголь в сплошной адсорбент, но даже в этом случае достигалась незначительная степень улучшения. С другой стороны, в настоящее время в продаже имеется активированный уголь /активированный уголь с большой удельной поверхностью/, имеющий сравнительно большую площадь поверхности и, следовательно, более высокую газоадсорбционную способность на единицу объема. Однако такие улучшенные активированные угли являются дорогостоящими.
Более того, в отношении адсорбции и десорбции газа активированный уголь ввиду значительного изменения в диаметре его пор обладает возрастающе-нестабильной адсорбционно-десорбционной характеристикой при повторении адсорбции и десорбции газа. Это означает, что активированный уголь создает проблему при повторном использовании.
Ввиду вышеизложенного главная цель изобретения состоит в предложении улучшенной технологии, которая при небольших затратах обеспечивает большую объемную способность по адсорбции и хранению газа и также лучшую повторяемость газоадсорбционной характеристики. Другой целью является создание автомобиля на газообразном топливе, использующего эту технологию
Еще одной целью изобретения является создание нового металлоорганического комплекса, пригодного в качестве вещества для адсорбции и удержания газа, например, метана для использования, например, в устройстве для хранения газа и автомобиле на газообразном топливе.
Краткое содержание изобретения
Вышеуказанная цель достигается благодаря изобретению, изложенному в пункте 1 формулы. А именно, согласно изобретению, предлагается устройство для использования при хранении газа, содержащего метан в качестве основного компонента, которое включает в себя отверстие для входа и выхода из него газа, подлежащего хранению, газонепроницаемый механизм, способный поддерживать газ в сжатом состоянии внутри контейнера, сосуд под давлением, в котором можно постоянно поддерживать нормальную температуру; сосуд под давлением с помещенным в него металлорганическим комплексом, имеющим одномерную канальную структуру.
При вышеуказанной конструкции в сосуд под давлением этого устройства помещен металлоорганический комплекс, имеющий одномерную канальную структуру. В этот сосуд вводят газ, содержащий метан в качестве основного компонента, для адсорбции и удержания или хранения на металлоорганическом комплексе, помещенном в этот сосуд. Это хранение происходит в виде адсорбции и удерживания газа внутри одномерной канальной структуры комплекса и оно возможно при нормальной температуре. Кроме того, для высвобождения газа из устройства /т. е. десорбции газа из металлоорганического комплекса/ открывают, например, клапан на выходном отверстии для понижения давления внутри сосуда под давлением, благодаря чему газ десорбируется с металлоорганического комплекса и выпускается из устройства для использования с определенной целью. В вышеизложенном случае металлоорганический комплекс спрессован до высокой плотности с тем, чтобы обеспечить высокую адсорбционную способность. Этот комплекс соответственно имеет более высокую газоадсорбционную удерживающую способность на единицу объема по сравнению, например, с вышеупомянутым активированным углем.
Металлоорганический комплекс предпочтительно содержит, по крайней мере, один комплекс, выбранный из группы, состоящей из терефталевая кислота - медь, фумаровая кислота - медь, 1,4-транс-циклогександикарбоновая кислота - медь, бифенилдикарбоновая кислота - медь, фумаровая кислота - молибден, 1,4-транс-циклогександикарбоновая кислота - молибден, бифенилдикарбоновая кислота - молибден, терефталевая кислота - хром, фумаровая кислота - хром, 1,4-транс-циклогександикарбоновая кислота - хром, бифенилдикарбоновая кислота - хром, терефталевая кислота - родий, фумаровая кислота - родий, 1,4-транс-циклогександикарбоновая кислота - родий, бифенилдикарбоновая кислота - родий, терефталевая кислота - палладий, фумаровая кислота - палладий, 1,4-трансциклогександикарбоновая кислота - палладий, бифенилдикарбоновая кислота - палладий, терефталевая кислота - вольфрам, фумаровая кислота - вольфрам, 1,4-транс-циклогександикарбоновая кислота - вольфрам и бифенилдикарбоная кислота - вольфрам.
Благодаря использованию металлорганического комплекса вышеупомянутого вида с его отличной способностью адсорбировать метан в условиях повышенного давления и нормальной температуры газ можно эффективно хранить в сравнительно ограниченном объеме.
Устройство для хранения газа согласно изобретения может быть использовано в автомобиле на газообразном топливе, имеющем двигатель внутреннего сгорания, работающий на газе, поступающем из устройства для хранения газа.
В автомобиле на газообразном топливе чем меньше объем бака для топливного газа, тем лучше. В таком случае устройство для хранения газа согласно изобретению удовлетворяет этому требованию, а в автомобиле на газовом топливе, в котором используется это компактное устройство для хранения газа, можно сберечь большое пространство для размещения иных частей автомобиля, чем бак для хранения газообразного топлива.
Конкретнее в этом автомобиле на газообразном топливе можно в сравнительно небольшом объеме при относительно низком давлении хранить большое количество топливного газа с тем, чтобы этот автомобиль мог за один раз пробегать большее расстояние несмотря на наличие в нем компактного топливного бака. Это усовершенствование будет способствовать популярности автомобилей на газообразном топливе, что в конце концов будет содействовать ограничению загрязнения окружающей среды благодаря использованию автомобиля чистой энергии.
Металлоорганический комплекс, используемый в этом автомобиле, предпочтительно представляет собой, по крайней мере, один комплекс дикарбоновой кислоты с медью, выбранный из группы, состоящей из терефталевая кислота - медь, фумаровая кислота - медь, 1,4-транс-циклогександикарбоновая кислота - медь, бифенилдикарбоновая кислота - медь, фумаровая кислота - молибден, 1,4-транс-циклогександикарбоновая кислота - молибден, бифенилдикарбоновая кислота - молибден, терефталевая кислота - хром, фумаровая кислота - хром, 1,4-транс-циклогександикарбоновая кислота - хром, бифенилдикарбоновая кислота - хром, терефталевая кислота - родий, фумаровая кислота - родий, 1,4-трансциклогександикарбоновая кислота - родий, бифенилдикарбоновая кислота - родий, терефталевая кислота - палладий, фумаровая кислота - палладий, 1,4-трансциклогександикарбоновая кислота-палладий, бифенилдикарбоновая кислота - палладий, терефталевая кислота - вольфрам, фумаровая кислота - вольфрам, 1,4-транс-циклогександикарбоновая кислота - вольфрам и бифенилдикарбоновая кислота - вольфрам.
При этой особенности можно в автомобиле эффективно использовать выдающуюся способность по хранению газа, предоставляемую вышеуказанным металлорганическим комплексом, и достигнуть вышеупомянутых преимуществ.
При способе хранения газа согласно настоящему изобретению необходимый газ адсорбируют и удерживают в условиях повышенного давления и нормальной температуры на адсорбционно-удерживающем веществе, содержащем в качестве основного компонента металлоорганический комплекс с одномерной канальной структурой.
При вышеуказанном способе хранения газа для его адсорбции и хранения используют адсорбционно-удерживающее вещество, которое в качестве основного компонента включает в себя металлоорганический комплекс с одномерной канальной структурой и содержит, по крайней мере, один комплекс, выбранный из группы, состоящей из терефталевая кислота - медь, фумаровая кислота - медь, 1,4-транс-циклогександикарбоновая кислота - медь, бифенилдикарбоновая кислота - медь, фумаровая кислота - молибден, 1,4-транс-циклогександикарбоновая кислота - молибден, бифенилдикарбоновая кислота - молибден, терефталевая кислота - хром, фумаровая кислота - хром, 1,4-транс-циклогександикарбоновая кислота - хром, бифенилдикарбоновая кислота - хром, терефталевая кислота - родий, фумаровая кислота - родий, 1,4-транс-циклогександикарбоновая кислота-родий, бефенилдикарбоновая кислота - родий, терефталевая кислота - палладий, фумаровая кислота - палладий, 1,4-транс-циклогександикарбоновая кислота - палладий, бифенилдикарбоновая кислота - палладий, терефталевая кислота - вольфрам, фумаровая кислота - вольфрам, 1,4-транс-циклогександикарбоновая кислота - вольфрам и бифенилдикарбоновая кислота - вольфрам. Такой металлоорганический комплекс, как указанный выше, адсорбирует и удерживает необходимый газ, содержащий метан в качестве основного компонента, и эта адсорбция может происходить в условиях повышенного давления и нормальной температуры. Этот факт заново открыт данным изобретателем. При этом способе можно эффективно использовать такое выдающееся свойство этого комплекса.
Кроме того, этот металлоорганический комплекс можно сравнительно легко получить из легкодоступных и недорогих материалов, так что этот способ обеспечивает значительную экономическую выгоду. Более того, поскольку можно иметь комплекс со сравнительно высокой плотностью благодаря его соответствующему формованию, его объемная адсорбционная способность может быть значительно увеличена, так что этот способ обеспечивает также дополнительное преимущество в смысле способности хранить газ. Кроме того, диаметр пор комплекса довольно стабилен по всей структуре комплекса. Следовательно, этот комплекс может избавить от такой проблемы, как сохранение на комплексе ненамеренно адсорбированного иного газового компонента, чем необходимый газовый компонент, что имело бы результатом ухудшение повторяемости.
Что касается вещества для адсорбции и удерживания метана, также относящегося к настоящему изобретению, то это вещество получают путем смешивания дикарбоновой кислоты, растворенной в органическом растворителе, с раствором, содержащим, по крайней мере, одну соль, выбранную из группы солей меди, молибдена, хрома, родия, вольфрама и палладия. Вещество в качестве своего основного компонента содержит металлоорганический комплекс, имеющий одномерную канальную структуру.
Металлоорганический комплекс, используемый в веществе для адсорбции и удерживания метана, получают путем смешивания дикарбоновой кислоты, растворенной в органическом растворителе, с раствором, содержащим, по крайней мере, одну соль, выбранную из группы солей меди, молибдена, хрома, родия, вольфрама и палладия.
Металлоорганический комплекс, используемый в веществе для адсорбции и удерживания метана, предпочтительно получают путем смешивания дикарбоновой кислоты, растворенной в органическом растворителе, с добавкой, содержащей, по крайней мере, одну органическую кислоту, выбранную из группы, состоящей из формиата, ацетата и трифторацетата и пропионовой кислоты, и затем смешивания этой смеси с раствором, содержащим, по крайней мере, одну соль, выбранную из группы, состоящей из солей меди, молибдена, хрома, родия, вольфрама и палладия.
При вышеизложенном, вводя добавку в раствор дикарбоновой кислоты, можно стабилизировать кристаллическую структуру, благодаря чему можно контролировать адсорбционную способность. Кроме того, поскольку вышеописанный процесс синтеза является сравнительно простым, то можно получать недорогой комплекс.
Более того, путем выбора надлежащего вида дикарбоновой кислоты можно регулировать диаметр пор, благодаря чему можно получить адсорбционно-удерживающее вещество, наилучшим образом соответствующее свойствам данного газа.
Раствором, содержащим соль меди, может быть раствор, содержащий, по крайней мере, один вид соли, выбранной из группы, состоящей из формиата меди, ацетата меди, сульфата меди, нитрата меди и карбоната меди. В качестве раствора, содержащего соль хрома, соль молибдена и соль родия, предпочитается раствор ацетата хрома, ацетата молибдена или ацетата родия. В качестве раствора, содержащего соль вольфрама или соль палладия, предпочитается раствор их ацетата или хлорида.
Вышеупомянутые растворы - недорогие и легкие в обращении, что полезно для крупномасштабного синтеза.
Более того, металлорганический комплекс, используемый согласно изобретению, может содержать комплекс бифенилкарбоновой кислоты с медью, полученный путем смешивания раствора бифенилдикарбоновой кислоты с раствором, содержащим соль двухвалентной меди.
Вышеупомянутый комплекс дикарбоновой кислоты с медью сам по себе является новым веществом.
Этот новый комплекс бифенилдикарбоновой кислоты с медью далее будет описан с использованием в качестве примера комплекса 4,4'-бифенилдикарбоновой кислоты с медью
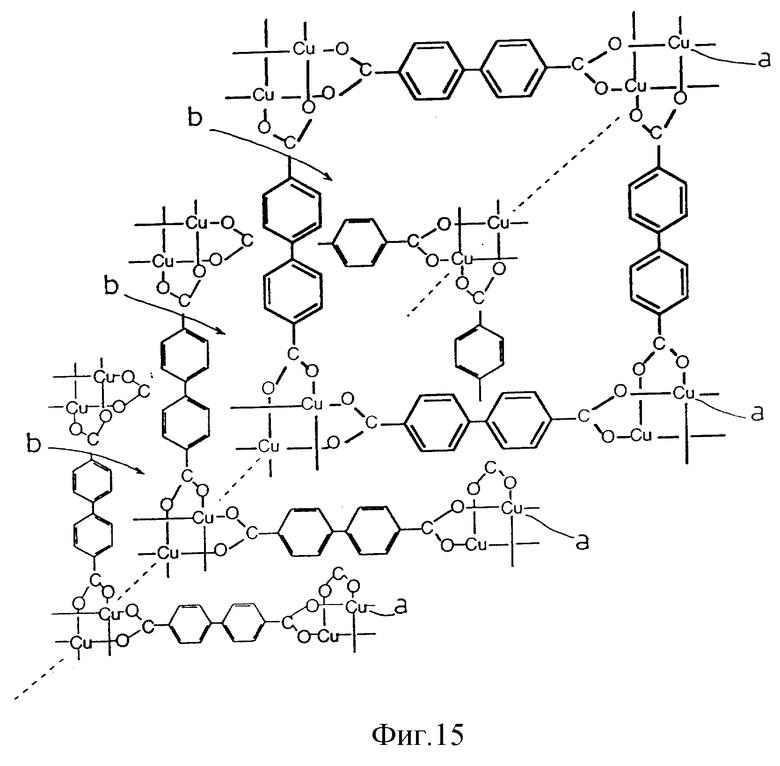
Конкретнее, основываясь на измерении его магнитной восприимчивости, полагают, что этот новый комплекс 4,4'-бифенилдикарбоной кислоты с медью имеет плоскую или двухкамерную решетчатую структуру, в которой некоторое количество двухядерных структур с дикарбоновыми кислотами, координированными вокруг иона меди, связаны друг с другом посредством связи их примыкающих ионов меди через дикарбоновую кислоту. Ионы меди присутствуют в точках пересечения a, a, a. . . решетки. Кроме того, согласно данным о структурах различных известных комплексов меди /фиг. 15/, полученным при структурном анализе с моделированием на компьютере в соответствии с методом молекулярной динамики /МД/, множество вышеописанных двухмерных структур, как полагают, должны быть кристаллизованы таким образом, чтобы соответствующие точки пересечения вертикально уложенных решеток находились по вертикали вровень с промежутками b, b, b, ... между примыкающими точками пересечения, образуя вместе одномерную канальную структуру.
Кроме того, исследовали свойства нового комплекса 4,4'-бифенилдикарбоновой кислоты с медью. Как показало это исследование, комплекс обладает адсорбционной способностью по отношению к топливным газам, как например, метану, этану, пропану и бутану и к кислороду, азоту и т.п. Более того, согласно рентгенограмме, полученной с него, расстояние между соседними ионами меди составляет приблизительно  /фиг. 16/.
/фиг. 16/.
Предполагается, что благодаря вышеописанной канальной структуре комплекс 4,4'-бифенилдикарбоновой кислоты с медью обеспечивает газоадсорбционный эффект, а также каталитическое действие для осуществления изомеризации, полимеризации, окисления и восстановления различных соединений, введенных в канальную структуру.
Раствор 4,4'-бифенилдикарбоновой кислоты может содержать добавку из органической кислоты.
Такой комплекс 4,4'-бифенилдикарбоновой кислоты с медью может быть легко получен смешиванием раствора бифенилдикарбоновой кислоты с раствором, содержащим соль двухвалентной меди. При проведении такой реакции с введением заранее добавки из органической кислоты в раствор 4,4'-бифенилдикарбоновой кислоты величину pH можно регулировать для приведения конкретных условий реакции в соответствие с выбранной солью меди, с тем, чтобы можно было при таких мягких условиях реакции эффективно получать комплекс 4,4'-бифенилдикарбоновой кислоты с медью и, в конце концов получать недорогой продукт.
Органической кислотой может быть, по крайней мере, один вид кислоты, выбранной из группы, состоящей из формиата, ацетата, трифторацетата и пропионовой кислоты, а растворителем в растворе, содержащим соль меди, спирт, как например, метанол, этанол, пропанол или органический растворитель, как, например, бензол, толуол, ацетонитрил, тетрагидрофуран, диметилсульфоксид, диметилформамид, диметилацетамид, гексан, ацетон и т.п.
Если органическая кислота относится, по крайней мере, к одному виду, выбранному из группы, состоящий из формиата, ацетата, трифторацетата и пропионовой кислоты, то едва ли возможно неблагоприятное воздействие на вышеописанную реакцию.
Например, даже если солью меди будет, по крайней мере, один вид соли, выбранной из группы, состоящей из фумарата меди и ацетата меди, едва ли будет какое-либо неудобство, которое привело бы к разрушению образовавшегося комплекса бифенилдикарбоновой кислоты с медью. Между прочим, если солью меди является неорганическая соль меди, как, например, сульфат меди, нитрат меди и карбонат меди, то это едва ли окажет неблагоприятное влияние на вышеописанную реакцию. Кроме того, реакция синтеза может быть осуществлена без введения добавки.
Для вышеуказанной реакции в качестве растворителя в растворе, содержащем соль меди, пригодны спирт, как например, метанол, этанол, пропанол или органический растворитель, как например, бензол, толуол, ацетонитрил, тетрагидрофуран, диметилсульфоксид, диметилформамид, гексан, ацетон и т.п., так что комплекс бифенилдикарбоновой кислоты с медью может быть эффективно получен при мягких условиях реакции. Следовательно, комплекс бифенилдикарбоновой кислоты с медью может быть получен при низких затратах и тем самым служить созданию недорого продукта.
Бифенилдикарбоновой кислотой также предпочтительно является 4,4'-бифенилдикарбоновая кислота.
При использовании этой 4,4'-бифенилдикарбоновой кислоты становится возможным успешное получение комплекса бифенилдикарбоновой кислоты с медью, имеющего максимальную адсорбционную способность.
Другие признаки изобретения изложены в зависимых пунктах формулы. При этих дополнительных признаках можно достигнуть еще более благоприятных функций и результатов.
Согласно вышеописанным различным признакам настоящего изобретения стало возможным создание устройства для хранения газа, обладающего большей объемной емкостью по газу, а также автомобиля на газообразном топливе, имеющего конструктивные преимущества.
Более того, стало также возможным создание вещества для адсорбции и удерживания метана, которое обладает большей объемной адсорбционной способностью и лучшей повторяемостью и которое также можно легко и недорого синтезировать, а также способа хранения газа, обладающего такими особенностями.
Кроме того, при этом способе хранения газа благодаря соответствующему выбору вида дикарбоновой кислоты, составляющей комплекс, возможно высокоэффективное хранение газа, соответствующее конкретному виду используемого газа.
Дополнительные и другие цели, признаки и результаты изобретения станут более очевидными из следующего более подробного описания вариантов осуществления изобретения со ссылкой на прилагаемые чертежи
Кратное описание чертежей
Фиг. 1 - схематическое изображение автомобиля на газообразном топливе.
Фиг. 2 - схематическое изображение, иллюстрирующее предполагаемую структуру комплекса терефталевой кислоты с медью.
Фиг. 3 - график, иллюстрирующий газоадсорбционную способность /изотерму адсорбции/ комплекса терефталевой кислоты с медью.
Фиг. 4 - график, иллюстрирующий газоадсорбционную способность /изотерму адсорбции/ комплекса фумаровой кислоты с медью.
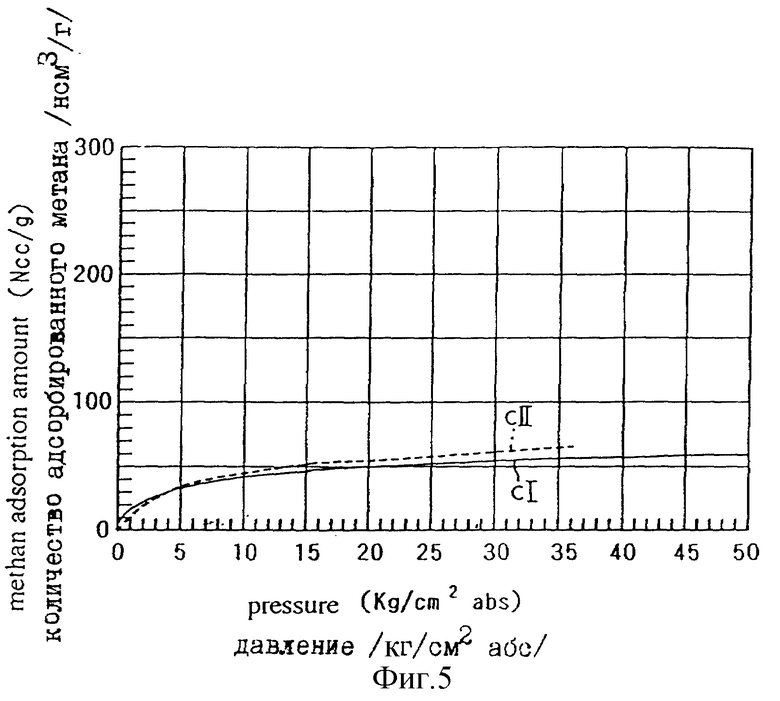
Фиг. 5 - график, иллюстрирующий газоадсорбционную способность /изотерму адсорбции/ комплекса 1,4-циклогександикарбоновой кислоты с медью.
Фиг. 6 - график, иллюстрирующий газоадсорбционную способность /изотерму адсорбции/ комплекса нафталиндикарбоновой кислоты с медью.
Фиг. 7 - график, иллюстрирующий газоадсорбционную способность /изотерму адсорбции/ комплекса фенилендикарбоновой кислоты с медью.
Фиг. 8 - график, сравнительно иллюстрирующий газоадсорбционные способности /изотермы адсорбции/ комплекса терефталевой кислоты с медью, различных формованных продуктов из него и активированного угля.
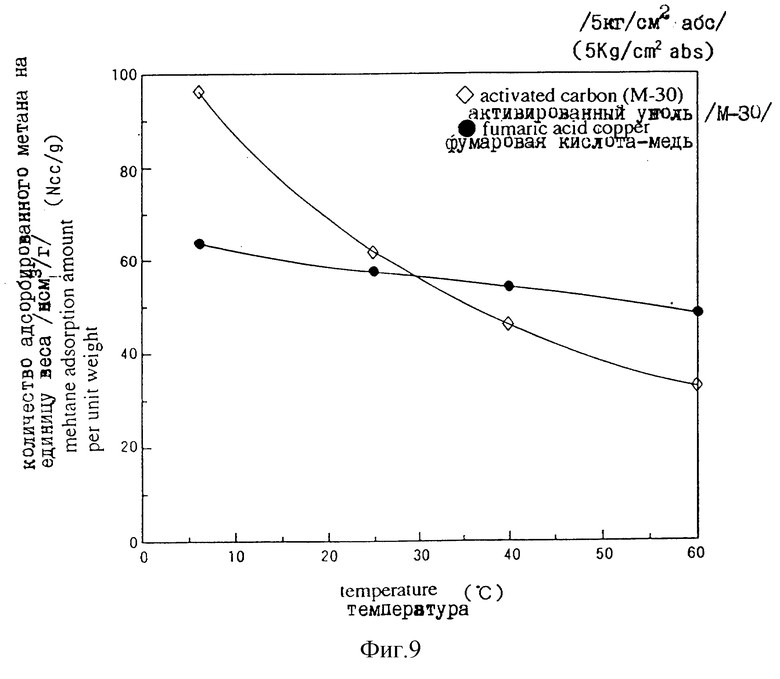
Фиг. 9 - график, сравнительно иллюстрирующий газоадсорбционные способности /изобары адсорбции/ на единицу веса комплекса терефталевой кислоты с медью и активированного угля в зависимости от температуры.
Фиг. 10 - график, сравнительно иллюстрирующий газоадсорбционные способности /изобары адсорбции/ на единицу объема комплекса терефталевой кислоты с медью и активированного угля в зависимости от температуры.
Фиг. 11 - график, иллюстрирующий адсорбционную способность по топливному газу /изотерму адсорбции/ комплекса терефталевой кислоты с медью.
Фиг. 12 - график, иллюстрирующий адсорбционную способность по топливному газу /изотерму адсорбции/ комплекса фумаровой кислоты с медью.
Фиг. 13 - график, иллюстрирующий газоадсорбционную способность /изотерму адсорбции/ комплекса фумаровой кислоты с медью для другого газа.
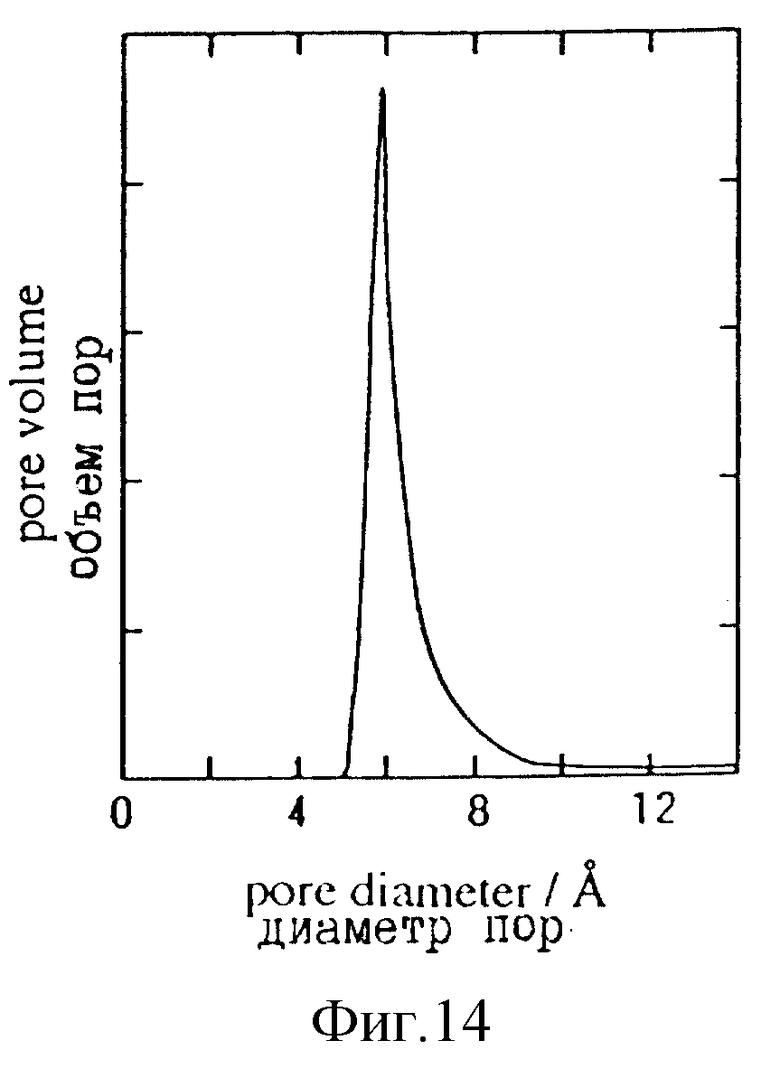
Фиг. 14 - график, иллюстрирующий распределение диаметра пор в комплексе терефталевой кислоты с медью
Фиг. 15 - схематическое изображение трехмерной структуры комплекса 4,4'-бифенилдикарбоновой кислоты с медью.
Фиг. 16 - график, иллюстрирующий порошковую рентгенограмму комплекса 4,4'-бифенилдикарбоновой кислоты с медью.
Фиг. 17 - график, иллюстрирующий распределение диаметра пор в комплексе 4,4'-бифенилдикарбоновой кислоты с медью.
Фиг. 18 - адсорбционная способность по метану /изотерма адсорбции/ комплекса 4,4'-бифенилдикарбоновой кислоты с медью.
Фиг. 19 /a/, 19 /b/ - графики, иллюстрирующие адсорбционные способности по топливному газу /изотермы адсорбции/ комплекса 4,4'-бифенилдикарбоновой кислоты с медью.
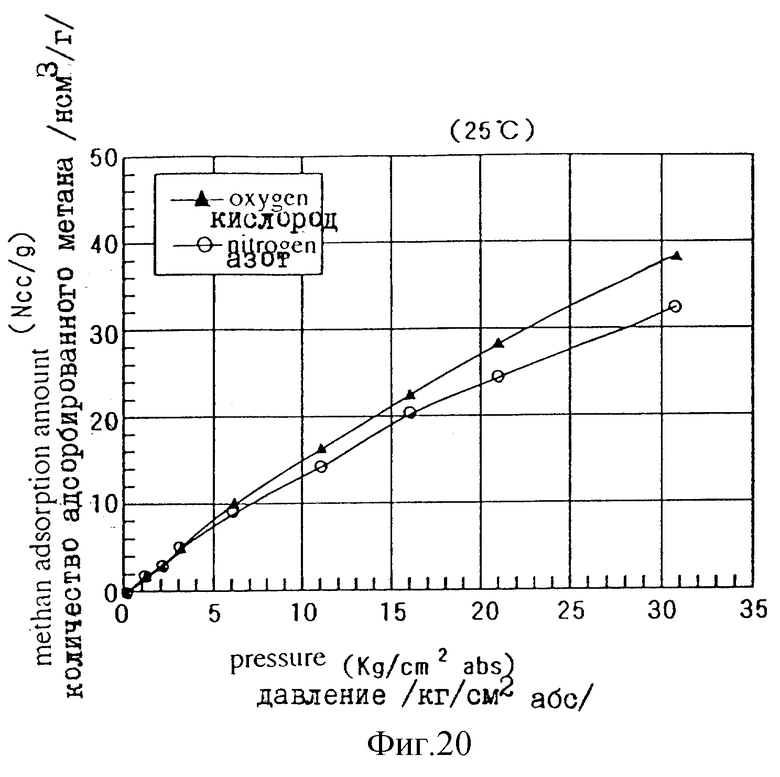
Фиг. 20 - график, иллюстрирующий газоадсорбционные способности по кислороду и азоту /изотермы адсорбции/ комплекса 4,4'-бифенилдикарбоновой кислоты с медью, и
Фиг. 21 - график, иллюстрирующий адсорбционные способности по метану комплексов соответственно фумаровой кислоты с молибденом, терефталевой кислоты с молибденом и циклогександикарбоновой кислоты с молибденом.
Описание предпочтительных вариантов осуществления изобретения
Далее будут описаны предпочтительные варианты осуществления изобретения со ссылкой на прилагаемые чертежи.
На фиг. 1 схематически показан автомобиль на газообразном топливе 2, оснащенный устройством для хранения газа согласно настоящему изобретению. Этот автомобиль на газообразном топливе 2 содержит в себе топливный бак 1 в виде устройства для хранения газа согласно изобретению и двигатель 2 в виде двигателя внутреннего сгорания, получающего природный газ из топливного бака 1, хранящего этот газ, смешивающего этот газ с необходимым для горения кислородсодержащим газом /например, воздухом/ и создающего движущую силу для движения автомобиля в результате сгорания этой газовой смеси.
Топливный бак 1 содержит т.н. сосуд под давлением и два отверстия - выходное 5a и входное 5b, через которые газ, подлежащий хранению в этом баке, может входить и выходить из него, Вблизи каждого выходного и входного отверстий расположены клапаны 6, образующие газонепроницаемый механизм для поддержания газа под повышенным давлением внутри сосуда под давлением 4. На соответствующей газозаправочной станции 7 топливный бак 1 под давлением заполняют природным газом, используемым в качестве топлива. Нет необходимости говорить, что этот топливный бак 1 с газом обычно находится при нормальных температурных условиях без специального охлаждения. Это значит, что при повышении температуры в летнее время бак 1 подвергается воздействию сравнительно высокой температуры. При таких условиях металлоорганический комплекс, относящийся к настоящему изобретению и описываемый в дальнейшем, может действовать эффективно, сохраняя высокую адсорбционную способность в таком интервале сравнительно высоких температур /т.е. 25 - 60oC/.
В топливном баке 1 находится металлоорганический комплекс 8, приготовленный согласно настоящему изобретению. Этот металлоорганический комплекс 8 адсорбирует природный газ /например, газ, включающий в себя метан в качестве основного компонента/ при повышенном давлении и нормальной температуре. При открывании выпускного клапана 6 адсорбированный газ десорбируется с металлоорганического комплекса 8 и направляется в двигатель 3, в котором газ сгорает с созданием движущей силы для автомобиля.
Конкретнее металлоорганический комплекс представляет собой, например, комплекс терефталевой кислоты с медью, имеющий одномерную канальную структуру и плотность в прессованном состоянии, равную 1,53 г/см3/ прессованный под давлением 650 кг/см2/.
Далее будут описаны некоторые особые способы синтеза металлорганического комплекса.
/1/ Синтез металлоорганических комплексов
Металлоорганический комплекс, используемый при настоящем изобретении, имеет одномерную канальную структуру. Типичным примером такого комплекса является комплекс дикарбоновой кислоты с медью.
/1/-1. Условия синтеза комплекса дикарбоновой кислоты с медью
Дикарбоновую кислоту растворяют в органическом растворителе, в который для регулирования pH в качестве добавки вводят органическую кислоту /эта добавка обязательно необходима в случае использования формиата меди, карбоната меди или ацетата меди/. В этот раствор по каплям подают раствор формиата меди или ацетата меди. Эту смесь растворов оставляют в покое от нескольких часов до нескольких дней, а твердое вещество, выпадающее в ней в осадок, удаляют путем вакуумного фильтрования и затем высушивают в течение пяти часов при 120oC, получая необходимое химическое соединение.
В качестве дикарбоновой кислоты можно использовать любую из следующих кислот: терефталевую кислоту, фумаровую кислоту, 1,4-транс-циклогександикарбоновую кислоту, 2,6-нафталиндикарбоновую кислоту, 1.4-нафталиндикарбновую кислоту, муконовую кислоту, 1,4-фенилендиакриловую кислоту, 1,4-фенилендиуксусную кислоту, адипиновую кислоту, субериновую кислоту, бифениловый эфир дикарбоновой кислоты, дикарбоксидифенилсульфоновую кислоту, 4,4'-бифенилдикарбновую кислоту и т.п. Благодаря выбору из этих дикарбоновых кислот можно регулировать размер канала.
Из вышеуказанных кислот предпочтительно являются терефталевая кислота, фумаровая кислота, 1,4-транс-циклогександикарбоновая кислота и 2,6-нафталиндикарбоновая кислота. При использовании этих кислот можно получить комплекс дикарбоновой кислоты с большой площадью удельной поверхности и большой адсорбционной способностью.
В качестве органического растворителя можно использовать спирт, как например, метанол, этанол, пропанол или органический растворитель, как например, бензол, толуол, ацетонитрил, тетрагидрофуран, диметилсульфоксид, диметилформамид, гексан, ацетон, и т.п., или смесь этих растворителей, которые могут растворять дикарбоновую кислоту и соединение меди.
Из вышеуказанных растворителей предпочитаются метанол, этанол, диметилформамид и смесь спирта и диметилформамида. Эти спирты могут легко растворять вещества, но не растворяют продукт реакции. Кроме того, они не координируются в комплексе, так что можно легко предотвращать образование неадсорбирующего и неудерживающего комплекса.
В качестве органической кислоты можно использовать формиат, ацетат, трифторацетат и пропионовую кислоту. Из них предпочитаются формиат и ацетат.
При реакции синтеза температура реакции может изменяться приблизительно от -20 до 80oC, причем реакция возможна при нормальной температуре.
Кроме того, что касается концентрации веществ при реакции синтеза, концентрация дикарбоновой кислоты должна быть 0,005 моль/л - 0,1 моль/л, предпочтительно 0,02 моль/л - 0,08 моль/л. При концентрации в пределах последнего интервала можно получить особенно удовлетворительный результат. Далее, что касается вышеуказанного вещества, то количество фумарата меди и ацетата меди, добавляемых в качестве медной соли органической кислоты, должно составлять 0,5 - 2 мольных эквивалента по отношению к дикарбоновой кислоте. Если это количество будет меньше указанного интервала, то уменьшится выход. Наоборот, если это количество будет больше 2 мольного эквивалента, то будет происходить нежелательная побочная реакция ввиду его связи с координационным числом меди /координируются 2 атома меди/. Более того, образованию комплекса может содействовать введение в качестве добавки органической кислоты в количестве порядка 0,1 - 2,0%, предпочтительно 0,5 - 1,0%. В этом случае если количество добавки будет меньше вышеопределенного интервала, то адсорбционная способность не увеличится в достаточной степени. Наоборот, если это количество будет больше указанного интервала, то труднее будет получить необходимое вещество.
Между прочим, комплекс бифенилдикарбоновой кислоты с медью, используемый согласно изобретению, представляет собой новый комплекс дикарбоновой кислоты с медью, открытый данными изобретателями. Далее будут описываться условия синтеза этого комплекса.
Для получения этого комплекса бифенилдикарбоновой кислоты с медью раствор бифенилдикарбоновой кислоты с введенной в него добавкой, состоящей, по крайней мере, из одного вида органической кислоты, выбранной из группы, состоящей из формиата, ацетата, трифторацетата и пропионовой кислоты, смешивают с другим раствором, в котором, по крайней мере, один вид соли меди, выбранный из группы, состоящей из формиата меди, ацетата меди, сульфата меди, нитрата меди и карбоната меди, растворен в органическом растворителе, содержащем, по крайней мере, один вид растворителя, выбранного из группы, состоящий из метанола, этанола, пропанола, бензола, толуола, ацетонитрила, тетрагидрофурана, диметилсульфоксида, диметилформамида, диметилацетамида, гексана, ацетона и т.п. Затем эту смесь растворов оставляют в покое для получения комплекса.
В качестве альтернативы раствор бифенилдикарбоновой кислоты смешивают с раствором, в котором, по крайней мере, один вид соли меди, выбранной из группы, состоящей из формиата меди, ацетата меди, сульфата меди, нитрата меди и карбоната меди, растворен в органическом растворители, содержащем, по крайней мере, один вид растворителя, выбранного из группы, состоящей из метанола, этанола, пропанола, бензола, толуола, ацетонитрила, тетрагидрофурана, диметилсульфоксида, диметилформамида, гексана, ацетона и т.п. Затем из этой смеси растворов можно получить желаемый комплекс в виде продукта ее осаждения.
Этот новый комплекс бифенилдикарбоновой кислоты с медью используют в качестве материала для адсорбции и удерживания газообразного метана. Например, при давлении около 30 г/см2 /абс./ комплекс в виде порошка мог бы адсорбировать и удерживать около 150 нсм3/г.
/1/-2. Примеры синтеза комплексов дикарбоновой кислоты и меди
Были предприняты попытки синтезировать следующие комплексы дикарбоновой кислоты и меди: терефталевая кислота - медь, фумаровая кислота - медь, 1,4-трансциклогександикарбоновая кислота - медь, 2,6-нафталиндикарбоновая кислота - медь, п-фенилендиуксусная кислота - медь и бифенилдикарбоновая кислота - медь.
[a] Терефталевая кислота - медь
/1/ 1,2 г терефталевой кислоты при нагревании растворяли в растворителе, представляющем собой смесь 800 см3 метанола и 30 см3 муравьиной кислоты. После этого раствор охлаждали до нормальной температуры, а затем в этот раствор вводили по каплям другой раствор, в котором 3,0 г формиата меди было растворено в 150 см3 метанола, после чего оставляли в покое на два дня. Затем продукт в виде осадка отфильтровывали под вакуумом и высушивали 4 часа при 120oC, в результате чего получали 2,1 г комплекс терефталевой кислоты с медью. Это вещество имело площадь удельной поверхности, равную 220 м2/г. Измерение по методу НК с использованием аргона показало, что это вещество имело диаметр пор в 6,0 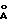 /фиг. 14/. Между прочим, при другом измерении по методу МР с использованием азота его диаметр пор оказался равным 9,3
/фиг. 14/. Между прочим, при другом измерении по методу МР с использованием азота его диаметр пор оказался равным 9,3  Кроме того, установлено, что для измерения диаметра пор в комплексе дикарбоновой кислоты с медью этого вида пригоден метод НК, который, как обычно считалось, пригоден для измерения диаметра пор меньше 10
Кроме того, установлено, что для измерения диаметра пор в комплексе дикарбоновой кислоты с медью этого вида пригоден метод НК, который, как обычно считалось, пригоден для измерения диаметра пор меньше 10 
/II/ 0,70 г терефталевой кислоты при нагревании растворяли в растворителе из смеси 400 метанола и 20 см3 ацетата. После охлаждения раствора до нормальной температуры в него по каплям вводили другой раствор, в котором 0,95 г формиата меди было растворено в 50 см3 метанола, и затем оставляли в покое на два дня. После этого продукт в виде осадка отфильтровывали под вакуумом и в течение 4 ч высушивали при 110oC, в результате чего получали 0,41 г комплекса терефталевой кислоты с медью.
/III/ 0,41 г терефталевой кислоты при нагревании растворяли в растворителе из смеси 250 см3 метанола и 15 см3 муравьиной кислоты. После этого раствор охлаждали до нормальной температуры, в этот раствор по каплям вводили другой раствор, в котором 0,50 г ацетата меди было растворено в 40 см3 метанола, и затем оставляли в покое на несколько дней. После этого продукт в виде осадка отфильтровывали под вакуумом и в течение 4 ч высушивали при 110oC, в результате чего получали комплекс терефталевой кислоты с медью.
[b] Фумаровая кислота - медь
/1/ 1,2 г фумаровой кислоты при нагревании растворяли в растворителе из смеси 100 см3 метанола и 12 см3 муравьиной кислоты. После этого раствор охлаждали до нормальной температуры, в этом раствор вводили по каплям другой раствор, в котором 3,48 г формиата меди было растворено в 100 см3 метанола, и затем оставляли в покое на один день. После этого продукт в виде осадка отфильтровывали под вакуумом и в течение 4 ч высушивали при 120oC, в результате чего получали 1,37 г комплекса фумаровой кислоты с медью.
Это вещество имело площадь удельной поверхности, равную 450 м3/г.
/II/ 1,74 г фумаровой кислоты и 40 см3 ацетата при нагревании растворяли в 100 см3 метанола, и в этот раствор по каплям вводили 100 см3 раствора метанола, содержащего 2,98 г растворенного в нем ацетата меди. После этого раствор оставляли в покое на два дня при комнатной температуре. Продукт в виде осадка отфильтровывали под вакуумом и высушивали в течение 3 ч при 110oC, в результате чего получали 1,37 г комплекса фумаровой кислоты с медью. В этом случае полученное вещество также имело большую площадь удельной поверхности и проявлено адсорбционную способность в отношении метана.
/III/ 1,74 г фумаровой кислоты растворяли в растворителе из смеси 100 см3 метанола и 8 см3 муравьиной кислоты. Затем в вышеуказанный раствор при перемешивании и нормальной температуре вводили по каплям другой раствор, в котором 3,38 г формиата меди было растворено в 100 см3 метанола. После этого оставляли раствор в покое на один день. Продукт в виде осадка отфильтровывали под вакуумом и высушивали в течение 4 ч при 120oC, в результате чего получали 1,23 г комплекса фумаровой кислоты с медью. Это вещество имело площадь удельной поверхности, равную 480 м3/г.
/IV/ 1,74 г муравьиной кислоты растворяли в растворителе из смеси 100 см3 метанола и 1 см3 муравьиной кислоты. Затем в вышеуказанный раствор при перемешивании и нормальной температуре вводили по каплям другой раствор, в котором 3,74 г сульфата меди /CuSО4 • 5H2O/ было растворено в 100 см3 метанола и оставляли в покое на один день. После этого продукт в виде осадка отфильтровывали под вакуумом и высушивали в течение 4 ч при температуре 120oC, в результате чего получали 0,3 г комплекса фумаровой кислоты с медью.
/V/ 0.58 г фумаровой кислоты растворяли в растворителе из смеси 40 см3 метанола и 12 см3 муравьиной кислоты. Затем в вышеуказанный раствор при перемешивании и нормальной температуре вводили по каплям другой раствор, в котором 1,0 г ацетата меди было растворено в 80 см3 метанола. После этого оставляли раствор в покое на несколько дней. Продукт в виде осадка отфильтровывали под вакуумом и высушивали в течение 4 ч при 110oC, в результате чего получали 0,3 г комплекса фумаровой кислоты и меди.
Измерения по методу НК с использованием аргона показали, что эти комплексы фумаровой кислоты с медью имели диаметр пор около 5,4 
[c] 1,4-транс-циклогександикарбоновая кислота - медь
/1/ 2,53 г 1,4-транс-циклогександикарбоновой кислоты при нагревании растворяли в растворителе из смеси 100 см3 метанола и 14 см3 муравьиной кислоты. После этого раствор охлаждали до нормальной температуры. В этот раствор при перемешивании вводили по каплям другой раствор, в котором 3,38 г формиата меди было растворено в 100 см3 метанола, и затем оставляли в покое на один день. После этого продукт в виде осадка отфильтровывали под вакуумом и высушивали в течение 4 ч при 120oC, в результате чего получали 1,71 г комплекса 1,4-транс-циклогександикарбоновой кислоты с медью. Это вещество имело площадь удельной поверхности в 480 м3/г и диаметр пор в 4,7 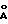
/II/ 2,58 г 1,4-транс-циклогександикарбоновой кислоты при нагревании растворяли в растворителе из смеси 100 см3 метанола и 20 см3 муравьиной кислоты. После охлаждения этого раствора до нормальной температуры в него при перемешивании вводили по каплям другой раствор, в котором 3,38 г формиата меди было растворено в 100 см3 метанола, и затем оставляли в покое на несколько дней. После этого продукт в виде осадка отфильтровывали под вакуумом и высушивали в течение 4 ч при температуре 110oC, в результате чего получали 1,43 г комплекса 1,4-транс-циклогександикарбоновой кислоты с медью
[d] 2,6-нафталиндикарбоновая кислота - медь
/1/ 0,40 г 2,6-нафталиндикарбоновой кислоты при нагревании растворяли в растворителе из смеси 4000 см3 метанола и 5 см3 муравьиной кислоты. После охлаждения этого раствора до нормальной температуры в него при перемешивании вводили по каплям другой раствор, в котором 3,00 г формиата меди было растворено в 100 см3 метанола, и затем оставляли в покое на несколько дней. После этого продукт в виде осадка отфильтровывали под вакуумом и высушивали в течение 4 ч при температуре 110oC, в результате чего получали 0,35 г комплекса 2,6-нафталиндикарбоновой кислоты с медью.
[e] п-фенилендиуксусная кислота - медь
/1/ 2,58 г п-фенилендиуксусной кислоты при нагревании растворяли в растворителе из смеси из 100 см3 метанола и 2,5 см3 муравьиной кислоты. После охлаждения этого раствора до нормальной температуры в него при перемешивании вводили по каплям другой раствор, в котором 2,00 г формиата меди было растворено в 150 см3 метанола, и затем оставляли в покое на несколько дней. После этого продукт в виде осадка отфильтровывали под вакуумом и высушивали в течение 4 ч при 110oC, в результате чего получали 1,40 г комплекса п-фенилендиуксусной кислоты с медью.
[f] 4,4'-бифенилдикарбоновая кислота - медь
A. Раствор дикарбоновой кислоты приготавливали путем растворения 0,25 г 4,4'-бифенилдикарбоновой кислоты в растворе из смеси 60 см3 диметилформамида и 1 см3 муравьиной кислоты. Раствор формиата меди приготавливали путем растворения 0,5 г фумарата меди в метаноле. Затем раствор формиата меди вводили по каплям и смешивали с раствором дикарбоновой кислоты, перемешивая последний при нормальной температуре. После этого смесь растворов оставляли в покое на один день, и в виде осадка получали комплекс 4,4'-бифенилдикарбоновой кислоты с медью. Затем продукт в виде осадка отфильтровывали под вакуумом и высушивали в течение 4 ч при 100oC, в результате чего получали 0,29 г 4-4'-бифенилдикарбоновой кислоты с медью.
B. Раствор дикарбоновой кислоты приготавливали путем растворения 0,25 г 4,4'-бифенилдикарбоновой кислоты в 60 см3 диметилформамида. С другой стороны, приготавливали раствор сульфата меди путем растворения 0,25 г сульфата меди /CuSO4•5H2O/ в диметилформамиде. Затем раствор сульфата меди вводили по каплям и смешивали с раствором дикарбоновой кислоты, перемешивая последний при нормальной температуре. После этого смесь растворов оставляли в покое на один день, и в виде осадка получали комплекс 4,4'-бифенилдикарбоновой кислоты с медью. Затем продукт в виде осадка отфильтровывали под вакуумом и высушивали в течение 4 ч при 100oC, в результате чего получали 0,25 г комплекса 4,4'-бифенилдикарбоновой кислоты с медью.
/2/ Структура комплексов
Наличие одномерной канальной структуры в вышеописанных комплексах подтвердили порошковые рентгенограммы и распределения диаметров пор. По измерению магнитной восприимчивости установлено, что эти комплексы имеют решетчатоподобную двухмерную структуру, в которой некоторое количество двухядерных структур с дикарбоновыми кислотами, координированными вокруг иона меди, связаны друг с другом посредством взаимной связи их соседних ионов меди через дикарбоновую кислоту. Ионы меди присутствуют в точках пересечения A, A, A, . . . решетки. Кроме того, как полагают, множество вышеописанных двухмерных структур должны быть кристаллизованы таким образом, чтобы соответствующие точки пересечения вертикально уложенных решеток по вертикали находились вровень с зазорами B, B ... между соседними точками пересечения, образуя вместе одномерную канальную структуру /например, на фиг. 2 показана предполагаемая структура комплекса терефталевой кислоты с медью/. Кроме того, на основании вышеуказанных результатов можно предполагать, что диаметр пор может меняться с изменением вида применяемой дикарбоновой кислоты.
/3/ Свойства различных металлоорганических комплексов
/3/-1. Зависимость количества адсорбированного газообразного метана от давления
Весовые количества метана, адсорбированного на металлоорганических комплексах, полученных вышеописанными способами, измеряли в интервале абсолютного давления 0 - 32 кг/см3.
Результаты измерений показаны на фиг. 3 - 7. На каждой из этих фигур горизонтальная ось обозначает давление (кг/см3 абс.), а вертикальная ось - количество адсорбированного метана, измеренного при 25oC /т.е. изотерму адсорбции/. При этом на фигурах пример /1/ из раздела /a/ обозначен как a1. Сходные обозначения используются и для других примеров.
Как показано, было обнаружено, что все из этих комплексов дикарбоновой кислоты с медью адсорбируют метан при повышенном давлении и нормальной температуре /например, 25oC/.
/3/-2. Зависимость количества адсорбированного газообразного метана от давления формования
В случае использования комплекса в устройстве для хранения газа или в автомобиле на газообразном топливе металлоорганический комплекс, полученный вышеописанным способом, подвергают формованию под давлением для получения заданной величины плотности в формованном состоянии. Далее будут описаны изменения, которые происходят в адсорбиционных характеристиках вследствие такого процесса формования.
При последующем описании в сравнении с активированным углем излагаются результаты исследования плотностей соответствующих комплексов дикарбоновой кислоты с медью, формованных под давлением, т.е. комплекса терефталевой кислоты с медью /a1/, комплекса фумаровой кислоты с медью /b1/ и комплекса циклогександикарбоновой кислоты с медью /c1/. Между прочим, при исследовании зависимости от давления формования сравнивались результаты при давлениях формования 650 кг/см2 и 250 кг/см2. Однако активированный уголь не формовали под давлением 650 кг/см2.
В нижеприведенной табл. 1 сравниваются насыпные плотности соответствующих веществ при отсутствии их формования под давлением и плотности после формования под давлением.
На фиг. 8 показаны изменения, вызванные формованием под давлением, в газоадсорбционной способности на единицу объема комплекса терефталевой кислоты с медью /a1/, комплекса фумаровой кислоты с медью /b1/ и активированного угля. На этой фигуре горизонтальная ось обозначает давление (кг/см2 абс.) и вертикальная ось - количество адсорбированного метана на единицу объема. Кроме того, каждый график относится к адсорбционно-удерживающим материалам, обозначенным ниже.
○ - комплекс терефталевой кислоты с медью /a1/, не формованный под давлением.
• - комплекс терефталевой кислоты с медью /a1/, формованный под давлением 250 кг/см2.
Δ - комплекс терефталевой кислоты с медью /a1/, формованный под давлением 650 кг/см2.
Δ комплекс фумаровой кислоты с медью /b1/, формованный под давлением 650 кг/см2.
 - активированный уголь, не формованный под давлением.
- активированный уголь, не формованный под давлением.
 - активированный уголь, формованный под давлением 250 кг/см2.
- активированный уголь, формованный под давлением 250 кг/см2.
Как можно видеть из этой фигуры, комплексы дикарбоновой кислоты, подвергшиеся формованию, имеют высокую плотность после формования и обладают больше газоадсорбционной способностью по сравнению с активированным углем.
Когда главной целью является адсорбция метана, предпочитается, чтобы металлоорганический комплекс имел площадь удельной поверхности в пределах от нескольких до 1500 м2/г, предпочтительно 50 - 1000 м2/г, может обеспечить высокую адсорбционную способность. Если площадь удельной поверхности меньше нескольких м2/г, то происходит значительное снижение адсорбционной способности. Наоборот, если эта площадь больше 1500 м2/г, то уменьшается количество получаемого комплекса.
С другой стороны, диаметр пор предпочтительно должен быть в пределах 3 - 13  , а более предпочтительно - в пределах 5 - 12
, а более предпочтительно - в пределах 5 - 12  . Если этот диаметр меньше 3
. Если этот диаметр меньше 3  , то происходит значительное снижение адсорбционной способности. Наоборот, если диаметр больше 13
, то происходит значительное снижение адсорбционной способности. Наоборот, если диаметр больше 13  , то также значительно снижается адсорбционная способность.
, то также значительно снижается адсорбционная способность.
/3/-3. Зависимость количества адсорбционного метана от температуры
Данные изобретатели исследовали адсорбционную способность по отношению к метану комплекса фумаровой кислоты с медью в интервале температур 5 - 60oC для его применения в автомобиле на газообразном топливе, сравнивая ее с адсорбционной способностью активированного угля.
Результаты исследования показаны на фиг. 9 - 10. На каждой из этих фигур горизонтальная ось обозначает температуру, а вертикальная ось - количество адсорбированного метана. На фиг. 9 показаны количества адсорбированного метана на единицу веса, а на фиг. 10 - количества адсорбированного метана на единицу объема. Кроме того, значок • обозначает результаты, полученные с комплексом фумаровой кислоты с медью, в то время как другой значок  обозначает результаты, полученные с активированным углем. В этих случаях все материалы были в порошкообразном виде.
обозначает результаты, полученные с активированным углем. В этих случаях все материалы были в порошкообразном виде.
Как можно видеть из фиг. 9 и 10, с повышением температуры уменьшаются количества адсорбированного метана. Однако для комплекса фумаровой кислоты с медью снижение этого количества меньше, чем для активированного угля. Кроме того, комплекс фумаровой кислоты с медью первоначально имеет более высокую объемную адсорбционную способность, чем активированный уголь. Поэтому можно понять, что этот материал является весьма полезным.
А именно, если это адсорбирующе-удерживающее вещество использовать в автомобиле на газообразном топливе, то в заданном объеме можно хранить большое количество, например, автомобильного природного газа. Или в меньшем объеме можно хранить такое же количество газа. Следовательно, это вещество будет очень полезным для этой области применения.
/3/-4. Адсорбционный эффект в отношении других газов
Исследовалось также то, проявляют ли вышеописанные комплексы дикарбоновой кислоты с медью адсорбционную способность в отношении других газов, отличных от метана.
/I/ Исследовали адсорбционную способность комплекса терефталевой кислоты с медью [aII] и комплекса фумаровой кислоты с медью [bIII] в отношении газообразных углеводородов. Результаты исследования показаны на фиг. 11 и 12.
Как можно видеть из фиг. 11 и фиг. 12, комплексы дикарбоновой кислоты с медью, как установлено, проявляют в общем высокую газоадсорбционную способность в отношении топливных газов.
/II/ Кроме того, исследовали адсорбционную способность комплекса фумаровой кислоты с медью [bV] в отношении газообразных кислорода и водорода. Результаты исследования показаны на фиг. 13.
Как можно видеть из фиг. 13, этот комплекс дикарбоновой кислоты с медью, как установлено, может адсорбировать различные газы независимо от их вида.
/3/-5. Свойства комплекса 4,4'-бифенилдикарбоновой кислоты с медью
а/ Площадь удельной поверхности комплекса 4,4'-бифенилдикарбоновой кислоты с медью, синтезированного в предшествующем примере [f] A, по методу Браунауэра-Эммета-Теллера. Как показало исследование, этот комплекс имеет площадь удельной поверхности, равную 900 м2/г.
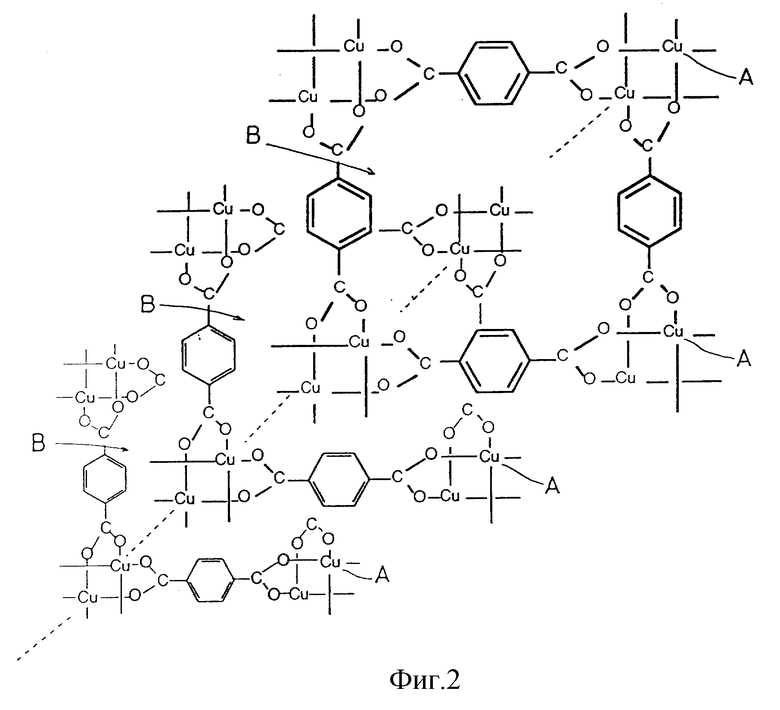
б/ Средний диаметр пор в комплексе 4,4'-бифенилдикарбоновой кислоты с медью, синтезированного в предшествующем примере [f] A, по методу НК. Как показано исследование, этот комплекс имеет диаметр пор, равный 7, 8 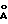 /см. фиг. 17/.
/см. фиг. 17/.
в/ Исследовали адсорбционно-удерживающую способность комплекса 4,4'-бифенилдикарбоновой кислоты с медью в отношении газообразного метана. Результаты исследования показаны на фиг. 18.
Как обнаружено, этот комплекс 4,4'-бифенилдикарбоновой кислоты с медью может адсорбировать и удерживать газообразной метан при повышенном давлении и, следовательно, может быть эффективно использован в качестве вещества для адсорбции и удерживания газообразного метана.
г/ Исследовали адсорбционно-удерживающую способность комплекса 4,4'-бифенилдикарбоновой кислоты с медью, синтезированного в предшествующем примере [f] , в отношении газообразных этана, пропана и бутана. Результаты исследования показаны на фиг. 19 /a/ и /b/.
Как обнаружено, этот комплекс 4,4'-бифенилдикарбоновой кислоты может адсорбировать и удерживать различные газы под повышенным давлением и, следовательно, может быть эффективно использован в качестве вещества для адсорбции и удерживания топливного газа при его применении в топливном баке автомобиля на газообразном топливе и т.п.
д/ Кроме того, исследовали также адсорбционный эффект в отношении кислорода и азота. Результаты исследования показаны на фиг. 20. Как показано, кроме топливного газа, комплекс может эффективно адсорбировать и удерживать различные газы, когда подлежащие удерживанию газы вводятся в одномерную канальную структуру. Таким образом, используя комплекс 4,4'-бифенилдикарбоновой кислоты с медью для поддержки различных катализаторов, можно предположить, что этот комплекс обеспечивает каталитические реакции для различных введенных в него газов.
/4/ Другие комплексы дикарбоновой кислоты с металлом
/4/-1. Отдельные примеры синтеза
а/ Фумаровая кислота - молибден
0,597 г /5,14 ммоля/ фумаровой кислоты и 1000 г /2,34 ммоля/ ацетата молибдена растворяли в 900 мл метанола. После перемешивания раствора в течение трех дней при комнатной температуре его оставляли в покое на несколько дней. Затем продукт в виде осадка отфильтровывали под вакуумом, достаточно промывали метанолом и после этого сушили под вакуумом в течение 4 ч при 60oC, в результате чего получали 0,970 г желаемого вещества. Это вещество имело площадь удельной поверхности, равную 469 м2/г. Измерение по методу НК с использованием аргона показало, что вещество имеет диаметр пор, равный 5,8  .
.
b/ Терефталевая кислота - молибден
0,854 г /5,14 ммоля/ терефталевой кислоты и 1000 г /2.34 ммоля/ ацетата молибдена растворяли в 900 мл метанола. После перемешивания раствора в течение трех дней при комнатной температуре его оставляли в покое на несколько дней. После этого продукт в виде осадка отфильтровывали под вакуумом, достаточно промывали метанолом и затем сушили под вакуумом в течение 4 часов при 60oC, в результате чего получали 1,387 г желаемого вещества. Это вещество имело площадь удельной поверхности, равную 519 м2/г. Измерение по методу НК с использованием аргона показало, что вещество имеет диаметр пор, равный 5,7  .
.
c/ Циклогександикарбоновая кислота - молибден
0,885 г /5,14 ммоля/ циклогександикарбоновой кислоты и 1000 г /2,34 ммоля/ ацетата молибдена растворяли в 900 мл метанола. После перемешивания раствора в течение трех дней при комнатной температуре его оставляли в покое на несколько дней. После этого продукт в виде осадка отфильтровывали под вакуумом, достаточно промывали метанолом и затем высушивали под вакуумом в течение 4 часов при 60oC, в результате чего получали 1,216 г желаемого вещества. Это вещество имело площадь удельной поверхности, равную 212 м2/г. Измерение по методу НК с использованием аргона показало, что вещество имеет диаметр пор, равный 5,2  .
.
d/ Фумаровая кислота - хром
0,597 г /5,14 ммоля/ фумаровой кислоты и 0,880 г /2,24 ммоля/ ацетата хрома /II/ растворяли в 900 мл метанола. После перемешивания раствора в течение трех дней при комнатной температуре его оставляли в покое на несколько дней. После этого продукт в виде осадка отфильтровывали под вакуумом, достаточно промывали метанолом и затем высушивали под вакуумом в течение 4 часов при 60oC, в результате чего получали 0,805 г желаемого вещества. Это вещество имело площадь удельной поверхности, равную 183 м2/г. Измерение по методу НК с использованием аргона показало, что вещество имеет диаметр пор, равный 5,0  .
.
e/ 1,4-транс-циклогександикарбоновая кислота - родий
0,885 г /5,14 ммоля/ 1,4-транс-циклогександикарбоновой кислоты и 0,517 г /1,17 ммоля/ димера ацетата родия
/(Rh2CH3COO)4/ растворяли в 900 мл метанола. После перемешивания раствора в течение трех дней при комнатной температуре его оставляли в покое на несколько дней. После этого продукт в виде осадка отфильтровывали под вакуумом, достаточно промывали метанолом и затем сушили под вакуумом в течение 4 ч при 60oC, в результате чего получали 0,824 г, желаемого вещества.
/4/-2. Зависимость количества адсорбированного газообразного метана от давления
В отношении некоторых металлоорганических комплексов, полученных вышеописанными способами, в интервале 0-36 кг/см2 измеряли по весу количества метана, адсорбированные ими.
Результаты измерений показаны на фиг. 21. На этой фигуре значком Δ графически обозначен комплекс фумаровой кислоты с медью, o - комплекс терефталевой кислоты с молибденом и  - комплекс 1,4-транс-циклогександикарбоновой кислоты с молибденом. Горизонтальная ось соответствует давлению (кг/см2 абс. ), а вертикальная ось - количеству адсорбированного метана, измеренному при 25oC /т.е. изотерма адсорбции/.
- комплекс 1,4-транс-циклогександикарбоновой кислоты с молибденом. Горизонтальная ось соответствует давлению (кг/см2 абс. ), а вертикальная ось - количеству адсорбированного метана, измеренному при 25oC /т.е. изотерма адсорбции/.
Как показано, все эти металлоорганические комплексы, как обнаружено, проявляли хорошие свойства по адсорбции метана.
По существу сходные результаты были получены в отношении комплексов 4,4'-бифенилдикарбоновая кислота - молибден, терефталевая кислота - хром, фумаровая кислота - хром, 1,4-транс-циклогексановая кислота - хром, бифенилдикарбоновая кислота - хром, терефталевая кислота - родий, бифенилдикарбоновая кислота - родий, терефталевая кислота - палладий фумаровая кислота - палладий, 1,4-транс-циклогександикарбоновая кислота - палладий, бифенилдикарбоновая кислота - палладий, терефталевая кислота - вольфрам, фумаровая кислота - вольфрам, 1,4-транс-циклогександикарбоновая кислота - вольфрам и бифенилдикарбоновая кислота - вольфрам. Однако эти результаты не показаны.
Кроме того, подтвердилось, что комплексы дикарбоновой кислоты с вольфрамом и дикарбоновой кислоты с палладием по свойствам адсорбировать метан превосходит активированный уголь.
Изобретение может быть воплощено в других конкретных формах без отступления от его сути или существенных признаков. Поэтому данные варианты осуществления изобретения следует во всех отношениях рассматривать как иллюстративные и неограничительные. Пределы изобретения указаны скорее прилагаемой формулой, чем предшествующим описанием, и поэтому подразумеваются, что в ней охватываются все изменения, которые подпадают под понятие и пределы эквивалентности формулы.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОБОГАЩЕНИЯ ГОРЮЧЕГО ГАЗА | 2011 |
|
RU2550899C2 |
| УСТРОЙСТВО ДЛЯ КОНЦЕНТРИРОВАНИЯ ГОРЮЧЕГО ГАЗА И СПОСОБ КОНЦЕНТРИРОВАНИЯ ГОРЮЧЕГО ГАЗА | 2007 |
|
RU2439132C2 |
| УСТРОЙСТВО ДЛЯ ОБОГАЩЕНИЯ ГОРЮЧЕГО ГАЗА | 2011 |
|
RU2550889C2 |
| СИСТЕМА ОБОГАЩЕНИЯ ГОРЮЧЕГО ГАЗА | 2011 |
|
RU2542982C2 |
| СИСТЕМА КОНЦЕНТРИРОВАНИЯ ВОСПЛАМЕНЯЮЩЕГОСЯ ГАЗА | 2007 |
|
RU2443763C2 |
| СИСТЕМА ОБРАБОТКИ ГОРЮЧЕГО ГАЗА И СПОСОБ ОБРАБОТКИ ГОРЮЧЕГО ГАЗА | 2008 |
|
RU2460761C2 |
| КАТАЛИЗАТОР ДЛЯ КАТАЛИТИЧЕСКОГО НЕПОЛНОГО ОКИСЛЕНИЯ УГЛЕВОДОРОДОВ И СПОСОБ ПОЛУЧЕНИЯ СИНТЕЗ-ГАЗА | 2009 |
|
RU2432992C1 |
| АДСОРБЕНТ ДЛЯ УДАЛЕНИЯ УГЛЕВОДОРОДОВ ИЗ ВЫХЛОПНЫХ ГАЗОВ АВТОМОБИЛЯ | 2009 |
|
RU2406558C1 |
| Способ хранения природного газа при помощи адсорбции в промышленных газовых баллонах | 2015 |
|
RU2616140C1 |
| ГАЗОСМЕШИВАЮЩЕЕ УСТРОЙСТВО И УСТРОЙСТВО ДЛЯ ПРОИЗВОДСТВА СИНТЕЗ-ГАЗА | 2008 |
|
RU2434805C2 |















Использование: изобретение относится к технике хранения газа, содержащего метан в качестве основного компонента, и касается также его применения в качестве топливного бака в автомобиле на газообразном топливе. Сущность изобретения: устройство для хранения газа, содержащего метан в качестве основного компонента, содержит сосуд под давлением, который можно постоянно поддерживать при нормальной температуре, входное/выходное отверстие для обеспечения входа или выхода из него газа, подлежащего хранению, газонепроницаемый механизм для поддержания газа в сжатом состоянии внутри сосуда и сосуд под давлением, который можно постоянно поддерживать при нормальной температуре. В сосуд под давлением помещен металлоорганический комплекс, имеющий одномерную канальную структуру. Изобретение предлагает улучшенную технологию, которая при небольших затратах обеспечивает большую объемную способность по адсорбции и хранению газа, а также лучшую повторяемость газоадсорбционной характеристики. 4 с. и 20 з.п.ф-лы, 1 табл., 21 ил.
Приоритет по пунктам и признакам:
13.02.95 по пп.1, 10, 11, 15;
13.11.95 по пп.3 - 9, 16 - 24;
13.02.95 по пп.2, 12 - терефталевая кислота - медь, фумаровая кислота - медь, 1,4-транс-циклогександикарбоновая кислота - медь;
13.11.95 по пп.2, 12 - бифенилдикарбоновая кислота - медь;
12.02.96 по пп.2, 12 - металлоорганические комплексы металлов, отличные от меди;
13.02.95 по пп.13, 14 - медьсодержащее вещество;
12.02.96 по пп.13, 14 - другие металлсодержащие вещества.
| КЛАВИШНЫЙ МЕХАНИЗМ ПНЕВМАТИЧЕСКОГО ЯЗЫЧКОВОГО КЛАВИШНОГО МУЗЫКАЛЬНОГО ИНСТРУМЕНТА | 2000 |
|
RU2172985C1 |
| АППАРАТ ДЛЯ АККУМУЛИРОВАНИЯ ВОДОРОДА | 1992 |
|
RU2037737C1 |
| АВТОМОБИЛЬНЫЙ БАЛЛОН ДЛЯ СЖИЖЕННОГО ГАЗА | 1991 |
|
RU2018452C1 |
Авторы
Даты
2000-04-27—Публикация
1996-02-12—Подача