Изобретение относится к медицине, а именно к педиатрии. В настоящее время широкое распространение в нашей стране получил "Детский панадол", основным действующим веществом которого является парацетамол. В доступной литературе представлены такие эффекты парацетамола, как жаропонижающий, болеутоляющий, противовоспалительный (Запруднов А.М. Синдром Рея в детском возрасте. Парацетамол в педиатрической практике. - Москва, 1995; Справочник Видаль, 1996), обусловленные влиянием препарата на центр терморегуляции в гипоталамусе и способностью ингибировать синтез простагландинов.
Технический результат направлен на улучшение функциональных свойств нейтрофилов путем использования в качестве иммуномодулятора препарата "Детский панадол", что позволит, с одной стороны, уменьшить риск повреждающего воздействия активированных клеток на организм, а с другой, оказать стимулирующий эффект на нейтрофилы со сниженной функциональной активностью. Результатом модуляции функциональных свойств нейтрофилов явится предупреждение развития воспалительных осложнений, сокращение сроков заболеваний и более благоприятные их исходы.
Теоретическим обоснованием данного способа являются следующие данные.
Нейтрофилы занимают одну из наиболее активных позиций в системе гуморально-клеточной кооперации крови и соединительной ткани (Маянский А.Н., Маянский Д. Н. Очерки о нейтрофиле и макрофаге. - Новосибирск: Наука, Сибирское отделение, 1989), что делает их универсальной мишенью и соответственно индикатором различных нарушений гомеокинеза. Мембрана лейкоцитов при развитии физиологических процессов является биологически активной поверхностью, отражающей многие стороны обменных процессов. Одним из важных механизмов участия нейтрофилов в воспалительном процессе является адгезия, которая предшествует выходу лейкоцитов в ткани для выполнения специфических функций. Изменение адгезивного потенциала клеток, являющееся реактивным усилением их физиологической функции, связано с состоянием плазматической мембраны.
При патологических процессах, сопровождающихся воспалением, активация фагоцитов может приводить к перекисному повреждению клеточных мембран и липопротеидов плазмы крови (Н.К.Зенков Роль нейтрофилов в развитии процессов перекисного окисления липидов // В кн.: Актуальные вопросы патофизиологии: Тез.докл. - Новосибирск, 1985; Г.И.Клебанов, Л.А.Нифонтова. Изменение функциональной активности полиморфно-ядерных лейкоцитов при сосудистых поражениях головного мозга // Восьмой Всесоюзной съезд невропатологов, психиаторов и кардиологов: Тез.докл.- Москва.- 1988.-Т.3.- С. 113-115).
Токсическое действие перекисей лежит в основе завершенного фагоцитоза. Основным продуктом процесса фагоцитоза является активированный кислород, активацию которого обеспечивают энзимные системы лейкоцитов (О.Н.Ржевская, Н. А. Коровина. Клиническое значение определения показателей перекисного окисления липидов при воспалительных заболеваниях почек у детей//Вопр. охр. мат. и детства.- 1984. - N 4.- С.31-33). Образующиеся в большом количестве первичные и вторичные продукты перекисного окисления фосфолипидов обладают выраженным вазоконстрикторным действием (Н. В.Азизов. Значение перекисных процессов в патогенезе токсических состояний у детей.- Автореф.дисс...канд. мед. наук.- Москва, 1986). Л.О.Бадалян, А.И.Берестов, И.Т.Ильчук (Нарушение обмена липидов при нейротоксикозах у детей//Педиатрия.-1983.-N 2.- С. 15-19) сообщают, что у детей раннего возраста при острых респираторных заболеваниях нарушения в липидном спектре мембран эритроцитов сводятся к снижению содержания общих фосфолипидов, которые замещаются лизоформами и нейтральными липидами, что является результатом не только усиленного использования фосфолипидов клеточных мембран в энергетических целях, но и активного вовлечения их в процессы переокисления.
Таким образом, активность биологических процессов нейтрофилов выражается через состояние их мембран (изменение прилипающей способности, текучести биомембран, проницаемости), что может служить надежным индикатором функциональных изменений нейтрофилов в ответ на инфекционное воздействие.
Данное обстоятельство позволяет изучить механизмы антипиретического и противовоспалительного действия "Детского панадола" через модуляцию клеточной мембраны нейтрофилов.
Методологически изучение проводилось следующим образом:
Исследование включало изучение иммуномодулирующих свойств парацетамола, показанием для назначения которого являлись гипертермические состояния, возникающие при острых заболеваниях респираторной системы (ОРВИ, острый бронхит, острая пневмония) у детей, препаратом "Детский панадол" в возрастных дозах, обозначенных в аннотации, в течение 3 дней. Острые респираторные заболевания служили как модель патологического состояния, наиболее часто регистрируемого у детей. В качестве контролируемых параметров использовались показатели гемограммы, микровязкости мембран нейтрофилов (метод тонкослойной хроматографии общих липидов на пластинах "Сорбтон" по В.Н.Ростовцеву, Г.Е. Резнику. Количественное определение липидных фракций плазмы крови // Лаб. дело.- 1982.- N 4.- С.26-29, спонтанной адгезии нейтрофилов (метод M.H.Goldrosen (1979) в модификации Н.Л.Вартаняна, И.С.Лугановой, М.Н.Блинова. Реакция торможения прилипания лейкоцитов у больных острым лейкозом//Гематология и трансфузиология.-1988.-Т.33, N2.-C.24-27), определяемые до и на четвертые сутки от начала терапии панадолом.
Эффективность терапии оценивалась с помощью клинических осмотров, проводимых по той же схеме.
Под наблюдением находилось 40 детей основной и 20 группы сравнения с аналогичной патологией, не получавших препарата. Показанием для назначения препарата являлась гиперпирексия. В рассматриваемой группе больных уровень температурной реакции находился в пределах от 37,0o до 39,9oC (табл. 1). В абсолютном большинстве случаев панадол при пероральном применении показал себя высокоэффективным жаропонижающим препаратом, вызывающим снижение температурной реакции как субфебрильного, так и фебрильного типа уже в первые сутки лечения.
Нами осуществлена оценка влияния препарата на другие признаки острых заболеваний респираторной системы инфекционно-воспалительной природы (табл. 2).
До терапии панадолом в 8,1% наблюдений состояние больных расценивалось как тяжелое и в 67,6% средней тяжести. После трехдневного лечения почти у 4/5 пациентов общее состояние отмечено как удовлетворительное и только у 21,6% средней тяжести.
Как видно из представленных данных, по большинству из контролируемых клинических показателей отмечена благоприятная положительная динамика симптомов, указывающая на хороший противовоспалительный эффект лекарственного препарата.
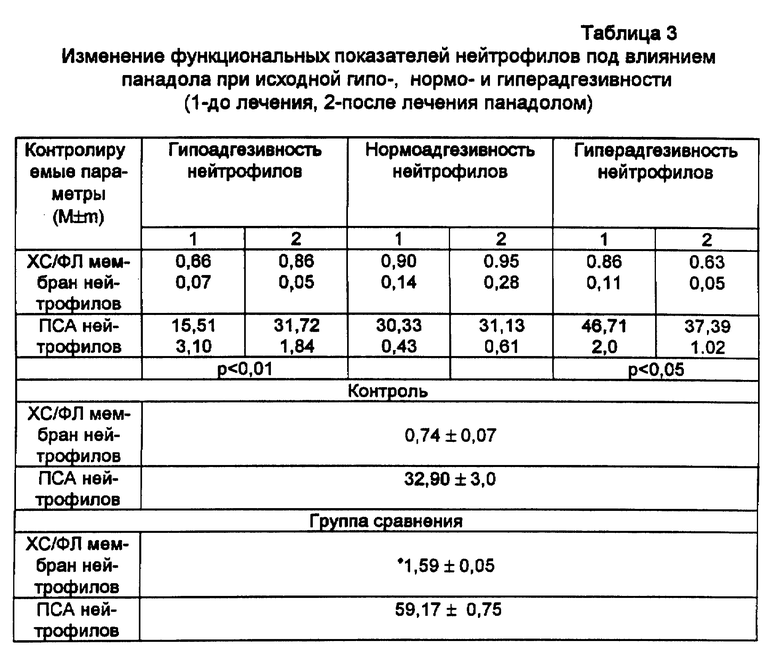
При исследовании влияния панадола на отдельные функциональные показатели лейкоцитов установлено, что его эффекты дифференцируются в зависимости от исходного уровня нейтрофилов. В качестве базового оценочного показателя использовали величину спонтанной адгезии нейтрофилов, характеризующую гипо-, нормо- или гиперфункцию клеток (табл.3).
Как видим, панадол оказывает отчетливое рекондиционирующее влияние в отношении лейкоцитарных клеток, восстанавливая адгезивную способность лейкоцитов со сниженной или повышенной функцией.
Можно полагать, что механизм такого воздействия опосредуется через стабилизацию клеточной мембраны, о чем свидетельствуют изменения показателей микровязкости мембран, коррелирующие с показателями спонтанной адгезии нейтрофилов.
Итак, терапия панадолом приводит к стабилизации клеток, что вызывает отчетливый клинический эффект, происходящий на фоне нормализации общего состояния.
В сравнении с контролируемыми параметрами у детей группы сравнения, не получавших панадола, в основной группе отмечено более раннее (на 0,85 сут) наступление и стабилизация полученного эффекта.
Клинические примеры. Больная Лена В., 8 мес. Ребенок от 1 доношенной беременности, протекавшей на фоне гестоза 1 половины, анемии. Масса ребенка при рождении 3.200 г, длина 51 см. Приложена к груди в первые сутки, естественное вскармливание до 7 мес. Голову держит с 2 мес, сидит с 6 мес, первые зубы с 8 мес. В возрасте 3 месяцев перенесла острое респираторно-вирусное заболевание. С рождения наблюдается невропатологом по поводу перинатальной энцефалопатии.
Настоящее заболевание у ребенка манифестировалось респираторным синдромом (насморк, сухой кашель). Со вторых суток состояние ухудшилось: повысилась температура тела до 38.8oC, отмечено снижение аппетита, вялость. При осмотре состояние ребенка расценено как средне тяжелое. Ребенок в сознании, психоэмоциональная лабильность. Кожные покровы чистые, гиперестезия кожи. Легкий цианоз носогубного треугольника. Частота дыханий 50 в мин. При перкуссии коробочный звук над обоими легкими. Дыхание проводится во все отделы, жесткое, выслушиваются единичные сухие хрипы. Пульс 140 ударов в минуту. Тоны сердца ясные, ритмичные. Живот мягкий, безболезненный. Печень выступает на 0.5 см из-под края реберной дуги, селезенка не пальпируется.
Общий анализ крови: эритроциты - 4.2 Т/л, гемоглобин-124 г/л, лейкоциты-11.5 Г/л, эозинофилы - 2%, нейтрофилы палочкоядерные - 2%, сегментоядерные - 36%, лимфоциты - 56%, моноциты - 4%, СОЭ 12 мм/час. Показатель спонтанной адгезии нейтрофилов - 48,5%, коэффициент Хс/Фл мембран нейтрофилов - 0.66 у.е.
Ребенку назначен "Детский панадол" в возрастной дозе. Через 3 дня после лечения состояние больного расценено как близкое к удовлетворительному. Ребенок в сознании, активен, на осмотр реагирует адекватно. Аппетит сохранен, объем питания удерживает. Кожные покровы чистые, телесной окраски. Мышечный тонус удовлетворительный. Кашель влажный, продуктивный, стал реже.
Отделяемое из носовых ходов уменьшилось. Частота дыханий - 30 в минуту. Дыхание пуэрильное с жестковатым оттенком, проводится во все отделы, хрипов нет. Частота сердечных сокращений - 128 ударов в минуту. Тоны сердца ритмичные, ясные. Живот мягкий, безболезненный. Печень 0.5 см из-под края реберной дуги.
Показатель адгезии нейтрофилов - 35.78%, показатель Хс/Фл - 0.72 у.е.
Итак, проведенное клиническое исследование показало высокую эффективность препарата "Детский панадол" при острых инфекционно-воспалительных заболеваниях респираторной системы, сопровождающихся гиперпирексией (лихорадкой). Установлено, что препарат оказывает модулирующий эффект в отношении клеточных мембран лейкоцитов, что способствует улучшению их функциональной активности, сокращает сроки воспалительной реакции, способствует более раннему клиническому выздоровлению.
С другой стороны, можно полагать, что стабилизация цитомембран лейкоцитов препятствует воздействию на клетки различных инфекционных и неинфекционных пирогенов, образованию и выделению из них вторичных эндогенных пирогенов, прерывая каскадную лихорадочную реакцию. Мы ни в одном случае не наблюдали рецидива гипертермии у больных основной группы наблюдения, в то время как в группе сравнения у 15,0% пациентов выявлено повторное повышение температуры тела на третьи сутки заболевания.
Таким образом, заявляемое средство оказывает целенаправленное терапевтическое воздействие на нейтрофилы, профилактируя повреждение тканей полиморфно-ядерных лейкоцитов, прерывая каскадную лихорадочную реакцию, что позволяет улучшить исходы, предупредить развитие осложнений, уменьшить продолжительность гиперепирексии и сократить длительность течения заболеваний.


Изобретение относится к медицине, а именно к педиатрии. Выявлены иммуномодулирующие свойства парацетамола, ранее известного для лечения гипертермических состоянии, возникающих при острых заболеваниях респираторной системы (ОРВИ, острый бронхит, острая пневмония) у детей. Острые респираторные заболевания служили как модель патологического состояния у детей. В качестве контролируемых параметров использовались показатели гемограммы микровязкости мембран нейтрофилов, спонтанной адгезии нейтрофилов, определяемые до и на четвертые сутки от начала терапии панадолом. Выявлено целенаправленное иммуномодулирующее воздействие заявляемого средства на нейтрофилы, восстанавливающее их функциональную активность, профилактируя повреждение тканей полиморфно-ядерными лейкоцитами. С другой стороны, стабилизация мембраны лейкоцитов препятствует воздействию на клетки различных инфекционных и неинфекционных пирогенов, образованию и выделению из них вторичных эндогенных пирогенов, прерывая каскадную лихорадочную реакцию. Изобретение позволяет улучшить исходы, предупредить развитие осложнений, уменьшить продолжительность гиперепирексии и сократить длительность течения заболеваний. 3 табл.
Применение панадола в качестве средства стабилизации клеточной мембраны и улучшения функциональных свойств нейтрофилов со сниженной функциональной активностью у детей с острыми заболеваниями инфекцинно-воспалительной природы.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Машковский М.Д | |||
| Лекарственные средства | |||
| - М.: Медицина, 1993, ч.1, с.203 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Ткаченко В.К | |||
| и др | |||
| Пути оптимизации лекарственных нагрузок при острых респираторных вирусных инфекциях у детей | |||
| Педиатрия | |||
| - М.: Медицина, 1988, N 7, с.63-68 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| WO 96040152 A1, 19.12.96. | |||
Авторы
Даты
2000-06-20—Публикация
1997-04-09—Подача