Предлагаемое изобретение относится к терапии и предназначено для лечения состоянии и заболеваний, сопровождающихся гиперагрегацией тромбоцитов. В настоящее время в результате многочисленных экспериментальных и клинических исследований установлено, что повышенная способность тромбоцитов к агрегации сопровождает течение ряда тяжелых болезней человека: инфаркта миокарда, сердечной и церебральной ишемии, атеросклероза, сахарного диабета, гипертонической болезни и др. При сахарном диабете, в частности, гиперкоагуляция является одним из этиологических факторов диабетических ангиопатий, которые становятся ведущей причиной инвалидизации и смертности больных. Гиперагрегация приводит к накоплению в циркулирующей крови тромбоцитарных агрегатов и в конечном итоге к окклюзии сосудов. Известно, что при прогрессировании вышеуказанных заболеваний нарастает гиперкоагуляция крови и депрессия фибринолиза.
В терапии и профилактике заболеваний и состояний, сопровождающихся гиперагрегацией тромбоцитов, в настоящее время широко используют антиагреганты: пентоксифиллин (трентал); тиклопедин (тиклид).
Недостатком вышеуказанных препаратов как при внутривенном, так и при оральном их применении являются геморрагические осложнения, тромбопения, лейкопения, агранулоцитоз, выраженные аллергические реакции, а также невозможность использования этих препаратов из-за их противопоказаний при выраженном склерозе коронарных сосудов и сосудов мозга, при обострении язвенной болезни желудка и двенадцатиперстной кишки, заболеваниях печени, беременности и кормлении грудью.
Задачей предлагаемого способа является получение препарата, который расширяет диапазон использования и позволяет получить желаемый дезагрегирующий эффект при отсутствии побочных геморрагических осложнений и т.д. за счет использования препарата, обладающего как дезагрегирующим, так и фибринолитическим эффектом.
Известно, что тромбоцитам принадлежит важная роль в поддержании нормальной резистенции и функции кровеносных сосудов. Тромбоциты для выполнения своих функций содержат в себе более пятидесяти биологически активных веществ. Все эти вещества находятся в тромбоцитах раздельно в плотных гранулах, α- гранулах и лизосомах. Примечательно, что тромбоциты несут в себе биологически активные вещества диаметрально противоположного действия, например, активаторы и ингибиторы фибринолитической системы, агреганты и дезагреганты. Поэтому трудно себе представить, что в процессе необратимой агрегации тромбоцитов, когда одновременно происходит и выделение биологически активных веществ, и формирование тромбоцитарной пробки, чтобы последняя удерживала в себе равновесное содержание активаторов и ингибиторов фибринолитической системы, а также агрегантов и дезагрегантов. В этом случае тромбоцитам вряд ли удалось реализовать свою основную физиологическую функцию в закрытии дефекта в кровеносном сосуде.
Исходя из этого была поставлена задача, получение препарата из аутоплазмы, обладающего дезагрегирующим и фибринолитическим действием. Так как в тромбоцитарной пробке преобладают вещества, угнетающие фибринолиз и агреганты, вещества же противоположного действия по мере формирования тромбоцитарного сгустка (тромба) выделяются тромбоцитами в плазму и уносятся током крови, то поэтому, запустив механизм необратимой агрегации тромбоцитов (in vitrum) с последующим их удалением, получают плазму - аутогемокомпонентный препарат, обладающий дезагрегирующим и фибринолитическим действием. Формирование тромбоцитарной пробки, т.е. запуск механизма необратимой агрегации происходит при воздействии на тромбоциты тромбина, коллагена и АДФ (аденозин дифосфорной кислоты). Вышеуказанные агреганты широко используются в клинико-лабораторной практике. Известно, что аденозин трифосфорная кислота (АТФ) не относят к агрегантам и поэтому в этом качестве ее никогда не использовали в клинико-лабораторной практике. Однако еще в 1965 г. G. Marr показал, что в плазме уже через несколько секунд 50% АТФ превращается в АДФ (Баркаган 3.С., "Геморрагические заболевания и синдромы". М., 1980, с. 12-13).
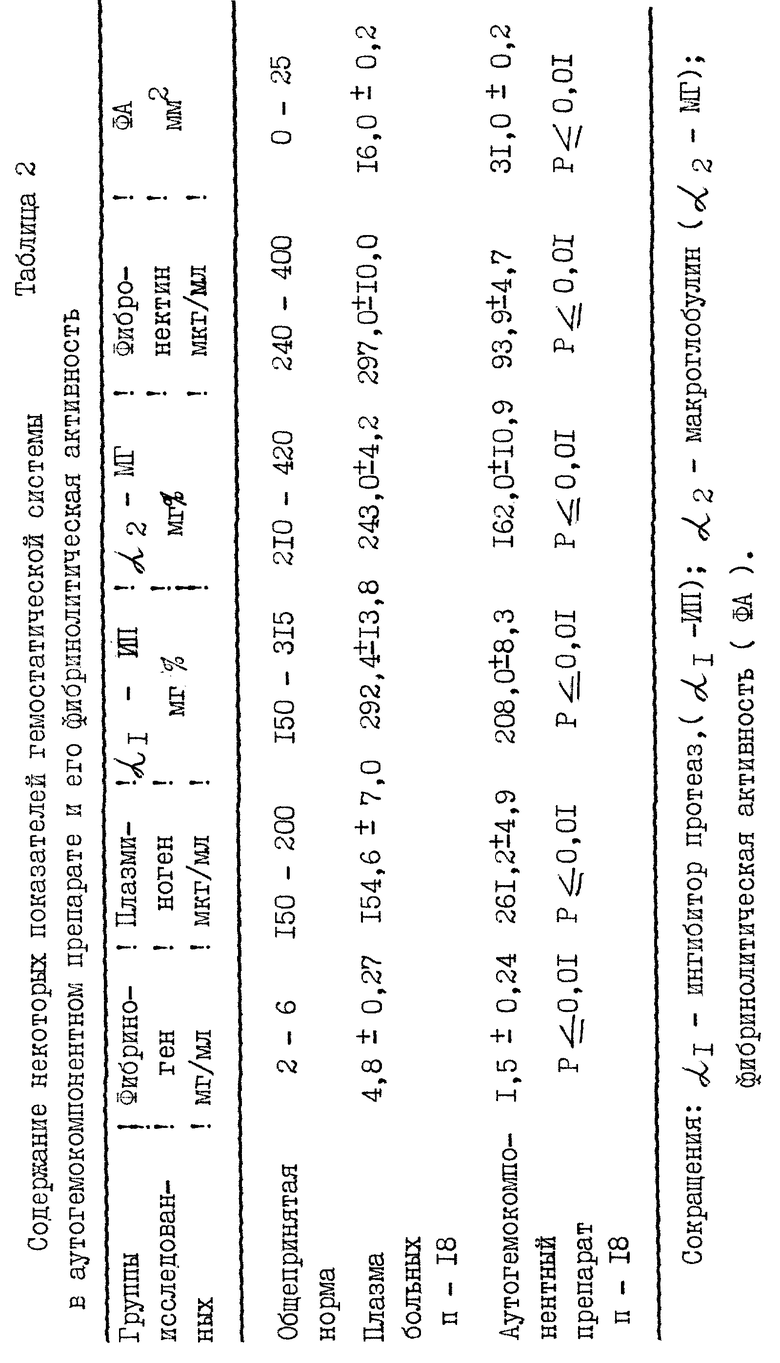
Исследования показали, что при предлагаемом способе лечения состояний, сопровождающихся гиперагрегацией тромбоцитов путем внутривенного введения аутогемокомпонентного препарата достоверно снижается агрегация тромбоцитов (P ≤ 0,01) (см. табл. 1). Кроме этого, в аутопрепарате по сравнению с интактной плазмой происходят следующие качественные и количественные изменения: повышается концентрация плазминогена (P ≤0,01), снижается (P ≤0,01) концентрация ингибиторов протеолитических ферментов (α1 - ингибитор протеаз; α2 - макроглобулин), снижается (P ≤ 0,01) концентрация фибриногена и фибронектина при одновременном повышении фибринолитической активности (P ≤ 0,01) (см. табл. 2). Методики определения указанных в таблице показателей общеизвестны (Калашников B. B., Маркова 0.А., Платонова Т.К., Свищев A.B. // Тезисы международного симпозиума "Проблемы развития работ по лабораторно-диагностической технике". ВНМТО МЗ СССР, Смоленск, 1988, с. 41-44 и с. 47-50; Андреенко Г.В., Карабасова М.А., Лютови Л.В. и др. "Методы исследования фибринолитической системы крови. - М., Издательство Московского Университета, 1981, с, 43- 46; Manchini G., Vaerman I.P., Carbonava A.0. Heremans I.E. A single-radial-diffusion method for the immunological quantitation of proteins, in Peeters H (Ed.). Protides of thebiological Fluids, Elsevier Publisching Comp. Amsterdam, London, New-Jork, 1964; 11th colloguirn, Brudes, 1963, p. 370-373). Дезагрегирующее свойство и повышение фибринолитической активности аутогемокомпонентного препарата достигалось только при условии одномоментного введения в кювету АТФ, необходимой для максимальной агрегации аутотромбоцитов. Результаты этих исследований послужили предпосылкой для предлагаемого способа лечения.
Способ осуществлялся следующим образом: кровь берут из локтевой вены в количестве, как правило, 10,0 мл, шприцем емкостью 10,0 мл, в котором находится антикоагулянт - гепарин в количестве 34 ЕД. Далее определяют агрегацию тромбоцитов по известному способу Born-O'Brien (Born V.R. Aggregation of blood plateletes by adenosine diphosphate and its reversal. Nature, 1962, vol. 194, p. 927-939), но с использованием в качестве агреганта аденозинтрифосфорную кислоту АТФ использовали в количестве 0,1-0,5 мг/мл в зависимости от индивидуальной реакции тромбоцитов на воздействие АТФ для достижения максимальной агрегации тромбоцитов (в среднем до 50% падения оптической плотности тромбоцитов). Затем полученную суспензию центрифугировали при скорости оборотов 3000 об/мин в течение 2-3 мин и полученную таким образом надосадочную жидкость (аутогемокомпонентный препарат) вводили внутривенно в количестве 5,0-10,0 мл.
Пример 1. Больной Н.И.Д., 37 лет. Диагноз. Сахарный диабет. Препролиферативная диабетическая ретинопатия обоих глаз. Страдает сахарным диабетом в течение 20 лет. Снижение остроты зрения на оба глаза отмечает последние 2 года. Коэффициент агрегации тромбоцитов повышен - 165,0 мм. В течение 4 лет принимает трентал и тиклид, однако коэффициент агрегации тромбоцитов остается резко повышенным.
До лечения. Коэффициент агрегации тромбоцитов 170,0 мм. На флюоресцентной ангиограмие глазного дна обоих глаз выявлены зоны ишемии сетчатки. Острота зрения: правого глаза -0,3 с коррекцией = 0,4, левого глаза - 0,3 с коррекцией = 0,5.
Лечение. Кровь брали из локтевой вены 20,0 мл стерильным шприцом емкостью 10,0 мл, в котором до забора крови находился гепарин 34,0 ЕД. Общепринятым способом отделяли эритроциты от плазмы крови. Полученную плазму делили для удобства на порции по 2,0 мл. В первой определяли агрегацию тромбоцитов (по вышеуказанному методы), добавляя постепенно АТФ. Максимальная агрегация тромбоцитов была достигнута при суммарном введении АТФ 0,4 мг/мл. В остальные порции интактной плазмы одномоментно вводили такое же количество АТФ -0,4 мг/мл и по достижении максимальной агрегации тромбоцитов производили центрифугирование при скорости оборотов 3000 об/мин в течение 2-3 мин и полученную таким образом надосадочную жидкость (аутогемокомпонентный препарат) вводили внутривенно в количестве 5,0-10,0 мл, через 14 сут, всего 5 инъекций.
Результаты лечения. Коэффициент агрегации тромбоцитов снизился до верхней границы нормы - 41,0 мм. Острота зрения повысилась на 0,1 на каждом глазу; уменьшилось число зон ишемии сетчатки.
Пример 2. Больной Ш.В.А., 58 лет, страдает ишемической болезнью сердца (стенокардией напряжения) около 9 лет. За последний год боли в области сердца участились до 4-5 раз в сутки, несмотря на максимальный режим приема сустка, нитронга и панангина, болевой синдром не купировался до 2 ч, боль сопровождалась чувством нехватки воздуха (одышкой) и учащенным сердцебиением. Кроме изменений на электрокардиограмме, характерных для ишемической болезни сердца, был повышен почти в 5 раз (180,0 мм) коэффициент агрегации тромбоцитов.
Лечение проводилось аутогемокомпонентным препаратом (на фоне обычного лечения - нитронг, сустак), который вводили внутривенно в количестве 5,0-10,0 мл, на курс лечения потребовалось 4 инъекции. На вторые сутки после начатого лечения состояние больного заметно улучшилось - исчезла одышка, частота и интенсивность боли в области сердца уменьшились при исследовании агрегации тромбоцитов - выявлен выраженный дезагрегационный эффект. Коэффициент агрегации снизился до 4 6 мм. Кроме того, на ЭКГ отмечена положительная динамика процесса, что свидетельствовало об эффективности использованного препарата.

Изобретение относится к медицине и предназначено для лечения состояний, сопровождающихся гиперагрегацией тромбоцитов. Для этого в аутоплазму добавляют аденозинтрифосфорную кислоту (АТФ), определяют ее количество, достаточное для максимальной агрегации тромбоцитов, и вводят ее в такой же объем интактной аутоплазмы. Затем ее центрируют и получающуюся надсадочную жидкость (аутогемокомпонентный препарат) вводят внутривенно в количестве 5,0 -10,0 мл. Способ позволяет эффективно лечить состояния, сопровождающиеся гиперагрегацией тромбоцитов. 2 табл.
Способ лечения состояний, сопровождающихся гиперагрегаций тромбоцитов путем внутривенного введения препарата - дезагреганта, отличающийся тем, что в качестве дезагреганта используют аутогемокомпонентный препарат, представляющий собой надосадочную жидкость аутокрови больного, полученную в результате агрегации тромбоцитов под одномоментным воздействием 0,1 - 0,5 мг АТФ на 1 мл плазмы и последующего центрифугированием, причем препарат вводят в количестве 5,0 - 10,0 мл.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Абдулкадыров К.М | |||
| Гемогомпонентная терапия при заболеваниях системы крови | |||
| - Клиническая медицина, 1994, N 2, с | |||
| Печь-кухня, могущая работать, как самостоятельно, так и в комбинации с разного рода нагревательными приборами | 1921 |
|
SU10A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Баркаган З.С | |||
| геморрагические заболевания и синдромы | |||
| - М., 1980, с | |||
| Способ гальванического снятия позолоты с серебряных изделий без заметного изменения их формы | 1923 |
|
SU12A1 |
Авторы
Даты
2000-06-20—Публикация
1997-02-12—Подача