Настоящее изобретение относится к способу очистки акриловой кислоты. Более конкретно, предлагается способ проведения непрерывного процесса с получением высокочистой акриловой кислоты, содержащей очень малые количества остаточного альдегида.
При получении акриловой кислоты каталитическим окислением пропилена до последующей очистки вначале акриловую кислоту (АК) и побочные продукты окисления получают в виде водного раствора АК. При осуществлении "процедуры экстракции/перегонки" водный раствор АК экстрагируют подходящим органическим растворителем, получая экстракт АК, который затем подвергают азеотропной перегонке и дегидратации, удаляя таким образом из экстракта воду и рекуперируя органический растворитель для повторного использования в процессе. При осуществлении другой процедуры очистки, "процедуры прямой перегонки", стадию экстрагирования водного раствора минуют и водный раствор АК обрабатывают непосредственно перегонкой и дегидратацией. При осуществлении любой процедуры полученная дегидратированная АК или "сырая" АК содержит кислотные примеси, в частности, уксусную кислоту, малеиновую кислоту и малеиновый ангидрид, а также содержит альдегидные примеси, в частности, акролеин, фурфурол и бензальдегид, и другие побочные продукты окисления. Уксусную кислоту можно удалять из дегидратированной АК фракционной перегонкой, получая АК с низким содержанием уксусной кислоты, которую также называют "сырой" АК и которая, тем не менее, содержит и другие компоненты. При осуществлении процедуры экстракции некоторое количество малеиновой кислоты и другие кислотные примеси сбрасывают в сточные воды, что требует, следовательно, дорогостоящей обработки сточных вод. При осуществлении процедуры прямой перегонки эти же самые примеси превращаются в сбрасываемое в отход органическое масло, которое можно сжигать, утилизируя его топливную ценность. Таким образом, несмотря на практическое применение в промышленности обоих способов, процедура прямой перегонки для более новых установок, предпочтительнее, даже несмотря на то, что ее осуществление усугубляет затруднения технологического порядка при очистке АК, содержащей заметные количества малеиновой кислоты и малеинового ангидрида. По настоящему изобретению можно применять оба эти метода, и оно особенно предпочтительно при осуществлении метода прямой перегонки.
Обычная фракционная перегонка сырой АК (САК) дает возможность удалять большую часть примесей малеиновой кислоты и малеинового ангидрида и других высококипящих примесей, таких как терефталевая кислота, получая таким путем перегнанную АК, которая может быть использована в качестве исходного материала для получения акрилатных эфиров или некоторых полимеров. Однако только обычная фракционная перегонка оказывается неэффективной при попытке снизить содержание альдегидов до необходимого уровня с получением высокочистой акриловой кислоты (ВЧАК), которую можно использовать для получения полимеров со средней молекулярной массой, превышающей среднюю молекулярную массу полимеров, полученных из перегнанной АК. Для получения ВЧАК "сырую" АК после процедуры либо экстракции/перегонки, либо прямой перегонки необходимо очищать до такой степени, которая превышает достигаемую обычной фракционной перегонкой, поскольку остаточные примеси, в частности, альдегиды, препятствуют протеканию реакций полимеризации. Содержание индивидуальных альдегидов должно быть ниже приблизительно десяти частей на миллион (частей/млн.), предпочтительно ниже пяти частей/млн. и наиболее предпочтительно ниже одной части/млн. ВЧАК, содержащая столь малые количества альдегидов, может быть использована, например, при получении суперабсорбентных полимеров и полимеров, являющихся эффективными диспергаторами в составе растворов для бурения нефтяных скважин и флокулянтами.
Известно, что перегонкой АК в присутствии аминов или аналогичных соединений содержание альдегидов в АК можно снизить до частей/млн. Так, например, в U.S.Research Disclosure N 167066 содержание фурфурола предлагается снижать до < 1 части/млн. обработкой сырой или перегнанной акриловой кислоты небольшими количествами флорглюцинола, орто(о-)- фенилендиамина, или анилина; полагают, что эти амины образуют с фурфуролом комплекс или его разлагают с получением продукта, который затем можно выделить фракционной перегонкой. В описании к патенту США 3725208 (далее "208") говорится, что при периодическом добавлении в частично очищенную (предположительно предварительно перегнанную) "сырую" акриловую кислоту, содержащую альдегиды, по меньшей мере одного из нижеследующих веществ: серная кислота, гидразин, фенилгидразин, анилин, моноэтаноламин, этилендиамин или глицин, и выдержке образовавшейся смеси в течение 3 ч при 70oC перед фракционной перегонкой получают дистиллят АК, содержащий уменьшенные количества альдегидов. В описании к патенту США 4828652 (далее "652") утверждается, что для обработки перед фракционной перегонкой сырой АК "технического сорта" (также предположительно перегнанного сорта) эффективны аминогуанидин или его соли в соотношении от 1 до 3 молей на моль альдегида с выдержкой по меньшей мере 1-1,5 ч.
Однако при осуществлении вышеописанных способов снижения содержания альдегидов возникают проблемы. Так, например, при осуществлении известных способов применяют прием единовременного или одноразового добавления аминов в АК сырых сортов или в сырую АК перегнанного сорта, и требуется значительная продолжительность выдержки перед перегонкой, как сказано в описании к патенту "652". В этом описании говорится также, что согласно предпринимавшимся ранее усилиям, связанным с добавлением гидразина или водных гидразиновых растворов, для снижения содержания фурфурола до уровня ниже 5 частей/млн. требовались приблизительно 4-мольный избыток гидразина на моль альдегида и особые условия перегонки. Более того, в таких условиях дистилляционная колонна становилась покрытой побочными продуктами. Хотя в описании к патенту "208" сказано, что можно использовать такие амины, как анилин, моноэтаноламин и этилендиамин, в указанных условиях наиболее низкого остаточного содержания альдегидов достигали только с помощью гидразина или фенилгидразина, и для достижения низкой концентрации альдегидов требовались их большие количества и длительное время выдержки. Если присутствовали малеиновая кислота и малеиновый ангидрид, то возникают дополнительные проблемы: когда их общее содержание в САК превышает приблизительно 0,1 вес.%, при добавлении избыточного количества амина либо по периодическому, либо по непрерывному методу может произойти образование обильного количества твердых частиц. Такие твердые частицы могут засорять оборудование и вызывать простой на время очистки. Кроме того, из-за параллельно протекающей реакции амина с малеиновым ангидридом необходимо добавлять избыточные количества амина, поскольку реакция с малеиновым ангидридом кинетически превосходит реакцию с фурфуролом и бензальдегидом. Реакции с малеиновым ангидридом можно избежать при помощи предварительной перегонки САК, однако это является дорогостоящей операцией, которую было бы целесообразно устранить. В дальнейшем было установлено, что при введении амина только в верхнюю часть или вблизи этой верхней части фракционной дистилляционной колонны во время перегонки САК возникает еще одна проблема: в случае, если САК содержит свыше приблизительно 10 частей/млн. акролеина, добавление амина таким путем вызывает интенсивное образование внутри колонны полимера и других твердых продуктов.
Таким образом, когда САК содержит не только альдегиды, но также и типичные примеси, упомянутые выше, прежде всего, малеиновую кислоту и малеиновый ангидрид, возникает необходимость в разработке эффективного способа, прежде всего способа непрерывного получения ВЧАК из САК.
Авторами настоящего изобретения разработан экономичный непрерывный способ снижения концентрации альдегидов в САК, содержащей существенные количества акролеина, фурфурола, а также малеиновых кислоты и ангидрида. Осуществление такого способа дает возможность получать ВЧАК, содержащую менее 10 частей/млн. , и позволяет достигать содержания менее 1 части/млн. индивидуального остаточного альдегида без необходимости предварительной перегонки САК для удаления малеинового ангидрида. Отличительные признаки изобретения применительны также в отношении более ранних технологических стадий, связанных с предварительными источниками АК, как это проиллюстрировано ниже. Более того, способ по изобретению позволяет предотвратить засорение оборудования полимерными и другими твердыми частицами, в частности, при использовании некоторых выбранных аминов. Такой способ позволяет также получать ВЧАК с содержанием малеинового ангидрида менее 100 частей/млн; его преимущество заключается в том, что с его помощью можно свести к минимуму применение дорогостоящих аминов и что его осуществление сопровождается образованием минимального количества новых сбрасываемых в отход материалов по сравнению с известными способами. В широком аспекте в предлагаемом по изобретению способе предусмотрено использование аминов выбранных групп в различных точках непрерывного процесса получения ВЧАК. В одном из вариантов для получения исходного потока сырой акриловой кислоты в САК добавляют один или несколько аминов из одной выбранной группы аминов (группы A). В исходном потоке САК амин группы A быстро реагирует с акролеином и другими "легкими" альдегидами (альдегидами, кипящими при более низкой температуре, чем АК), эффективно удаляя их из летучих компонентов в колонне. Исходный поток САК направляют во фракционную дистилляционную колонну и перегоняют. Благодаря разделительной способности колонны малеиновая кислота, малеиновый ангидрид и более высококипящие компоненты, такие как терефталевая кислота, удерживаются вблизи нижней части колонны. Одновременно с перегонкой исходного потока САК аминовый исходный поток из одного или нескольких аминов из другой выбранной группы аминов (группы B) вводят в верхнюю или вблизи верхней части колонны для упрощения удаления всех оставшихся летучих альдегидов, в частности, фурфурола, и малеинового ангидрида. Получаемый дистиллят, который может включать в себя полимеризационные стабилизаторы, представляет собой ВЧАК.
Более конкретно, предлагается способ непрерывного получения высокочистой акриловой кислоты (ВЧАК), включающий стадии:
а) подачи в дистилляционную колонну исходного потока сырой акриловой кислоты при температуре от 25 до 100oC, причем этот исходный поток включает в себя:
I) сырую акриловую кислоту и
II) минимально эффективное количество при величине молярного отношения в интервале от 0,1 до 2,0 к общему числу молей альдегидов, малеиновой кислоты и малеинового ангидрида в сырой акриловой кислоте по меньшей мере одного амина группы A, выбранного из группы, состоящей из:
I) первичного ариламина структурной формулы (I)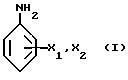
где значения X1 и X2 выбраны из группы, состоящей из H, NR2, OR, Cl и R, где значения R выбраны из H или C1-C2алкилов;
II) гидразина, необязательно его гидрата, формулы R2-NH-NH2, где значения R2 выбраны из H, фенила, 4-нитрофенила и 2,4-динитрофенила;
III) алкиленполиамина структурной формулы (II)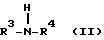
где значения R3 выбраны из H или C1-C6алкиленаминов, а R4 обозначает C1-C6алкиленамин, и
IV) α-аминокислоты, выбранной из группы соединений структурной формулы (III)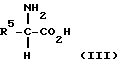
где значения R5 выбраны из H, R или R4; аргинина, аспарагиновой кислоты, глутаминовой кислоты, гистидина и метионина;
б) одновременной подачи в верхнюю часть дистилляционной колонны исходного аминового потока, содержащего минимально эффективное количество при величине молярного отношения от 0,01 до 1,0 к общему числу молей альдегидов, малеиновой кислоты и малеинового ангидрида в сырой акриловой кислоте по меньшей мере одного амина группы B, выбранного из группы, состоящей из о-, м-, п-фенилендиамина, 4-нитрофенилгидразина и 2,4-динитрофенилгидразина, и
в) фракционной перегонки исходного потока сырой акриловой кислоты в дистилляционной колонне в присутствии исходного аминового потока с отгонкой ВЧАК, содержащей остаточные количества индивидуальных альдегидов менее 10 частей/млн.
К другим аминам, которые, как было установлено, оказались эффективными в способе, описанном непосредственно выше, и которые входят в группу A аминов, относятся
I) первичный ариламин структурной формулы (IV)
где значения X3 выбраны из группы, состоящей из -COOH и -COOR6, где значения R6 выбраны из C1-C6алкилов, и
II) алканоламин структурной формулы (V)
HO-R7-NH2 (V)
где значения R7 выбраны из C2-C6алкиленов. Их использование в процессе получения ВЧАК идентично тому, что описано непосредственно выше в отношении определенных выше аминов группы A.
Непрерывный процесс можно также проводить путем добавления амина из группы A в предыдущую колонну, использованную для получения САК, например, в колонну азеотропной перегонки или колонну для удаления уксусной кислоты, более полно описанную ниже. Готовый поток САК направляют в конечную дистилляционную колонну с одновременными подачей амина из группы B в верхнюю часть этой конечной дистилляционной колонны и отгонкой ВЧАК.
В другом варианте выполнения изобретения для снижения содержания малеинового ангидрида ("малеина") в САК перед перегонкой прежде всего пригодны амины другой группы. Такая обработка особенно целесообразна, поскольку при этом образуются малеиновые аддукты, которые практически растворимы в САК, что дает возможность предотвратить засорение трубопроводов и дистилляционных колонн нерастворимыми материалами. Эту особую группу аминов называют группой S, и как и амины группы A, амины группы S, в дополнение к снижению концентрации малеинового компонента в САК, также высоко эффективны при снижении содержания акролеина на этой стадии обработки перед перегонкой. При такой обработке одному или нескольким аминам группы S дают время для реакции с потоком САК перед последующей ректификацией обработанного потока. Продолжительность выдержки в присутствии амина группы S определяют по тому количеству времени, которое требуется для снижения содержания акролеина до уровня менее 10 частей/млн., а малеинового ангидрида до менее 50% от его первоначального содержания в САК. По истечении времени такой выдержки в обработанный аминами S поток либо непосредственно перед перегонкой, либо, как описано выше для случая с аминами группы B, в верхнюю часть дистилляционной колонны добавляют один или несколько аминов из другой группы аминов, называемых аминами группы P, которые описаны ниже, для дополнительного снижения во время перегонки остаточной концентрации альдегидов, в частности, фурфурола и бензальдегида, до менее 10 частей/млн. Таким образом, дополнительно предлагается способ получения высокочистой акриловой кислоты (ВЧАК), включающий стадии:
а) введения в исходный поток сырой акриловой кислоты при величине молярного отношения от 0,1 до 2,0 к общему числу молей альдегидов, малеиновой кислоты и малеинового ангидрида в исходном потоке сырой акриловой кислоты одного или нескольких аминов группы S, выбранных из группы, которая охватывает
I) алкиленполиамин структурной формулы (II)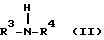
где значения R3 выбраны из H или C1-C6алкиленаминов, a R4 обозначает C1-C6алкиленамин;
II) орто-толуидин, мета-толуидин и
III) алканоламин формулы (V)
HO-R7-NH2 (V)
где значения R7 выбраны из C2-C6алкиленов;
б) выдержки исходного потока сырой акриловой кислоты и подаваемого амина группы S при температуре от 25 до 100oC при времени выдержки от 15 с до 150 ч с получением обработанного исходного потока;
в) подачи обработанного исходного потока в дистилляционную колонну;
г) одновременного введения при величине молярного отношения от 0,01 до 1,0 к общему числу молей альдегидов, малеиновой кислоты и малеинового ангидрида в сырой акриловой кислоте по меньшей мере одного амина группы P, выбранного из группы, которая включает о-, м-, п-фенилендиамины, 4-нитрофенилгидразин, 2,4-динитрофенилгидразин, фенилгидразин, гидразин и анилин, в обработанный исходный поток, направленный в дистилляционную колонну, необязательно в верхнюю часть этой дистилляционной колонны, и
д) перегонки обработанного исходного потока в присутствии амина группы P в дистилляционной колонне с получением ВЧАК, в которой остаточное содержание индивидуальных альдегидов составляет менее 10 частей/млн.
Как указано выше, САК представляет собой дегидратированную АК и обычно включает в себя, например, нижеследующие кислоты и альдегиды в указанных весовых количествах: акролеин, содержащийся в пределах приблизительно от нескольких частей/млн. до 300 частей/млн.; бензальдегид и фурфурол, содержание каждого из которых составляет примерно 200-400 частей/млн.; малеиновая кислота и малеиновый ангидрид (совместно) приблизительно до 1,0 вес.% (содержание измеряют в пересчете на малеиновую кислоту), и прочие компоненты, в частности, уксусную кислоту и терефталевую кислоту. Водные растворы АК и экстракт АК являются источниками АК, предшествующими САК, и содержат те же самые кислоты и альдегиды, что и САК, и воду.
В процессе приготовления исходного потока САК (или другого источника АК) амин группы A или S можно добавлять в САК (или другой источник АК) либо в чистом виде, либо в виде раствора в подходящем растворителе, таком как вода, или насыщенной карбоновой кислоте, такой как пропионовая, капроновая или валериановая кислота. Амин группы A или S выбирают из вышеописанных аминов и согласно изложенному ниже. R - алкильная группа структурной формулы (I) первичного ариламина - представляет собой C1-C6алкил, т.е. алкильную группу, содержащую от 1 до 6 углеродных атомов, в любой изомерной форме, в частности, метил, этил, пропил, изопропил, н-, изо- или втор.-бутил, гексил или изомер такой группы. R6 обозначает C1-C6алкил. Эффективны также дизамещенные первичные ариламины, в частности, диаминотолуолы и диметиланилины. Были охарактеризованы гидразины (или гидраты) R2-NH-NH2; достоинство гидрата состоит в простоте и безопасности обращения с ним. C1-C6алкиленовые группы, R3 и R4, алкиленполиамина содержат от 1 до 6 углеродных атомов каждая, в частности, метиленовые, этиленовые, пропиленовые, бутиленовые, гексиленовые и их изомеры, и несут первичные амины. К примерам алкиленполиаминов структурной формулы II относятся этилендиамин, диэтилентриамин и дипропилентриамин. Описаны альфа-аминокислоты. Обозначенные R7 C2-C6алкиленовые группы алканоламина V охватывают, например, этиленовые, пропиленовые, бутиленовые и гексиленовые группы и их изомеры. К примерам соединений V относятся моноэтаноламин, 1,3- и 1,2-пропаноламины.
Амин группы A выбирают с таким расчетом, чтобы он быстро и практически необратимо вступал в реакцию с акролеином и другими легкими альдегидами, присутствующими в САК или других источниках АК, предшествующих САК. Большинство аминов группы A вступает в реакцию в технологическом потоке как только САК или другой источник АК поступает совместно с амином в дистилляционную колонну; можно также принять меры для увеличения продолжительности пребывания по методам, известным в данной области техники, в частности, такие, как применение буферной емкости на линии непрерывной подачи сырья. Хотя группа A включает в себя относительно дорогостоящие амины, в частности, фенилендиамины, предпочтительно использовать менее дорогие амины, в частности, анилин, о-метиланилин, гидразингидрат, диэтилентриамин, лизин, метионин и глицин, которые особенно эффективны в отношении акролеина (было установлено, что такие алкиламины, как бутиламин, реагируют медленнее и их применение требуется в более существенных количествах, чем, например, анилина и других "быстрореагирующих" аминов, поэтому их не включают в число аминов группы A). Обычно просто использовать те амины группы A и их смеси, которые при температуре ниже 70oC находятся в жидком состоянии. По причинам стоимости, эффективности, доступности и простоты в обращении при выполнении изобретения класс предпочтительных аминов группы A включает в себя анилин, о-, м- и п-метиланилин, гидразин и гидразингидрат, диэтилентриамин, глицин, лизин, метионин и моноэтаноламин; принимая во внимание стоимость и эффективность при снижении загрязненности акролеином, более предпочтительны анилин, о-метиланилин, гидразин, гидразингидрат и моноэтаноламин; из них наиболее предпочтительными являются анилин и моноэтаноламин.
Одновременно с подачей в дистилляционную колонну исходного потока САК, содержащей амин группы A, либо в чистом виде, либо в форме раствора, как это описано для случая добавления амина группы A, один или несколько аминов группы B вводят в верхнюю часть той же самой колонны, т.е. вводят в головку или в пределах верхних 30% по высоте колонны, но всегда выше исходного потока САК, обработанной амином группы A. Эффективные амины группы B определены выше; их выбирают таким образом, чтобы они быстро и практически необратимо реагировали с фурфуролом. По причинам стоимости, доступности и эффективности предпочтительные амины группы B включают в себя мета-фенилендиамин, 4-нитрофенилгидразин и 2,4-динитрофенилгидразин; из них наиболее предпочтителен метафенилендиамин. С использованием предпочтительных аминов легко получать ВЧАК с остаточным содержанием индивидуальных альдегидов менее 5 частей/млн., а с помощью наиболее предпочтительных аминов - менее 1 части/млн.
Другим вариантом выполнения изобретения с использованием аналогичным путем аминов групп A и B является введение одного или нескольких аминов группы A в источник АК, например, в водный раствор АК, с получением исходного потока источника АК, который направляют в колонну азеотропной дегидратации. После дегидратации полученная САК характеризуется низким содержанием акролеина (< 10 частей/млн. ) и отсутствием влаги. Источником АК может также служить экстракт, т.е. водный раствор АК, подвергнутый экстракции подходящим органическим растворителем; вместо водного раствора акриловой кислоты в колонну азеотропной дегидратации направляют конечный экстракт АК. Как и любой источник АК, подаваемый в колонну, амин группы A также можно подавать в эту колонну азеотропной дегидратации в виде отдельного потока. Полученную САК с низким содержанием акролеина (теперь уже в дегидратированном виде) далее направляют, но не обязательно, в другую фракционную дистилляционную колонну для удаления уксусной кислоты с получением таким образом САК с низким содержанием акролеина, характеризующейся также низким содержанием уксусной кислоты (< 2000 частей/млн.), или непосредственно в конечную дистилляционную колонну. Достоинство добавления амина группы A в водный раствор или экстракт АК состоит в том, что любой раствор не содержит малеиновой кислоты в ее ангидридной форме, благодаря чему амин группы A не расходуется на его реакцию с малеиновым ангидридом.
Таким образом, предлагается также способ непрерывного получения высокочистой акриловой кислоты (ВЧАК), включающий стадии: а) подачи в первую дистилляционную колонну исходного потока источника акриловой кислоты при температуре от 25 до 100oC, причем этот исходный поток источника включает в себя I) источник акриловой кислоты, выбранный из группы, которая охватывает водный раствор акриловой кислоты и экстракт акриловой кислоты; II) минимальное эффективное количество при величине молярного отношения от 0,1 до 2,0 к общему числу молей альдегидов, малеиновой кислоты и малеинового ангидрида в источнике акриловой кислоты одного или нескольких аминов группы A, выбранных из тех же самых аминов группы А, что описана выше; б) дегидратации исходного потока источника акриловой кислоты с получением сырой акриловой кислоты с низким содержанием акролеина менее 10 частей/млн.; в) необязательной отгонки уксусной кислоты из сырой акриловой кислоты с низким содержанием акролеина с получением сырой акриловой кислоты с низким содержанием акролеина, характеризующейся пониженной концентрацией уксусной кислоты; г) последующей подачи в конечную дистилляционную колонну I) сырой акриловой кислоты с низким содержанием акролеина и II) одновременно в верхнюю часть этой конечной дистилляционной колонны исходного потока амина, содержащего минимально эффективное количество при величине молярного отношения от 0,01 до 1,0 к общему числу молей альдегида, малеиновой кислоты и малеинового ангидрида в сырой акриловой кислоте с низким содержанием акролеина одного или нескольких аминов группы B, выбранных из группы, которая охватывает о-, м-, п-фенилендиамины, 4-нитрофенилгидразин и 2,4-динитрофенилгидразин, и д) фракционной перегонки сырой акриловой кислоты с низким содержанием акролеина в этой конечной дистилляционной колонне с отгонкой ВЧАК, остаточное содержание индивидуальных альдегидов в которой составляет менее 10 частей/млн.
В другом варианте выполнения изобретения, в котором из аминов вышеописанных групп предусмотрено добавление одного или нескольких аминов группы A или, как в данном варианте, также группы S, в САК с высоким содержанием уксусной кислоты (> 2000 частей/млн.). Исходный поток такой САК с высоким содержанием уксусной кислоты можно направлять в колонну для отгонки уксусной кислоты, т.е. в дистилляционную колонну, используемую для эффективного снижения путем отгонки содержания уксусной кислоты в САК. В результате перегонки САК, обработанной амином группы A, получают САК с низким содержанием акролеина (а теперь также и с низким содержанием уксусной кислоты) (амин группы A можно вводить в колонну для удаления уксусной кислоты в виде отдельного потока по мере подачи в эту колонну САК с высоким содержанием уксусной кислоты). Далее САК с низким содержанием акролеина вводят в конечную дистилляционную колонну, в частности, в колонну для отгонки высокочистой акриловой кислоты, в которой осуществляют заключительные стадии перегонки.
Таким образом, дополнительно предлагается способ непрерывного получения высокочистой акриловой кислоты (ВЧАК), включающий стадии: а) подачи в колонну для отгонки уксусной кислоты исходного потока при температуре от 25 до 100oC, причем этот исходный поток включает в себя I) сырую акриловую кислоту с высоким содержанием уксусной кислоты и II) минимально эффективное количество при величине молярного отношения от 0,1 до 2,0 к общему числу молей альдегидов, малеиновой кислоты и малеинового ангидрида в сырой акриловой кислоте с высоким содержанием уксусной кислоты одного или нескольких аминов группы A или группы S, выбранных из тех же самых аминов групп A и S, что описаны выше; б) отгонки уксусной кислоты из исходного потока с получением сырой акриловой кислоты с низким содержанием акролеина, характеризующейся содержанием уксусной кислоты менее 2000 частей/млн. и содержанием акролеина < 10 частей/млн.; в) последующей подачи в конечную дистилляционную колонну I) сырой акриловой кислоты с низким содержанием акролеина и II) одновременно в верхнюю часть этой конечной дистилляционной колонны исходного потока амина, содержащего минимально эффективное количество при величине молярного отношения от 0,01 до 1,0 к общему числу молей альдегида, малеиновой кислоты и малеинового ангидрида в сырой акриловой кислоте с низким содержанием акролеина одного или нескольких аминов группы B, выбранных из группы, которая охватывает о-, м-, п-фенилендиамины, 4-нитрофенилгидразин и 2,4-динитрофенилгидразин, и г) фракционной перегонки сырой акриловой кислоты с низким содержанием акролеина в этой конечной дистилляционной колонне с отгонкой и получением таким образом ВЧАК, остаточное содержание индивидуальных альдегидов в которой составляет менее 10 частей/млн. В данном варианте, где используют один из аминов группы S, при осуществлении стадии отгонки уксусной кислоты обычно предусмотрена достаточная "продолжительность выдержки". Во время подачи обработанной амином САК с низким содержанием уксусной кислоты в дистилляционную колонну амин группы P можно использовать путем одновременной подачи при величине молярного отношения от 0,01 до 1,0 к общему числу молей альдегидов, малеиновой кислоты и малеинового ангидрида в сырой акриловой кислоте по меньшей мере одного амина группы B, упомянутой выше, или фенилгидразина, гидразина или анилина в обработанную амином сырую акриловую кислоту с низким содержанием уксусной кислоты, поступающую в дистилляционную колонну, необязательно в верхнюю часть этой дистилляционной колонны с последующей отгонкой обработанной амином сырой аминокислоты с низким содержанием уксусной кислоты в присутствии амина группы P в этой дистилляционной колонне с получением в результате ВЧАК, остаточное содержание индивидуальных альдегидов в которой составляет менее 10 частей/млн.
Достоинство таких технических решений, где предусмотрено использование, например, либо водных источников АК, либо САК с высоким содержанием уксусной кислоты, заключается в том, что акролеин и другие легкие альдегиды удаляют в начале процесса очистки АК в сочетании с таким дополнительным преимуществом, как ослабление тенденции к полимеризации АК в процессе ее очистки, что позволяет, следовательно, уменьшить количество ингибитора полимеризации при проведении последующих операций обработки. Таким образом, амины группы A или S могут эффективно использоваться для частичной очистки акриловой кислоты в ходе проведения непрерывного процесса на стадии, предшествующей подаче в конечную фракционную дистилляционную колонну, с получением ВЧАК и для устранения в определенной мере тенденции акриловой кислоты к полимеризации в процессе очистки. Точно также предпочтительные амины группы A и группы B, описанные выше, предпочтительно использовать в вариантах выполнения изобретения в отношении водных растворов как источников АК и САК с высоким содержанием уксусной кислоты. Вышеописанные способы позволяют получать ВЧАК с остаточным содержанием индивидуальных альдегидов < 10 частей/млн., предпочтительно < 5 частей/млн. и наиболее предпочтительно < 1 части/млн., причем использование предпочтительных аминов позволяет легко достичь содержания < 5 частей/млн. и более предпочтительных - < 1 части/млн.
Чтобы свести к минимуму потери АК в форме полимера любую перегонку по изобретению проводят под пониженным давлением, обычно менее 200 мм рт.ст., при температуре в нижней части колонны менее 150oC, предпочтительно менее приблизительно 100oC. Когда в САК или другие источники АК, описанные выше, вводят амин группы A или S, температура содержащего АК исходного потока должна превышать 25oC, предпочтительно быть выше 40oC, достигая уровня 100oC; температурный интервал от 40 до 80oC предпочтителен. При таких температурах образуется меньше твердых частиц, чем при температуре 25oC и ниже.
Непрерывные процессы по изобретению отличаются от "периодических" процессов; в ходе проведения этих последних в дистилляционную установку загружают фиксированное количество САК или источника АК, которое вступает в реакцию с фиксированным количеством амина с уменьшением содержания альдегида (благодаря однократному добавлению амина или добавлению одной порцией), после чего проводят перегонку с получением фиксированного количества очищенного продукта. Для периодических процессов из-за времени, которое требуется для загрузки, реакции, перегонки и очистки, характерна пониженная производительность в сравнении с непрерывными процессами по изобретению. Непрерывные процессы по изобретению отличаются также от "совмещенных периодических и непрерывных" процессов, в которых обработку САК или источника АК амином для уменьшения содержания альдегида проводят вначале в реакторе периодического действия, а затем предварительно обработанную САК или другой источник непрерывно подают в дистилляционную колонну. Для проведения этих последних процессов требуется наличие дополнительных реакторов и емкостей для хранения, которые необязательны в ходе проведения непрерывного процесса по изобретению. В варианте с применением аминов группы S аминовую обработку можно производить с помощью операции периодического типа, хотя предпочтителен непрерывный вариант. После обработки амином группы S оставшиеся стадии обработки амином группы P и перегонки предпочтительно осуществлять непрерывно.
"Минимально эффективное количество" одного или нескольких аминов группы A, добавляемое в сырье для дистилляционной колонны (или непосредственно в саму колонну), определяют измерением содержания акролеина на выходе (например, в дистилляте) из дистилляционной колонны или другой установки, в которую направляют обработанный амином группы A поток (в вариантах, в которых амин группы A вводят в точках технологической линии перед стадией конечной перегонки, содержание акролеина измеряют в основном АК содержащем потоке, получаемом из установки, например, в потоке нижней части, в которую вводят обработанный амином поток). В любом случае амин группы A добавляют в источник, подаваемый в установку, до тех пор, пока измеренное содержание акролеина не достигнет менее 10 частей/млн. Количество амина группы A, необходимое для снижения содержания акролеина до < 10 частей/млн., определяют как "минимально эффективное количество" для амина (аминов) группы A. Минимально эффективное количество амина группы A превышает то минимально эффективное количество, которое обычно необходимо для достижения пониженного содержания остаточного акролеина, в частности, такого, как 5 и 1 часть/млн., но количество всех используемых аминов группы A находится в вышеуказанном интервале.
Минимально эффективное количество амина группы B определяют измерением содержания фурфурола в дистилляте конечной дистилляционной колонны. Затем количество амина группы B, которое добавляют в конечную дистилляционную колонну, увеличивают до тех пор, пока измеренное содержание фурфурола не достигнет < 10 частей/млн. Количество амина группы B, которое конкретно необходимо для снижения содержания фурфурола до < 10 частей/млн., определяют как "минимально эффективное количество" амина (аминов) группы B. В вариантах выполнения изобретения, в которых используют амин группы B, минимально эффективное количество амина группы B определяют после определения минимально эффективного количества амина группы A и по мере того, как продолжается подача амина группы A. Минимально эффективное количество амина группы B превышает то минимально эффективное количество, которое обычно необходимо для достижения пониженного содержания остаточного фурфурола, в частности, такого, как 5 и 1 часть/млн., но количество всех используемых аминов группы B находится в вышеуказанном интервале.
Амин группы S выбирают с учетом того, чтобы он быстро и практически необратимо реагировал с акролеином и другими легкими альдегидами, присутствующими в САК или других источниках АК, предшествующих САК, с образованием аддуктов малеинового ангидрида, которые практически растворимы в обработанной САК. Термины "практически растворимый" или "практически ненерастворимый" означают, что количество нерастворимого твердого материала в обработанной смеси с САК не превышает 1 вес.% от веса обработанной смеси; в предпочтительном варианте содержание нерастворимого твердого материала составляет < 0,1 вес. %. Амины группы S особенно эффективны, когда содержание малеина превышает 0,1 вес. % от САК, где нерастворимый твердый материал, образующийся не благодаря аминам группы A, а по другим причинам, может вызвать проблемы из-за присутствия в технологическом потоке твердого материала. Большинство аминов группы S вступает в технологическом потоке в реакцию по мере поступления САК или другого источника АК в дистилляционную колонну в присутствии таких аминов; необходимо принять меры для увеличения "продолжительности выдержки" по методам, известным в данной области техники, в частности, таким, как применение буферной емкости на линии непрерывной подачи. Продолжительность выдержки может быть достаточно короткой, измеряемой секундами, когда температура обработанного потока САК приближается, например, к 100oC, а также довольно длительной, до 150 ч, когда температура обработанного потока приближается к комнатной. Необходимо иметь в виду, что продолжительность выдержки могла бы быть увеличена неопределенно, как, например, для операции периодического типа до нескольких недель; столь большая продолжительность предусмотрена рамками изобретения. Нормальная продолжительность выдержки обычно составляет менее 150 ч.
Минимально эффективное количество одного или нескольких аминов группы S является таким, которое снижает содержание акролеина до менее 10 частей/млн. , а содержание малеинового ангидрида до менее 50% от его начальной концентрации в период выдержки. В общем, чем больше количество в указанных интервалах, тем короче продолжительность выдержки. Минимально эффективное количество амина группы S больше минимально эффективного количества, которое обычно необходимо для достижения пониженного остаточного содержания акролеина, в частности, такого, как 5 и 1 часть/млн., и содержания малеинового ангидрида менее 50%, но количество всех используемых аминов группы S находится в вышеуказанном интервале.
Амины группы P представляют собой амины выбранной группы, используемые для "окончательной обработки" САК, обработанной аминами группы S. Критерии их выбора аналогичны критериям, указанным в отношении аминов группы B. Действительно, амины группы P включают в себя амины группы B, а также вышеупомянутые анилин, гидразин и фенилгидразин. Амины группы P оказались неожиданно эффективными, когда для преддистилляционной обработки используют амины группы S, поскольку амины группы S эффективно снижают содержание малеина и других примесей до такого достаточно низкого уровня, при котором практически исключается образование нерастворимых твердых материалов с аминами группы P перед и во время перегонки.
Остаточное содержание индивидуальных альдегидов в получаемой согласно всем вариантам выполнения изобретения ВЧАК составляет менее 10 частей/млн.
Некоторые варианты выполнения настоящего изобретения далее подробно описаны в нижеследующих примерах.
Примеры
Общая процедура
В примерах и сравнительных примерах используют следующие аббревиатуры: САК - сырая акриловая кислота; ГХ - гидрохинон; МеГХ - монометиловый эфир гидрохинона; мФД - м-фенилендиамин; ФТЗ - фенотиазин; МЭА - моноэтаноламин; Пр. - пример; к.т. - комнатная температура, означающая температуру окружающей среды или приблизительно равную 25oC; символами < и > обозначено соответственно "меньше" и "больше". Для анализа состава на акролеин, бензальдегид и фурфурол использовали газовую хроматографию, а для определения малеиновых кислоты и ангидрида - жидкостную хроматографию высокого давления; пороги чувствительности в обоих методах анализа составляли < 1 части/млн. Результаты анализов на малеиновые кислоту и ангидрид объединяли, поскольку при осуществлении процедуры анализа весь ангидрид преобразовывали в кислоту; таким образом, результаты анализа на малеиновые кислоты и ангидрид выражены как содержание "малеиновой кислоты/ангидрида" (когда данные содержания малеиновой кислоты/ангидрида приведены для дистиллята, они, наиболее вероятно, относятся к малеиновому ангидриду, поскольку по данным парциального давления известно, что малеиновая кислота отгоняется с головными погонами из колонны, из которой в виде головного погона получают акриловую кислоту, в ничтожных количествах). Когда амины вводили в САК или другие источники АК, добавляемое количество выражали в величине молярного соотношения между амином и общим числом молей акролеина, бензальдегида, фурфурола и малеиновой кислоты/ангидрида, измеренным в исходном потоке установки, в которую подавали этот исходный поток. Для примеров с перегонкой данные анализов дистиллята обычно были средними для двух или большего числа анализов проб, ежечасно отбираемых в устойчивом режиме, т.е. при проведении непрерывной операции. Данные анализов, превышавшие 100 частей/млн., обычно округляли до двух значащих цифр.
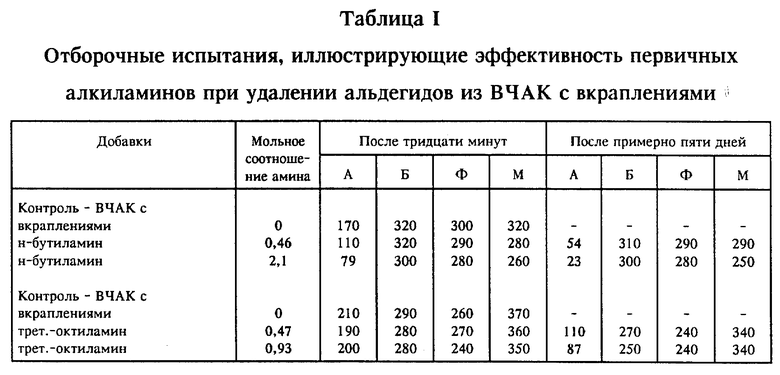
Отборочные испытания проводили добавлением указанных количеств амина в аликвоты исходного раствора ВЧАК с вкраплениями нижеследующих примесей, взятыми в количествах, указанных в примерах в частях/млн.: акролеин, бензальдегид, фурфурол и малеиновый ангидрид (в таблицах акролеин, бензальдегид, фурфурол и малеиновую кислоту/ангидрид обозначали соответственно символами A, Б, Ф и М, а данные приводили в частях/млн.). Аликвоты, содержавшие амин, во всех случаях, за исключением специально оговоренных, перемешивали в течение тридцати минут при 23-25oC и непосредственно после этого анализировали. По истечении приблизительно пяти дней выдержки при 23-25oC аликвоты, содержавшие амин, анализировали повторно. Контрольными образцами служили те образцы с вкраплениями, в которые амин не добавляли.
При проведении отборочных испытаний для определения того, какие амины могли бы быть полезными в качестве аминов группы A, B, S или P по изобретению, пользовались нижеследующими критериями. Амин считали полезным для использования в качестве амина группы A или S, если при величине относительного молярного количества до 2 он уменьшал содержание акролеина до < 10 частей/млн. Амин считали особенно эффективным, если снижение содержания акролеина достигалось в течение 30 мин. Что касается амина, который может быть использован в качестве амина группы A или S, то нет необходимости в том, чтобы он снижал концентрацию бензальдегида и/или фурфурола до конечного низкого уровня ВЧАК (достигаемого с последующим использованием амина группы B или P). Амин группы S дополнительно демонстрировал практически полное отсутствие нерастворимых твердых материалов в потоке САК (т.е., как указано выше, содержание нерастворимых твердых материалов не превышало 1 вес.% от веса потока) и снижение содержания малеинового ангидрида в течение 5-дневной выдержки при комнатной температуре до уровня ниже 70% от его первоначальной концентрации. Амин считали приемлемым для использования в качестве амина группы B, если он (I) демонстрировал 50%-ное снижение содержания фурфурола в течение 30 мин при величине молярного отношения к нему амина менее 1,0 и (II) проявлял обратимость реакции с фурфуролом (при величине молярного отношения к нему амина менее 1,0), в результате которой по истечении приблизительно 5 дней в контрольном образце количество образовавшегося фурфурола достигало менее чем 70%-ного уровня от первоначального. Аналогичные критерии были применимы в отношении аминов группы P: либо те же, что и для аминов группы B, либо способность по меньшей мере к 90%-ному снижению содержания фурфурола в дистилляте при использовании в сочетании с амином группы S.
Пример 1; получение ВЧАК, когда амином группы A служил анилин, а амином группы B - мФД
Использовали колонну Олдершоу 2,54 см (один дюйм) с пятнадцатью тарелками, снабженную ребойлером с паровым обогревом. САК, содержавшую 85 частей/млн. акролеина, 220 частей/млн. бензальдегида, 240 частей/млн. фурфурола и 7200 частей/млн. малеиновой кислоты/ангидрида, предварительно подогревали пропусканием ее через теплообменник. В движущийся поток предварительно подогретой САК добавляли анилин (при величине молярного соотношения 0,5) и температуру этого движущегося исходного потока САК во время его подачи в "куб", т. е. в сосуд в нижней части колонны, поддерживали на требуемом уровне. Колонна работала при следующих условиях: давление в головке - приблизительно 35 мм рт. ст. ; расход потока САК - примерно 211 г/ч; флегмовое число - около 1,6; процентная доля всего исходного продукта, удаляемого в виде дистиллята, - приблизительно 86%; температура исходного потока САК - примерно 50oC; температура в кубе колонны - примерно 83oC и температура в головке колонны - приблизительно 65oC. С целью ингибировать полимеризацию ингибитор использовали в следующем количестве от количества САК: примерно 0,5 вес.% воздуха в ребойлер, приблизительно 0,1 вес.% МеГХ в конденсаторе, около 0,03 вес. % ФТЗ и примерно 0,06 вес.% ГХ на тарелку N 11 (нумерация снизу вверх). Одновременно с этим на пятнадцатую тарелку, в верхнюю часть колонны, при величине молярного соотношения 0,08 подавали мФД. В стабильных условиях в течение семичасового периода дистиллят ВЧАК постоянно содержал < 1 части/млн. каждой из таких примесей, как акролеин, бензальдегид и фурфурол, а также 2 части/млн. малеиновой кислоты/ангидрида. При этом не возникало никаких проблем с образованием твердых материалов в трубопроводах, питающих куб колонны, или в самом кубе, а также проблем, связанных с образованием какого-либо полимера или других твердых материалов в колонне.
Пример 2; получение ВЧАК, когда амином группы A служил гидразингидрат, а амином группы B - мФД
Повторяли условия эксперимента примера 1, за исключением того, что (I) в куб вместо анилина вводили гидразингидрат (при величине молярного соотношения 0,5), (II) мФД (при величине молярного соотношения 0,2) вводили на одиннадцатую тарелку и (III) САК содержала 91 часть/млн. акролеина, 210 частей/млн. бензальдегида, 250 частей/млн. фурфурола и 6100 частей/млн. малеиновой кислоты/ангидрида. В стабильных условиях в течение двух часов дистиллят ВЧАК постоянно содержал < 1 части/млн. каждой из таких примесей, как акролеин, бензальдегид и фурфурол, а также 2 части/млн. малеиновой кислоты/ангидрида. При этом не возникало никаких проблем с образованием твердых материалов в кубе колонны, а также проблем, связанных с образованием какого-либо полимера или других твердых материалов в колонне. Довольно несущественные количества твердых материалов наблюдали в трубопроводе для исходного потока САК, но в такой концентрации, которая не препятствовала проведению непрерывного процесса.
Гидразин испытывали без амина группы B в условиях, аналогичных тем, что указаны в примере 1, за исключением того, что (I) гидразин вводили в куб колонны при величине молярного соотношения 0,7 и (II) в колонну вводили амин группы В. В стабильных условиях в течение трех часов дистиллят содержал 2 части/млн. акролеина, < 1 части/млн. бензальдегида, < 1 части/млн. фурфурола и 13 частей/млн. малеиновой кислоты/ангидрида. Это показывает, что при некоторых условиях с использованием одного гидразина (при величине молярного соотношения 0,7) достигали относительно низкого содержания примесей, но он был не столь низким, как достигаемый с использованием также амина группы B, как это изложено в вышеприведенном Пр.2.
Сравнительный пример 1: перегонка САК без добавления амина группы A или B
В эксперименте сравнительного примера 1 создавали условия, аналогичные описанным в примере 1, за исключением того, что (I) в куб колонны не добавляли никакого амина группы A, (II) в колонну не вводили амина группы B и (III) САК содержала 66 частей/млн. акролеина, 230 частей/млн. бензальдегида, 270 частей/млн. фурфурола и 6600 частей/млн. малеиновой кислоты/ангидрида. В стабильных условиях в течение восемнадцати часов дистиллят постоянно содержал 38 частей/млн. акролеина, 3 части/млн. бензальдегида, 91 часть/млн. фурфурола и 70 частей/млн. малеиновой кислоты/ангидрида. При этом не возникало никаких проблем с образованием твердых материалов в трубопроводах, питающих куб колонны, или в самом кубе, а также проблем, связанных с образованием какого-либо полимера или других твердых материалов в колонне, но без добавления какого-либо амина содержание примесей в дистилляте значительно превышало допустимые пределы для ВЧАК.
Сравнительный пример 2: перегонка САК, когда амином группы A служил анилин, но без добавления какого-либо амина группы B
В эксперименте сравнительного примера 2 создавали условия, идентичные тем, что описаны в примере 1, за исключением того, что (I) в куб колонны вводили анилин (при величине молярного соотношения 0,6), (II) а в колонну амина группы В не добавляли. В стабильных условиях в течение двух часов дистиллят постоянно содержал < 1 части/млн. акролеина, 1 часть/млн. бензальдегида, 46 частей/млн. фурфурола и 58 частей/млн. малеиновой кислоты/ангидрида. При этом не возникало никаких проблем с образованием твердых материалов в трубопроводах, питающих куб колонны, или в самом кубе, а также проблем, связанных с образованием какого-либо полимера или других твердых материалов в колонне. Таким образом, хотя анилин, вводимый в куб, снижал содержание акролеина в достаточной мере, его было недостаточно для снижения содержания фурфурола до допустимого для ВЧАК уровня.
Сравнительный пример 3: перегонка САК, когда амином группы A служил анилин и исходный поток САК подавали при 23-25oC
В эксперименте сравнительного примера 3 создавали условия, идентичные тем, что описаны в примере 1, за исключением того, что (I) в куб колонны вводили анилин (при величине молярного соотношения 0,6), (II) в колонну амина группы B не добавляли, (III) САК содержала 91 часть/млн. акролеина, 210 частей/млн. бензальдегида, 250 частей/млн. фурфурола и 6100 частей/млн. малеиновой кислоты/ангидрида и (IV) температуру подачи исходного потока САК в колонну поддерживали на уровне 23-25oC. При этих условиях линия подачи САК засорялась твердыми частицами по истечении 4 ч, вынуждая останавливать работу колонны. Эти твердые частицы идентифицировали 1H-ЯМР-спектроскопией как N-фенилмалеиновую кислоту, т.е. продукт реакции анилина с малеиновым ангидридом.
Сравнительный пример 4: перегонка САК без амина группы A, когда амином группы B служит мДФ
В эксперименте сравнительного примера 4 создавали условия, идентичные тем, что описаны в примере 1, за исключением того, что (I) в куб колонны не вводили амина группы A, (II) в колонну вводили мДФ (при величине молярного соотношения 0,05), (III) САК содержала 69 частей/млн. акролеина, 230 частей/млн. бензальдегида, 270 частей/млн. фурфурола и 8100 частей/млн. малеиновой кислоты/ангидрида и (IV) температуру подачи исходного потока САК в колонну поддерживали на уровне 23-25oC. При этих условиях работа колонны нарушалась образованием большого количества полимера и других твердых частиц, что являлось причиной остановки колонны по истечении 30 мин. Кроме того, непосредственно перед остановкой дистиллят содержал 63 части/млн. акролеина, < 1 части/млн. бензальдегида, 4 части/млн. фурфурола и 2 части/млн. малеиновой кислоты/ангидрида. Таким образом, добавление амина только в верхнюю часть колонны оказывалось недостаточным для получения ВЧАК, поскольку образование полимера и других твердых частиц в колонне препятствовало непрерывной работе колонны. Данные показывали, что когда в САК не вводили амина группы A, но в верхнюю часть колонны добавляли амин группы B, в колонне происходило образование большого количества полимера и других твердых частиц.
Сравнительный пример 5: отборочные испытания с добавлением первичного алкиламина в ВЧАК с вкраплениями примесей
В эксперименте сравнительного примера 5 осуществляли вышеописанную общую процедуру отборочных испытаний, за исключением того, что в качестве аминов использовали первичные алкиламины. Полученные результаты сведены в таблицу I, данные которой показывают, что типичные первичные алкиламины, н-бутиламин и трет.-октиламин не могли служить аминами группы A (или группы B). Хотя первичные алкиламины оказывались в определенной мере пригодными для снижения содержания акролеина, они были неэффективными при получении ВЧАК.
Пример 3: oтборочные испытания с добавлением первичного ариламина во ВЧАК с вкраплениями примесей, в САК и водный раствор акриловой кислоты
В эксперименте примера 3 осуществляли вышеописанную общую процедуру отборочных испытаний за исключением того, что (I) в качестве аминов использовали первичные ариламины и (II) амин добавляли в аликвоты либо исходной ВЧАК с вкраплениями примесей, либо САК или водного раствора акриловой кислоты. Использовали эти источники АК, содержавшие акролеин, бензальдегид, фурфурол и малеиновую кислоту/ангидрид в количествах, указанных в таблице II в частях/млн. Водный раствор акриловой кислоты содержал приблизительно 35% воды.
Если основываться на вышеописанных критериях, то данные отборочных испытаний таблицы II показывают, что в качестве аминов группы A эффективными оказывались нижеследующие первичные ариламины: анилин, м-фенилендиамин, п-фенилендиамин, 1,5-диаминонафталин, п-аминофенол, п-метоксианилин, п-хлоранилин, о-метиланилин, м-метиланилин, п-метиланилин и п-нитроанилин. Кроме того, из таблицы II видно, что м-фенилендиамин являлся исключительно эффективным амином группы B; пригодным амином группы В являлся также п-фенилендиамин.
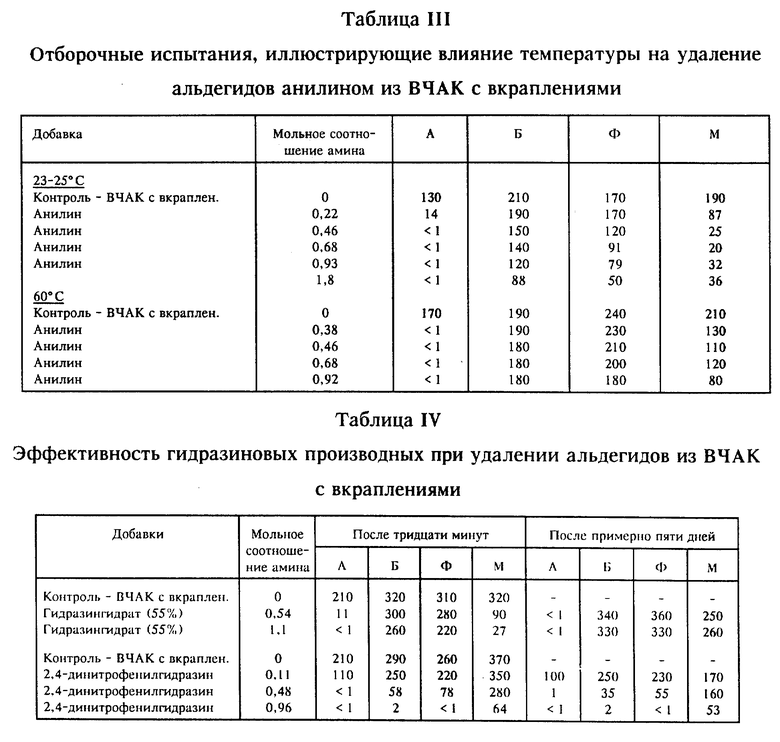
Пример 4: oтборочные испытания с исследованием эффекта температуры на добавление анилина в ВЧАК с вкраплениями примесей (23-25 и 60oC)
В эксперименте примера 4 пользовались общей процедурой, описанной выше для отборочных испытаний, за исключением того, что (I) использованный амин представлял собой анилин, (II) испытание проводили либо при 23-25oC, либо при 60oC и (III) аликвоты, содержавшие амин, анализировали только один раз по истечении 30 мин. Полученные результаты сведены в таблицу III; данные показывают, что по истечении тридцати минут анилин вступал в реакцию с компонентами, расположенными в следующем порядке снижения ее скорости: акролеин > малеиновый ангидрид > фурфурол > бензальдегид. Реакционная способность проявляла тенденцию к идентичности при 23-25 и 60oC. Однако при одном и том же количестве анилина содержание бензальдегида, фурфурола и малеинового ангидрида при температуре 60oC было более высоким, чем при 23-25oC. Таким образом, когда в САК или источник АК вводят амин группы A, для получения преимуществ от уменьшенного количества твердых частиц (как описано выше) предпочтительны также повышенные температуры, в частности, 50-60oC.
Пример 5: отборочные испытания с добавлением гидразингидрата и 2.4-динитрофенилгидразина в ВЧАК с вкраплениями примесей
В эксперименте примера 5 пользовались общей процедурой, описанной выше для отборочных испытаний, за исключением того, что аминами служили гидразин и его производные. Результаты, сведенные в таблицу IV, показывают, что как гидразингидрат, так и 2,4-динитрофенилгидразин оказывались эффективными в качестве аминов группы A; этот последний амин проявлял себя как исключительно эффективный амин группы B.
Пример 6: oтборочные испытания с добавлением алкиленполиамина или α-аминокиcлоты в ВЧАК с вкраплениями примесей
В эксперименте примера 6 пользовались общей процедурой, описанной выше для отборочных испытании, за исключением того, что аминами служили либо алкиленполиамины, либо α-аминокислоты. При этом в водный раствор добавляли глицин. Результаты сведены в таблицу V.
Приведенные в таблице V данные отборочных испытаний показывают, что диэтилентриамин, глицин, лизин, аргинин и гистидин оказывались эффективными аминами группы A.
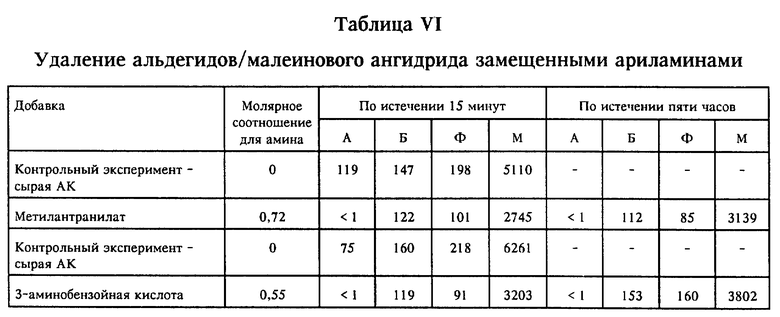
Пример 7: oтборочные испытания с добавлением ариламинов структурной формулы IV в ВЧАК с вкраплениями
В эксперименте примера 7 пользовались общей процедурой, описанной выше для отборочных испытаний, за исключением того, что в качестве аминов применяли метилантранилат или 3-аминобензойную кислоту. Эти испытания проводили при 48-52oC с использованием исходного раствора САК "контрольного" состава; результаты сведены в таблицу VI.
Представленные в таблице VI данные отборочных испытаний показывают, что эти замещенные ариламины оказывались высокоэффективными при снижении содержания акролеина до уровня ниже 10 частей/млн.
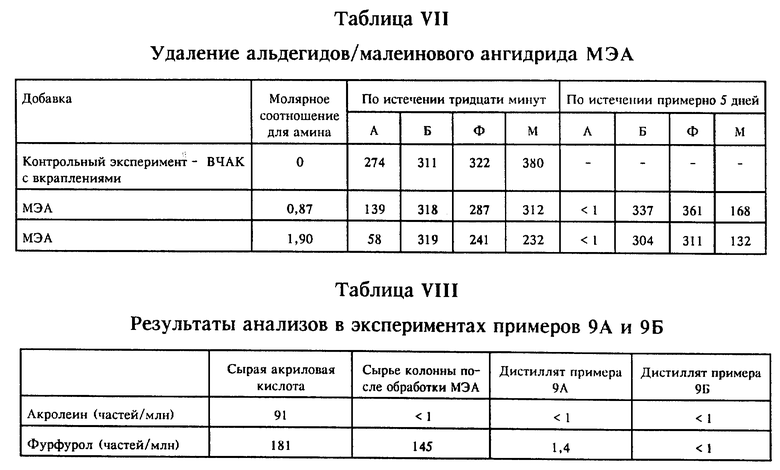
Пример 8: oтборочные испытания с добавлением моноэтаноламина в ВЧАК с вкраплениями
В эксперименте данного примера пользовались общей процедурой, описанной выше для отборочных испытаний, за исключением того, что в качестве амина применяли моноэтаноламин (МЭА). Аликвоты, содержавшие МЭА, перемешивали 30 мин при комнатной температуре и анализировали; анализ производили также по истечении 5-дневного периода выдержки. Полученные результаты сведены в таблицу VII. Данные этого отборочного испытания показывают, что моноэтаноламин оказывался исключительно эффективным при снижении содержания акролеина до менее 10 частей/млн. по истечении 5 дней при к.т., а также при уменьшении за тот же период содержания малеиновой кислоты/ангидрида до уровня существенно ниже 70% от их начального количества. Несмотря на замедленную реакцию в сравнении с реакцией некоторых вышеупомянутых аминов группы A. МЭА оказывался эффективным при уменьшении содержания акролеина в течение 30 мин и очень эффективным в течение увеличенного периода выдержки при комнатной температуре. При этом не наблюдали образования нерастворимых твердых частиц.
Пример 9: получение ВЧАК, когда амином группы S служил МЭА, а амином группы P - мФД
Пользовались колонной Олдершоу 5,08 см (два дюйма) с пятнадцатью тарелками, снабженной двухтрубчатым ребойлером с паровым обогревом. Исходную сырую акриловую кислоту обрабатывали при комнатной температуре смешением САК с 0,37 вес.% амина группы S, моноэтаноламина (МЭА), за период от 4 до 15 ч до подачи в главную расходную емкость дистилляционной колонны. Затем предварительно подогретую исходную сырую акриловую кислоту нагревали пропусканием через отдельный теплообменник. В предварительно подогретую и предварительно обработанную САК в процессе подачи этой смеси в дистилляционный куб добавляли амин группы P, м-фенилендиамин (мФД). Продолжительность контактирования между предварительно обработанной САК и мФД до подачи в куб составляла ≤ 10 с. Проводили два эксперимента:
Пр. 9А, в эксперименте которого в предварительно обработанную сырую акриловую кислоту добавляли 0,03-0,04 вес.% мФД, и
Пр. 9Б, в эксперименте которого в предварительно обработанную сырую акриловую кислоту добавляли 0,08-0,09 вес.% мФД. В таблице VIII сопоставлены результаты анализов исходной САК и соответствующих дистиллятов.
Данные показывают, что описанное сочетание МЭА с мФД оказывалось высокоэффективным при уменьшении содержания примесей; при большей величине молярного соотношения Пр. 9Б концентрацию фурфурола также снижали до < 1 части/млн. При этом не наблюдали никакого образования твердых частиц ни в питающих линиях или расходной емкости, ни в процессе перегонки, что подтверждает эффективность сочетания амина группы S с амином группы P.
Сравнительный пример 6: перегонка САК, когда амином группы S служил моноэтаноламин и без добавления амина группы P
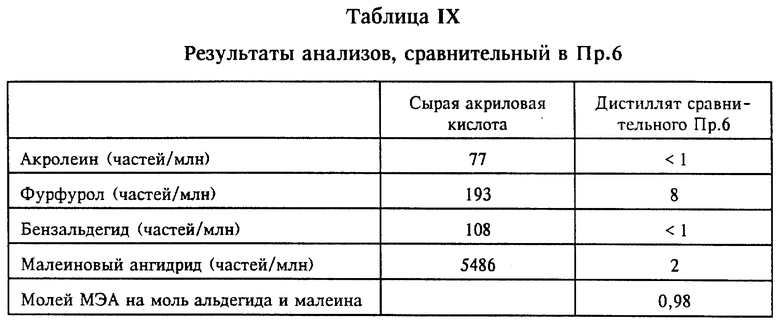
Данный пример иллюстрирует результаты перегонки САК, обработанной амином группы S, при отсутствии амина группы P. Создавали условия обработки и перегонки, аналогичные тем же условиям в эксперименте примера 9. САК обрабатывали 0,37 вес.% амина группы S, МЭА, в течение 4-15 ч до ее подачи в главную расходную емкость дистилляционной колонны, но без добавления амина группы P в предварительно обработанное сырье или в верхнюю часть дистилляционной колонны до или в процессе перегонки. После проведения перегонки в течение десяти часов в колонне и кубе не наблюдали образования полимерных или других твердых частиц, что указывало на эффективность МЭА в этой функции. Тем не менее, результаты анализов таблицы IX показывают, что остаточные примеси не удалялись столь же эффективно, как в случае использования также амина группы P (в частности, Пр.9); содержание фурфурола оказывалось более высоким, чем желательно, хотя МЭА эффективно снижал содержание акролеина до < 1 части/млн., а малеинового ангидрида до 2 частей/млн.
Сравнительный пример 7: обработка САК без использования аминов какой-либо группы
B данном сравнительном эксперименте без добавления какого-либо амина любой из вышеописанных групп, но при тех же условиях перегонки, что создавали в эксперименте примера 9, получали перегнанную САК, которая содержала 18 частей/млн. акролеина, 77 частей/млн. фурфурола, 3 части/млн. бензальдегида и 46 частей/млн. малеинового ангидрида. Это демонстрирует эффективность аминов как группы S, так и группы P, когда их использовали совместно, в частности в эксперименте примера 9.
Пример 10: получение ВЧАК, когда амином группы S служил МЭА, а амином группы P - анилин
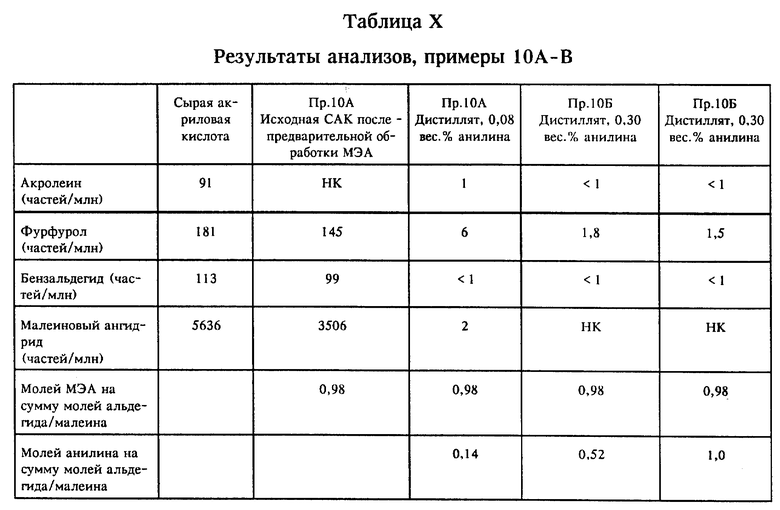
В экспериментах этого примера для получения ВЧАК последовательно использовали МЭА, амин группы S, и анилин, амин группы P. САК вначале обрабатывали 0,37 вес. % МЭА при комнатной температуре в течение 4-15 ч до подачи в главную расходную емкость дистилляционной колонны. Анилин вводили в предварительно обработанную сырую акриловую кислоту непосредственно перед перегонкой в концентрации 0,08 вес.% (Пр.10А), 0,30 вес.% (Пр.10Б) и 0,60 вес.% (Пр. 10В) от веса предварительно обработанной САК. Соответствующий исходный материал перегоняли с получением результатов анализов, которые сведены в таблицу X. По истечении в общем 23 ч процесса не наблюдали образования полимерных или других твердых частиц в колонне или кубе и не сталкивались ни с какими технологическими проблемами.
Результаты демонстрируют эффективность таких аминов при выполнении ими их соответствующих функций.
Пример 11: отборочные испытания аминов группы S в САК
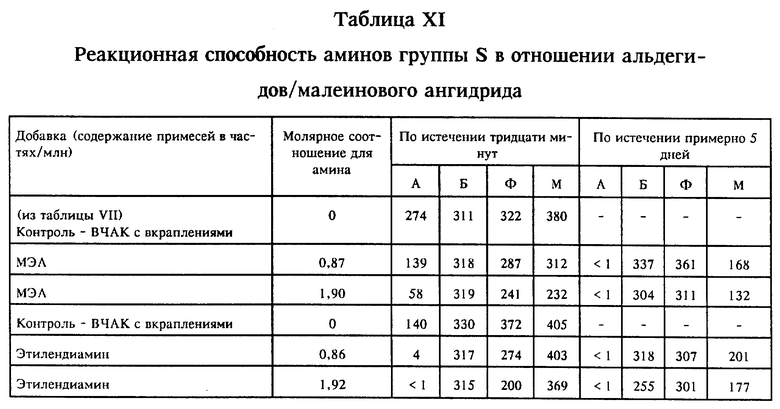
В качестве типичных аминов группы S оценивали эффективность МЭА и этилендиамина. Отборочные испытания проводили добавлением амина в указанных количествах в аликвоты исходного раствора ВЧАК с вкраплениями примесей в количестве 300 частей/млн. каждой из нижеследующих примесей: акролеин (А), бензальдегид (Б), фурфурол (Ф) и малеиновый ангидрид (М). Аликвоты, содержавшие амин, перемешивали тридцать минут при 23-25oC и непосредственно после этого анализировали. По истечении приблизительно пяти дней выдержки при 23-25oC аликвоты, содержавшие амин, анализировали повторно. Контрольными образцами служили те образцы с вкраплениями примесей, в которые амин не добавляли. В таблицу XI сведены результаты анализов, которые показывают эффективность этих аминов при снижении содержания акролеина и, по истечении 5 дней, малеинового ангидрида. Существенных количеств нерастворимых твердых частиц не обнаруживали; добавка только этилендиамина давала более 0,1 вес.% твердых частиц от общего веса смеси.
При проведении аналогичных испытаний с орто- и мета-толуидином при величинах молярного соотношения 0,9 и 1,0 снижали содержание акролеина в течение 30 мин до < 1 части/млн., а малеинового ангидрида за то же самое время до < 70% от первоначального количества без образования твердых частиц, что демонстрировало их эффективность в качестве аминов группы S (с другой стороны, добавление пара-толуидина давало более 1 вес.% твердых частиц, как определяли пропусканием испытываемой смеси через сито, поэтому его считали неудовлетворительным амином группы S).
Пример 12: oтборочные испытания типичных аминов группы P в САК
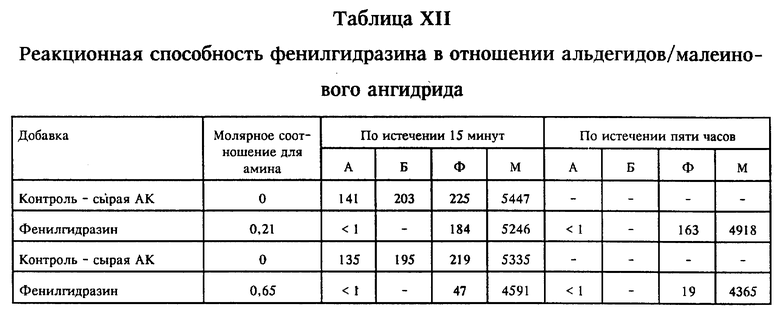
На эффективность при снижении содержания примесей в САК и ВЧАК с вкраплениями оценивали некоторые типичные амины группы P. Результаты оценки большинства охарактеризованных аминов группы P сведены в таблицу XII. С использованием САК, содержавшей примеси в количествах, указанных в таблице XII, оценивали также фенилгидразин. Отборочные испытания проводили при 48-52oC; результаты, полученные по истечении времени выдержки и сведенные в таблицу XII, показывают, что фенилгидразин проявлял некоторую полезность при снижении содержания фурфурола, в частности, при использовании молярного соотношения, равном 0,65. Количество акролеина быстро уменьшалось до менее 1 части/млн.
Испытание с использованием гидразина примера 2, которое проводили без амина группы B, показало, что гидразин, тем не менее, оказывается эффективным амином группы P, в частности, при уменьшении содержания бензальдегида и фурфурола в дистилляте до уровня менее 1 части/млн.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛАКРИЛАТА (ВАРИАНТЫ) | 1996 |
|
RU2161150C2 |
| УЛУЧШЕННЫЙ СПОСОБ СЕЛЕКТИВНОГО УДАЛЕНИЯ ПРОПИОНОВОЙ КИСЛОТЫ ИЗ ПОТОКОВ (МЕТ)АКРИЛОВОЙ КИСЛОТЫ | 2008 |
|
RU2491271C2 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДНОЙ (МЕТ)АКРИЛОВОЙ КИСЛОТЫ | 2009 |
|
RU2513746C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРА В ВОДНОЙ СИСТЕМЕ, СОПОЛИМЕР, КОМПЛЕКС И РЕАКЦИОННАЯ СМЕСЬ | 1995 |
|
RU2177953C2 |
| Смазочная композиция | 1978 |
|
SU1064870A3 |
| СПОСОБ ОЧИСТКИ (МЕТ)АКРИЛОВОЙ КИСЛОТЫ | 2004 |
|
RU2350598C2 |
| СПОСОБ РЕКТИФИКАЦИОННОГО РАЗДЕЛЕНИЯ ЖИДКОСТИ, СОДЕРЖАЩЕЙ АКРИЛОВУЮ КИСЛОТУ | 2004 |
|
RU2395485C2 |
| ОТВЕРЖДАЕМАЯ ВОДНАЯ КОМПОЗИЦИЯ | 2010 |
|
RU2573017C2 |
| СРЕДСТВО ДЛЯ СНИЖЕНИЯ ЛЕТУЧЕСТИ ИНГРЕДИЕНТОВ КОЖИ | 1992 |
|
RU2078829C1 |
| СШИВАЮЩИЙ АГЕНТ И СПОСОБ СШИВАНИЯ СВЯЗУЮЩЕГО ПОЛИМЕРА ПОКРЫТИЯ | 1994 |
|
RU2135525C1 |




Изобретение относится к способу получения высокочистой акриловой кислоты (варианты) с остаточным содержанием альдегидов менее 10 частей/млн. путем фракционной дистилляции при температуре от 25 до 100oC с добавлением аминосоединения, выбранного из: группы A - первичного ариламина формулы (IV), где X3 выбирают из -COOH и -COOR6, R6 - C1-C6 алкил, алканоламина формулы HO-R7-NH2, R7 - C2-C6 алкилен; группы B - o-, м-, п-фенилендиамин, 4-нитрофенилгидразин, 2,4-динитрофенилгидразин; группы S-орто- или мета-толуидин; группы P- o-, м-, п-фенилендиамин, 4-нитрофенилгидразин, 2,4-динитрофенилгидразин, фенилгидразин, гидразин, анилин. В этих способах амины выбранных групп используют последовательно, предпочтительно, непрерывно с селективным снижением содержания, например, акролеина и фурфурола, и процесс можно проводить в присутствии, в качестве примесей, малеиновой кислоты и малеинового ангидрида. Технический результат - экономичный непрерывный способ снижения концентрации альдегидов в сырой акриловой кислоте при производстве высокочистой акриловой кислоты. 3 с. и 1 з.п.ф-лы, 12 табл.
а) стадию подачи в дистилляционную колонну потока сырой акриловой кислоты при температуре 25 - 100oC, причем этот поток включает в себя I) сырую акриловую кислоту и II) минимально эффективное количество, при молярном отношении 0,1 - 2,0 к общему числу молей альдегидов, малеиновой кислоты и малеинового ангидрида в сырой акриловой кислоте, по меньшей мере одного амина группы A, выбранного из i) первичного ариламина формулы IV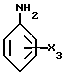
где значения X3 выбирают из группы, состоящей из -COOH и -COOR6, где значения R6 выбирают из C1 - C6-алкилов, и ii) алканоламина формулы V
HO-R7-NH2,
где значения R7 выбирают из C2 - C6-алкиленов;
б) стадию одновременной подачи в верхнюю часть дистилляционной колонны аминового потока, содержащего в молярном отношении 0,01 - 1,0 к общему числу молей альдегидов, малеиновой кислоты и малеинового ангидрида в сырой акриловой кислоте, по меньшей мере, один амин из группы B, включающей о-, м-, п-фенилендиамин, 4-нитрофенилгидразин и 2,4-динитрофенилгидразин, и
в) стадию перегонки потока сырой акриловой кислоты в дистилляционной колонне в присутствии аминового потока с получением ВЧАК, характеризующейся остаточным количеством индивидуального альдегида менее 10 ч./млн.
а) стадию подачи в первую дистилляционную колонну потока источника акриловой кислоты при температуре 25 - 100oC, причем поток источника акриловой кислоты включает в себя I) источник акриловой кислоты, выбранный из группы, содержащей водный раствор акриловой кислоты, экстракт акриловой кислоты или сырую акриловую кислоту, содержащую уксусную кислоту в количестве свыше 2000 ч. /млн; II) в молярном отношении 0,1 - 2,0 к общему числу молей альдегидов, малеиновой кислоты и малеинового ангидрида в указанном потоке акриловой кислоты по крайней мере один амин группы A, выбранный из i) первичного ариламина структурной формулы IV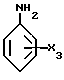
где значения X3 выбирают из группы, состоящей из -COOH и -COOR6, где R6 выбирают из C1 - C6-алкилов, и ii) алканоламина формулы V
HO-R7-NH2
где значения R7 выбирают из C2 - C6-алкиленов;
б) при условии, если поток источника акриловой кислоты выбран из группы, содержащей водный раствор акриловой кислоты и экстракт акриловой кислоты, проводят стадию дегидратации потока источника акриловой кислоты с получением сырой акриловой кислоты с низким содержанием акролеина, концентрация которого составляет менее 10 ч./млн;
в) при условии, если поток источника акриловой кислоты представляет собой сырую акриловую кислоту, содержащую уксусную кислоту в количестве свыше 2000 ч./млн, проводят стадию отгонки уксусной кислоты с получением сырой акриловой кислоты с низким содержанием акролеина, составляющим менее чем 10 ч. /млн, и с содержанием уксусной кислоты менее, чем 2000 ч./млн;
г) стадию последующей подачи в конечную дистилляционную колонну I) сырой акриловой кислоты с низким содержанием акролеина и II) одновременной подачи в верхнюю часть конечной дистилляционной колонны аминового потока, содержащего в молярном отношении 0,01 - 1,0 к общему числу молей альдегидов, малеиновой кислоты и малеинового ангидрида в сырой акриловой кислоте с низким содержанием акролеина по меньшей мере один амин из группы B, включающей о-, м-, п-фенилендиамин, 4-нитрофенилгидразин и 2,4-динитрофенилгидразин, и
д) стадию перегонки акриловой кислоты с низким содержанием акролеина в конечной дистилляционной колонне с отгонкой ВЧАК, характеризующейся остаточным количеством индивидуального альдегида менее 10 ч./млн.
а) стадию введения в поток сырой акриловой кислоты, содержащий сырую акриловую кислоту или сырую акриловую кислоту, содержащую уксусную кислоту в количестве свыше 2000 ч./млн, в молярном отношении 0,1 - 2,0 к общему числу молей альдегидов, малеиновой кислоты и малеинового ангидрида в исходном потоке сырой акриловой кислоты одного или нескольких аминов группы S, выбранных из i) орто-толуидин, мета-толуидин и ii) алканоламина формулы V
HO-R7-NH2
где значения R7 выбирают из C2 - C6-алкиленов;
б) при условии, что, если поток акриловой кислоты представляет собой сырую акриловую кислоту, проводят стадию выдержки потока сырой акриловой кислоты и добавленного амина группы S при температуре 25 - 100oC в течение времени выдержки 15 - 150 ч с получением обработанного потока и последующую подачу этого обработанного потока в дистилляционную колонну;
в) при условии, что если поток акриловой кислоты представляет собой сырую акриловую кислоту, содержащую уксусную кислоту в количестве свыше 2000 ч. /млн, проводят стадию подачи указанного потока и амина группы S в колонну для отгонки уксусной кислоты при температуре 25 - 100oC с получением обработанного амином потока и отгонку уксусной кислоты из этого обработанного амином потока, с последующим получением обработанного амином сырой акриловой кислоты с низким содержанием уксусной кислоты, составляющим менее чем 2000 ч./млн, и последующую подачу этой обработанной амином сырой акриловой кислоты с низким содержанием уксусной кислоты в дистилляционную колонну;
г) стадию одновременного введения в молярном отношении 0,01 - 1,0 к общему числу молей альдегидов, малеиновой кислоты и малеинового ангидрида в сырой акриловой кислоте по меньшей мере одного амина группы P, выбранного из о-, м-, п-фенилендиамина, 4-нитрофенилгидразина, 2,4-динитрофенилгидразина, фенилгидразина, гидразина и анилина, в обработанный поток, направляемый в дистилляционную колонну, необязательно в верхнюю часть этой дистилляционной колонны, и д) стадию перегонки обработанного потока в дистилляционной колонне в присутствии амина группы P с получением таким образом ВЧАК, характеризующейся остаточным количеством индивидуального альдегида менее 10 ч./млн.
| 1972 |
|
SU422135A3 | |
| US 3725208 A, 03.04.1973 | |||
| US 3859175 A, 07.01.1975. | |||
Авторы
Даты
2000-08-20—Публикация
1995-11-29—Подача