Изобретение относится к области фармации и касается способа получения средства из растительного сырья, обладающего желчегонной и противовоспалительной активностью.
Известен способ получения отвара зубчатки обыкновенной (Николаев С.М., Самбуева З. Г. , Баторова С.М., Хингеева С.Л. Перспективные виды растений с желчегонным действием из арсенала тибетской медицины // Известия СО АМН СССР, Новосибирск, 1987, с. 48-51), применяющегося в качестве желчегонного средства. Для приготовления отвара измельченное лекарственное растительное сырье - траву зубчатки обыкновенной заливают водой комнатной температуры, взятой с учетом коэффициента водопоглощения, в соответствующей емкости и настаивают на кипящей водяной бане при частом помешивании в течение 30 мин, затем охлаждают 10 мин, процеживают (отжимая остаток растительного материала) и прибавляют воду до необходимого объема извлечения. Недостатком данного способа является относительно низкая желчегонная активность по сравнению с суммой, полученной по заявленному способу.
Задачей изобретения является повышение выхода действующих веществ, увеличение желчегонной активности и установление противовоспалительного действия.
Для решения указанной задачи измельченный растительный материал (трава зубчатки обыкновенной) экстрагируют 35-45% спиртом этиловым в соотношении сырье: экстрагент 1:(12-14) с учетом коэффициента водопоглощения в течение 60 минут при температуре 60-65oC и постоянном помешивании. Процесс повторяют дважды. Аналогичным способом проводят третью экстракцию в течение 30 минут. Водно-спиртовые извлечения объединяют и упаривают до 1/3 первоначального объема.
Полученный продукт очищают сепарированием и высушивают в вакуум-сушильном шкафу. Выход готового продукта составляет 20,58% от массы растительного материала. Выявленные отличительные признаки позволяют сделать вывод о соответствии предложенного технического решения критерию "новизна".
Одной из актуальных проблем медицинской науки и практического здравоохранения является профилактика и лечение заболеваний печени и желчевыводящих путей. Социальная значимость этой проблемы обусловлена широким распространением, разнообразием этиологических факторов и особой тяжестью заболеваний, приводящих к потере трудоспособности населения. В связи с этим, поиск и разработка новых эффективных лекарственных средств из растительного сырья, обладающих малой токсичностью и не оказывающих побочное действие при длительном применении, является актуальной задачей.
Учитывая потребности практического здравоохранения в лекарственных препаратах растительного происхождения, предназначенных для лечения заболеваний печени и желчевыводящих путей, разработан способ получения сухого экстракта из травы зубчатки обыкновенной.
Дальнейшие исследования и приведенные в тексте данные позволяют сделать заключение о соответствии предлагаемого решения критерию "изобретательский уровень" и предложенные в формуле изобретения позволяют достичь поставленной цели.
Конечный продукт - аморфный порошок коричневато-черного цвета, потеря в массе при высушивании 3,5%.
Нами проведен химический анализ сухого экстракта.
1. На основании качественного фитохимического анализа сухого экстракта установлено наличие:
1) флавоноидов
0,1 г полученного экстракта растворяют в 50 мл 40% спирта.
К 3 мл полученного раствора прибавляют 3 мл 2% раствора алюминия хлорида, появляется желтое окрашивание.
Тонкослойной хроматографией на пластинках марки "Силуфол" в системе растворителей хлороформ-уксусная кислота (5:2): при просматривании хроматограммы в УФ-свете до и после обработки парами аммиака обнаружены: апигенин - Rf = 0,69, лютеолин - Rf = 0,8; лютеолин-7-глюкозид - Rf = 0,6. Идентификацию их проводили по сравнению с аутентичными образцами.
2) дубильных веществ.
0,05 г полученного экстракта растворяют в 5 мл воды очищенной.
К 2 мл полученного раствора прибавляют 2-3 капли раствора железо-аммониевых квасцов, появляется черно-зеленое окрашивание.
3) иридоидов
0,05 г полученного экстракта растворяют в 5 мл воды очищенной.
К 2 мл полученного раствора прибавляют несколько капель реактива Шталя (1 г п-диметиламинобензальдегида, 5 г фосфорной кислоты и 50 г уксусной кислоты, разбавляют водой до 100 мл), доводят до кипения на водяной бане, появляется голубое окрашивание.
4) фенолкарбоновых кислот
двумерной восходящей хроматографией на бумаге марки FN-12 в системе растворителей: 1. н-бутанол-уксусная кислота - вода (4:1:5).
2. 15% уксусная кислота.
После обработки хроматограммы в парах аммиака и просматривании в УФ-свете идентифицированы с аутентичными образцами:
кофейной кислоты Rf = 0,79 (1); Rf = 0,53 (2).
Разработана методика количественного определения суммы флавоноидов.
2. Количественное определение суммы флавоноидов спектрофотометрическим методом.
Аналитическую пробу сырья измельчают до размера частиц, проходящих сквозь сито с отверстиями диаметром 1 мм.
Около 1,0 г (точная навеска) измельченного сырья помещают в коническую колбу со шлифом вместимостью 100 мл, прибавляют 50 мл 70% спирта, взвешивают. Колбу присоединяют к обратному холодильнику и нагревают на кипящей водяной бане в течение 60 мин, периодически встряхивания для смыкания частиц со стенок. После охлаждения до комнатной температуры колбу взвешивают, доводят 70% спиртом до первоначальной массы. Извлечение фильтруют через воронку с ватным тампоном в сухую колбу вместимостью 100 мл, отбрасывая первые 10 мл фильтрата (р-р A).
В мерную колбу вместимостью 25 мл приливают 2 мл р-ра A и 2 мл р-ра алюминия хлорида в 70% спирте и доводят объем раствора 70% спиртом до метки и перемешивают. Через 30 мин измеряют оптическую плотность р-ра на спектрофотометре при длине волны 395 нм в кювете с толщиной слоя 10 мм.
В качестве раствора сравнения используют раствор, состоящий из 2 мл извлечения, 1 капли разведенной уксусной кислоты и доведенной 70% спиртом до метки в мерной колбе вместимостью 25 мл.
Параллельно измеряют оптическую плотность р-ра Государственного стандартного образца (ГСО) лютеодина, приготовленного аналогично испытуемому р-ру.
Содержание суммы флавоноидов в пересчете на лютеолин на абсолютно сухое сырье в процентах (X) вычисляют по формуле: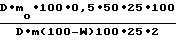
где D - оптическая плотность испытуемого раствора;
Dо - оптическая плотность раствора ГСО лютеолина;
m - масса сырья в граммах;
mо - масса ГСО лютеолина в граммах;
W - потеря в массе при высушивании сырья в граммах.
Найдено 0,64 ± 0,02% флавоноидов.
Предлагаемый способ получения достаточно прост, не требует сложной системы очистки, позволяет получить продукт постоянного состава. Технология может быть внедрена на предприятиях по выпуску лекарственных препаратов.
Для доказательства существенности предложенных признаков изучены влияние состава и природы экстрагента, его соотношение с сырьем, температурного режима, степени измельчения сырья, продолжительности и кратности числа экстракций на выход биологически активных веществ из исследуемого лекарственного растения.
Количественная оценка велась по выходу суммы экстраактивных веществ (ГФ XI, вып. 1, с. 295) и содержанию суммы флавоноидов в пересчете на лютеолин-стандарт.
Метрологическая характеристика определения суммы экстрактивных веществ и суммы флавоноидов проводилась на образце зубчатки обыкновенной, собранной в Иволгинском районе в 1998 (таблица 1).
Подбор оптимального экстрагента является одним из основных моментов при получении извлечений. Для подбора типа экстрагента изучения процессы экстрагирования сырья водой, этиловым спиртом различной концентрации: 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 95.
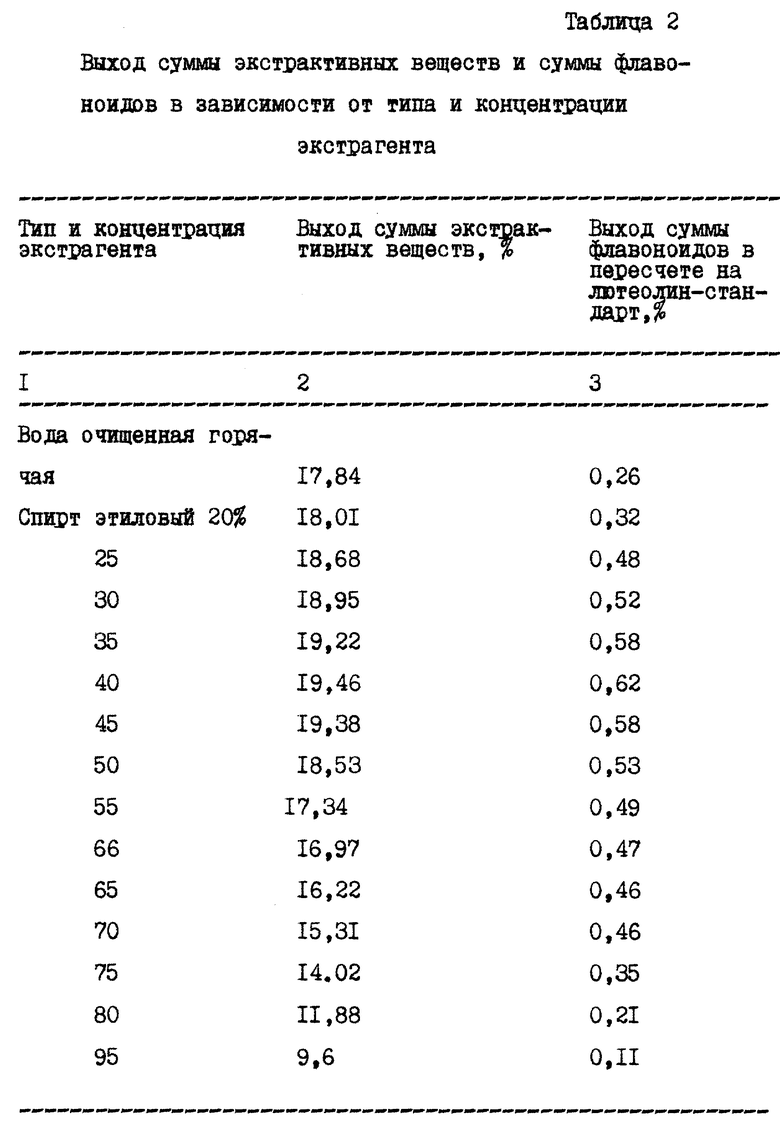
Результаты представлены в таблице 2.
Как видно из таблицы, 35-45% спирт является оптимальным экстрагентом, т. к. позволяет получить наибольшее количество суммы флавоноидов с учетом выхода суммы экстрактивных веществ.
Известно, что размер частиц сырья обусловливает полноту и скорость перехода в раствор экстрагируемых веществ. Установлена зависимость выхода суммы флавоноидов и суммы экстрактивных веществ от степени измельчения сырья. Сырье подвергалось измельчению до диаметра частиц 0,5; 1; 2; 3; 5; 7; 10 мм.
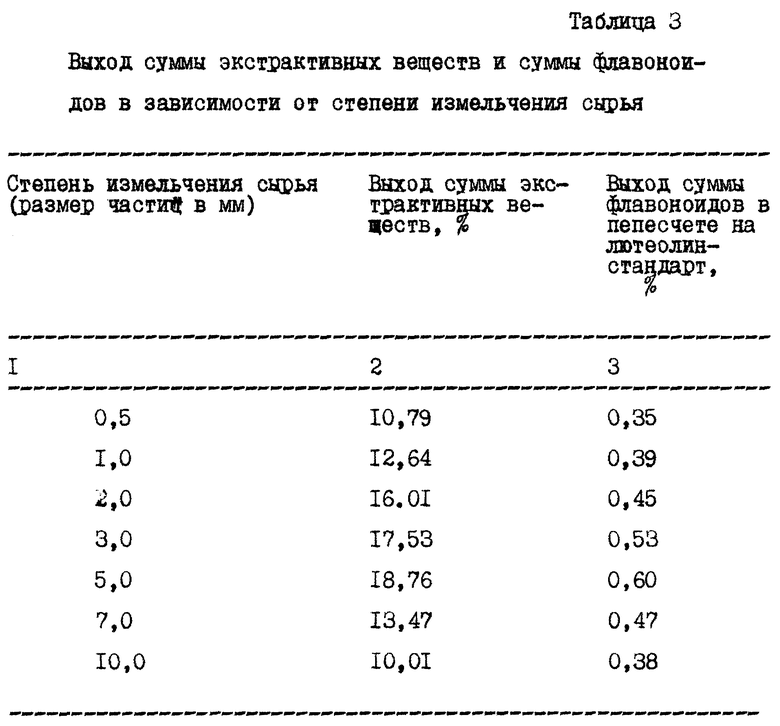
Данные анализа представлены в таблице 3.
Оптимальной степенью измельчения сырья является размер частиц 5 мм.
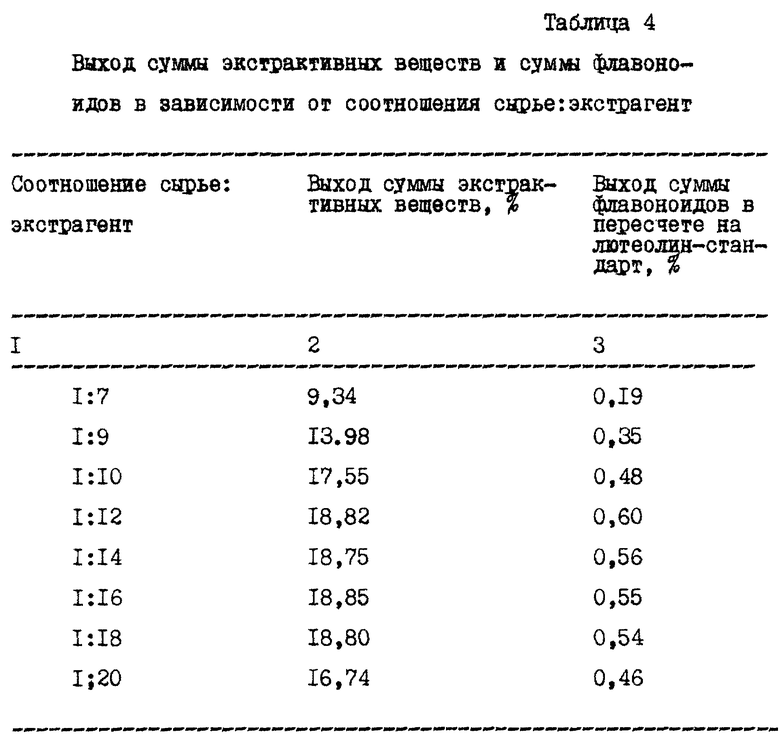
Подробно оптимальное соотношение сырье-экстрагент для однократного залива сырья см. в таблице 4.
Максимальный выход экстрактивных веществ и флавоноидов наблюдается при соотношении сырья и экстрагента 1:12. Дальнейшее увеличение объема соотношения сырье: экстрагент до (1:12) нецелесообрзано, поскольку увеличивается расход экстрагента.
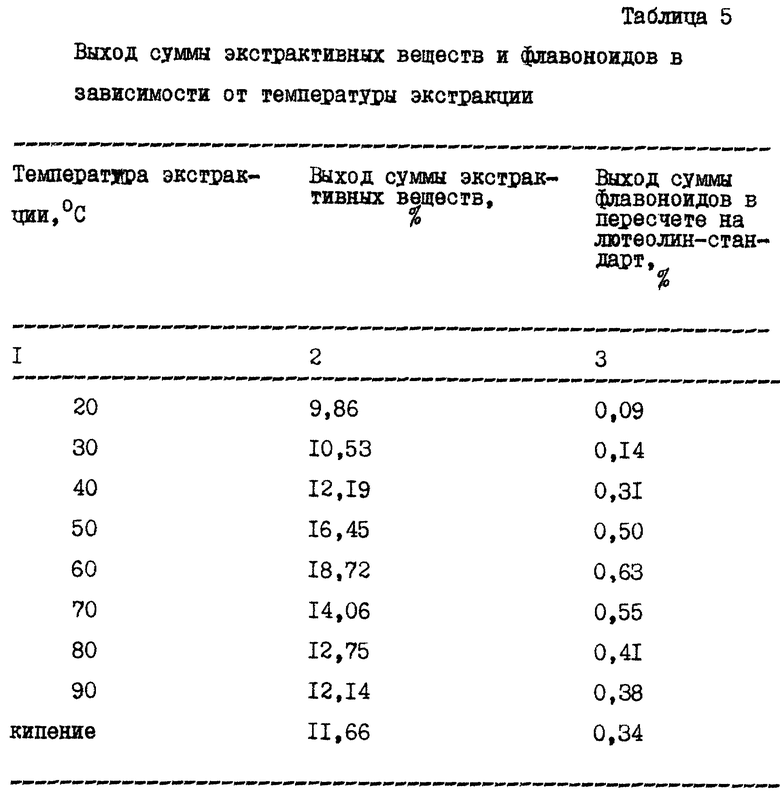
На основании экспериментальных данных можно заключить, что увеличение температуры экстрагента положительно влияет на ход процесса экстракции. Установлено, что при 60oC наблюдается максимальный выход экстрактивных веществ и флавоноидов (таблица 5).
С целью определения продолжительности и кратности числа экстракции изучена зависимость времени достижения равновесной концентрации в системе сырье-экстрагент при трехкратной экстракции сырья.
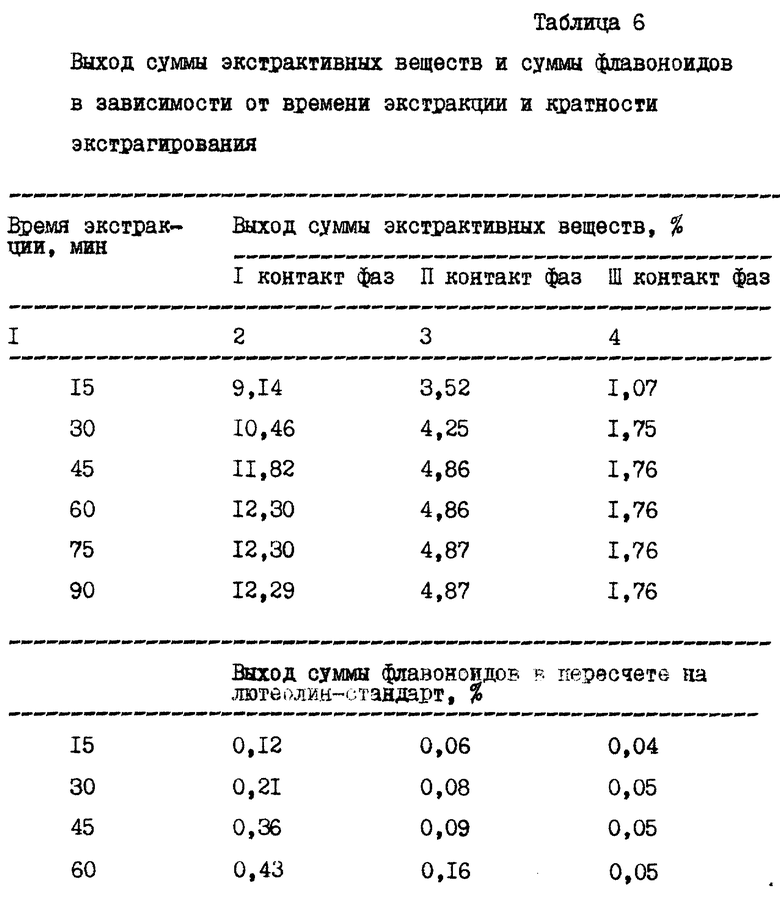
Для этого проводили экстракцию измельченного сырья 40% спиртом в соотношении 1:12 на водяной бане при температуре 60oC при постоянном перемешивании с обратным холодильником. Через заданные промежутки времени (15, 30, 45, 60, 75, 90 минут) извлечения фильтровали (1 контакт фаз), определяя содержание суммы экстрактивных веществ и суммы флавоноидов. Аналогичным образом проводили две последующие экстракции отжатого сырья при том же промежутке времени, подавая каждый раз 40% спирт в количестве, равном объему слитого извлечения (II и III контакт фаз), также анализировали на содержание суммы экстрактивных веществ и суммы флавоноидов. Экспериментальные данные свидетельствуют, что равновесное состояние наступает при I, II контактах фаз через 60 минут, при III контакте фаз через 30 минут (таблица 6).
В течение I контакта фаз экстрагируется около 60-70% экстрактивных веществ и суммы флавоноидов. II контакт обеспечивает выход 20-30% и III контакт - 10-20%, т.е. для полноты истощения сырья достаточно трехкратной экстракции.
Определение выхода экстрактивных веществ во всех указанных экспериментах проводили по следующей однотипной методике, приведенной в ГФ XI (Государственная фармакология СССР, вып. 1. Общие методы анализа, МЗ СССР, Н-е изд. доп. М., 1987 - 336 с).
Пример 1.
1 кг травы зубчатки обыкновенной измельчают на мельнице до размера частиц диаметром 5 мм (сито N 20 ГОСТ 214-83). Измельченное сырье загружают в экстракционный аппарат с мешалкой и внешним паровым обогревом. Заливают 12 л 35% спирта в соотношении сырье:экстрагент 1:12 с учетом коэффициента водопоглощения. Экстрагируют при температуре 55oC и постоянном перемешивании в течение 60 мин. Извлечение фильтруют через серошинельное сукно в сборник. Проводят еще 2 экстракции в течение 60 мин и 30 мин, подавая каждый раз в экстрактор спирт 35% в количестве, равном объему слитого, 1-й слив - 9,9 л, 2-й слив - 9,8 л, 3-й слив - 10 л. Объединенные водно-спиртовые извлечения упаривают примерно до 1/3-1/4 первоначального объема. Кубовый остаток от трех извлечений подвергают очистке сепарированием и сушат на нержавеющих противнях в вакуумной сушилке при 65-70oC 8 часов. Получают 195,0 г готового продукта, что составляет 19,50% сухого экстракта от массы исходного сырья.
Сухой экстракт представляет собой аморфный порошок коричневато-черного цвета с приятным запахом, комкуется, с вяжущим вкусом. Потеря в массе при высушивании - 3,5%.
Определение острой токсичности сухого экстракта травы зубчатки обыкновенной проводилось на белых мышах обоего пола (масса 20,0±2,0 г) при внутрибрюшинном введении. Полученные данные обработаны статистически с использованием метода Кербери. Испытуемое средство вводили в дозах 500-6000 мг/кг с интервалом между дозами в 200 мг/кг. Наблюдение за животными проводили в течение 14 суток. Установлено, что LD50 сухого экстракта травы зубчатки обыкновенной при внутрибрюшинном введении белым мышам составляет 5234 мг/кг, что позволяет отнести испытуемое средство по классификации К.К. Сидорова (О классификации токсических ядов при парентаральных способах введения // Токсикология новых промышленных химических веществ, М. 1973, вып. 13, с. 47-51) к относительно безвредным веществам.
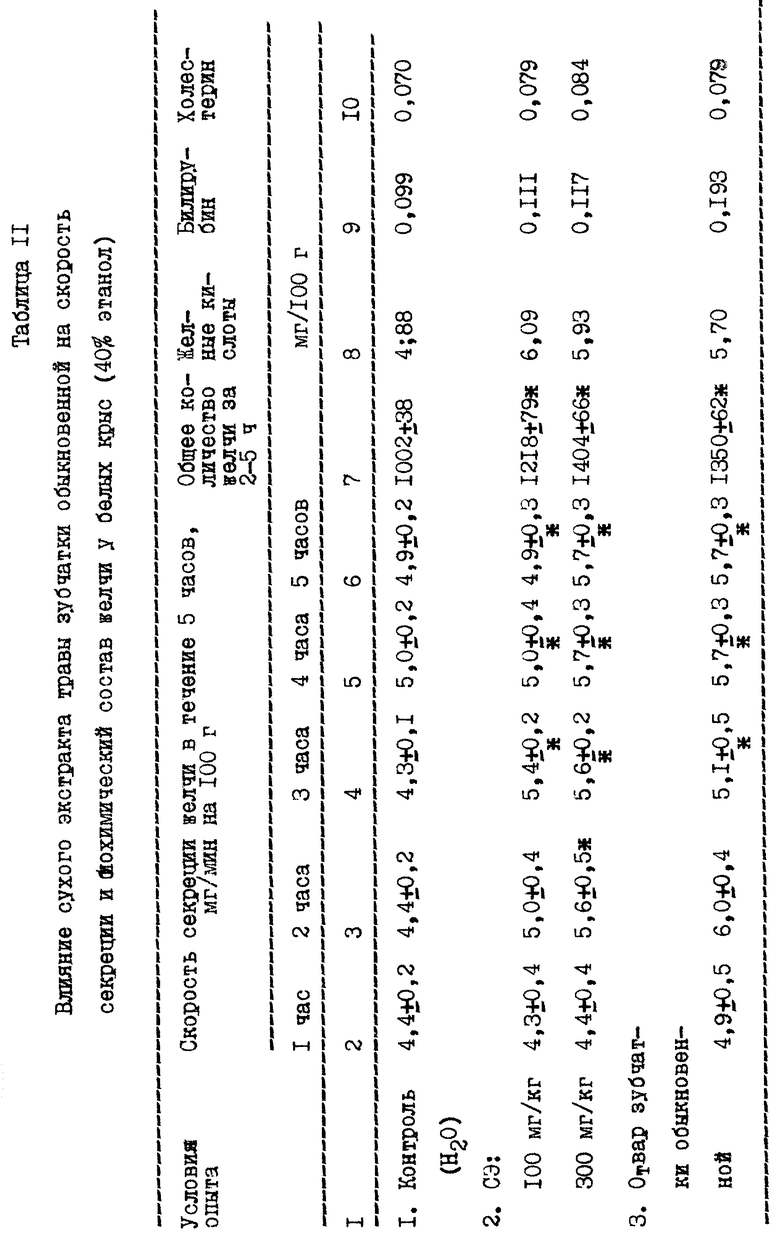
Оценку желчегонной активности экстракта зубчатки обыкновенной проводили на беспородных крысах обоего пола с исходной массой 170-200 г в условиях острых опытов по общепринятой методике. Крыс наркотизировали внутрибрюшинным введением 1% раствора барбамила в объеме 0,8 мл/100 г массы. Желчь получали с помощью полиэтиленовой канюли, вставленной в общий желчевыводящий проток, через каждый час в течение 5 часов подряд. Сухой экстракт (СЭ) в виде водного раствора вводили в двенадцатиперстную кишку шприцом в дозах 100 и 300 мг/кг (дозы, при которых установлена выраженная желчегонная активность). Крысам контрольной группы вводили эквиобъемное количество дистиллированной воды. В качестве препарата сравнения использовали отвар зубчатки обыкновенной, который вводили по аналогичной схеме. О степени желчегонной активности судили по скорости секреции и общему количеству выделенной желчи, по содержанию в желчи желчных кислот (Карбач Я.И. Количественное определение желчных кислот в желчи и крови с применением хроматографического метода // Биохимия, 1961, т. 21, N 2, с. 305-309), а также по количеству выделенных с желчью билирубина и холестерина. Общее количество холестерина определяли по методике С.М. Дроговоз (Нарушение интенсивности желчеотделения и химического состава желчи при дистрофии печени, вызванной четыреххлористым углеродом. // Вопросы медхимии, 1971 - вып. 4, с. 397-400), а билирубина - по методу Ван-дер Берга в модификации Н.П. Скакуна. (Нейрогуморальный механизм желчегонного действия инсулина // Проблемы эндокринологии. 1956, N 6, с. 75-78). Статистическая обработка полученных результатов, представленных в таблице 7, проведена по Е.В. Монцевичюте-Эрингене (упрощенные математико-статистические методы в медицинской исследовательской работе // Патологическая физиология и экспериментальная терапия, 1964, N 4, с. 71-78).
Как следует из таблицы 7, экстракт зубчатки обыкновенной оказывает выраженное желчегонное действие. При этом скорость секреции желчи через 1 час после введения экстракта зубчатки обыкновенной возрастала на 34%, а в последующие часы, в частности, при дозе 300 мг/кг - почти в 1,5 раза превышала контроль. Кроме того, экстракт зубчатки стимулировал синтез и выделение желчных кислот, способствовал секреции билирубина и экскреции холестерина с желчью. При этом желчегонная активность предлагаемого средства была выше, чем у отвара зубчатки обыкновенной.
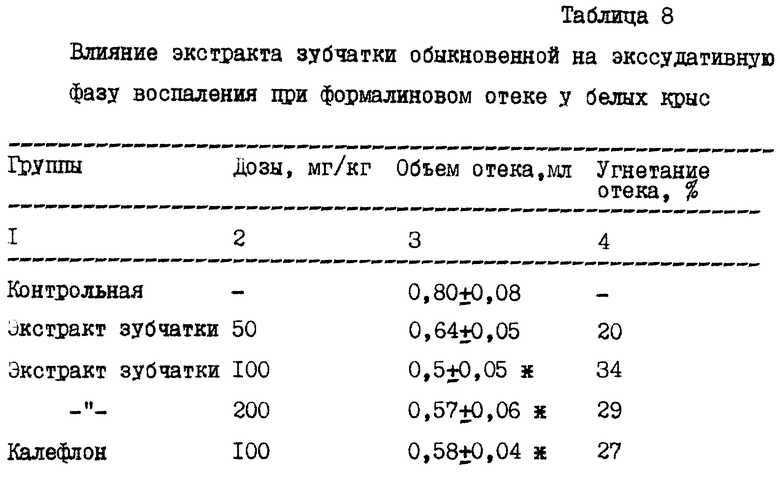
Изучали влияние экстракта зубчатки на экссудативную фазу воспаления по общепринятой методике на 30 беспородных белых крысах обоего пола массой 180-200 г. Асептическое воспаление конечности вызывали субплантарным введением в правую заднюю лапку крысы 0,1 мл 3% раствора формалина (Стрельников Ю. Е. Сравнительная характеристика противовоспалительного действия некоторых пиримидиновых производных // Фармакология и токсикология. 1960, N 6, с. 526-531). Водный раствор экстракта зубчатки вводили внутрижелудочно в дозах 50, 100 и 200 мг/кг в объеме 1 мл/100 г за 3 часа до введения флогогенного агента, а затем через 5 и 18 часов после этого. Животным контрольной группы в равном объеме вводили дистиллированную воду по аналогичной схеме. В качестве препарата сравнения использовали калефлон в дозе 100 мг/кг. Через 24 часа после введения формалина определяли величину отека онкометрическим методом по разности между объемами воспаленной и невоспаленной лапок животных. Полученные данные приведены в таблице 8.
Как следует из данных, приведенных в таблице 8, экстракт зубчатки обыкновенной во всех исследованных дозах оказывал антиэксудативное действие. При этом выраженность его эффекта зависела от используемой дозы, если при введении экстракта зубчатки обыкновенной в дозе 50 мг/кг обнаруживалась лишь тенденция к уменьшению объема отека (различие недостоверно), то увеличение дозы испытуемого фитоэкстракта сопровождалось повышением его активности так: введение его в дозах 100 и 200 мг/кг угнетало развитие отека соответственно на 34 и 29% по сравнению с данными животных контрольной группы. При этом препарат сравнения оказывал аналогичное антиэкссудаитвное действие.
Пример 2.
1 кг травы зубчатки обыкновенной измельчали на мельнице до размера частиц диаметром 5 мм (сито N 20 ГОСТ 214-83). Измельченное сырье загружали в экстракционный аппарат с мешалкой и внешним паровым обогревом. Заливали 12 л 40% спирта в соотношении сырье:экстрагент 1:13 с учетом коэффициента водопоглощения. Экстрагируют при температуре 60oC и постоянном перемешивании в течение 60 мин. Извлечение фильтруют через серошинельное сукно в сборник. Проводят еще 2 экстракции в течение 60 мин и 30 мин, подавая каждый раз в экстрактор спирт 40% в количестве, равном объему слитого, 1-й слив - 9,9 л, 2-й слив - 9,7 л, 3 слив - 9,8 л. Объединенные водно-спиртовые извлечения упаривают примерно до 1/3 - 1/4 первоначального объема. Кубовый остаток от трех извлечений подвергают очистке сепарированием и сушат на нержавеющих противнях в вакуумной сушилке при 65-70oC 8 часов. Получают 201,5 г готового продукта, что составляет 20,15% сухого экстракта от веса исходного сырья.
Сухой экстракт представляет собой аморфный порошок коричневато-черного цвета с приятным запахом, комкуется, с вяжущим вкусом. Потеря в массе при высушивании - 2,9%.
Оценку желчегонной активности экстракта зубчатки обыкновенной проводили по методике, описанной в примере 1.
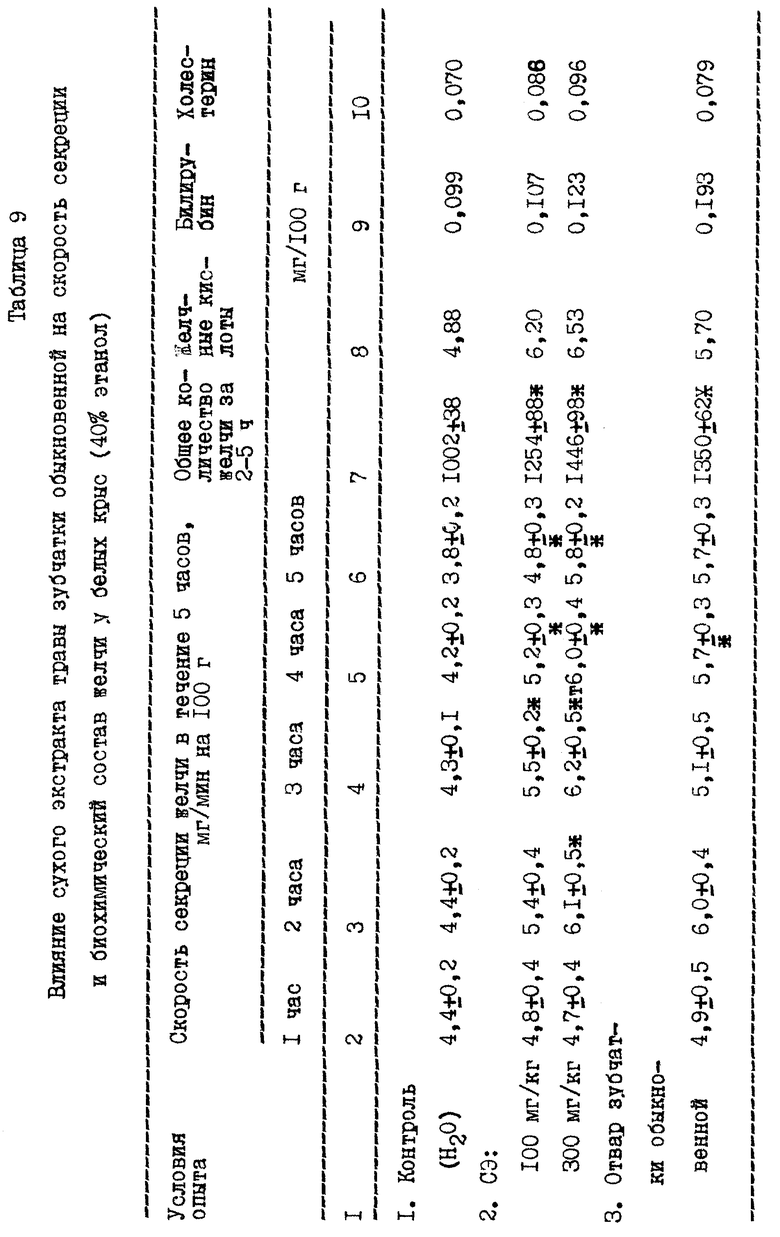
Результаты приведены в табл. 9.
Установлено, что 40% экстракт зубчатки обыкновенной оказывает выраженное желчегонное действие. Под влиянием экстракта зубчатки обыкновенной скорость секреции желчи при дозе 300 мг/кг возрастала со 2 по 5 часы опыта на 39-52% по сравнению с контролем. Экстракт зубчатки, проявляя свойство истинных холесекретиков, стимулировал синтез желчных кислот. Экстракт также ускорял выведение билирубина и холестерина с желчью. При этом желчегонная активность экстракта превосходила таковую у отвара зубчатки обыкновенной.
Исследовали влияние экстракта зубчатки обыкновенной на течение острого перитонита. Эксперименты проведены на белых бесплодных крысах обоего пола массой 160-180 г. Острый перитонит вызывали внутрибрюшинным введением животным 1 мл 0,2% раствора нитрата серебра (Александров П.И., Сперанская Т.В. , Бобков Ю. Г. и соавт. Влияние рутина и эскуламина на некоторые модели асептического воспаления // Фармакология и токсикология, 1986, N 1, с. 84-86). Испытуемый фитоэкстракт в дозе 100 мг/кг вводили за 30 мин и через 1 час после инъекции флогогенного агента. Животные контрольной группы получали эквиобъемное количество дистиллированной воды. В качестве препарата сравнения использовали калефлон в дозе 100 мг/кг. Через 24 часа от начала эксперимента определяли объем экссудата в брюшной полости и количество дегранулированных тучных клеток в брыжейке. Для этого брыжейку фиксировали смесью Карнуа и окрашивали 0,05% раствором толуидинового синего. Подсчет количества дегранулированных тучных клеток осуществляли в 100 полях зрения при увеличении х20.
Полученные данные приведены в таблице 10.
Как следует из приведенной таблицы 10, развитие острого перитонита сопровождалось появлением в брюшной полости экссудата красновато-бурого цвета и тотальной дегрануляцией тучных клеток. На фоне введения экстракта зубчатки в дозе 100 мг/кг объем внутрибрюшинной жидкости уменьшался в 2,5 раза по сравнению с данными крыс контрольной группы, что свидетельствует о наличии у испытуемого экстракта выраженной антиэкссудативной активности. Вместе с этим у животных опытной группы внутрибрюшинная жидкость имела опалесцирующий оттенок, что свидетельствует о значительном снижении в ней числа эритроцитов. Введение экстракта зубчатки сопровождалось также существенным снижением дегрануляции тучных клеток: так, количество их в процентном отношении уменьшилось более чем в 2,5 раза по сравнению с таковым у животных контрольной группы. Полученные данные свидетельствуют, что экстракт зубчатки в дозе 100 мг/кг оказывает противовоспалительное действие при остром перитоните.
Пример 3.
1 кг травы зубчатки обыкновенной измельчают на мельнице до размера частиц диаметром 5 мм (сито N 20 ГОСТ 214-83). Измельченное сырье загружают в экстракционный аппарат с мешалкой и внешним паровым обогревом. Заливают 12 л 45% спирта в соотношении сырье:экстрагент 1:14 с учетом коэффициента водопоглощения. Экстрагируют при температуре 65oC и постоянном перемешивании в течение 60 мин. Извлечение фильтруют через серошинельное сукно в сборник. Проводят еще 2 экстракции в течение 60 мин и 30 мин, подавая каждый раз в экстрактор спирт 40% в количестве, равном объему слитого, 1-й слив - 9,8 л, 2-ой слив - 10 л, 3-й слив - 9,8 л. Объединенные водно-спиртовые извлечения последовательно порциями упаривают примерно до 1/3-1/4 первоначального объема. Кубовый остаток от трех извлечений подвергают очистке сепарированием и сушат на нержавеющих противнях в вакуумной сушилке при 65-70oC 8 часов. Получают 199,5 г готового продукта, что составляет 19,95% сухого экстракта от веса исходного сырья.
Сухой экстракт представляет собой аморфный порошок коричневато-черного цвета с приятным запахом, комкуется, с вяжущим вкусом. Потеря в массе при высушивании - 3,8%.
Оценку желчегонной активности экстракта зубчатки обыкновенной проводили по методике, аналогичной в примера 1 и 2.
Результаты представлены в таблице 11.
Из приведенных в таблице 11 данных следует, что 45% экстракт зубчатки обыкновенной также оказывает желчегонное действие, незначительно уступающее действию 40% экстракта, и при этом превосходит аналогичное действие отвара зубчатки.
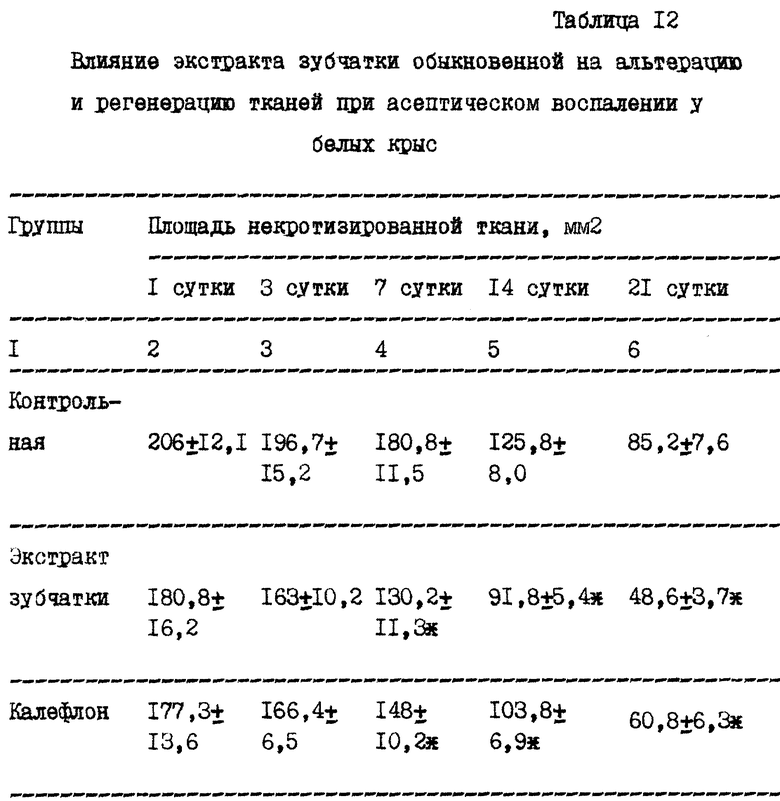
Изучали влияние экстракта зубчатки обыкновенной на процессы альтерации и регенерации тканей. Эксперименты проведены на белых беспородных крысах обоего пола массой 160-180 г. Воспалительный процесс моделировали по методу Менкина (Ойвин И. А., Шетель С.Л. Методика изучения местных нарушений капиллярной проницаемости. Материалы по патогенезу воспаления и патологии белков крови. Душанбе, 1961, т. 49, N 5, с. 167-173) путем подкожного введения белым крысам в область спины 0,5 мл 9% раствора уксусной кислоты, одновременно внутрибрюшинно вводили раствор декстрана в дозе 300 мг/кг. Водный раствор экстракта зубчатки вводили внутрижелудочно в дозе 100 мг/кг за 1 час до введения флорогенного агента, а затем ежедневно 1 раз в сутки в течение всего эксперимента. Крысы контрольной группы получали эквиобъемное количество дистиллированной воды по аналогичной схеме. В качестве препарата сравнения использовали калефлон в дозе 100 мг/кг. Площадь некротизированной ткани оценивали на 1, 3, 7, 14 и 21 сутки эксперимента путем нанесения контура некроза на прозрачную пленку. Полученные данные представлены в таблице 12.
Как следует из данных, приведенных в таблице 12, курсовое введение экстракта зубчатки в дозе 100 мг/кг оказывает противовоспалительное действие, снижая степень деструкции тканей при альтерации уксусной кислотой и способствуя ускоренной регенерации поврежденной ткани. При этом тестирование на 1 и 3 сутки эксперимента обнаружило лишь тенденцию к уменьшению площади некротизированной ткани (соответственно на 13 и 17% по сравнению с контролем, различие недостоверно), то на 7, 14 и 21 сутки установлено достоверное снижение этого показателя соответственно на 28, 27 и 43% по сравнению с аналогичными данными контрольной группы. При введении препарата сравнения установлена аналогичная тенденция: достоверное уменьшение степени деструкции тканей обнаружено лишь на 7 сутки опыта, однако при дальнейшем наблюдении (на 14 и 21 сутки) калефлон оказывал менее выраженное противовоспалительное действие, чем экстракт зубчатки обыкновенной.
Сравнительная характеристика заявляемого способа с выбранным прототипом представлена в табл. 13.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ЖЕЛЧЕГОННОЙ И ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ | 1999 |
|
RU2159123C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО АДАПТОГЕННОЙ АКТИВНОСТЬЮ | 1997 |
|
RU2135198C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ГЕПАТОЗАЩИТНОЙ АКТИВНОСТЬЮ | 2008 |
|
RU2366445C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ГИПОТЕНЗИВНОЙ АКТИВНОСТЬЮ | 2000 |
|
RU2182487C2 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ | 1999 |
|
RU2160599C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ГИПОГЛИКЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 1999 |
|
RU2141841C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ЖЕЛЧЕГОННОЙ, ПРОТИВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЯМИ | 2014 |
|
RU2557990C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ГИПОЛИПИДЕМИЧЕСКОЙ АКТИВНОСТЬЮ | 2000 |
|
RU2173161C1 |
| СПОСОБ ПОЛУЧЕНИЯ СРЕДСТВА, ОБЛАДАЮЩЕГО ПРОТИВОВОСПАЛИТЕЛЬНОЙ АКТИВНОСТЬЮ | 2002 |
|
RU2206333C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОВОСПАЛИТЕЛЬНОЙ И ОТХАРКИВАЮЩЕЙ АКТИВНОСТЬЮ | 1999 |
|
RU2166954C2 |




Изобретение относится к области фармации и касается способа получения средства и растительного сырья, обладающего желчегонной и противовоспалительной активностью. Растительный материал (трава зубчатки обыкновенной) экстрагируют 35 - 45% спиртом этиловым в соотношении сырье:экстрагент = 1 : 12 - 14 с учетом коэффициента водопоглощения в течение 60 мин при температуре 60 - 65oC и постоянном помешивании. Процесс повторяют дважды. Аналогичным способом проводят третью экстракцию в течение 30 мин. Объединенные водно-спиртовые извлечения фильтруют, упаривают до 1/3 первоначального объема. Кубовый остаток сепарируют. Полученный продукт доупаривают приблизительно до 1/5 первоначального объема и высушивают в вакуум-сушильном шкафу. Изобретение позволяет повысить желчегонную и противовоспалительную активность. 13 табл.
Способ получения средства, обладающего желчегонной и противовоспалительной активностью, путем экстракции растительного сырья - травы зубчатки обыкновенной, отличающийся тем, что экстракцию проводят 35 - 45% этиловым спиртом в соотношении сырье - экстрагент = 1 : 12 - 14 два раза по 60 мин, третью экстракцию осуществляют в течение 30 мин, объединенные извлечения упаривают, очищают сепарированием, концентрируют доупаркой и высушивают в вакуум-сушильном аппарате.
| НИКОЛАЕВ С.М | |||
| и др | |||
| Перспективные виды растений с желчегонным действием из арсенала тибетской медицины | |||
| Известия СО АМН СССР | |||
| - Новосибирск, 1987, с.48-51 | |||
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства | |||
| - М.: Медицина, 1986, ч.1, с.514, 515 | |||
| СРЕДСТВО, ОБЛАДАЮЩЕЕ РЕГЕНЕРАТИВНОЙ АКТИВНОСТЬЮ | 1994 |
|
RU2080871C1 |
| ГЕПАТОПРОТЕКТОРНОЕ, ЖЕЛЧЕГОННОЕ, ПРОТИВОЯЗВЕННОЕ, АНТИСЕПТИЧЕСКОЕ, АНТИСКЛЕРОТИЧЕСКОЕ И СНИЖАЮЩЕЕ ПРОЛИФЕРАЦИЮ КЛЕТОК ПРОСТАТЫ СРЕДСТВО "ТЫКВЕОЛ" | 1997 |
|
RU2104028C1 |
| RU 2064300 C1, 27.02.1996. | |||
Авторы
Даты
2000-12-20—Публикация
1999-10-22—Подача