Изобретение относится к средству для профилактики и лечения диабетических осложнений, а именно к средству для профилактики и лечения диабетической невропатии, нефропатии, офтальмопатии и артериосклероза. В частности, настоящее изобретение относится к средству для профилактики и лечения диабетических осложнений, включающему в качестве активного ингредиента 4-[α-гидрокси-2-метил-5-(1- имидазолил)-бензил]-3,5-диметилбензойную кислоту, ее оптически активное соединение или ее фармацевтически приемлемую соль. Настоящее изобретение относится, кроме того, к способу соответствующей профилактики и лечения диабетических осложнений.
Предпосылки изобретения
Открытие инсулина и его клиническое применение привело к существенному прогрессу в лечении диабета. Поддержание жизнедеятельности пациентов с диабетами, которые до тех пор считались смертельно больными, впоследствии поразительно улучшилось. Однако новой проблемой явились хронические осложнения диабета.
Терапия диабета нацелена на предупреждение таких хронических осложнений и на практике состоит из дополнительного контроля за глюкозой крови и прямого лечения осложнений. Главными хроническими осложнениями диабета, как известно, являются невропатия, нефропатия, офтальмопатия, артериосклероз и тому подобное (David М. с соавт., N. Engl. J. Med., 328, р.1676-1685 (1993)).
Считается, что ответственными за начало и ход хронических осложнений диабета являются различные факторы. Например, известна теория аномального метаболизма сорбита, по которой причина заключается в активном стимулировании метаболического пути образования из сорбита высокомолекулярного спирта (Gabbay K. H. с соавт., N. Engl. J. Med. 228, р.831-837 (1973)), теория нарушения кровообращения, причиной которого является уменьшенный кровоток, связанный с ангиопатией (Dyck P.J. с соавт., Proc. Natl. Acad. Sci. USA, 82, p.2513-2517 (1985)), теория, объясняющая данное заболевание соединением, получаемым в результате реакции неферментативного связывания белка и снижения уровня глюкозы (AGE: повышенное содержание конечного продукта образования сахара) (Brownlee М. с соавт., N. Engl. J. Med. 318, р.1315-1321 (1988)) и тому подобное. На основании каждой из этих гипотез создавали ингибитор альдозоредуктазы и липопростагландин E1, а также ингибитор образования AGE, который находится в стадии разработки.
У больных диабетом наблюдают ускоренную агрегацию тромбоцитов, при этом известно, что этот механизм агрегации активирует биосинтез тромбоксана (сокращенно именуемый ниже TX) A2, связанного с гипергликемией. Это считается одной из причин диабетических хронических заболеваний (Giovanni Davi M.D. с соавт. , N. Engl. J. Med. 322, р.1769-1774 (1990)). В соответствии с этим липопростагландин E1 (именуемый ниже иногда Lipo PGE1), положительно влияет на периферическое кровообращение или ингибирующий агрегацию тромбоцитов, 6-[4-(1- циклогексил-1,2,3,4-тетразол-5-ил)бутокси] -3,4-дигидрокарбостирил (цилостазол) и 6-[4-(R)-[хлорфенилсульфонамидо] - 1-(3-пиридилметил)пирролидин-2 (S) -ил)-5-(Z)-гексеновая кислота гидрохлорид (исследовательский номер: KDI-792), обладающий антагонистичной к рецептору/ингибирующей синтез активностью ТХА2, находятся в процессе разработки в качестве агентов для профилактики и лечения диабетических осложнений.
С другой стороны, в просмотренной публикации Японского патента N 41143/1993 описана 4-[α-гидрокси-2-метил-5-(1- имидазолил)бензил]-3,5-диметилбензойная кислота, обладающая фармакологическими активностями, такими как строго ингибирующая биосинтез ТХА2 активность, ингибирование агрегации тромбоцитов, сосудорасширяющее действие и тому подобное; она пригодна для профилактики и лечения тромбозов, внутримозгового кровоизлияния, инфаркта миокарда, острой сердечной недостаточности, стенокардии, гипертонии, астмы, нефрита и тому подобное; ее оптически активное соединение и ее фармацевтически приемлемая соль. Все же неизвестно, что эти соединения действуют в качестве агентов для профилактики и лечения диабетических осложнений.
В данных обстоятельствах создание нового терапевтического средства для непосредственного действия на хронические осложнения диабета для соответствующей профилактики и лечения диабета, который обладает способностью обеспечивать лучшее качество жизни, является желательным.
Указанные Lipo PGE, цилостазол, KDI-792 и им подобные, которые созданы в качестве средств для профилактики и лечения диабетических осложнений, средств, улучшающих периферическое кровообращение, средств, ингибирующих агрегацию тромбоцитов, и средств, обладающих антагонистичной к рецептору ТХА2 ингибирующей синтез активностью, проявляют лишь краткосрочную активность и требуют 2-3-кратного ежедневного введения. Принимая во внимание соответствующее качество жизни пациентов с диабетом, этого явно недостаточно.
Авторы настоящего изобретения подтвердили, что озагрель натрия [натрий (Е)-p-(имидазол-1-илметил)циннамат] , ингибирующий синтез ТХА2, тормозит запуск биосинтеза ТХА2 у крыс с диабетом, но не улучшает сниженную скорость проводимости хвостового нерва. Это дает основание полагать, что не каждый ингибитор синтеза ТХА2 является эффективным при диабетических осложнениях.
Описание изобретения
Авторы настоящего изобретения провели интенсивные исследования в этом направлении и обнаружили, что 4-[α-гидрокси-2-метил-5-(1-имидазолил)бензил] -3, 5-диметилбензойная кислота, ее оптически активное соединение и ее фармацевтически приемлемая соль, обладающие фармакологическими активностями, состоящими из активности, ингибирующей биосинтез ТХА2, активности, ингибирующей агрегацию тромбоцитов, и сосудо-расширяющего действия, представляются пригодными для профилактики и лечения диабетических осложнений, а именно для профилактики и лечения диабетической невропатии, нефропатии, офтальмопатии и артериосклероза, и что ее активность является длительно действующей при малых дозах, делая тем самым возможным однократное ежедневное применение, что позволяет осуществлять настоящее изобретение.
В соответствии с этим настоящее изобретение обеспечивает нижеследующее.
1) Средство для профилактики и лечения диабетических осложнений, включающее 4-[ α-гидрокси-2-метил-5-(1- имидазолил)-бензил]-3,5-диметилбензойную кислоту, ее оптически активное соединение или ее фармацевтически приемлемую соль в качестве активного ингредиента.
2) Средство для профилактики и лечения диабетических осложнений, включающее 4-[α-гидрокси-2- метил-5-(1-имидазолил)-бензил] -3,5-диметилбензоат натрия дигидрата в качестве активного ингредиента.
3) Средство для профилактики и лечения диабетических осложнений, включающее (S)-(-)-4-[α-гидрокси-2-метил-5-(1-имидазолил)бензил]-3,5- диметилбензойную кислоту или ее фармацевтически приемлемую соль в качестве активного ингредиента.
4) Средство для профилактики и лечения диабетических осложнений, включающее (S)-(-)-4-[α-гидрокси-2-метил-5-(1- имидазолил)бензил]-3,5-диметилбензоат натрия 2/3-гидрат, в качестве активного ингредиента.
5) Средство для профилактики и лечения по вышеуказанным пунктам 1)-4), в которых соответствующее диабетическое осложнение представлено, как минимум, одним из представителей, выбранным из группы, состоящей из невропатии, нефропатии, офтальмопатии и артериосклероза.
6) Средство для профилактики и лечения по вышеуказанным пунктам 1)-4), в которых диабетическое осложнение представляет собой невропатию.
7) Средство для профилактики и лечения по вышеуказанным пунктам 1)- 4), в которых диабетическое осложнение представляет собой нефропатию.
8) Средство для профилактики и лечения по вышеуказанным пунктам 1)-4), в которых диабетическое осложнение представляет собой офтальмопатию.
9) Средство для профилактики и лечения по вышеуказанным пунктам 1)-4), в которых диабетическое осложнение представляет собой артериосклероз.
10) Способ профилактики и лечения диабетических осложнений, включающий применение эффективного количества 4-[ α - гидрокси-2-метил-5-(1-имидазолил)бензил] -3,5-диметилбензойной кислоты, ее оптически активного соединения или ее фармацевтически приемлемой соли.
11) Способ профилактики и лечения диабетических осложнений, включающий применение эффективного количества 4-[ α -гидрокси- 2-метил-5-(1-имидазолил)бензил]-3,5-диметилбензоата натрия дигидрата.
12) Способ профилактики и лечения диабетических осложнений, включающий применение эффективного количества (S)-(-) -4-[ α - гидрокси-2-метил-5-(1-имидазолил) бензил] -3,5- диметилбензойной кислоты или ее фармацевтически приемлемой соли.
13) Способ профилактики и лечения диабетических осложнений, включающий применение эффективного количества (S)-(-)-4-[ α - гидрокси-2-метил-5-(1-имидазолил)бензил]-3,5-диметилбензоата натрия 2/3-гидрата.
14) Способ по любому из вышеуказанных пунктов 10)- 13), в которых диабетическое осложнение представлено, как минимум, одним из группы, состоящей из невропатии, нефропатии, офтальмопатии и артериосклероза.
15) Способ по любому из вышеуказанных пунктов 10)-13), в которых диабетическое осложнение представляет собой невропатию.
16) Способ по любому из вышеуказанных пунктов 10)-13), в которых диабетическое осложнение представляет собой нефропатию.
17) Способ по любому из вышеуказанных пунктов 10)-13), в которых диабетическое осложнение представляет собой офтальмопатию.
18) Способ по любому из вышеуказанных пунктов 10)-13), в которых диабетическое осложнение представляет собой артериосклероз.
19) Использование 4- [α-гидрокси-2-метил-5-(1-имидазолил)-бензил]-3,5- диметилбензойной кислоты, ее оптически активного соединения или ее фармацевтически приемлемой соли для получения лекарственного средства для профилактики и лечения диабетических осложнений.
20) Использование 4-[α-гидрокси-2-метил-5-(1-имидазолил)- бензил]-3,5-диметилбензоата натрия дигидрата для получения лекарственного средства для профилактики и лечения диабетических осложнений.
21) Использование (S)-(-)-4-[α-гидрокси-2-метил-5-(1- имидазолил)бензил] -3,5-диметилбензойной кислоты или ее фармацевтически приемлемой соли для получения лекарственного средства для профилактики и лечения диабетических осложнений.
22) Использование (S)-(-)-4-[ α -гидрокси-2-метил-5- (1-имидазолил)бензил]-3,5-диметилбензоата натрия 2/3-гидрата для получения лекарственного средства для профилактики и лечения диабетических осложнений.
23) Использование по любому из вышеуказанных пунктов 19)-22), в которых диабетическое осложнение представлено, как минимум, одним из представителей, выбранным из группы, состоящей из невропатии, нефропатии, офтальмопатии и артериосклероза.
24) Использование по любому из вышеуказанных пунктов 19)-22), в которых диабетическое осложнение представляет собой невропатию.
25) Использование по любому из вышеуказанных пунктов 19)-22), в которых диабетическое осложнение представляет собой нефропатию.
26) Использование по любому из вышеуказанных пунктов 19)-22), в которых диабетическое осложнение представляет собой офтальмопатию.
27) Использование по любому из вышеуказанных пунктов 19)-22), в которых диабетическое осложнение представляет собой артериосклероз.
28) Фармацевтическая композиция для профилактики и лечения диабетических осложнений, которая включает эффективное количество 4-[α-гидрокси-2-метил-5-(1-имидазолил)бензил] -3,5- диметилбензойной кислоты, ее оптически активное соединение и фармацевтически приемлемый носитель.
29) Фармацевтическая композиция для профилактики и лечения диабетических осложнений, которая включает эффективное количество 4-[ α -гидрокси-2-метил-5- (1-имидазолил)бензил] -3,5-диметилбензоата натрия дигидрата и фармацевтически приемлемый носитель.
30) Фармацевтическая композиция для профилактики и лечения диабетических осложнений, которая включает эффективное количество (S)-(-)-4-[ α -гидрокси-2-метил-5-(1-имидазолил]-бензил] -3,5-диметилбензойной кислоты или ее фармацевтически приемлемой соли и фармацевтически приемлемый носитель.
31) Фармацевтическая композиция для профилактики и лечения диабетических осложнений, которая включает эффективное количество (S)-(-)-4-[α-гидрокси-2-метил-5-(1-имидазолил)-бензил] -3,5- диметилбензоата натрия 2/3-гидрата и фармацевтически приемлемый носитель.
32) Фармацевтическая композиция по любому из вышеуказанных пунктов 28)-31), в которых диабетическое осложнение представлено, как минимум, одним из представителей, выбранным из группы, состоящей из невропатии, нефропатии, офтальмопатии и артериосклероза.
33) Фармацевтическая композиция по любому из вышеуказанных пунктов 28)-31), в которых диабетическое осложнение представляет собой невропатию.
34) Фармацевтическая композиция по любому из вышеуказанных пунктов 28)-31), в которых диабетическое осложнение представляет собой нефропатию.
35) Фармацевтическая композиция по любому из вышеуказанных пунктов 28)-31), в которых диабетическое осложнение представляет собой офтальмопатию.
36) Фармацевтическая композиция по любому из вышеуказанных пунктов 28)-31), в которых диабетическое осложнение представляет собой артериосклероз.
37) Коммерческая упаковка, включающая фармацевтическую композицию, по любому из вышеуказанных пунктов 28)-31) и описание ее содержания, причем данное описание утверждает, что указанная фармацевтическая композиция может или должна использоваться для профилактики и лечения диабетических осложнений.
Подробное описание настоящего изобретения
Воздействие в качестве средства для профилактики и лечения диабетических осложнений, представленных в настоящем изобретении, а именно воздействие в качестве средства для профилактики и лечения невропатии, нефропатии, офтальмопатии и артериосклероза, можно подтвердить, регистрируя изменения скорости проводимости хвостового нерва крысы, скорости проводимости седалищного нерва, степени гломерулярного расстройства, количества экскретируемого с мочой альбумина, при офтальмоскопическом обследовании степени катаракты, степени гипертрофии и тому подобное.
В диабетических осложнениях настоящего изобретения невропатия означает симметричную полиневропатию сенсорных, двигательных или вегетативных нервов и локальную или полидомную невропатию церебрального нерва; а офтальмопатия означает катаракту, глаукому, ретинопатию, ирит и тому подобное.
Соединения настоящего изобретения могут быть синтезированы способами, описанными в публикации Японского Патента N 41143/1993 и в неизученной публикации Японского патента N 215771/1990 с незавершенной экспертизой.
Фармацевтически приемлемые соли соединений настоящего изобретения включают, например, соли неорганической кислоты, такой как хлористоводородная кислота, бромистоводородная кислота и серная кислота; кислые аддитивные соли органической кислоты, такой как фумаровая кислота, малеиновая кислота, миндальная кислота, лимонная кислота, винная кислота, салициловая кислота и тому подобное; соли металла, такого как натрий, калий, литий, кальций, магний, цинк и алюминий и соли аминокислоты, такой как лизин. Кроме того, охвачены также гидраты, такие как 1/2-гидрат, 1/3- гидрат, 2/3-гидрат, моногидрат, 3/2-гидрат и дигидрат.
Предпочтительные соединения настоящего изобретения включают 4-[α-гидрокси-2-метил-5-(1-имидазолил)бензил] -3,5-диметилбензоат натрия дигидрат (ниже иногда именуемый соединением A-1), (S)-(-)-4-[α-гидрокси-2-мeтил-5-(1-имидaзoлил)бензил] -3,5-диметилбензоат натрия 2/3-гидрат (ниже иногда именуемый соединением A-2), (R)-(+)-4-[α-гидрокси-2-метил- 5-(1-имидазолил)бензил] -3,5-диметилбензоат натрия 2/3 гидрат (ниже иногда именуемый соединением A-3), (S)-(-)-4-[α-гидрокси- 2-метил-5-(1-имидазолил)бензил] -3,5-диметилбензойная кислота (ниже иногда именуемая соединением A-4) и (R)-(+)-4-[α-гидрокси-2- метил-5-(1-имидазолил)бензил]-3,5-диметилбензойная кислота (ниже иногда именуемая соединением A-5). Соединение A-1 представляет собой кристаллы с точкой плавления 271-285oC. Соединение A-2 имеет вращение плоскости поляризации света [α]
Данное средство для профилактики и лечения диабетических осложнений в соответствии с настоящим изобретением создано в качестве общего фармацевтического препарата. Например, соответствующее соединение настоящего изобретения создано в дозовой форме, подходящей для перорального или парентерального введения, такой как фармацевтическая композиция или таблетка, пилюля, порошок, гранула, капсула, пастилка, сироп, жидкий раствор, эмульсия, суспензия, инъекция (жидкого раствора, суспензии), суппозитории, летучий препарат, чрескожный поглотитель, глазные капли, глазная мазь и тому подобное, которые получали путем смешивания данного соединения с фармацевтически приемлемым носителем (напр., наполнитель, связывающее вещество для приготовления таблетки, дезинтегрирующее вещество, корректирующее вещество, корригирующее вещество, эмульгирующий агент, разбавитель, солюбилизатор и тому подобное). При получении твердого препарата использовали добавку, такую как сахароза, лактоза, целлюлоза, D-маннит, мальтит, декстран, крахмал, агар, аргинаты, хитины, хитозаны, пектин, трагакантовые камеди, гуммиарабик, желатины, коллагены, казеин, альбумин, фосфат кальция, сорбит, глицин, карбоксиметилцеллюлоза, поливинилпирролидон, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, глицерин, полиэтиленгликоль, кислый углекислый натрий, стеарат магния, тальк и тому подобное. При необходимости изготавливали таблетки с обычным таблеточным покрытием, например таблетка, покрытая сахарной оболочкой, таблетка, покрытая энтеросолюбильной оболочкой, таблетка с пленочным покрытием или двухслойная таблетка или многослойная таблетка.
При получении полутвердого препарата используют животные и растительные жиры и масла (напр., оливковое масло, кукурузное масло, касторовое масло и тому подобное), минеральное масло и жиры (напр., вазелин, белый вазелин, твердый парафин и тому подобное), воск (напр., масло хохобы, карнаубский воск, желтый пчелиный воск и тому подобное), частично синтезированный или полностью синтезированный глицериновый эфир жирной кислоты (напр., эфир лауриновой кислоты, эфир миристиновой кислоты, эфир пальмитиновой кислоты и т. п. и пр. Примеры коммерчески доступных его продуктов включают Witepsol (производит Dynamite Novel), Pharmasol (производит NOF Corporation) и тому подобное.
При получении жидкого препарата используют добавку, такую как хлорид натрия, сорбит, глицерин, оливковое масло, пропиленгликоль, этиловый спирт и тому подобное. При получении инъецируемого материала, в частности, используют стерильный водный раствор (напр., физиологический раствор или изотонический раствор) или маслянистую жидкость (напр., кунжутное масло и масло соевых бобов). При необходимости можно также использовать суспендирующий агент (напр. , натрий-карбоксиметилцеллюлозу), неионогенное поверхностно-активное вещество, солюбилизатор (напр., бензилбензоат и бензиловый спирт) и тому подобное. При получении глазных капель используют водную жидкость или водный раствор, которая, в частности, представляет собой стерильный водный раствор для инъекций. Эта жидкость для глазных капель может содержать разнообразные подходящие добавки, такие как буфер (предпочтительно, боратный буфер, ацетатный буфер, карбонатный буфер и тому подобное, используемые для снижения раздражения), изотонический агент, солюбилизатор, консервант, сгуститель, хелатирующий агент, агент для доведения pH (предпочтительно, pH, как правило, доводят примерно до 6-8,5), соединение ароматического ряда и тому подобное.
Количество данного активного ингредиента в этих препаратах составляет 0,1-100% по массе, соответственно 1-50 мас.% на данный препарат. Дозу варьируют в зависимости от симптоматики, веса тела, возраста пациентов и тому подобное. В случае перорального применения доза составляет, как правило, около 0,01-50 мг/кг веса тела/день для взрослого, которую предпочтительно назначают в виде однократной дозы или нескольких доз.
ПРИМЕРЫ
Данное средство для профилактики и лечения диабетических осложнений в настоящем изобретении более конкретно объясняется с помощью рецептурных примеров и фармакологической активности. Следует отметить, что настоящее изобретение не ограничивается этими иллюстративными примерами.
Рецептурный пример 1: Таблетка с пленочным покрытием
Соединение A-1 - 50,0 мг
D-маннит - 70,5 мг
Кукурузный крахмал - 16,0 мг
Кислый углекислый натрий - 15,0 мг
Гидроксипропилметилцеллюлоза - 3,0 мг
Тальк - 5,0 мг
Стеарат магния - 0,5 мг
Соединение A-1, D-маннит, кукурузный крахмал и кислый углекислый натрий смешивали, а водный раствор гидроксипропилметилцеллюлозы распыляли для поточного гранулирования. Полученные гранулы просеивали через сито с 24-меш и добавляли тальк и стеарат магния. Полученную смесь обрабатывали в ротационном компрессоре (Kikusui Seisakusho), чтобы получить таблетки весом 160 мг, каждая. Затем агент для пленочного покрытия, включающий гидроксипропилметилцеллюлозу в качестве основы пленочного покрытия, наносили из расчета 6 мг на таблетку.
Рецептурный пример 2: Тонкие гранулы
Соединение A-1 - 10%
D-маннит - 89,5%
Гидроксипропилцеллюлоза - 0,5%
Соединение A-1 и D-маннит смешивали и добавляли водный раствор гидроксипропилцеллюлозы. Полученную смесь месили, затем гранулировали и сушили при 50oC. Полученные гранулы просеивали через сито с 32-меш для получения тонких гранул.
Рецептурный пример 3: Таблетки
Соединение A-1 - 50,0 мг
D-маннит - 30,0 мг
Кукурузный крахмал - 19,0 мг
Кислый углекислый натрий - 15,0 мг
Гидроксипропилметилцеллюлоза - 1,5
Тальк - 4,0 мг
Стеарат магния - 0,5 мг
Соединение A-1, D-маннит, кукурузный крахмал и кислый углекислый натрий смешивали, а водный раствор гидроксипропилметилцеллюлозы распыляли для поточного гранулирования. Полученные гранулы просеивали через сито с 24-меш и добавляли тальк и стеарат магния. Полученную смесь обрабатывали в ротационном компрессоре (Kikusui Seisakusho), чтобы получить таблетки весом 120 мг, каждая.
Рецептурный пример 4: Тонкие гранулы
Соединение A-2 - 5%
D-маннит - 92%
Гидроксиметилпропилцеллюлоза - 3%
Соединение A-2 и D-маннит смешивали и добавляли водный раствор гидроксипропилметилцеллюлозы. Полученную смесь месили, затем гранулировали и сушили при 50oC. Полученные гранулы просеивали через сито с 32-меш, чтобы получить тонкие гранулы.
Фармакологическая активность данного фармацевтического агента настоящего изобретения поясняется на экспериментальных примерах.
Экспериментальный пример 1
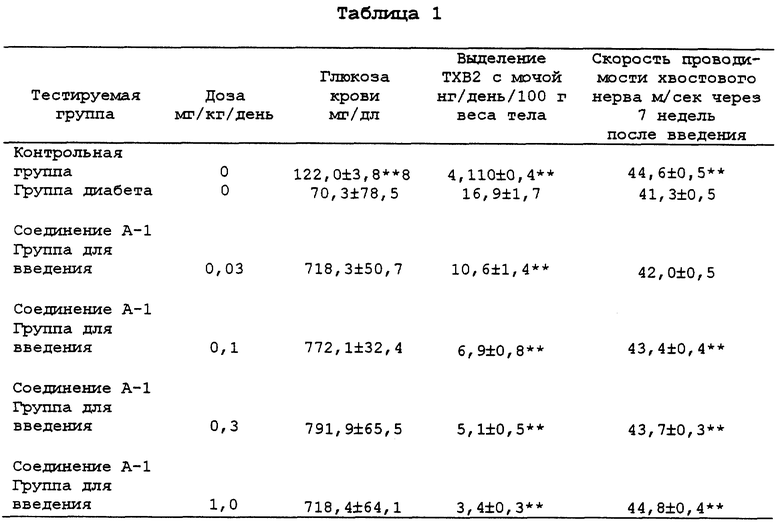
Диабет индуцировали внутривенным введением стрептозотоцина (65 мг/кг) 6-недельным самцам крыс Sprague-Dawley. Через 2-4 недели после начала диабета 0,5%-ную суспензию гидроксипропилметилцеллюлозы, содержащую соединение настоящего изобретения, вводили перорально один раз в день. Через 4-7 недель после введения измеряли скорость проводимости хвостового нерва с помощью индуктивного потенциала испытательного устройства (Neuropack 2, выпускаемый Ninon Kohden) в соответствии с модификацией метода Miyoshi (Fukuoka Medical Journal, vol. 62, pp. 588-603 (1971)). Для точности подкожную температуру хвоста поддерживали на уровне 37oC, а хвостовой нерв чрескожно стимулировали электричеством в 2-х точках для стимуляции (интервал 6 см). Расстояние между точками стимуляции делили на разность между латентными состояниями на индуцируемой электромиограмме, чтобы получить скорость проводимости нерва. Что касается испытуемой группы в табл. 1, уровень сахара в крови измеряли через 6 недель после ведения. Через 7 недель после введения измеряли выделение с мочой ТХВ2, который является стабильным метаболитом TXA2 (см. табл.1).
Полученные данные представлены в виде средней ± стандартная ошибка для группы из 11-12 крыс. Каждую группу сравнивали с группой диабета по критерию Dunnett (**P<0,01).
Из приведенных результатов экспериментального примера следует, что данное соединение A-1 настоящего изобретения уменьшает выделение ТХВ2 с мочой, количество которого повышено при диабете, и повышает скорость проводимости хвостового нерва дозо-зависимым образом, которая была снижена при диабете, не влияя на уровень глюкозы в крови.
Полученные данные (см. табл. 2) представлены в виде средней ± стандартная ошибка для группы из 10 крыс. Каждую группу сравнивали с группой диабета по критерию Dunnett (**P<0,01).
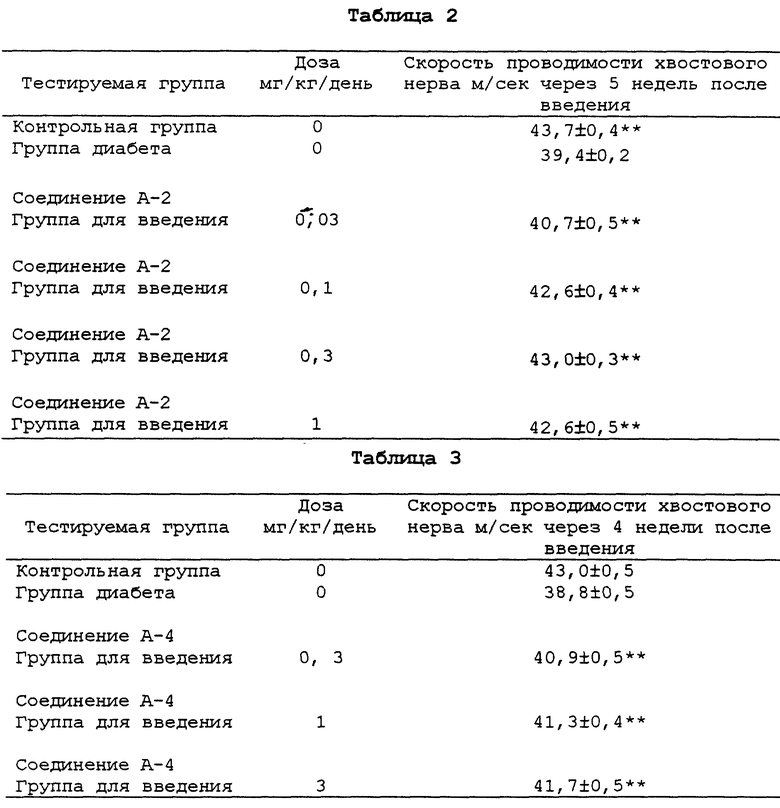
Полученные данные (см. табл. 3) представлены в виде средней ± стандартная ошибка для группы из 10 крыс. Соединение, вводимое каждой группе, сравнивали с группой диабета по критерию Dunnet (**P<0,01).
Из приведенных результатов экспериментальных примеров следует, что соединение A-2 и соединение A-4 настоящего изобретения препятствуют снижению скорости проводимости хвостового нерва дозо-зависимым образом.
Экспериментальный пример 2
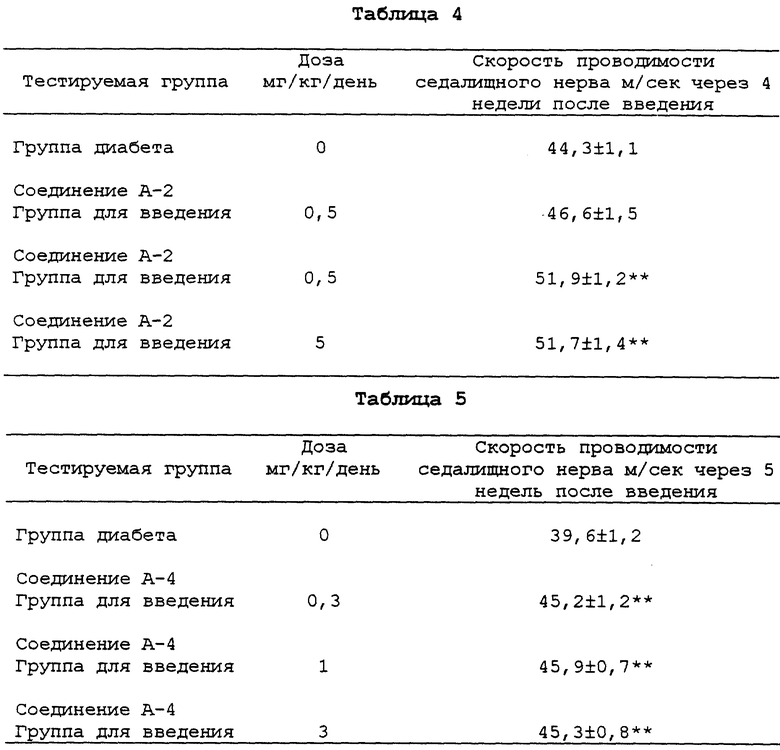
0,5%-ную суспензию гидроксипропилметилцеллюлозы, содержащую соединение настоящего изобретения, вводили перорально 9-недельным самцам мышей, со спонтанным диабетом (db/db), один раз в день. Через 4-5 недель после введения измеряли скорость проводимости седалищного нерва с помощью индуктивного потенциала испытательного устройства (Neuropack 2, производимый Nihon Kohden) в соответствии с модификацией метода Yasuda (Diabetes, 38, р.832-838 (1989)). Для точности ректальную температуру поддерживали на уровне 37oC и две точки на седалищной вырезке и голеностопном суставе стимулировали чрескожно электричеством. Расстояние между точками стимулирования делили на разность между неактивными состояниями в индуцируемой электромиограмме, чтобы получить скорость проводимости нерва (см.табл. 4).
Полученные данные представлены в виде средней ± стандартная ошибка для 7-9 мышей в группе. Каждую группу сравнивали с группой диабета по критерию Dunnett (**P<0,01).
Полученные данные (см. табл. 5) представлены в виде средней ± стандартная ошибка для 8-9 мышей в группе. Каждую группу сравнивали с группой диабета по критерию Dunnett (**P<0,01).
Из приведенных результатов экспериментальных примеров следует, что данное соединение A-2 и соединение A-4 настоящего изобретения повышают скорость проводимости седалищного нерва у мышей со спонтанным диабетом.
Экспериментальный пример 3
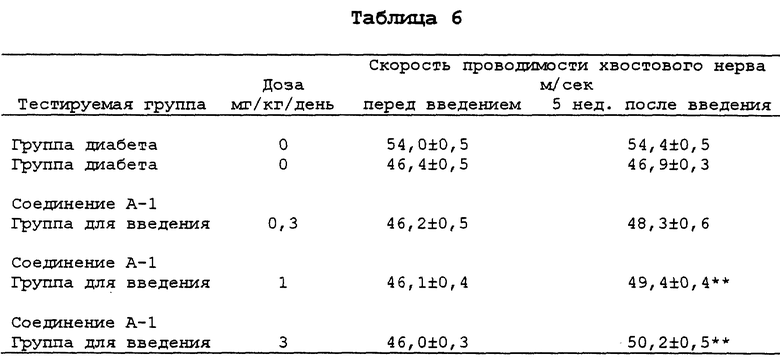
У 6-недельных крыс-самцов Sprague- Dawley диабет индуцировали внутривенным введением стрептозотоцина (65 мг/кг). Начиная с 16 недель после начала диабета, один раз в день перорально вводили 0,5%-ную суспензию гидроксипропилметилцеллюлозы, содержащую соединение A-1. Через 5 недель после введения измеряли скорость проводимости хвостового нерва с помощью индуктивного потенциала испытательного устройства (Neuropack 2, производимый Nihon Kohden) в соответствии с модификацией метода Miyoshi (Fukuoka Medical Journal, vol/62, pp.588-603 (1971)). Для точности подкожную температуру мышиного хвоста поддерживали на уровне 37oC, а нерв мышиного хвоста чрескожно стимулировали электричеством по 2-м точкам стимуляции (интервал 6 см). Расстояние между этими точками стимуляции делили на разность между латентными состояниями в индуцируемой электромиограмме, чтобы получить скорость проводимости нерва (см. табл. 6).
Полученные данные представлены в виде средней ± стандартная ошибка для группы из 10 мышей. Каждую группу сравнивали с группой диабета по критерию Dunnett (P**<0,01).
Из вышеприведенных результатов экспериментального примера следует, что данное соединение A-1 повышает скорость проводимости хвостового нерва дозо-зависимым образом, которая понижалась с развитием диабета.
Экспериментальный пример 4
У 5-недельных крыс-самцов Sprague-Dawley диабет индуцировали внутривенным введением стрептозотоцина (65 мг/кг). Начиная с 9 недель после начала диабета, один раз в день перорально вводили 0,5%-ную суспензию гидроксипропилметилцеллюлозы, содержащую соединение A-1. Через 9 недель с момента введения удаляли почку для определения степени гломерулярного нарушения и фиксировали в 10%-ном забуференном нейтральном формалиновом растворе. Тканевые срезы окрашивали гематоксилинэозином. Состояние клубочков оценивали в соответствии со степенью обструкции в 5 стадий (0: нет обструкции, 1: до 25% обструкции, 2: до 50% обструкции, 3: до 75% обструкции, 4: до 100% обструкции). В образце оценивали пятьдесят клубочков и полученную общую оценку использовали в качестве показателя степени гломерулярного нарушения. Эту операцию осуществляли "вслепую" (см. табл. 7).
Полученные данные представлены в виде средней ± стандартная ошибка. Каждую группу сравнивали с группой диабета по критерию Dunnett (*P<0,05).
Из приведенных результатов экспериментального примера следует, что данное соединение A-1 настоящего изобретения тормозит развитие гломерулярных нарушений, обусловленных диабетом, дозо-зависимым образом.
Экспериментальный пример 5
У 6-недельных крыс-самцов Sprague-Dawley диабет индуцировали внутривенным введением стрептозотоцина (65 мг/кг). Начиная с 2-х недель после начала диабета, один раз в день перорально вводили 0,5%-ную суспензию гидроксипропилметил-целлюлозы, содержащую соединение A-1. Мочу собирали в течение 24 часов, иногда с недельным интервалом. Количество экскретируемого альбумина мочи определяли в иммуноферментном анализе. Кроме того, фотографировали сетчатку и путем подсчета обследовали регенерирующиеся кровеносные сосуды. После завершения введения лекарственного средства подопытных крыс забивали и кровеносные сосуды, такие как аорта, брали для создания тканевых образцов. Такой образец, окрашенный гематоксилин-эозином, обследовали под световым микроскопом для количественного определения степени tunica intima.
Из приведенных рецептурных примеров и фармакологических экспериментов ясно, что фармацевтическое средство настоящего изобретения пригодно для профилактики и лечения диабетических осложнений, а именно диабетической невропатии, нефропатии, офтальмопатии, артериосклероза и тому подобное. Действие данного лекарственного средства является длительным при очень малых дозах и однократное введение в день представляется достаточным.

Изобретение относится к медицине, в частности к средству для профилактики и лечения диабетических осложнений, включающему в качестве активного ингредиента 4-[α-гидрокси- 2-метил-5-(1-имидазолил)-бензил] -3,5-диметилбензойную кислоту, ее оптически активное соединение или ее фармацевтически приемлемую соль, а также относится к фармацевтической композиции и к способу профилактики и лечения диабетических осложнений, в частности диабетической невропатии, нефропатии, офтальмопатии, артериосклероза. Лекарственное средство является длительным при очень малых дозах и достаточно однократного ежедневного введения. 12 с. и 15 з.п. ф-лы, 7 табл.
| Упаковка для мелких предметов | 1982 |
|
SU1089002A1 |
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
| СПОСОБ ПОЛУЧЕНИЯ КРЕМНИЙОРГАНИЧЕСКИХ СОЕДИНЕНИЙ С ХРОМТРИКАРБОНИЛЬНЫМИ ГРУППАМИ | 0 |
|
SU379579A1 |
Авторы
Даты
2001-09-10—Публикация
1996-12-24—Подача