Область техники
Данное изобретение относится к стимуляторам экспрессии MAG. Особенно, настоящее изобретение относится к стимуляторам экспрессии MAG (миелин-ассоциированный гликопротеин), которые можно использовать в качестве агента для профилактики и/или лечения заболеваний, в основном представляющих гипомиелинизацию и, кроме того, дисмиелинизацию или демиелинизацию. Более конкретно, настоящее изобретение относится к стимуляторам экспрессии MAG, содержащим 4-[α-гидрокси-5-(1-имидазолил)-2-метилбензил]-3,5-диметилбензойную кислоту, ее оптически активную форму или ее фармацевтически приемлемую соль в качестве активного ингредиента.
Предпосылки создания изобретения
Позвоночные животные имеют развитый миелинированный нерв, чтобы быть способными к обработке с большой скоростью большой информации. Миелиновая оболочка, которая является характеристикой миелинированного нерва, образуется после окружения нервного аксона цитоплазмической мембраной олигодендроцита или шванновской клетки и имеет многослойную структуру. В результате нерв становится изолированным, а также приобретает очень высокий импеданс и очень низкую емкость. Натриевые каналы присутствуют при аккумуляции в перехвате Ранвье, который является границей участка между миелиновой оболочкой и другой миелиновой оболочкой, облегчают сальтаторную проводимость импульса и способны к обработке с большой скоростью большой информации (а именно, обладают высокой скоростью нервной проводимости).
Основным компонентом, образующим миелиновую оболочку, является миелин, и в качестве компонента для стабилизации многослойной структуры миелиновой оболочки известны миелинспецифические белки. Из них протеолипидный белок и белок Ро вовлекаются в перекрестное сшивание и адгезию между миелиновыми мембранами и миелиновый основной белок (далее называемый МВР) присутствует в цитоплазме миелиновых оболочек и вовлекается в уплотнение оболочек (Morell P. et al., in Basic Neurochemistry, Siegel GJ et al. Eds. Ravan Press, p.117-143 (1994)). Кроме того, миелин-ассоциированный гликопротеин (в дальнейшем иногда называемый MAG) вовлекается в адгезию между аксоном и миелиновыми оболочками (Quarles RH, Myelin-associated glycoprotein: functional and clinical aspects, in Neuronal and Glial Proteins: Structure, Function and Clinical Application, Marangos PJ et al. Eds. Academic Press, New York, p. 295 (1988)).
MAG принадлежит к суперсемейству иммуноглобулинов и электрофоретическая подвижность его составляет 100 кДа. Когда начинается миелинизация, MAG экспрессируется олигодендроцитом в центральной нервной системе и шванновскими клетками в периферической нервной системе. Доля MAG в миелине составляет только 1% в центральной нервной системе и 0,1% в периферической нервной системе. В последнее время было внесено, что MAG не только играет роль в качестве простой молекулы адгезии, но также позитивно вовлекается в образование и поддержание миелиновой оболочки, как указано выше.
В шванновской клетке, где MAG экспрессируется избыточно in vitro, стимулируется миелинизация (Owens GC et al., J. Cell Biol., 111, p.1171-1182 (1990)), но в шванновской клетке, где экспрессия MAG уменьшается, миелинизация подавляется (Owens GC et al., Neuron, 7, р.565-575 (1991)). In vivo число миелинизированных нервов у мышей с дефицитом MAG уменьшается и число немиелинизированных нервов увеличивается, что, как считается, вызвано замедлением в образовании миелина (Bartsch S. et al. Brain Res 762, р.231-234 (1997)). С другой стороны, имеется также сообщение, документально показывающее, что несмотря на морфологическое нарушение, наблюдаемое в периаксональном пространстве между аксоном и миелиновой оболочкой, не обнаружено различия в числе миелинизированных нервов, толщине миелиновой оболочки или диаметре аксона нормальных мышей и мышей с дефицитом MAG (Li С. et al. Nature, 369, р.747-750 (1994)). Следовательно, остаются неизвестными многие аспекты относительно связи между MAG и миелинизацией.
Что касается молекулярного механизма миелинизации, в настоящее время имеется только сообщение о том, что MAG связывается с рецептором аксона с активацией тирозинкиназы Fyn (Umemori H. et al. Nature, 367, р.572-576 (1994)) и затем стимулирует экспрессию гена МВР (Umemori H., J.Neurosci, 19, р.1393-1397 (1999)), которое не является достаточным для выяснения механизма.
В качестве заболеваний, в основном представляющих гипомиелинизацию и, кроме того, дисмиелинизацию или демиелинизацию, известны рассеянный склероз, энцефалит, миелит, синдром Гийена-Барре, хронический воспалительный демиелинизирующий полирадикулит, токсикоз, вызванный тяжелыми металлами, дифтерийный токсикоз, гипотиреоз, метахроматическая лейкодегенерация, болезнь Шарко-Мари-Тута и тому подобное (Takeshi Yasuda et al., Clinical Test, 40, p.760-766 (1996)).
Сообщается, что эти заболевания лечат интерфероном, стероидом, γ-глобулином, заменой плазмы или иммуносупрессантом (Gen Sobue, Brain and Development, 30, p.115-120 (1998), Hajime Harukawa et al., Nippon Rinsho, 55, p.187-194 (1997)), но ситуация с лечением не является полностью удовлетворительной. Поскольку у пациентов с рассеянным склерозом исчезновение MAG наблюдают на ранних стадиях заболевания (Moller JR, Ann. Neurol., 22, р.469-474 (1987)), предполагается, что лекарственное средство, которое стимулирует экспрессию MAG, является эффективным для профилактики и/или лечения вышеуказанных заболеваний.
В патентах Японии JP-A-60-34952, JP-B-64-7074, JP-B-3-16348, JP-B-4-15781, JP-B-4-15782, JP-B-5-29031, JP-B-5-41143 и JP-B-5-74589 описывается соединение формулы (I), которое будет описано ниже и которое можно использовать для профилактики и лечения тромбоза, удара, инфаркта миокарда, внезапной сердечной смерти, стенокардии, гипертензии, астмы, нефрита и тому подобное, его оптически активные формы и фармацевтически приемлемые соли, обладающие фармакологическим действием, таким как сильнодействующее ингибирующее действие на биосинтез TXA2, ингибирующее действие на агрегацию тромбоцитов и сосудорасширяющее действие и тому подобное. В WO 97/24333 описывается, что 4-[α-гидрокси-5-(1-имидазолил)-2-метилбензил]-3,5-диметилбензойная кислота, ее оптически активные формы и ее фармацевтически приемлемые соли являются полезными агентами для профилактики и/или лечения диабетических осложнений.
Однако не описывается или не предполагается, что соединение формулы (I), которое будет указано ниже, обладает действием, способствующим экспрессии MAG.
Целью настоящего изобретения являются стимуляторы экспрессии MAG. Более конкретно, целью настоящего изобретения являются стимуляторы экспрессии MAG, которые могут быть агентами для профилактики и/или лечения заболеваний, в основном представляющих гипомиелинизацию и, кроме того, дисмиелинизацию или демиелинизацию.
Описание изобретения
Авторы настоящего изобретения провели интенсивные исследования и обнаружили, что соединение формулы (I), его оптически активная форма и его фармацевтически приемлемая соль стимулируют экспрессию MAG и что они могут быть полезными в качестве агента для профилактики и/или лечения заболеваний, в основном представляющих гипомиелинизацию и, кроме того, дисмиелинизацию или демиелинизацию.
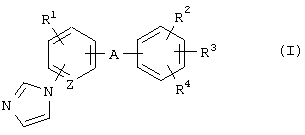
(1) Стимулятор экспрессии MAG, содержащий соединение формулы (I)
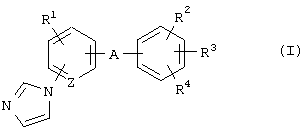
где R1 представляет атом водорода, атом галогена, алкильную группу или алкоксигруппу;
R2 и R3 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу;
R4 представляет алкильную группу, -СООН, -COOR5, -CONR6R7, -CH2NR6R7, -CH2OH или -CH2OR8;
где R5 и R8 представляют, каждый, алкильную группу и
R6 и R7 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу или R6 и R7 в комбинации образуют имидазол вместе с соседним атомом азота;
А представляет -СН(ОН)-, -С(=O)- или -СН2- и
Z представляет =СН- или =N-,
его оптически активную форму или его фармацевтически приемлемую соль (далее иногда будет называться соединением).
(2) Стимулятор экспрессии MAG вышеуказанного (I), который является подходящим для лечения заболевания млекопитающих, в том числе человека, вызванного гипомиелинизацией.
(3) Стимулятор экспрессии MAG вышеуказанного п.(1), который является подходящим для лечения млекопитающих, в том числе человека, где заболевание, в основном, представляет дисмиелинизацию или демиелинизацию.
(4) Стимулятор экспрессии MAG вышеуказанного (1), который является подходящим для лечения млекопитающих, в том числе человека, причем заболеванием является рассеянный склероз, энцефалит, миелит, синдром Гийена-Барре, хронический воспалительный демиелинирующий полирадикулит, токсикоз, вызванный тяжелыми металлами, дифтерийный токсикоз, гипотиреоз, метахроматическая лейкодегенерация или болезнь Шарко-Мари-Тута.
(5) Стимулятор экспрессии MAG по любому из вышеуказанных п.п. от (1) до (4), где в формуле (I) R1 представляет атом галогена, алкильную группу или алкоксигруппу.
(6) Стимулятор экспрессии MAG, включающий 4-[α-гидрокси-5-(1-имидазолил)-2-метилбензил]-3,5-диметилбензойную кислоту, ее оптически активную форму или ее фармацевтически приемлемую соль.
(7) Способ стимуляции экспрессии MAG, который включает введение соединения формулы (I)
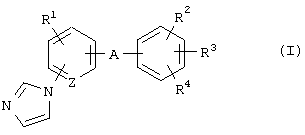
где R1 представляет атом водорода, атом галогена, алкильную группу или алкоксигруппу;
R2 и R3 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу;
R4 представляет алкильную группу, -СООН, -COOR5, -CONR6R7, -CH2NR6R7, -CH2OH или -CH2OR8;
где R5 и R8 представляют, каждый, алкильную группу и
R6 и R7 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу или R6 и R7 в комбинации образуют имидазол вместе с соседним атомом азота;
А представляет -СН(ОН)-, -С(=O)- или -CH2- и
Z представляет =СН- или =N-,
его оптически активной формы или его фармацевтически приемлемой соли млекопитающим, включая человека.
(8) Способ вышеуказанного п.(7), где в формуле (I) R1 представляет атом галогена, алкильную группу или алкоксигруппу.
(9) Способ стимуляции экспрессии MAG, который включает введение 4-[α-гидрокси-5-(1-имидазолил)-2-метилбензил]-3,5-диметилбензойной кислоты, ее оптически активной формы или ее фармацевтически приемлемой соли млекопитающим, в том числе человеку.
(10) Способ профилактики и/или лечения заболевания, вызванного гипомиелинизацией, который включает введение соединения формулы (I)
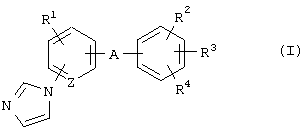
где R1 представляет атом водорода, атом галогена, алкильную группу или алкоксигруппу;
R2 и R3 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу;
R4 представляет алкильную группу, -СООН, -COOR5, -CONR6R7, -CH2NR6R7, -CH2OH или -CH2OR8;
где R5 и R8 представляют, каждый, алкильную группу и
R6 и R7 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу или R6 и R7 в комбинации образуют имидазол вместе с соседним атомом азота;
А представляет -СН(ОН)-, -С(=O)- или -СН2- и
Z представляет =СН- или =N-,
его оптически активную форму или его фармацевтически приемлемую соль млекопитающим, включая человека.
(11) Способ вышеуказанного п.(10), где в формуле (I) R1 представляет атом галогена, алкильную группу или алкоксигруппу.
(12) Способ профилактики и/или терапии заболевания, вызванного гипомиелинизацией, который включает введение 4-[α-гидрокси-5-(1-имидазолил)-2-метилбензил]-3,5-диметилбензойной кислоты, ее оптически активной формы или ее фармацевтически приемлемой соли млекопитающим, в том числе человеку.
(13) Способ профилактики и/или лечения заболевания, в основном представляющего собой дисмиелинизацию или демиелинизацию, который включает введение соединения формулы (I)
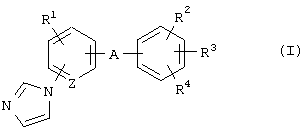
где R1 представляет атом водорода, атом галогена, алкильную группу или алкоксигруппу;
R2 и R3 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу;
R4 представляет алкильную группу, -СООН, -COOR5, -CONR6R7, -CH2NR6R7, -CH2OH или -CH2OR8;
где R5 и R8 представляют, каждый, алкильную группу и
R6 и R7 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу или R6 и R7 в сочетании образуют имидазол вместе с соседним атомом азота;
А представляет -СН(ОН)-, -С(=O)- или -CH2- и
Z представляет =СН- или =N-,
его оптически активной формы или его фармацевтически приемлемой соли млекопитающим, включая человека.
(14) Способ вышеуказанного п.(13), где в формуле (I) R1 представляет атом галогена, алкильную группу или алкоксигруппу.
(15) Способ профилактики и/или лечения заболевания, в основном представляющего дисмиелинизацию или демиелинизацию, который включает введение 4-[α-гидрокси-5-(1-имидазолил)-2-метилбензил]-3,5-диметилбензойной кислоты, ее оптически активной формы или ее фармацевтически приемлемой соли млекопитающим, в том числе человеку.
(16) Способ профилактики и/или лечения рассеянного склероза, энцефалита, миелита, синдрома Гийена-Барре, хронического воспалительного демиелинизирующего полирадикулита, токсикоза, вызванного тяжелыми металлами, дифтерийного токсикоза, гипотиреоза, метахроматической лейкодегенерации или болезни Шарко-Мари-Тута, который включает введение соединения формулы (I)
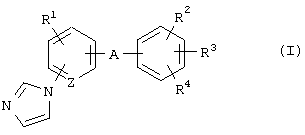
где R1 представляет атом водорода, атом галогена, алкильную группу или алкоксигруппу;
R2 и R3 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу;
R4 представляет алкильную группу, -СООН, -COOR5, -CONR6R7, -CH2NR6R7, -CH2OH или -CH2OR8;
где R5 и R8 представляют, каждый, алкильную группу и
R6 и R7 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу или R6 и R7 в сочетании образуют имидазол вместе с соседним атомом азота;
А представляет -СН(ОН)-, -С(=O)- или -СН2- и
Z представляет =СН- или =N-,
его оптически активной формы или его фармацевтически приемлемой соли млекопитающим, включая человека.
(17) Способ вышеуказанного п.(16), где в формуле (I) R1 представляет атом галогена, алкильную группу или алкоксигруппу.
(18) Способ профилактики и/или лечения рассеянного склероза, энцефалита, миелита, синдрома Гийена-Барре, хронического воспалительного демиелинирующего полирадикулита, токсикоза, вызванного тяжелыми металлами, дифтерийного токсикоза, гипотиреоза, метахроматической лейкодегенерации или болезни Шарко-Мари-Тута, который включает введение 4-[α-гидрокси-5-(1-имидазолил)-2-метилбензил]-3,5-диметилбензойной кислоты, ее оптически активной формы или ее фармацевтически приемлемой соли млекопитающим, в том числе человеку.
(19) Применение соединения формулы (I)

где R1 представляет атом водорода, атом галогена, алкильную группу или алкоксигруппу;
R2 и R3 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу;
R4 представляет алкильную группу, -СООН, -COOR5, -CONR6R7, -CH2NR6R7, -СН2ОН или -CH2OR8;
где R5 и R8 представляют, каждый, алкильную группу и
R6 и R7 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу или R6 и R7 в сочетании образуют имидазол вместе с соседним атомом азота;
А представляет -СН(ОН)-, -С(=O)- или -СН2- и
Z представляет =СН- или =N-,
его оптически активной формы или его фармацевтически приемлемой соли для получения стимулятора экспрессии MAG.
(20) Применение вышеуказанного п.(19), где в формуле (I) R1 представляет атом галогена, алкильную группу или алкоксигруппу.
(21) Применение 4-[α-гидрокси-5-(1-имидазолил)-2-метилбензил]-3,5-диметилбензойной кислоты, ее оптически активной формы или ее фармацевтически приемлемой соли для получения стимулятора экспрессии MAG.
(22) Применение соединения формулы (I)
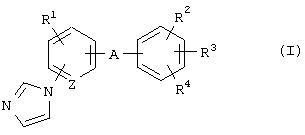
где R1 представляет атом водорода, атом галогена, алкильную группу или алкоксигруппу;
R2 и R3 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу;
R4 представляет алкильную группу, -СООН, -COOR5, -CONR6R7, -CH2NR6R7, -CH2OH или -CH2OR8;
где R5 и R8 представляют, каждый, алкильную группу и
R8 и R7 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу или R6 и R7 в сочетании образуют имидазол вместе с соседним атомом азота;
А представляет -СН(ОН)-, -С(=O)- или -СН2- и
Z представляет =СН- или =N-,
его оптически активной формы или его фармацевтически приемлемой соли для получения стимулятора экспрессии MAG, подходящего для лечения заболевания у млекопитающих, включая человека, которое вызвано гипомиелинизацией.
(23) Применение вышеуказанного п.(22), где в формуле (I) R1 представляет атом галогена, алкильную группу или алкоксигруппу.
(24) Применение 4-[α-гидрокси-5-(1-имидазолил)-2-метилбензил]-3,5-диметилбензойной кислоты, ее оптически активной формы или ее фармацевтически приемлемой соли для получения стимулятора экспрессии MAG, подходящего для лечения заболевания у млекопитающих, включая человека, которое вызвано гипомиелинизацией.
(25) Применение соединения формулы (I)
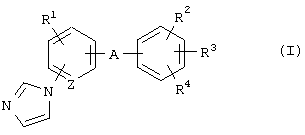
где R1 представляет атом водорода, атом галогена, алкильную группу или алкоксигруппу;
R2 и R3 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу;
R4 представляет алкильную группу, -СООН, -COOR5, -CONR6R7, -CH2NR6R7, -CH2OH или -CH2OR8;
где R5 и R8 представляют, каждый, алкильную группу и
R6 и R7 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу или R6 и R7 в сочетании образуют имидазол вместе с соседним атомом азота;
А представляет -СН(ОН)-, -С(=O)- или -СН2- и
Z представляет =СН- или =N-,
его оптически активной формы или его фармацевтически приемлемой соли для получения стимулятора экспрессии MAG, подходящего для лечения заболевания у млекопитающих, включая человека, которое в основном представляет дисмиелинизацию или демиелинизацию.
(26) Применение вышеуказанного п.(25), где в формуле (I) R1 представляет атом галогена, алкильную группу или алкоксигруппу.
(27) Применение 4-[α-гидрокси-5-(1-имидазолил)-2-метилбензил]-3,5-диметилбензойной кислоты, ее оптически активной формы или ее фармацевтически приемлемой соли для получения стимулятора экспрессии MAG, подходящего для лечения заболевания у млекопитающих, включая человека, которое в основном представляет дисмиелинизацию или демиелинизацию.
(28) Использование соединения формулы (I)
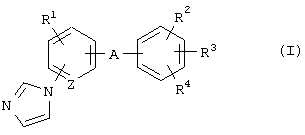
где R1 представляет атом водорода, атом галогена, алкильную группу или алкоксигруппу;
R2 и R3 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу;
R4 представляет алкильную группу, -СООН, -COOR5, -CONR6R7, -CH2NR6R7, -CH2OH или -CH2OR8;
где R5 и R8 представляют, каждый, алкильную группу и
R6 и R7 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу или R6 и R7 в сочетании образуют имидазол вместе с соседним атомом азота;
А представляет -СН(ОН)-, -С(=O)- или -СН2- и
Z представляет =СН- или =N-,
его оптически активной формы или его фармацевтически приемлемой соли для получения стимулятора экспрессии MAG, подходящего для лечения заболевания у млекопитающих, включая человека, которое является рассеянным склерозом, энцефалитом, миелитом, синдромом Гийена-Барре, хроническим воспалительным демиелинизирующим полирадикулитом, токсикозом, вызванным тяжелыми металлами, дифтерийным токсикозом, гипотиреозом, метахроматической лейкодегенерацией или болезнью Шарко-Мари-Тута.
(29) Применение вышеуказанного п.(28), где в формуле (I) R1 представляет атом галогена, алкильную группу или алкоксигруппу.
(30) Применение 4-[α-гидрокси-5-(1-имидазолил)-2-метилбензил]-3,5-диметилбензойной кислоты, ее оптически активной формы или ее фармацевтически приемлемой соли для получения стимулятора экспрессии MAG, подходящего для лечения заболевания у млекопитающих, включая человека, которое является рассеянным склерозом, энцефалитом, миелитом, синдромом Гийена-Барре, хроническим воспалительным демиелинизирующим полирадикулитом, токсикозом, вызванным тяжелыми металлами, дифтерийным токсикозом, гипотиреозом, метахроматической лейкодегенерацией или болезнью Шарко-Мари-Тута.
(31) Коммерческая упаковка, включающая стимулятор экспрессии MAG, включающий соединение формулы (I)
где R1 представляет атом водорода, атом галогена, алкильную группу или алкоксигруппу;
R2 и R3 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу;
R4 представляет алкильную группу, -СООН, -COOR5, -CONR6R7, -CH2NR6R7, -CH2OH или -CH2OR8;
где R5 и R8 представляют алкильную группу и
R6 и R7 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу или R6 и R7 в сочетании образуют имидазол вместе с соседним атомом азота;
А представляет -СН(ОН)-, -С(=O)- или -СН2- и
Z представляет =СН- или =N-,
его оптически активную форму или его фармацевтически приемлемую соль, и связанную с ним письменную инструкцию, причем письменная инструкция устанавливает, что стимулятор экспрессии MAG может или должен быть использован для стимуляции экспрессии MAG.
(32) Коммерческая упаковка по вышеуказанному (31), где в формуле (I) R1 представляет атом галогена, алкильную группу или алкоксигруппу.
(33) Коммерческая упаковка, включающая стимулятор экспрессии MAG, включающий 4-[α-гидрокси-5-(1-имидазолил)-2-метилбензил]-3,5-диметилбензойную кислоту, ее оптически активную форму или ее фармацевтически приемлемую соль, и связанную с ним письменную инструкцию, причем письменная инструкция устанавливает, что стимулятор экспрессии MAG может или должен быть использован для стимуляции экспрессии MAG.
Краткое описание чертежей
Фиг.1, фиг.2 и фиг.3 представляют собой микроскопические фотографии, показывающие результаты экспериментального примера 1, где фиг.1 показывает влияние негативного контрольного соединения (ДМСО) на миелинизацию аксона.
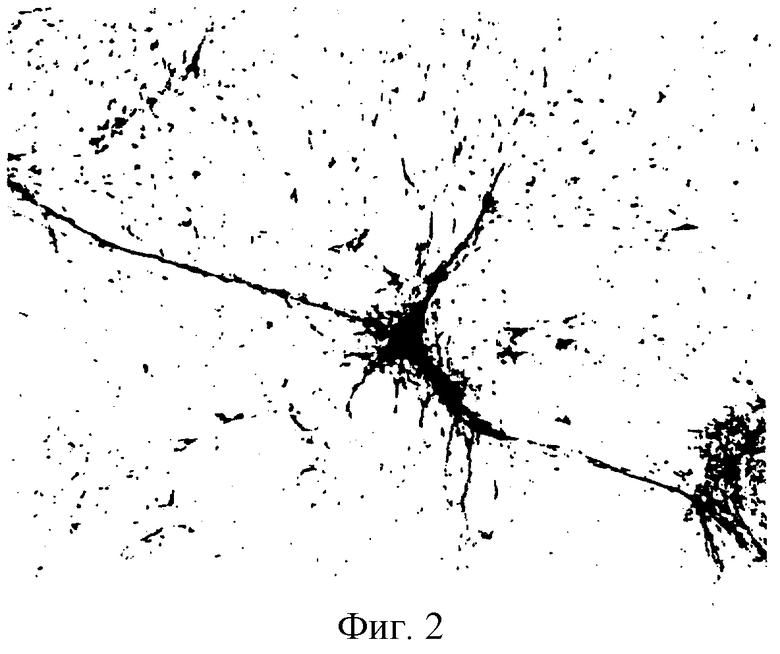
Фиг.2 представляет микроскопическую фотографию, показывающую влияние позитивного контрольного соединения (аскорбиновой кислоты) на миелинизацию аксона.
Фиг.3 представляет микроскопическую фотографию, показывающую влияние соединения настоящего изобретения (Y-128, которое будет указано позднее) на миелинизацию аксона.
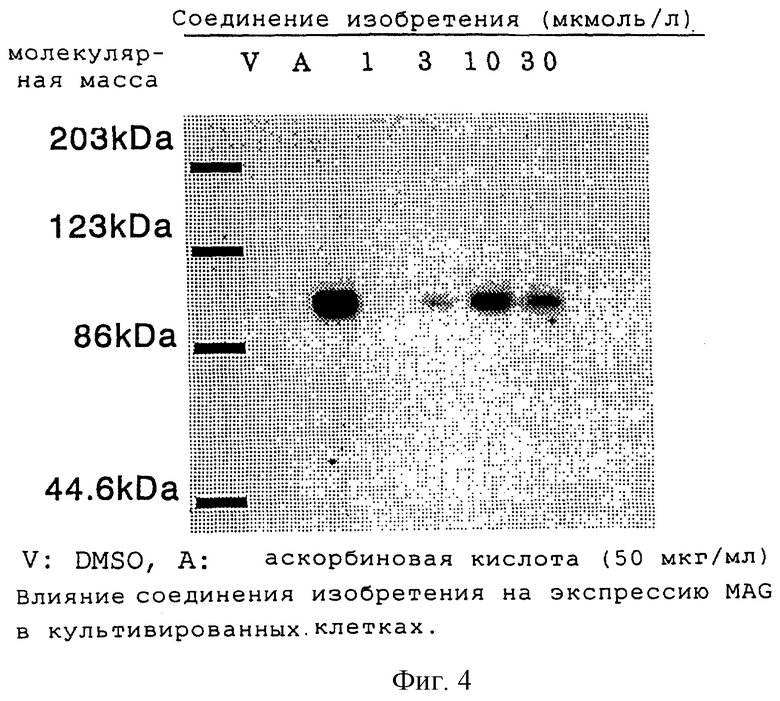
На фиг.4 показано изображение на рентгеновской пленке, полученное в экспериментальном примере 2, и экспрессия MAG в клетках, культивированных с соединением настоящего изобретения, негативным контрольным соединением или позитивным контрольным соединением.
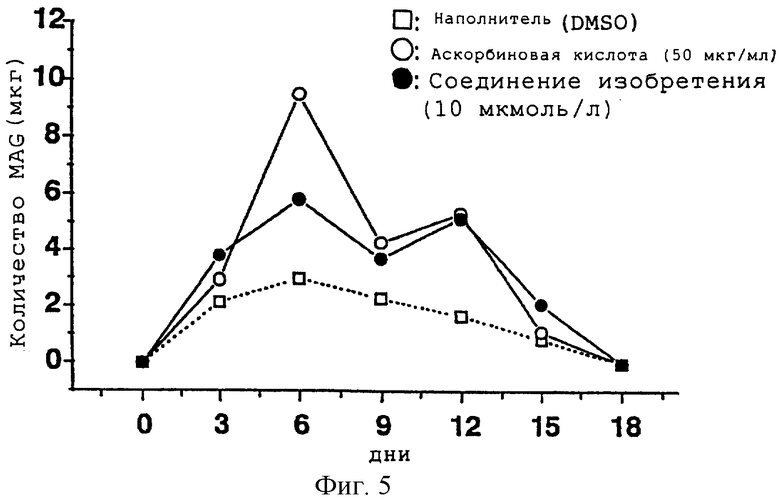
На фиг.5 показаны результаты экспериментального примера 3 и изменения в зависимости от времени экспрессии MAG в клетках, культивированных с соединением настоящего изобретения, негативным контрольным соединением или позитивным контрольным соединением.
Осуществление изобретения
Стимулятор экспрессии MAG настоящего изобретения включает любой стимулятор, пока он может стимулировать in vitro или in vivo экспрессию MAG при определенном уровне гена или уровне белка.
Заболевание, вызванное гипомиелинизацией, представляет собой заболевание млекопитающих, в том числе человека, включающее любое заболевание, в основном представляющее болезненное состояние гипомиелинизации, дисмиелинизации или демиелинизации.
Кроме того, заболевание, в основном представляющее дисмиелинизацию или демиелинизацию, означает заболевания млекопитающих, в том числе человека, и включает любое заболевание, в основном представляющее болезненное состояние гипомиелинизации, дисмиелинизации или демиелинизации. Примеры его включают рассеянный склероз, энцефалит, миелит, синдром Гийена-Барре, хронический воспалительный демиелинирующий полирадикулит, токсикоз, вызванный тяжелыми металлами, дифтерийный токсикоз, гипотиреоз, метахроматическая лейкодегенерация, болезнь Шарко-Мари-Тута и тому подобное.
В настоящем описании определение каждого символа в формуле (I) следующее.
Атом галогена у R1 может быть атомом хлора, атомом брома, атомом фтора и атомом иода, предпочтительно атомом хлора.
Алкильная группа у R1, R2, R3, R4, R5, R6, R7 и R8 представляет собой алкильную группу с неразветвленной или разветвленной цепью, имеющую от 1 до 10 атомов углерода, такую как метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил, гексил, гептил, октил, нонил, децил и тому подобное, предпочтительно алкильную группу, имеющую от 1 до 4 атомов углерода.
Алкоксигруппа у R1 представляет алкоксигруппу с неразветвленной или разветвленной цепью, имеющую от 1 до 6 атомов углерода, такую как метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, втор-бутокси, трет-бутокси, пентилокси, гексилокси и тому подобное.
Соединение настоящего изобретения можно синтезировать способом, описанным в патентах Японии JP-A-60-34952, JP-B-64-7074, JP-B-3-16348, JP-B-4-15781, JP-B-4-15782, JP-B-5-29031, JP-B-5-41143 и JP-B-5-74589.
Оптически активную форму соединения настоящего изобретения можно получить общепринятым способом, таким как рацемическое расщепление и тому подобное.
Фармацевтически приемлемая соль соединения настоящего изобретения в качестве примера представляется кислотно-аддитивными солями с неорганической кислотой, такой как хлористовородная кислота, бромистоводородная кислота, серная кислота и тому подобное, или органическими кислотами, такими как фумаровая кислота, малеиновая кислота, миндальная кислота, лимонная кислота, винная кислота, салициловая кислота и тому подобное, солями с металлом, таким как натрий, калий, кальций, магний, алюминий и тому подобное, и солями с аминокислотами, такими как лизин и тому подобное. Кроме того, включаются также их 1/2 гидрата, 1/3 гидрата, 2/3 гидрата, моногидрат, 3/2 гидрата, дигидрат и тому подобное. Соли этих соединений можно получить общепринятым способом.
Соединение настоящего изобретения можно использовать в качестве активного ингредиента стимулятора экспрессии MAG для стимуляции экспрессии MAG у млекопитающих, таких как человек, корова, лошадь, собака, мышь, крыса и тому подобное. Кроме того, соединение настоящего изобретения можно использовать в качестве агента для профилактики и/или лечения заболеваний, в основном представляющих гипомиелинизацию, кроме того, дисмиелинизацию или демиелинизацию, особенно, в качестве агента для профилактики и/или лечения рассеянного склероза, энцефалита, миелита, синдрома Гийена-Барре, хронического воспалительного демиелинирующего полирадикулита, токсикоза, вызванного тяжелыми металлами, дифтерийного токсикоза, гипотиреоза, метахроматической лейкодегенерации и болезни Шарко-Мари-Тута.
Из соединений настоящего изобретения предпочтительными являются следующие соединения.
(1) 2-(1-имидазолил)-α-(2,4,6-триметилфенил)бензолметанол;
(2) 2-(1-имидазолил)-2′,4′,6′-триметилбензофенон;
(3) 4-(1-имидазолил)-α-(2,4,6-триметилфенил)бензолметанол;
(4) 3-хлор-4-(1-имидазолил)-α-(2,4,6-триметилфенил)-бензолметанол;
(5) 3-(1-имидазолил)-α-(2,4,6-триметилфенил)бензолметанол;
(6) 2-хлор-5-(1-имидазолил)-α-(2,4,6-триметилфенил)-бензолметанол;
(7) 5-(1-имидазолил)-2-метил-α-(2,4,6-триметилфенил)-бензолметанол и его моногидрохлорид;
(8) 5-(1-имидазолил)-2-метокси-α-(2,4,6-триметилфенил) бензолетанол;
(9) 5-(1-имидазолил)-2-метил-α-(4-гидроксиметил-2,6-диметилфенил)бензолметанол;
(10) 2-хлор-5-(1-имидазолил)-α-(4-гидроксиметил-2,6-диметилфенил)бензолметанол;
(11) 5-(1-имидазолил)-2-метил-α-(4-метоксиметил-2,6-диметилфенил)бензолметанол;
(12) 4-[α-гидрокси-5-(1-имидазолил)-2-метилбензил]-3,5-диметилбензойная кислота и 1/2 гидрат ее натриевой соли;
(13) метил-4-[α-гидрокси-5-(1-имидазолил)-2-метилбензил]-3,5-диметилбензоат;
(14) 5-(1-имидазолил-2,2′,6′-триметил-4′-(1-имидазолилметил)бензофенон;
(15) этил-4-[α-гидрокси-5-(1-имидазолил)-2-метилбензил]-3,5-диметилбензоат;
(16) N-метил-4-[α-гидрокси-5-(1-имидазолил)-2-метилбензил]-3,5-диметилбензамид;
(17) 4-[α-гидрокси-2-хлор-5-(1-имидазолил)бензил]-3,5-диметилбензойная кислота;
(18) 4-[α-гидрокси-5-(1-имидазолил)-2-метоксибензил]-3,5-диметилбензойная кислота;
(19) (S)-4-[α-гидрокси-5-(1-имидазолил)-2-метилбензил]-3,5-диметилбензойная кислота (далее иногда обозначаемая Y-128);
(20) 4-[5-(1-имидазолил)-2-метилбензил]-3,5-диметилбензойная кислота;
(21) метил-(S)-4-[α-гидрокси-5-(1-имидазолил)-2-метилбензил]-3,5-диметилбензоат;
(22) α-[2-(1-имидазолил)пиридин-5-ил]-2,4,6-триметилбензолметанол.
Стимулятор экспрессии MAG настоящего изобретения изготовляют в виде фармацевтической композиции или фармацевтического препарата и вводят перорального или парентерально. Например, соединение настоящего изобретения и фармацевтически приемлемый носитель (например, эксципиент, связующее, дезинтегратор, корригент, отдушку, эмульгатор, разбавитель, солюбилизатор и т.д.) смешивают с получением фармацевтической композиции или фармацевтического препарата в подходящей форме для перорального или парентерального введения. Фармацевтический препарат включает твердый препарат, полутвердый препарат и жидкий препарат, их примерами являются таблетка, пилюля, порошок, гранула, капсула, пастилка, сироп, раствор, эмульсия, суспензия, инъекция (жидкость, суспензия и т.д.), суппозиторий, форма для ингаляции, подкожно поглощаемое лекарственное средство, глазные капли, глазную мазь и тому подобное.
Когда получают твердый препарат, используют добавки. Примеры добавки включают сахарозу, лактозу, целлюлозу, D-маннит, мальтит, декстран, крахмал, агар, альгинат, хитин, хитозан, пектин, трагакантовую камедь, аравийскую камедь, желатин, коллаген, казеин, альбумин, фосфат кальция, сорбит, глицин, карбоксиметилцеллюлозу, поливинилпирролидон, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, глицерин, полиэтиленгликоль, гидрокарбонат натрия, стеарат магния, тальк и тому подобное. Таблетки можно получить в виде таблеток, на которые нанесено обычное покрытие, когда необходимо, получают таблетки, покрытые сахаром, таблетки с энтеросолюбильным покрытием и таблетки, покрытые пленкой. Кроме того, можно получить двухслойные и многослойные таблетки.
Когда получают полутвердый препарат, можно использовать растительные и животные жиры и масла (оливковое масло, кукурузное масло, касторовое масло и т.д.), минеральные жиры и масла (вазелин, белый вазелин, твердый парафин и т.д.), воски (масло жожоба, карнаубский воск, пчелиный воск и т.д.), частично синтезированный или полностью синтезированный эфир глицерина и жирной кислоты (глицерид лауриновой кислоты, миристиновой кислоты или пальмитиновой кислоты и т.д.) и тому подобное. Примерами коммерчески доступных вышеуказанных продуктов являются витепсол (изготовлен Dynamitnovel Ltd.), фармазол (NOF Corporation) и тому подобное.
Когда получают жидкий препарат, используют добавки. Например, хлорид натрия, сорбит, глицерин, оливковое масло, пропиленгликоль, этиловый спирт и тому подобное. В частности, когда получают инъекцию, используют стерильный водный раствор (например, физиологический раствор), изотонический раствор или маслянистый раствор (например, кунжутное масло, соевое масло). Когда необходимо, можно совместно использовать подходящий суспендирующий агент (например, натрийкарбоксиметилцеллюлозу), неионогенное поверхностно-активное вещество, солюбилизатор (например, бензилбензоат, бензиловый спирт) и тому подобное. Когда получают глазные капли, используют водную жидкость или водный раствор. В частности, для инъекции используют стерильный водный раствор. Глазные капли могут содержать, если необходимо, различные добавки, такие как буфер, агент изотоничности, солюбилизатор, консервант, агент вязкости, хелатирующий агент, агент, регулирующий рН, и корригент. В качестве буфера для снижения раздражения предпочтительны боратный буфер, ацетатный буфер, карбонатный буфер и тому подобное. Значение рН предпочтительно регулируют обычно приблизительно до 6-8,5.
Содержание соединения настоящего изобретения в фармацевтической композиции или фармацевтическом препарате составляет 0,1-100 мас.% от массы фармацевтической композиции или фармацевтического препарата, в подходящем случае 1-50 мас.%. Хотя доза варьирует в зависимости от симптома, массы тела, возраста и подобных характеристик пациентов, она обычно составляет приблизительно 0,01-100 мг/кг при пероральном введении взрослому пациенту в день и ее предпочтительно вводят один или несколько раз в день. Для введения используют пероральный, ректальный и парентеральный (например, внутримышечный, внутривенный, чрескожный и подкожный) пути в ведения.
Примеры
Настоящее изобретение описано в деталях в следующих примерах, называемых примерами готовых препаративных форм и экспериментальными примерами. Они никоим образом не ограничивают настоящее изобретение.
Пример 1. Готовая препаративная форма: покрытая пленкой таблетка, мг:
Y-128 50,0
D-маннит 70,5
Кукурузный крахмал 16,0
Гидрокарбонат натрия 15,0
Гидроксипропилметилцеллюлоза 3,0
Тальк 5,0
Стеарат магния 0,5
Y-128, D-маннит, кукурузный крахмал и гидрокарбонат натрия смешивают и смесь применяют для грануляции в псевдоожиженном слое при разбрызгивании водного раствора гидроксипропилметилцеллюлозы. Гранулят пропускают через сито 24 меш и добавляют тальк и стеарат магния. С использованием роторного таблеточного пресса (Kikusui Seisakusho Ltd.) получают таблетки, каждая весом 160 мг. Затем, с использованием гидроксипропилметилцеллюлозы в качестве основы для пленочного покрытия наносят 6 мг покрытия на таблетку для получения покрытых пленкой таблеток.
Пример 2. Готовая препаративная форма: мелкие гранулы, %:
Y-128 10
D-маннит 89,5
Гидроксипропилцеллюлоза 0,5
Y-128 и D-маннит смешивают и добавляют водный раствор гидроксипропилцеллюлозы. Смесь разминают, гранулируют и сушат при 50°С. Гранулят пропускают через сито 32 меш для получения мелких гранул.
Пример 3. Готовая препаративная форма: таблетка, мг:
Y-128 50,0
D-маннит 30,0
Кукурузный крахмал 19,0
Гидрокарбонат натрия 15,0
Гидроксипропилметилцеллюлоза 1,5
Тальк 4,0
Стеарат магния 0,5
Y-128, D-маннит, кукурузный крахмал и гидрокарбонат натрия смешивают, и смесь применяют для флуидизированной грануляции в псевдоожиженном слое при разбрызгивании водного раствора гидроксипропилметилцеллюлозы. Гранулят пропускают через сито 24 меш и добавляют тальк и стеарат магния. С использованием роторного таблеточного пресса (Kikusui Seisakusho Ltd.) получают таблетки, каждая весом 120 мг.
Пример 4. Готовая препаративная форма: мелкие гранулы, %:
Y-128 5
D-маннит 92
Гидроксипропилметилцеллюлоза 3
Y-128 и D-маннит смешивают и добавляют водный раствор гидроксипропилметилцеллюлозы. Смесь разминают, гранулируют и сушат при 50°С. Гранулят пропускают через сито 32 меш для получения мелких гранул.
Фармакологическое действие промотора экспрессии MAG настоящего изобретения объясняется в следующих примерах, называемых экспериментальными примерами.
Экспериментальный пример 1
Получение нервных клеток по методу Seung U. Kim (экспериментальные протоколы для мозга и нервов - из культивированных клеток для функционального анализа, ed. Katsuhiko Mikoshiba, Takao Shimuzu, Yodosha). To есть у самки-крысы с 18-дневной беременностью (Crj: CD(SD)IGS) вынимали эмбрион, у которого под стереоскопическим микроскопом удаляли дорсальные ганглии спинномозговых нервных корешков (далее называемые DRG). DRG обрабатывали 0,25% трипсином и ДНКазой I при 37°С для диспергирования клеток. Прилипшие клетки, другие, не нервные клетки, удаляли и клетки (5000 клеток) высевали на покрытом полилизином планшете. Клетки культивировали в DMEM (модифицированная по способу Дульбекко среда Игла), содержащей 10% ФТС (фетальная телячья сыворотка), дополненной фактором роста нервов (далее обозначаемый NGF, 50 нг/мл), в инкубаторе с атмосферой СО2. После 3 дней культивирования среду заменяли на среду, содержащую Ara-C (1 мкмоль/л), для удаления пролиферативных клеток, других не нервных клеток.
Получение шванновских клеток по методу Ichiro Matsuoka (Springer Neuroscience Lab Manual 1, ed. Hiroshi Hatanaka, Springer-Verlag Tokyo). To есть седалищный нерв новорожденной крысы (от 1 до 3 дней после рождения), (Crj: CD(SD)IGS) удаляли под стереоскопическим микроскопом и удаляли адвентициальную оболочку. Клетки были диспергированы обработкой системой трипсин/коллагеназа и ДНКазой I в CMF-HBSS. С использованием колбы для культуры клетки культивировали в DMEM, содержащей 10% ФТС, в инкубаторе с атмосферой СО2. После культивирования в среде, содержащей Ara-C, клетки выделяли и суспензию клеток обрабатывали последовательно анти-Тhy 1.1 и кроличьим комплементом для удаления клеток, других, не шванновских клеток. С использованием покрытой коллагеном колбы для культуры клетки культивировали в DMEM, содержащей 10% ФТС, в инкубаторе с атмосферой CO2.
Спустя 1 неделю после начала культивирования нервных клеток DRG шванновские клетки (20000 клеток) культивировали на планшете, на котором были культивированы нервные клетки DRG. Средой для совместного культивирования была DMEM, содержащая 2 мкмоль/л форсколина, 50 нг/мл NGF и 10% ФТС. На следующий день после присоединения шванновских клеток каждые 2 или 3 дня добавляли соединение настоящего изобретения (вышеуказанное Y-128, 3 мкмоль/л), растворенное в диметилсульфоксиде (ДМСО), или в качестве позитивного контрольного соединения аскорбиновую кислоту (50 мкг/мл). В качестве негативного контрольного соединения таким же способом обрабатывали наполнителем ДМСО.
Спустя 2 недели после начала совместного культивирования миелин окрашивали по методу Eldridge С F et al. (J. Cell Biol., 105, р.1023-1034 (1987)). То есть клетки фиксировали 10% нейтральным забуференным раствором формалина и сохраняли при 4°С в течение ночи. После удаления раствора формалина клетки фиксировали снова 0,1% раствором тетраоксида осмия в течение 1 час и окрашивали красителем суданом черным B в течение 30 мин. Окрашенный образец (12 лунок для каждой группы) наблюдали под микроскопом и выбирали часть, где аксон в каждой лунке был очень заметно окрашен, и эту часть фотографировали камерой поляроид.
Фиг.1 - фиг.3 показывают окрашенный аксон в каждой группе. В группе добавления среды аксон не был окрашен ни в какой лунке (см. фиг.1). В группе добавления аскорбиновой кислоты аксон был интенсивно окрашен в каждой лунке (см. фиг.2). В группе добавления соединения настоящего изобретения (Y-128) (3 мкмоль/л) аксон был окрашен так же интенсивно, как в группе добавления аскорбиновой кислоты, в 5 лунках из 12 лунок (см. фиг.3). Из вышеуказанного экспериментального примера стало ясно, что соединение настоящего изобретения (Y-128) стимулировало миелинизацию аксона.
Экспериментальный пример 2
По методу, описанному в экспериментальном примере 1, совместно культивировали нервные клетки и шванновские клетки. Раствор ДМСО, содержащий соединение настоящего изобретения (Y-128, 1, 3, 10 или 30 мкмоль/л) или аскорбиновую кислоту (50 мкг/мл), в качестве позитивного контрольного соединения добавляли к среде каждые 2 дня в течение 2 недель. Таким же способом добавляли в качестве негативного контрольного соединения наполнитель ДМСО. Спустя 2 недели после начала добавления соединения среду удаляли и буфер для образца, содержащий додецилсульфат натрия (ДСН), добавляли в лунку для солюбилизации клеток.
Часть их разделяли электрофорезом с гелем полиакриламида и мигрированный белок переносили к мембране PVDF (поливинилиденфторид). Целевой белок детектировали иммуноблоттингом и хемилюминесценцией на рентгеновской пленке. Полосу, детектированную у миграции приблизительно 100 кДа, идентифицировали как сигнал относящегося к миелину гликопротеина (MAG). Рентгеновскую пленку сканировали и изображение переносили в компьютер и экспрессию MAG полуколичественно определяют с использованием программного обеспечения для анализа, ImageQuaNT (Molecular Dynamics). Фиг.4 показывает экспрессию MAG на рентгеновской пленке. Из вышеуказанного экспериментального примера было ясно, что соединение настоящего изобретения (Y-128) повышало экспрессию MAG в концентрации от 3 мкмоль/л.
Экспериментальный пример 3
По методу, описанному в экспериментальном примере 1, нервные клетки DRG и шванновские клетки культивировали совместно. Раствор ДМСО, содержащий соединение настоящего изобретения (Y-128, 10 мкмоль/мл) или аскорбиновую кислоту (50 мкг/мл), в качестве позитивного контрольного соединения добавляли в среду каждые 2 дня. Среду ДМСО добавляли таким же способом в качестве негативного контрольного соединения. Таким же способом, как в экспериментальном примере 2, MAG количественно определяли до добавления соединений на 3, 6, 9, 12, 15 и 18 дни после добавления. Результаты показаны на фиг.5.
Из вышеуказанного экспериментального примера стало ясно, что соединение настоящего изобретения (Y-128) повышало экспрессию MAG максимально спустя 6 и 12 дней после добавления и через 18 дней экспрессия MAG исчезала. Изменения экспрессии MAG в зависимости от времени соединением настоящего изобретения (Y-128) были такие же, как изменения, вызванные позитивным контрольным соединением, аскорбиновой кислотой.
Экспериментальный пример 4: Экспериментальный аллергический энцефаломиелит (ЕАЕ (экспериментальный аутоиммунный энцефаломиелит))
Миелиновый основной белок морской свинки получают экстракцией гомогената спинного мозга кислотой и осаждением сульфатом аммония. Миелиновый основной белок и такое же количество полного адъюванта Фреинда (содержащий 4 мг/мл микобактерии H37Ra) смешивают и эмульгируют. Полученную эмульсию (0,1 мл) вводят инъекцией один раз в подошву задней конечности самки крысы Lewis возраста от 8 до 12 недель. Y-128 (10 мг/кг) вводят перорально один раз в день в течение 4 недель сразу после индукции ЕАЕ. После последнего введения оценивают симптом крысы, как указано ниже, на основании которого оценивают действие.
0: без симптома, 1: хвост мягко свисает, 2: паралич задней конечности, 3: паралич всех конечностей, 4: на грани смерти, 5: смерть.
Экспериментальный пример 5: аллергический неврит (EAN (экспериментальный аутоиммунный неврит))
Белковый пептид (100 мкг, соответствующий аминокислотной последовательности 53-78 бычьего белка Р2) и такое же количество полного адъюванта Фреинда (содержащего 0,5 мг/мл микобактерий туберкулеза) смешивают и эмульгируют. Полученную эмульсию (0,1 мл) вводят инъекцией один раз в подошву задней конечности самки крысы Lewis возраста от 6 до 8 недель. Y-128 (10 мг/кг) вводят перорально один раз в день в течение 4 недель сразу после индукции ЕАЕ. После последнего введения оценивают симптом крысы, как указано ниже, на основании которого оценивают действие соединения. 0: без симптома, 1: хвост с ослабленным усилием, 2: хвост мягко свисает, 3: нарушение в удерживании равновесия, 4: исчезновение удерживания равновесия, 5: атактическая походка, 6: слабый паралич задней конечности, 7: серьезный паралич всех конечностей, 8: на грани смерти, 9: смерть.
Промышленная применимость
Стимулятор экспрессии MAG настоящего изобретения можно использовать в качестве агента для профилактики и/или лечения заболеваний, в основном представляющих гипомиелинизацию и, кроме того, дисмиелинизацию или демиелинизацию. Более конкретно, его можно использовать в качестве агента для профилактики и/или лечения заболеваний млекопитающих, включая людей, таких как рассеянный склероз, энцефалит, миелит, синдром Гийена-Барре, хронический воспалительный демиелинирующий полирадикулит, токсикоз, вызванный тяжелыми металлами, дифтерийный токсикоз, гипотиреоз, метахроматическая лейкодегенерация, болезнь Шарко-Мари-Тута и тому подобное.
Послесловие
Данная заявка основана на заявке на патент №144336/1999, поданной в Японии, содержание которой, таким образом, включается в качестве ссылки. Настоящее изобретение не должно ограничиваться конкретными воплощениями, описанными в данном описании. На основании описания настоящего изобретения среднему специалисту в данной области должны быть ясны варианты и модификации настоящего изобретения. Имеется в виду, что такие варианты и модификации находятся в пределах объема настоящего изобретения. Любые цитированные описания различных публикаций включаются во всей их полноте в настоящее изобретение в качестве ссылки на них.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРОИЗВОДНЫЕ АЗАБИФЕНИЛАМИНОБЕНЗОЙНОЙ КИСЛОТЫ В КАЧЕСТВЕ ИНГИБИТОРОВ DHODH | 2008 |
|
RU2481334C2 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО И СПОСОБ ЛЕЧЕНИЯ ПОВЫШЕННОГО ГЛАЗНОГО ДАВЛЕНИЯ И/ИЛИ ГЛАУКОМЫ | 1995 |
|
RU2123847C1 |
| ПРОИЗВОДНЫЕ АМИНОСПИРТОВ ИЛИ ПРОИЗВОДНЫЕ ФОСФОРНЫХ КИСЛОТ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ УКАЗАННЫЕ ПРОИЗВОДНЫЕ | 2003 |
|
RU2330839C2 |
| НОВЫЕ ПРОИЗВОДНЫЕ ИНДОЛА, ОБЛАДАЮЩИЕ ИНГИБИРУЮЩЕЙ АКТИВНОСТЬЮ В ОТНОШЕНИИ IκB КИНАЗЫ β | 2008 |
|
RU2470918C2 |
| ТРЕХЪЯДЕРНЫЕ КОНДЕНСИРОВАННЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2000 |
|
RU2211837C2 |
| ХИРАЛЬНЫЕ ДИАЦИЛГИДРАЗИНОВЫЕ ЛИГАНДЫ ДЛЯ МОДУЛЯЦИИ ЭКСПРЕССИИ ЭКЗОГЕННЫХ ГЕНОВ С ПОМОЩЬЮ ЭКДИЗОН-РЕЦЕПТОРНОГО КОМПЛЕКСА | 2008 |
|
RU2490253C2 |
| СУЛЬФОНАМИДНЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ | 2009 |
|
RU2502730C2 |
| ПРОИЗВОДНЫЕ ЦИКЛИЧЕСКИХ АМИНОВ, СПОСОБ ИНГИБИРОВАНИЯ | 1998 |
|
RU2216540C2 |
| ПРОИЗВОДНЫЕ АМИНОХИНОЛИНА И АМИНОПИРИДИНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛИГАНДОВ АДЕНОЗИНА A | 2002 |
|
RU2278112C2 |
| ПРОИЗВОДНЫЕ 1,3-ДИОКСОЛ/4,5-h//2,3/БЕНЗОДИАЗЕПИНА, ЯВЛЯЮЩИЕСЯ ИНГИБИТОРАМИ AMPA/КАИНАТНОГО РЕЦЕПТОРА, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ, СПОСОБ ЛЕЧЕНИЯ | 1998 |
|
RU2208014C2 |

Изобретение относится к области медицины и касается стимулятора экспрессии MAG (миелин-ассоциированного гликопротеина), содержащего соединение формулы (I):
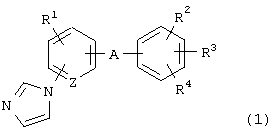
Соединение пригодно для лечения заболеваний, представляющих гипомиелинизацию, дисмиелинизацию или демиелинизацию. 9 c. и 21 з.п. ф-лы, 5 ил.

где R1 представляет атом водорода, атом галогена, алкильную группу или алкоксигруппу;
R2 и R3 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу;
R4 представляет алкильную группу, -СООН, -COOR5, -CONR6R7, -CH2NR6R7, -CH2OH или -CH2OR8, где R5 и R8 представляют каждый алкильную группу и R6 и R7 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу или R6 и R7 в комбинации образуют имидазол вместе с соседним атомом азота;
А представляет -СН(ОН)-, -С(=O)- или -CH2-;
Z представляет =СН- или =N-,
его оптически активную форму или его фармацевтически приемлемую соль.
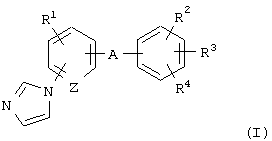
где R1 представляет атом водорода, атом галогена, алкильную группу или алкоксигруппу;
R2 и R3 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу;
R4 представляет алкильную группу, -СООН, -COOR5, -CONR6R7, -CH2NR6R7, -CH2OH или -CH2OR8, где R5 и R8 представляют, каждый, алкильную группу и R6 и R7 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу или R6 и R7 в комбинации образуют имидазол вместе с соседним атомом азота;
А представляет -СН(ОН)-, -С(=О)- или -СН2-;
Z представляет =СН- или =N-,
его оптически активной формы или его фармацевтически приемлемой соли млекопитающим, включая человека.
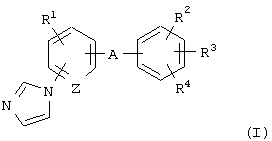
где R1 представляет атом водорода, атом галогена, алкильную группу или алкоксигруппу;
R2 и R3 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу;
R4 представляет алкильную группу, -СООН, -COOR5, -CONR6R7, -CH2NR6R7, -СН2ОН или -CH2OR8, где R5 и R8 представляют, каждый, алкильную группу и R6 и R7 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу или R6 и R7 в комбинации образуют имидазол вместе с соседним атомом азота;
А представляет -СН(ОН)-, -С(=O)- или -CH2-;
Z представляет =СН- или =N-,
его оптически активную форму или его фармацевтически приемлемую соль млекопитающим, включая человека.
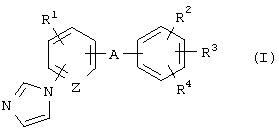
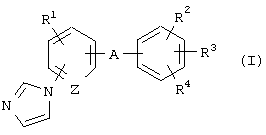
где R1 представляет атом водорода, атом галогена, алкильную группу или алкоксигруппу;
R2 и R3 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу;
R4 представляет алкильную группу, -СООН, -COOR5, -CONR6R7, -CH2NR6R7, -CH2OH или -CH2OR8, где R5 и R8 представляют, каждый, алкильную группу и R6 и R7 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу или R6 и R7 в сочетании образуют имидазол вместе с соседним атомом азота;
А представляет -СН(ОН)-, -С(=O)- или -СН2-;
Z представляет =СН- или =N-,
его оптически активной формы или его фармацевтически приемлемой соли млекопитающим, включая человека.
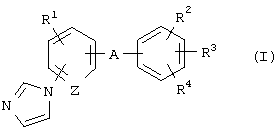
где R1 представляет атом водорода, атом галогена, алкильную группу или алкоксигруппу;
R2 и R3 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу;
R4 представляет алкильную группу, -СООН, -COOR5, -CONR6R7, -CH2NR6R7, -CH2OH или -CH2OR8, где R5 и R8 представляют каждый алкильную группу и R6 и R7 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу или R6 и R7 в сочетании образуют имидазол вместе с соседним атомом азота;
А представляет -СН(ОН)-, -С(=О)- или -СН2-;
Z представляет =СН- или =N-,
его оптически активной формы или его фармацевтически приемлемой соли млекопитающим, включая человека.
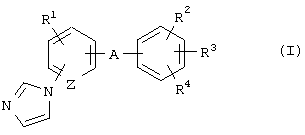
где R1 представляет атом водорода, атом галогена, алкильную группу или алкоксигруппу;
R2 и R3 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу;
R4 представляет алкильную группу, -СООН, -COOR5, -CONR6R7, -CH2NR6R7, -CH2OH или -CH2OR8, где R5 и R8 представляют, каждый, алкильную группу и R6 и R7 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу или R6 и R7 в сочетании образуют имидазол вместе с соседним атомом азота;
А представляет -СН(ОН)-, -С(=O)- или -CH2-;
Z представляет =СН- или =N-,
его оптически активной формы или его фармацевтически приемлемой соли для получения стимулятора экспрессии MAG.
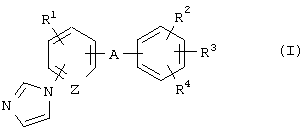
где R1 представляет атом водорода, атом галогена, алкильную группу или алкоксигруппу;
R2 и R3 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу;
R4 представляет алкильную группу, -СООН, -COOR5, -CONR6R7, -CH2NR6R7, -СН2ОН или -CH2OR8, где R5 и R8 представляют, каждый, алкильную группу и R6 и R7 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу или R6 и R7 в сочетании образуют имидазол вместе с соседним атомом азота;
А представляет -СН(ОН)-, -С(=O)- или -СН2-;
Z представляет =СН- или =N-,
его оптически активной формы или его фармацевтически приемлемой соли для получения стимулятора экспрессии MAG, пригодного для лечения заболевания, вызванного гипомиелинизацией, у млекопитающих, включая человека.
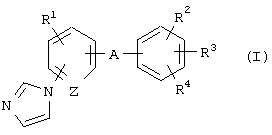
где R1 представляет атом водорода, атом галогена, алкильную группу или алкоксигруппу;
R2 и R3 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу;
R4 представляет алкильную группу, -СООН, -COOR5, -CONR6R7, -CH2NR6R7, -СН2ОН или -CH2OR8, где R5 и R8 представляют, каждый, алкильную группу и R6 и R7 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу или R6 и R7 в сочетании образуют имидазол вместе с соседним атомом азота;
А представляет -СН(ОН)-, -С(=O)- или -СН2-;
Z представляет =СН- или =N-,
его оптически активной формы или его фармацевтически приемлемой соли для получения стимулятора экспрессии MAG, пригодного для лечения заболевания, которое представляет дисмиелинизацию или демиелинизацию, у млекопитающих, включая человека.
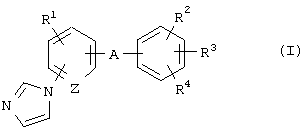
где R1 представляет атом водорода, атом галогена, алкильную группу или алкоксигруппу;
R2 и R3 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу;
R4 представляет алкильную группу, -СООН, -COOR5, -CONR6R7, -CH2NR6R7, -CH2OH или -CH2OR8, где R5 и R8 представляют, каждый, алкильную группу и R6 и R7 являются одинаковыми или разными и каждый представляет атом водорода или алкильную группу или R6 и R7 в сочетании образуют имидазол вместе с соседним атомом азота;
А представляет -СН(ОН)-, -С(=О)- или -СН2-;
Z представляет =СН- или =N-,
его оптически активной формы или его фармацевтически приемлемой соли для получения стимулятора экспрессии MAG, пригодного для лечения заболевания, включающего рассеянный склероз, энцефалит, миелит, синдром Гийена-Барре, хронический воспалительный демиелинизирующий полирадикулит, токсикоз, вызванный тяжелыми металлами, дифтерийный токсикоз, гипотиреоз, метахроматическую лейкодегенерацию или болезнь Шарко-Мари-Тута, у млекопитающих, включая человека.
| Устройство для забора и удаления илистых грунтов | 1979 |
|
SU881218A1 |
| RU 97111858 А, 20.06.1999. | |||
Авторы
Даты
2004-12-10—Публикация
2000-05-25—Подача