Изобретение относится к медицине, а именно, к препаратам, используемым в диагностике, и в частности к получению пула нормальной плазмы из донорской крови. Указанный материал находит применение в качестве контрольного материала при исследовании патологий гемостаза, таких как гемофилия А и В, болезнь Виллебранда и других, а также при мониторинге терапии антикоагулянтами различного типа.
Качество исследования патологий гемостаза значительно повышается в случае использования в процессе исследования контрольных референтных материалов. Таким контрольным материалом является пул нормальной плазмы, аттестованный по основным параметрам коагулограммы.
Пул нормальной плазмы получают из крови не менее чем 20 здоровых доноров в возрасте от 20 до 40 лет, не принимающих медикаменты и контрацептивы. Пул нормальной плазмы характеризуют значениями активированного парциального тромбопластинового времени (АПТВ), протромбинового времени, тромбинового времени и содержания фибриногена. Для использования пула нормальной плазмы в качестве референтного материала эти показатели не должны существенно меняться в процессе хранения пула.
Наиболее близким по совокупности существенных признаков к заявляемому изобретению является способ [патент РФ N 1592717, МКИ A 61 K 35/16, опубликованный 1990, БИ N 34] получения пула нормальной плазмы, включающий смешение донорской крови, взятой от отдельных доноров, с раствором-консервантом, отделение плазмы крови, объединение плазмы, полученной из крови отдельных доноров, сублимационную сушку плазменного пула. Раствор-консервант в известном способе содержит растворенные в 100 мл дистиллированной воды 3,8 г цитрата натрия, 1 мл 10%-ного раствора азида натрия, 0,05 мл контрикала и 8,925 г N-(2-гидроксиэтил)- пиперaзин-N'-2-этaнcульфoнoвoй кислоты (сокращенно HEPES). Сублимационную сушку под вакуумом производят при температуре от - 35-58oC до 5oC в течение 36-38 часов. Полученный плазменный пул охарактеризован по следующим параметрам: активность факторов протромбинового комплекса 91% (через 12-14 месяцев хранения 101%), фактора V 99% (94%), VII+X - 98% (102%), pH 7,36 (7,45) и содержание фибриногена 2 г/л (1,5 г/л).
Недостатком известного способа получения плазменного пула является очень высокое содержание N-(2-гидроксиэтил)-пиперазин-N'-2-этансульфоновой кислоты в растворе-консерванте: его расход на 1 мл полученной плазмы составляет 26,7 мг. Высокая цена указанного препарата и его большой расход делают известный способ получения плазменного пула нерентабельным, а сам пул плазмы слишком дорогим для использования в практическом здравоохранении.
Техническая задача, на решение которой направлено заявляемое изобретение, состоит в снижении расхода HEPES на 1 мл плазменного пула с сохранением показателей референтного материала в пределах нормы.
Указанная задача решается тем, что в способе получения пула нормальной донорской плазмы, включающем смешение донорской крови, взятой от отдельных доноров, с консервантом, содержащим цитрат натрия и азид натрия, отделение плазмы крови, объединение плазмы, полученной из крови отдельных доноров, и сублимационную сушку плазменного пула в присутствии N-(2-гидроксиэтил)- пиперазин-N'-2-этансульфоновой кислоты, используют консервант, дополнительно содержащий вещество, выбранное из группы, включающей глицин и аспарагиновую кислоту, или их смесь, а N-(2-гидроксиэтил)-пиперазин-N'-2-этансульфоновую кислоту вводят в объединенный плазменный пул перед сублимационной сушкой в количестве 3,5-4,5 мг на 1 мл плазмы.
При получении плазменного пула использовали вещества, выпускаемые промышленностью:
- цитрат натрия, ГОСТ 3161-57;
- глицин, ГОСТ 5860-68;
- аспарагиновая кислота, ТУ 5П-168-69;
- вода дистиллированная, ГОСТ 6909-71;
- азид натрия фирмы ISN, США, каталожный N 102891;
- HEPES фирмы Sigma, США, каталожный N H0891.
Донорская кровь отбиралась в соответствии с Инструкцией по медицинскому освидетельствованию доноров плазмы крови и костного мозга, утвержденной MЗ РФ 16.11.98.
Далее заявляемый способ иллюстрируется примерами.
Пример 1.
Готовят консервирующий раствор: 3 г глицина, 3,8 г цитрата натрия, 1 мл 10% раствора азида натрия растворяют в 100 мл дистиллированной воды. Раствор разливают по 2,5 мл в 20 пластиковых центрифужных пробирок. Донорскую кровь от 20 здоровых лиц в возрасте от 20 до 40 лет, не принимающих медикаменты и контрацептивы, берут по 25 мл в центрифужные пробирки с консервирующим раствором. Кровь центрифугируют при 3000 об/мин, 4oC в течение 20 минут. Отбирают плазму и повторно центрифугируют в том же режиме в течение 10 минут. Дважды отцентрифугированную плазму объединяют в один флакон емкостью 500 мл. К пулу плазмы добавляют HEPES из расчета 4 мг HEPES на каждый мл плазмы. Нативный пул разливают по 2 мл в силиконированные флаконы и замораживают при температуре -50oC. Затем кассеты с замороженной плазмой загружают в сублимационный аппарат, полку которого предварительно охлаждают до -40oC. Включают вакуум-насос и понижают давление в сублиматоре до 3•0,01 мм рт. ст. Через 5 часов после включения вакуум-насоса начинают подогрев полки. Повышение температуры полки производят постепенно для плавного увеличения температуры пула нормальной плазмы. Конечная температура в препарате 10oC. Общая продолжительность сушки 34 часа.
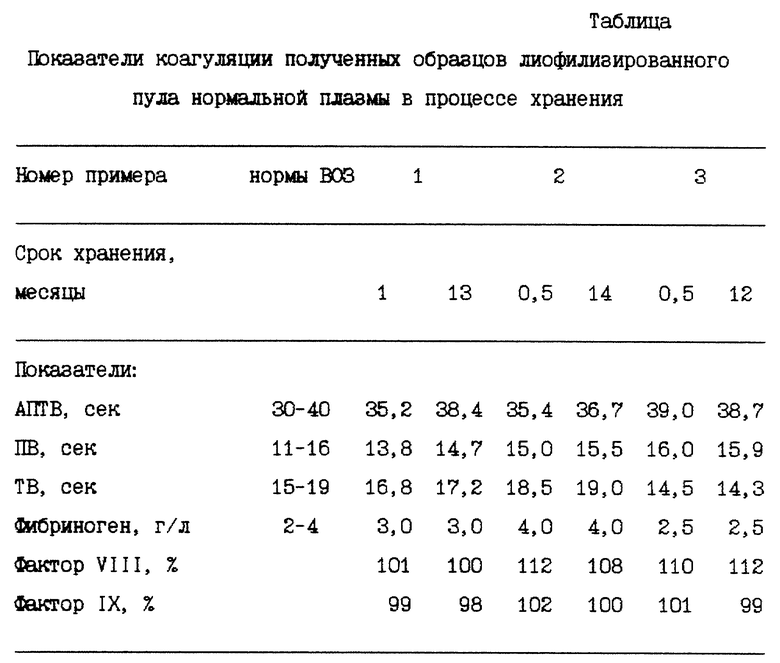
Через месяц после получения и через 13 месяцев были определены следующие показатели коагуляции: АПТВ, сек; протромбиновое время (ПВ), сек; тромбиновое время (ТВ), сек; содержание фибриногена, г/л; активность фактора VIII, %; активность фактора IX, %.
Показатели коагуляции определялись методами, изложенными в учебном пособии "Гемостаз", под редакцией Н.Н. Петрищева, Л.П. Папаян, Санкт-Петербург, 1999, а также в книге Балуда В.П., Баркаган З.С., Гольдберг Е.Д. и др. "Лабораторные методы исследования системы гемостаза", Томск, 1980.
Результаты определения представлены в таблице.
Пример 2.
Готовят консервирующий раствор: 4 г аспарагиновой кислоты, 3,2 г цитрата натрия, 1 мл 10% раствора азида натрия, 100 мл дистиллированной воды. Раствор разливают по 2,5 мл в 23 пластиковые центрифужные пробирки. Донорскую кровь от 23 здоровых лиц в возрасте от 20 до 40 лет, не принимающих медикаменты и контрацептивы, берут по 25 мл в центрифужные пробирки с консервирующим раствором. Кровь центрифугируют при 3000 об/мин, 6oC в течение 20 минут. Отбирают плазму и повторно центрифугируют в том же режиме в течение 10 минут. Дважды отцентрифугированную плазму объединяют в один флакон емкостью 500 мл. К пулу плазмы добавляют HEPES из расчета 3,5 мг HEPES на каждый мл плазмы. Нативный пул разливают по 2 мл в силиконированные флаконы и замораживают при температуре -60oC. Затем кассеты с замороженной плазмой загружают в сублимационный аппарат, полку которого предварительно охлаждают до -35oC. Включают вакуум-насос и понижают давление в сублиматоре до 4•0,01 мм рт. ст. Через 5 часов после включения вакуум-насоса начинают подогрев полки. Повышение температуры полки производят постепенно для плавного увеличения температуры пула нормальной плазмы. Конечная температура в препарате 10oC. Общая продолжительность сушки 35 часов.
Через 0,5 месяца и через 14 месяцев после получения пула плазмы были определены те же, что и в примере 1, показатели коагуляции. Результаты определения представлены в таблице.
Пример 3.
Готовят консервирующий раствор: 1,2 г глицина, 2,2 г аспарагиновой кислоты, 3,8 г цитрата натрия, 1 мл 10% раствора азида натрия, 100 мл дистиллированной воды. Раствор разливают по 2,5 мл в 21 пластиковую центрифужную пробирку. Донорскую кровь от 21 здорового лица в возрасте от 20 до 40 лет, не принимающего медикаменты и контрацептивы, берут по 25 мл в центрифужные пробирки с консервирующим раствором. Кровь центрифугируют при 3000 об/мин, 4oC в течение 20 минут. Отбирают плазму и повторно центрифугируют в том же режиме в течение 10 минут. Дважды отцентрифугированную плазму объединяют в один флакон емкостью 500 мл. К пулу плазмы добавляют HEPES из расчета 4,5 мг HEPES на каждый мл плазмы. Нативный пул разливают по 2 мл в силиконированные флаконы и замораживают при температуре -55oC. Затем кассеты с замороженной плазмой загружают в сублимационный аппарат, полку которого предварительно охлаждают до -40oC. Включают вакуум-насос и понижают давление в сублиматоре до 5•0,01 мм рт. ст. Через 5 часов после включения вакуум-насоса начинают подогрев полки. Повышение температуры полки производят постепенно для плавного увеличения температуры пула нормальной плазмы. Конечная температура в препарате 11oC. Общая продолжительность сушки 36 часов.
Показатели коагуляции полученного пула плазмы определяли через 0,5 и через 12 месяцев после получения. Результаты определения представлены в таблице.
Как видно из таблицы, полученный заявляемым способом пул нормальной плазмы стабилен при хранении в течение года; при этом не изменяется активность весьма лабильных факторов свертывания VIII и IX. Это позволяет использовать пул, полученный заявляемым способом, для исследования факторов свертывания. Значительное снижение содержания HEPES, использование других недорогих материалов - глицина и аспарагиновой кислоты снижает стоимость контрольного материала и делает его более доступным практическому здравоохранению.
| название | год | авторы | номер документа |
|---|---|---|---|
| КОНСЕРВАНТ ДЛЯ ОТМЫТЫХ ЭРИТРОЦИТОВ | 2002 |
|
RU2225692C2 |
| СПОСОБ ПОЛУЧЕНИЯ РЕАКТИВА ДЛЯ ОПРЕДЕЛЕНИЯ АКТИВИРОВАННОГО ПАРЦИАЛЬНОГО ТРОМБОПЛАСТИНОВОГО ВРЕМЕНИ | 1995 |
|
RU2104551C1 |
| СПОСОБ ПОЛУЧЕНИЯ КОНТРОЛЬНОЙ ПЛАЗМЫ С НОРМАЛЬНЫМ УРОВНЕМ ПРОТРОМБИНОВОГО КОМПЛЕКСА | 2004 |
|
RU2270020C2 |
| СПОСОБ ПОЛУЧЕНИЯ КОНСЕРВАНТА ДЛЯ ЭРИТРОЦИТОВ | 1995 |
|
RU2098959C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИАГНОСТИКУМА ДЛЯ КОНТРОЛЯ АНТИКОАГУЛЯНТНОЙ ТЕРАПИИ | 1991 |
|
RU2013778C1 |
| СПОСОБ ПОЛУЧЕНИЯ ИММУНОГЛОБУЛИНА ДЛЯ ВНУТРИВЕННОГО ВВЕДЕНИЯ | 1992 |
|
RU2068695C1 |
| КРОВЕЗАМЕНИТЕЛЬ - ПЕРЕНОСЧИК КИСЛОРОДА, СОСТАВ ДЛЯ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ПОЛУЧЕНИЯ ПОЛИМЕРНОГО МОДИФИЦИРОВАННОГО ГЕМОГЛОБИНА | 1999 |
|
RU2162707C2 |
| СПОСОБ ПОЛУЧЕНИЯ РЕАКТИВА ДЛЯ ОПРЕДЕЛЕНИЯ АКТИВИРОВАННОГО ПАРЦИАЛЬНОГО ТРОМБОПЛАСТИНОВОГО ВРЕМЕНИ | 1990 |
|
RU1767743C |
| ПОЛИФУНКЦИОНАЛЬНЫЙ КРОВЕЗАМЕНИТЕЛЬ ДЛЯ ЛЕЧЕНИЯ КРОВОПОТЕРИ И ШОКА | 1998 |
|
RU2136291C1 |
| Добавочный раствор для хранения концентрата тромбоцитов | 2019 |
|
RU2720487C1 |
Изобретение относится к медицине, а именно к препаратам, используемым в диагностике патологий гемостаза. Способ включает смешение донорской крови с консервантом, содержащим цитрат натрия и азид натрия, отделение плазмы, объединение плазмы, полученной из крови отдельных доноров, и сублимационную сушку плазменного пула в присутствии N-(2-гидроксиэтил)-пиперазин-N'-2- этансульфоновой кислоты. Консервант дополнительно содержит глицерин и аспарагиновую кислоту, или их смесь. N-(2-гидроксиэтил)-пиперазин-N'-2-этансульфоновую кислоту вводят в плазменный пул перед сублимационной сушкой в количестве 3,5-4,5 мг на 1 мл плазмы. Технический результат: снижение расхода N-(2-гидроксиэтил)-пиперазин-N'-2-этансульфоновой кислоты на 1 мл плазменного пула. 1 табл.
Способ получения пула нормальной плазмы путем смешения донорской крови, взятой от отдельных доноров с консервантом, содержащим цитрат натрия и азид натрия, отделение плазмы крови, объединение плазмы, полученной из крови отдельных доноров, и сублимационную сушку плазменного пула в присутствии N-(2-гидроксиэтил)-пиперазин-N'-2-этансульфоновой кислоты, отличающийся тем, что используют консервант, дополнительно содержащий вещество, выбранное из группы, включающей глицин и аспаргиновую кислоту, или их смесь, а N-(2-гидроксиэтил)-пиперазин-N'-2-этансульфоновую кислоту вводят в объединенный пул перед сублимационной сушкой в количестве 3,5-4,5 мг на 1 мл плазмы.
| SU 1592717 А, 15.09.1990 | |||
| СОСТАВ ДЛЯ СТАБИЛИЗАЦИИ ПЛАЗМЫ КРОВИ, СПОСОБ ПАСТЕРИЗАЦИИ ПЛАЗМЫ И ИСПОЛЬЗОВАНИЕ СТАБИЛИЗИРОВАННОЙ ПЛАЗМЫ В ТЕРАПИИ | 1998 |
|
RU2112522C1 |
| US 5030554 А, 09.07.1991 | |||
| УСТРОЙСТВО ДЛЯ КРЕПЛЕНИЯ ПЛЕНОЧНОГО ОГРАЖДЕНИЯ | 2013 |
|
RU2526660C1 |
| Торфодобывающая машина с вращающимся измельчающим орудием | 1922 |
|
SU87A1 |
Авторы
Даты
2001-10-20—Публикация
2000-06-06—Подача