Данное изобретение относится к технологии производства эпоксидов, более конкретно к катализатору для эпоксидирования олефинов и способу получения эпоксидов.
Эпоксидирование олефинов водной перекисью водорода происходит только в присутствии органических или неорганических активаторов или катализаторов. При этом перенос атома кислорода от перекиси водорода на субстрат может происходить стехиометрически или в виде каталитической реакции. Однако недостаток способа, заключающийся в необходимости использования активатора или катализатора при применении перекиси водорода, более чем компенсируется его экологическим потенциалом. В противоположность другим оксидантам, при окислении перекисью водорода в качестве побочного продукта образуется только вода. Кроме того, дополнительным преимуществом перекиси водорода является высокое содержание активного кислорода - 47%, которое намного превышает содержание кислорода у всех других общепринятых окислителей (за исключением кислорода).
До настоящего времени перекись водорода использовали в промышленности, главным образом, в качестве неселективного окислителя, как, например, для отбеливания бумаги, текстильных изделий и целлюлозы или при обработке сточных вод. Значительная часть мирового производства перекиси водорода расходуется на получение неорганических пероксосоединений для моющих средств. Только около 10% используется для производства органических химикатов, таких, как перкарбоновые кислоты или N-оксиды, что не в последнюю очередь объясняется отсутствием подходящих селективных активаторов или катализаторов.
Одним из самых распространенных методов стехиометрического активирования перекиси водорода является превращение с карбоновыми кислотами в перкарбоновые кислоты, которые могут эпоксидировать большое число олефинов. Однако при этом проблематичным является чувствительность к кислотам многих эпоксидов, особенно в водной среде, а также лабильность перкарбоновых кислот, что ведет к потере выхода.
Содержащие пероксогруппы комплексные соединения переходных металлов, такие, как MO(O2)2L2 (M = Mo или W, L = вода, диметилформамид или гексаметилфосфотриамид), которые могут быть легко получены из перекиси водорода и соответствующей окиси металла MO3, также могут эпоксидировать олефины, что соответствует стехиометрическому активированию перекиси водорода. Соединения этого особого типа особенно отличаются своей легкой доступностью.
Для каталитического активирования при эпоксидировании олефинов перекисью водорода используют, например, катализаторы, образованные из вышеупомянутых комплексных соединений переходных металлов, содержащих пероксогруппы, MO(O2)2L2. Так, в патенте США 3953362 (1) в качестве катализаторов для эпоксидирования перекисью водорода описаны молибденовые комплексы, получаемые из окиси молибдена, перекиси водорода и третичных аминов, три органических остатка которых в каждом случае представляют собой алкильные группы с 1-10 атомами углерода или арильные группы с 6-10 атомами углерода, или N-оксидов таких третичных аминов.
Заявка на европейский патент N 215415 (2) касается способа окисления олефинов в альдегиды или кетоны с помощью оксодипероксо-молибденовых или оксодипероксо-вольфрамовых комплексов с фосфотриамидным, а также аминоксидным или фосфиноксидным лигандами. В качестве примеров аминоксидов приводятся пиридин-N-оксид, 4-пиколин-N-оксид, триоктиламин-N-оксид и фенилпропилпиридин-N-оксид, в качестве примера фосфиноксида называется триметилфосфиноксид.
Из заявки на европейский патент N 097551 (3) известно о применении комплексов ванадия, ниобия и тантала формулы MO(O2)2L2 с фосфоамидным, а также аминоксидным или фосфиноксидным лигандами в качестве катализаторов эпоксидиро-вания для олефинов. В качестве примеров аминоксидов называются триметиламин-N-оксид, N-метилморфолин-N-оксид, пиридин-N-оксид, 2-, 3- или 4-пиколин-N-оксиды, хинолин-N-оксид и 2,2г-бипиридин-N-оксид, в качестве примеров фосфиноксидов называются трифенилфосфиноксид, триметил-фосфиноксид, метилдифенилфосфиноксид, диэтилфенилфосфиноксид и триморфолинофосфиноксид.
Однако недостатками описанных в работах (1)-(3) комплексов являются сравнительно низкие активность, избирательность по эпоксиду и степень превращения олефина при эпоксидировании олефинов водной перекисью водорода.
Задачей данного изобретения является разработка катализатора на основе металлических комплексов для эпоксидирования олефинов водной перекисью водорода, который обладает высокой активностью и эффективностью и может получаться простым и экономичным образом.
Поставленная задача решается предлагаемым катализатором, состав которого соответствует общей формуле (I)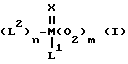
в которой M означает металл 6-ой побочной группы Периодической системы элементов,
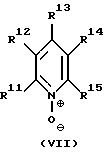
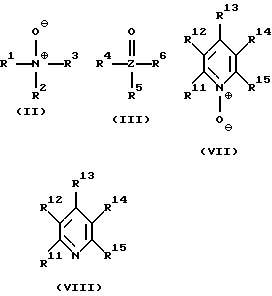
L1 означает аминоксидный лиганд формулы II, фосфаноксидный или арсаноксидный лиганд формулы III, пиридин-N-оксидный лиганд формулы VII или пиридиновый лиганд формулы VIII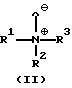
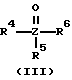
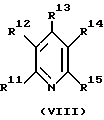
в которых R1-R3 представляют собой одинаковые или различные алкильные остатки с 1-30 атомами углерода, аралкильные остатки с 7-30 атомами углерода или арильные остатки с 6-30 атомами углерода, которые в качестве функциональных групп дополнительно могут содержать атомы кислорода простого эфира, карбонильные группы, гидроксильные группы, алкоксигруппы, карбоксильные группы, цианогруппы, группы сложного эфира карбоновой кислоты, сульфогруппы, группы фосфоновой кислоты, нитрогруппы, атомы галоидов и/или незамещенные или замещенные алкильным остатком с 1 - 4 атомами углерода аминогруппы, причем, по крайней мере, один из остатков R1 - R3 должен содержать, по меньшей мере, 11 атомов углерода, а оба других остатка вместе могут быть связаны в кольцо, и
R4-R6 представляют собой одинаковые или различные алкильные остатки с 4 - 30 атомами углерода, аралкильные остатки с 7-30 атомами углерода или арильные остатки с 10-30 атомами углерода, которые в качестве функциональных групп дополнительно могут содержать атомы кислорода простого эфира, карбонильные группы, гидроксильные группы, алкоксигруппы, карбоксильные группы, цианогруппы, группы сложного эфира карбоновой кислоты, сульфогруппы, группы фосфоновой кислоты, нитрогруппы, атомы галоидов и/или незамещенные или замещенные алкильным остатком с 1-4 атомами углерода аминогруппы, и
R11-R15 независимо друг от друга каждый означает водород или одинаковые или различные алкильные остатки с 1-30 атомами углерода, аралкильные остатки с 7-30 атомами углерода или арильные остатки с 6-30 атомами углерода, либо алкоксигруппы с 1-30 атомами углерода, аралкоксигруппы с 7-30 атомами углерода, арилоксигруппы с 6-30 атомами углерода или дигидрокарбиламиногруппы с одинаковыми или различными алкильными остатками с 1-30 атомами углерода, аралкильными остатками с 7-30 атомами углерода и/или арильными остатками с 6-30 атомами углерода в качестве гидрокарбильных остатков, которые в качестве функциональных групп дополнительно могут содержать атомы кислорода простого эфира, карбонильные группы, гидроксильные группы, алкоксигруппы, карбоксильные группы, цианогруппы, группы сложного эфира карбоновой кислоты, сульфогруппы, группы фосфоновой кислоты, нитрогруппы, атомы галоидов и/или незамещенные или замещенные алкильным остатком с 1-4 атомами углерода аминогруппы, причем, по крайней мере, один из остатков R11 - R15 должен представлять собой водород, сумма атомов углерода в остатках R11 - R15 должна равняться, по крайней мере, 8, и остатки R11 - R15 могут быть попарно связаны в кольца,
L2 означает вспомогательный лиганд из группы: оксо, галогениды, псевдогалогениды, карбоксилаты, феноляты, алкоголяты, еноляты, кетоны, простые эфиры, амины, амиды, мочевина, производные мочевины и воду или дополнительный лиганд L1, либо одну свободную координационную связь,
X означает оксокислород или незамещенный или замещенный алкилом с 1-4 атомами углерода имидо-лиганд,
Z означает атом фосфора или атом мышьяка,
m означает число 1 или 2 и
n означает число 1, 2 или 3.
Катализаторы формулы I согласно изобретению отличаются от известных из уровня техники тем, что в лигандах L1 они содержат остатки с длинной цепью или более объемные остатки, чем в описанных до этого аминоксидной или фосфаноксидной системах. У аминоксидного лиганда формулы II, по крайней мере, один из трех остатков R1-R3 должен содержать, по меньшей мере, 11, предпочтительно, по меньшей мере, 12, в частности, по меньшей мере, 14 атомов углерода. При этом предпочтительно речь идет о линейной или разветвленной алкильной группе. У фосфаноксидного или арсаноксидного лигандов формулы III нижний предел для величины линейных или разветвленных алкильных остатков R4-R6 составляет 4, предпочтительно 6, в частности, 8 атомов углерода, нижний предел для величины аралкильных остатков R4-R6 составляет 7, предпочтительно 9, в частности, 12 атомов углерода, и нижний предел для величины арильных остатков R4-R6 составляет 10, предпочтительно 12, в частности, 14 атомов углерода. У пиридин-N-оксидного и пиридинового лигандов формулы VII и, соответственно, VIII сумма атомов углерода у заместителей кольца должна равняться, по меньшей мере, 8, предпочтительно, по меньшей мере, 9; в частности, один из остатков R11-R15 представляет собой линейный с длинной цепью или разветвленный алкильный остаток, по крайней мере, с 8, прежде всего, по меньшей мере, с 9 атомами углерода.
В качестве переходных металлов для катализаторных комплексов согласно изобретению используют, в частности, титан, цирконий, гафний, ванадий, ниобий, тантал, хром, молибден, вольфрам, марганец и рений. Особенно предпочтительными являются молибден и вольфрам.
Типичными примерами амин-N-оксидных лигандов формулы II являются:
диметил-н-ундециламиноксид,
диметил-н-додециламиноксид,
диметил-н-тетрадециламиноксид,
диметил-н-гексадециламиноксид,
диметил-н-октадециламиноксид,
диметил-н-эйкозиламиноксид,
метил-ди(н-додецил)аминоксид,
метил-ди(н-октадецил)аминоксид,
три(н-додецил)аминоксид,
три(н-октадецил)аминоксид,
бензил-ди(н-додецил)аминоксид,
дифенил-н-октадециламиноксид,
N-ундецилморфолиноксид,
N-додецилпиперидиноксид,
диметил-(6-фенилгексил)аминоксид,
диметил-бисфениламиноксид и
метил-н-додецил-(6-фенилгексил)аминоксид.
Типичными примерами фосфаноксидных (фосфиноксидных) и арсаноксидных лигандов формулы III являются:
три-н-бутилфосфан- и арсаноксид,
три-трет.-бутилфосфан- и арсаноксид,
три-н-гексилфосфан- и арсаноксид,
три-н-октилфосфан- и арсаноксид,
три-(2-этилгексил)фосфан- и арсаноксид,
три-н-додецилфосфан- и арсаноксид,
три-н-октадецилфосфан- и арсаноксид,
ди-н-бутил-н-октилфосфан- и арсаноксид,
н-бутил-ди-н-октилфосфан- и арсаноксид,
трибензилфосфан- и арсаноксид,
бензил-ди-н-октилфосфан- и арсаноксид,
нафтил-ди-н-октилфосфан- и арсаноксид и
ди-н-бутил-нафтилфосфан- и арсаноксид.
Типичными примерами пиридин-N-оксидных и пиридиновых лигандов формул VII и VIII, соответственно, являются:
4-(1-октил)пиридин и соответствующий N-оксид,
4-[1-(2-этилгексил)]пиридин и соответствующий N-оксид,
4-(1-нонил)пиридин и соответствующий N-оксид,
4-(5-нонил)пиридин и соответствующий N-оксид,
4-(1-децил)пиридин и соответствующий N-оксид,
4-(1-додецил)пиридин и соответствующий N-оксид,
4-(н-октилокси)пиридин и соответствующий N-оксид,
4-(2-этилгексилокси)пиридин и соответствующий N-оксид,
4-(н-нонилокси)пиридин и соответствующий N-оксид,
4-(ди-н-октиламино)пиридин и соответствующий N-оксид и
4-(ди-2-этилгексиламино)пиридин и соответствующий N-оксид.
Если у остатков R1-R6 и R11-R15 появляются дополнительные атомы кислорода простого эфира, то такие остатки образованы, в частности, от соответствующих этиленоксидных, пропиленоксидных или бутиленоксидных, либо тетрагидрофурановых продуктов реакций.
Заместители у R1-R6 и R11-R15, представляющие собой алкоксигруппы и группы сложных эфиров карбоновой кислоты, несут предпочтительно алкильные остатки с 1-4 атомами углерода, прежде всего метил или этил. Атомы галоидов у R1-R6 и R11-R15 означают, прежде всего, хлор или бром. Количество перечисленных функциональных групп для R1-R6 и R11-R15, если таковые имеются, обычно составляет от 1 до 3, число атомов кислорода простого эфира, в зависимости от длины цепи, составляет от 1 до 14.
Приведенные в качестве замещающей группы вспомогательные лиганды L2 являются обычно применяемыми и поэтому известны специалисту.
Предпочтительными катализаторами согласно изобретению являются соединения формул (а) или (б)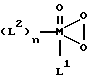
или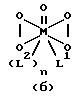
в которых L2 означает воду, а переменные M, L1 и n имеют вышеуказанные значения.
Предпочтительной формой катализаторов согласно изобретению являются катализаторы формул (I) и (а) или (б), в которых L1 означает аминоксидный лиганд II, который в качестве остатков R1-R3 несет алкильные группы с 1-20 атомами углерода, причем, по крайней мере, один из остатков R1-R3 должен означать алкильную группу с 12-20 атомами углерода, а оба других остатка могут быть связаны друг с другом в насыщенное пяти- или шестичленное кольцо, которое может содержать еще дополнительные гетероатомы из группы кислорода и азота.
Другой предпочтительной формой катализаторов согласно изобретению являются катализаторы формул (I) и (а) или (б), в которой L1 означает фосфаноксидный или арсаноксидный лиганд формулы III, который в качестве остатков R4-R6 несет алкильные группы с 4-20 атомами углерода.
Катализаторные комплексы формулы (I) согласно изобретению выгодно получать таким образом, чтобы эти каталитически активные комплексы изготовлялись из другого комплекса металла M и перекиси водорода.
Обычно получают комплексы формулы (I) путем замены лигандов L в уже вышеупомянутых, содержащих пероксогруппы комплексных соединениях переходных металлов MX(O2)m(L2)n+1, причем M, X, m и n имеют указанные значения и L означает, прежде всего, воду, диметилформамид или гексаметилфосфотриамид, на аминоксиды формулы II или фосфаноксиды формулы III. Сами эти комплексы - предшественники чаще всего очень просто получают из недорогих исходных веществ (окись металла, перекись водорода и лиганд или его предшественник).
Целесообразно получать катализаторы формулы I in situ или путем растворения окислов металлов в избытке водной перекиси водорода или из легко доступных предшественников, таких, как MO2Cl2(ДМЭ) (ДМЭ = диметоксиэтан) с использованием для активирования необходимых количеств аминоксида формулы II, фосфан- или арсаноксида формулы III, пиридин-N-оксида формулы VII или пиридина формулы VIII. Вместо амин-N-оксидов или фосфан- или арсаноксидов можно также непосредственно использовать соответствующие амины, либо фосфаны или арсаны, поскольку in situ они окисляются перекисью водорода в желаемые амин-N-оксиды или фосфаноксиды. Катализаторы можно изготовлять in situ или отдельно получать, выделять и охарактеризовывать.
В качестве предшественников для катализаторных комплексов формулы I согласно изобретению подходят также комплексы формулы VI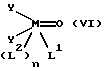
в которой Y означает галогенид, например хлор, или псевдогалогенид, например роданид, а переменные M, X, L1, L2 и n имеют вышеуказанные значения. При воздействии перекиси водорода комплексы формулы VI легко превращаются в комплексы формулы I.
Катализаторы формулы I согласно изобретению прекрасно подходят для каталитического активирования реакций окисления, особенно для эпоксидирования олефинов, прежде всего, перекисью водорода в качестве эпоксидирующего агента.
Таким образом, объектом данного изобретения является также способ получения эпоксидов общей формулы IV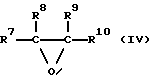
в которой остатки R7-R10 являются одинаковыми или различными и означают водород или незамещенные или замещенные алкильные, алкенильные, гетероалкильные, циклоалкильные, арильные или гетероарильные остатки, причем остатки R7-R10 могут быть также связаны друг с другом в кольца, либо означают заместители на основе элементов 4-7 главных подгрупп Периодической системы элементов, из олефинов общей формулы V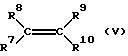
и водной перекиси водорода, который отличается тем, что эпоксидирование олефинов формулы V осуществляют в присутствии катализаторов формулы I согласно изобретению.
Применяемые олефины могут быть самыми разнообразными по характеру и числу заместителей. Типичными примерами олефинов, которые можно эпоксидировать способом согласно изобретению, являются этилен, пропен, 1-бутен, 2-бутен, изобутен, 1,3-бутадиен, 1-пентен, 2-пентен, изопрен, циклопентен, 1-гексен, циклогексен, α- моноолефины с 8-24 атомами углерода, стирол, инден, норборнен, циклопентадиен, дициклопентадиен, а также олигомеры алкенов с активными двойными связями, такие, как полипропен и полиизобутен.
Олефины формулы V у олефиновой двойной связи могут также нести заместители на основе элементов 4-7 главных подгрупп Периодической системы, примерами чему являются винилсиликоны, виниламины, винилфосфаны, простые виниловые эфиры, винилсульфиды и галоидированные алкены, такие, как винилхлорид, винилиденхлорид или трихлорэтилен.
Для осуществления эпоксидирования согласно изобретению обычно вносят катализатор формулы I и добавляют требуемые количества водной перекиси водорода и олефина, при необходимости, растворенного в соответствующем инертном органическом растворителе. Область концентрации водной перекиси водорода может находиться между 2 и 70 мас.%, особенно между 5 и 50 мас.%. В качестве инертных органических растворителей подходят, например, хлороформ, дихлорметан, эфир, сложные эфиры карбоновых кислот или ароматические углеводороды. При этом в большинстве случаев образуется двухфазная реакционная смесь. При применении смешивающихся с водой растворителей, таких, как метанол, ацетон, диметоксиэтан или диоксан, также может быть осуществлена гомогенная реакция.
Условия реакции эпоксидирования согласно изобретению являются очень мягкими, что является ее преимуществом вследствие высокой реакционной способности образующихся эпоксидов. Стандартно реакцию осуществляют при температуре от -20 до 160oC, особенно от -20 до 100oC, прежде всего от 50 до 80oC, а также в такой области температур, которая благоприятна и для отвода выделяющегося при реакции тепла. Повышенное давление необходимо только в случае легколетучих олефинов, таких, как, например, пропен или бутен; обычно реакцию осуществляют при атмосферном давлении.
Путем применения лигандов формул II, III, VII или VIII с липофильными заместителями в форме остатков с длинной цепью или объемных остатков получают, как правило, поверхностно-активные катализаторы, так что эпоксидирование может также успешно происходить в двухфазной системе, то есть в двух полностью друг с другом не смешивающихся жидких фазах. Эти варианты способа имеют, во-первых, то преимущество, что можно окислять также липофильные, не растворимые в воде олефины, и, во-вторых, что образовавшиеся эпоксиды остаются в органической фазе и таким образом подавляется образование нежелательных побочных продуктов. Кроме того, облегчается отделение продуктов реакции, получаемых по двухфазному варианту способа. По предпочтительному варианту способа согласно изобретению эпоксидируют пропен в пропиленоксид, в частности в двухфазной системе.
Также по другому предпочтительному варианту способа согласно изобретению эпоксидируют 1,3-бутадиен в винилоксиран, в частности в двухфазной системе.
С помощью высокоактивных катализаторов формулы I согласно изобретению простым и экономичным способом получают эпоксиды в мягких и щадящих условиях из олефинов с помощью водной перекиси водорода с высокой селективностью и высокой степенью превращения.
Примеры получения
Пример 1
Получение концентрированных растворов катализаторов
а) Получение водного концентрированного раствора [Mo(O)(O2)(H2O)2]
В 24,0 г (212 ммолях) 30 мас.%-ного раствора перекиси водорода при интенсивном перемешивании суспендируют 6,00 г (41,7 ммоля) [MoO3]. Бесцветную суспензию перемешивают 4 ч при 40oC, при этом образуется прозрачный светло-желтый раствор, который сохраняли при 4oC. Содержание [Mo(O)(O2)(H2O)2]: 1,39 ммоль/г.
б) Получение водного концентрированного раствора [W(O)(O2)(H2O)2]
В 24,0 г (212 ммолях) 30 мас.%-ного раствора перекиси водорода при интенсивном перемешивании суспендируют 8,00 г (32,0 ммоля) [WO3•H2O]. Желтую суспензию перемешивают 6 ч при 40oC, при этом образуется молокообразный мутный раствор. После отделения нерастворимого остатка (25 мг) центрифугированием прозрачный бесцветный раствор сохраняли при 4oC. Содержание [W(O)(O2)(H2O)2]: 1,01 ммоль/г.
Пример 2
Получение катализаторов [M(O)(O2)2L1]
а) Получение [Mo(O)(O2)2{OP(н-октил)3}]
К 1,86 г (2,58 ммоля) Mo - концентрированного раствора (пример Ia) сначала прибавляют 4 мл тетрагидрофурана. При перемешивании и температуре 25oC прибавляют 500 мг (1,29 ммоля) три-н-октилфосфан-оксида [OP(н-октил)3]. После 2 ч интенсивного перемешивания желтый раствор концентрируют в вакууме до объема около 3 мл, при этом выделяется желтое масло. Реакционную смесь экстрагируют хлористым метиленом (3 раза по 5 мл). Объединенные экстракты полностью упаривают в вакууме. Светло-желтый воскообразный остаток промывают водой (2 раза по 2 мл) и сушат 6 ч при 25oC/10-5 мбар.
Выход: 675 мг (93%) светло-желтого воска.
ДТА (дифференциальный термический анализ): 81oC (экзотермическое разложение).
Элементный анализ: C24H51PO6Mo (562,6)
вычислено: C 51,24 H 9,14
найдено: C 51,68 H 9,45
б) Получение [W(O)(O2)2{OP(н-октил)3}]
К 6,00 г (6,06 ммоля) W - концентрированного раствора (пример 1б) сначала прибавляют 12 мл тетрагидрофурана. При перемешивании и температуре 25oC к раствору прибавляют 1,50 г (3,87 ммоля) [OP(н-октил)3]. После 4 ч интенсивного перемешивания бесцветный раствор концентрируют в вакууме до объема около 5 мл, при этом выделяется бесцветное масло. Реакционную смесь экстрагируют хлористым метиленом (3 раза по 10 мл). Объединенные экстракты полностью упаривают в вакууме. Бесцветный маслянистый остаток промывают водой (3 раза по 15 мл) и сушат 6 ч при 25oC/10-5 мбар.
Выход: 2,40 г (95%) бесцветного масла.
ДТА: 98oC (экзотермическое разложение).
Элементный анализ: C24H51PO6W (650,0)
вычислено: C 44,35 H 7,91
найдено: C 45,14 H 8,53
в) Получение [Mo(O)(O2)2{ONMe2(н-C18H37)}]
К 5,00 г (6,95 ммоля) Mo - концентрированного раствора (пример 1а) прибавляют при перемешивании и температуре 25oC 6,00 г (5,74 ммоля) диметил-н-октадециламиноксида [ONMe2(н-C18H37)] (30 мас.% в воде), при этом спонтанно образуется бледно-желтый осадок. После 2 ч интенсивного перемешивания осадок отфильтровывают, промывают водой (3 раза по 50 мл) и сушат в вакууме 6 ч при 25oC/10-5 мбар.
Выход: 2,00 г (71%) бледно-желтого, аморфного твердого вещества
ДТА: 78oC (экзотермическое разложение)
Элементный анализ: C20H43MoNO6 (489,5)
вычислено: C 49,07 H 8,85 N 2,86
найдено: C 49,07 H 8,88 N 2,82
г) Получение [Mo(O)(O2)2{ON(додецил)3}]
К 2,00 г (2,87 ммоля) Mo - концентрированного раствора (пример 1а) прибавляют при перемешивании и температуре 25oC 1,20 г (2,23 ммоля) три-н-додециламиноксида [ON(додецил)3] , растворенный в 5 мл хлористого метилена. После 5 ч интенсивного перемешивания при 25oC органическую фазу отделяют, промывают водой (3 раза по 5 мл) и полностью упаривают в вакууме. Бледно-желтый аморфный остаток сушат 6 ч при 25oC/10-5 мбар.
Выход: 2,81 г (95%) бледно-желтого, аморфного твердого вещества
ДТА: 75oC (экзотермическое разложение)
Элементный анализ: C36H75MoNO6 (713,9)
вычислено: C 60,57 H 10,59 N 1,96
найдено: C 60,62 H 10,72 N 1,95
д) Получение [W(O)(O2)2{ON(додецил)3}]
К 3,00 г (3,03 ммоля) W - концентрированного раствора (пример 1б) прибавляют при перемешивании и температуре 25oC 1,30 г (2,42 ммоля) [ON(додецил)3] , растворенного в 5 мл хлористого метилена. После 5 ч интенсивного перемешивания при 25oC органическую фазу отделяют, промывают водой (3 раза по 5 мл) и полностью упаривают в вакууме. Бесцветный, липкий остаток сушат 6 ч при 25oC/10-5 мбар.
Выход: 1,84 г (95%) бесцветного, липкого воска.
ДТА: 68oC (экзотермическое разложение).
Элементный анализ: C36H75WNO6 (801,8)
вычислено: C 53,93 H 9,43 N 1,75
найдено: C 53,88 H 9,29 N 1,67
Пример 3
Каталитическое окисление циклооктена и 1-октена 30 мас.%-ной перекисью водорода с in situ образованными катализаторами типа MO(O2)2L1(H2O)
К аликвотной части (0,36 ммоля ≥ 4 мол.%) описанного в примере 1 концентрированного раствора катализатора прибавляют при 25oC 36 ммолей 30%-ной перекиси водорода и 9 ммолей олефина. Затем реакционный раствор смешивают с 0,36 ммоля фосфаноксидного или амин-N-оксидного лиганда, растворенного в 4 мл хлороформа, и перемешивают 24 ч при 60oC. Определение степени превращения олефина и избирательности по эпоксиду проводят газохроматографически.
Результаты опытов обобщены и представлены в таблице 1.
В принципе такие же результаты получают также с аналогами описанных в примере 2, отдельно полученных катализаторов (в каждом случае с 0,36 ммоля, растворенными в 4 мл хлороформа).
Примеры 4 и 5
Эпоксидирование с L1 = три(н-додецил)-арсаноксид
В стеклянный автоклав помещают 1-октен (500 мг, 4,45 ммоля), MO3 (0,17 ммоля, 4,0 мол.% относительно 1-октена, в виде 0,5 М раствора в 30%-ной перекиси водорода) и три(н-додецил)-арсаноксид (0,17 ммоля, растворенные в 3 мл хлороформа). Затем добавляют перекись водорода (17,8 ммоля, в виде 30%-ного водного раствора) и перемешивают при 60oC. Октенэпоксид является единственным обнаруженным продуктом реакции. Выходы октеноксида при различном времени реакции сведены в таблице 2.
Примеры 6 и 7
Эпоксидирование с L1 = 4-(5-нонил)-пиридин
В стеклянный автоклав помещают 1-октен (500 мг, 4,45 ммоля), MO3 (0,17 ммоля, 4,0 мол. % относительно 1-октена, в виде 0,5 М раствора в 30%-ной перекиси водорода) и 4-(5-нонил)-пиридин (0,17 ммоля, растворенные в 3 мл хлороформа). Затем добавляют перекись водорода (17,8 ммоля, в виде 30%-ного водного раствора) и перемешивают при 60oC. Октенэпоксид является единственным обнаруженным продуктом реакции. Выходы октеноксида при различном времени реакции сведены в таблице 3.
Примеры 8 и 9
Эпоксидирование с L1 = 4-(5-нонил)-пиридин-N-оксид
В стеклянный автоклав помещают 1-октен (500 мг, 4,45 ммоля), MO3 (0,17 ммоля, 4,0 мол. % относительно 1-октена, в виде 0,5 М раствора в 30%-ной перекиси водорода) и 4-(5-нонил)-пиридин-N-оксид (0,17 ммоля, растворенные в 3 мл хлороформа). Затем добавляют перекись водорода (17,8 ммоля, в виде 30%-ного водного раствора) и перемешивают при 60oC. Октенэпоксид является единственным обнаруженным продуктом реакции. Выходы октеноксида при различном времени реакции сведены в таблице 4.
Примеры 10 и 11
Эпоксидирование с L1 = 4-(диоктиламино)-пиридин
В стеклянный автоклав помещают 1-октен (500 мг, 4,45 ммоля), MO3 (0,17 ммоля, 4,0 мол.% относительно 1-октена, в виде 0,5 М раствора в 30%-ной перекиси водорода) и 4-(диоктиламино)-пиридин (0,17 ммоля, растворенные в 3 мл хлороформа). Затем добавляют перекись водорода (17,8 ммоля, в виде 30%-ного водного раствора) и перемешивают при 60oC. Октенэпоксид является единственным обнаруженным продуктом реакции. Выходы октеноксида при различном времени реакции сведены в таблице 5.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЭПОКСИДИРОВАНИЯ ПРОХИРАЛЬНОГО ОЛЕФИНА | 1995 |
|
RU2204562C2 |
| КАТАЛИТИЧЕСКИЕ СИСТЕМЫ ДЛЯ ОЛИГОМЕРИЗАЦИИ ЭТИЛЕНА В ЛИНЕЙНЫЕ АЛЬФА-ОЛЕФИНЫ | 2003 |
|
RU2315658C2 |
| ПРОИЗВОДНЫЕ КАРБОНОВЫХ КИСЛОТ | 1995 |
|
RU2180335C2 |
| ПРОИЗВОДНЫЕ ПИРИМИДИН- И ТРИАЗИНКАРБОНОВЫХ КИСЛОТ ДЛЯ ПРИМЕНЕНИЯ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 1995 |
|
RU2163808C2 |
| КАТАЛИЗАТОРЫ ОТБЕЛИВАНИЯ | 2011 |
|
RU2578565C2 |
| ПИРИДИЛДИАМИДНЫЕ КОМПЛЕКСЫ ПЕРЕХОДНЫХ МЕТАЛЛОВ, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ | 2009 |
|
RU2514405C2 |
| Z-1,2,-ДИАРИЛАЛЛИЛХЛОРИДЫ | 1992 |
|
RU2096401C1 |
| НОВЫЕ РУТЕНИЕВЫЕ КОМПЛЕКСЫ, ИХ ПРИМЕНЕНИЕ В РЕАКЦИЯХ МЕТАТЕЗИСА И СПОСОБ ПРОВЕДЕНИЯ РЕАКЦИИ МЕТАТЕЗИСА | 2013 |
|
RU2586213C1 |
| КАТАЛИЗАТОРЫ НА ОСНОВЕ ПЕРЕХОДНОГО МЕТАЛЛА 8 ГРУППЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И СПОСОБ ИХ ПРИМЕНЕНИЯ В РЕАКЦИИ МЕТАТЕЗИСА | 2014 |
|
RU2674471C2 |
| ЛИГАНДЫ И ВКЛЮЧАЮЩИЕ ИХ КАТАЛИТИЧЕСКИЕ СИСТЕМЫ ДЛЯ ОЛИГОМЕРИЗАЦИИ ЭТИЛЕНА С ПОЛУЧЕНИЕМ ЛИНЕЙНЫХ АЛЬФА-ОЛЕФИНОВ | 2002 |
|
RU2292343C2 |
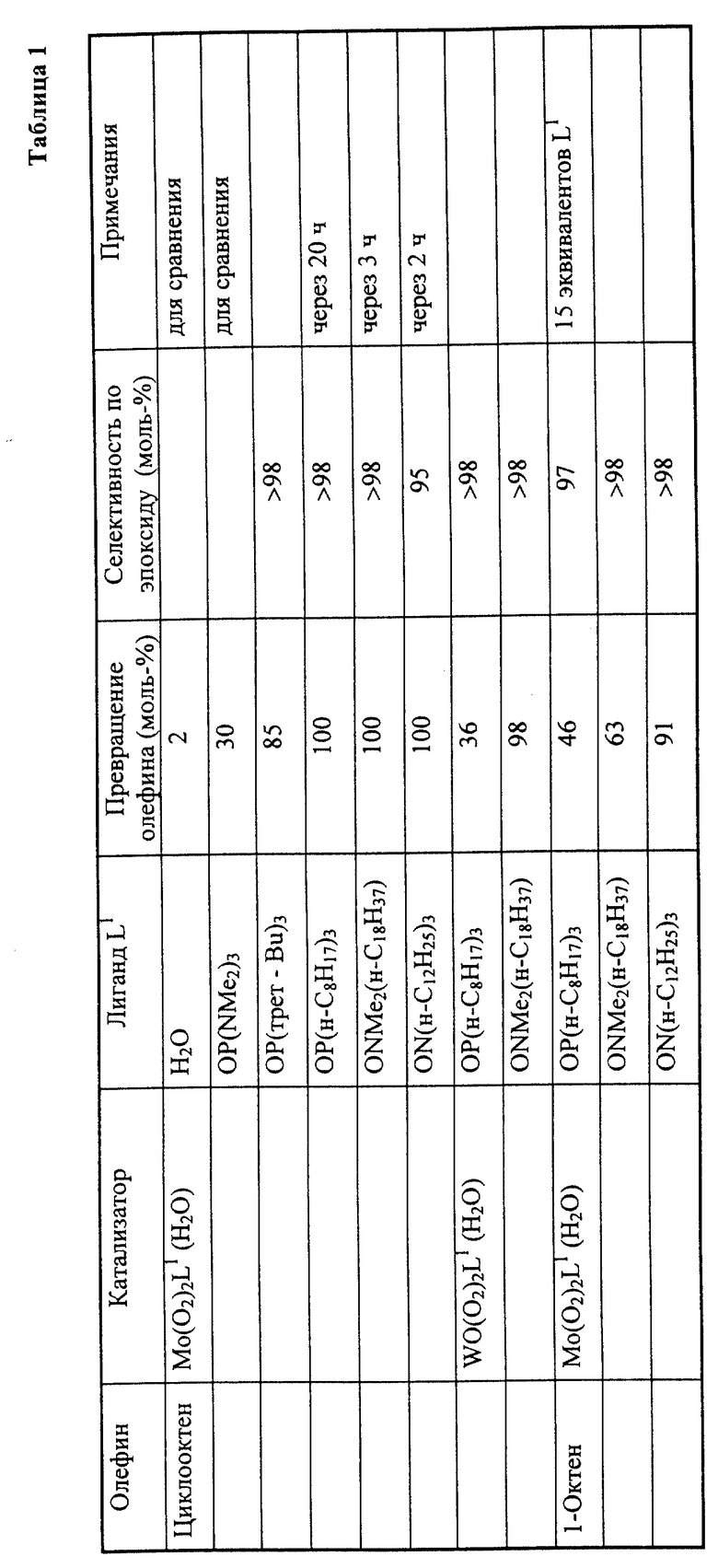




Описывается новый катализатор для эпоксидирования олефинов общей формулы (I), где М означает металл 6-ой побочной группы Периодической системы элементов, L1 означает аминоксидный лиганд формулы (II), фосфаноксидный или арсаноксидный лиганд формулы (III), пиридин-N-оксидный лиганд формулы (VII) или пиридиновый лиганд формулы (VIII), где значения R1 -R3, R4-R6, R11-R15 могут быть довольно разнообразными: L2 означает вспомогательный лиганд из группы: оксо, галогениды, псевдогалогениды, карбоксилаты, феноляты, алкоголяты, еноляты, кетоны, простые эфиры, амины, амиды, мочевина, производные мочевины и воду или дополнительный лиганд L1, либо одну свободную координационную связь, Х означает оксо-кислород или незамещенный или замещенный алкилом с 1-4 атомами углерода имидо-лиганд, Z означает атом фосфора или атом мышьяка, m означает число 1 или 2 и n означает число 1, 2 или 3. Описывается также способ получения эпоксидов. Технический результат - повышение активности, эффективности катализатора и упрощение процесса получения эпоксидов. 2 с. и 7 з.п. ф-лы, 5 табл.
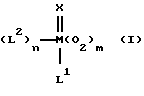
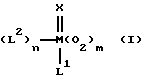
в которой М означает металл - 6-й побочной группы Периодической системы элементов;
L1 означает аминоксидный лиганд формулы (II), фосфаноксидный или арсаноксидный лиганд формулы (III), пиридин-N-оксидный лиганд формулы (VII) или пиридиновый лиганд формулы (VIII)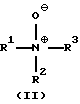
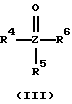
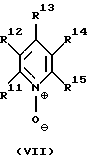
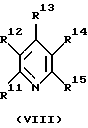
в которых R1 - R3 означают одинаковые или различные алкильные остатки с 1-30 атомами углерода, аралкильные остатки с 7-30 атомами углерода или арильные остатки с 6-30 атомами углерода, которые в качестве функциональных групп дополнительно могут содержать атомы кислорода простого эфира, карбонильные группы, гидроксильные группы, алкоксигруппы, карбоксильные группы, цианогруппы, группы сложного эфира карбоновой кислоты, сульфогруппы, группы фосфоновой кислоты, нитрогруппы, атомы галоидов и/или незамещенные или замещенные алкильным остатком с 1-4 атомами углерода аминогруппы, причем, по крайней мере, один из остатков R1 - R3 должен содержать, по меньшей мере, 11 атомов углерода, а оба других остатка вместе могут быть связаны в кольцо;
R4 - R6 означают одинаковые или различные алкильные остатки с 4-30 атомами углерода, аралкильные остатки с 7-30 атомами углерода или арильные остатки с 10-30 атомами углерода, которые в качестве функциональных групп дополнительно могут содержать атомы кислорода простого эфира, карбонильные группы, гидроксильные группы, алкоксигруппы, карбоксильные группы, цианогруппы, группы сложного эфира карбоновой кислоты, сульфогруппы, группы фосфоновой кислоты, нитрогруппы, атомы галоидов и/или незамещенные или замещенные алкильным остатком с 1-4 атомами углерода аминогруппы;
R11 - R15 независимо друг от друга каждый означает водород или одинаковые или различные алкильные остатки с 1-30 атомами углерода, аралкильные остатки с 7-30 атомами углерода или арильные остатки с 6-30 атомами углерода либо алкоксигруппы с 1-30 атомами углерода, аралкоксигруппы с 7-30 атомами углерода, арилоксигруппы с 6-30 атомами углерода или дигидрокарбиламиногруппы с одинаковыми или различными алкильными остатками с 1-30 атомами углерода, аралкильными остатками с 7-30 атомами углерода и/или арильными остатками с 6-30 атомами углерода в качестве гидрокарбильных остатков, которые в качестве функциональных групп дополнительно могут содержать атомы кислорода простого эфира, карбонильные группы, гидроксильные группы, алкоксигруппы, карбоксильные группы, цианогруппы, группы сложного эфира карбоновой кислоты, сульфогруппы, группы фосфоновой кислоты, нитрогруппы, атомы галоидов и/или незамещенные или замещенные алкильным остатком с 1-4 атомами углерода аминогруппы, причем, по крайней мере, один из остатков R11 - R15 должен представлять собой водород, сумма атомов углерода в остатках R11 - R15 должна равняться, по крайней мере, 8 и остатки R11 - R15 могут быть попарно связаны в кольца,
L2 означает вспомогательный лиганд из группы: оксо, галогениды, псевдогалогениды, карбоксилаты, феноляты, алкоголяты, еноляты, кетоны, простые эфиры, амины, амиды, мочевина, производные мочевины и воду или дополнительный лиганд L1 либо одну свободную координационную связь,
Х означает оксо-кислород или незамещенный или замещенный алкилом с 1-4 атомами углерода имидо-лиганд;
Z означает атом фосфора или атом мышьяка;
m означает число 1 или 2;
n означает число 1,2 или 3.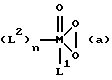
или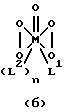
в которой L2 означает воду, а переменные М, L1 и n имеют указанные в пп. 1-4 значения.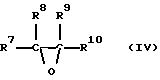
в которой остатки R7 - R10 являются одинаковыми или различными и означают водород или незамещенные или замещенные алкильные, алкенильные, гетероалкильные, циклоалкильные, арильные или гетероарильные остатки, причем остатки R7 - R10 могут быть также вместе связаны в кольца либо означают заместители на основе элементов 4-7 главных групп Периодической системы элементов, путем эпоксидирования олефинов общей формулы (V)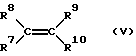
водной перекисью водорода в присутствии катализатора, отличающийся тем, что в качестве катализатора используют соединения общей формулы (I) по пп. 1-5.
| Прицепной к трактору агрегат для нарезки слоя торфа на кирпичи и укладки их на просушку | 1951 |
|
SU97551A1 |
| ЕР 215415 А2, 25.03.1987 | |||
| WO 9620788 А1, 11.07.1996 | |||
| Способ получения окисей олефинов | 1983 |
|
SU1182041A1 |
| Способ приготовления катализатора для эпоксидирования олефиновых углеводородов | 1970 |
|
SU456631A1 |
Авторы
Даты
2001-12-20—Публикация
1996-09-04—Подача