Данное изобретение касается новых биопрепаратов, неотъемлемой составной частью которых являются этерифицированные производные гиалуроновой кислоты или перекрестно связанные производные гиалуроновой кислоты, для использования в области хирургии, в особенности, для использования при предотвращении послеоперационных спаек.
Уровень техники
Образование послеоперационных спаек является частым осложнением в абдоминальной хирургии или хирургии таза, которое может приводить к выраженной болезненности. Многие факторы могут влиять на развитие спаек: механическая травма, химические вещества, высыхание слизистой в комбинации с кровью, ишемией, инфекцией и чужеродным веществом - известно, что все они увеличивают образование спаек. Другими причинами являются воспалительные заболевания внутри брюшной полости и врожденные аномалии. Патофизиологический механизм все еще остается неясным, но доказан общий центральный путь, в котором важную роль играет перитонеальный фибринолиз.
Хирургическая травма ткани вызывает освобождение серозно-геморрагического эксудата, который формирует фибриновый мостик, который существует несколько дней, в течение которых происходит размножение клеток. Если в течение этого периода эксудат не абсорбируется или не лизируется, возникают неразмножающиеся фибробласты, и последующее отложение коллагена приводит к образованию постоянного рубца, соединяющего две прилегающие поверхности, называемого спайкой. Наконец, образование спайки представляется результатом воспалительной реакции.
В этом последнем случае, исследование было сфокусировано, главным образом, на поиске биоабсорбируемых веществ с коротким временем существования in vivo, действующих в качестве барьера для образования спайки до тех пор, пока не произойдет заживление, для того, чтобы устранить проблемы, создаваемые не абсорбируемыми материалами (инфекция, кальцификация имплантатов, образование рубца и т.д.).
Одним из особенно перспективных полимеров является Гиалуроновая Кислота (ГК), компонент внеклеточного матрикса, обнаруженный повсеместно в теле человека. Показано, что растворы гиалуроновой кислоты снижают образование послеоперационных спаек после абдоминальных (Urman, В. et al., Effect of Hyaluronic Acid on Postoperative Intraperitoneal Adhesions Formation in the Rat Model, Fertil. Steril. 1991, 56:563; Shushan A. et al., Hyaluronic Acid for Preventing Experimental Postoperative-intraperitoneal Adhesions, J. Reprod. Med. 1994; 39:398) и ортопедических операций (Hadberg, L, Gerdin, В. , Sodium Hyaluronate as an adjunctive in adhesion prevention after flexor tendon surgery in rabbits, J. Hand. Surg. 1992; 17A:935).
Фирма Fidia Advanced Biopolymers разработала химические производные гиалуроновой кислоты, т.е. внутренние сложные эфиры (ряд АСР) и сложные эфиры с неактивными спиртами (ряд HYAFF) (Rastrelli, A. et al., Hyaluronic Acid Esters, A New Class of Semisynthetic Biopolymers: Chemical and Physico-chemical Properties, Clinical Implant Materials, Advanced in Biomaterials, G. Heinrike, V. Sollz and AJC Lee (Eds), Elsevier, Amsterdam 1990; 9:199-205), которые обнаруживают физико-химические свойства, отличающиеся от свойств ГК (т. е. более высокое время жизни и возможность производства для получения соответствующих средств), но имеющие свойства переносимости и биосовместимости, типичные для исходного биологического полимера. Более того, эти производные охарактеризованы с химической и токсикологической точки зрения.
Целью данного изобретения было разработать серии ACP гелей, чтобы попытаться оценить их эффект при предотвращении спаек.
Появление спаек, или фиброзных масс, которые образуются между прилежащими друг к другу тканями, подвергшимися травме или ишемии вследствие хирургической операции, все еще остается одним из наиболее тяжелых осложнений при многих хирургических процедурах. Для того, чтобы избежать этого осложнения, было предложено большое количество методов, но проблема осталась в основном неразрешенной.
Одним из предложенных методов было использование суспензий декстрана (diZerega G. S. , "Contemporary adhesion prevention" ("Современные методы предотвращения спаек") Fertility and Sterility, Vol. 61, N 2, February' 94), инъецируемых в перитонеальное пространство после хирургической операции. Клинические результаты использования таких растворов декстрана очень противоречивы. Более того, использование растворов декстрана часто сопровождалось осложнениями, включая отеки, боли в животе и одышку.
Также предлагалось использование преград в виде определенных структур (например, сеток, мембран) (diZerega G.S., "Contemporary adhesion prevention" ("Современные методы предотвращения спаек") Fertility and Sterility, Vol. 61, N 2, February' 94) или вязких гелей (Genzyme, Патенты США N 4,937,270 - N 5,017,229), помещаемых между поврежденными органами. Однако, эти преграды в основном оказались неэффективными, поскольку они вызывали ишемические или воспалительные реакции, обусловленные присутствием инородных тел. Единственными материалами, в настоящее время одобренными для клинического использования, являются преграды на основе окисленной регенерированной целлюлозы ( Interceed® ) и преграды на основе растянутого политетрафторэтилена (е-ПТФЭ) ( Goretex® - патенты США N 4, 478, 665 и N 4, 482, 516) или полиэтилена, или полипропилена.
В дополнение к тому факту, что клинические исследования эффективности таких барьеров дали очень противоречивые результаты, следует также отметить, что оба вышеуказанных материала связаны с важными противопоказаниями. Использование барьерных мембран из e- PTFE, или полиэтилена, или полипропилена включает имплантацию синтетического материала, который является чужеродным для организма человека и не способен к биодеградации, и который может потребовать повторной хирургической операции для удаления или репозиции барьерной мембраны из-за нежелательных реакций воспалительного типа.
В преклинических и клинических моделях сетки на основе окисленной регенерированной целлюлозы были признаны эффективными для предотвращения образования спаек, но только в том случае, если их наложению предшествовал полный гемостаз.
Поэтому было предложено использование вязких растворов гиалуроновой кислоты (ГК) с большим молекулярным весом как вспомогательного средства для предотвращения спаек (Grainger D. A. et al., "The use of hyaluronic acid polymers to reduce postoperative adhesions", J. of Gynecol. Surg., Vol. 7, N 2. 1991; Hurman В. et al., "Effect of hyaluronic acid on postoperative intraperitoneal adhesion formation in the rat model", Fertility and Sterility, Vol. 56, N 3, September 1991; Shushan A. et al., "Hyaluronic acid for preventing experimental postoperative intraperitoneal adhesions", J. of Reproductive Med., Vol. 39, N 5, May 1994; Mitchell J.D. et al., "Reduction in experimental pericardial adhesions using a hyaluronic acid bioabsorbable membranes", Eur. J. Cardio-thorac. Surg.,8, 149-152, 1994). Гиалуроновая кислота сама по себе, однако, характеризуется очень быстрым временем абсорбции, которое несопоставимо с временем сохранения, необходимым для предотвращения спаек. Более того, природная гиалуроновая кислота не может быть подвергнута технологическому процессу и как таковая не может быть трансформирована в форму биоматериала. Чтобы продлить время ее деградации и позволить ее переработку в различные физические формы для использования в различных областях хирургии, были разработаны эфиры гиалуроновой кислоты и перекрестно связанные производные гиалуроновой кислоты. Получение эфиров гиалуроновой кислоты, где все или часть карбоксильных групп этерифицированы, получение перекрестно связанных производных гиалуроновой кислоты, где часть карбоксильных групп подвергается перекрестному связыванию, и способы их использования в фармацевтическом, косметическом и хирургическом секторах и в виде биодеградируемых пластмасс описаны в патентах США N 4,851,521 и N 4,965,353, европейских патентах ЕР 0216453 и ЕР 0341745.
Сущность изобретения
Задача, решаемая настоящим изобретением, заключается в получении биоматериалов для использования с целью предотвращения послеоперационных спаек. Биоматериалы согласно изобретению включают бензиловые эфиры гиалуроновой кислоты и/или внутренне перекрестно связанные производные гиалуроновой кислоты и могут быть в форме гелей, мембран, сеток тканого или нетканого полотна. Предлагается также новый способ предотвращения хирургических спаек ткани путем наложения на ткань, вовлеченную в хирургическую операцию биоматериала согласно изобретению.
Перечень фигур чертежей
Фиг. 1-10 являются графиками результатов исследования спаек в модельных экспериментах на животных - крысах.
Сведения, подтверждающие возможность осуществления изобретения
Настоящее изобретение, таким образом, описывает получение средств для медико-санитарной помощи и хирургии на основе бензилового эфира гиалуроновой кислоты или перекрестно связанных производных гиалуроновой кислоты, используемых по отдельности или в смесях друг с другом, характеризующиеся высокой биосовместимостью и возможностью трансформации в физические формы, которые делают их пригодными для различных способов использования в хирургии, включая лапароскопическую хирургию. Материалы также являются полностью биодеградируемыми и не требуют удаления с места аппликации, тем самым устраняя необходимость повторной хирургической операции. Будучи приготовлены в форме гелей, перекрестно связанные производные обеспечивают материалы со значительно большей вязкостью, чем немодифицированный полимер, и с очень вариабельным временем деградации. Более того, как материалы на основе бензиловых эфиров, так и материалы на основе перекрестно связанных производных, являющиеся предметом данного изобретения, могут быть в форме мембран, сеток, тканого или нетканого полотна (приготовленных в соответствии с процедурами, per se описанными в патентных документах США N 4,851,521; N 4,956,353; WO 93/11804; WO 93/11803; WO 94/17837 и EP 0341745) и характеризуются следующими техническими характеристиками:
- мембраны варьируют по толщине между 10 мкм и 1,5 мм, предпочтительно между 20-50 мкм;
- ткани или сетки варьируют по толщине между 200 мкм и 1,5 мм;
- нетканые материалы по существу характеризуются базисной плотностью, варьирующей между 20 г/м2 и 500 г/м2, и толщиной между 0,2 мм и 5 мм, предпочтительно менее 1 мм.
Эти материалы могут быть использованы по отдельности или вместе друг с другом, или с другими материалами, состоящими из синтетических полимеров (например, гели на основе перекрестно связанной гиалуроновой кислоты + полипропилен, или мембраны, неотъемлемой составной частью которых являются этерифицированные производные ГК + полипропилен, или мембраны, включающие этерифицированные производные ГК, покрытые гелем из аутоперекрестно связанной ГК).
Таким образом, данное изобретение также включает использование композитных материалов в форме гелей (для перекрестно связанных производных), мембран, тканых или нетканых материалов, неотъемлемой составной частью которых являются бензиловые сложные эфиры или перекрестно связанные производные гиалуроновой кислоты вместе с не подвергающимися биодеградации материалами в форме сеток, или мембран, или нетканых материалов, таких, как e-ПТФЭ, полиэтилен, полипропилен, полиэфир (Дакрон®). Данное изобретение, следовательно, включает новый класс медико- санитарных и хирургических средств, которые могут быть использованы в области хирургии для предотвращения образования послеоперационных спаек.
Материалы
Как отмечено выше, данное изобретение характеризуется материалами, включающими производные гиалуроновой кислоты, особенно производными в виде бензиловых сложных эфиров и производными с внутренними перекрестными связями.
Термин "гиалуроновая кислота" (также обозначаемая далее, как "ГК") используется в литературе для обозначения кислых полисахаридов с различным молекулярным весом, состоящих из остатков D-глюкуроновой кислоты и N-ацетил-D-глюкозамина, которые в естественных условиях присутствуют на клеточных поверхностях, среди основных внеклеточных веществ соединительных тканей позвоночных, в синовиальной жидкости суставов, в стекловидном теле глаза, в ткани пупочного канатика человека и в петушиных гребнях.
Гиалуроновая кислота играет важную роль в биологическом организме, во-первых, как механическая опора клеток многих тканей, таких как кожа, связки, мышцы и хрящи, и поэтому является главным компонентом внеклеточного матрикса. Но гиалуроновая кислота выполняет также другие функции в биологических процессах, такие, как гидратация тканей, смазывание, миграция клеток, функционирование и дифференциация клеток (см., например, A. Balazs et al., Cosmetics & Toiletries, N 5/84, pp. 8-17). Гиалуроновая кислота может также быть экстрагирована из вышеуказанных природных тканей, таких как петушиные гребни, или также из некоторых бактерий. В настоящее время гиалуроновая кислота может быть получена также микробиологическими методами. Молекулярный вес цельной гиалуроновой кислоты, полученной путем экстракции, находится в диапазоне 8-13 миллионов. Однако, молекулярная цепь полисахарида очень легко может быть разрушена под влиянием различных физических и химических факторов, таких как механические воздействия, или под влиянием радиации, гидролиза, окисления или ферментативных агентов. По этой причине при обычных процедурах очистки исходных экстрактов часто получают деградированные фракции с более низким молекулярным весом (см. Balazs et al., цитировано выше). Гиалуроновая кислота, ее молекулярные фракции и соответствующие соли были использованы в качестве медикаментов, и их использование также предполагается в косметических препаратах (см., например, вышеуказанную статью Balazs et al. и патент Франции N 2478468).
Хотя термин "гиалуроновая кислота" обычно используется в неподходящем смысле, означая, как видно из вышеизложенного, целую серию полисахаридов с различными остатками D-глюкуроновой кислоты и N-ацетил-D-глюкозамина с различными молекулярными весами или даже их деградированные фракции, и хотя множественное число "гиалуроновые кислоты" представляется более подходящим, далее описание будет продолжаться с использованием единственного числа для ссылок на гиалуроновую кислоту в ее различных формах, включая ее молекулярные фракции, и аббревиатура "ГК" также будет часто использоваться для обозначения этого широкого термина.
1. Производные в виде бензиловых эфиров
Первый предпочтительный материал, являющийся предметом изобретения, основан на бензиловом сложном эфире гиалуроновой кислоты, в частности, 80-100% эфирах, где от 80% до 100% карбоксильных групп ГК этерифицированы. Такие бензиловые эфиры, где 80-99% карбоксильных групп ГК этерифицированы бензильной группой, обозначаются как "частичные эфиры", поскольку только часть карбоксильных групп этерифицирована, а оставшиеся карбоксильные группы являются либо свободными, либо образуют соли со щелочными или щелочноземельными металлами, такими, как натрий, кальций или калий.
Наиболее предпочтительными для биоматериалов, являющихся предметом изобретения, являются так называемые "полные" бензиловые сложные эфиры, где все карбоксильные группы ГК этерифицированы. В этих полных эфирах все карбоксильные группы ГК могут быть этерифицированы бензильной группой (также обозначаются как HYAFF 11), или часть (от 75% до 99%) может быть этерифицирована бензильной группой, а все остальные карбоксильные группы этерифицированы липидной цепью/алкильной группой от C10-20 алифатических спиртов - образования, которые могут быть обозначены как "смешанные" эфиры. Из этих алифатических спиртов наиболее предпочтительны пальмитиновый спирт (С16-гексадецил) и стеариновый спирт (C18-октадецил). Эти смешанные эфиры также могут быть в форме частичных эфиров, т.е. производных, где часть (от 75% до 99%) карбоксильных групп этерифицирована бензильными группами, а некоторые, но не все оставшиеся карбоксильные группы этерифицированы С10-C20 алифатическим спиртом. Из них наиболее предпочтительными являются те, которые, по меньшей мере, на 75% этерифицированы бензильными группами и, по меньшей мере, на 5% этерифицированы C10-C20 алифатическими спиртами.
Бензиловые эфиры гиалуроновой кислоты, в соответствии с изобретением, могут быть получены способами, известными per se для этерификации карбоксильных кислот, например, при обработке свободной гиалуроновой кислоты спиртом (бензилом и/или C10-C20 спиртами) в присутствии катализирующих веществ, таких, как сильные неорганические кислоты или ионные обменники кислотного типа, или этерифицирующим агентом, способным вводить желаемый спиртовой остаток в присутствии неорганических или органических оснований.
Бензиловые сложные эфиры гиалуроновой кислоты могут, однако, быть получены более эффективно в соответствии с особым методом, описанным в документе ЕР 0216453. Этот метод состоит в обработке четвертичной аммониевой соли гиалуроновой кислоты этерифицирующим агентом, предпочтительно в апротонном органическом растворителе.
Для получения бензиловых эфиров можно использовать гиалуроновые кислоты любого происхождения, как например, кислоты, экстрагированные из вышеуказанных природных исходных материалов, например из петушиных гребней. Получение таких кислот описано в литературе: предпочтительно используются очищенные гиалуроновые кислоты. В соответствии с изобретением, преимущественно используемыми являются гиалуроновые кислоты, содержащие молекулярные фракции интегральных кислот, полученные непосредственно путем экстракции органических материалов с молекулярными весами, варьирующими в широком диапазоне, например, от примерно 90%-80% (М = 11,7- 10,4 миллионов Дальтон) до 0,2% (М = 30000 Дальтон) молекулярного веса интегральной кислоты, имеющей молекулярный вес 13 миллионов Дальтон, предпочтительно, между 5% и 0,2%. Такие фракции могут быть получены при помощи различных процедур, описанных в литературе, таких, как гидролиз, окисление, энзиматические или физические процедуры, такие, как механические или радиационные процедуры. Поэтому в ходе одних и тех же процедур экстракции часто образуются первичные экстракты (например, смотри процитированную выше статью Balazs et al. в "Cosmetics & Toiletries"). Разделение и очистка полученных молекулярных фракций производится при помощи известных методик, например, путем молекулярной фильтрации.
Одной из фракций очищенной ГК, пригодной для использования в соответствии с изобретением, является, например, та, которая известна как "невоспалительный- NIF-NaГK" - гиалуронат натрия, описанный Balazs в брошюре "Healon" - A guide to its use in Ophthalmic Surgery, D. Miller & R.Stegmann, eds. John Wiley & Sons, N.Y., 81983: p. 5.
Особенно важными в качестве исходных материалов для бензиловых эфиров являются две очищенных фракции, которые можно получить из гиалуроновой кислоты (например, гиалуроновой кислоты, экстрагированной из петушиных гребней), известные как "Гиаластин" ("Hyalastine") и "Гиалектин" ("Hyalectin"). Фракция Гиаластин имеет средний молекулярный вес примерно от 50000 до 100000 Дальтон, тогда как фракция Гиалектин имеет средний Дальтон примерно между 500000 и 730000. Также была выделена объединенная фракция этих двух фракций и охарактеризована как имеющая средний молекулярный вес примерно от 250000 до 350000 Дальтон. Эта объединенная фракция может быть получена в количестве 80% от всей гиалуроновой кислоты, которую можно извлечь из определенного исходного материала, тогда как фракция Гиалектин может быть получена в количестве 30%, а фракция Гиаластина в количестве 50% исходной ГК. Получение этих фракций описано в документе ЕР 0138572.
Следующие примеры описывают получение бензиловых эфиров ГК.
Пример 1 - Получение бензилового эфира гиалуроновой кислоты (ГК)
12,4 г тетрабутиламмониевой соли ГК с молекулярным весом 170000 Дальтон, что соответствует 20 мэкв мономера, растворяют в 620 мл диметилсульфоксида при 25oC, добавляют 4,5 г (25 мэкв) бензилбромида и 0,2 г иодида тетрабутиламмония, раствор в течение 12 часов выдерживают при 30oC.
Результирующую смесь медленно вливают в 3500 мл этилацетата при постоянном перемешивании. Образуется преципитат, который фильтруют и промывают четыре раза 500 миллилитрами этилацетата и в конце высушивают под вакуумом в течение двадцати четырех часов при 30oC.
Получают 9 г продукта бензилового эфира, соответствующего заголовку данного примера. Количественное определение сложноэфирных групп выполняют в соответствии с методом, описанным на страницах 169-172 работы Siggia S. and Hann J.G. "Quantitative organic analysis via functional groups", 4th edition, John Wiley and Sons.
Пример 2 - Получение бензилового эфира гиалуроновой кислоты (ГК)
3 г калиевой соли ГК с молекулярным весом 162000 Дальтон суспендируют в 200 мл диметилсульфоксида; добавляют 120 мг иодида тетрабутиламмония и 2,4 г бензил бромида.
Суспензию выдерживают при перемешивании в течение 48 часов при 30oC. Результирующую смесь медленно вливают в 1000 мл этилацетата при постоянном перемешивании. Образуется преципитат, который фильтруют и промывают четыре раза 150 миллилитрами этилацетата и в конце высушивают под вакуумом в течение двадцати четырех часов при 30oC.
Получают 3,1 г продукта бензилового эфира, соответствующего заголовку данного примера. Количественное определение сложноэфирных групп выполняют в соответствии с методом, описанным на страницах 169-172 работы Siggia S. and Hann J.G. "Quantitative organic analysis via functional groups", 4th edition, John Wiley and Sons.
Пример 3 - Получение производного гиалуроновой кислоты с 75% карбоксильных функциональных групп, этерифицированных бензиловым спиртом, и оставшимися 25%, этерифицированными октадециловым спиртом (стеариловым спиртом, CH3-(CH2)16-CH2-OH)
6,21 г тетрабутиламмониевой соли гиалуроновой кислоты с молекулярным весом 180000 Дальтон (10 мэкв) растворяют в 248 г диметилсульфоксида (ДМСО) при комнатной температуре.
К этому раствору добавляют 0,89 мл бензилбромида (7,5 мэкв), и раствор оставляют стоять при 30oC в течение 12 часов. Затем раствор охлаждают до комнатной температуры и добавляют 0,83 г октадецилбромида (2,5 мэкв). Раствор выдерживают при 30oC в течение 24 часов. Затем добавляют 2,5% раствор (вес/вес) NaCl в воде, и результирующую смесь приливают к 750 мл ацетона, в это время перемешивая. Образуется преципитат, который фильтруют и промывают три раза в 100 мл ацетона в воде в соотношении 5:1, три раза 100 миллилитрами ацетона, и затем высушивают в высоком вакууме в течение 24 часов при 30oC. В результате получают 5,1 грамма желаемого продукта. Количественное определение содержания бензилового спирта и гексадецилового спирта выполняют при помощи газовой хроматографии с последующим щелочным гидролизом. Общее содержание сложноэфирных групп количественно определяют в соответствии с методом омыления, описанным на страницах 169-172 "Quantitative organic analysis via functional groups", 4th edition (John Wiley and Sons).
Пример 4 - Получение производного гиалуроновой кислоты с 75% карбоксильных функциональных групп, этерифицированных бензиловым спиртом, и оставшимися 25%, этерифицированными гексадециловым спиртом (цетиловым пальмитиловым спиртом, CH3-(CH2)16-CH2-ОН)
6,21 г тетрабутиламмониевой соли гиалуроновой кислоты с молекулярным весом 180000 Дальтон (10 мэкв) растворяют в 248 мл диметилсульфоксида (ДМСО) при комнатной температуре.
К этому раствору добавляют 0,89 мл бензилбромида (7,5 мэкв), и раствор оставляют стоять при 30oC в течение 12 часов. Затем раствор охлаждают до комнатной температуры и добавляют 0,76 г гексадецилбромида (2,5 мэкв). Раствор нагревают до 30oC в течение 24 часов. Затем добавляют 2,5% раствор (вес/вес) NaCl в воде, и результирующую смесь приливают к 750 мл ацетона, в это время перемешивая. Образуется преципитат, который фильтруют и промывают три раза в 100 мл ацетона в воде в соотношении 5:1, три раза 100 мл ацетона, и затем высушивают в высоком вакууме в течение 24 часов при 30oC. В результате получают пять граммов желаемого продукта. Количественное определение содержания бензилового спирта и гексадецилового спирта выполняют при помощи газовой хроматографии с последующим щелочным гидролизом. Общее содержание эфирных групп количественно определяют в соответствии с методом омыления, описанным на страницах 169-172 "Quantitative organic analysis via functional groups" 4th edition (John Wiley and Sons).
2. Производные гиалуроновой кислоты с внутренними перекрестными связями
Производные гиалуроновой кислоты с перекрестными связями, использованные в материалах по настоящему изобретению, описаны в документе ЕР 0341745. Эти производные с перекрестными связями являются меж- и/или внутримолекулярными сложными эфирами гиалуроновой кислоты, где часть карбоксильных групп этерифицирована гидроксильными группами той же молекулы и/или других молекул гиалуроновой кислоты с формированием таким образом лактонов или внутримолекулярных сложноэфирных связей. Эти "внутренние" эфиры, в которых нет внедрения ОН групп других спиртов, также могут быть обозначены как "аутоперекрестно связанная гиалуроновая кислота", так как образование моно- или полимолекулярной перекрестной связи является следствием вышеуказанной внутренней этерификации. Прилагательное "перекрестно связанный" обозначает перекрестные соединения между карбоксилами и гидроксилами молекул гиалуроновой кислоты.
Аутоперекрестно связанными продуктами, в частности, являются неполные внутренние сложные эфиры, в которых процент "поперечных связей" варьирует предпочтительно между 0,5 и 20%, чаще всего составляя 4,5/5,0% от числа карбоксильных групп в гиалуроновой кислоте. В процессе получения карбоксильные группы молекулы гиалуроновой кислоты активируются при добавлении веществ, способных индуцировать такую активацию. Нестабильные промежуточные продукты, полученные в реакции активации, спонтанно отделяются или после добавления катализаторов, и/или вследствие возрастания температуры, образуя вышеуказанные внутренние сложноэфирные связи с гидроксилами той же самой или другой молекулы гиалуроновой кислоты. В соответствии с желаемым уровнем внутренней этерификации либо все, либо аликвотная часть карбоксильных функциональных групп активируются (аликвотную часть получают путем использования избытка активирующих веществ или путем соответствующих методов дозирования).
Карбоксильные группы, конвертируемые во внутренние сложноэфирные группы, могут быть активированы, начиная с гиалуроновой кислоты, содержащей свободные карбоксильные группы, или, предпочтительно, с ГК, содержащей карбоксильные группы в виде солей, например, солей металлов, предпочтительно, щелочных и щелочноземельных металлов, и кроме того, с четвертичных аммониевых солей, такими, как описанные ниже. Тем не менее, соли на органической основе, такие, как амины, могут также быть использованы как исходные вещества.
Методы активации свободных или образовавших соли карбоксильных групп известны per se, в частности, в области синтеза пептидов, и специалисты в данной отрасли науки могут легко определить, какой метод является наиболее подходящим, и особенно, можно или нет использовать исходные вещества в их свободной форме или в виде солей. Методы активации per se, известные для процедур синтеза пептидов и пригодные для процедур получения по настоящему изобретению, описаны, например, в Bodanszky, М., In search of new methods in peptide synthesis, Int. J. Peptide Protein Res. 25, 1985, 449-474; и Gross, E. et al, The Peptides, Analysis, Synthesis, Biology, Academic Press, Inc., 1979, Vol. 1, Chapter 2. В соответствии с такими процедурами, карбоксильный компонент активируется, и это значит, что карбоксильный компонент превращается в реактивную форму. Такая активация обычно включает реакцию между кислотой и активирующим агентом, в соответствии со схемой: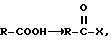
где X - часть, оттягивающая на себя электроны. Большинство активированных производных карбоксильных кислот поэтому являются смешанными ангидридами, включающими в широком смысле также азиды кислоты и хлорангидриды, которые могут быть признаны смешанными ангидридами азотоводородной кислоты и HCl, в качестве активирующих агентов. Кроме того, активация карбоксильного компонента может быть выполнена путем образования промежуточных "активированных эфиров". Эти "активированные эфиры" могут быть различных типов, но особенно полезными "активированными эфирами" являются те, которые получены при использовании дициклогексилкарбодиимида, p-нитрофениловых эфиров, трихлорфениловых эфиров, пентахлорфениловых эфиров и O-ацильных производных гидроксиламинов, в частности, эфиров N- гидроксисукцинимида.
Все эти различные типы процедур активации пригодны для получения перекрестно связанной ГК в соответствии с настоящим изобретением, поскольку все эти процедуры могут быть охарактеризованы как включающие в качестве важного компонента реакцию карбоксильной группы с активирующим агентом, которая обязательно приводит к образованию заместительной группы, которая легко реагирует с гидроксильной группой, так что легко образует внутреннюю сложноэфирную связь, характерную для продуктов по настоящему изобретению, число карбоксильных функциональных групп, которые могут быть превращены во внутренние сложные эфиры, в пропорции к числу активированных карбоксильных функциональных групп, и их число зависят от качества используемого активирующего агента.
Предпочтительные процедуры для получения перекрестно связанной ГК поэтому характеризуются обработкой ГК, имеющей свободные или образовавшие соли карбоксильные группы, агентом, который активирует карбоксильную функциональную группу, возможно, в присутствии вспомогательного агента, способствующего образованию промежуточных активированных производных, и/или четвертичных органических или неорганических оснований, при воздействии на смесь нагреванием или излучением (в частности, УФ излучением), и, если желательно, путем образования солей из свободных карбоксильных групп или путем освобождения карбоксигрупп, образовавших соли. Из веществ, способных активировать карбоксильную группу, могут быть использованы обычные, описанные в литературе, например, те, которые обычно используются в синтезе пептидов, за исключением, однако, тех, которые могут проявлять эффект нарушения или разрушения молекулярной структуры исходной ГК, таких, как те, которые используются для образования галогенидов карбоксильных групп. Предпочтительными веществами, которые приводят к образованию активированных эфиров, являются такие вещества, как карбодиимиды, дициклогексилкарбодиимид, бензилизопропилкарбодиимид, бензил-этил-карбодиимид, этоксиацетилен; реагент Вудварда (N-этил-5-фенилизоксазолиум-3- сульфонат), или галогеновые производные алифатических, циклоалифатических или ароматических углеводородов, или гетероциклического соединения с галогеном, приобретающим подвижность в присутствии одной или более активирующих групп, такие, как хлорацетонитрил и особенно соли 2-хлор-N-алкилпиридина, такие, как хлорид 2-хлор-N-метил-пиридина или другие производные алкилов с неразвитыми алкильными группами, такие, как производные алкилов с количеством атомов углерода до 6. Конечно, вместо хлорных производных могут быть использованы другие галогеновые производные, такие, как бромидные производные.
Эта реакция активации может быть выполнена в органических растворителях, особенно, апротонных растворителях, таких как диалкилсульфоксиды, диалкилкарбоксиламиды, такие, в частности, как диалкилсульфоксиды низших алкилов, в частности, диметилсульфоксид, сульфоксиды полиметилена, такие как сульфоксид тетраметилена, диалкилы или сульфоны полиметилена, такие, как сульфон тетраметилена, сульфолан и диалкиламиды низших алифатических кислот, в которых алкильные группы имеют максимально шесть атомов углерода, такие, как диметил- или диэтилформамид, или диметил- или диэтилацетамид. Однако могут быть использованы также другие растворители, и они не всегда должны быть апротонными, такие как спирты, простые эфиры, кетоны, сложные эфиры, такие, как низшие алифатические диалкилоксикарбиды, такие как диметоксиэтан и особенно алифатические или гетероциклические спирты и кетоны с низкой точкой кипения, такие как низшие N-алкил-пирролидоны, такие, как N-метилпирролидон или N-этил-пирролидон, гексафторизопропанол и трифторэтанол. Если галогеновые производные используются в качестве карбоксил-активирующих веществ, особенно в форме солей, таких, как вышеуказанный хлорид 2-хлор-N- метилпиридиния, лучше использовать соли металлов или соли органического основания исходного полисахарида, особенно, одну из солей четвертичного аммония, описанных ниже, такую, как соль тетрабутиламмония. Эти соли имеют особое преимущество, являясь очень хорошо растворимыми в вышеуказанных органических растворителях, в которых можно лучше всего влиять на реакцию образования перекрестных связей, гарантируя таким образом прекрасный выход. Можно порекомендовать добавить к смеси вещество, способное вытеснять кислоту, такое, как органические основания, карбонаты, бикарбонаты или ацетаты щелочных или щелочноземельных металлов, или органические основания и, особенно, четвертичные основания, такие, как пиридин и его гомологи, такие, как коллидин, или алифатические аминные основания, такие, как триэтиламин или N-метил-пиперазин.
Использование солей четвертичного аммония представляет собой процедуру, имеющую особые преимущества. Такие аммониевые соли хорошо известны и их получают тем же способом, что и другие известные соли. Они являются производными алкилов, имеющих предпочтительно число атомов углерода от 1 до 6. Предпочтительно использовать соли тетрабутиламмония. Одна из вариаций процедуры, в которой используются соли четвертичного аммония, состоит в реагировании соли щелочного металла, например, натриевой или калиевой соли, в присутствии катализирующего количества соли четвертичного аммония, такой, как иодид тетрабутиламмония.
Вещества, катализирующие активацию карбоксильных групп, которые следует добавлять к активирующим агентам, сообщаются в литературе, и они также предпочтительно являются основаниями, такими, как указанные ранее. Так например, когда карбоксильные группы активируются изотиазоловыми солями, предпочтительно добавить к реакционной смеси некоторое количество триэтиламина.
Реакция образования активированных промежуточных веществ, особенно таких, как сложные эфиры, проводится при температуре, рекомендованной в литературе, но эту температуру, однако, можно варьировать в зависимости от необходимых условий, что может легко определить специалист в данной области науки. Образование внутренних сложноэфирных связей может происходить в достаточно широком диапазоне температур, например, между 0oC и 150oC, предпочтительно при комнатной температуре или несколько более высокой, например, между 20oC и 75oC. Повышение температуры благоприятствует образованию внутренних сложноэфирных связей, как и воздействие излучения подходящей длины волны, например такого, как ультрафиолетовое излучение.
Субстрат гиалуроновй кислоты может быть любой природы и может быть различных типов, обсуждавшихся выше. Предпочтительными исходными материалами являются ГК, которые имеют средний молекулярный вес от 150000 до 730000, предпочтительно от 150000 до 450000 Дальтон.
Кроме того, количество внутренних перекрестных связей варьирует, но предпочтительные материалы, соответствующие изобретению, используют ГК с количеством перекрестных связей на уровне от 4,5 до 5% карбоксильных групп.
Следующие примеры описывают получение перекрестно связанных продуктов ГК, полезных для изготовления материалов согласно настоящему изобретению.
Пример 5 - Получение гиалуроновой кислоты (ГК) с 1% перекрестных связей
Описание продукта:
1% карбоксильных групп использован для внутренней этерификации.
99% карбоксильных групп образуют соли с натрием.
6,21 г тетрабутиламмониевой соли ГК с молекулярным весом 170,000 Дальтон, что соответствует 10 мэкв мономера, растворяют в 248 мл ДМСО при 25oC, добавляют 0,01 г (0,1 мэкв) триэтиламина.
Пример 6 - Получение гиалуроновой кислоты с 5% перекрестных связей
Описание продукта:
5% карбоксильных групп использовано для внутренней этерификации.
95% карбоксильных групп образуют соли с натрием.
6,21 г тетрабутиламмониевой соли ГК с молекулярным весом 85,000 Дальтон, что соответствует 10 мэкв мономера, растворяют в 248 мл ДМСО при 25oC, добавляют 0,051 г (0,5 мэкв) триэтиламина, и результирующую смесь перемешивают в течение 30 минут.
Раствор 0,128 г (0,5 мэкв) иодида 2-хлор-1-метилпиридиния в 60 мл ДМСО медленно добавляют по каплям в течение периода времени, равного 1 часу, и смесь выдерживают в течение 15 часов при 30oC.
Затем добавляют раствор, образованный из 100 мл воды и 2,5 г хлорида натрия, и результирующую смесь затем медленно приливают к 750 мл ацетона, сохраняя постоянное перемешивание. Образуется преципитат, который затем фильтруют и промывают три раза 100 миллилитрами водного раствора ацетона в пропорции 5:1, и, наконец, высушивают в вакууме в течение 24 часов при 30oC.
Получают 3,95 г соединения, соответствующего заголовку примера. Количественное определение сложноэфирных групп выполняют в соответствии с методом омыления, описанным на стр. 169-172 "Quantitative organic analysis via functional groups", 4th edition (John Wiley and Sons).
Пример 7: Получение гиалуроновой кислоты с 10% перекрестных связей
Описание продукта:
10% карбоксильных групп использовано для внутренней этерификации.
90% карбоксильных групп образуют соли с натрием.
6,21 г тетрабутиламмониевой соли ГК с молекулярным весом 620000 Дальтон, что соответствует 10 мэкв мономера, растворяют в 248 мл ДМСО при 25oC. Добавляют 0,101 г (1,0 мэкв) триэтиламина, и результирующую смесь перемешивают в течение 30 минут.
Раствор 0,255 г (1,0 мэкв) иодида 2-хлор-1-метил-пиридиния в 60 мл ДМСО медленно добавляют по каплям в течение периода времени, равного 1 часу, и смесь выдерживают в течение 15 часов при 30oC.
Затем добавляют раствор, образованный из 100 мл воды и 2,5 г хлорида натрия, и результирующую смесь затем медленно приливают к 750 мл ацетона, осуществляя постоянное перемешивание. Образуется преципитат, который затем фильтруют и промывают три раза в 100 мл смеси ацетона с водой в соотношении 5: 1, и три раза при помощи 100 мл ацетона, и, наконец, высушивают в вакууме в течение 24 часов при 30oC.
Получают 3,93 г соединения, соответствующего заголовку примера. Количественное определение сложноэфирных групп выполняют в соответствии с методом омыления, описанным на стр. 169-172 "Quantitative organic analysis via functional groups", 4th edition (John Wiley and Sons).
Пример 8: Получение гиалуроновой кислоты с 10% перекрестных связей
Описание продукта:
10% карбоксильных групп использовано для внутренней этерификации.
90% карбоксильных групп образуют соли с натрием.
6,21 г тетрабутиламмониевой соли ГК с молекулярным весом 170000 Дальтон, что соответствует 10 мэкв мономера, растворяют в 248 мл ДМСО при 25oC, добавляют 0,118 г (1,0 мэкв) хлорида пиридина и результирующую смесь перемешивают в течение 30 минут.
Раствор 0,16 г (мэкв) N-бензил-N-этил-карбодиимида в 20 мл ДМСО медленно добавляют по каплям в течение периода времени, равного 1 часу, и смесь выдерживают при 30oC в течение 45 часов.
Затем добавляют раствор, образованный из 100 мл воды и 2,5 г хлорида натрия, и результирующую смесь затем медленно приливают к 750 мл ацетона, обеспечивая постоянное перемешивание. Образуется преципитат, который затем фильтруют и промывают три раза 100 мл смеси ацетона с водой в соотношении 5: 1, и три раза при помощи 100 мл ацетона, и, наконец, высушивают в вакууме в течение 24 часов при 30oC.
Получают 3,9 г соединения, соответствующего заголовку примера. Количественное определение сложноэфирных групп выполняют в соответствии с методом омыления, описанным на стр. 169-172 "Quantitative organic analysis via functional groups", 4th edition (John Wiley and Sons).
3. Получение биоматериалов:
Следующие примеры описывают получение хирургических/медико-санитарных продуктов, соответствующих изобретению, которые включают полный бензиловый сложный эфир ГК или аутоперекрестно связанное производное ГК, или их комбинации. Как отмечено выше, процедуры изготовления мембран, тканых тканей, плетеных сеток и нетканых тканей описаны в патентах США N 4,851,521; N 4,965,353; международных заявках WO 93/11804; WO 93/11803; WO 94/17837 и в документе ЕР 0341745.
Пример 9 - Получение продукта на основе HYAFF 11 + полипропиленовая сетка
Приготавливают раствор HYAFF 11 (100% бензилового эфира гиалуроновой кислоты) в ДМСО (110 мг/мл). После полного растворения раствор фильтруют через фильтрационную ткань с ячейками 20 мкм и дегазируют путем выдерживания в вакууме в течение 2 часов. 5 мл раствора отливают и распределяют по стеклянной пластинке, после чего сверху помещают полипропиленовую сетку (6 х 11 см), а затем поверх нее наливают 10 мл раствора. Раствор равномерно распределяют поверх сетки, и любой избыток удаляют.
Стеклянную пластинку погружают в ванну, содержащую этанол/H2O (90:10) на 5 часов, чтобы обеспечить коагуляцию препарата, а затем пластинку отделяют; затем препарат погружают в ванну с абсолютным спиртом на 16 часов. Затем его высушивают на пластинке в вакууме в течение 30 минут при 63oC.
Пример 10: Приготовление продукта на основе нетканого полотна из HYAFF 11, покрытого пленкой из HYAFF 11
Приготавливают раствор HYAFF 11 в ДМСО (110 мкг/мл). После полного растворения раствор фильтруют через фильтрационную ткань с ячейками 20 мкм и дегазируют путем выдерживания в вакууме в течение 2 часов. 5 мл раствора отливают и распределяют по стеклянной пластинке, после чего сверху помещают марлю из HYAFF 11 (10 х 20 см), стараясь обеспечить ее прилегание без каких-либо складок или пузырьков воздуха, а затем поверх нее наливают 10 мл раствора. Раствор равномерно распределяют поверх марли, и любой избыток удаляют.
Стеклянную пластинку на 30 минут погружают в ванну, содержащую этанол, чтобы обеспечить коагуляцию препарата, и пластинку отделяют. Затем препарат оставляют в этаноле на 16 часов и высушивают на пластинке в вакууме при 63oC в течение 30 минут.
Пример 11 - Мембрана из HYAFF с укреплением из HYAFF 7
Композитная мембрана, содержащая бензиловый эфир гиалуроновой кислоты HYAFF 11, т. е. гиалуроновую кислоту, на 100% этерифицированную бензиловым спиртом, с укреплением сеткой, содержащей этиловый эфир гиалуроновой кислоты HYAFF 7, т. е. гиалуроновую кислоту, на 100% этерифицированную этанолом, базисный вес 14 мг/см2, толщина 0,25 мм, предел прочности при растяжении и относительное удлинение в сухом виде не менее 400 кг/см2 и 7% соответственно, предел прочности при растяжении и относительное удлинение во влажном состоянии - 50 кг/см2 и 55% соответственно, сопротивление разрыву в сухом виде - 90 кг/см2, сопротивление разрыву во влажном виде - 50 кг/см2, была изготовлена в соответствии со следующей процедурой.
Сетку из HYAFF 7 получали, используя раствор HYAFF 7 в диметилсульфоксиде в концентрации 125 мг/мл. Раствор при помощи редукторного дозировочного насоса накачивали в многоканальную фильеру для экструзии в жидком виде, содержащую 100 отверстий, каждое с диаметром 65 мкм.
Экструдированную множественную нить помещают в ванну для коагуляции, содержащую абсолютный этанол, и затем перемещают по транспортирующим роликам в три последовательные ванны для промывки, также содержащие абсолютный этанол. Соотношение между скоростью третьего ролика (III) и скоростью первого ролика (I) называется вытяжным отношением и имеет значение 1,05, тогда как скорости отдельных роликов равны: 23 об/мин (ролик I), 24 об/мин (ролики II и III), 25 об/мин (ролик IV). Когда множественная нить пройдет через ванны для промывки, ее высушивают теплым воздухом при температуре 45oC и наматывают на рамку для намотки. Нить равна 237 denier. Множественную нить затем скручивают с периодом 135 раз на метр и сплетают на ткацком станке в гладкую трикотажную ткань класса 14. С ткацкого станка ткань пропускают через каландр, который делает ее тоньше.
На полимерную основу наносится покрытие двумя пульверизаторами, которые распыляют раствор HYAFF 11 в диметилсульфоксиде с концентрацией 40 мг/мл.
Сетку с таким напылением помещают в ванну для коагуляции, содержащую абсолютный спирт, в камеру для промывки, содержащую чистую дистиллированную воду, и в специальную сушильную камеру с температурой 50oC.
Пример 12 - Нетканое полотно, содержащее HYAFF 11
Нетканое полотно, содержащее бензиловый эфир гиалуроновой кислоты HYAFF 11 с плотностью 40 г/м2 и толщиной 0,5 мм, получали путем следующей процедуры.
Раствор HYAFF 11 в диметилсульфоксиде с концентрацией 135 мг/мл приготавливали в баке и подавали при помощи редукторного дозировочного насоса в многоканальную фильеру для экструзии в жидком виде, содержащую 3000 отверстий, каждое с диаметром 65 мкм.
Экструдированную множественную нить помещают в ванну для коагуляции, содержащую абсолютный этанол. Затем ее перемещают по транспортирующим роликам в две последовательные ванны для промывки, содержащие абсолютный этанол. Вытяжное соотношение первого ролика устанавливается равным нулю, тогда как тяговое соотношение между другими роликами устанавливается равным 1,05. После того, как масса пройдет через ванны для промывки, моток нитей высушивают горячим воздухом при 45-50oC и разрезают роликовым ножом на волокна размером 40 мм.
Массу волокон, полученную таким образом, насыпают в жолоб, ведущий к кардочесальной/поперечно-трепальной машине, из которой она выходит в виде полотна, толщиной 1 мм и плотностью 40 мг/м2. Полотно затем опрыскивают раствором HYAFF 11 в диметилсульфоксиде с концентрацией 80 мг/мл, помещают в ванну для коагуляции в этаноле, в камеру для промывки и, наконец, в сушильную камеру.
Окончательная толщина материала равна 0,5 мм.
Пример 13 - Нетканое полотно, содержащее HYAFF 11 и HYAFF 7
Нетканое полотно с плотностью 200 г/м2 и толщиной 1,5 мм, содержащее смесь этилового эфира гиалуроновой кислоты, HYAFF 7, и бензилового эфира гиалуроновой кислоты, HYAFF 11, в равных количествах, получали путем следующей процедуры.
Волокна HYAFF 7 и HYAFF 11 длиной 3 м, полученные в процессе прядения, описанном в примере 10, тщательно перемешивали в спиральной мешалке. Смесь волокон подавали в кардочесальную машину, из которой она выходила в виде полотна толщиной 1,8 мм, плотностью 200 г/м2.
Полотно пропускали через машину для пробивания отверстий иглами, которая трансформировала его в нетканое полотно толщиной 1,5 мм, плотностью 200 г/м2, в котором два исходных материала были полностью перемешаны друг с другом.
Пример 14 - Нетканое полотно из частичного и полного бензилового эфира
Нетканое полотно с плотностью 40 г/м2 и толщиной 0,5 мм, содержащее смесь бензилового эфира гиалуроновой кислоты, HYAFF 11, и частичного (75%) бензилового эфира гиалуроновой кислоты, HYAFF 11p75, в равных процентных соотношениях, было изготовлено путем следующей процедуры.
HYAFF 11p75 приготавливали следующим образом. 10 г тетрабутиламмониевой соли гиалуроновой кислоты, м. в. = 620,76 Дальтон, что эквивалентно 16,1 нмоль, растворяли в смеси N- метилпирролидона/H2O, 90/10, 2,5% по весу, чтобы получить 400 мл раствора. Раствор охлаждали до 10oC, затем его продували пузырьками очищенного N2 в течение 30 минут. Этот раствор затем этерифицировали при помощи 1,49 мл (эквивалентно 12,54 ммоль) бромистого бензила. Раствор осторожно встряхивали в течение 60 часов при 15-20oC.
Последующую очистку выполняли путем преципитации в этилацетате с последующим добавлением насыщенного раствора хлорида натрия и последующими промывками смесью этилацетата/абсолютного спирта, 80/20. Твердую фазу отделяли путем фильтрации и обрабатывали безводным ацетоном. Таким образом получали 6,8 г продукта, что эквивалентно выходу, равному 95%.
Волокна HYAFF 11 и HYAFF 11p75 длиной 40 мм, полученные в процедуре, описанной в примере 1, тщательно перемешивали в спиральной мешалке.
Перемешанные волокна подавали в кардочесальную машину, из которой они выходили в виде полотна толщиной 1 мм и плотностью 40 мг/м2. Полотно затем опрыскивали раствором HYAFF 11 в диметилсульфоксиде с концентрацией 80 мг/мл, помещали в спиртовую ванну для коагуляции, затем в камеру для промывки, содержащую воду или смесь воды и этанола с содержанием этанола от 10% до 95%, и, наконец, в сушильную камеру.
Материал имел окончательную толщину 0,5 мм, и волокна HYAFF 11 и HYAFF 11p75 были полностью перемешаны и соединены друг с другом.
Пример 15 - Многослойное нетканое полотно на основе HYAFF 11
Многослойное нетканое полотно, состоящее из слоя бензилового эфира гиалуроновой кислоты, HYAFF 11, и слоя нетканой вискозы (Jettex 2005 фирмы ORSA), базисная плотность 80 г/м2, толщина 2 мм, и процент абсорбции воды 560% по весу, получали путем следующей процедуры.
Слой, который вступает в контакт с кожей, содержит волокна HYAFF 11, произведенные методом влажного прядения, и имеет форму листа весом 30 г/м2. Волокна были сформованы в листы.
Этот слой присоединяется путем сшивания ко второму слою нетканой вискозы с базисной плотностью 30 г/м2.
Конечное нетканое полотно, таким образом, содержит два исключительно плотно соединенных слоя с общей базисной плотностью 80 г/м2, толщиной 2 мм и процентом абсорбции воды, равным 560% по весу.
Пример 16 - Многослойное нетканое полотно на основе HYAFF 11
Многослойная нетканое полотно, содержащее слой бензилового эфира гиалуроновой кислоты, HYAFF 11, и альгината кальция в соотношении 1:1, и укрепляющее нетканое полотно из полипропилена (скрученная нетканая основа, 50 г/м2 фирмы NEUBERGER) с базисной плотностью 70 г/м2, толщиной 1,5 мм и процентом абсорбции воды, равным 450% от веса, получали согласно следующей процедуре.
Волокна HYAFF 11 и альгината кальция длиной 40 мм, полученные традиционными методами влажного прядения, смешивали, превращали в слой с весом 20 г/м2 и соединяли путем сшивания со штапельным нетканым полотном с базисным весом 50 г/м2.
Результирующий материал содержит два слоя нетканого полотна с общей базисной плотностью 70 г/м2, толщиной 1,5 мм и процентом абсорбции воды, равным 450% от веса.
Пример 17 - Многослойное нетканое полотно на основе HYAFF 11
Многослойное нетканое полотно, содержащее слой бензилового эфира гиалуроновой кислоты HYAFF 11 и слой полиуретановой губки, такой, как LYOBEND (фирмы DELCON) с базисной плотностью 100 г/м2, толщиной 6 мм и процентом абсорбции воды, равным 860% от веса, было получено путем следующей процедуры.
Слой, который вступает в контакт с кожей, содержит волокна HYAFF 11, полученные по методу влажного прядения и превращенные в полотно с плотностью 45 г/м2, которое путем сшивания соединяют со вторым слоем полиуретановой губки.
Результирующий нетканый продукт содержит два исключительно плотно соединенных слоя с общей базисной плотностью 100 г/м2, толщиной 6 мм и процентом абсорбции воды, равным 860% от веса.
Пример 18 - Получение мембраны, изготовленной из производного гиалуроновой кислоты с 80% карбоксильных функциональных групп, этерифицированных бензиловым спиртом (C6H5 - CH2-ОН), 10% карбоксильных функциональных групп, участвующих в образовании внутренних сложноэфирных связей, и оставшимися 10%, образующими соли с натрием
6,21 г тетрабутиламмониевой соли гиалуроновой кислоты с молекулярным весом 180000 Дальтон (10 мэкв) растворяли в 248 мл диметилсульфоксида (ДМСО) при температуре окружающей среды. К этому раствору добавляли 0,951 мл бензилбромида (8,0 мэкв), и раствор оставляли стоять в течение 12 часов при 30oC. Добавляли 0,101 г триэтиламина (1,0 мэкв), и раствор перемешивали в течение 30 минут. Добавляли раствор 0,255 г (1,0 мэкв) иодида 2-хлоро-1- метил-пиридина в 60 мл ДМСО, и смесь оставляли стоять 15 часов при 30oC.
Добавляли 2,5% раствор (вес/объем) NaCl в воде, и результирующую смесь вливали в 750 мл ацетона при перемешивании. Образуется преципитат, который фильтруют и промывают три раза в 100 мл ацетона/воды 5:1, три раза - 100 миллилитрами ацетона, и в конце высушивают под вакуумом в течение 24 часов при 30oC. Таким образом получают 4,5 г желаемого продукта. Количественное определение содержания бензилового спирта выполняют при помощи газовой хроматографии с последующим щелочным гидролизом. Общее содержание сложноэфирных групп измеряют по методу омыления, описанному на стр. 169-172 "Quantitative organic analysis via functional groups" 4th edition (John Wiley and Sons).
Полученное таким образом сложноэфирное производное растворяют до концентрации 150 мг/мл в ДМСО при температуре 30oC. Растворенное производное фильтруют через сетку размером 20 мкм и помещают в экструзионный реактор, соединенный с экструдером пленки толщиной < 1 мм. Продукт экструдируют в ванну для коагуляции, содержащую растворитель, который позволяет экстрагировать ДМСО из продукта (например, этанол), и материал из пленочного экструдера наматывают на ряд роликов, оборудованных воздушными фенами для просушивания мембраны.
ПРЕКЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ
Нижеследующие исследования демонстрируют результаты, которые показывают полезность продуктов согласно настоящему изобретению для предотвращения послеоперационных спаек, и которые превосходят результаты для таких продуктов, полученных ранее существовавшими продуктами.
Исследование 1
Это исследование демонстрирует высокую частоту встречаемости образования хирургических спаек, наблюдавшуюся на модели повреждения, созданного в печени крысы, выбранной в качестве положительного контроля для сравнения профилактического действия медико-санитарных и хирургических средств, полученных из ГК, относительно образования спаек.
Для этих экспериментов были использованы крысы линии Sprague Dawley, с весом между 275 и 300 г. 21 животное было подвергнуто повреждениям.
Каждое животное было подвергнуто лапаротомии путем рассечения брюшной полости после анестезии раствором Кетамина (100 мг/кг) и Ксилазина (11 мг/кг), приготовленного в стерильных условиях и инъецированного внутримышечным путем.
Печень находили и открывали; на нижней доле производили скарификацию, прикладывая небольшое давление стерильным тампоном до тех пор, пока не появлялась кровь. После остановки кровотечения с поврежденной поверхности лапаротомию закрывали швом из шелковой нити размера 3,0. Животных умерщвляли через 7-21 день.
Спайку оценивали по легкости, с которой прилегающие поверхности (верхняя и нижняя) доли можно было отделить хирургическим пинцетом, на основании следующей шкалы:
0 - нет спайки - две поверхности можно разделить;
1 - слабая - умеренная спайка, поверхности можно разделить, раздвигая их пинцетом;
2 - выраженная спайка между двумя поверхностями, любая попытка отделить их приводит к разрыву тканей.
На этой модели на животных спайки, которые оценивались 2 баллами, были признаны клинически значимыми.
В этой положительной контрольной группе (с образованием спаек) 17 животных из 21 (80,9%) обнаружили образование спаек с оценкой 2.
Исследование 2
Это исследование иллюстрирует достоверное снижение образования спаек, если используется гель, изготовленный из перекрестно связанной гиалуроновой кислоты (ACP), или марля на основе HYAFF 11 (бензиловый эфир ГК) используется отдельно или в комбинации с гемостатиком SurgicelTM и Гепарином 50 EA/мл. Гель ACP распыляли по поверхности, подлежащей обработке.
Хирургический протокол, описанный в Примере 1, был использован в качестве модели на животном, чтобы вызвать образование спаек.
Достоверное снижение образования спаек между двумя прилегающими поверхностями левой доли печени проиллюстрировано таблицей 1.
Очевидно, что использование этих слабо биозависимых биоматериалов в качестве непроницаемого для воспалительных клеток барьера между двумя прилегающими поверхностями уменьшает образование спаек по сравнению с 80,9% спаек, наблюдавшихся в контрольной группе, описанной в Примере 1.
Исследование 3
Этот пример демонстрирует высокую частоту образования хирургических спаек, наблюдавшуюся на модели хирургического повреждения, вызываемого на брюшной стенке крысы для использования в качестве положительного контроля и для сравнения с профилактическим действием медико-санитарных средств, включающих производные ГК по настоящему изобретению (HYAFF 11 + полипропиленовая сетка), при образовании спаек.
Всего повреждению было подвергнуто 24 животных (12 контрольных, 12 опытных).
Каждое животное было подвергнуто лапаротомии путем рассечения брюшной полости после анестезии раствором Кетамина (100 мг/кг) и Ксилазина (11 мг/кг), приготовленного в стерильных условиях и инъецированного внутримышечным путем.
Лоскут с левой стороны разреза поднимали двумя хирургическими пинцетами, чтобы обнажить брюшную стенку. Область поверхности брюшины размером 1,5 х 1,5 см удаляли хирургическими ножницами, пока не появлялся эксудат, без удаления мышечной связки. В контрольной группе было необходимо пришить полипропиленовую сетку (по размеру в два раза больше области повреждения) швом из биоабсорбируемого материала Vycil размера 6,0 поверх травмированной поверхности, чтобы гарантировать сопротивление брюшной стенки растяжению. Перед аппликацией материала поврежденную поверхность нужно было подвергнуть полному гемостазу.
После умерщвления через 14 дней, среднее время диапазона, приведенного в Примере 1, спайки оценивали по следующей шкале:
0 - отсутствие спайки;
1 - слабая спайка без васкуляризации, легко может быть разделена;
2 - умеренная спайка без васкуляризации, может быть разорвана вручную;
3 - плотная спайка, непрозрачная и васкуляризованная, трудно отделить, необходимо использование скальпеля;
4 - очень плотная спайка, толстая, непрозрачная и васкуляризованная, может быть удалена только с помощью хирургических ножниц с результирующей деструкцией тканей.
Спайки с оценкой > 2 были признаны значимыми.
В позитивной контрольной группе (образование спаек) 12 животных из 12 (100%) обнаружили образование спаек с оценкой > 2; тогда как достоверное снижение частоты образования спаек между брюшной стенкой и внутренними органами происходило, если использовали продукт в соответствии с нестоящим изобретением, как показано в таблице 2.
Очевидно, что использование вышеуказанного материала из HYAFF 11, являющегося предметом изобретения, в качестве барьера (непроницаемого для воспалительных клеток) между поврежденной внутренней поверхностью (брюшная стенка) и прилежащими органами снижает образование спаек по сравнению со 100% спаек в контрольной группе, где использовали только полипропиленовую сетку.
Исследование 4
Это исследование иллюстрирует возможности перекрестно связанной гиалуроновой кислоты (ACP) в форме геля, используемого в качестве покрытия для уменьшения образования хирургических спаек, на модели повреждения, создаваемого в слепой кишке крысы.
Этот тип повреждения вызывает образование спаек при лечении после хирургической операции только промыванием солевым раствором и гемостазом, как сообщается ниже.
Как и в Исследовании 1, были использованы крысы Sprague Dawley весом 275-300 г. Каждое животное было подвергнуто лапаротомии путем рассечения брюшной полости после анестезии раствором Кетамина (100 мг/кг) и Ксилазина (11 мг/кг), приготовленного в стерильных условиях и инъецированного внутримышечным путем. Слепую кишку находили и открывали. На поверхности кишки создавали термическое повреждение твердым телом с использованием медного диска диаметром 1 см, соединенного с паяльным устройством, настроенным при помощи электроники на 69,5oC. Его оставляли в контакте с поверхностью кишки на 15 с. Таким образом вызывали хорошо очерченное повреждение с эксудатом. После промывания поврежденной области солевым раствором и осуществления гемостаза при помощи SurgicelTM лапаротомию закрывали швом из шелка размера 3,0.
После умерщвления через 14 дней, среднее время диапазона, приведенного в Исследовании 1, спайки оценивали по следующей шкале:
0 - отсутствие спайки;
1 - слабая спайка без васкуляризации, легко может быть разделена;
2 - умеренная спайка без васкуляризации, может быть разорвана вручную;
3 - плотная спайка, непрозрачная и васкуляризованная, трудно отделить, необходимо использование скальпеля;
4 - очень плотная спайка, толстая, непрозрачная и васкуляризованная, может быть удалена только с помощью хирургических ножниц с результирующей деструкцией тканей.
На этой модели на животных спайки с оценкой > 2 были признаны значимыми.
Существует явное снижение образования спаек, если ACP гель используется в качестве барьера, по сравнению с контрольными животными, которых лечили только промыванием солевым раствором и гемостазом (таблица 3).
Очевидно, что использование вышеуказанного материала в качестве барьера снижает образование спаек по сравнению с контрольным лечением, состоявшим только в промывании солевым раствором и гемостазе.
Исследование 5 - Эффект производных гиалуроновой кислоты HYAFF-7 и HYAFF 11p75 в предотвращении послеоперационных спаек на модели повреждения печени у крыс
Модель на животных
Самцы крыс Harlan SD весом 250 г.
Тип повреждения:
Область брюха тщательно промывали раствором иода, затем для обнажения печени выполняли лапаротомию примерно на 3 см. Нижнюю правую долю печени повреждали путем трения и повреждения, наносимого стерильным деревянным шпателем до тех пор, пока не выступала кровь.
Тестируемые материалы:
Эксперимент 1: HYAFF 11p75, 75% частичный бензиловый эфир гиалуроновой кислоты в форме марли и нетканого полотна.
Эксперимент 2: HYAFF 7, полный этиловый эфир гиалуроновой кислоты в форме марли и нетканого полотна.
Аппликация материала: после тщательного гемостаза при помощи обычных гемостатиков тестовые и контрольные материалы помещали между нижней (область повреждения) и верхней долями печени (прилежащие поверхности) без использования швов, чтобы таким образом создать барьерный эффект и предотвратить образование спаек.
Оценки и наблюдения:
Наблюдения производили между седьмым и двадцать первым днем после хирургической операции. Спайки, которые образовались, были оценены на основании следующей визуальной шкалы:
0 - отсутствие спаек;
1 - слабые спайки;
2 - заметное присутствие спаек.
Кроме оценки спайки в баллах, оценивали уровень воспаления при микроскопическом наблюдении (реакция ткани на аппликацию материала), окрашивая гистологический образец гематоксилином/эозином и тройной краской по Меллори.
Результаты:
Эксперимент 1:
В Эксперименте 1 материалы на основе HYAFF 11p75, частичного бензилового эфира гиалуроновой кислоты, тестировали отдельно, в комбинации с гемостатиком SurgicelTM и в комбинации с гемостатиком плюс насыщение гепарином (1,000 ед/мл). Эти процедуры являются обычными в хирургической практике.
Фиг. 1 является графиком, изображающим влияние биоматериалов, если они использовались отдельно. Не было обнаружено эффекта предотвращения спаек в случае биоматериалов на основе HYAFF 11p75 и Interceed, и даже, если казалось, что существует тенденция к улучшению, достоверных различий не было, в последнем случае, доли печени были полностью спаянными и можно было наблюдать выраженную воспалительную реакцию. То же самое наблюдалось при гистологическом исследовании биопсий, где можно было видеть очевидное присутствие воспалительных клеток, нейтрофилов и макрофагов, а также зрелых коллагеновых волокон.
На фиг. 2 и 3 показаны результаты в случае, когда материалы были использованы в комбинации с SurgicelTM и SurgicelTM + гепарин. Тенденция, наблюдавшаяся на фиг. 1, была подтверждена при использовании материалов на основе HYAFF 11p75. При этом представляется, что Interceed, насыщенный гепарином, давал лучшие эффекты. Эта ситуация была подтверждена гистологическими наблюдениями.
Итак, материалы на основе HYAFF 11p75 не могут быть использованы для предотвращения послеоперационных спаек, так как воспалительный эффект, по-видимому, вызван выделением низкомолекулярных олигомеров гиалуроновой кислоты, принимая во внимание экстремально короткие периоды деградации продуктов.
Эксперимент 2
В Эксперименте 2 биоматериалы на основе HYAFF 7, этилового эфира гиалуроновой кислоты, были тестированы в комбинации с Surgicel и Surgicel + гепарин. Ни в одном случае не наблюдали эффекта предотвращения послеоперационных спаек. Представляется, что Interceed, использованный с Surgicel + гепарин, давал более позитивный эффект (фиг. 4).
Микроскопическое наблюдение подтвердило эти данные и выявило значительное количество воспалительных клеток и коллагеновых волокон в случае лечения HYAFF 7. В этом случае, как и в последнем из упомянутых, биоматериалы на основе HYAFF 7 не могут использоваться для предотвращения послеоперационных спаек, так как существует вероятность, что есть прогрессивное выделение этанола в организм.
Исследование 6 - Эффективность биоматериалов на основе HYAFF 11 по предотвращению послеоперационных спаек на двух различных моделях повреждений, вызываемых у животных: 1) интрапеченочная скарификация у крысы: 2) повреждения брюшной стенки у крысы
Модель на животных 1
После того, как область брюха была продезинфицирована иодом и этанолом, выполняли срединный разрез, чтобы обнажить печень.
В этой модели на животных внутреннюю поверхность нижней доли печени соскабливали до тех пор, пока не начинал выделяться эксудат. Место эрозии подвергалось тщательному гемостазису при помощи Tambotamp (Ethicon), и материал оставляли на поврежденной поверхности без наложения швов в связи с высокими мукоадгезивными характеристиками продукта.
Были тестированы два продукта на основе HYAFF 11, оба варианта имеющихся в продаже непрерывных мембран толщиной 20 мкм, называемые Transprocess и Hyalobarrier 20. Макроскопическая оценка была выполнена через 14 дней после операции с использованием системы баллов, описанной выше, для оценки спаек. Далее была выполнена оценка процента животных с оценкой спаек = 2 (достоверные спайки).
Результаты
Фиг. 5 является графическим представлением оценок спаек, полученных в эксперименте. Hyalobarrier 20 снижает частоту образования спаек по сравнению с контролями, не получавшими лечения, и с двумя видами лечения низко- и высокомолекулярной гиалуроновой кислотой. В случае другого материала на основе HYAFF 11, Transprocess, была отмечена сходная тенденция, но без статистически достоверных отличий. Фиг. 6 показывает проценты случаев спаек с оценкой = 2 в каждой группе лечения (хирургически достоверная спайка). Тенденция, выявленная на предыдущем графике (фиг. 1), была подтверждена и в этом случае уменьшением спаек с оценкой =2 (процент менее 50% для лечения при помощи Hyalobarrier 20 и Transprocess).
Модель на животных 2
После того, как область брюха была продезинфицирована иодом и этанолом, выполняли срединную лапаротомию длиной примерно 5 см, чтобы обнажить брюшную стенку и брюшину.
При помощи скальпеля был выполнен разрез размером 2 см х 2 см, а затем брюшину и мышечный слой удаляли. В этом типе операции необходимо пришивать к поврежденной области материал, который способствует росту ткани, чтобы гарантировать адекватное напряжение растяжения и предотвратить коллапс перитонеальной стенки. В основном, используются не разрушаемые материалы с полимерной основой, такие, как сетки из полипропилена, полиэфира или растянутого политетрафторэтилена. Использования таких материалов самих по себе, однако, не достаточно, чтобы избежать образования спаек с петлями кишечника с последующей обструкцией кишки и хронической болью.
Макроскопические оценки были выполнены через 14 дней после операции с применением оценок в баллах, идущих от 0 до 4. Далее была произведена оценка процента животных с оценкой спайки > 2 (достоверные спайки).
Результаты:
Этот эксперимент демонстрирует, что покрытие из HYAFF 11 на синтетической сетке из Prolene (полипропиленовая сетка, широко используемая в абдоминальной хирургии) и слой HYAFF 11 на сетке из Prolene, прикрепленные при помощи швов, могут снижать образование послеоперационных спаек. Фиг. 7 показывает, что комбинированный продукт, названный Hyalobarrier Plus (распыленный и коагулированный HYAFF 11 на пролене), и пленка из Hyalobarrier, пришитая к пролену, достоверно снижают спайки по сравнению с одной проленовой сеткой. Фиг. 8 подтверждает эту тенденцию низким процентом спаек с оценкой > 2 (достоверные спайки) вследствие лечения при помощи HYAFF 11 по сравнению с наблюдавшимся после использования одной проленовой сетки.
Исследование 7 - Эффекты биоматериалов из ACP- геля на предотвращение образования послеоперационных спаек через 14 дней на модели повреждения печени крысы и на модели повреждения кишечника крысы
Целью данного исследования было оценить эффективность биоматериалов на основе ACP-геля для снижения или предотвращения образования послеоперационных спаек. Влияние тестируемых материалов оценивали по сравнению с высокомолекулярной гиалуроновой кислотой и с биоматериалами, имеющимися в продаже, окисленной регенерированной целлюлозой (TC 7 Interceed*), используемыми в тазовоабдоминальной и гинекологической хирургии для предотвращения образования спаек.
Были использованы модель повреждения печени крысы и модель ожога кишечника крысы, так как они являются охарактеризованными моделями индукции экспериментальных спаек. Эффекты тестовых и контрольных материалов на предотвращение послеоперационных спаек оценивали при макроскопическом наблюдении места повреждения с использованием оценки спаек.
Модель повреждения печени у крыс (Эксперимент 1) и модель повреждения кишечника у крыс (Эксперимент 2) были использованы, так как они являются стандартизованными и воспроизводимыми моделями экспериментальной индукции спаек. Биоматериалы на основе ACP использовали после повреждения в качестве барьера между прилегающими поверхностями доли печени и внутренних органов.
В обоих экспериментах оценивалась эффективность ACP-гелей по их способности предотвращать или снижать образование спаек по сравнению с TC7 Interceed, абсорбируемым барьером адгезии из окисленной целлюлозы, широко используемым в клинической практике, раствором сополимеров "Thermogel", раствором высокомолекулярной гиалуроновой кислоты и группой не получавших лечения животных (ложно оперированных).
Исходные данные:
Эксперимент 1 - Скарификация печени крысы (см. табл. 4).
Гели ACP суспендировали в воде при концентрации 60 мг/мл. Тестируемые материалы приобретали стерилизованными в автоклаве и в шприце объемом 5 мл и манипулировали ими в стерильных условиях. ACP-гели апплицировали в качестве покрытия скарифицированных поверхностей доли печени после гемостаза при помощи Tambotamp®. Каждое животное получало количество, достаточное для того, чтобы полностью покрыть поврежденную зону (около 2 мл) при однократном введении во время операции (см. табл. 5).
Interceed разрезали при стерильных условиях, его использовали отдельно и насыщали в Гепарине (500 Ед/мл), затем апплицировали так, чтобы разделять две прилегающие поверхности долей печени на расстоянии, превышающем границы поврежденной зоны на несколько мм. HYAL, гиалуроновую кислоту с высоким молекулярным весом (растворенную в воде в концентрации 10 мг/мл) и Thermogel приобретали в стерильном шприце.
Interceed апплицировали путем непосредственной аппликации без хирургического шва. HYAL, гиалуроновую кислоту и Thermogel апплицировали на поврежденную поверхность (покрытие) при помощи шприца после гемостаза. Каждое животное получало количество, достаточное для того, чтобы полностью покрыть или закрыть поврежденную поверхность при однократном применении во время операции.
ПЛАН ЭКСПЕРИМЕНТА
Для этого эксперимента были использованы крысы Sprague Dawley (275-300 г). На основании опыта, полученного из предыдущих экспериментов, период, равный 14 дням, был признан адекватным моментом времени для оценки образования спаек в этой модели на животных. Исходя из количества животных, необходимых для данного исследования, животных подготавливали в следующие друг за другом дни.
Было использовано в общей сложности 78 животных в соответствии со следующей схемой (см. табл. 6).
Подготовка животных:
Животных наркотизировали внутримышечной инъекцией Кетамина (Gellini Pharmaceutical)/Ксилазина (Bayer), брили и затем дезинфицировали раствором иода и этанолом. После лапаротомии на левом боку левую долю печени отгибали вверх и внутренние поверхности левой и медиальной долей печени скарифицировали путем осторожного трения деревянным аппликатором до тех пор, пока не получали проявлений кровотечения или серозного эксудата.
Применение материалов:
После гемостаза, производимого при помощи Surgicel® или TabotampTM, тестируемые и контрольные материалы размещали между поверхностями двух долей так, чтобы покрыть всю скарифицированную область и создать барьер между долями.
Место операции закрывали швами из шелка размера 3,0 в два слоя.
После конца хирургической операции в течение 4 дней вводили антибиотик (Прокациллин подкожно 30000 МЕ/крысу) и анальгетик (Темгезик, в/мыш, 0,05 мг/кг).
Оценка спаек:
Через 14 дней после операции животных умерщвляли при помощи CO2.
Уровень спайки оценивали путем макроскопического наблюдения. Использовали следующую оценку спаек:
0 = Нет спайки.
1 = Спайка от слабой до умеренной. Две доли печени разделяли хирургически путем механического растяжения при помощи пинцета.
2 = Явная спайка, две доли печени были полностью соединены, любая попытка отделения вызывала разрыв ткани.
Способность материалов к рассасыванию оценивали при помощи визуальной оценки присутствия материалов; далее, место воздействия фотографировали.
После того, как были выполнены макроскопические наблюдения, печень полностью удаляли хирургическим путем и помещали в 10% формалин с буферным раствором на 48 часов. После фиксации из печени удаляли при помощи рассекающего скальпеля поперечный срез толщиной 2 мм, включающий скарифицированную область. Полученные таким образом образцы подвергали гистологическому анализу.
Анализ ткани:
Гистологический анализ:
Образцы фиксировали в нейтральном 10% формалине, содержащем буферный раствор, а затем дегидратировали и заливали в парафин по стандартным методикам; срезы толщиной 8 мкм окрашивали Masson's Trichnome (на воспалительную реакцию ткани) и, при необходимости, Толуидиновым синим (на присутствие остатков материала).
Эксперимент 2 - Ожог кишечника крысы (см. табл. 7).
5% гели ACP с высоким м.в. партии 3/94 суспендировали в воде при концентрации 20 мг/мл, ACP 5% партии 101/94 суспендировали при концентрации 50 мг/мл. Все тестируемые материалы поставлялись стерилизованными при помощи автоклава и в 5 мл шприце, и ими манипулировали в стерильных условиях. ACP гели наносились так, чтобы покрыть обожженные поверхности кишечника после гемостаза при помощи Tambotamp®. Каждое животное получало количество, достаточное для того, чтобы полностью покрыть поврежденную область (около 2 мл) при введении одной дозы во время хирургической операции (см. табл. 8)
Interceed разрезали при стерильных условиях, его использовали отдельно и насыщали в Гепарине (500 Ед/мл), затем апплицировали так, чтобы разделять две прилегающие поверхности долей печени, на площади, превышающей края поврежденной области на несколько мм. HYAL, гиалуроновую кислоту с высоким молекулярным весом (растворенную в воде при концентрации 10 мг/мл) и Thermogel покупали в стерильном шприце.
Interceed апплицировали путем непосредственной аппликации без хирургического шва. Гиалуроновую кислоту и Thermogel апплицировали на поврежденную поверхность (покрытие) при помощи шприца после гемостаза. Каждое животное получало количество, достаточное для того, чтобы полностью покрыть или закрыть поврежденную поверхность при однократном применении во время операции.
ПЛАН ЭКСПЕРИМЕНТА
Для этого эксперимента были использованы крысы Sprague Dawley (275-300 г). На основании опыта, полученного из предыдущих экспериментов, период, равный 14 дням, был признан адекватным моментом времени для оценки образования спаек в этой модели на животных.
Исходя из количества животных, необходимых для данного исследования, животных подготавливали в следующие друг за другом дни.
Было использовано в общей сложности 59 животных в соответствии со следующей схемой (см. табл. 9).
Подготовка животных:
Животных наркотизировали внутримышечной инъекцией Кетамина (Gellini Pharmaceutical)/Ксилазина (Bayer), брили и затем дезинфицировали раствором иода и этанолом. Через кожу и мышечную ткань выполняли разрез брюшной стенки по средней линии так, чтобы обнажить кишечник. Ожог производили путем прикладывания к поверхности слепой кишки медного диска (диаметром 1 см) с электронной регулировкой нагрева при использовании стандартного давления на 15 с при 69,3oC.
Использование материалов:
После гемостаза, производимого при помощи Surgicel® или TabotampTM, тестируемые и контрольные материалы помещали на поверхность кишечника без шва так, чтобы покрыть всю обожженную область и создать барьер между брюшиной и внутренними органами.
Мышечно-брюшинный слой зашивали непрерывными швами из шелка размера 3-0, слой кожи кожными скобками и непрерывным швом из шелка размера 3-0.
После конца хирургической операции в течение 4 дней вводили антибиотик (Прокациллин подкожно 30000 ME/крысу) и анальгетик (Темгезик, в/мыш, 0,05 мг/кг). Наблюдения и определения
Оценка спаек:
Через 14 дней после операции животных умерщвляли при помощи CO2.
Уровень спаек оценивали при макроскопическом наблюдении. Использовали следующую оценку спаек:
0 = Нет спайки.
1 = Низкие, не васкуляризованные, легко рассекаемые.
2 = Умеренные, не васкуляризованные, непрерывные, рассекаемые вручную.
3 = Непрозрачные, васкуляризованные, трудно рассекаемые, необходимо разделение скальпелем.
4 = Плотные, непрозрачные, васкуляризованные, рассекаемые только хирургическими ножницами и с повреждением ткани.
Способность материалов к рассасыванию оценивали при помощи визуальной оценки присутствия материалов; далее, место воздействия фотографировали.
Результаты
Эксперимент 1
Одно животное погибло во время проведения анестезии, размещение биоматериалов было легко выполнено. Было отмечено, что биоматериалы прочно присоединились к ткани нижней доли печени. После хирургической операции не отмечалось клинических признаков заболевания или страданий у животных, которые были обработаны ACP.
Два животных, обработанных гиалуроновой кислотой, погибли через два дня после хирургической операции. Некроскопическое исследование показало внутренние кровотечения.
Оценка образования спаек: Спайки, образовавшиеся между двумя прилежащими поверхностями доли печени в результате повреждения тканей, оценивали через 14 дней. Все материалы деградировали ко времени наблюдения; оценка спаек (фиг. 9) у животных, обрабатывавшихся биоматериалом ACP 5% (серия 104/96), была значительно ниже, чем у всех контрольных материалов и необработанных контрольных животных. При обработке 5% ACP (серия 101/96) снижение спаек было выше, чем у TC7 Interceed, насыщенного гепарином, но не отмечалось статистически достоверных различий, тем не менее, оба вида обработки обнаружили достоверные различия (p < 0,05) по сравнению с контрольными и необработанными животными.
Гистоморфологическое наблюдение: При микроскопическом исследовании на 14 день после хирургической операции было обнаружено, что материалы из ACP были в высокой степени биосовместимы и наблюдалась очень низкая воспалительная реакция, в частности, присутствовало мало воспалительных клеток, таких как нейтрофилы и гигантские клетки, не отмечалось миграции или увеличения количества этих клеток внутри щели между двумя долями, TC7 Interseed* обнаружил реакцию ткани, вследствие которой во многих случаях поверхности печени были частично соединенными; микроскопическое исследование доказало присутствие организованных коллагеновых фибрилл, воспалительная реакция казалась сниженной, если этот материал насыщали раствором гепарина. В большинстве срезов биоматериалы представлялись полностью биодеградированными. Необработанные контрольные животные дали умеренную или высокую воспалительную реакцию.
Эксперимент 2
В общей сложности 2 животных погибли во время проведения анестезии, размещение биоматериалов было выполнено легко, и они не сдвигались после размещения. После хирургической операции не было отмечено клинических признаков заболевания или страданий животных в группе, где был использован ACP.
Четверо животных, обработанных гиалуроновой кислотой с молекулярным весом 1,2•106 Дальтон, и трое животных с Thermogel погибли между вторым и пятым днями после хирургической операции. Некроскопическое исследование обнаружило у всех животных внутренние кровотечения.
Оценка образования спаек: В этом эксперименте через 14 дней после хирургической операции (фиг. 10), ACP 5%-гели 101/94 и 3/94 обнаружили снижение образования послеоперационных спаек по сравнению с гиалуроновой кислотой с молекулярным весом 1,2•106 Дальтон и необработанными контрольными животными, влияние ACP-гелей было сопоставимо с влиянием Interseed Barrier, насыщенного гепарином, статистическое различие было обнаружено между этими воздействиями и необработанными контрольными группами (p < 0,05); все лечебные и контрольные материалы были полностью абсорбированы.
Гистоморфологическое наблюдение: при микроскопическом наблюдении через 14 дней после обработки ACP была обнаружена низкая воспалительная реакция ткани, толщина грануляционной ткани была очень малой, и не отмечалось неблагоприятной реакции на кишечнике, а также спайки с прилежащей поверхностью брюшины. Коллагеновые фибриллы начинали организовываться, и процесс заживления был завершен. При обработке гиалуроновой кислотой наблюдали воспалительную реакцию со значительным присутствием коллагеновых волокон, которые индуцируют спайку; была видна толстая грануляционная ткань. Те же гистоморфологические проявления были отмечены у необработанных контрольных животных.
Обсуждение
Образование спаек находится среди ведущих причин послеоперационной смертности при операциях на органах брюшной полости и таза, часто приводя к непроходимости тонкого кишечника и другим важным патологиям. Когда в процесс вовлечены внутренние органы таза, эти спайки обладают потенциальной возможностью нарушать физиологическую функцию и приводить к бесплодию. Механизм образования и преобразования послеоперационных спаек остается недостаточно ясным. Экспериментальные данные наводят на мысль, что спайки образуются между двумя хирургически травмированными поверхностями при естественном соприкосновении в ходе процесса заживления, поскольку более эффективным является объединение двух участков повреждения ткани в единую зону заживления, что приводит к соединительным спайкам между двумя прилегающими поверхностями.
В этом скрининге было обнаружено, что использование традиционного хирургического гемостатического агента Surgicel®) после хирургической операции и последующее размещение барьера из биодеградируемых производных гиалуроновой кислоты предотвращает образование спаек. Кроме того, материалы могут быть использованы в соединении с фибринолитическими агентами. Снижение спаек превосходило аналогичный эффект окисленной регенерированной целлюлозы TC 7 Interceed*.
Биоматериалы из HYAFF® 11 обнаружили хорошую биосовместимость и обеспечивали очень низкое воспаление. Скорость деградации исследованных FAB-биоматерилов была различной и зависела от различной физической формы лечения; биоматериалы из HYAFF® 11 существовали в организме несколько недель. Диапазон контролируемых скоростей деградации, который может быть получен для этих производных гиалуроновой кислоты, может с пользой эксплуатироваться для предотвращения послеоперационных спаек в различных анатомических зонах и способах применения, например, в гинекологической и абдоминально-тазовой областях.
Результаты доказывают, что производные гиалуроновой кислоты (марля и мембраны из HYAFF® 11) играют роль в предотвращении образования спаек после хирургической операции.
Таким образом, из описания изобретения должно быть очевидно, что оно может быть осуществлено во многих вариантах. Такие варианты не должны рассматриваться как отклонения от духа и сферы действия изобретения, и подразумевается, что все подобные модификации, которые должны быть очевидны для специалиста в данной области, охватываются нижеследующей формулой изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| БИОМАТЕРИАЛЫ, СОСТОЯЩИЕ ИЗ СУЛЬФАТИРОВАННОЙ ГИАЛУРОНОВОЙ КИСЛОТЫ И ГЕЛЛАНА, ПРИМЕНЯЕМЫЕ ДЛЯ ПРЕДОТВРАЩЕНИЯ СПАЕК В ПОЗВОНОЧНИКЕ | 2005 |
|
RU2383336C2 |
| СПОСОБ НАНЕСЕНИЯ НА ПОВЕРХНОСТЬ ПРЕДМЕТОВ ПОКРЫТИЯ НА ОСНОВЕ ГИАЛУРОНОВОЙ КИСЛОТЫ, ЕЕ ПРОИЗВОДНЫХ И ПОЛУСИНТЕТИЧЕСКИХ ПОЛИМЕРОВ | 1996 |
|
RU2173563C2 |
| КОМПОЗИЦИОННАЯ МЕМБРАНА, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СПОСОБ НАПРАВЛЕННОЙ РЕГЕНЕРАЦИИ ТКАНЕЙ С ЕЕ ПРИМЕНЕНИЕМ | 1992 |
|
RU2128057C1 |
| ВЯЗКОЭЛАСТИЧНЫЕ ГЕЛИ В КАЧЕСТВЕ НОВЫХ НАПОЛНИТЕЛЕЙ | 2010 |
|
RU2543329C2 |
| НЕТКАНЫЙ МАТЕРИАЛ, СПОСОБ ЕГО ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ | 1992 |
|
RU2133127C1 |
| ВЯЗКОЭЛАСТИЧНЫЕ ГЕЛИ В КАЧЕСТВЕ НОВЫХ НАПОЛНИТЕЛЕЙ | 2014 |
|
RU2692800C2 |
| СПОСОБ ПОЛУЧЕНИЯ МОДИФИЦИРОВАННОЙ ГИАЛУРОНОВОЙ КИСЛОТЫ | 2000 |
|
RU2191782C2 |
| ХИРУРГИЧЕСКИЕ БАРЬЕРЫ С ИНГИБИРУЮЩИМИ ОБРАЗОВАНИЕ СПАЕК СВОЙСТВАМИ | 2008 |
|
RU2480246C2 |
| СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ ПОСЛЕОПЕРАЦИОННОГО СПАЕЧНОГО ПРОЦЕССА | 2002 |
|
RU2227742C1 |
| ТАКСАНЫ, КОВАЛЕНТНО СВЯЗАННЫЕ С ГИАЛУРОНОВОЙ КИСЛОТОЙ ИЛИ ПРОИЗВОДНЫМИ ГИАЛУРОНОВОЙ КИСЛОТЫ | 2003 |
|
RU2384593C2 |
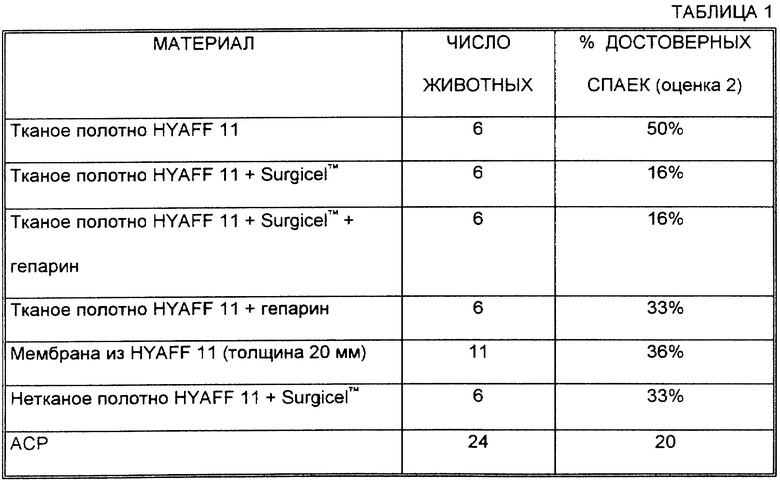
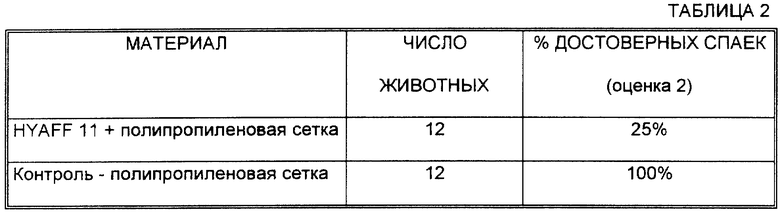
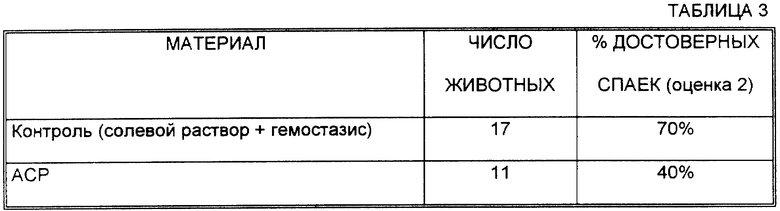

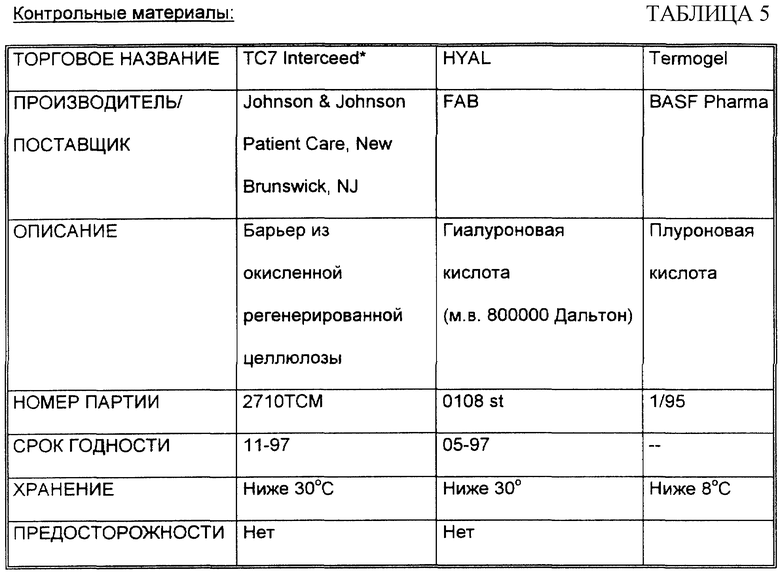
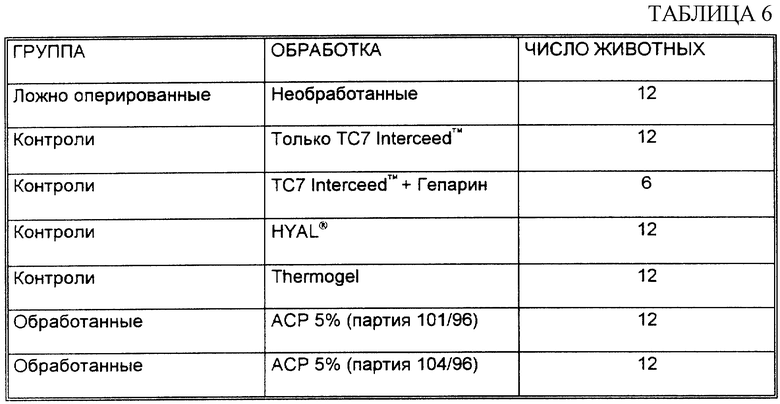
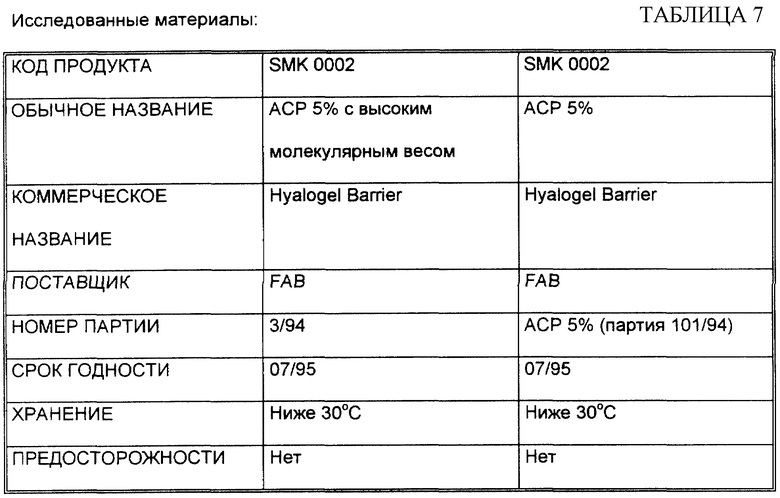
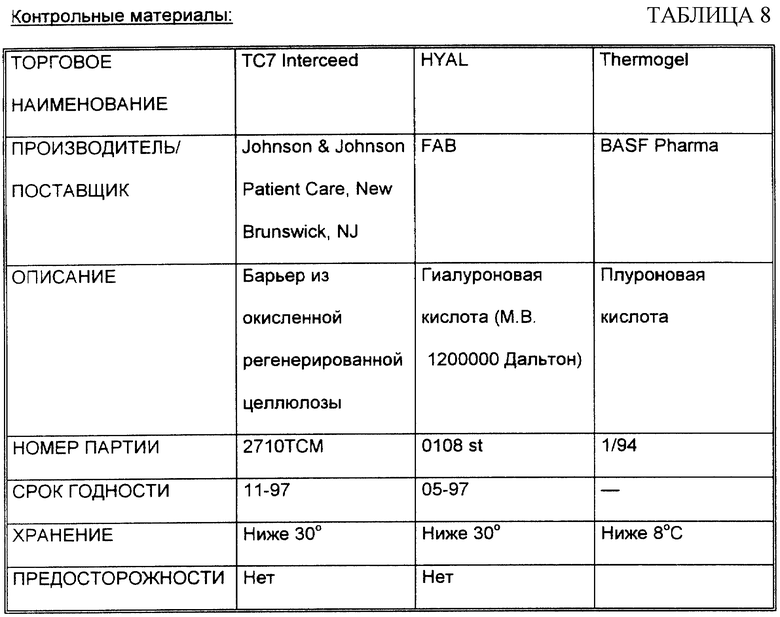
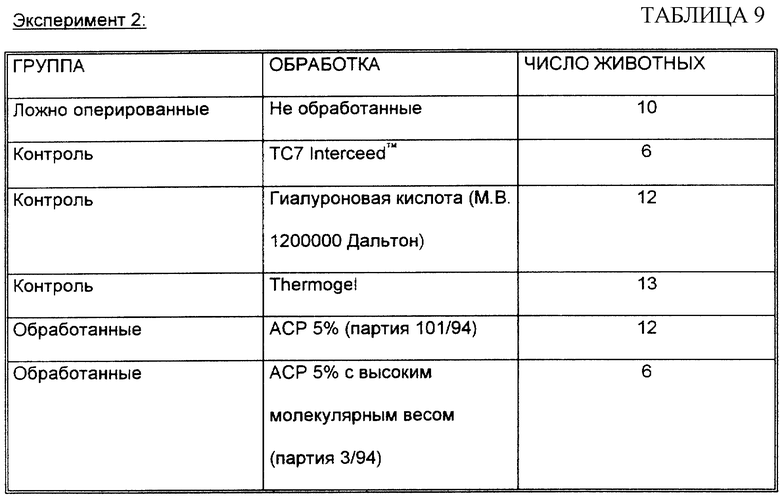
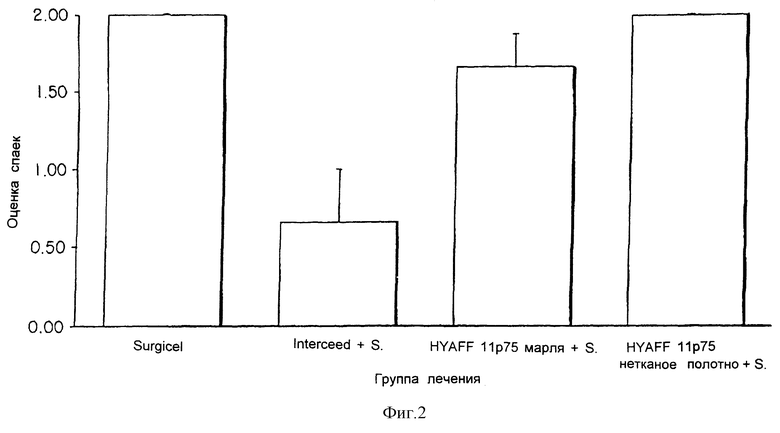
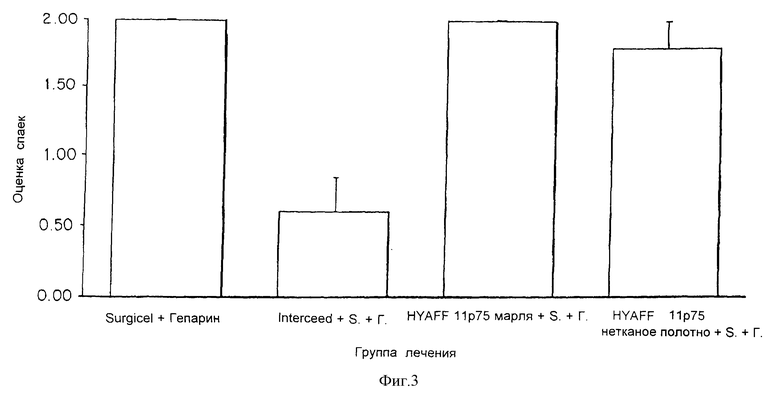
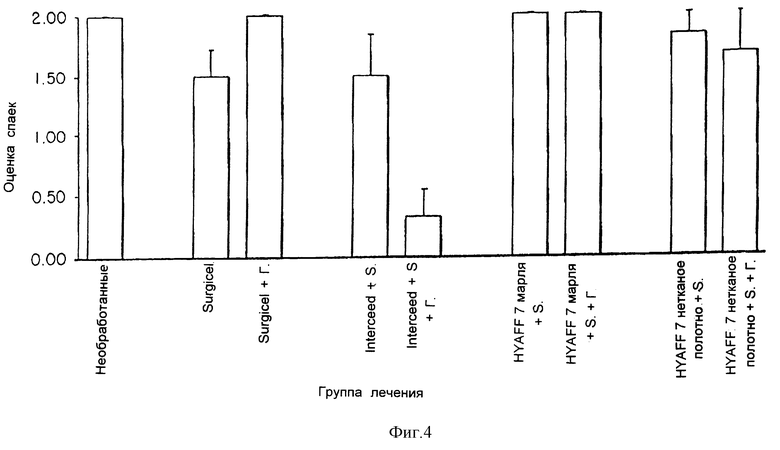
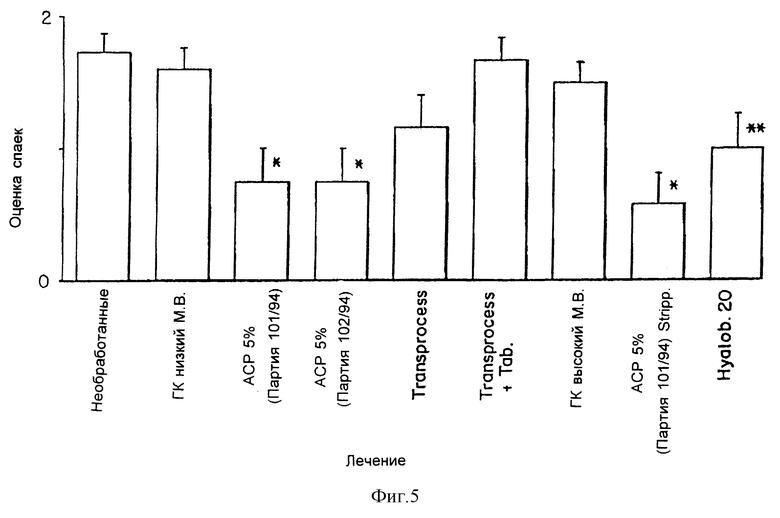
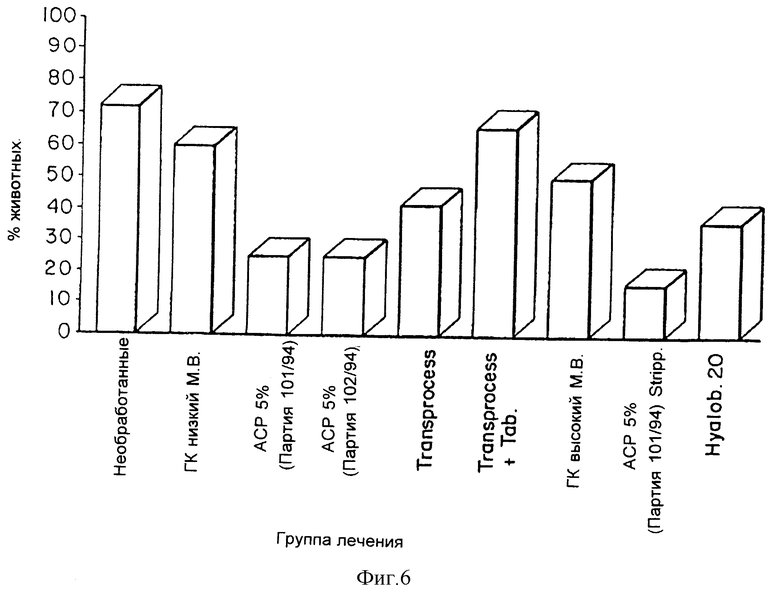
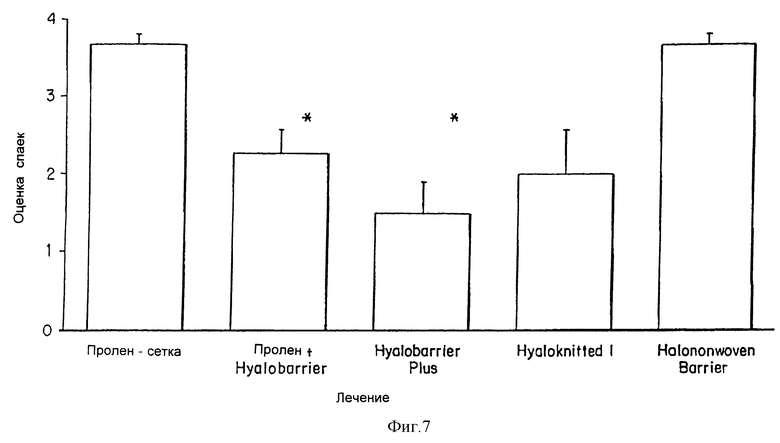
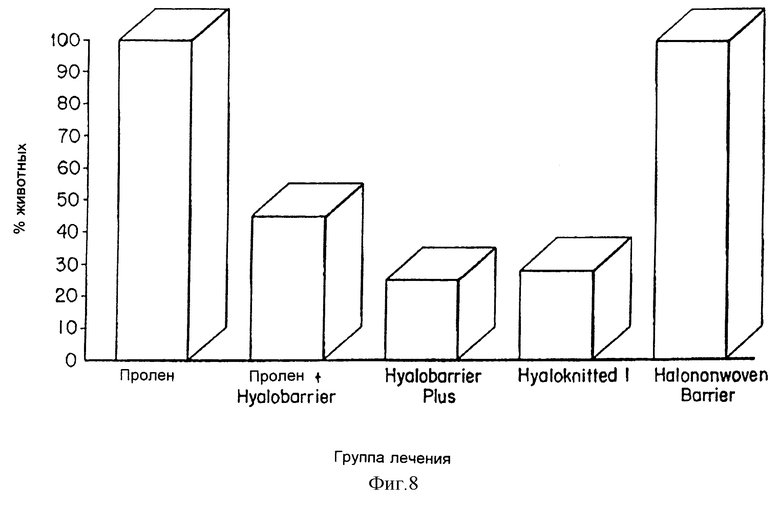
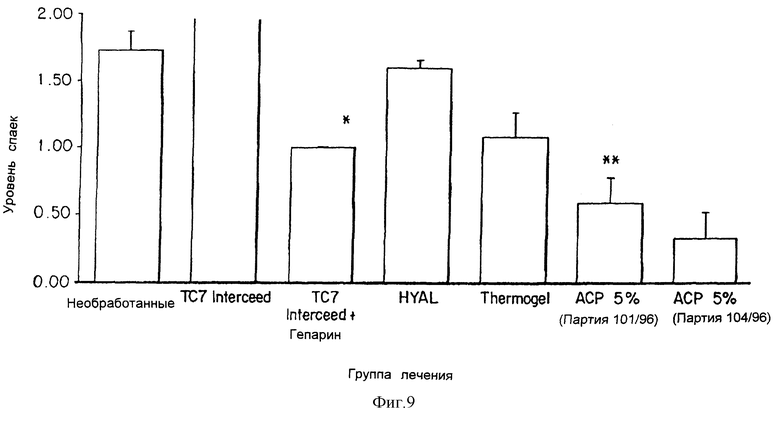
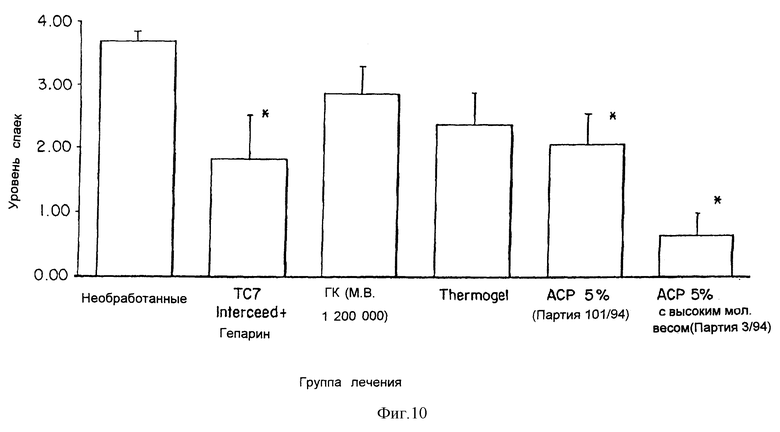
Изобретение может быть использовано в хирургии. Биоматериал представляет собой бензиловый эфир гиалуроновой кислоты, в котором от 75 до 100% карбоксильных групп гиалуроновой кислоты этерифицированы бензильным радикалом. До 25% карбоксильных групп могут быть этерифицированы алкильным радикалом С10-С20-алифатического спирта при условии, что по меньшей мере 80% карбоксильных групп этерифицированы. Биоматериал выполнен в форме мембраны, сетки, тканого или нетканого полотна или геля. Другой вариант биоматериала содержит по меньшей мере одно производное гиалуроновой кислоты, представляющее собой аутоперекрестно связанное производное гиалуроновой кислоты, в котором от 0,5 до 20% карбоксильных групп гиалуроновой кислоты перекрестно связаны с гидроксильной группой той же или другой молекулы гиалуроновой кислоты. Способ предотвращения послеоперационных спаек ткани состоит в наложении на ткань, вовлеченную в хирургическую операцию, биоматериала. Изобретение позволяет создать барьер для образования спайки до тех пор, пока не произойдет заживление, чтобы устранить такие проблемы, как инфекция, кальцификация имплантатов, образование рубца и т.д. 3 с. и 9 з.п. ф-лы, 9 табл., 10 ил.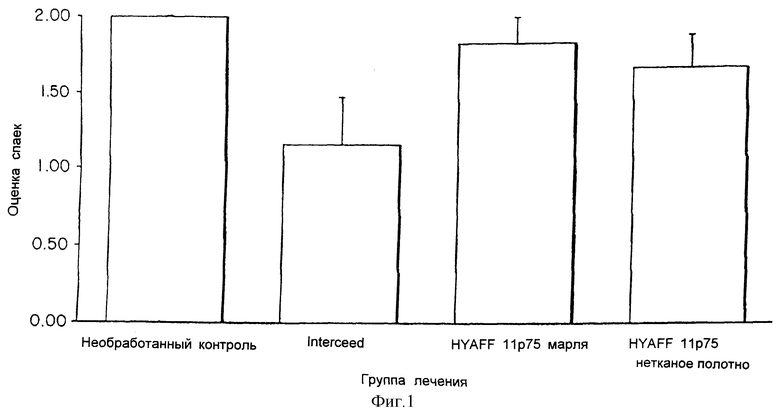
| Экономайзер | 0 |
|
SU94A1 |
| Пюпитр для работы на пишущих машинах | 1922 |
|
SU86A1 |
| Домовый номерной фонарь, служащий одновременно для указания названия улицы и номера дома и для освещения прилежащего участка улицы | 1917 |
|
SU93A1 |
| RU 97102350 A1, 27.02.1999. | |||
Авторы
Даты
2001-12-27—Публикация
1996-08-29—Подача