Изобретение относится к области биохимии и может быть использовано в медицине.
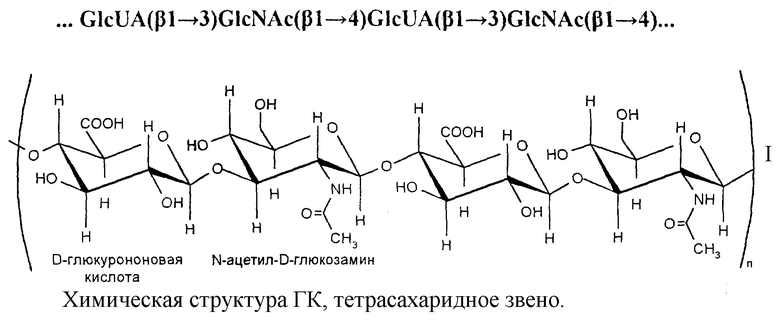
Гиалуроновая кислота (ГК), природный полисахарид из класса гликозаминогликанов, состоит из повторяющихся единиц D-глюкуроновой кислоты и N-ацетил-D-глюкозамина (см. формулу I в конце описания).
ГК находится в межклеточном матриксе всех высших животных и может быть выделена различными методами из соединительной ткани или получена с помощью продуцирующих ГК специальных бактерий.
ГК является полианионным полимером с молекулярной массой от нескольких сотен Да до 10 миллионов Да (средняя М=1-2 млн Да). Эти характеристики обусловливают уникальные физико-химические свойства полисахарида и его производных.
Биологические функции ГК можно разделить на "пассивные" и "активные". Как инертный материал ГК участвует в гомеостазе тканей, в стерическом регулировании (осмос) проникновения каких-либо субстанций, выполняет функцию "смазки", улучшающей подвижность суставов, и т. д.
"Активные" функции ГК заключаются в специфическом связывании с белками в межклеточном матриксе и на поверхности клетки; такое взаимодействие играет важную роль в образовании хрящевой ткани, в процессах клеточной пролиферации, в морфогенезе и эмбриональном развитии животных, а также в механизмах воспаления и возникновения рака.
ГК находит применение как адьювант в офтальмологии (препараты Ргоvisk, Healon), как матрица в так называемых "системах доставки" лекарственных средств, а также в хирургии для предупреждения послеоперационой адгезии тканей (спаечной болезни). Установлено, что ГК усиливает абсорбцию лекарств и некоторых протеинов через слизистые оболочки, а эффективность применения некоторых лекарств, например нестероидных противовоспалительных средств или циклоспорина, заметно улучшается в сочетании с ГК. В комбинации с ГК некоторые лекарственные субстанции образуют в эпидермисе как бы депо этих лекарств и высвобождаются из композиции медленнее, чем в отсутствие ГК.
Функционализация ГК или синтез биоконъюгатов с ГК имеет ряд преимуществ по сравнению с простыми смесями ГК-лекарство. Во-первых, химическая модификация позволяет изменить физико-химические свойства ГК под соответствующее применение и может значительно воздействовать на клиренс производных ГК. Во-вторых, биоконъюгаты ГК могут обладать большей растворимостью по сравнению с самими лекарствами. В-третьих, гидрогели ГК-лекарство могут применяться для локального контролируемого высвобождения субстанций в органах-мишенях. И, наконец, высокая аффинность рецепторов ГК в метастазирущих клетках может быть использована для направленной доставки противоопухолевых агентов в клетки-мишени.
Как известно, полимерные материалы широко используются для изготовления разнообразных медицинских изделий. Синтетические полимеры оптимизируются по механическим свойствам и часто не обладают достаточной биосовместимостью; напротив, биополимеры обычно не имеют необходимых механических характеристик. Смешивая синтетические полимеры с биологическими макромолекулами, например, ГК, можно получить композиты с требуемыми физико-химическими и биологическими свойствами.
Композиции ГК с полиакриловой кислотой приготовляют растворением обоих полимеров в воде в различных соотношениях, затем формируют пленки, которые лиофилизируют и подвергают реакции сшивки с помощью термической обработки при 130oС в вакууме в течение 24 ч [Cascone M., Sim В., Downes S. Blends of synthetic and natural polymers as drug delivery systems for gormone. // Biomaterials. - 1995. - V.16. - P.569]. Гидрогели ГК-поливиниловый спирт также изготовляют растворением обоих полимеров в воде в разных пропорциях.
На основе смеси двух анионных полимеров: ГК и карбоксиметилцеллюлозы (КМЦ) были созданы биоабсорбирующие пленочные материалы Seprafilm, применяющиеся для предупреждения послеоперационных спаек. В присутствии водорастворимого 1-(3-диметиламинопропил)-3-этилкарбодиимида (КДИ) к карбоксильным группам ГК или КМЦ были присоединены четвертичные аммониевые группы, с помощью которых усиливалось взаимодействие между полимерными цепями компонентов смеси [US Patent 5017229. - 1991 г.; Burns J., Burgess L., Skinner K. , Rose R. et al. A hyaluronate based gel for the prevention of postsurgical adhesion: Evaluation in two animal species. // Fertil. Steril. - 1996. - V. 66. - P.814].
Известна технология изготовления композитного материала из ГК и коллагена, которая основана на комплексировании обоих компонентов в коагулят с последующей сшивкой при помощи глиоксаля или диальдегида [Rehakova M., Bakos D. , Vizarova К. et al. Properties of collagen and hyaluronic acid composite materials and their modification by crosslinking. // J. Biomed. Mater. Res. - 1996. - V.30. - P.369]. Ателоколлаген, суспендированный в 0,5 M СН3СООН при рН 3,2, добавляли в раствор ГК. После коагуляции, промывания и высушивания осадка получали тонкую пленку, которую затем подвергали сшивке в растворе диальдегида.
Известны полимерные комплексы ГК и ее натриевых, калиевых или литиевых солей с природными полисахаридами и белками: хитином, альгиновой кислотой, фибрином, коллагеном и т.д., которые могут применяться в качестве покрытия различных медицинских изделий, например искусственных сосудистых протезов [ЕР 0544259 A1].
Новые биоматериалы на основе ГК могут быть получены с помощью разнообразных реакций по функциональным группам полимера. Например, при реакции этерификации ГК на первом этапе формируют тетраалкиламмониевую соль ГК в ДМФА, затем проводят реакцию с первичными спиртами, например этиловым, пропиловым, пентиловым, бензиловым или додециловым [Hant J., Joshi H., Stella V. J. et al. Diggusion and drug release in polymer films prepared from ester derivatives of hyaluronic acid. // J. Controlled Rel. - 1990. - V.12. - P. 159] . В зависимости от природы спирта и количества модифицируемых групп ГК можно в широких пределах варьировать свойства получаемых материалов.
С помощью реакции этерификации к тетрабутиламмониевой соли ГК можно присоединять и некоторые лекарственные субстанции, содержащие гидроксильную группу. Неполные эфиры ГК с противовоспалительными стероидами были синтезированы при помощи реакции этерификации с предварительным формированием тетрабутиламмониевой соли ГК. Полностью или частично этерифицированная гидрокортизоном ГК в настоящее время исследуется как новый биоматериал в различных лекарственных формах, например микросферах, таблетках, пилюлях или пленках [Benedetti L.M., Торр Е.М., Stella V.J. Microspheres of hyaluronic acid esters - fabrication methods and in vitro hydrocortisone release. // J. Controlled Rel. - 1990. - V. 13. - Р.33].
С использованием метода карбодиимидной активации синтезировано много биоконъюгатов ГК с лекарственными средствами. Большинство проводимых опытов основано на реакции КДИ-активированной карбоксильной функции D-глюкуроновой кислоты в ГК с соединением, содержащим аминогруппы.
Сложный эфир хлорамфеникола с аланином был присоединен к различным гликозаминогликанам через КДИ-активированные карбоксигруппы полисахаридов и аминогруппы аланина. Таким же образом аминогруппы антрациклиновых антибиотиков адриамицина (доксорубицина) и дауномицина, а также митомицина были связаны с активированными группами ГК [Сеrа С., Terbojevich M. et al. Antracycline antibiotics supported on water-soluble polysaccharides: Synthesis and physicochemical characterization. // Int. J. Biol. Macromol. - 1988, - V.10. - P.66].
Запатентованы биоматериалы на основе ГК, карбоксиметилцеллюлозы, альгиновой кислоты и др., одна часть карбоксильных групп которых используется для сшивки макромолекул, другая часть этерифицируется моно- или полиспиртами или взаимодействует с аминами, включая различные лекарственные вещества. Активирующим агентом карбоксигрупп в этом случае является 2-хлор-1-метилпиридинийиодид, а реакции со спиртами или аминами проводят при нагревании или воздействии радиации [ЕР 341745] . Материалы, синтезированные описанным способом, могут предназначаться для изготовления фармацевтических композиций, различных медицинских изделий, например хирургических нитей, пленок для регенерации эпидермиса, для лечения кожных заболеваний и т.п.
Для уменьшения растворимости ГК и, следовательно, пролонгирования действия лекарственных средств, используемых с ней в комбинации, применяется реакция сшивки ГК по карбоксильным или гидроксильным группам полимера. Сшивающими реагентами могут являться оксихлорид фосфора (V), дивинилсульфон, эпоксисоединения, диальдегиды, диамины, дигидразиды и т.д. В некоторых реакциях внутри- и межмолекулярной сшивки полимерных цепей ГК, например, с использованием дигидразида адипиновой кислоты требуется применение КДИ [Vercruysse К.Р., Prestwich G.D. Hyauronate derivatives in drug delivery. // Therapeutic Drug Carrier Systems. - 1998. - V. 15. - N 5. - P.513-555]. Из сшитой ГК могут быть изготовлены гидрогели или пленки.
Реакцию так называемой ионной сшивки ГК проводят с помощью солей трехвалентного железа: получают гидрогель ГК с 0,5% FeCl3 (фирмы Этикон) [Johns D. B. , Rodgers K.E., Donahue W.D. et al. Reduction of adhesion formation by postoperative administration of ionically cross-linked hyaluronic acid. // Fertil Steril. -1997. - N 68(1). - P.37-42]. Такой гидрогель предназначается для профилактики послеоперационной спаечной болезни в абдоминальной хирургии.
Наиболее близким к предлагаемому изобретению является получение ГК, модифицированной по карбоксильным группам ε-аминокапроновой кислотой. ε-Аминокапроновая кислота является известным кровоостанавливающим средством. Присоединение ε-аминокапроновой кислоты осуществляется посредством активации кислотных групп ГК с помощью КДИ или N-гидроксисукцинимида. В этом случае получаются производные ГК, растворимые в органических растворителях. Вторично активируя с помощью КДИ уже карбоксильные группы ε-аминокапроновой кислоты, можно проводить дальнейшую модификацию ГК, например, дауномицином [ЕР 0506976 B1, 1992].
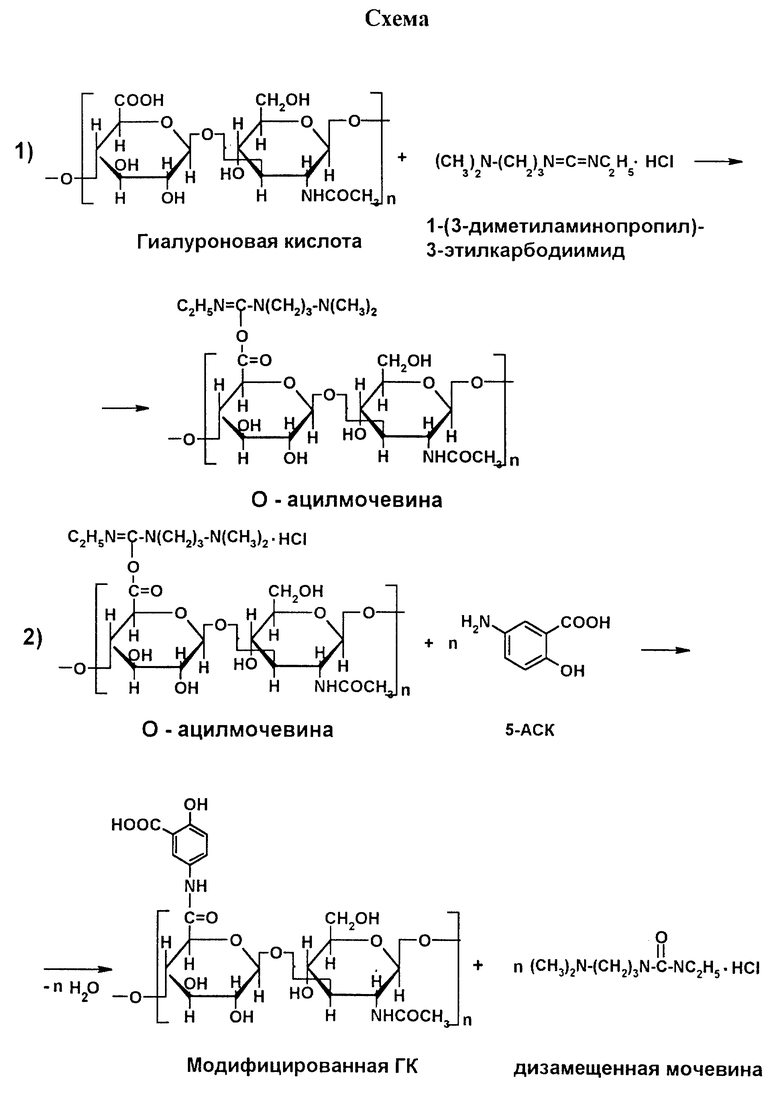
Авторами предлагается химически модифицированная ГК, полученная из ГК и 5-аминосалициловой кислоты (5-АСК) методом карбодиимидной активации карбоксильных групп полисахарида. Модифицированную ГК с различной степенью замещения карбоксильных групп (от 30 до 50 мол.%) получают следующим образом.
Пример 1. 1 г ГК растворяют в 50 мл воды с рН 4,7-4,8, добавляют 0,476 г водорастворимого 1-(3-диметиламинопропил)-3-этилкарбодиимида. Затем этот раствор при интенсивном перемешивании приливают к 0,382 г 5-АСК, суспендированной в 40 мл воды, с рН 4,7-4,8 при 40oС. После добавления всего раствора температуру реакционной смеси снижают до комнатной и реакцию проводят в течение 1 часа. По завершении реакции с целью удаления низкомолекулярных исходных соединений раствор модифицированной ГК диализуют против подкисленной дистиллированной воды в течение 24 ч, затем продукт очищают на колонке с оксидом алюминия. После очистки на колонке рН водного раствора полимера доводят НСl до 3-4 и осаждают 4-кратным объемом этилового спирта, осадок центрифугируют, промывают спиртом, затем эфиром и высушивают в вакууме. Таким образом получают модифицированную ГК с кислотными группами в составе 5-АСК со степенью замещения карбоксильных групп полимера 30 мол.% (см. схему в конце описания). Количество 5-АСК, ковалентно связанной с полимером, определяют фотометрически при 304 нм после гидролиза точной навески продукта в 20%-ной соляной кислоте. Сразу после осаждения модифицированная ГК (в виде кислоты) хорошо растворяется в воде, после высушивания ее растворимость значительно уменьшается.
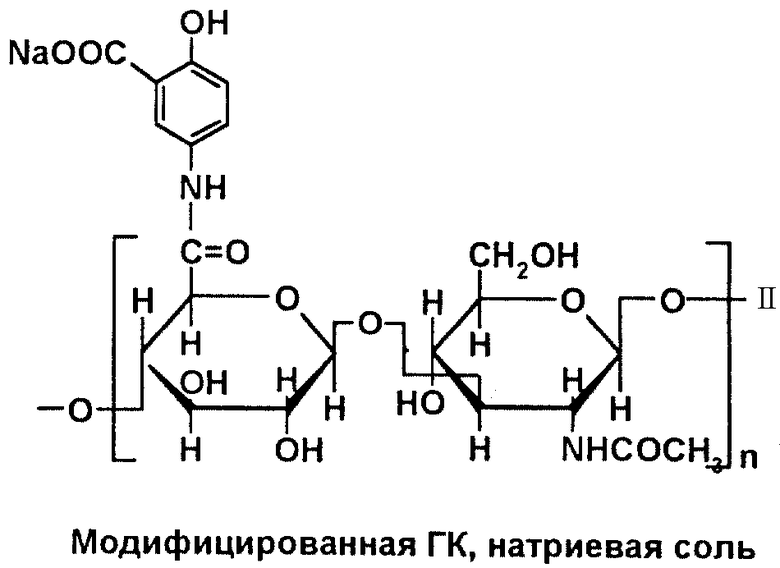
Если после очистки ГК окисью алюминия полимер осаждать спиртом из раствора с рН 8,0-8,5, можно получать натриевую соль модифицированной ГК (см. формулу II в конце описания). Натриевая соль модифицированной ГК является хорошо растворимым в воде полимером, из которого можно изготовлять лекарственные пленки различного назначения.
Пример 2. Реакцию ГК с 5-АСК проводят аналогично примеру 1. Время реакции - 4 ч. При этом количество 5-АСК, ковалентно связанной с полимером, составляет 50 мол.%.
В зависимости от времени проведения реакции можно получать продукты с различной степенью замещения карбоксильных групп ГК.
Как все салицилаты, модифицированная ГК способна образовывать окрашенные комплексы с FеСl3, которые являются малорастворимыми в воде соединениями. Обрабатывая поверхность пленок из модифицированной ГК раствором FеСl3, можно изготовлять нерастворимые в воде материалы.
Как известно, 5-АСК относится к классу нестероидных противовоспалительных препаратов (препарат Месалазин) и обладает такими же свойствами, как и ацетилсалициловая кислота [Машковский М.Д. Лекарственные средства. - Харьков: Торсинг, 1997. - Т. 2. - 590 c.]. В составе модифицированной ГК 5-АСК также может проявлять противовоспалительные свойства. В связи с этим на модели острого воспаления, создаваемого с помощью 3%-ного формалина у крыс, были оценены противовоспалительные свойства модифицированной ГК [Бондарев А. И. , Давыдова В.А., Зарудий Ф.С., Башкатов С.А. Противовоспалительная и анальгезирующая активность комплексов антифлогистиков с глицирризиновой кислотой. // Фармакология и токсикология. - 1991. - 5. - С.47-50].
Изучение противовоспалительных свойств проводили на белых крысах массой 180-200 г. Опытную группу крыс вначале лечили с помощью внутрибрюшинного введения раствора модифицированной ГК в дозе 60 мг/кг. Через 30 мин в апоневроз задней лапки крыс вводили 0,1 мл 3%-ного формалина, вследствие чего развивался отек лапки. Контрольная группа крыс оставалась нелеченной. Через 3 ч сравнивали лапку с отеком с лапкой без отека путем измерения количества воды, вытесняемой из сосуда при погружении лапок до нижнего сустава костей голени. Установлено достоверное уменьшение отека лапок леченых крыс по сравнению с контрольной группой животных (Р<0,05).
Пленки, изготовленные из модифицированной ГК (натриевой соли), были испытаны в качестве эксплантатов для защиты анастомозов у беспородных собак после выполнения резекций тонкого кишечника.
Опыты проводили на 21 беспородной собаке весом 10-15 кг. Под тиопенталовым наркозом проводили резекции тонкой кишки с наложением двухрядного анастомоза "конец в конец". У 9 собак анастомоз был защищен аппликацией эксплантата без дополнительной фиксации, т.е. только за счет хорошей адгезии пленки к тканям кишки. Животных выводили из опыта на 3-ий, 7-ой и 30-ый день. Проведен анализ гистологического материала, окрашенного гематоксилинэозином, выполнены гистохимические реакции на гликозаминогликаны по Хейлу и на гликоген (ШИК-реакция). Гистохимические реакции оценивали по 4-балльной шкале: инактивная, слабая, умеренная и высокая активности.
Сравнительные результаты морфологических исследований приведены в таблице.
Как следует из приведенных результатов экспериментов, применение пленочных эксплантатов на основе гиалуроновой кислоты способствует активной регенерации тканей, предупреждает воспалительный и спаечный процессы в области межкишечного анастомоза.
Модифицированную гиалуроновую кислоту также можно применять для пропитки шовного материала (хирургических нитей), искусственных сосудистых протезов и т.п.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ЗАЩИТЫ АНАСТОМОЗОВ ПРИ РЕЗЕКЦИЯХ КИШЕЧНИКА | 2000 |
|
RU2192256C2 |
| ПРОИЗВОДНЫЕ ГИАЛУРОНОВОЙ КИСЛОТЫ С ПОНИЖЕННОЙ БИОДЕГРАДИРУЕМОСТЬЮ | 2007 |
|
RU2350625C2 |
| СПОСОБ ПРОФИЛАКТИКИ РЕОККЛЮЗИЙ ПРИ ОПЕРАЦИЯХ НА МАГИСТРАЛЬНЫХ СОСУДАХ | 1999 |
|
RU2185171C2 |
| СПОСОБ ПРОФИЛАКТИКИ АСЕПТИЧЕСКОГО ВОСПАЛЕНИЯ ПРИ ОПЕРАЦИЯХ НА МАГИСТРАЛЬНЫХ СОСУДАХ | 1999 |
|
RU2180846C2 |
| КОНЪЮГАТ ГИАЛУРОНОВОЙ КИСЛОТЫ С НОВОКАИНОМ С АМФОТЕРНЫМИ СВОЙСТВАМИ | 2011 |
|
RU2473351C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1- И 2-ХЛОРАДАМАНТАНОВ ИЗ 1- И 2-АДАМАНТАНОЛОВ | 2000 |
|
RU2178400C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОТЕЗОВ КРОВЕНОСНЫХ СОСУДОВ | 2001 |
|
RU2241414C2 |
| СПОСОБ ПОЛУЧЕНИЯ 1-АДАМАНТИЛАЛКИЛОВЫХ ЭФИРОВ | 1998 |
|
RU2145593C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОБЛАДАЮЩИХ ПОНИЖЕННОЙ РАСТВОРИМОСТЬЮ В ВОДЕ ПЛЕНОЧНЫХ МАТЕРИАЛОВ НА ОСНОВЕ МОДИФИЦИРОВАННЫХ АМИНОСАЛИЦИЛОВЫМИ КИСЛОТАМИ КАРБОКСИЛСОДЕРЖАЩИХ ПОЛИСАХАРИДОВ | 2007 |
|
RU2343932C1 |
| СПОСОБ ГИДРОФОБИЗАЦИИ ДРЕВЕСНЫХ ПОРОШКОВ | 1999 |
|
RU2158193C1 |



Описывается способ получения химически модифицированной гиалуроновой кислоты, заключающийся в активации карбоксильных групп гиалуроновой кислоты 1-(3-диметиламинопропил)-3-этилкарбодиимидом и реакции образующейся O-ацилмочевины с водной суспензией 5-аминосалициловой кислоты при начальной температуре реакции 40oС в течение 2-4 ч с последующей очисткой полимерного амида диализом, оксидом алюминия и осаждением этиловым спиртом. В зависимости от времени проведения реакции получают гиалуроновую кислоту с различной степенью замещения карбоксильных групп. Пленки из модифицированного полисахарида можно использовать как биоматериал в абдоминальной хирургии для защиты анастомозов при резекциях кишечника, для пропитки шовного материала (хирургических нитей), искусственных протезов и т.п. 1 табл.
Способ получения модифицированной гиалуроновой кислоты, заключающийся в карбодиимидной активации карбоксильных групп гиалуроновой кислоты и последующей реакции образующейся О-ацилмочевины с соединением, содержащим аминогруппу, отличающийся тем, что гиалуроновая кислота сначала взаимодействует с 1-(3-диметиламинопропил)-3-этилкарбодиимидом с образованием О-ацилмочевины, а затем О-ацилмочевина реагирует с водной суспензией 5-аминосалициловой кислоты при начальной температуре реакции 40oС в течение 2-4 ч, после чего продукт диализуют против подкисленной дистиллированной воды, затем очищают на колонке с оксидом алюминия, осаждают этиловым спиртом и высушивают под вакуумом.
| ЕР 0506976 А, 07.10.1997 | |||
| ЕР 0544259 А, 02.06.1993 | |||
| US 5017229 А, 21.05.1991 | |||
| КРАНОВЫЙ ЗАХВАТ ДЛЯ МОНТАЖА ИЗДЕЛИЙ | 0 |
|
SU341745A1 |
| RU 98111765 А, 20.05.2000 | |||
| КОМПОЗИЦИИ С ЗАМЕДЛЕННЫМ (ПРОЛОНГИРОВАННЫМ) ВЫСВОБОЖДЕНИЕМ | 1990 |
|
RU2093148C1 |
| МНОГОКОМПОНЕНТНАЯ ДОЗИРОВАННАЯ ФОРМА С КОНТРОЛИРУЕМЫМ ВЫДЕЛЕНИЕМ АКТИВНОГО ИНГРЕДИЕНТА | 1991 |
|
RU2111743C1 |
Авторы
Даты
2002-10-27—Публикация
2000-09-21—Подача