Изобретение относится к области медицины и может быть использовано как средство, регулирующее функции предстательной железы, для профилактики и лечения заболеваний предстательной железы.
В настоящее время заболевания предстательной железы занимают существенное место среди урологической патологии, имеют тенденцию к увеличению и приобретают все возрастающую социальную значимость [1,2] .
В консервативном лечении больных с заболеваниями предстательной железы с учетом патогенетических механизмов применяются в основном следующие традиционные лечебные средства различной направленности действия [3] :
- антибактериальное и противовоспалительное действие - антибиотики и сульфаниламидные препараты;
- нормализация микроциркуляции - трентал, галидор, эскузан;
- спазмолитическое действие - но-шпа, баралгин;
- нормализация уровня половых гормонов - метилтестостероп, сустанон-250;
- коррекция иммунопатологических реакций - продигиозан, пирогенал, левамизол, тавегил, фенкарол;
- и др.
Однако применение этих лекарственных средств позволяет воздействовать только на отдельные звенья этиопатогенеза различных заболеваний предстательной железы, не оказывая специфического действия на ткань простаты.
Заявляемое пептидное соединение - тетрапептид - структурных аналогов не имеет.
Среди наиболее близких аналогов по применению известны лекарственные препараты, стимулирующие метаболические процессы в предстательной железе: раверон [3] и простатилен (сампрост) [4] .
В качестве протипа заявляемого фармологического средства выбран препарат простатилен [4] , представляющий собой препарат полипептидной природы, полученный из ткани предстательной железы половозрелых животных. Однако применение этих средств ограничено в связи со сложностью способов получения, малым выходом активных веществ, значительной вариабельностью их физико-химических свойств, а также из-за возможного возникновения у больных аллергических реакций.
Препарат пептидной природы вводят пациентам парентерально, курсами до момента достижения терапевтического эффекта. Указанный способ и выбран в качестве прототипа заявляемого способа регулирования функции предстательной железы.
Заявляемое изобретение направлено на получение нового биологически активного соединения пептидной природы, регулирующего функции предстательной железы.
Согласно изобретению заявляется тетрапептид лизил-глутамил-аспартил-пролин общей формулы: Lys-Glu-Asp-Pro. Тетрапептид лизил-глутамил-аспартил-пролин со следующей аминокислотной последовательностью: Lys-Glu-Asp-Pro, отвечающий изобретению, проявляет биологическую активность, а именно - восстанавливает функции предстательной железы и стенки мочевого пузыря, нормализует показатели местного иммунитета, стимулирует противовоспалительные реакции и показатели системы антиоксидантной защиты.
Тетрапептид получают классическим методом пептидного синтеза в растворе [5] .
Действие тетрапептида Lys-Glu-Asp-Pro, направленное на регуляцию функций предстательной железы, выявлено при его экспериментальном изучении.
Изучение биологической активности проводили на эксплантатах мочевого пузыря, исследуя тканеспецифическое действие тетрапептида, на крысах, изучая противовоспалительное действие при бактериальном простатите и влияние на показатели системы антиоксидантной защиты у старых животных.
Согласно изобретению фармакологическое средство, регулирующее функции предстательной железы, содержит в качестве активного начала эффективное количество тетрапептида формулы лизил-глутамил-аспартил-пролин (Lys-Glu-Asp-Pro) или его солей.
Согласно изобретению фармакологическое средство, регулирующее функции предстательной железы, может содержать соли по аминогруппе (ацетат, гидрохлорид, оксалат), или по карбоксильным группам (соли металлов натрия, калия, кальция, лития, цинка, магния, а также других органических и неорганических катионов аммония, триэтиламмония).
Согласно изобретению фармакологическое средство предназначено для парентерального, интраназального, перорального или местного применения.
Заявляемое фармакологическое средство регулирует функции предстательной железы, оказывает противовоспалительное и антиоксидантное действие.
Понятие "фармакологическое средство", используемое в данной заявке, подразумевает использование любой лекарственной формы, содержащей тетрапептид или его соли, которые могут найти профилактическое и/или лечебное применение в медицине в качестве средства для регуляции функций предстательной железы.
Понятие "эффективное количество", используемое в данной заявке, подразумевает использование того количества активного начала, которое в соответствии с его количественными показателями активности и токсичности, а также на основании знаний специалиста должно быть эффективным в данной лекарственной форме.
Понятие "фармацевтическая композиция", используемое в данной заявке, подразумевает различные лекарственные формы препарата.
Для получения фармацевтических композиций, отвечающих изобретению, предлагаемый тетрапептид или его фармацевтически приемлемые производные смешиваются как активный ингредиент с фармацевтическим носителем согласно принятым в фармацевтике способам компаундирования. Носитель может иметь различные формы, которые зависят от лекарственной формы препарата, желаемой для введения в организм, например парентерального, интраназального, перорального или местного.
Для парентерального, интраназального или местного введения носитель обычно включает стерильную воду, хотя могут быть включены другие ингредиенты, способствующие стабильности, или для сохранения стерильности.
Согласно изобретению способ включает профилактическое или лечебное введение пациенту заявляемого фармакологического средства в дозах 0,01-100 мкг/кг массы тела по крайней мере один раз в день в течение периода, необходимого для достижения терапевтического эффекта - 10-40 дней в зависимости от характера течения патологического процесса.
Согласно изобретению тетрапептид активен при введении его в дозах 0,01-100 мкг/кг массы тела, хотя могут быть использованы и более низкие (высокие) дозы в зависимости от характера течения патологического процесса.
Изобретение иллюстрируется примером синтеза тетрапептида формулы лизил-глутамил-аспартил-пролин (Lys-Glu-Asp-Pro) (пример 1), примерами испытания токсичности и биологической активности тетрапептида (примеры 2,3,4,5), а также примерами результатов клинического применения тетрапептида, демонстрирующими его фармакологические свойства и подтверждающими возможность достижения профилактического и/или лечебного эффекта (примеры 6,7).
Пример 1. Синтез тетрапептида Lys-Glu-Asp-Pro
1. Название соединения: лизил-глутамил-аспартил-пролин.
2. Структурная формула: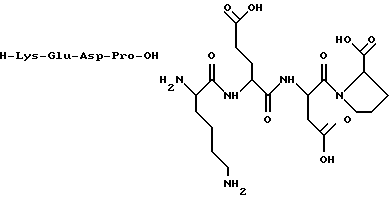
3. Брутто-формула без противоиона: С20Н33N5O9.
4. Молекулярный вес без противоиона: 487,51.
5. Противоион: ацетат.
6. Внешний вид: белый аморфный порошок без запаха.
7. Способ синтеза: пептид получен классическим методом синтеза в растворе по схеме: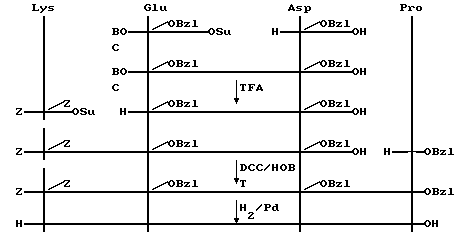
Z - бензилоксикарбонильная группа;
ВОС - трет. бутилоксикарбонильная группа;
Osu - N-оксисукцинимидный эфир;
OBzl - бензиловый эфир;
DCC - N, N'-дициклогексилкарбодиимид;
НОВТ - N-оксибензотриазол.
В качестве растворителя использовали N, N'-диметилформамид, при введении аспарагиновой кислоты использовали защиту α-СООН группы солеобразованием с триэтиламином. Деблокирование ВОС-защитной группы проводили раствором трифторуксусной кислоты (TFA), Z-защитных групп каталитическим гидрогенолизом. Выделение и очистка препарата осуществлялись методом препаративной ВЭЖХ на колонке с обращенной фазой.
Характеристики готового препарата:
аминокислотный анализ: Lys 0,98, Glu 1,01, Asp 1,01, Pro 1,00;
содержание основного вещества: 98,36% (по ВЭЖХ, 220 нм);
ТСХ индивидуален, Rf = 0,61 (силикагель, ацетонитрил-вода 1: 1);
содержание влаги: 6%.
рН 0,001% раствора: 5,55.
удельное оптическое вращение: [α]
Пример синтеза:
1) BOC-Glu(OBzl)-Asp(OBzl)-OH (I), N-трет. бутилоксикарбонил-(γ-бензил)глутамил-(β-бензил)аспартат.
N-оксисукцинимидный эфир N-трет. бутилоксикарбонил-(γ-бензил)глутаминовой кислоты BOC-Glu(OBzl)-OSu 4,34 г (0,0100 моль) растворяют в 20 мл диметилформамида, добавляют триэтиламин 1,72 мл (0,0125 моль) и β-бензиласпартат 2,80 г (0,0125 моль). Перемешивают при комнатной температуре 24 ч. Продукт высаживают 0,5 н. раствором серной кислоты (150 мл), экстрагируют в этилацетат (3•30мл), промывают 0,5 н. раствором серной кислоты (2•20 мл), водой, 5% раствором бикарбоната натрия (1•20 мл), водой, 0,5 н. раствором серной кислоты (2•20 мл), водой и сушат над безводным сульфатом натрия. Этилацетат фильтруют, упаривают в вакууме при 40oС, остаток сушат в вакууме над P2O5. Получают масло 5,68 г (≈100%).
Rf= 0,42 (бензол-ацетон 2: 1, пластинки ПТСХ-П-В-УФ Sorbfil, силикагель СТХ-1ВЭ 8-12 мкм, проявление УФ и хлор/бензидин).
2) TFA.H-Glu(OBzl)-Asp(OBzl)-OH (II), трифторацетат ((γ-бензил)-глутамил-(β-бензил)аспартата.
N-трет. бутилоксикарбонил(γ-бензил)глутамил-(β-бензил)аспартат (I) 5,68 г (≈0,01 моль) растворяют в 20 мл смеси дихлорметан-трифторуксусная кислота (3: 1). Через 2 часа растворитель упаривают в вакууме при 40oС, упаривание повторяют с новой порцией дихлорметана (2•10 мл), остаток сушат в вакууме над NaOH. Получают масло 5,80 г (≈100%).
Rf= 0,63 (н-бутанол-пиридин-уксусная кислота-вода, 15: 10: 3: 12).
3) Z-Lys(Z)-Glu(OBzl)-Asp(OBzl)-OH (III), N, Nε-дибензилоксикарбониллизил-(γ-бензил)глутамил-(β-бензил)аспартат.
Трифторацетат -(γ-бензил) глутамил-(β-бензил)аспартата (II) 5,65 г (0,01 моль) растворяют в 10 мл диметилформамида, добавляют триэтиламин 2,80 мл (0,02 моль) и N-оксисукцинимидный эфир N, Nε-дибензилоксикарбониллизина 6,64 г (0,013 моль). Смесь перемешивают 24 часа при комнатной температуре.
Продукт высаживают 0,5 н раствором серной кислоты (150 мл), экстрагируют в этилацетат (3•30 мл), промывают 0,5 н. раствором серной кислоты (2•20 мл), водой, 5% раствором бикарбоната натрия (1•20 мл), водой, 0,5 н. раствором серной кислоты (2•20 мл), водой и сушат над безводным сульфатом натрия. Этилацетат фильтруют, упаривают в вакууме при 40oС, остаток закристаллизовывают в системе этилацетат/гексан. Продукт отфильтровывают и сушат в вакууме над Р2O5. Выход 6,04 г (72%). Т пл. = 142oС.
Rf= 0,60 (бензол-ацетон, 1: 1).
4) Z-Lys(Z)-Glu(OBzl)-Asp(OBzl)-Pro-OBzl (IV), бензиловый эфир N, Nε-дибензилоксикарбониллизил-(γ-бензил)глутамил-(β-бензил)аспартилпролина.
HCl.H-Pro-OBzl, гидрохлорид бензилового эфира пролина 0,72 г (3 ммоль) суспендируют в 15 мл тетрагидрофурана и при перемешивании добавляют триэтиламин 0,4 мл (3 ммоль), далее через 5 мин. N, Nε-дибензилоксикарбониллизил-(γ-бензил)
глутамил-(β-бензил)аспартат (III) 1,68 г (2 ммоль), N-оксибензотриазол 0,27 г (2 ммоль) и охлаждают смесь до 0oС. Затем добавляют охлажденный до 0oС раствор N, N'-дициклогексилкарбодиимида 0,42 г (2 ммоль) в 5 мл тетрагидрофурана, перемешивают смесь при этой температуре 2 часа и оставляют на ночь перемешиваться при комнатной температуре. Осадок дициклогексилмочевины отфильтровывают, растворитель упаривают в вакууме, остаток растворяют в 30 мл этилацетата и промывают раствор 1 н. раствором соляной кислоты, водой, 5%-ным раствором бикарбоната натрия, водой, 1 н. раствором соляной кислоты, водой и сушат над безводным сульфатом натрия. Растворитель упаривают в вакууме и продукт закристаллизовывают в системе этилацетат/гексан. Выход 1,39 г (68%). Т. пл. = 147-150oС.
Rf= 0,54 (бензол-ацетон, 2: 1).
5) H-Lys-Glu-Asp-Pro-OH (V), лизил-глутамил-аспартил-пролин.
Бензиловый эфир N, Nε-дибензилоксикарбониллизил-(γ-бензил)глутамил-(β-бензил) аспартилпролина (III) 1,24 г гидрировали в системе метанол-вода-уксусная кислота (3: 1: 1) над катализатором Pd/C. Контроль за полнотой деблокирования в ТСХ системах бензол-ацетон (2: 1) и ацетонитрил-уксусная кислота-вода (5: 1: 3). По окончании реакции катализатор отфильтровывают, фильтрат упаривают в вакууме и остаток закристаллизовывают в системе вода/метанол. Продукт сушат в вакууме над КОН. Выход 0,526 г (90%).
Rf= 0,61 (ацетонитрил-вода, 1: 1).
Для очистки 500 мг препарата растворяли в 4 мл 0,01% трифторуксусной кислоты (рН пробы 2,21) и подвергали высокоэффективной жидкостной хроматографии на колонке с обращенной фазой 50•250 мм Diasorb-130-C16T, 7 мкм. Хроматограф Beckman System Gold, 126 Solvent Module, 168 Diode Array Detector Module. Условия хроматографирования А: 0,1% TFA; В: 50% MeCN/0,1% TFA, градиент В 0-->16% за 240 мин. Объем пробы 5 мл, детекция при 215 нм, сканирование 190-600 нм, скорость потока 10 мл/мин. Отбирали фракцию 105-135 мин.
Растворитель упаривали в вакууме при температуре не выше 40oС, упаривание многократно (5 раз) повторяли с 10 мл 10% раствора уксусной кислоты. Окончательно остаток растворяли в 20 мл деионизованной воды и лиофилизовывали. Получено 280 мг очищенного препарата в виде аморфного белого порошка без запаха.
Для получения соответствующих солей по карбоксильным группам к свободному тетрапептиду добавляют рассчитанное количество водного раствора гидроокиси соответствующего металла (NaOH, КОН, Zn(OH)2, LiOH, Ca(OH)2, Mg(OH)2, NH4OH). Для получения триэтиламмониевой соли обработку проводят аналогичным образом, используя в качестве основания триэтиламин.
6) Анализ готового препарата.
Содержание основного вещества определяли методом ВЭЖХ на колонке Supelco LC-18-DB 4,6•250 mm, gard. LC-18-DB. A: 0,1% TFA; В: 50% MeCN/0,1%TFA; grad. В 0-->20% за 30 мин. Скорость потока 1 мл/мин. Детекция при 220 нм, сканирование 190-600 нм, проба 20 μl. Содержание основного вещества 98,56%.
Аминокислотный анализ проводили на анализаторе AАА"Т-339" Prague. Гидролиз в 6 н. НСl при 125oС 24 ч
Lys 0,98; Glu 1,01; Asp 1,01; Pro 1,00
ТСХ: индивидуален, Rf= 0,61 (ацетонитрил-вода, 1: 1 пластинки ПТСХ-П-В-УФ Sorbfil, силикагель СТХ-1ВЭ 8-12 мкм, проявление хлор/бензидин).
Содержание влаги: 7% (гравиметрически по потере массы при сушке 20 мг при 100oС).
рН 0,001% раствора: 5,55 (потенциометрически).
Удельное оптическое вращение: [α]
Фармакологическое средство в форме раствора получают следующим образом: тетрапептид (или его соли), полученные описанным выше способом, растворяют в 0,9% изотоническом растворе NaCl с содержанием тетрапептида 10 мкг в 1 мл раствора.
Пример 2. Изучение токсичности тетрапептида Lys-Glu-Asp-Pro
Изучение общетоксического действия тетрапептида Lys-Glu-Asp-Pro проводилось в соответствии с "Правилами доклинической оценки безопасности фармакологических средств (GLP)".
Цель изучения состояла в определении переносимых токсических доз препарата, оценке степени и характера патологических изменений в различных органах и системах организма и выявлении зависимости токсических эффектов от дозы и длительности применения препарата. Определение острой токсичности тетрапептида Lys-Glu-Asp-Pro проводили по методу Кербера. Исследование проведено на 78 белых беспородных мышах-самцах массой 20-22 г, содержавшихся на стандартном режиме и получавших стандартное питание в условиях вивария. Животные были разделены случайным распределением на 6 равных групп по 13 мышей в каждой. Препарат вводили животным однократно внутримышечно в объеме 0,25 мл в дозах 1 мг/кг, 2 мг/кг, 3 мг/кг, 4 мг/кг, 5 мг/кг; (в несколько тысяч раз превышающих терапевтическую дозу, рекомендуемую для клинического изучения). Животным контрольной группы в том же объеме вводился физиологический раствор.
В течение 72 часов и далее через 14 суток ни в одной группе животных гибели мышей не обнаружено. Не отмечено каких-либо изменений общего состояния, поведения, двигательной активности, волосяного и кожного покрова, физиологических отправлений животных.
Таким образом, тетрапептид Lys-Glu-Asp-Pro в дозах, превышающих терапевтическую, рекомендуемую для клинических испытаний, в несколько тысяч раз, не вызывает острых токсических реакций, что указывает на большую терапевтическую широту препарата.
Исследование подострой токсичности тетрапептида Lys-Glu-Asp-Pro проведено на 48 белых беспородных крысах массой 170-240 г. Ежедневно однократно животным опытных групп вводили препарат внутримышечно в течение 90 дней в дозах 1 мкг/кг, 0,3 мг/кг, 3 мг/кг в 0,5 мл физиологического раствора. Животным контрольной группы вводили в том же объеме физиологический раствор. На протяжении всего периода исследования животные находились под ежедневным наблюдением. Отмечали поведение животных, потребление корма и воды, состояние волосяного покрова и слизистых оболочек. Проводили еженедельное взвешивание животных. До введения препарата, на 30, 60 и 90 сутки после начала введения препарата у животных исследовали морфологический состав и свойства периферической крови. При завершении эксперимента исследовали биохимические и коагулологические показатели крови.
Изучение хронической токсичности тетрапептида Lys-Glu-Asp-Pro проводили на 56 белых беспородных крысах массой 150-270 г. Животным ежедневно вводили внутримышечно препарат в дозах 1 мкг/кг, 0,1 мг/кг, 1 мг/кг в 0,5 мл физиологического раствора в течение 6 месяцев. Отмечали поведение животных, потребление корма и воды, состояние волосяного покрова и слизистых оболочек. Взвешивание животных проводилось ежедневно в первые 3 месяца эксперимента, затем 1 раз в месяц. Через 3 месяца после начала введения и при завершении эксперимента проводили гематологические и биохимические исследования. Оценивали функции сердечно-сосудистой системы, печени, поджелудочной железы, почек и надпочечников. После окончания введения препарата часть животных подвергали патоморфологическому исследованию с целью оценки состояния различных отделов головного и спинного мозга, сердца, аорты, легких, печени, почек, органов эндокринной и иммунной систем.
При оценке общего состояния животных, морфологических и биохимических показателей периферической крови, морфологического состояния внутренних органов, состояния сердечно-сосудистой и дыхательной систем, функции печени и почек патологические изменения в организме не обнаружены. Изучение подострой и хронической токсичности тетрапептида Lys-Glu-Asp-Pro свидетельствует об отсутствии побочных эффектов при длительном применении препарата в дозах, превышающих терапевтическую в 100-1000 раз.
Пример 3. Влияние тетрапептида Lys-Glu-Asp-Pro на развитие эксплантатов мочевого пузыря
Эксперименты проведены на 45 фрагментах мочевого пузыря 10-11-суточных эмбрионов цыпленка. Питательная среда для культивирования эксплантатов состояла из 35% раствора Игла, 25% фетальной сыворотки теленка, 35% раствора Хенкса, 5% куриного эмбрионального экстракта, в среду добавляли глюкозу (0,6%), инсулин (0,5 ЕД/мл), пенициллин (100 ЕД/мл), глутамин (2 мМ). Фрагменты мочевого пузыря помещали в эту среду и культивировали в чашках Петри в термостате при 36,7oС в течение 2 суток. В экспериментальную среду добавляли тетрапептид в концентрациях 2, 10, 20, 50, 100, 200, 400 нг/мл. Критерием биологической активности служил индекс площади (ИП) - отношение площади всего эксплантата вместе с зоной роста к исходящей площади фрагмента мочевого пузыря. Значения ИП выражали в процентах, контрольное значение ИП принималось за 100%. На фиг. 1 показано влияние тетрапептида на развитие эксплантатов мочевого пузыря.
Установлено, что через 1 сутки культивирования происходило распластывание эксплантатов на коллагеновой подложке и начиналось выселение пролиферирующих и мигрирующих клеток по периферии эксплантата. На 3-и сутки культивирования при концентрации тетрапептида 20 нг/мл наблюдалось достоверное повышение ИП эксплантатов на 23% по сравнению с контрольными значениями ИП (фиг. 2). При исследовании эксплантатов мочевого пузыря на более длительных сроках культивирования (7 дней) были выявлено аналогичное стимулирующее действие тетрапептида в той же концентрации.
Таким образом, тетрапептид Lys-Glu-Asp-Pro оказывает стимулирующее регуляторное действие на рост эксплантатов мочевого пузыря.
Пример 4. Влияние тетрапептида Lys-Glu-Asp-Pro на течение экспериментального хронического простатита
Исследование проведено на 41 белых беспородных крысах-самцах со средней массой тела 230 г. Бактериальный простатит у крыс вызывали путем трансуретрального введения суспензии энтеротоксигенной E. coli К-2935 (01: К1: Н-). Под легким эфирным наркозом животным после обработки наружного отверстия уретры 70% спиртом вводили в мочеиспускательный канал смазанный глицерином катетер, через который шприцом инсталлировали 0,2 мл взвеси бактерий (109 КФЕ/мл). Контрольным животным через катетер вводили по 0,2 мл 0,9% физиологического раствора. Через 45 дней после бактериального заражения крысам с развившимся хроническим простатитом начинали вводить ежедневно подкожно тетрапептид Lys-Glu-Asp-Pro в дозе 0,1 мкг на инъекцию. Введение препарата продолжали в течение 10 дней. Контрольные группы состояли из интактных животных, животных с хроническим простатитом без лечения и крыс, получавших по аналогичной схеме инъекции 0,9% физиологического раствора.
Все крысы были умервщлены путем декапитации на 70 день опыта. Животных подвергали полной аутопсии, тщательно осматривали яички и их придатки, предстательную железу, семенные пузырьки, бульбоуретральные железы, мочевой пузырь, почки с мочеточниками, а также остальные внутренние органы. Для гистологического исследования вентральную часть предстательной железы фиксировали в 10% нейтральном формалине и после стандартной проводки через серию растворителей заливали в парафин. Срезы тканей толщиной 5-7 мкм окрашивали гематоксилин-эозином.
Для сравнения выраженности простатита в различных группах была разработана следующая 5-балльная шкала:
1 балл - следы простатита (мелкие очаги фиброза, интерстициальной лимфоцитарной и гистиоцитарной инфильтрации);
2 балла - очаги хронического простатита с воспалительной инфильтрацией (в основном интерстициальной), занимающие менее 1/4 среза железы;
3 балла - очаги простатита с крупными воспалительными инфильтратами вокруг протоков, ацинусов и кровеносных сосудов, со скоплением лейкоцитов в просветах желез, занимающие 1/4-1/2 среза железы;
4 балла - выраженный простатит, захватывающий 1/2-3/4 среза железы;
5 баллов - резко выраженный простатит с поражением более 3/4 среза железы.
Участки предстательной железы брали также для электронно-микроскопического исследования и изучения содержания цинка, который входит в состав соединений, обладающих антимикробной активностью.
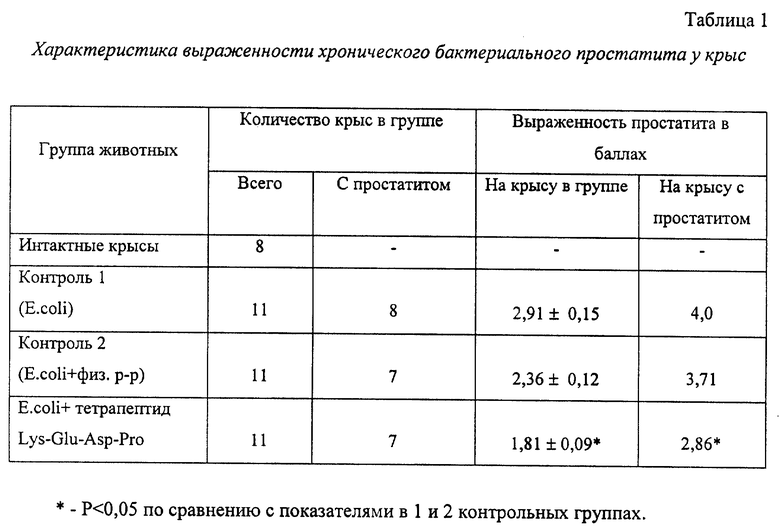
В результате проведенного исследования установлено, что применение тетрапептида Lys-Glu-Asp-Pro в 7 случаях из 11 способствовало положительной динамике воспалительного процесса в предстательной железе. При гистологическом изучении препаратов железы отмечались в основном признаки хронического воспаления, захватывающие менее 1/2 среза железы. При этом в большинстве протоков и ацинусов воспалительные инфильтраты не были обнаружены. Средний балл выраженности простатита составил 1,81±0,09, как видно из таблицы 1.
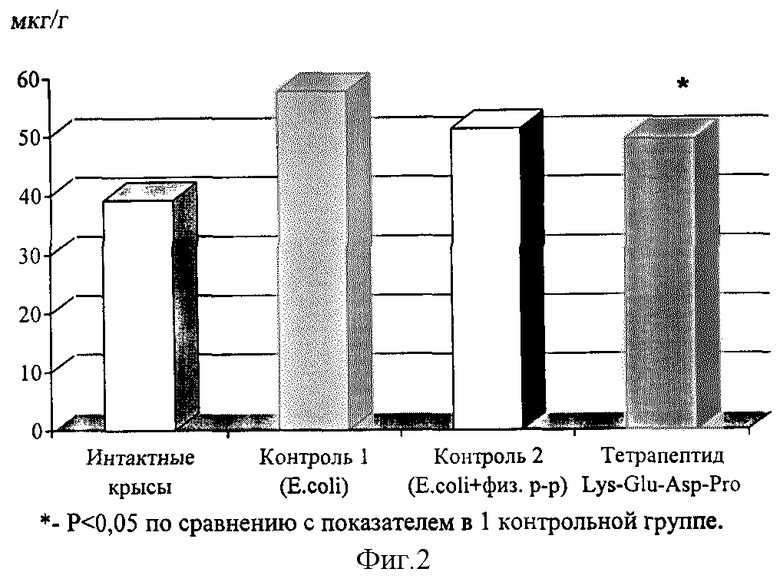
Содержание цинка в ткани предстательной железы увеличивалось в зависимости от выраженности простатита. На фиг. 2 показано влияние тетрапептида Lys-Glu-Asp-Pro на концентрацию цинка в ткани предстательной железы крыс с хроническим бактериальным простатитом.
После применения тетрапептида средняя концентрация цинка снижалась (фиг. 2), что коррелировало с показателем выраженности простатита.
Таким образом, применение тетрапептида Lys-Glu-Asp-Pro способствовало активизации реакций местного иммунитета, повышению антимикробной защиты ткани предстательной железы, что сопровождалось уменьшением воспалительных реакций.
Пример 5. Влияние тетрапептида Lys-Glu-Asp-Pro на процессы свободнорадикального окисления у старых крыс
Одними из наиболее характерных признаков старения являются нарушения антиоксидантной защиты и нейрогуморальной регуляции функций организма, сопровождающиеся в том числе инволюцией половых желез.
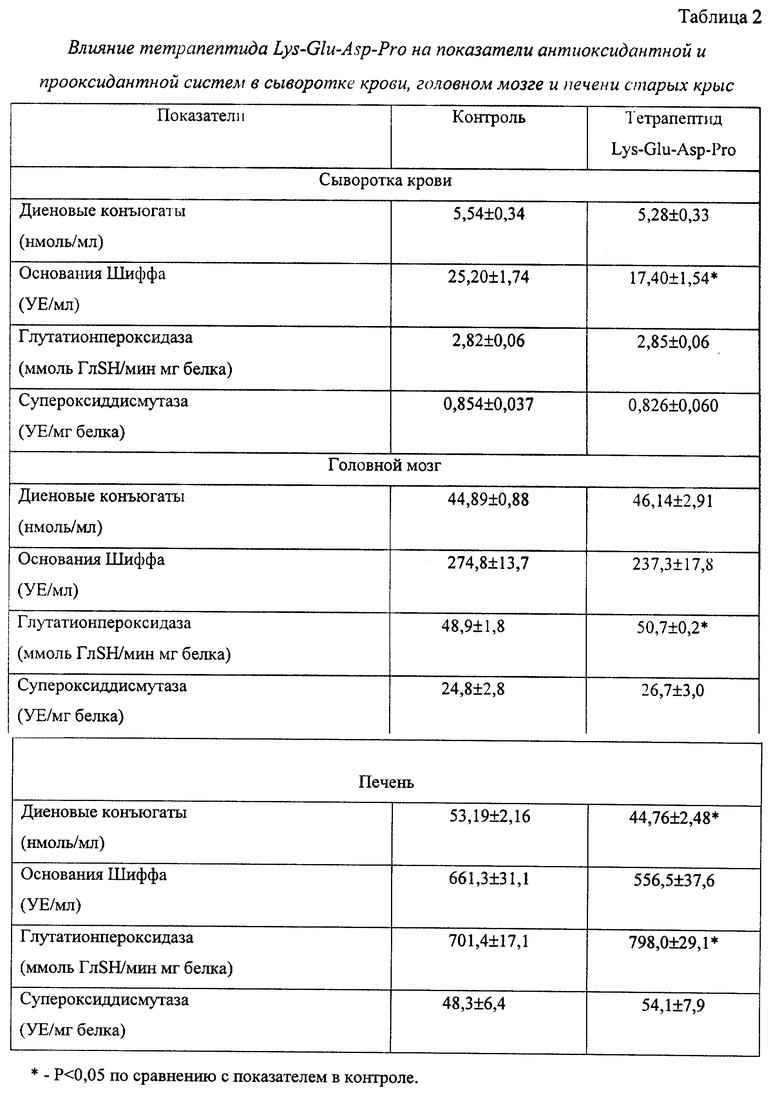
Исследование влияния тетрапептида Lys-Glu-Asp-Pro на процессы свободнорадикального окисления проведено на 18 крысах-самцах в возрасте 24 мес. Тетрапептид вводили животным подкожно в течение 10 дней в дозе 0,1 мкг на инъекцию. Животные контрольной группы по аналогичной схеме получали инъекции 0,9% физиологического раствора. Умерщвление крыс осуществляли на следующий день после окончания введения препарата. После этого готовили образцы тканей головного мозга, печени и сыворотки крови. В приготовленных образцах по уровню содержания диеновых конъюгатов и оснований Шиффа исследовали интенсивность перекисного окисления липидов (ПОЛ). Определяли также активность глутатионпероксидазы и супероксиддисмутазы, используя метод подавления биологическим материалом окисления нитросинего тетразолия.
В результате проведенного исследования установлено, что применение тетрапептида Lys-Glu-Asp-Pro вызывало снижение образования первичных продуктов ПОЛ-диеновых конъюгатов в печени и конечных продуктов ПОЛ-оснований Шиффа в сыворотке крови. Вместе с тем тетрапептид оказывал также достоверное действие и на ферментативное звено антиоксидантной системы в печени и головном мозге. В печени тетрапептид Lys-Glu-Asp-Pro вызывал повышение активности глутатионпероксидазы, а в головном мозге повышение активности супероксиддисмутазы.
Таким образом, применение тетрапептида Lys-Glu-Asp-Pro у старых крыс-самцов оказывает нормализующее действие на механизмы антиоксидантнои защиты, связанные с возрастными инволютивными изменениями органов репродуктивной системы.
В результате экспериментального изучения установлено, что тетрапептид Lys-Glu-Asp-Pro не обладает токсичностью, стимулирует рост эксплантатов мочевого пузыря, способствует активизации реакций местного иммунитета, нормализации метаболических процессов и микроциркуляции в предстательной железе, обладает антиоксидантным действием.
Выявленные в результате экспериментального доклинического исследования свойства тетрапептида Lys-Glu-Asp-Pro позволяют считать показанным его профилактическое и/или лечебное применение в качестве лекарственного средства для лечения заболеваний предстательной железы, сопровождающихся воспалительными и дизурическими нарушениями.
Приведенные ниже примеры результатов клинического изучения заявляемого тетрапептида демонстрируют его фармакологические свойства и подтверждают возможность достижения терапевтического эффекта путем введения фармакологического средства, содержащего тетрапептид Lys-Glu-Asp-Pro (или его соли).
Пример 6. Эффективность применения фармакологического средства, содержащего тетрапептид Lys-Glu-Asp-Pro, у больных хроническим простатитом
Исследование эффективности клинического применения фармакологического средства проведено у 35 больных хроническим простатитом в возрасте 23-45 лет.
Основными проявлениями хронического простатита были ноющие боли типичной локализации, различные нарушения мочеиспускания, расстройства способности к совершению половых сношений и признаки невротического состояния.
Все больные ранее получали традиционные лекарственные средства симптоматического и патогенетического действия, при применении которых отмечался кратковременный терапевтический эффект, требующий увеличения дозы препаратов на курс лечения и продолжительного их приема. Фармакологическое средство вводили внутримышечно 1 раз в день в дозе 0,01- 100 мкг/кг массы тела в течение 10-40 дней в зависимости от степени тяжести заболевания. Контрольная группа состояла из 14 аналогичных больных, которым назначалось традиционное лечение.
Эффективность лечения фармакологическим средством оценивали на основании динамики жалоб больных, общеклинического исследования крови и мочи, биохимического изучения крови, коагулограммы крови до и после окончания лечения. Степень брюшного давления при мочеиспускании и характер струи мочи выражали в баллах от 1 до 5 (1 - норма, 5 - наибольшие изменения показателя). Определяли максимальную, среднюю скорость и время мочеиспускания, время достижения максимальной скорости мочевыделения, оценивали флуорометрический индекс. Наряду с вышеуказанными исследованиями производили пальпаторную оценку предстательной железы, лабораторное исследование ее секрета, более углубленное изучение состояния копулятивной функции. Проводили также ультразвуковое исследование предстательной железы.
Основное внимание при оценке результатов лечения хронического простатита было уделено клиническим критериям. По окончании лечения болевые ощущения полностью исчезали у 64,0% и значительно уменьшались у 32,7% больных, предъявляющих соответствующие жалобы. У 3,3% больных лечение не дало ожидаемого эффекта, и динамики болевых ощущений не наблюдалось. Из числа больных, страдающих нарушением половой функции, 44,4% указали на полное ее восстановление и 41,8% отметили улучшение. Положительное действие препарата проявлялось как относительно улучшения качества эрекции, так и усиления оргазма и ликвидации его болезненности. Отмечалось также увеличение продолжительности полового акта. К концу лечения 37,1% больных сообщили о восстановлении либидо.
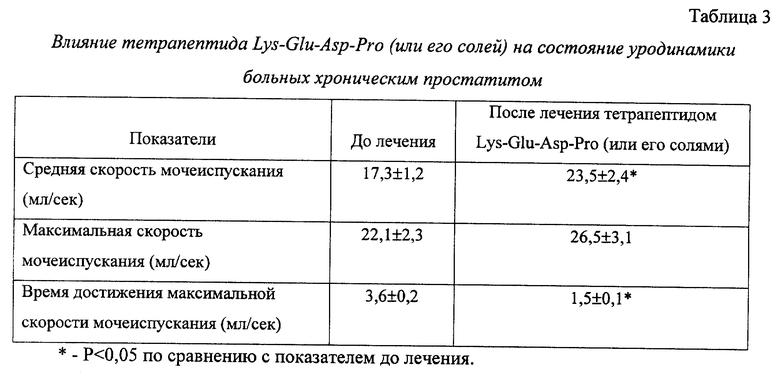
Поллакиурия (учащение мочеиспускания) полностью перестала беспокоить 87,5% больных. Исчезла потребность ночного мочеиспускания. Странгурия (затрудненное мочеиспускание) перестала беспокоить 80,7% больных, 15,9% отметили заметное усиление струи мочи и облегчение акта мочеиспускания. Суммарные сведения об изменении акта мочеиспускания у больных хроническим простатитом после лечения фармакологическим средствoм представлены в таблице 3.
Следует отметить, что урофлуограммы, записанные после лечения у больных хроническим простатитом I и II стадии, показали восстановление основных параметров мочеиспускания до нормальных значений. При III стадии болезни этому препятствовало снижение эластичности шейки мочевого пузыря из-за склеротических изменений ткани предстательной железы, тем не менее у них наблюдалось заметное усиление струи мочи. При пальпации предстательной железы через прямую кишку определялась тенденция к восстановлению ее размеров и консистенции после лечения фармакологическим средством. При этом исчезали участки уплотнения, а само исследование становилось безболезненным. Наблюдавшееся уменьшение размеров предстательной железы, расцениваемое как результат уменьшения отека межуточной ткани и свидетельствующее о ликвидации активности воспалительного процесса в ней, подтверждалось и результатами ультразвуковой диагностики. Выполненные в динамике общеклинические и биохимические исследования крови не выявили каких-либо существенных отклонений от нормальных показателей.
Благодаря восстановлению функции предстательной железы под влиянием фармакологического средства наблюдалось улучшение свойств ее секрета. Это обеспечивало увеличение содержания подвижных сперматозоидов в эякуляте на 11,8%. Снижение активности воспалительного процесса подтверждалось уменьшением количества лейкоцитов в эякуляте, секрете предстательной железы и моче. Одновременно наблюдалось уменьшение в исследуемом материале содержания клеток спущенного эпителия.
Пример 7. Эффективность применения фармакологического средства, содержащего тетрапептид Lys-Glu-Asp-Pro (или его соли) у больных аденомой предстательной железы
Фармакологическое средство применяли для лечения 19 больных аденомой предстательной железы I-II стадии в возрасте 51-67 лет. Характерными симптомами заболевания у больных аденомой предстательной железы была упорная дизурия, не поддающаяся традиционным методам лечения, ослабленная струя мочи, снижение способности к совершению половых актов. Все больные в течение различного времени получали традиционные лекарственные средства симптоматического и патогенетического действия.
Фармакологическое средство вводили внутримышечно 1 раз в день в дозе 0,01-100 мкг/кг массы тела в течение 10-40 дней в зависимости от клинических проявлений заболевания. Контрольная группа состояла из 17 аналогичных больных, которым назначалось традиционное лечение. Эффективность лечения фармакологическим средством оценивали на основании динамики жалоб больных. Степень брюшного давления при мочеиспускании и характер струи мочи выражали в баллах от 1 до 5 (1 - норма, 5 - наибольшие изменения показателя). Определяли максимальную, среднюю скорость и время мочеиспускания, время достижения максимальной скорости мочевыделения, оценивали флуорометрический индекс. Проводили ультразвуковое исследование предстательной железы. Динамика результатов исследования у больных аденомой предстательной железы до и после окончания курса лечения фармакологическим средством представлена в таблице 4.
Состояние больных аденомой предстательной железы после лечения фармакологическим средством характеризовалось улучшением субъективных и объективных показателей уродинамики. К концу лечения у 37,3% больных отмечалось усиление либидо.
Таким образом, фармакологическое средство, содержащее тетрапептид Lys-Glu-Asp-Pro (или его соли) целесообразно применять для лечения воспалительных заболеваний предстательной железы и дизурических расстройств.
Источники информации
1. Люлько А. В. , Юнда И. О. , Серняк П. С. и др. Заболевания предстательной железы. - Киев: Здоров'я, 1984. - 280 с.
2. Ткачук В. Н. , Горбачев А. Г. , Агулянский Л. И. Хронический простатит. - Л. : Медицина, 1989. -208 с.
3. Машковский М. Д. Лекарственные средства (Пособие для врачей). - М. : Медицина, 1993. Ч. I. 736 с. Ч. II. 688 с.
4. Регистр лекарственных средств России. Изд. шестое. - М. : РЛС-2000, 1998. 1072 с.
5. Якубке Х. -Д. , Ешкайт X. Аминокислоты, пептиды, белки: Пер. с нем. - М. : Мир, 1985. 456 с.

Изобретение относится к области медицины и может быть использовано как средство, регулирующее функции предстательной железы. Предлагается биологически активное соединение общей формулы Lys-Glu-Asp-Pro, обладающее способностью регулировать функции предстательной железы, и фармакологичecкoe средство, содержащее в качестве активного начала эффективное количество тетрапептида формулы Lys-Glu-Asp-Pro или его солей, предназначенное для парентерального введения. Согласно изобретению способ регулирования функции предстательной включает лечебное введение пациенту фармакологического средства в дозах 0,01-100 мкг/кг массы тела по крайней мере один раз в день в течение периода, необходимого для достижения терапевтического эффекта. Технический результат: средство обладает способностью регулировать функции предстательной железы, нормализует метаболизм и микроциркуляцию в предстательной железе, обладает антиоксидантным действием. 4 с. и 5 з. п. ф-лы, 2 ил. , 4 табл.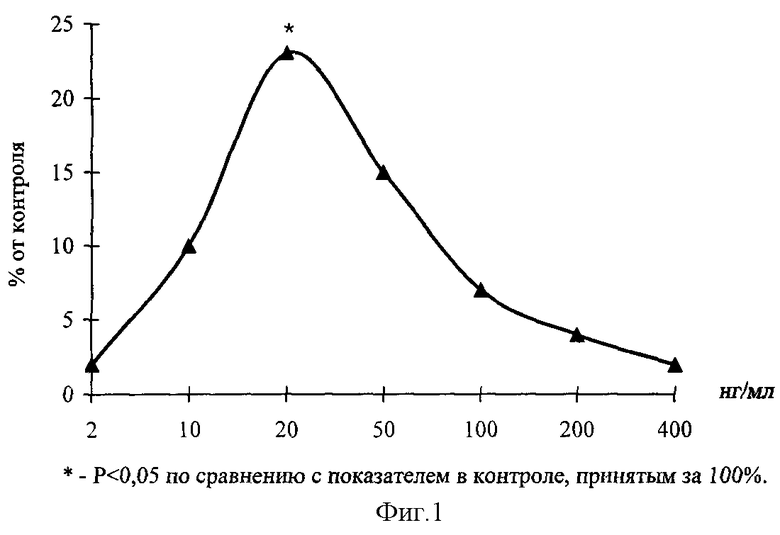
| Регистр лекарственных средств России | |||
| Энциклопедия лекарств | |||
| Изд | |||
| шестое | |||
| ЩИТОВОЙ ДЛЯ ВОДОЕМОВ ЗАТВОР | 1922 |
|
SU2000A1 |
| Способ получения тетрапептидов или их кислотно-аддитивных солей | 1981 |
|
SU1082319A3 |
| Устройство для учета длины и количества вырабатываемых на протяжных станках труб | 1939 |
|
SU61788A1 |
| Приспособление для перегрузки штучных грузов с кареток подвесной железной дороги на повозки | 1927 |
|
SU7604A1 |
| US 4005194 А1, 23.06.1975 | |||
| ФОРМА ДЛЯ ИЗГОТОВЛЕНИЯ ИЗДЕЛИЙ ИЗ БЕТОНА | 2002 |
|
RU2228262C2 |
| EP 0799241 А1, 08.10.1997 | |||
| Установка для активации цементной суспензии | 1982 |
|
SU1065214A1 |
Авторы
Даты
2002-01-10—Публикация
2001-01-25—Подача