В последнее десятилетие механическая травма, наряду с онкологической и сердечно - сосудистой патологией, превратилась в одну из ведущих проблем медицины. В наиболее дееспособном возрасте травма и ее осложнения находятся на первом месте среди причин летального исхода [Цибуляк В.Н., 1984, 1995]. В общей структуре современного политравматизма особенно часто повреждаются конечности, череп, органы грудной клетки и таза, то есть сочетанные и множественные повреждения с развитием синдрома взаимного отягощения. Патогенетические факторы при современных исследованиях гиповолемического шока представляют собой сложную структуру нарушения витальных функций по дифференцированному типу (депрессия гемодинамики, внешнего дыхания), поражения микроциркуляторной системы (кризис периферической циркуляции, коагулопатия), что в конечном итоге приводит к поражению системного метаболизма [Зильбер А.П., 1984] . Тканевая гипоксия и дизоксия, анаэробный гликолиз, поражение эндотелиальной проницаемости, тканевые метаболиты (оксид азота, аденилаты, каллекреин - кининовая система, эйкосаноиды) и многие другие факторы приводят в конечном итоге к нарушению энергообеспечения ткани и клетки, снижению интенсивности синтеза АТФ и макроэргов [Кулагин В.К., 1981; Дерябин И.И., 1987]. В период восстановления кровотока (реперфузия) наблюдается эффекты ионного, кальциевого парадокса. И в ишемизированной ткани, и в период восстановления перфузии капиллярона активизируются эффекты перекисного окисления липидов, с одновременным угнетением антиоксидантной активности [Зильбер А.П., 1995]. Все перечисленное ведет к усугублению течения гиповолемического шока, и развитию полиорганной недостаточности. При проведении интенсивной терапии немаловажное значение имеет дифференцированная коррекция нарушений метаболизма, исходя из положения, что организм на шокогенную травму (и любой стресс) реагирует по трем вариантам: гиперергическому, нормоэргическому и гипоэргическому. Выяснение характера реагирования ведет к назначению таких групп препаратов, которые были способны селективно угнетать или интенсифицировать метаболизм тканей, что в конечном итоге приводит к оптимизации терапии и повышению выживаемости больных. В подобных условиях немаловажное значение приобретает такой неинвазивный мониторинг витальных функций, который сопровождается возможностью контроля регуляторной активности нервной системы [Астахов А.А., 1996].
Такой тип мониторинга в сочетании с уже известным методом реовазографии, способен более точно подходить к особенностям энергообеспечения и коррекции.
Известен способ проведения кардиоритмографии с математическим анализом сердечного ритма с последующей оценкой вегетативного статуса организма. По характеру и выраженности вегетативной регуляции судят об адекватности терапии операционного стресса и проводимого анестезиологического пособия [Баевский P.M., Кириллов О.И., Клецкин С.З. Математический анализ изменений сердечного ритма при стрессе. - М.: Наука. - 1984. - С.93-116]. Недостатком этой методики являются: отсутствие анализа мощности колебаний по трем диапазонам спектра - энергетики регуляции, не предлагаются варианты коррекции измененных состояний вегетативной структуры, описание способа предлагается только в условиях анестезиологического пособия.
Известен способ математического анализа вариабельности параметров гемодинамики (ударный объем, фракция выброса, амплитуда пульсации трех классов сосудов) с характеристиками гипердинамического и гиподинамического типов реагирования у больных реанимационного профиля и пациентов в условиях наркоза, которые сопровождались изменениями тонуса вегетативной нервной системы в сторону симпатикотонии или парасимпатикотонии [Астахов А.А. Физиологические основы биоимпедансного мониторинга гемодинамики в анестезиологии с помощью системы "Кентавр". - Челябинск. - 1996. - С.62-83]. Недостатком способа является отсутствии дифференцированного подхода к коррекции измененных энергетических состояний и биохимических исследований, которые бы подтверждали характер изменения энергетики регуляции.
Известен способ спектрального анализа вариабельности кардиоритма, с разделением исследуемых больных на три группы по уровню энергетики спектральной плотности мощности (гиперадаптивное состояние, энергодефицитное состояние и нормальные показатели). Назначение препаратов для терапии заболеваний сердечно-сосудистой системы корригировалось по данным кардиоритмографии [Флейшман А.Н. Классификация спектральных показателей медленных колебаний гемодинамики - основа прогноза, патогенетической терапии и оценки функционального состояния человека//Сборник трудов симпозиума "Медленные колебательные процессы в организме человека: теория, практическое применение в клинической медицине и профилактике". - Новокузнецк. - 1997. - С.24-34]. Недостатком этого метода является описание последнего только для вариантов терапевтической патологии и отсутствие связи типов реагирования регуляции и показателей системной гемодинамики.
Наиболее близким к заявляемому является способ внутривенного введения даларгина с целью коррекции реакции организма при геморрагическом шоке и острой массивной кровопотере. При этом гиперергическая реакция организма приобретает характер нормоэргической [Шерман Д.М., Грач В.М. Влияние внутривенного введения даларгина на течение и исход реакции организма на острую массивную кровопотерю // Патологическая физиология и экспериментальная терапия. - 1995, 2. - С. 30-32].
Недостатком данного способа является отсутствие четкого контроля за эффективностью изменения реакции организма, неэффективность способа при констатации гипоэргического типа реакции кровообращения при шоке.
Задача данного изобретения - повысить эффективность проводимых противошоковых мероприятий на основе дифференцированного назначения препаратов, корригирующих метаболизм у больных с тяжелой сочетанной травмой, по данным спектрального анализа вариабельности сердечного ритма.
Поставленная задача достигается тем, что дополнительно к проводимой противошоковой терапии проводится ритмокардиографический мониторинг вариабельности сердечного ритма и при гиперергическом типе реагирования и значениях спектральной плотности мощности больше 130 мс2/Гц больному вводят даларгин в дозе 1-2 мкг/кг массы тела внутривенно болюсно однократно, а при гипоэргическом типе реагирования и значениях спектральной плотности мощности кардиоритма меньше 25 мс2/Гц больному вводят неотон в дозе 60 мг/кг массы тела инфузионно однократно.
Новизна способа:
1. Определение типа реагирования по данным вариабельности кардиоритма в условиях гиповолемического шока позволяет обеспечить проведение дифференцированной метаболической коррекции. На основе конкретных показателей спектрального анализа вариабельности кардиоритма (спектральная плотность мощности и частота колебаний) возможно разделить исследуемых пациентов на три группы по реагированию - гиперергическую, нормоэргическую и гипоэргическую, и на две группы по типу вегетативной регуляции - парасимпатическую и симпатическую. На основе типов реагирования проводят терапию по коррекции метаболизма, целью которой является повышение или понижение интенсивности процесса энергообеспечения. Подтверждением возможности проводить подобные исследования и оценивать энергообеспечение по данным ритмокардиографии является параллельное изучение показателей реовазографии (сердечный индекс), при этом мы получили сильную коррелятивную связь между показателями спектральной плотности мощности (СПМ) и сердечного индекса. Гиперергическому типу реагирования соответствует гиперкинетический тип гемодинамики, гипоэргическому варианту реагирования - гипокинетический тип гемодинамики.
2. Выбранные значения спектральной плотности мощности подтверждены проведенным комплексом биохимических исследований, ведущим показателем среди всех тестов является артериовенозный градиент АТФ. В случае гиперергического типа реагирования получен показатель градиента с отрицательным знаком, что свидетельствует об эффекте интенсивного расходования (катаболизма) макроэргических фосфатов в тканях. Гипоэргический тип характеризуется градиентом с положительным знаком, что является подтверждением нарушенного потребления АТФ в тканях и клетках, снижением интенсивности метаболизма и развитием энергодефицита по типу гипоэргоза.
3. Введение препарата даларгин в группе больных с гиперергическим типом реагирования обусловлено тем, что даларгин в дозе 1-2 мкг/кг массы тела обеспечивает подавление интенсивности метаболических процессов, предотвращает эффект повышенного расходования АТФ, снижает интенсивность процессов перекисного окисления липидов, что, по данным ритмокардиографии, проявляется снижением показателей СПМ до уровня нормальных цифр (25 - 130 мс2/Гц) и нормализацией сердечного индекса по данным реографии.
4. Введение препарата неотон (экзогенный фосфокреатинин) в группе больных с гипоэргическим типом реагирования обусловлено тем, что неотон в дозе 60 мг/кг массы тела обеспечивает повышение интенсивности метаболических процессов, увеличивает содержание АТФ и иных макроэргических источников в тканях, модулирует интенсивность процессов перекисного окисления липидов, что, по данным ритмокардиографии, проявляется повышением показателей СПМ до уровня нормальных цифр (25 -130 мс2/Гц) и нормализацией сердечного индекса по данным реографии.
Сущность способа заключается в следующем: при поступлении пациента с тяжелой множественной сочетанной травмой, осложненной травматическим шоком II -III ст. по классификации Кейта, обследуют по методике кардиоритмографии, интегральной реовазографии и проводят комплекс биохимических тестов (показатели перекисного окисления липидов, антиоксидантная активность крови, показатели липидного обмена, молочная и пировиноградная кислота, концентрация АТФ и неорганического фосфора). Кардиоритмографию записывают на трех этапах: при поступлении, через 6-8 часов и через сутки после начала интенсивной терапии. Кардиоритмограмма подвергается спектральному анализу, в котором основными являются две характеристики: частотно-спектральная и амплитудно-спектральная. Оценивается три пика спектра по частоте:
- очень низкая частота (VLF - уегу low frequency) в диапазоне 0...0,04 Гц,
- низкая частота (LF - iow frequency) в диапазоне 0,04...0,15 Гц,
- высокая частота (HF - high frequency) в диапазоне 0,15...0,5 Гц.
Амплитудная характеристика вычисляется в единицах спектральной плотности мощности - СПМ (мс2/Гц).
Для оценки вегетативной регуляции определяли преобладание СПМ в диапазонах высокой (парасимпатическая) или низкой (симпатическая) частот.
Оценка энергетики спектра проводилась в диапазоне очень низкой частоты колебаний [Флейшман А.Н., 1997]. При этом состояние выше 130 мс2/Гц расценивали как гиперэргический тип, состояние ниже 25 мс2/Гц - как гипоэргический тип. Определение СПМ в пределах нормы (25 - 130 мс2/Гц) характеризовали как нормоэргический тип регуляции. Среди всех биохимических параметров наиболее информативным оказался показатель артериовенозного градиента АТФ как характеризующий энергообеспечение ткани и состояние распада или синтеза (катаболизма или анаболизма) макроэргических молекул. Гиперергическому типу реакции соответствует отрицательный градиент АТФ, что объясняется повышенным распадом макроэрга в тканях, массивным его потреблением. Гипоэргический тип характеризуется положительным знаком артериовенозной разницы АТФ, что свидетельствует о нарушениях утилизации АТФ, снижении интенсивности обменных процессов. В обоих случаях имеет место повышенное содержание продуктов перекисного окисления липидов, снижение активности антиоксидантной активности, накопление молочной кислоты.
Сердечный индекс в динамике исследования оказался признаком, имеющим сильную корреляционную связь с показателями СПМ. При этом гиперергический тип по кардиоритмограмме соответствовал гиперкинетическому варианту гемодинамики, гипоэргический тип - гипокинетическому варианту кровообращения. При исследовании артериовенозного градиента АТФ получили прямую сильную связь между значениями последнего и характером реагирования энергетики регуляции. Таким образом, для оценки энергообеспечения организма имеется возможность применять только инструментальные неинвазивные методы мониторинга (в частности показатели СПМ при исследовании спектра медленных колебаний), без сочетанного применения биохимических тестов определения АТФ в крови.
После первичного обследования больного (на этапе исходного состояния при поступлении) мы проводили - в дополнение к общепринятой терапии шока - введение препаратов для дифференцированной коррекции метаболизма.
При наличии у больного гиперергического типа реагирования (высокие цифры СПМ, повышение сердечного индекса, отрицательный показатель градиента АТФ) больному вводился даларгин в дозе 1-2 мкг/кг массы тела внутривенно болюсно. В анестезиологическом пособии предпочтение отдавалось барбитуратам ультракороткого типа действия или пропофолу. Препараты подавляют гиперергическую реакцию катаболизма основных макроэргов, снижают уровень обменных процессов, переводя регуляцию и метаболизм на нормальный уровень функционирования.
При появлении у больного гипоэргического типа реагирования в комплекс интенсивной терапии вводился неотон (экзогенный фосфокреатинин) в дозе 60 мг/кг массы тела инфузионно, гипертонический раствор натрия хлорида и кетамин как препарат выбора для обезболивания в периоперационном периоде. Отмечался значительный подъем СПМ, увеличение сердечного индекса до нормальных цифр. Гипоэргический тип переходил в нормоэргический.
При нормальных показателях кардиоритмограммы, реовазограммы и артериовенозной разницы АТФ, то есть нормоэргическом типе реагирования проводили общепринятую терапию гиповолемического шока без добавления препаратов дифференцированной метаболической коррекции.
Пример 1. Больной Б., 23 года, поступил в отделение догоспитальной реанимации с диагнозом: сочетанная множественная травма: ушиб головного мозга средней степени тяжести, перелом основания черепа, сквозное ранение левой гайморовой пазухи, проникающее ранение левого глазного яблока, закрытый перелом левой бедренной кости, закрытый перелом обеих костей левой голени, травматическая болезнь в стадии травматического шока III ст. При поступлении состояние тяжелое, сознание угнетено до уровня сопор - кома I, оценка по шкале Глазго 7 баллов, нестабильная гемодинамика, АД 60/40 мм рт.ст., тахикардия до 120 в минуту брадипное до 8 в минуту, SaO2 80%. Проведены первичные реанимационные мероприятия. Исходная запись реовазограммы - гиперкинетический вариант гемодинамики, по данным кардиоритмограммы - гиперергическая регуляция с преобладанием тонуса симпатического отдела вегетативной нервной системы. Интенсивная противошоковая терапия составила 5200 мл, кортикостероиды. При записи ритмографических и реовазографических показателей через 7 часов от начала интенсивной терапии характер регуляции и гемодинамики не изменился, отмечено значительное повышение СПМ в диапазоне очень низкой частоты - до 700 мс2/Гц. Выполнена операция: ПХО ран лицевого скелета, репозиция переломов голени. Состояние больного после поступления в отделение реанимации из операционной оставалось тяжелым. На первые сутки фиксировался гиперергический тип кардиоритмограммы и гиперкинетический вариант гемодинамики. Отмечали постоянное преобладание симпатического типа регуляции на протяжении всего послеоперационного периода. (см. табл.1).
Больной в течение 3 суток находился на ИВЛ, в коме, оценка по шкале Глазго 5 баллов, нестабильная гемодинамика отмечалась через сутки после оперативного вмешательства. На фоне продолжающихся реанимационных мероприятий на 4 сутки нахождения в отделение реанимации отмечен летальный исход. Специфической дифференциальной метаболической коррекции не проводилось.
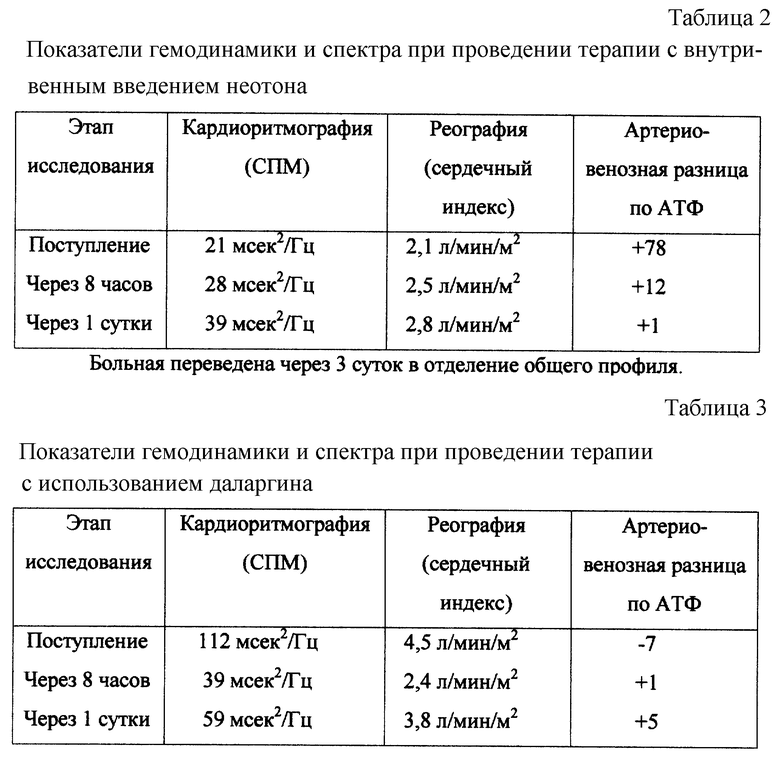
Пример 2. Больная Т., 70 лет, поступила в отделение догоспитальной реанимации с диагнозом: сочетанная множественная травма: закрытый перелом правой бедренной кости, закрытый перелом обеих костей левого предплечья, перелом лонной и седалищной костей с обеих сторон, травматическая болезнь в стадии травматического шока II ст. Состояние больной тяжелое, сознание ясное, заторможена, гемодинамика нестабильная, АД 90/40 мм рт.ст., тахикардия до 110 в минуту, тахипное до 24 в минуту, SaO2 90%. При поступлении по данным реовазографии отмечали гипокинетический вариант гемодинамики, по записи ритмокардиограммы - гипоэргический тип реагирования с преобладанием симпатической регуляции. Больной по данным исследования регуляции и энергетики в состав общепринятой противошоковой интенсивной терапии ( инфузионно-трансфузионная, коррекция нарушений КЩС, обезболивание опиоидными агонистами) включены следующие препараты для дифференцированной коррекции метаболизма: кетамин в дозе 100 мг в/в, неотон в виде в/в инфузии 2000 мг в течение 1 часа. После проведения дифференцированной терапии показатели СПМ в кардиоритмографическом исследовании повысились до нормоэргического варианта энергетики регуляции, тип гемодинамики зафиксирован нормокинетической. В последующем больной проведена иммобилизация переломов наложением скелетного вытяжения, состояние больной стабилизировалось, переведена из противошоковой палаты в отделение реанимации. Динамическое наблюдение через сутки показало наличие у больной нормоэргического типа реакции энергетики и сохранение парасимпатического варианта регуляции (см. табл.2 и 3).

Изобретение относится к медицине, анестезиологии. У больного с тяжелой травмой записывают кардиоритмограмму. Проводят ее спектральный анализ. Определяют спектральную плотность мощности (СПМ) в диапазоне очень низких частот с выявлением гиперэргического, нормоэргического и гипоэргического типов реагирования. При гиперергическом типе реагирования и значениях СПМ больше 130 мс2 больному вводят даларгин в дозе 1-2 мкг/кг массы тела внутривенно болюсно однократно. При гипоэргическом типе реагирования и значениях СПМ меньше 25 мс2 больному вводят неотон в дозе 60 мг/кг массы тела инфузионно однократно. Способ позволяет повысить эффективность проводимых противошоковых мероприятий на основе дифференцированного назначения препаратов, корригирующих метаболизм у больных с тяжелой сочетанной травмой. 3 табл.
Способ метаболической коррекции в комплексе интенсивной терапии гиповолемического шока путем подбора медикаментозных препаратов, отличающийся тем, что дополнительно к проводимой противошоковой терапии проводят спектральный анализ вариабельности медленных колебаний кардиоритма, и при гиперергическом типе реагирования и значениях спектральной плотности мощности больше 130 мс2/Гц больному вводят даларгин в дозе 1 - 2 мкг/кг массы тела внутривенно болюсно однократно, а при гипоэргическом типе реагирования и значениях спектральной плотности мощности кардиоритма меньше 25 мс2/Гц больному вводят неотон в дозе 60 мг/кг массы тела инфузионно однократно.
| RU 20686500 С1 (МИРОНОВ В.А.), 19.03.1997 | |||
| ШЕРМАН Д.М., ГРАЧ В.М | |||
| Влияние внутривенного введения даларгина на течение и исход реакции организма на острую массивную кровопотерю | |||
| - Патологическая физиологическая и экспериментальная терапия, 1995, № 2, с | |||
| Способ обработки медных солей нафтеновых кислот | 1923 |
|
SU30A1 |
| МИХАЙЛОВ Н.Н., СЛЕПУШКИН В.Д | |||
| Фармакологические подходы к терапии метаболических нарушений при травматическом шоке в эксперименте | |||
| Сб.: Экспериментальные, клинические и организационные проблемы общей реаниматологии | |||
| - М., 1996, с | |||
| Гидравлический способ добычи торфа | 1916 |
|
SU206A1 |
| ПЕРЕПАЧ Н.Б и др | |||
| Применение неотона для профилактики сердечной недостаточности у больных инфарктом миокарда | |||
| - Клиниче ская медицина, 1997, 75, №10, с | |||
| Устройство для устранения мешающего действия зажигательной электрической системы двигателей внутреннего сгорания на радиоприем | 1922 |
|
SU52A1 |
Авторы
Даты
2002-04-27—Публикация
1998-12-15—Подача