В последние три десятилетия существенные усилия направлены на идентификацию способов контроля скорости освобождения лекарственного средства из фармацевтических таблеток. Для контроля растворения, а следовательно, абсорбции лекарственных средств, в ядра таблеток вводят наполнители. Таблетки и сфероиды покрывают полимерами для обеспечения медленного, диффузионно-контролируемого освобождения или освобождения в конкретном месте лекарственных средств.
Кроме того, были получены дозированные лекарственные формы в виде таблеток и капсулированных сфероидов, содержащие составные лекарственные средства либо в смеси, либо в виде отдельных слоев таблеток или сфероидов. Разработаны лекарственные средства, которые осуществляют сложные функции или обеспечивают синергизм. Такие таблетки особенно полезны в тех обстоятельствах, когда обычная терапия диктует использование более чем одного лекарственного средства, обладающего различными, но совместимыми активностями. Например, диуретические средства часто применяют вместе с гипотензивными средствами, а средства, способствующие сохранению беременности, в сочетании с эстрогенами.
В соответствии с данным изобретением разработана фармацевтическая таблетка, содержащая внутреннее спрессованное ядро и наружное сахарное покрытие, где указанное спрессованное ядро необязательно содержит одно или более нестероидных фармакологически активных средств, которые обычно применяют в сочетании с гормональным стероидом либо не содержат этих средств, и улучшение заключается во включении в указанное сахарное покрытие гормонального стероида и микрокристаллической целлюлозы в количестве, контролирующем скорость освобождения гормонального стероида.
Спрессованное ядро таблетки может быть лишено какого-либо лекарственного средства или оно может содержать фармацевтическое средство, другое, чем стероид, которое совместимо со стероидом и каким-либо другим терапевтический средством в сахарном покрытии. Так, покрытые сахаром таблетки данного изобретения могут содержать одно или более фармакологически активных средств, в тех случаях, когда улучшение покрытых сахаром таблеток предшествующего уровня техники состоит во включении некоторого количества микрокристаллической целлюлозы, контролирующего скорость освобождения гормонального стероида в сочетании с гормональным стероидом в указанное сахарное покрытие. Покрытая сахаром таблетка может быть в завершение всего покрыта цветными покрытиями и полирована, как принято для покрытых таблеток.
Содержимое ядра таблеток совершенно не зависит от сахарного покрытия в том смысле, что сахарное покрытие и гормональный стероид, содержащийся в нем, растворяются до распада спрессованного ядра таблетки и растворения какого-либо лекарственного компонента, присутствующего в ядре. Компоненты-наполнители, используемые для приготовления ядра таблетки, могут включать фармацевтически приемлемые водорастворимые и/или водонерастворимые вещества, такие как лактоза, фосфат кальция, крахмал, карбонат кальция, декстроза, сорбит, магнит, микрокристаллическая целлюлоза, сахароза, поливинилпирролидон, метилцеллюлоза, карбоксиметилцеллюлоза, альгинаты, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, этилцеллюлоза, натрий кроскармелоза, натрий крахмал гликолат, стерат магния, стеариновая кислота, полиэтиленгликоль, натрий лаурилсульфат, дымообразный (тонкодисперсный) диоксид кремния, тальк и т.п.
Сахарное покрытие, содержащее гормональный стероид, кроме того, содержит микрокристаллическую целлюлозу в количестве, контролирующем скорость высвобождения стероида и, при определенных обстоятельствах, поливинилпирролидон, чтобы способствовать в применении сахарного покрытия.
Ядро таблетки получают прессованием смеси, которую предпочтительно гранулируют, фармацевтически приемлемых наполнителей и, при необходимости, терапевтического средства, совместимого со стероидом, который подлежит включению в сахарное покрытие с контролирующим скорость освобождения количеством микрокристаллической целлюлозы. Ядро таблетки может иметь непластифицированное или пластифицированное изолированное покрытие, предназначенное для модификиции характеристик освобождения лекарственного средства, для любого лекарственного средства(в), содержащегося(ихся) внутри ядра, или для защиты их от влаги и/или кислорода. Не содержащие лекарственное средство ядра являются теми ядрами, которые обычно используют в качестве плацебо-таблеток в фармакологических исследованиях.
Данное изобретение обеспечивает улучшенную спрессованную таблетку, в которой, помимо обычного внутреннего ядра таблетки, необязательно содержащего лекарственное средство или произвольно содержащего одно или более лекарственных средств, которые фармакологически совместимы со стероидом в наружном сахарном покрытии, присутствует сахарное покрытие, которое включает гормональный стероид в количестве от около 0,1 до около 20,0% по массе сахарного покрытия; микрокристаллическую целлюлозу в количестве от около 0,1 до около 3,0% по массе сахарного покрытия; поливинилпирролидон в количестве от около 0 до около 5% по мессе сахарного покрытия, и сахар. Исходя из стандартной дозы, таблетка содержит от около 0,01 до около 50,0 мг, предпочтительно от около 0,015 до около 40,0 мг и более предпочтительно от около 0,02 до около 30,0 мг, суммарной загрузки гормонального стероида в нагруженном слое сахарного покрытия. При необходимости можно использовать нижнее покрытие из инертно наполненного сахара поверх изолированного покрытия до нагруженного стероидом слоя сахарного покрытия. Нижний слой сахарного покрытия, содержащий инертный наполнитель, может быть изготовлен с сахарозой, содержащей от около 7,5 до около 15,0% микрокристаллической целлюлозы. Наружное сахарное покрытие может содержать окрашивающий агент, такой как диоксид титана или первичный, вторичный или серый отбеливатель, как принято в области таблетирования. При необходимости окрашивающее средство может быть применено в виде отдельного слоя покрытия поверх наружного сахарного слоя. Для окончательного завершения таблетки можно использовать финишную полировку.
Сахар, используемый при получении сахарных покрытий, упоминаемых на протяжении данного описания, представляет сахарный продукт, такой как сахароза, полученная из свеклы, или тростника, или крахмала, источники конвертированного сахарида или полисахарида, которые считаются подходящими для целей покрытия таблеток. Общепринятым предпочтительным сахаром является сахароза.
Обнаружено, что освобождение гормонального стероида из сахарного покрытия можно контролировать путем ограничения количества микрокристаллической целлюлозы до от около 0,1 до около 3,0% массы сахарного покрытия. Такое использование небольшого количества микрокристаллической целлюлозы в сахарном покрытии отличается от использования этого наполнителя в качестве вспомогательной добавки для прессования или для того, чтобы способствовать распаду ядра таблетки. В последнем случае концентрацию микрокристаллической целлюлозы можно повысить вплоть до от 15 до 30% по массе.
Примеры гормональных стероидов, подходящих для включения в формуляции сахарных покрытий данного изобретения, включают, например, один или более из следующих стероидов: медроксипрогестерон ацетат, левоворгестрел, гестоден, медрогестон, эстрадиол, эстриол, эфинилэстрадиол, местранол, эстрон, диенестрол, гексэстрол, диэтилстильбэстрол, прогестерон, дезогестрел, норгестимат, гидроксипрогестерон, норэфиндрон, норэфиндон ацетат, норгестрел, мегестрол ацетат, метилтестостерон, этилэстренол, метандиенон, оксандролон, тримегестон, дионогест и т.п.
Кроме того, тканевые селективные прогестероны и/или антагонисты прогестерона, которые могут иметь или могут не иметь типичной стероидной функциональности, могут быть введены в формуляцию при этой технологии. К ним относятся, но ими не ограничиваются: RU-486, онапристон, ZК-137316, ОRG-31730 и НRР-2000. При необходимости в сахарных покрытиях могут быть использованы в комбинации эстрогенные стероиды и прогестогенные стсронды.
С целью иллюстрировать in vitro контроль скорости растворения стероида в отсутствие и в присутствии микрокристаллической целлюлозы, представлены следующие неограничивающие иллюстративные примеры:
Пример 1. Используя либо неперфорированную, либо перфорированную ванну для покрытия, на ядро таблетки наносят сахарное покрытие, состоящее из следующих твердых веществ, %:
Сахароза, NF - 87
Поливинилпирролидон - 3
Медроксипрогестерон ацетат, USP - 10
Скорость растворения стероида определяют в соответствии с <711 >, Фармакопея США (USP) XX, р. 959 (1980), используя Аппарат 2, при скорости вращения 50 об/мин, при растворении в 0,54% натрий лаурилсульфате в воде при 37oC, повторяя испытания 6 раз (Способ А). KB представляет коэффициент вариации между этими испытаниями, выраженный в процентах.
Время (мин) - Освобожденный стероид, % (КВ%)
5 - 93 (5,2)
10 - 94 (5,3)
30 - 95 (5,3)
60 - 95 (5,4)
120 - 95 (5,4)
Пример 2. Таблетки, покрытые тем же самым способом, тем же самым сахарным покрытием, как и выше, растворяют в 0,13% натрий лаурилсульфате в 0,1 N НСl при 37oС, используя USP Аппарат 1, при скорости вращения 100 об/мин, повторяя испытания 6 раз (Способ В).
Результаты этого исследования были следующими:
Время (мин) - Освобожденный стероид, % (КВ%)
5 - 83 (6,0)
10 - 85 (5,8)
30 - 85 (6,2)
60 - 85 (6,1)
120 - 85 (6,2)
Пример 3. Дополнительные таблетки, покрытые тем же самым способом, той же самой сахарной композицией, подвергают процедуре теста на растворение в потоке (flow-through) в 0,12% натрий лayрилсульфате в 0,1 N НСl при 37oС, используя SOTAX Dissotest Аппарат, при скорости потока 5,7 мл/мин (Способ С). Результаты трех отдельных испытаний были следующими:
Время (мин) - Освобожденный стероид, % (КВ%)
30 - 90,9 (2,9)
60 - 94,2 (3,0)
90 - 95,3 (2,9)
120 - 96,0 (3,0)
210 - 97,4 (3,0)
300 - 98,9 (3,6)
Из этих in vitro исследований ясно, что медроксипрогестерон ацетат, используемый здесь как типичный гормональный стероид, освобождается из сахарного покрытия чрезвычайно быстро.
Пример 4. Для целей сравнения и для иллюстрации неожиданных свойств сахарных покрытий данного изобретения сахарное покрытие, состоящее из следующих твердых веществ, наносят на ядро таблетки, %
Сахароза, NF - 86,5
Микрокристаллическая целлюлоза - 0,5
ПВП (PVР) - 3,0
Медроксипрогестерон ацетат, USР - 10,0
Используя таблетки, покрытые сахаром, содержащим микрокристаллическую целлюлозу, и следуя Способу А, получают следующие in vitro данные по растворению из трех испытаний:
Время (мин) - Освобожденный стероид, % (КВ%)
5 - 19,5 (49,5)
10 - 29,9 (32,8)
30 - 50,0 (23,0)
60 - 61,6 (19,5)
120 - 74,2 (19,2)
Пример 5. В случае других таблеток, покрытых сахаром, содержащим микрокристаллическую целлюлозу, полученных тем же самым способом, как описано выше, следуя Способу В, в шести испытаниях получают следующие данные:
Время (мин) - Освобожденный стероид, % (КВ%)
5 - 2,3 (34,4)
10 - 8,2 (27,0)
30 - 17,9 (16,1)
60 - 26,5 (13,6)
120 - 32,7 (16,6)
Пример 6. Следуя способу С, в случае таблеток, содержащих микрокристаллическую целлюлозу в сахарном покрытии, в трех испытаниях, получают следующие данные:
Время (мин) - Освобожденный стероид, % (КВ%)
30 - 2,8 (34,4)
60 - 4,1 (24,8)
90 - 5,1 (22,3)
120 - 6,4 (22,3)
210 - 11,0 (19,4)
300 - 14,3 (11,0)
Из этих данных очевидно, что небольшое количество микрокристаллической целлюлозы в сахарном покрытии (в этом случае 0,5% по массе твердых веществ сахарного покрытия) заметно тормозит скорость освобождения гормонального стероида.
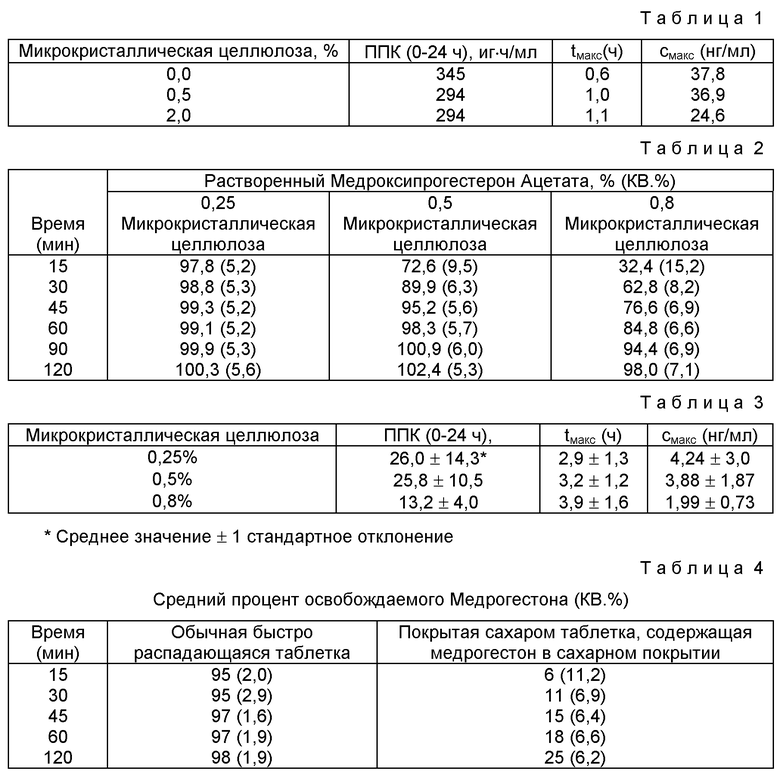
Пример 7. Получают покрытые сахаром таблетки, в которых сахарное покрытие содержит 0,01, 0,5% или 2% микрокристаллической целлюлозы в комбинации с 3,0% поливинилпирролидона, 10,0% медроксигестерон ацетата и сахарозу. Четырем коротконогим гончим собакам, в условиях голодания, вводят эти таблетки и определяют уровни стероида в плазме крови через 0; 0,5; 1; 1,5; 2; 3; 5; 8; 12; 16 и 24 ч. Полученные данные наносят на график, и рассчитывают площадь под кривой (ППК) ва протяжении 24-часового периода времени, и определяют время, при котором достигается максимальная концентрация в плазме (см. табл. 1).
Из этих in vitvo данных на собаках очевидно, что заметное изменение в биодоступности гормонального стероида происходит, когда концентрация микрокристаллической целлюлозы в сахарном покрытии увеличивается от 0,0 до концентрации, составляющей 0,5 - 2,0% микрокристаллической целлюлозы. Таким образом, скорость освобождения гормонального стероида, включенного в сахарное покрытие, можно контролировать включением очень малых количеств микрокристаллической целлюлозы в сахарное покрытие.
Пример 8. Получают покрытые сахаром таблетки, в которых сахарное покрытие содержит 0,25%, 0,5% или 0,8% микрокристаллической целлюлозы в комбинации с 0,5% поливиниллирролилова, 5,0% медроксипрогестерон ацетата и сахарозой. Эти таблетки подвергают in vitro тесту на растворение, применяя USР Аппарат для дезинтеграции (USP XX, <201>, р.958) (1980) со средой раствореня с 0,54% натрий лаурилсульфатом при 37oС. Данные испытаний: приведены в табл. 2.
Эти лекарственные формы также оценивают в исследовании на биодоступность для человека. Эти лекарственные формы вводят по перекрестной схеме двенадцати здоровым субъектам женского пола. Образцы крови отбирают через 0,5; 1; 1,5; 2; 2,5; 3; 4,5; 6; 8 и 12 ч и плазму анализируют на медроксипрогестерон ацетат. Получают следующие данные (см. табл. 3).
Из данных по in vitro растворению и in vitro биодоступности для человека очевидно, что характеристики освобождения лекарственного средства и биодоступность гормонального стероида контролируются концентрацией микрокристаллической целлюлозы в сахарном покрытии,
Пример 9. Сахарное покрытие, содержащее 5 мг медрогестона в матрице сахарозы с 0,4% микрокристаллической целлюлозы и 0,5% поливиниллирролидона, наносят на изолированное и покрытое сахаром ядро таблетки. In vitro профиль растворения этой дозированной лекарственной формы сравнивают с профилем растворения быстрораспадающейся спрессованной таблетки, содержащей 5 мг медрогестона, используя тест растворения, описанный в <711> USP XX, р.959 (1980), применяя Аппарат 2, работающий при 50 об/мин, с 900 мл 0,54% натрий лаурилсульфатом при 37oС. Получают следующие данные (см. табл. 4).
Драматическое действие понижения растворения медрогестона ясно демонстрируется, когда гормон включен в сахарное покрытие, содержащее 0,4% микрокристаллической целлюлозы.
Один предпочтительный вариант воплощения данного изобретения представляет спрессованную таблетку, в которой ядро таблетки содержит стандартную дозу эстрогенного соединения или его смеси в количестве от около 0,1 до около 5,0 мг или более предпочтительно от около 0,3 до около 2,5 мг, в комбинации со стандартными вспомогательными добавками для прессования и наполнителями. Наиболее желательно, чтобы конъюгированные эстрогены, находящиеся в ядре таблетки, включали встречающийся в природе конъюгированный эстрогенный продукт, известный как Premarin®.Сверху сахарного покрытия на спрессованной таблетке наносят дополнительное сахарное покрытие, содержащее от около 1 до около 50 мг и предпочтительно от около 1,5 до около 30,0 мг, медроксипрогестерон ацетата, цветное покрытие и, наконец, полированное покрытие. Для других применений предпочтительно применять не содержащее медикамент ядро с сахарным покрытием, содержащим стероид, такой как тримегестон, и, более предпочтительно, сахарное покрытие, содержащее смесь стероидов, таких как тримегестон и конъюгированный эстроген.
Изобретение относится к области фармации. Прессованная лекарственная таблетка содержит ядро и сахарное покрытие, причем указанное сахарное покрытие содержит дозу гормонального стероида и микрокристаллическую целлюлозу. Предложенный состав таблетки позволяет регулировать скорость высвобождения гормонального стероида. 2 с. и 5 з.п. ф-лы, 4 табл.
| US 5382434 A, 17.01.1995 | |||
| WO 9517168 A1, 29.06.1995 | |||
| RU 93058406/14 A, 10.10.1996 | |||
| US 5547948 A, 20.08.1996. |
Авторы
Даты
2002-04-27—Публикация
1997-01-08—Подача