Изобретение относится к области медицины, в частности к разработке композиции, обладающей антиВИЧ и антигерпесной активностью, на основе средств природного происхождения.
Распространение в последнее десятилетие ВИЧ-инфекции на территории Российской Федерации требует поиска препаратов на основе природных, достаточно физиологичных продуктов, которые одновременно были бы приемлемы и эффективны в качестве химиотерапевтических средств.
Синдром приобретенного иммунодефицита (СПИД) сопровождается развитием инфекций вирусной, бактериальной, грибковой или протозойной природы. Из вирусных инфекций на фоне ВИЧ-заражения наиболее часто встречающимся является заболевание, вызванные вирусами семейства Herpes [1].
Одним из наиболее эффективных средств, приемлемых в настоящее время против СПИДа, является азидотимидин, синтезированный Дж. Хоравицем (США) в 1964 г. В 1985 г. была обнаружена его антиВИЧ-активность, препарат также способен подавлять сопутствующие инфекции.
Применение азидотимидина основано на предполагаемом существовании двоякого механизма подавления синтеза вирусной ДНК: конкурентном ингибировании и терминации синтеза цепи ДНК. Причем конкурентное ингибирование состоит в том, что азидотимидинтрифосфат, образовавшийся в клетке человеческого организма под действием ферментативного фосфорилирования на поглощенный ею азидотимидин, к которому присоединяется цепочка из трех фосфатных групп, связывается с обратной транскриптазой именно в том участке, где обычно в норме связывается его аналог - тимидинтрифосфат как один из мономеров ДНК, а при терминации синтеза цепи ДНК обратная транскриптаза ошибочно включает азидотимидинтрифосфат в растущую цепь вирусной ДНК вместо тимидинтрифосфата и присоединение следующего нуклеотида становится невозможным, потому что в молекуле азидотимидинтрифосфата нет гидроксильной группы, которая необходима для образования связи со следующим нуклеотидом, в результате синтез ДНК прекращается.
Однако азидотимидин обладает высокой токсичностью для костного мозга - главного кроветворного органа и поэтому смертелен для ослабленного детского организма. Кроме того, азидотимидин вызывает побочные явления, связанные с перенесенными ранее заболеваниями, например гастритом и вирусным гепатитом.
Против герпесной инфекции в последние годы применяется препарат ацикловир (АЦ), представляющий собой синтетический аналог нуклеозида. Проникая в клетки, пораженные вирусом, превращается в монофосфат (под влиянием фермента тимидин-киназы, вырабатываемого вирусом), а затем в ди- и трифосфат (под влиянием клеточных киназ). Активная форма ацикловира - трифосфат подавляет вирусную ДНК-полимеразу и встраивается в структуру вирусной ДНК, в результате чего нарушается репликация вирусной ДНК [2].
Вышеописанные препараты являются химически синтезированными, достаточно токсичными, их применение целесообразно для пациентов, пораженных инфекционным заболеванием, и не могут быть использованы с профилактическими целями, их применение у детей если возможно, то с крайней осторожностью.
В последние годы разработан ряд препаратов на основе природных средств, в частности продуктов пчеловодства, которые могут быть использованы как иммунотропные и противоинфекционные. Например, известно лекарственное средство на основе прополиса (RU 2109514, 27.04.98), обладающее противоинфекционной активностью, еще один препарат на основе прополиса (RU 2132689, 10.07.99), имеющий иммунотропное действие. Известен также препарат на основе меда (RU 2133616, 27.07.99), для которого показана иммунотропная активность.
Однако перечисленные средства имеют общее противоинфекционное и иммунотропное действие, а конкретная противоВИЧ и противогерпесная активность для них не показана.
Наиболее близким аналогом является разработка, описанная в патенте RU 2020942 (15.10.97), в которой для профилактики и лечения ВИЧ-инфекции используют цветочный или падевый мед, содержащий галлий и германий.
Задачей настоящего изобретения является создание препарата, обладающего выраженной противоВИЧ и противогерпесной активностью, который можно использовать для лечения больных ВИЧ и/или герпесной инфекцией, а также для профилактических целей при названных инфекциях, дающего эффект в сроки, превышающие таковые для прототипа.
Для этого в препарат на основе природных продуктов пчеловодства: меда цветочного или падевого и спиртового экстракта прополиса дополнительно вносят микродозы нитрата галлия и получают композицию при следующем соотношении компонентов, вес. ч.:
Галлия нитрат (100-250 мкг/мл) - 1
Прополис (5%-ный экстракт) - 1
Мед - 10
Противовирусные испытания активного компонента (нитрата галлия) были проведены на культуре клеток и отражены в следующих примерах.
ПРИМЕР 1. Использовали перевиваемые лимфобластоидные клетки человека МТ-4. Клетки культивировали в концентрации 3,0-5,0•105 клеток в 1 мл среды RPMI 1640 с добавлением 10% сыворотки эмбрионов коров и 100 мкг/мл гентамицина. Жизнеспособность клеток определяли окраской 0,4% раствора трипанового синего с последующим подсчетом в камере Горяева.
Препаратами для исследования служили нитрат галлия, полученный по методу В.Н. Позднякова, для контроля использовали азидотимидин (АЗТ) (ретровир производства GlaxoWellcome).
Исследование противовирусной активности препаратов проводили на модели лимфобластоидных клеток в пластиковой 24-луночной панели (Costar, США). Препарат вносили одновременно с инфицированием культуры клеток вирусом иммунодефицита человека 1-го типа согласно схеме опыта. Множественность инфекции составила 0,001 lgTЦД50 (50% тканево-цитопатическое действие) на клетку. После этого культуры клеток инкубировали при 37oС в атмосфере с 5% СО2, 98% влажности в течение 3-5 дней до момента учета результатов.
Исследование репродукции ВИЧ проводили с помощью оценки вирусиндуцированного цитопатического действия в культурах клеток. Процент защиты клеток от действия вируса рассчитывали по формуле (Montefiori, 1989), [3].
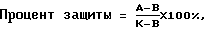
где А - число жизнеспособных клеток в опытной группе,
В - то же в инфицированной культуре (контроль вируса),
К - то же в контрольной неинфицированной культуре.
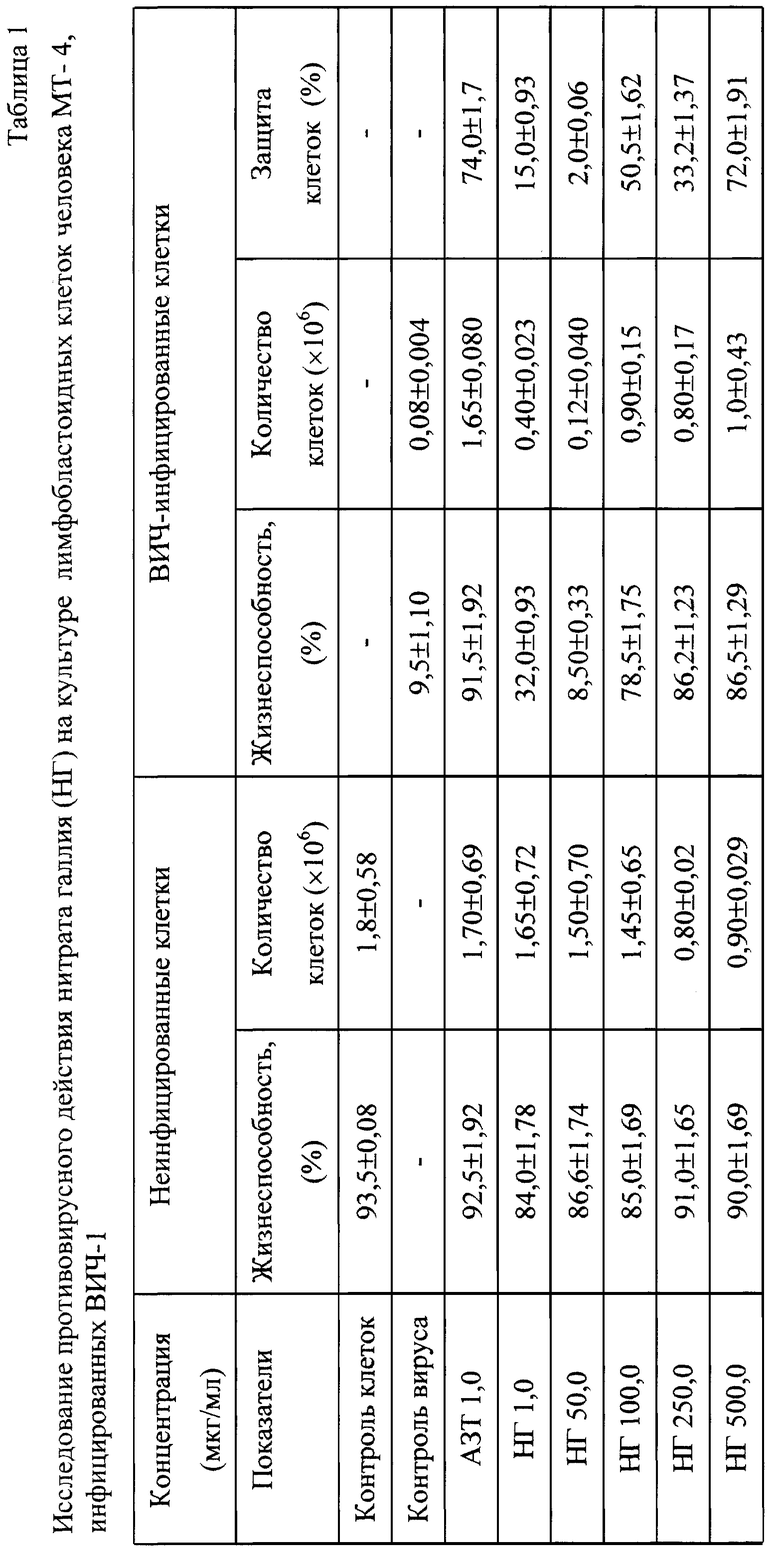
Полученные результаты (таблица 1) показали, что препарат галлия был малотоксичен в дозах 1-250 мкг/мл (снижение жизнеспособности клеток на 7,0-9,5%); при концентрации галлия 1000 мкг/мл отмечено заметное цитотоксическое действие; препарат сохранял жизнеспособность ВИЧ-инфицированных клеток в концентрации НГ 100-500 мкг/мл в пределах 78,5-86,2%.
ПРИМЕР 2. Противогерпесное действие исследовали также на перевиваемых лимфобластоидных клетках человека МТ-4, инфицированных вирусом герпеса человека 1-го типа. Культивирование клеток и определение их жизнеспособности проводили, как в примере 1.
Препаратом для сравнения, использованным в данном исследовании, был ацикловир (АЦ).
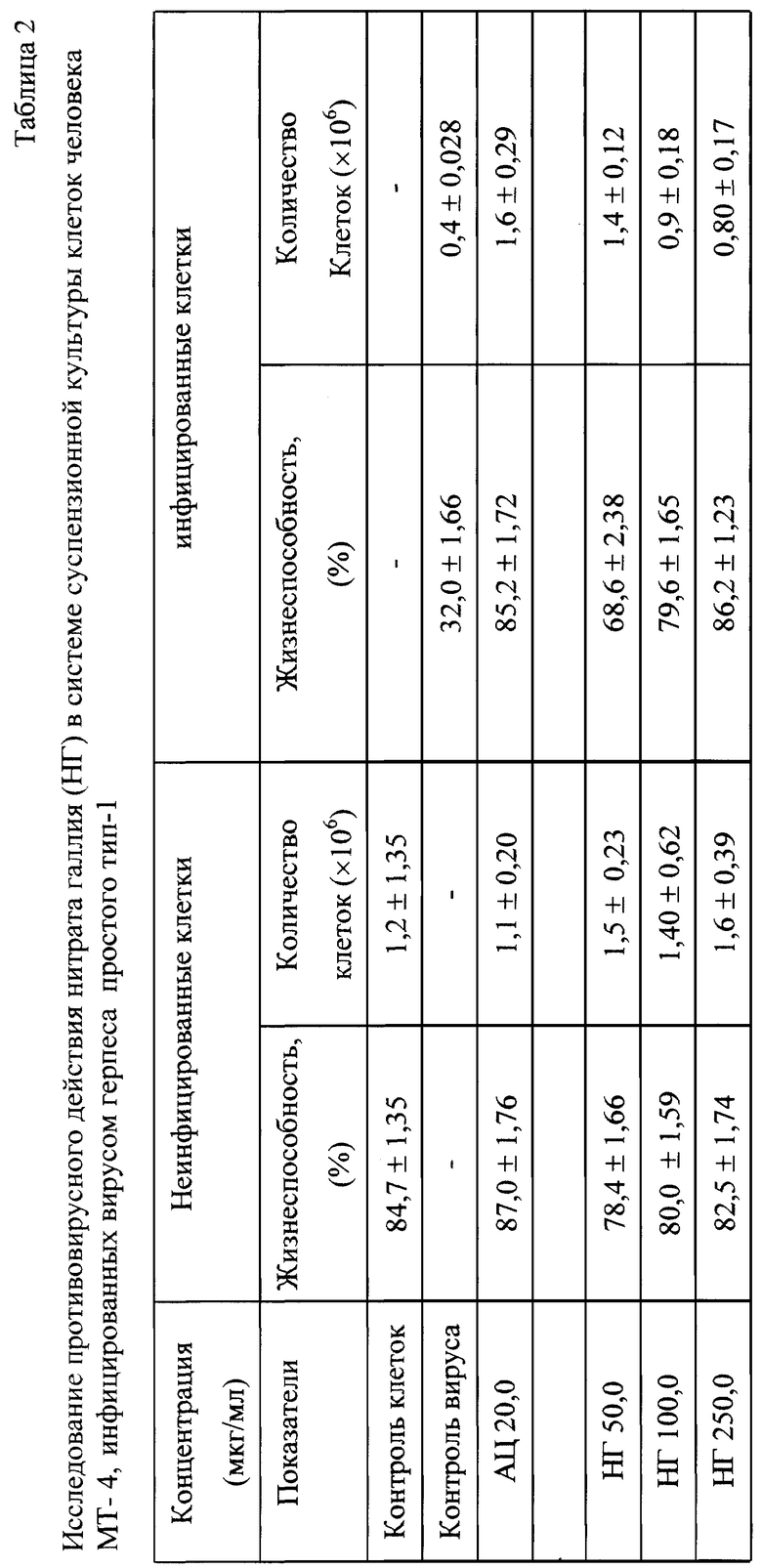
Результаты испытания действия галлиевого препарата (НГ) в системе суспензионной культуры клеток МТ-4, инфицированной вирусом герпеса простого, представлены в таблице 2. Из таблицы видно, что введение нитрата галлия позволяет сохранить жизнеспособность инфицированных клеток в 62,4-68,6% случаев.
Сущность изобретения заключается в создании композиции с использованием нитрата галлия, способной осуществить физико-химическую защиту лимфоцитов (в частности, Т4-хелперов), являющихся важным звеном иммунной системы человека. Нитрат галлия вводят в смесь меда (цветочного или падевого) с 5%-ным экстрактом прополиса в соотношении мед: прополис: НГ как 10:1:1. Препарат галлия, весьма эффективный in vitro, в составе с медом, являющимся природным галлийсодержащим продуктом и экстрактом прополиса, образует новую антивирусную композицию, конкретно направленную и быстро действующую, которую можно использовать как перорально, так и наружно.
Конкретное противоВИЧ и противогерпесное действие композиции было проверено с помощью испытаний на добровольцах, имеющих соответствующее вирусное заболевание.
Для пациентов использовали курс 50-100 г композиции 3 раза в день в течение 7-10 дней для приема перорально. Контроль проводили по количеству Т4-лимфоцитов в периферической крови, являющихся одним из основных показателей эффективности средств при ВИЧ-инфекции. Количественая норма Т4-лимфоцитов составляет для взрослых 800-1800, для детей свыше 1000 клеток/мкл.
Приводим некоторые примеры использования разработанной нами композиции.
ПРИМЕР 3. Пациент А., 1983 г. рожд., болен СПИДом, проведен трехкратный курс лечения композицией по 100 г в течение 10 дней каждый. В результате уровень Т4-лимфоцитов поднялся от 500 до 800 клеток/мкл.
ПРИМЕР 4. Пациент Б., 1986 г. рожд., больной СПИДом, сопровождающимся рецидивирующим герпесом. Пациент принял трехкратный курс лечения по 7 дней каждый по 100 г 3 раза в день перорально. Уровень Т4-лимфоцитов увеличился с 350 до 700 клеток/мкл, при этом рецидивирующий герпес был полностью излечен.
ПРИМЕР 5. Пациент М., 1982 г. рожд., больной СПИДом, прошел трехкратный курс по 10 дней каждый перорального лечения композицией, при этом уровень Т4-лимфоцитов увеличился с 350 до 900 клеток/мкл, практически приблизившись к норме.
ПРИМЕР 6. Пациент П., 1948 г. рожд., больной простым герпесом (высыпания на коже), принимал накожные аппликации в течение 5 дней по 14-16 часов. После курса лечения высыпания исчезли полностью.
Проведенные испытания, как лабораторные, так и клинические показали, что заявленная композиция более эффективна, чем продукт, описанный в прототипе, и позволяет добиться результата в более короткие сроки, может быть использована как для лечения вирусинфицированных пациентов, так и для профилактики. Композиция может быть с успехом применена для лечения и защиты от ВИЧ и герпесной инфекции не только у взрослых, но и у детей и подростков.
Источники информации
1. М.С. Балаян. Приобретенный иммунодефицитный синдром, Клиническая медицина, т. 62, 9, 1984 г.
2. Справочник Видаль, 1999, с. В-749.
3. Montefiori D.C., Robinson W.K., Mitchell W.M. "AIDS-res. Human retrovirus", 1989, v. 5, 2, 193-203.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ВИЧ-ИНФЕКЦИИ | 1991 |
|
RU2020942C1 |
| СПОСОБ ДОСТИЖЕНИЯ РЕМИССИИ В ОТНОШЕНИИ ОППОРТУНИСТИЧЕСКИХ ИНФЕКЦИЙ У БОЛЬНЫХ ВИЧ | 2008 |
|
RU2367452C1 |
| ПРОТИВОВИРУСНОЕ СРЕДСТВО К РНК- И ДНК-СОДЕРЖАЩИМ ВИРУСАМ | 1996 |
|
RU2136286C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВЕЩЕСТВА, ОБЛАДАЮЩЕГО ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ | 1993 |
|
RU2049479C1 |
| ПРОИЗВОДНЫЕ БЕНЗОТРОПОЛОНА, ОБЛАДАЮЩИЕ АНТИ-ВИЧ АКТИВНОСТЬЮ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ИНГИБИРОВАНИЯ ВИЧ-1 ИНТЕГРАЗЫ | 2007 |
|
RU2359954C2 |
| АМИД ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ С 5-АМИНОУРАЦИЛОМ, ПРОЯВЛЯЮЩИЙ АНТИ-ВИЧ АКТИВНОСТЬ | 2001 |
|
RU2199547C2 |
| КОМПЛЕКСНАЯ АУТОЛОГИЧНАЯ ВАКЦИНА ПРОТИВ ВИЧ-ИНФЕКЦИИ И СПИД | 2005 |
|
RU2306950C2 |
| ПРИМЕНЕНИЕ БЕЛКОВ В КАЧЕСТВЕ АНТИРЕТРОВИРУСНЫХ АГЕНТОВ | 1997 |
|
RU2203071C2 |
| АМИД β-ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ С 6-АМИНО-2-ТИО-УРАЦИЛОМ, ПРОЯВЛЯЮЩИЙ АНТИ-СПИД-АКТИВНОСТЬ | 1991 |
|
RU2024547C1 |
| ПРОИЗВОДНЫЕ БЕНЗОТРОПОЛОНА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СПОСОБ ИНГИБИРОВАНИЯ РЕПЛИКАЦИИ ВИРУСОВ | 2007 |
|
RU2359955C2 |
Изобретение относится к медицине, в частности к созданию композиции на основе природных продуктов, обладающей антиВИЧ и антигерпесной активностью. Сущность изобретения заключается в создании композиции, содержащей мед цветочный или падевый, 5%-ный спиртовой экстракт прополиса и водный раствор нитрата галлия (НГ) в концентрации 100-250 мкг/мл при соотношении компонентов (вес.ч.) мед: экстракт прополиса: НГ как 10:1:1. Техническим результатом изобретения является создание композиции более эффективной и физиологичной, пригодной для перорального и наружного применения как у взрослых, так и у детей и подростков. 2 табл.
Композиция, обладающая антиВИЧ и антигерпесной активностью, на основе продуктов пчеловодства, отличающаяся тем, что содержит натуральный цветочный или падевый, мед, 5%-ный спиртовой экстракт прополиса, а также содержит водный раствор нитрата галлия в концентрации 100-250 мкг/мл при следующем соотношении компонентов, вес. ч. :
Раствор нитрата галлия - 1
Экстракт прополиса - 1
Мед - 10
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ВИЧ-ИНФЕКЦИИ | 1991 |
|
RU2020942C1 |
| СПОСОБ ПОДАВЛЕНИЯ ВИЧ-ИНФЕКЦИИ | 1993 |
|
RU2043767C1 |
| US 4596710 А, 24.06.1986 | |||
| US 5093134 A, 03.03.1992 | |||
| US 5175006 A, 29,12,1992 | |||
| Младенов С | |||
| Мед и медолечение | |||
| София, 1970, с.112-129. | |||
Авторы
Даты
2002-05-27—Публикация
2001-02-23—Подача