Предлагаемое изобретение относится к новым химическим соединениям, конкретно к амиду глицирризиновой кислоты с 5-аминоурацилом: 3-О-{2-O-[N-(β-D-глюкуронопиранозил)-5-аминоурацил-N-(β-D-глюкуронопиранозил)-5-аминоурацил]} -(3β, 20β)-11-оксо-олеан-12-ен-30-карбоновой кислоте формулы (Iб), проявляющему анти-ВИЧ активность.
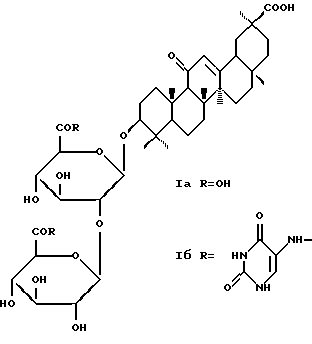
Указанное соединение и его свойства в литературе не описаны.
В настоящее время во всем мире интенсивно ведутся исследования по поиску новых противовирусных средств для борьбы с такими опасными для жизни человека вирусными заболеваниями, как лихорадки Эбола, Марбурга, гепатиты В и С, синдром приобретенного иммунодефицита (СПИД), вызываемого вирусом иммунодефицита человека (ВИЧ).
В 1987-1988 гг. группой японских ученых была обнаружена способность глицирризиновой кислоты (ГК) - основного ингредиента экстракта корней солодки голой (Glycyrrhiza glabra) и уральской (Gl. Uralensis) ингибировать ВИЧ in vitro и in vivo [1-3]. ГК была успешно использована в условиях клиники для лечения больных СПИДом [4]. Предварительные клинические исследования показали, что при введении ГК больным СПИДом в дозе до 1,6 г в сутки увеличивается число Т4-лимфоцитов и снижается содержание вирусного антигена [4].
Механизм анти-ВИЧ действия ГК и ее производных связан со способностью потенциировать образование интерферона в плазме крови [5], а также блокированием протеинкиназы С, необходимой для связывания вируса с Т4 рецепторами [6, 7] . Установлено, что ГК непосредственно препятствует связыванию ВИЧ с клеткой. Однако, как показали наши исследования, ГК малоэффективна на модели хронической инфекции ВИЧ [8].
Задача, на решение которой направлено заявленное техническое решение, заключается в поиске новых производных ГК, обладающих анти-ВИЧ активностью. В заявленном техническом решении синтезировано новое соединение - амид ГК с 5-аминоурацилом: 3-О-{2-О-[N-(β-D-глюкуронопиранозил)-5-аминоурацил-N-(β-D-глюкуронопиранозил)-5-аминоурацил] }-(3β,20β)-11-оксо-олеан-12-ен-30-карбоновая кислота формулы (Iб), проявляющий анти-ВИЧ активность. Биологические свойства данного соединения были изучены в лаборатории ретровирусов Института молекулярной биологии ГНЦ ВБ "Вектор".
Синтез амида (Iб) осуществлен путем конденсации глицирризиновой кислоты с 5-аминоурацилом в смеси диметилформамида и пиридина в присутствии дициклогексилкарбодиимида (ДЦГК) с выходом 56%.
Противовирусная активность препарата изучалась на традиционной модели первично инфицированных ВИЧ лимфоидных клеток МТ-4. В работе использовали штамм ВИЧ-1/ЭВК. В качестве препаратов сравнения использовали известный анти-ВИЧ препарат - ингибитор вирусной обратной транскриптазы - азидотимидин (АЗТ) в концентрации 1 мкг/мл и очищенную глицирризиновую кислоту (ГК) (95%) в концентрации 100 мкг/мл. Основным недостатком АЗТ является его высокая цитотоксичность: CD50 = 3,5 мкМ [8, 9].
Цитотоксичность предлагаемого соединения (Iб) оценивали на культуре перевиваемых лимфоцитов человека линии МТ-4. Долю жизнеспособных клеток подсчитывали в камере Горяева после окрашивания трипановым синим. Строили дозазависимую кривую и определяли концентрацию соединения, вызывающую гибель 50% клеток - CD50.
Для оценки анти-ВИЧ активности исследуемого соединения клетки МТ-4 инфицировали штаммом ВИЧ-1/ЭВК с множественностью заражения 0,2-0,5 инфекционных единиц на клетку. Ингибирующий эффект препарата оценивали на 4-е сутки культивирования измерением количества вирусного антигена р24 и суммарного вирусного антигена иммуноферментным методом, а также измерением активности вирусспецифического фермента РНК-зависимой ДНК-полимеразы. Кроме того, определяли степень защиты инфицированных клеток МТ-4 от гибели в результате вирусной (ВИЧ) инфекции. На основе полученных результатов строили дозазависимые кривые и определяли количественные характеристики ингибирования репродукции ВИЧ: ID50 - концентрацию соединения, на 50% подавляющую продукцию вируса или обеспечивающую 50%-ную защиту клеток; ID90 - концентрацию соединения, на 90% подавляющую продукцию вируса или обеспечивающую 90%-ную защиту клеток; IS - индекс селективности - отношение токсичной дозы соединения CD50 к его эффективной дозе ID50.
Установлено, что для исследуемого препарата 50%-ная цитотоксическая доза (CD50) составила 2080 мкг/мл или 1998 мкМ. Для препаратов сравнения - ГК (95% чистоты) CD50 = 756 мкМ, для АЗТ - 3,5 мкМ [9].
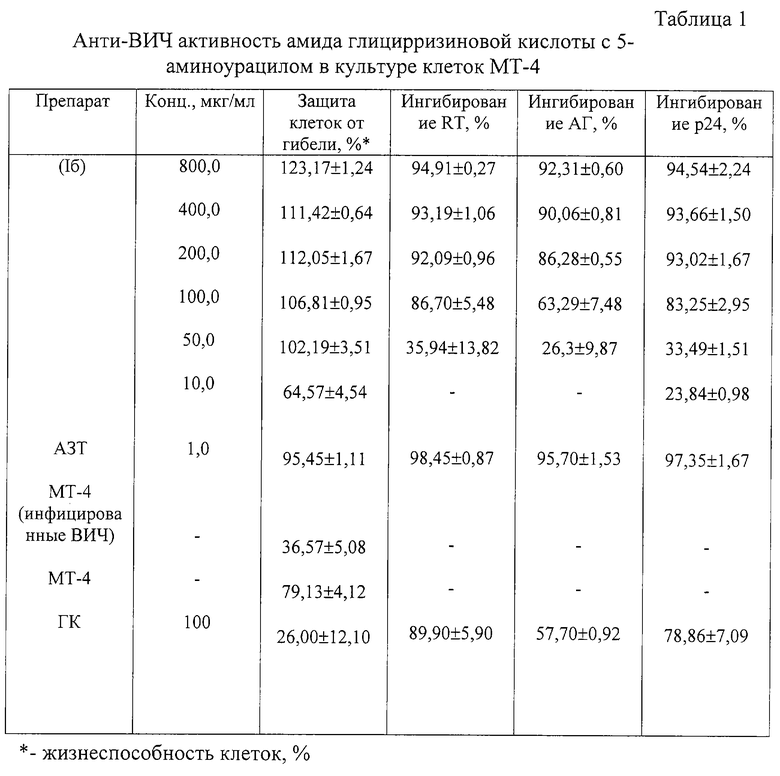
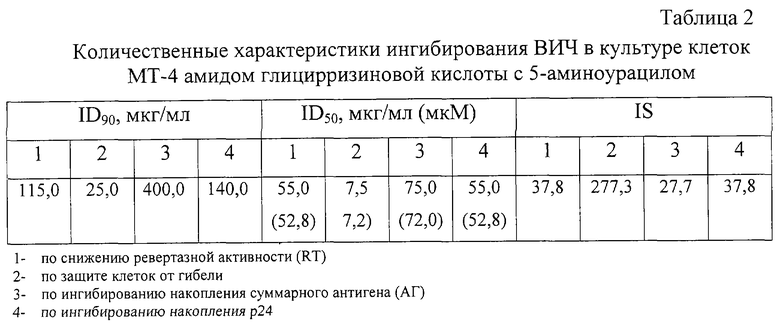
В табл. 1 и 2 приведены результаты проведенных экспериментов по оценке анти-ВИЧ активности амида ГК с 5-аминоурацилом. Исследуемый препарат (Iб) проявляет выраженную анти-ВИЧ активность, с высокой эффективностью ингибируя накопление вирусспецифического белка р24 (87-95% в концентрации 100-800 мкг/мл) (табл. 1), ID50 = 55 мкг/мл (52,8 мкМ) по данному параметру противовирусной активности (табл. 2); суммарного вирусного антигена (АГ) (ID50 = 75 мкг/мл или 72,0 мкМ), снижая активность вирусной обратной транскриптазы (ревертазы) (RT) (ID50 = 55 мкг/мл или 52,8 мкМ) (табл. 2), а также обеспечивая эффективную защиту клеток МТ-4 от гибели в результате вирусной инфекции (103-123% в концентрациях 50-800 мкг/мл) (табл. 1). Препараты сравнения защищают клетки МТ-4 от гибели соответственно ГК на 26%, АЗТ на 95% (табл. 1). В табл. 2 приведены количественные характеристики ингибирования ВИЧ в культуре клеток МТ-4 амидом ГК с 5-аминоурацилом (ID90, ID50, IS). Химиотерапевтический индекс (IS) для данного препарата по разным параметрам составил от 27,7 до 277,3, что существенно превышает таковой для ГК (от 4,4 до 24,0 для очищенного препарата) [8, 9]. Препарат практически не обладает цитотоксической активностью в исследованном диапазоне концентраций: CD50 = 1998 мкМ, в то время как АЗТ почти в 540 раз токсичнее: CD50 = 3,5 мкМ).
Таким образом, впервые получен амид ГК с 5-аминоурацилом формулы (Iб), проявляющий выраженную анти-ВИЧ активность в культуре клеток МТ-4, превосходящую противовирусный эффект природного гликозида - глицирризиновой кислоты, с высокой эффективностью (103-123%) защищающий клетки МТ-4 от гибели в результате ВИЧ-инфекции и обладающий низкой цитотоксичностью. Препарат почти в 540 раз менее цитотоксичен, чем известный анти-ВИЧ препарат азидотимидин (АЗТ).
Сущность технического решения поясняется следующими примерами.
Пример 1. Синтез амида глицирризиновой кислоты с 5-аминоурацилом (Iб)
К раствору 0,82 г (1 ммоль) глицирризиновой кислоты (95%) в смеси 25 мл диметилформамида и 5 мл пиридина при 0-5oС прибавили 0,42 г (3 ммоль) 5-аминоурацила и 0,45 г (2,2 ммоль) N,N'-дициклогексилкарбодиимида и перемешивали смесь при этой температуре 1 ч, выдержали смесь с периодическим перемешиванием при 20-22oС 24 ч. Осадок N,N'-дициклогексилмочевины отфильтровали, фильтрат разбавили холодной водой, подкислили лимонной кислотой до рН ~ 4, осадок отфильтровали, высушили и переосадили из водного диоксана. Сухой остаток перемешивали в 20 мл кислого ацетона (ацетон + НСl, рН ~2) 30 мин, отфильтровали, промыли чистым ацетоном и высушили. Выход 56%. Rf=0,4 (хлороформ-метанол-вода) (силуфол).
ИК-спектр, ν, см-1: 3600-3200 (ОН, NH), 1720 (СООН), 1670 (С=О), 1580 (пиримидин), 1550 (CONH). УФ-спектр, λmax, нм (lg ε): 240 (4,20); 287 (3,87). Спектр ЯМР 13С (ДМСО-d6, δ, м.д.): 88,50 (С3); 55,77 (С5); 43,22 (С8); 61,45 (С9); 36,94 (С10); 199,58 (С11); 128,52 (С12); 169,60 (С13); 50,41 (С18); 46,70 (С20); 179,28 (C30); 105,01 (С1'); 83,00 (С2'); 74,54 (C3'); 71,89 (С4'); 76,26 (С5'); 167,44 (С6'); 103,32 (С1'); 74,50 (С2''); 74,98 (C3''); 71,89 (С4''); 76,26 (С5''); 167,14 (С6''). Другие сигналы (остатки урацила): 163,16; 160,85; 160,77; 154,56; 150,00; 113,37; 113,18. Найдено, %: N 8,17. C50H68N6O18. Вычислено, %: N 8,07.
Пример 2. Изучение цитотоксичности и анти-ВИЧ активности амида глицирризиновой кислоты с 5-аминоурацилом (Iб).
Цитотоксичность препарата оценивали на культуре перевиваемых лимфоцитов человека линии МТ-4. Препарат растворяли в ДМСО и в соответствующих разведениях вносили в лунки 96-луночных культуральных планшетов (по три лунки на каждое разведение) при рассеве клеток, при этом конечная концентрация ДМСО в культуральной среде не превышала 1%. Посевная концентрация составляла 5•105 клеток/мл. Далее клетки культивировали на ростовой среде (среда RPMI-1640 с добавлением 10% сыворотки плода коровы, 0,06% L-глутамина, 100 мкг/мл гентамицина и 60 мкг/мл линкомицина) при 37oС и 5% углекислого газа в течение 4 суток. По окончании инкубации подсчитывали долю жизнеспособных клеток в камере Горяева после окрашивания трипановым синим. Строили дозазависимую кривую и определяли концентрацию соединения, вызывающую гибель 50% клеток - CD50.
Установлено, что для амида (Iб) 50%-ная цитотоксическая доза (CD50) составила 2080 мкг/мл или 1998 мкМ, в то время как для ГК CD50 = 756 мкМ, для АЗТ 3,5 мкМ [8, 9]. Таким образом, предлагаемое соединение (Iб) является менее токсичным веществом для клеток иммунной системы МТ-4, чем препараты сравнения.
Для оценки анти-ВИЧ активности исследуемого соединения клетки МТ-4 инфицировали штаммом ВИЧ-1/ЭВК с множественностью заражения 0,2-0,5 инфекционных единиц на клетку. После адсорбции вируса в течение 1 часа при 37oС инфицированные и контрольные клетки разводили ростовой средой до посевной концентрации 5•105 клеток/мл и вносили в лунки 96-луночных культуральных планшетов. Затем вносили растворы исследуемого соединения (по три лунки на каждое разведение) и далее культивировали как описано выше. Конечная концентрация препарата в культуральной среде составляла от 0,001 до 20 мкг/мл.
Ингибирующий эффект препарата оценивали на 4-е сутки культивирования измерением количества вирусного антигена р24 и суммарного вирусного антигена иммуноферментным методом, а также измерением активности вирусспецифического фермента РНК-зависимой ДНК-полимеразы. Кроме того, определяли анти-ВИЧ активность, исходя из степени защиты инфицированных клеток от гибели в результате вирусной инфекции, подсчитывая долю жизнеспособных клеток в камере Горяева после окрашивания трипановым синим. На основе полученных результатов строили дозазависимые кривые и определяли количественные характеристики ингибирования репродукции ВИЧ: ID50 - концентрацию соединения, на 50% подавляющую продукцию вируса или обеспечивающую 50%-ную защиту клеток; ID90 - концентрацию соединения, на 90% подавляющую продукцию вируса или обеспечивающую 90%-ную защиту клеток; IS - индекс селективности - отношение токсичной дозы соединения CD50 к его эффективной дозе ID50. В качестве препаратов сравнения использовали очищенную глицирризиновую кислоту (95%) (ГК) и известное анти-ВИЧ средство - азидотимидин (АЗТ).
В табл. 1 и 2 приведены результаты проведенных экспериментов по оценке анти-ВИЧ активности амида глицирризиновой кислоты с 5-аминоурацилом. Показано, что исследуемый препарат проявляет выраженную анти-ВИЧ активность, с высокой эффективностью ингибируя накопление вирусспецифического белка р24 (ID50 = 55 мкг/мл или 52,8 мкМ), суммарного вирусного антигена (ID50 = 75 мкг/мл или 72,0 мкМ), снижая активность обратной транскриптазы (ревертазы) (RT) (ID50 = 55 мкг/мл или 52,8 мкМ) (табл. 2), а также обеспечивая эффективную защиту клеток МТ-4 от гибели (102-123%) (табл. 1) в результате вирусной инфекции. Количественные характеристики ингибирования ВИЧ в культуре клеток МТ-4 амидом ГК с 5-аминоурацилом (Iб) (ID50, ID90, IS) приведены в табл. 2. Химиотерапевтический индекс (IS) для данного препарата по разным параметрам составил от 27,7 до 277,3, что существенно превышает таковой для очищенной ГК (4,4 - 24,0) [9].
Источники информации
1. M.Ito, A.Sato, K.Hirabayashi, F.Tanabe, Sh.Shigeta, M.Baba, E.De Clerq, H.Nakashima, N.Yamamoto. Mechanism of inhibitory effect of glycyrrhizin on replication of human immunodeficiency virus (HIV). //Antiviral Res., 1988, v.10, N 6, p.289-298.
2. M.Ito, H.Nakashima, M.Baba, R.Puwels, E.De Clercq, Sh.Shigeta, N.Yamamoto. Inhibitory effect of glycyrrhizin on the in vitro infectivity and cytopathic activity of the human immunodeficiency virus [HIV (HTLV-III/LAV)] . //Antiviral Res., 1987, v.7, N 3, p.l27-137.
3. M.Ito, H.Nakashima, N.Yamamoto. Glycyrrhizin and its salts for inhibiting growth of virus of acquied immune deficiency syndrom (AIDS). //Eur. Pat. 255420, 1988. //Chem. Abstr, v.l09, 116062v.
4. M.Ito. Clinical effects of glycyrrhizin on human immunodeficiency virus disease. //Jikken Igaku, 1989, v.7, N 7, p.858-860. //Chem. Abstr, v. 111, R49739x.
5. Y.Feng, T.Zhu. Effect of glycyrrhizin on the production of γ-interferon (IFN) from human spleen cells. //Zhonghuo Weish Cngutuxue He Hianyxue Zazhi, 1986, v.6, N 2, p.99-102. //Chem. Abstr., v.l05, 18041k.
6. T. S.Tochikara, H.Nakashima, Y.Yamamoto. Antiviral agents with activity against human retroviruses. //J. Acquied Immune Def. Syndrome, 1989, N 2, р.441-447.
7. Г. А. Толстиков, Л.А.Балтина, Э.Э.Шульц, А.Г.Покровский. Глицирризиновая кислота. //Биоорган. химия, 1997, т.23, 9, с.691-709.
8. О. А. Плясунова. Скрининг и изучение препаратов - ингибиторов вируса иммунодефицита человека. Дисс. канд. биол. наук в форме научного докл. Кольцово, 1992, 55 с.
9. О.А.Плясунова, И.Н.Егоричева, Н.В.Федюк, А.Г.Покровский, Л.А.Балтина, Ю. И. Муринов, Г.А.Толстиков. Изучение анти-ВИЧ активности β-глицирризиновой кислоты. //Вопросы вирусологии, 1992, 5-6, с.235-238.
| название | год | авторы | номер документа |
|---|---|---|---|
| ГЛИКОПЕПТИД ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ С S-БЕНЗИЛ-L-ЦИСТЕИНОМ, ПРОЯВЛЯЮЩИЙ АНТИ-ВИЧ АКТИВНОСТЬ | 2001 |
|
RU2198177C2 |
| ГЛИКОПЕПТИД ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ С ГЛИЦИЛ-L-ФЕНИЛАЛАНИНОМ, ПРОЯВЛЯЮЩИЙ АНТИ-ВИЧ-1 АКТИВНОСТЬ | 2006 |
|
RU2315058C1 |
| СРЕДСТВО, ПРЕДСТАВЛЯЮЩЕЕ СОБОЙ 3-O-β-D-ГЛЮКУРОНОПИРАНОЗИЛ-β-D-ГЛЮКУРОНОПИРАНОЗИД ОЛЕАН-9( 11),12( 13)-ДИЕН-30-ОВОЙ КИСЛОТЫ, ПРОЯВЛЯЮЩЕЕ АНТИ-ВИЧ-1 АКТИВНОСТЬ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2011 |
|
RU2475246C2 |
| АМИД β-ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ С 6-АМИНОУРАЦИЛОМ, ПРОЯВЛЯЮЩИЙ АНТИ-СПИД-АКТИВНОСТЬ | 1991 |
|
RU2024545C1 |
| 3,28-ДИ-О-НИКОТИНАТ БЕТУЛИНА, ПРОЯВЛЯЮЩИЙ ГЕПАТОПРОТЕКТОРНУЮ И АНТИ-ВИЧ АКТИВНОСТЬ | 1999 |
|
RU2174982C2 |
| СРЕДСТВО, ПРЕДСТАВЛЯЮЩЕЕ СОБОЙ АМИД ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ С 5-АМИНОУРАЦИЛОМ, ПРОЯВЛЯЮЩЕЕ ПРОТИВОВИРУСНУЮ АКТИВНОСТЬ В ОТНОШЕНИИ ВИРУСА ГРИППА A/H1N1 | 2014 |
|
RU2568849C9 |
| N'-{N-[3-ОКСО-20(29)-ЛУПЕН-28-ОИЛ]-9-АМИНОНОНАНОИЛ}-3-АМИНО-3-ФЕНИЛПРОПИО НОВАЯ КИСЛОТА, ОБЛАДАЮЩАЯ ИММУНОСТИМУЛИРУЮЩЕЙ И ПРОТИВОВИРУСНОЙ АКТИВНОСТЬЮ | 2002 |
|
RU2211843C1 |
| АМИД β-ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ С 6-АМИНО-2-ТИО-УРАЦИЛОМ, ПРОЯВЛЯЮЩИЙ АНТИ-СПИД-АКТИВНОСТЬ | 1991 |
|
RU2024547C1 |
| ДИ- И ТРИНИКОТИНАТЫ ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ И ИНГИБИТОР РЕПРОДУКЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА | 2006 |
|
RU2304145C1 |
| АМИД β-ГЛИЦИРРИЗИНОВОЙ КИСЛОТЫ С МЕТИЛОВЫМ ЭФИРОМ L -ГИСТИДИНА, ПРОЯВЛЯЮЩИЙ АНТИ-СПИД-АКТИВНОСТЬ | 1991 |
|
RU2024543C1 |
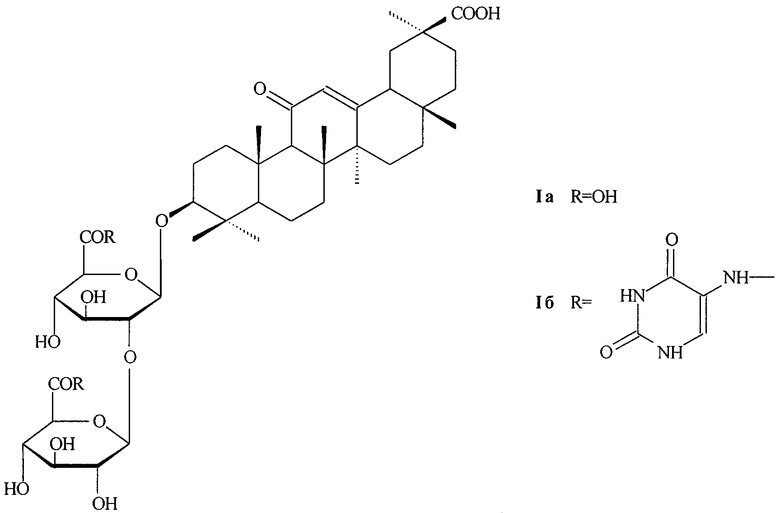
Изобретение относится к новому химическому соединению, а именно к амиду глицирризиновой кислоты с 5-аминоурацилом формулы I, проявляющему анти-ВИЧ активность, в культуре клеток МТ-4, с высокой эффективностью ингибируя накопление вирусспецифического белка р24 (ID50 = 55 мкг/мл или 52,8 мкМ), суммарного вирусного антигена (ID50 = 75 мкг/мл или 72,0 мкМ), что снижает активность обратной транскриптазы (ревертазы) (RT) (ID50 = 55 мкг/мл или 52,8 мкМ). Химиотерапевтический индекс (IS) данного соединения по разным параметрам составил 27,7-277,3, что существенно превышает таковой для ГК (4,4-24,0) и обеспечивает эффективную защиту клеток МТ-4 от гибели (102-123%) в результате ВИЧ-инфекции. Защитный эффект превосходит защитное действие глицирризиновой кислоты (ГК) и азидотимидина. В отличие от последнего амид ГК с 5-аминоурацилом ~ в 540 раз менее токсичен для клеток (CD50 = 2080 мкг/мл или 1998 мкМ). 2 табл.
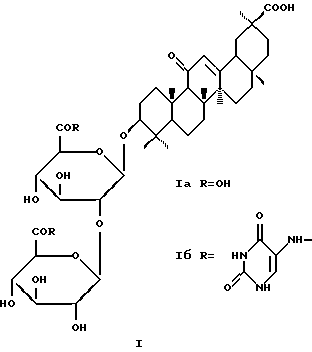
Амид глицирризиновой кислоты с 5-аминоурацилом формулы (I) (см. графическую часть)
проявляющий анти-ВИЧ активность.
| СЕЛЕКТОР СКОРОСТЕЙ НЕЙТРАЛЬНЫХ ЧАСТИЦ | 0 |
|
SU255420A1 |
| Толстиков Г.А | |||
| и др | |||
| Биоорганическая химия, 1997, т.23, № 9, с.691-709 | |||
| Плясунова О.А | |||
| и др | |||
| Вопросы вирусологии, 1992, № 5-6, с.235-238. | |||
Авторы
Даты
2003-02-27—Публикация
2001-03-30—Подача