Изобретение относится к медикаментозному контейнеру для хранения жидкого медикамента, а также к контейнеру, содержащему такой медикаментозный контейнер, по меньшей мере частично заполненный жидким медикаментом.
Традиционно медикаментозные контейнеры для хранения жидких медикаментов выполняют из стекла. Для некоторых медикаментов, таких как лекарственные препараты для перорального введения, используют контейнеры из непрозрачных полиэтиленов или полиэфиров. Такой полимерный контейнер, выполненный из полиэфира полигликолевой кислоты и терефталевого полиэфира, описан, например, в патенте США 4565851. Этот контейнер обеспечивает хороший барьер для кислорода и других газов, но не обеспечивает достаточных барьерных свойств по отношению к консервантам и воде.
Лекарственные препараты, такие как инсулин и гормон роста, поставляют в небольших контейнерах или ампулах. Такие ампулы обычно содержат от 1,5 до 10 мл готового к применению лекарственного препарата. Эти ампулы хранятся на складе при больнице или аптеке, а также у пользователя. Это значит, что срок их годности должен быть достаточно большим. Водные растворы или суспензии лекарственных препаратов, таких как инсулин или гормоны роста, обычно снабжают консервантом, таким как фенол и/или бензиловый спирт, и/или метакрезол. Введение консервантов является необходимым, поскольку стерилизация препаратов невозможна из-за чувствительности медикаментов, содержащих протеины, пептиды и/или последовательности оснований ДНК. Медикаменты в контейнерах, содержащих более одной дозы, например, для использования в пен-системах (ручка-шприц), имеют высокую степень риска загрязнения. Поэтому консерванты являются основными ингредиентами таких лекарственных препаратов, в частности лекарственных препаратов для парентерального введения. Фенол, бензиловый спирт и метакрезол могут использоваться в небольших количествах в парентеральных лекарственных препаратах, например, для внутримышечного введения. Водные растворы или суспензии лекарственных препаратов, содержащие консервант, могут храниться в стеклянных контейнерах до 2 лет.
В статье T.J. McCarthy "Interaction between aqueous preservative solutions and their plastic containers. III', Pharm. Weekblad, 107 (1972) описывается влияние хранения некоторых водных растворов консервантов в контейнерах из полипропилена (ПП), окрашенного белым перламутровым пигментом, и поливинилхлорида (ПВХ) соответственно, в частности на потери консервантов из растворов. В этой статье не обсуждается хранение водных растворов консервантов в прозрачных контейнерах. Кроме того, выводом данной статьи является то, что теряются большие количества некоторых видов консервантов из растворов, хранившихся в ПП. Похоже, однако, что ПВХ обеспечивает хороший барьер для консервантов. Однако вследствие содержания хлора ПВХ непригоден для применения из-за загрязнения окружающей среды.
JP-A-8-155007 описывает медицинский контейнер с улучшенной прозрачностью и теплостойкостью. Кроме того, изобретение относится к контейнеру, предотвращающему утечку консервантов. Реферат JP-A-8-155007, однако, не рассматривает физических параметров такого улучшения.
В работе Tarr et al., "Stability and sterility of biosynthetic human insulin stored in plastic insulin syringe for 28 days", American Society of Hospital Pharmacists, т.48, с.2631-34, 1991, описывается похожее испытание на хранение водных растворов фенола, бензилового спирта и метакрезола, соответственно, в полипропилен-полиэтиленовых шприцах, в частности, по отношению к потерям фенола, бензилового спирта и метакрезола соответственно из растворов.
Испытание охватывает только 28 дней, однако из этого испытания делается вывод, что полипропилен-полиэтиленовые шприцы не могут быть использованы для хранения лекарственных препаратов, содержащих фенол и/или бензиловый спирт, и/или метакрезол. Ампулы, содержащие инсулин или гормон роста, обычно хранят в холодильнике при температуре около 5oС при хранении на складе, в больнице или аптеке. При хранении пользователем они часто хранятся при комнатной температуре до 1 месяца. В частности, инсулин хранится при комнатной температуре, потому что пользователь (он или она) носит инсулин с собой все время. Концентрация инсулина и консервантов должна сохраняться постоянной на протяжении периода хранения. Если концентрация консерванта является слишком низкой, лекарственный препарат не будет достаточно сохранен.
Можно предложить получать лекарственный препарат с высокой начальной концентрацией консерванта. Это, однако, неприемлемо для парентерального применения. Потери воды в процессе хранения должны быть также очень низкими, потому что потеря слишком большого количества воды приводит к слишком высокой концентрации активного лекарственного препарата и, возможно, к слишком высокой концентрации консервантов. Если теряется слишком много воды, пользователь может получить чрезмерную дозу активного лекарственного препарата, такого как инсулин.
Кроме того, важно, чтобы пользователь мог визуально контролировать лекарственный препарат, чтобы гарантировать, что лекарственный препарат не кристаллизуется и не полимеризуется в результате, например, самоассоциирования или денатурирования, или что отсутствует другое видимое изменение лекарственного препарата, такое как окисление активного лекарственного препарата.
Задачей настоящего изобретения является создание медикаментозного контейнера из полимерного материала, причем этот материал является по существу инертным по отношению к лекарственному препарату, а контейнер является прозрачным и обеспечивает хороший барьер по отношению к метакрезолу/фенолу/бензиловому спирту и воде соответственно.
Другой задачей изобретения является создание медикаментозного контейнера, который является дешевым и простым в изготовлении.
Еще одной задачей изобретения является создание медикаментозного контейнера для длительного хранения водных медикаментов, таких как водные растворы инсулина или гормона роста человека.
Медикаментозные контейнеры по изобретению для хранения жидкого медикамента, содержащего один или более активных лекарственных препаратов, воду и метакрезол и/или фенол, и/или бензиловый спирт, имеют дальний и ближний конец и стенку, причем, по меньшей мере, две части стенки выполнены из полимерного материала. Эти полимерные части стенки имеют толщину от 0,3 мм до 3 мм, предпочтительно от 0,5 мм до 1 мм, светопропускание при 400 нм 25% или более, измеренное через обе противоположные части стенки контейнера, когда контейнер заполнен водой с использованием стандартного спектрофотометра и воздуха в качестве эталона, причем полимерные части стенки выполнены из материала, содержащего не менее 70 мас.% сополимера, состоящего из алифатических циклических или бициклических углеводородов с 5-7-звенными кольцом или кольцами и этилена или пропилена, причем материал имеет температуру стеклования выше 50oС, определенную с помощью дифференциальной сканирующей калориметрии при вырезании кусков из стенок контейнера и нагревании их в алюминиевой кювете от 10 до 270oС, со скоростью сканирования 10oС/мин, причем температура стеклования определяется как температура в точке сгиба и плотность 0,95 г/см3 или более.
Материал может содержать до 5 мас.% добавок, в частности, выбранных из антиоксидантов, смазывающих веществ, таких как стеараты или силиконы, поверхностно-активных веществ, зародышеобразователей и осветлителей, и до 30 мас. % инертных наполнителей, таких как стеклянные частицы, имеющие показатель преломления примерно равный показателю преломления полимерного материала, причем общее количество добавок и наполнителей составляет до 30 мас.%.
Как указано выше, рассеяние и поглощение видимого света материала должно быть небольшим, чтобы можно было контролировать качество лекарственного препарата в контейнере. Контроль качества может быть визуальным контролем инородных частиц, гомогенности суспензии, седиментации кристаллов, образования хлопьев, фибриллирования или полимеризации пептидов или протеинов в растворах и изменения спектра поглощения раствора лекарственного препарата.
Наиболее критическими являются изменения, которые влияют на концентрацию активного лекарственного препарата, или лекарства, в растворе, и полимеризация или осаждение в них могут быть очень трудными для обнаружения пользователем, особенно если контейнер имеет небольшое светопропускание.
Для некоторых инсулиновых рецептур важно, чтобы больной диабетом мог визуально видеть, что полимеризовано более 3% инсулина. Полимеризованный инсулин может визуально и с помощью спектрофотометра наблюдаться как изменение светопропускания. Обычное изменение пропускания инсулинового раствора, в котором полимеризовано 3% инсулина, соответствует изменению пропускания 1: 400 Ph.Eur. (Евр. фарм. стандарта), а обычное изменение пропускания инсулинового раствора, в котором полимеризовано 30% инсулина, соответствует изменению пропускания 1:40 стандарта Ph.Eur. (1997 European Pharmacopeia section 2.2 Physical and Physicochemical Methods. 2.2.1 Clearity and Degree of Opalescence of Liquids).
В стеклянном контейнере светопропускание обычно изменяется от примерно 94% до примерно 45% с 1:40 Ph.Eur при 400 нм и толщине стенки 0,9 мм. В аморфном циклическом полиолефине светопропускание обычно изменяется от примерно 85% до примерно 41%. с 1:40 Ph.Eur., что визуально различимо. В высокопрозрачном полипропилене пропускание обычно изменяется от примерно 40% до примерно 18%. В менее прозрачном полипропилене пропускание обычно изменяется от примерно 15% до примерно 6% или даже от примерно 4% до примерно 3%, причем все изменения определены с использованием стандарта 1:40 Ph.Eur.
Очевидно, что пациент лучше всего может обнаружить такую проблему в медикаментозном контейнере, в котором светопропускание является высоким, а изменения являются большими. На практике рекомендуется, чтобы светопропускание в 3 мл контейнере с толщиной стенки 0,9 мм, заполненном инсулиновым раствором, таким как Актрапид 100 межд.ед./мл (Ново-Нордиск A/S), было выше 25% при 400 нм, чтобы можно было визуально наблюдать полимеризацию более 3%.
Несколько пригодных материалов для упаковки парентеральных лекарств, консервированных метакрезолом, было неожиданно найдено в группе полиолефиновых материалов. Как указано выше, любой материал должен удовлетворять ряду технических условий, чтобы предотвратить утечку метакрезола и воды из лекарственной рецептуры и обеспечить визуальный контроль качества продукта.
Медикаментозные контейнеры по изобретению должны предпочтительно отвечать следующим требованиям:
полимерные части стенки должны иметь проницаемость метакрезола менее 0,0072 г/м2/24 ч, определенную после периода хранения 3 месяца при 37oС и 12% относительной влажности (отн.вл.) при контактировании полимерной стенки с водным метакрезольным раствором с концентрацией 3 мг/мл, и проницаемость для воды менее 0,4 г/м2/24 ч, определенную после периода хранения 3 месяца при 37oС и 12% отн.вл., более предпочтительно полимерные части стенки должны иметь проницаемость для метакрезола менее 0,0055 г/м2/24 ч и даже более предпочтительно менее 0,0020 г/м2/24 ч, определенную после 3-месячного периода хранения при 37oС и 12% отн.вл. при контактировании полимерной стенки с 3 мг/мл водным раствором метакрезола, и предпочтительно полимерные части стенки должны иметь проницаемость для воды менее 0,35 г/м2/24 ч, более предпочтительно менее 0,30 г/м2/24 ч, и даже более предпочтительно менее 0,20 г/м2/24 ч, определенную после 3-месячного периода хранения при 37oС и 12% отн.вл.
Предпочтительно полимерные части стенки имеют проницаемость для воды менее 0,025 г/м2/24 ч, определенную после 3-месячного хранения при 8oС и 13% отн.вл. в течение 36 месяцев, более предпочтительно, менее 0,021 г/м2/24 ч.
Метакрезол, бензиловый спирт и фенол все являются органическими растворителями с очень низкой растворимостью в воде. Метакрезол является менее полярным, чем фенол и бензиловый спирт, и поэтому будет диффундировать быстрей, чем фенол и бензиловый спирт, в очень гидрофобной среде. Кроме того, растворимость метакрезола будет выше в гидрофобной среде, такой как циклический полимер. Но хотя фенол и бензиловый спирт являются молекулами меньше метакрезола, и этот размер может быть важным для скорости диффузии, было установлено, что потери фенола или бензилового спирта будут меньше, чем потери метакрезола, и поэтому это достаточно для определения потерь метакрезола.
Согласно изобретению более предпочтительно, чтобы медикаментозный контейнер, в частности, для лекарства парентерального введения отвечал следующим требованиям:
потери воды должны быть менее 1,5% после хранения при 37oС и 12% отн.вл. в течение 3 месяцев и менее 1% после хранения при 8oС и 13% отн. вл. в течение 36 месяцев. Для 3 мл контейнера с внутренним диаметром 9,25 мм это соответствует проницаемости при 37oС примерно 0,35 г/м2/24 ч и при 8oС примерно 0,021 г/м2/24 ч.
Потери метакрезола должны быть менее 10% для целого контейнера и предпочтительно 7,5% для полимерных частей стенки контейнера после хранения в течение 3 месяцев при 37oС и 12% отн. вл. Для 3 мл контейнера с внутренним диаметром 9,25 мм и толщиной стенки 0,9 мм это соответствует проницаемости примерно 0,0053 г/м2/24 ч.
Согласно изобретению было установлено, что группа полимерных контейнеров отвечает описанию, а именно контейнеры, содержащие аморфные полимеры, состоящие из алифатических циклических или бициклических углеводородов с 5-7-звенным кольцом или кольцами и этилена или пропилена, причем материал имеет температуру стеклования выше 50oС, определенную методом дифференциальной сканирующей калориметрии при вырезании кусков из стенок контейнера и нагревании их в алюминиевой кювете от 10 до 270oС со скоростью 10oС/мин, причем температура стеклования определяется как температура в точке сгиба; и плотность 0,95 г/см3 или более.
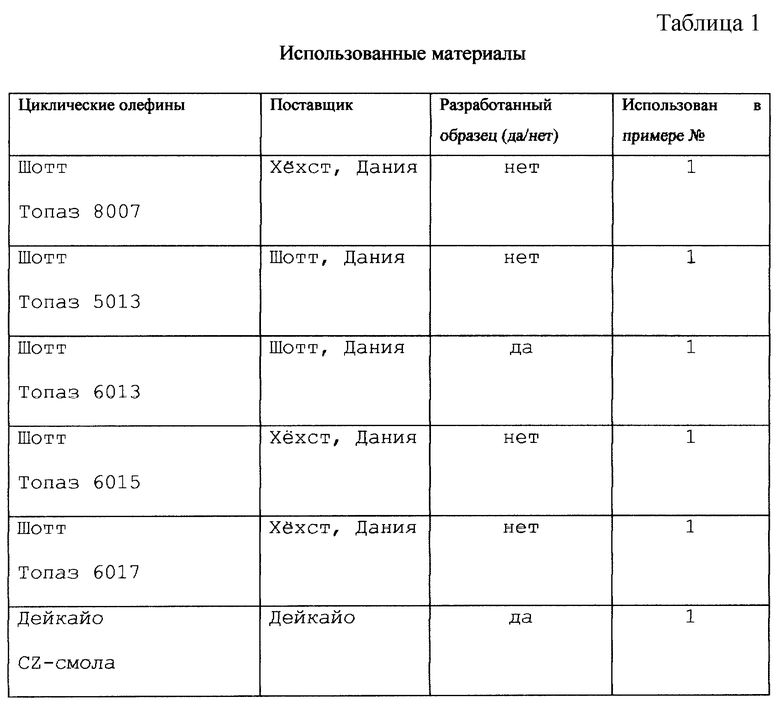
Аморфный сополимерный материал предпочтительно состоит из алифатических циклических углеводородов с 5-7-звенным кольцом или кольцами и этилена, и предпочтительно сополимерный материал является полностью аморфным, т.е. он имеет кристалличность менее 1 мас.%. Наиболее предпочтительно аморфный сополимерный материал является материалом типа, продаваемого под торговой маркой "Топаз", поставляемого фирмами Шотт и Хехст (смотри табл. 1).
Также предпочтительно, чтобы стенки из аморфного полимера контейнера по изобретению имели светопропускание при 400 нм 60% или более, и наиболее предпочтительно светопропускание при 400 нм 75% или более, определенное, как указано выше.
Плотность частей стенки из аморфного полимера по изобретению составляет предпочтительно между 0,95 г/см3 и 1,05 г/см3, более предпочтительно около 1,02 г/см3.
Температура стеклования (Тс=Тg), определенная, как указано выше, составляет предпочтительно не менее 75oС, и более предпочтительно не менее 100oС. Стерилизация водяным паром является пригодной для стерилизации контейнеров, имеющих Тс выше этих температур. Для контейнеров из полимеров, имеющих более низкую Тс, используется стерилизация гамма-излучением.
Обычно, чем выше отношение циклических компонентов к линейным компонентам в сополимере, тем выше Тс полимера. Водобарьерные свойства коррелируются с содержанием циклического компонента в полимере так, что водный барьер улучшается при снижении количества циклического компонента относительно линейного компонента до некоторой степени. Предпочтительно полимерный материал содержит, по меньшей мере, 20% линейного олефина, предпочтительно, по меньшей мере, 50% линейного олефина, такого как этилен.
Соответственно температура стеклования составляет предпочтительно максимум 200oС, в частности не более 170oС, и еще предпочтительнее не более 150oС.
Аморфный полимер предпочтительно содержит не менее 75%, более предпочтительно более 95% и наиболее предпочтительно 98 мас.% или более сополимерного материала, такого как полиолефин.
Остальную часть материала могут предпочтительно составлять до 5 мас.% добавок, в частности, выбранных из антиоксидантов, смазок, таких как стеараты и силиконы, поверхностно-активных веществ, зародышеобразователей, и инертных наполнителей, таких как стеклянные частицы, имеющие показатель преломления, примерно равный показателю преломления полимерного материала, причем общее количество добавок и наполнителей составляет до 30 мас.%.
Контейнер по изобретению, имеющий полимерные части стенки из аморфного полимерного материала, может иметь любую пригодную форму. Предпочтительно внутренняя поверхность стенки и предпочтительно также наружная поверхность стенки контейнера имеет по существу цилиндрическую форму, потому что если эластичный резиновый поршень вращается до некоторой степени в контейнере, он может сохранить свое уплотняющее действие, только когда по меньшей мере внутренняя поверхность контейнера имеет по существу цилиндрическую форму.
Контейнер может быть предпочтительно гильзой, дальний конец которой содержит протыкаемое уплотнение, а ближний конец содержит поршень. Такие гильзы известны в технике.
Полимерные части стенки составляют не менее 30%, предпочтительно более 50% и более предпочтительно более 80% площади стенки.
Контейнер может иметь толстые и тонкие части стенки. Улучшенное светопропускание может быть получено при снижении толщины одной или более частей стенки контейнера. Это очевидно будет влиять на барьерные свойства этих частей. Улучшенные барьерные свойства контейнера могут быть получены при увеличении толщины одной или более частей стенки контейнера.
В предпочтительном варианте изобретения контейнер является гильзой, имеющей полимерную стенку с цилиндрической внутренней стороной и дальний конец, содержащий прокалываемое уплотнение, и ближний конец, содержащий поршень, причем стенка имеет различную толщину, чтобы обеспечить очень прозрачное окно.
Стенка контейнера может быть предпочтительно получена инжекционным формованием, в частности, если главная часть или вся стенка выполняются из полимерного материала.
Изобретение также касается контейнера, содержащего вышеописанный медикаментозный контейнер, по меньшей мере частично заполненный жидким медикаментозным раствором, содержащим один или более активных лекарственных препаратов, воду и метакрезол и/или фенол и/или бензиловый спирт. Таким лекарственным препаратом предпочтительно является раствор гормонов роста человека или инсулина, предпочтительно содержащий 25-600 межд. ед. инсулина, 0,1-5 мг фенола или бензилового спирта и 0,5-5 мг метакрезола на 1 мл медикаментозного раствора.
В примерах используются следующие методы определения свойств материала.
Проницаемость
Из материалов формовали 3 мл контейнеры с наружным диаметром 11,05 мм, внутренним диаметром 9,25 мм и толщиной стенки 0,90 мм. Контейнеры герметизировали с помощью пробки из бром-бутилового каучука с одного конца и ламинатом из бром-бутилового/натурального каучука - с другого конца.
Проницаемость для метакрезола определяли после хранения контейнера с инсулином (Актрапид, 100 межд.ед/мл Ново-Нордиск A/S) при 37oС, 13% относительной влажности (отн.вл.) в течение 3 месяцев.
Пропускаемость воды определялась после хранения контейнера с инсулиновой рецептурой (Актрапид, 100 межд.ед/мл Ново-Нордиск A/S) при 37oС, 13% отн.вл. в течение 3 месяцев и при 8oС, 13% отн.вл. в течение 6, 12 и 18 месяцев.
Проницаемость метакрезола
Потери метакрезола определяли после хранения 3 месяца при 37oС методом ЖХВД (жидкостной хроматографии высокого давления) с исключением по размеру с использованием изократного элюирования подвижной фазой на колонке Уотерс Протеин-Пак 1-125 со следующей композицией: 600 г ледяной уксусной кислоты, 600 г ацетонитрила, 2,8 г L-аргинина и воды, добавляемой до 4000 г. Замороженные эталоны использовали для коррекции смещения в системе ЖХВД. Стеклянные контейнеры с такими же размерами, как у полимерных контейнеров, использовали для коррекции потерь через резиновую пробку и резиновое уплотнение. Проницаемость рассчитывали.
Водопроницаемость
Водопроницаемость определяли как потерю веса после периода в 3, 6 и 18 месяцев. Потери были линейными от времени в период испытаний, и результаты поэтому могут быть экстраполированы до 36 месяцев при 8oС. Стеклянные контейнеры с одинаковыми размерами использовали для сравнения.
Прозрачность
Прозрачность определяли с помощью стандартного спектрофотометра с использованием воздуха в качестве эталона. Контейнер помещали так, чтобы световой луч падал перпендикулярно к пластмассовой поверхности, и так, чтобы световой луч проходил через стенку контейнера, через водный раствор или воду, содержащиеся в нем, и через противоположную стенку контейнера в детектор. В этой системе свет проходит через двойную толщину стенки. Диаметр светового луча поддерживают небольшим по сравнению с диаметром контейнера, чтобы избежать отражения от поверхности контейнера.
Плотность
Плотность полимерных материалов определяли путем определения изменения объема водного раствора, содержащего детергент, при добавлении известного веса пластика к жидкости.
Содержание этилена
Содержание этилена определяли с использованием метода протонного ЯМР.
Температура стеклования
Температуру стеклования циклических полиолефиновых материалов определяли с помощью дифференциальной сканирующей калориметрии (ДСК). Образцы вырезали из контейнеров и помещали в алюминиевые кюветы. Образцы последовательно нагревали от 10oС до 270oС со скоростью 10oС/мин. Температуру стеклования определяли как температуру в точке сгиба на стадии подачи теплового потока, вызывающего достижение стеклования материала.
Материалы
В примерах использовали материалы, указанные в табл. 1.
Изученные материалы были получены от компаний в виде не выпускаемых промышленностью прозрачных материалов, разработанных для последующего промышленного выпуска. Разработанные материалы поэтому не выпускаются серийно, но могут быть получены от поставщика при запросе.
Пример 1
Инжекционным формованием получают контейнеры из 4 различных циклических полиолефинов (смотри таблицу 1). Размеры 3 мл контейнеров являются следующими: наружный диаметр - 11,05 мм, внутренний диаметр - 9,25 мм, толщина стенки - 0,90 мм. Контейнеры герметизируют пробкой из бром-бутилового каучука на одном конце и ламинатом из бром-бутилового/натурального каучука - на другом конце. Материалы "Топаз" фирмы Хехст состоят из элементов бициклического мономера в комбинации с элементами этилена, а CZ-смола от фирмы Дейкайо состоит из элементов моноциклического мономера.
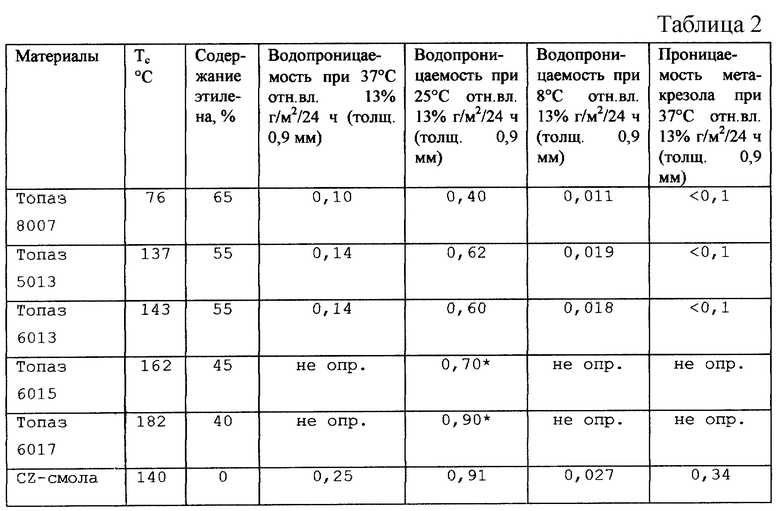
Водопроницаемость материалов определяется в 3 различных условиях. Проницаемость метакрезола определяется при 37oC. Приблизительное содержание этилена получено при изготовлении. Температура стеклования (Тс) определяется методом ДСК. Данные проницаемости при 25oC материалов Топаз 6015 и 6017 оцениваются по данным изготовлении и поставки и отмечены звездочкой.
Как видно из табл. 2, контейнеры из материалов Топаз 8007, Топаз 5013 и Топаз 6013 все являются превосходными в отношении как светопропускания, так и барьерных свойств.
Образец Топаза 8007, имеющий температуру стеклования 76oC, имеет немного меньшую проницаемость, чем образец из Топаза 5013 и Топаза 6013, имеющих высокую температуру стеклования 137 и 143oC соответственно.
CZ-смола исследуется для сравнения, причем содержание этилена CZ-смолы составляет 0, поэтому циклический компонент составляет 100% полимера. Высокое содержание циклического компонента ухудшает показатели водопроницаемости при всех температурах испытаний, особенно при 80oC. Также барьерные свойства по метакрезолу снижаются по сравнению с полимерами по изобретению.
Изобретение относится к медикаментозным контейнерам для хранения жидкого медикамента, такого как инсулин, содержащим дальний и ближний концы и стенку, причем, по меньшей мере, две противоположные части стенки выполнены из полимерного материала. Толщина полимерных частей стенки составляет между 0,3 и 3 мм, а светопропускание через полимерные части стенки при 400 нм составляет не менее 25%. Полимерные части стенки выполнены из материала, содержащего не менее 70 мас.% сополимерного материала, состоящего из алифатических циклических или бициклических углеводородов с 5-7-звенным кольцом или кольцами и этилена или пропилена, причем материал имеет температуру стеклования выше 50oС и плотность 0,95 г/см3 или более. Контейнер из полимерного материала является по существу инертным к лекарственному препарату и, кроме того, контейнер является прозрачным, в результате чего можно визуально контролировать содержимое контейнера, чтобы гарантировать, что лекарственный препарат не кристаллизован и не полимеризован. Выполнение контейнера обеспечивает хороший барьер для консервантов (метакрезол/фенол/бензиловый спирт) и для воды соответственно. 2 с. и 17 з.п.ф-лы, 2 табл.
| Топка с несколькими решетками для твердого топлива | 1918 |
|
SU8A1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| СПОСОБ ПОДГОТОВКИ ПАРАНТЕРАЛЬНОГО ЛЕКАРСТВЕННОГО СРЕДСТВА К ХРАНЕНИЮ | 1998 |
|
RU2134565C1 |
Авторы
Даты
2002-06-10—Публикация
1997-12-16—Подача