Изобретение относится к стабилизированному фармацевтическому препарату, включающему гормон роста, к методу изготовления такого препарата и использованию аспарагина для стабилизации препарата гормона роста.
Гормоны роста человека и обычных домашних животных являются белками, состоящими примерно из 191 аминокислоты, синтезируемыми и секретируемыми передней долей гипофиза. Человеческий гормон роста состоит из 191 аминокислоты.
Гормон роста является ключевым гормоном, вовлеченным в регуляцию не только соматического роста, но также в регуляцию метаболизма белков, углеводов и липидов. Основное действие гормона роста состоит в стимуляции роста.
Системы органов, на которые влияет гормон роста, включают скелет, соединительную ткань, мышцы и внутренние органы, такие как печень, кишечник и почки.
До разработки рекомбинантной технологии и клонирования гена гормона роста, вызывающих в настоящее время подъем производства, например, человеческого гормона роста (hGH) и Мет- hGH в промышленном масштабе, человеческий гормон роста мог получаться только путем экстракции из гипофизов человеческих трупов. Весьма лимитированные поставки гормона роста ограничивали его использование стимуляцией роста в действие и во время полового созревания для лечения карликовости и недоразвития, даже хотя и предлагалось лечение им малорослости (связанной с дефицитом гормона роста, нормальной малорослости и синдрома Тернера), дефицита гормона роста у взрослых, бесплодия, лечение ожогов, заживление ран, лечение дистрофии, применение для стимуляции обломков при срастании костных переломах, лечения остеопороза, диффузного желудочного кровотечения и ложных суставов.
Кроме того, было предложено применение гормона роста для увеличения скорости роста домашних животных или для снижения количества жира у животных, предполагаемых к забою для потребления человеком.
Фармацевтические препараты гормона роста имеют тенденцию к нестабильности. Образуются продукты разрушения такие, как дезамидированные или сульфоксидированные продукты и димерные или полимерные формы, особенно в растворах гормона роста.
Преобладающими реакциями разрушения hGH являются: 1) дезамидирование путем прямого гидролиза или через циклическое сукцинимидное промежуточное соединение с образованием различных количеств L-asp-hGH, L-изо-asp-hGH, D-asp-hGH и D-изо-asp-hGH (публикации 1 3), 2) окисление метиониновых остатков в положениях 14 и 125 (публикации 4 9), и 3) расщепление пептидных связей.
Дезамидирование происходит особенно у Asn в положении 149.
hGH довольно легко окисляется в положениях 14 и 125, особенно в растворе (4 8),
Окисление hGH в растворе с образованием сульфоксидов обычно является следствием кислорода, растворенного в препарате. Растворимость кислорода в дистиллированной воде составляет примерно 200 мкМ (9). Так как концентрация hGH в препарате, содержащем 4 IU/мл, составляет 1,3 мг/мл, соответствуя 60 nМ hGH, кислород будет присутствовать при условиях нормального хранения в избытке, примерно в 3000 раз больше стехиометрического количества для окисления hGH. Невозможно практически решить эту проблему путем дегазирования буферов перед упаковыванием и запечатыванием препаратов.
В настоящее время не считают, что эти продукты деградации обладают токсическим или измененным биологическим действием или свойствами связывания с рецептором, но есть указание на то, что стабильность конформации сульфоксидов снижается по сравнению с природным hGH.
Для разработки стабильного, растворенного препарата, содержащего hGH важно знать степень образования сульфоксидов так же, как и средства борьбы с окислением.
Кинетика деградации зависит от температуры, pH и различных добавок или адъювантов и лекарственной форме (препарате) hGH.
Из-за нестабильности гормон роста в настоящее время лиофилизуется и хранится в лиофилизованной форме при 4oC до перевода в прежнее состояние (реконституирования) для использования, чтобы минимизировать деградацию.
Лиофилизованные фармацевтические препараты, включающие hGH, в настоящее время реконструируется пациентом и затем хранятся в виде раствора во время использования в течение периода до 14 дней при 4oC, во время которого будет происходить некоторая деградация.
Кроме того, процесс перевода в прежнее состояние лиофилизованного гормона роста имеет тенденцию представлять трудности для больного.
Таким образом, в настоящее время предпочтительно реконструировать гормон роста как можно за меньший срок перед использованием и хранить и доставлять препарат в лиофилизованном состоянии. В цепи движения препарата от производителя до аптеки есть условия для осуществления манипуляций с препаратами при контролируемой низкой температуре, например, 4oC, что обеспечивает длительное хранение, до двух лет.
Однако, расширенное использование "пэн" систем для самолечения и обширная область применения требуют препарата, который стабилен в течение достаточно длительного срока до конечного использования в условиях, когда "достаточное" охлаждение не всегда доступно.
Предпочтительно, препарат должен быть стабилен у конечного пользователя в лиофилизованном состоянии в течение примерно одного месяца и дополнительно в течение одного месяца в реконструированном состоянии в "пэн" устройстве в течение преднамеренного периода использования картриджа.
Таким образом, существует потребность в более стабильных препаратах гормона роста, которые будут стабильны в лиофилизованном состоянии при относительно высокой температуре в течение какого-то периода и дополнительно в течение периода использования в растворе при относительно высокой температуре. Такая стабилизация имеет очень большое значение, когда введение гормона роста перемещается из клиник в дома отдельных лиц, которых нужно лечить, где нельзя достичь оптимального хранения, как указано выше.
Более того, изменение характера введения гормона роста в сторону использования "пэн" (закрытых) устройств требует стабильного растворенного препарата, содержащего гормон роста, чтобы облегчить манипуляции, которые должен выполнять пациент. Стабильный растворенный препарат, содержащий гормон роста может производиться готовым для использования в форме картриджей, установленных в закрытое устройство, используемое больным, который может в таком случае избежать реконституирования препарата, и следовательно, не будет содержать лиофилизованного препарата, подходящего растворителя для реконституирования также как не потребует необходимого умения и стерильного инструментария для стерильной подготовки препарата.
Из соображений безопасности желательно также избежать реконституирования лиофилизованного препарата непосредственно перед применением препарата.
Кроме того, было бы также выгодно исключить стадии лиофилизации при получении препаратов гормона роста. Лиофилизация длительный и дорогостоящий процесс, и часто "узким местом" в производстве является ограниченная мощность лиофильной сушилки.
Таким образом, существует необходимость снизить степень процессов деградации, чтобы дать возможность получения растворенных препаратов hGH, которые будут стабильны во время хранения и в течение периода использования до одного месяца.
Предыдущие попытки стабилизировать hGH не были полностью успешными в предотвращении образования димера. Проблемы, связанные с образованием димера отмечены, например, у Becker G.W. Biotechnology and Applied Biochemistry, 9, 478 (1987).
Международная патентная публикация N WO 89/09614 и Австралийская патентная заявка N 30771/89 раскрывают стабильную фармацевтическую лекарственную форму, содержащую человеческий гормон роста, глицин и маннит. Такой препарат демонстрирует улучшенную стабильность в течение обычной переработки и хранения в лиофилизованном состоянии, так же как и в течение периода использования после реконституирования.
Опубликованная Европейская патентная заявка N 303 746 раскрывает, что гормон роста животного можно стабилизировать различными стабилизаторами, обеспечивая пониженное образование нерастворимых веществ и сохранение активности в растворе в водной среде, и такие стабилизаторы включают некоторые полиолы, аминокислоты, полимеры аминокислот, имеющих заряженные боковые группы при физиологической величине pH и соли холина. Полиолы выбираются из группы, состоящей из невосстанавливающихся сахаров, спиртов сахаров, кислот сахаров, пентаэритрита, лактозы, растворимых в воде декстранов и фиколла; аминокислоты выбираются из группы, состоящей из глицина, саркозина, лизина или их солей, серина, аргинина или их солей, бетаина, N,N-диметилглицина, аспарагиновой кислоты или ее солей, глютаминовой кислоты или ее солей; полимеры аминокислот, имеющих заряженную боковую группу при физиологической pH могут выбираться из полилизина, полиаспарагиновой кислоты, полиглютаминовой кислоты, полиаргинина, полигистидина, полиорнитина и их солей; производные холина выбираются из группы, состоящей из холинхлорида, моно-холин-цитрата, битартрата холина, бикарбоната холина, трихолинцитрата, аскорбата холина, бората холина, глюконата холина, фосфата холина, дихолинсульфата и дихолинмуката.
В настоящее время было обнаружено, что препарат человеческого гормона роста, содержащий аспарагин в качестве добавки или буферного вещества, демонстрирует очень высокую стабильность в отношении дезамидирования, окисления и расщепления пептидных связей. Стабильность этого препарата дает возможность его хранения или перевозки в лиофилизованном состоянии или в форме растворенного или вновь растворенного препарата.
Таким образом, препарат данного изобретения может быть в форме лиофилизованного порошка, реконституируемого впоследствии с использованием общепринятых носителей, таких как дистиллированная вода или вода для инъекций, или в форме раствора, содержащего гормон роста. Такие носители или растворители могут включать общепринятые консерванты, такие как m-крезол и бензиловый спирт.
Предпочтительное осуществление изобретения представляется в форме фармацевтического препарата человеческого гормона роста, содержащего аспарагин в виде буферированного водного раствора гормона роста, забуференного аспарагиновым буфером. Такой препарат является формой, готовой к употреблению, и может храниться и перевозиться в виде водного раствора без какой-либо значительной деградации.
Из соображений стабильность pH раствора предпочтительно доводится до значения в интервале 2 8. Препараты, имеющие pH от 5 до 8 более предпочтительны, и наиболее предпочтительны препараты, имеющие pH от 6 до 7,5.
Для получения стабилизирующего эффекта аспарагин, предпочтительно, добавляется в количестве до 100 мМ. Концентрация аспарагина предпочтительно находится в интервале от 2 до 20 мМ, наиболее предпочтительно от 2 до 10 мМ.
Фармацевтический препарат данного изобретения может также находиться в форме лиофилизованного препарата.
Фармацевтический препарат изобретения может, кроме того, может содержать соли и сахариды, для того, чтобы облегчить его обработку, например, лиофилизацию. Обычно в качестве наполняющего агента для лиофилизации используется маннит.
Еще один аспект этого изобретения относится к использованию аспарагина для получения стабилизированного препарата гормона роста.
В настоящем контексте "гормон роста" может быть гормоном роста любого происхождения, таким как птичий, бычий, лошадиный, человеческий, овечий, свиной, лососевый, форелевый или тунцовый гормон роста, предпочтительно, бычьим, человеческим или свиным гормоном роста, причем наиболее предпочтителен человеческий гормон роста. В соответствии с изобретением используемый гормон роста может быть природным гормоном роста, выделенным из природного источника, например, путем экстрагирования гипофизов общепринятым способом, или гормоном роста, полученным с помощью рекомбинантных методик, например, как описано у E. B. Jensen and S. Carlsen в Biotech. and Bioeng 36, I-II (1990). "Гормон роста" также может быть усеченной формой гормона роста, в которой один или более аминокислотных остатков удален (удалены); его аналогом, в котором один или более аминокислотных остатков в природной молекуле замещен (замещены) другим аминокислотным остатком, предпочтительно остатком природной аминокислоты, если замещение не оказывает какого-либо вредного действия, такого как антигенность или пониженное действие; или его производным, например, имеющие N- или C-концевое продолжение, такое как Met-hGH, Met-Glu-Ala-Glu-hGH или Ala-Glu-hGH. Предпочтительным гормоном роста является hGH.
В настоящем контексте под "высокой стабильностью" понимается случай, когда препарат стабильнее общепринятого препарата, содержащего фосфатный буфер.
Термин "соли", использованный в этом описании для обозначения дополнительных составляющих фармацевтического препарата, включает такие общепринятые соли, как соли щелочных металлов, щелочноземельных металлов или аммонийные соли органических кислот, таких как лимонная кислота, виннокаменная кислота или уксусная кислота, например, цитрат натрия, тартрат натрия или ацетат натрия, или минеральных кислот, таких как соляная кислота, например, хлорид натрия.
"Сахариды" могут быть моносахаридами, дисахаридами или спиртами сахаров, которые обычно используются для фармацевтических препаратов, такими как лактоза или маннит.
Растворитель, используемый в препаратах данного изобретения, может быть водой, спиртом, таким как этиловый, н-пропиловый или изопропиловый, бутиловый спирт или их смеси. Растворитель может включать консервант, такой как м-крезол или бензиловый спирт.
Изобретение объясняется более подробно в нижеследующих примерах, которые иллюстрируют изобретение. Они не должны рассматриваться как ограничивающее объем изобретения, который определяется прилагаемой формулой изобретения.
Экспериментальная часть.
Пример.
Снижение дезамидирования.
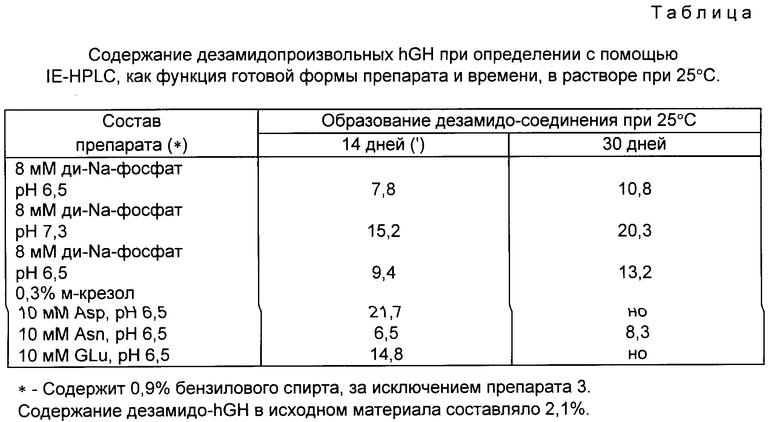
Степень дезамидирования оценивалась при 25oC для препаратов hGH, содержащих 6 IU hGH при pH 6,5 в присутствии 10 мМ Asn в сравнении с 8 мМ фосфатным буфером при том же самом значении pH и pH 7,3.
Препараты hGH получали путем растворения 20 мг hGH в 10 мл 10 мМ раствора аспарагина, приготовленного путем растворения 13,2 мг аспарагина в 10 мл деионизированной воды, содержащей 0,9% (объем/объем) бензилового спирта, и добавлением 0,1 норм. соляной кислоты до установленного pH.
Препараты hGH, представленные в нижеследующей таблице, хранили при 25oC и анализировали на содержание дезамидо-производных через 14 и 30 дней с помощью IE-HPL C. Результаты видны из нижеследующей таблицы.
Из вышеприведенной таблицы видно, что дезамидирование hGH снижается примерно на 25% при добавлении по сравнению с фосфатным буфером при pH 6,5.
Добавление Asp или Glu увеличивает скорость дезамидирования по сравнению с фосфатным буфером при pH 6,5.
Вышеприведенные результаты показывают, что степень дезамидирования снижается при снижении pH и добавлении аспарагина в низких концентрациях до 100 мМ, предпочтительно около 5 мМ. Степень дезамидирования может быть снижена более чем на 50% путем снижения pH и заменены фосфатного буфера аспарагином.
| название | год | авторы | номер документа |
|---|---|---|---|
| ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ, СОДЕРЖАЩИЙ ГОРМОН РОСТА ИЛИ ПРОИЗВОДНОЕ ГОРМОНА РОСТА И ГИСТИДИН ИЛИ ПРОИЗВОДНОЕ ГИСТИДИНА, ПРЕПАРАТ, ПРЕДСТАВЛЯЮЩИЙ СОБОЙ КРИСТАЛЛЫ ГОРМОНА РОСТА, СОДЕРЖАЩИЕ ГИСТИДИН ИЛИ ПРОИЗВОДНОЕ ГИСТИДИНА И СПОСОБ ПОЛУЧЕНИЯ КРИСТАЛЛОВ ГОРМОНА РОСТА И ГИСТИДИНА ИЛИ ПРОИЗВОДНОГО ГИСТИДИНА | 1992 |
|
RU2122426C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ГОРМОН РОСТА, АМИНОКИСЛОТУ И НЕИОНОГЕННЫЙ ДЕТЕРГЕНТ | 1997 |
|
RU2236250C2 |
| СПОСОБ ПОЛУЧЕНИЯ КРИСТАЛЛОВ ГР ИЛИ ПРОИЗВОДНЫХ ГР, КРИСТАЛЛЫ ЧЕЛОВЕЧЕСКИХ ГР ИЛИ ПРОИЗВОДНЫХ ЧЕЛОВЕЧЕСКИХ ГР И ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ | 1991 |
|
RU2108341C1 |
| СПОСОБ КОНЪЮГАЦИИ ПЕПТИДОВ, ОПОСРЕДОВАННОЙ ТРАНСГЛУТАМИНАЗОЙ | 2005 |
|
RU2385879C2 |
| СТАБИЛЬНЫЕ НЕВОДНЫЕ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 2008 |
|
RU2472492C2 |
| ИНСУЛИНОВЫЕ ПРЕПАРАТЫ, СОДЕРЖАЩИЕ УГЛЕВОДЫ | 1997 |
|
RU2204411C2 |
| ДИМЕР "КЛЕВЕРНОГО" ПЕПТИДА | 1995 |
|
RU2162857C2 |
| ЛИПОФИЛЬНЫЕ ПРОИЗВОДНЫЕ ПЕПТИДНЫХ ГОРМОНОВ | 1996 |
|
RU2171261C2 |
| СОЕДИНЕНИЯ, СПОСОБСТВУЮЩИЕ ВЫСВОБОЖДЕНИЮ ГОРМОНА РОСТА | 1994 |
|
RU2167881C2 |
| АНАЛОГИ ИНСУЛИНА ЧЕЛОВЕКА, СПОСОБ ИХ ПОЛУЧЕНИЯ, РАСТВОР ДЛЯ ИНЪЕКЦИЙ | 1986 |
|
RU2104305C1 |
Использование: в медицине, для стабилизации фармацевтического препарата гормона роста. Сущность изобретения: фармацевтический препарат содержит гормон роста и эффективное количество стабилизирующей аминокислоты - аспарагина. Применение аспарагина обеспечивает высокую стабильность препарата против дезамидирования, окисления и расщепления пептидных связей. Стабильность препарата дает возможность хранения и отгрузки его в офилизованном состоянии или в форме раствора при температуре окружающей среды. 2 с. и 5 з.п. ф-лы. 1 табл.
| ЕПВ, патент, 0303746, кл | |||
| Устройство для сортировки каменного угля | 1921 |
|
SU61A1 |
Авторы
Даты
1997-12-10—Публикация
1994-06-17—Подача