Изобретение относится к области удовлетворения жизненных потребностей человека, а именно к новым лекарственным средствам, которые могут найти применение в химико-фармацевтической и медицинской промышленности, конкретно к фосфорсодержащим производным изотиурония, в том числе новым химическим соединениям, влияющим на артериальное давление, которые обладают сосудосуживающим средством, используемым в случаях хронических и острых гипотонии (кровотечение, травма, шок, отравление), в том числе особенно в скорой и неотложной медицинской помощи.
В медицинской практике используют лекарственные вещества прессорного действия, которые воздействуют или за счет стимуляции альфа-адренергических рецепторов, или за счет прямого действия на гладкую мускулатуру сосудистой стенки. Чаще всего применяют адреномиметики, например адреналин, норадреналин, мезатон, метоксалин, эфедрин, фетанол и др., и препараты полипептидной природы, например глюкагон, антиотенинамид, октапрессин и т.п.
По фармакологическим свойствам наиболее близким аналогом предлагаемому соединению является известный лекарственный препарат мезатон (М.Д.Машковский. Лекарственные средства, изд. 12-е, М., Медицина, 1993, часть I, стр. 303).
Мезатон представляет собой 1-(м-оксифенил)-2-метиламиноэтанола гидрохлорид. Он селективно стимулирует α1-адренорецепторы, вызывает сужение артериол и повышение систолического и диастолического давления (с возможной рефлекторной брадикардией). Мезатон практически не имеет кардиостимулирующего действия. В отличие от адреналина и норадреналина мезатон не является катехоламином (он содержит лишь одну гидроксильную группу в ароматическом ядре) и мало подвержен действию фермента катехол-О-метилтрансферазы, в связи с чем более стоек, оказывает более длительный эффект. Антигипотензивное действие мезатона длится обычно около 20 минут после однократного внутривенного введения (М.Д.Машковский, Лекарственные средства, изд. 12-е, М., Медицина, 1993, часть I, стр. 303; О.М.Авакян, Фармакологическая регуляция функции адренорецепторов, М., Медицина, 1988, стр. 8).
Адреномиметики, в том числе мезатон, имеют некоторые общие недостатки, так они увеличивают потребление кислорода тканями, вызывают метаболический ацидоз, могут вызвать аритмии (особенно во время общего наркоза), оказывают возбуждающее действие на ЦНС (О.М.Авакян, Фармакологическая регуляция функции адренорецепторов, М., Медицина, 1988, стр. 8, В.Г.Кулинский, А.Н.Ковалевский, Бюл.эксперим.биол.мед., 1984, стр. 9, "Дуалистический контроль катехоламинами потребления кислорода организмом мышей"). Для них характерно возникновение вторичной гипотензии. Адреномиметики не корригируют артериальную гипотензию, вызванную адреноблокаторами, в условиях метаболического ацидоза имеют лишь слабый антигипотензивный эффект (C.Kortanje, V.I.Mathy, R.Chartdorp, Haunyn-Gohinedeleg is Arh. Pharmacol., v.330, N3, p. 187-192 (1985), "Influence respiratory acidosis or alkalosis on pressor responses imediated by and alfa-adrenoreceptors in pithed normotensive rats", I.M.Autkunson, S. I.Dusting, V.I.Rand, Aust.J.Exp.Biol.Med., v.50, p.847-859 (1972), "Acidosis induced by catecholamines in acidosis").
Препараты с полипептидной структурой и большинство адреномиметиков имеют короткую продолжительность действия и для достижения пролонгированного эффекта их вводят в виде перфузии (I.M.Autkunson, S.I.Dusting, V.I.Rand, Aust. J.Exp.Biol.Med., v.50, p.847-859 (1972), "Acidosis induced by catecholamines in acidosis").
Химический синтез фосфорсодержащих производных S-алкилизотиурония впервые описан взаимодействием тиомочевины с триалкилфосфатами или диалкилфосфитами при нагревании в органическом растворителе, однако полученным соединениям приписано строение фосфатов N-алкилтиурония (J.B.Parker, Т.D. Smith, J.Chem.Soс., 1961, р.442-445, "The reaction of thiourea with dialkyl phosphites and trialkyl phosphates"). Позднее их строение было правильно установлено как фосфат или фосфинаты S-алкилизотиурония) (П.Г.Жеребченко, Ю. Д. Зильбер, Г. П. Поспехова и др., Радиобиология, т.8, стр. 582-587 (1968), "Радиозащитный эффект солей S-алкилзамещенных производных изотиомочевины при их раздельном и комбинированном изучении") и подтверждено физико-химическими методами анализа (Л.И.Мизрах, В.Г.Яковлев, Е.М.Юхно и др., ЖОХ, т.41, стр. 2654-2658 (1971), "Некоторые фосфорсодержащие производные изотиурония"), однако подробный метод их получения до сих пор не описан.
В литературе описано, что фосфорсодержащие производные S-алкилизотиурония обладают выраженным радиопротекторным действием (П.Г.Жеребченко, Ю.Д. Зильбер, Г. П. Поспехова и др. . Радиобиология, т.8, стр. 582-587 (1968), "Радиозащитный эффект солей S-алкилзамещенных производных изотиомочевины при их раздельном и комбинированном изучении"; Н.А.Изможеров, Ю.В.Гилев, Л.И.Мизрах и др. . Тезисы докладов на 2-й Всесоюзной конференции по фармакологии противолучевых препаратов, М. , 1972, стр. 129-133, "Модификация лучевой гибели животных с помощью фосфорсодержащих производных изотииурония"; Н.А. Изможеров, Л.И.Мизрах, В.В.Кожевников и др., там же, стр. 133-136, "Противолучевая эффективность на клеточном уровне фосфорсодержащих производных изотииурония"; Т.Ю.Ильюченок, Л.М.Фригидова, Ю.В.Завьялов и др.. Фармакология и токсикология, т.39, стр. 191-198 (1972), "Радиозащитные свойства некоторых фосфорсодержащих производных изотииурония"; Ж.А.Голощапова, Лучевое воздействие, восстановление и химическая защита. Свердловск, 1978, стр. 71-75, "Токсические и радиозащитные свойства некоторых фосфорсодержащих производных изотииурония"; Ж.А.Голощапова, Т.Н.Тужилкова, Л.И.Мизрах, Радиобиология, т.21, стр. 521-525 (1981), "Экспериментальное обоснование использования некоторых производных изотиурония в качестве радиозащитных соединений") и изучены некоторые токсикологические характеристики.
Задачей предлагаемого изобретения является поиск веществ, в том числе новых соединений, обладающих гипертензивной активностью и лишенных указанных недостатков адреномиметиков.
Поставленная задача решается использованием фосфорсодержащих производных S-алкилизотиурония, в том числе новых не описанных в литературе, общей формулы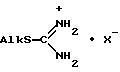
где Alk представляет собой разветвленный или неразветвленный алкил, а Х- - анион фосфорсодержащей кислоты, в качестве средств, влияющих на артериальное давление.
Их синтез осуществляется известными способами, чаще всего алкилированием тиомочевины соответствующими фосфорсодержащими производными, изредка использовали обменную реакцию солей.
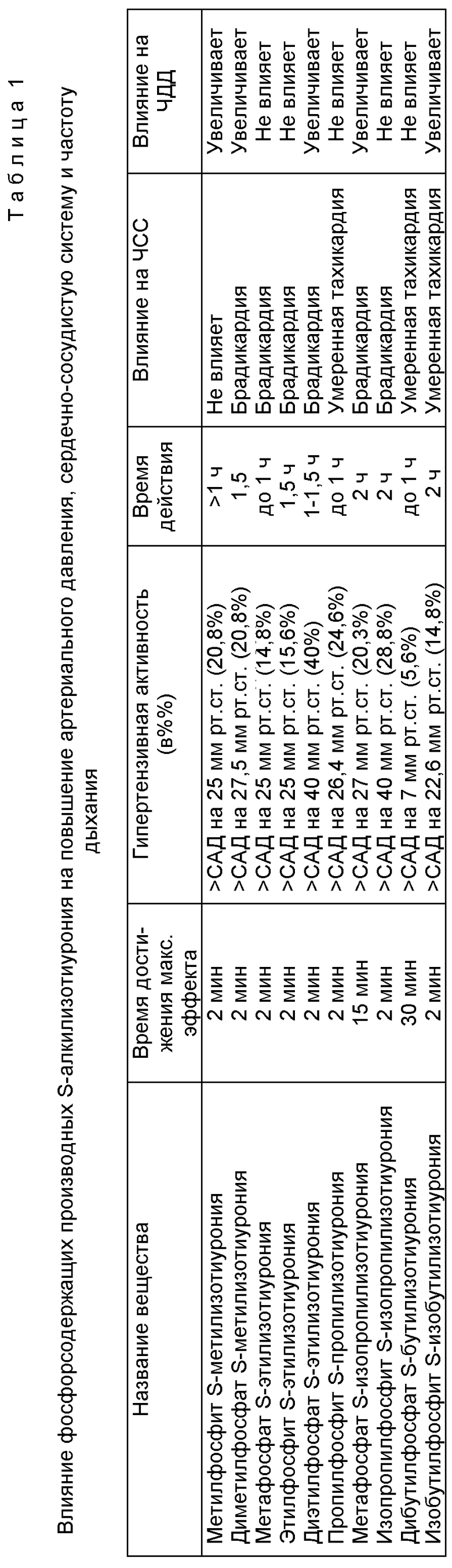
Как видно из приведенных ниже данных по биологическому изучению (фиг. 1-10, табл.1) фосфорсодержащих производных S-алкилизотиурония, последние обладают выраженным, как правило, быстрым и длительным влиянием на артериальное давление.
Следует особенно отметить новые химические соединения:
диметилфосфат S-метилизотиурония,
метафосфат S-изопропилизотиурония,
изобутилфосфит S-изобутилизотиурония.
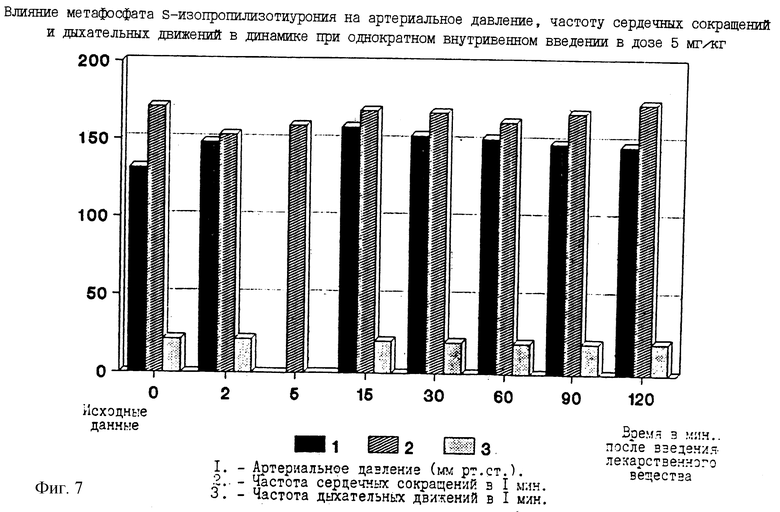
Полезно подчеркнуть, что метафосфат S-изопропилизотиурония, заметно увеличивая артериальное давление, не влияют на частоту дыхательных движений.
Наиболее подробно изучен диэтилфосфат S-этилизотиурония, эффект которого представлен в табл. 2-5 и фиг. 11-14.
Время действия диэтилфосфата S-этилизотиурония по сравнению с адреномиметиками (например, мезатоном) увеличивается в 2-3 раза (табл. 2-5, фиг. 11-13). Предлагаемое соединение не влияет отрицательно на кислотно-щелочное равновесие (табл. 6, 7), не вызывает вторичной гипотензии (фиг. 11-13), обладает специфической активностью в условиях действия α-адреноблокаторов (табл. 3), практически не уменьшает эффективности в условиях метаболического ацидоза (табл. 4), улучшает показатели системной гемодинамики при геморрагическом шоке (табл. 4).
При действии диэтилфосфата S-этилизотиурония показатели системной гемодинамики изменяются следующим образом: возрастает периферическое сосудистое сопротивление, увеличивается ударный объем и центральный объем циркулирующей крови, увеличивается работа левого желудочка (табл. 4).
При шоковых состояниях (травматическом, геморрагическом) внутримышечное введение диэтилфосфата S-этилизотиурония позволяет оказать помощь на догоспитальном этапе (табл. 4), чего нельзя добиться лекарственными средствами, используемыми в настоящее время.
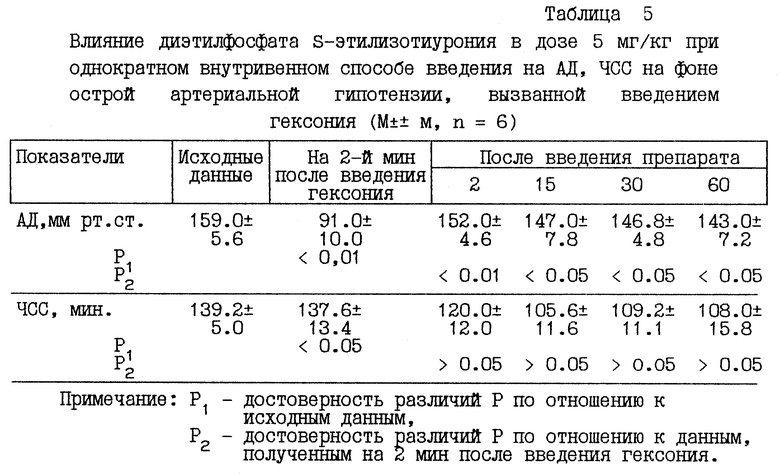
Рекомендуется использовать диэтилфосфат S-этилизотиурония в качестве лекарственного вещества для повышения артериального давления при острой артериальной гипотонии, вызванной хирургическими вмешательствами, травмами, отравлениями, шоковыми состояниями, кровотечениями, при перидуральной анестезии, при передозировке ганглиоблокаторов (табл. 5), альфа-адреноблокаторов (табл. 3), нейролептиков, анестетиков и при других состояниях, когда адреномиметики противопоказаны или неэффективны (табл. 6, 7).
Интересно, что влияние диэтилфосфата S-этилизотиурония сильнее в случае животных гипотоников, чем для нормотоников (фиг. 12, 13).
Все эти данные показывают, что предлагаемые соединения отличаются от известных средств, которые применяются для повышения кровяного давления.
В настоящее время подготавливается документация на диэтилфосфат S-этилизотиурония для направления в Фармакологический Комитет Минздравмедпрома РФ на предмет получения разрешения на проведение его клинических испытаний под названием "Дифетур", остальные вещества подвергаются расширенному биологическому и токсикологическому изучению.
Использование предлагаемых соединений в медицинской практике создает новые возможности в лечении острых и, возможно, хронических артериальных гипотензий, а также в случаях неотложной и скорой помощи.
Фосфорсодержащие производные S-алкилизотиурония могут применяться в удобной для данного конкретного случая лекарственной форме. Чаще всего предлагается использовать препараты в виде таблеток, ампул для внутримышечного или внутривенного введения, однако можно использовать и другие лекарственные формы, например свечи. В экстренных состояниях рекомендуется вводить препараты внутривенно или внутримышечно в виде 1-10% водных растворов в дозе 0,1-20 мг/кг массы тела, обычно 0,2-5 мг/кг.
Фосфорсодержащие производные S-алкилизотиурония являются малотоксичными (LD50 равняется 100-1000 мг/кг).
Относительными противопоказаниями являются: артериальная гипертензия, феохромоцитома, беременность. С осторожностью нужно назначать препарат людям пожилого возраста.
В случае передозировки препарата рекомендуется внутривенное введение антагонистов кальция (верапрамил) или папаверина.
Приведенные ниже экспериментальные данные иллюстрируют, но не ограничивают притязаний заявителя.
Синтез фосфорсодержащих производных S-алкилизотиурония.
Диэтилфосфат S-этилизотиурония.
В колбу загружают 36,6 г (0,201 М) триэтилфосфата и 15,2 г (0,2 М) предварительно измельченного тиокарбамида. Реакционную массу при перемешивании нагревают до 132-135oС и выдерживают при этой температуре до полного растворения тиокарбамида (примерно 3-5 мин). Продолжая перемешивание, нагревание прекращают и дают смеси самопроизвольно охлаждаться. При достижении реакционной смесью температуры 50-60oС к ней приливают 40 мл ацетона. При дальнейшем понижении температуры начинается кристаллизация продукта, которая завершается при перемешивании при комнатной температуре за 3 часа. Кристаллы отфильтровывают, промывают 10 мл ацетона и сушат до постоянного веса. Выделяют 26,6 г диэтилфосфата S-этилизотиурония-сырца, который перекристаллизовывают из ацетона. Получают 24,6 г (47,7% от теоретического) диэтилфосфата S-этилизотиурония с т.пл. 144-146oС, литературные данные т.пл. 145oС (J.B. Parker, 1961), содержание основного вещества 99.6%.
Найдено, %: С 32.57, Н 7.43, N 10.75, Р 11.87, S 12.47. C7H19N2O4PS. Вычислено, %: С 32.56, Н 7.36, N 10.85, Р 12.01, S 12.40.
Тонкослойная хроматография - пластины "силуфол" система:
водный аммиак:хлороформ: пропан-2-ол (1:8:4) Rf=0,19;
водный аммиак:хлороформ: пропан-2-ол (3:1:2) Rf=0,44.
Изопропилфосфит S-изопропилизотиурония.
Смесь 13,7 г (0,082 М) диизопрпопилфосфита и 6,2 г (0,082 М) тиомочевины нагревают в трехгорлой колбе, снабженной мешалкой и обратным холодильником с хлоркальциевой трубкой, до температуры 135oС. При этом происходит растворение тиомочевины и образуется гомогенная масса. Нагревание при этой температуре продолжают еще 60-75 мин до легкого покраснения реакционной массы. После чего охлаждают смесь до 40-50oС и при работающей мешалке заливают 50 мл ацетона. Через 30 мин сырец отфильтровывают и получают 10 г (50,8%). После перекристаллизации из смеси ацетон - этиловый спирт (2:1) получают 6,0 г изопропилфосфита S-изопропилизотиурония с т.пл. 169-171oС, литературные данные т. пл. 164oС (В. В. Орловский, Б.А.Вовси, ЖОХ, т. 39, стр. 1259-1260 (1969). К вопросу о взаимодействии диалкилфосфитов с тиомочевиной).
Метафосфат S-этилизотиурония.
Смесь 8,65 г (0,05 М) диэтилхлорфосфата и 3,8 г (0,05 М) хорошо измельченной тиомочевины нагревают при перемешивании, поднимая температуру до 145oС в течение 1,5 часов, выдерживают при этой температуре 10 мин, охлаждают, приливают смесь этанол - ацетон (3:2) и оставляют на ночь. Растирают осадок в этой смеси растворителей и фильтруют, после кристаллизации из водного спирта получают 6,0 г (65%) метафосфата S-этилизотиурония с т.пл. 224-225oС.
Найдено, %: С 19.57, Н 4.90, Р 16.73, S 17.32. C7H19N2O4PS. Вычислено, %: С 19.55, Н 4.90, Р 16.85, S 17.40.
Это же вещество получают и другим способом:
Смесь 4,25 г этилметафосфата и 3,0 г тиомочевины при перемешивании нагревают 1,5 часа до 145oС, выдерживают при этой температуре 10 мин, охлаждают и обрабатывают, как указано выше. Получают 5,0 г (69%) метафосфата S-этилизотиурония с т.пл. 223-224,5oС.
Другие соединения получены аналогично:
метилфосфит S-метилизотиурония с выходом 73%, т.пл. 119-120oС, литературные данные т.пл. 120oС (В.В.Орловский, 1969),
диметилфосфат S-метилизотиурония с выходом 54%,
этилфосфит S-этилизотиурония с выходом 62%, т.пл. 109-110oС, литературные данные т.пл. 112oС (В.В.Орловский, 1969),
пропилфосфит S-пропилизотиурония с выходом 40%, т.пл. 99-100oС, литературные данные т.пл. 102oС (В.В.Орловский, 1969),
метафосфат S-изопропилизотиурония с выходом 21%, т.пл. 257-259oС,
дибутилфосфат S-бутилизотиурония с выходом 38%, т.пл. 96-98oС, литературные данные т.пл. 98oС (В.В.Орловский, 1969),
изобутилфосфит S-изобутилизотиурония с выходом 43%, т.пл. 162-164oС.
Строение полученных соединений подтверждено ИК-спектрами - у всех полученных соединений имеются характерные полосы поглощения в области υPO 1195-1207 см-1, υCN 1680-1695 см-1, υNH 1568-1590 см-1, и УФ-спектрами, имеющими характерное коротковолновое поглощение с λmax =201-203 нм и 223-225 нм.
Биологическое изучение фосфорсодержащих производных S-алкилизотиурония.
В настоящем разделе приведены результаты первичной фармакологической оценки фосфорсодержащих производных S-алкилизотиурония. Опыты проведены на 52-х наркотизированных (этаминал натрия, 45 мг/кг, внутрибрюшинно) кошках обоего пола массой от 2,8 до 4,2 кг. Артериальное давление регистрировали с помощью ртутного манометра и ЭКГ во втором стандартном отведении. Одновременно регистрировали также частоту дыхания. Оценивали выраженность гипертензивного эффекта (в процентах к исходному уровню систолического артериального давления (САД)), длительность наблюдения составляла 1-3 часа, по ЭКГ подсчитывали частоту сердечных сокращений (ЧСС). Полученные результаты приведены на фиг. 1-10 и в табл. 1.
Метилфосфит S-метилизотиурония повышает артериальное давление на 20%. Гипергензивный эффект сохраняется в течение 1 часа, соединение не влияет на ЧСС (фиг. 1).
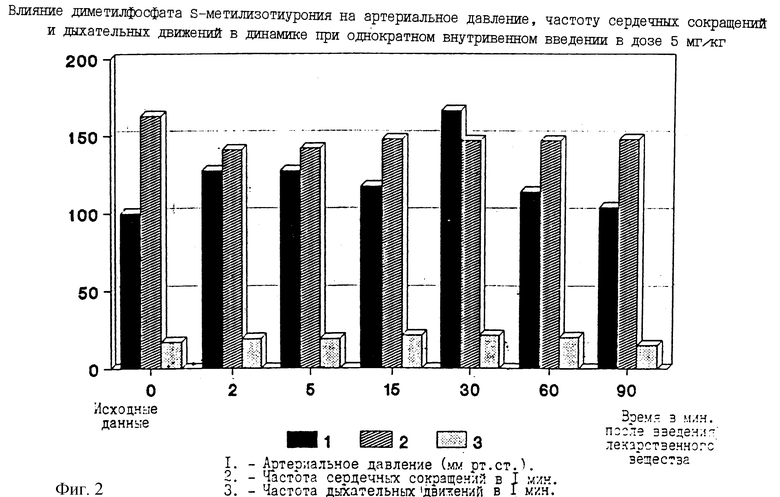
Диметилфосфат S-метилизотиурония - одно из наиболее активных соединений, оно повышает артериальное давление почти на 30%. Гипертензивный эффект сохраняется в течение 1,5 часов, соединение увеличивает частоту дыхательных движений (ЧДД) (фиг. 2).
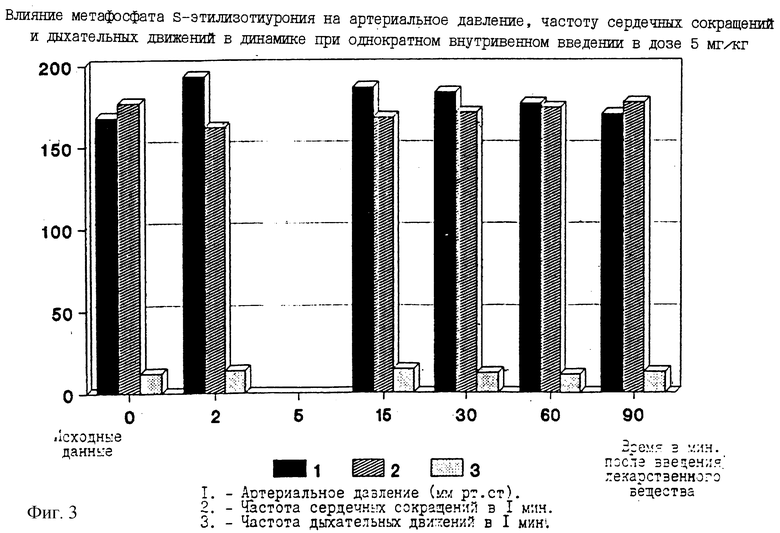
Метафосфат S-этилизотиурония повышает артериальное давление на 25 мм рт. ст., что составляет около 15% от исходного уровня. Гипертензия влияет на ЧДД (фиг. 3).
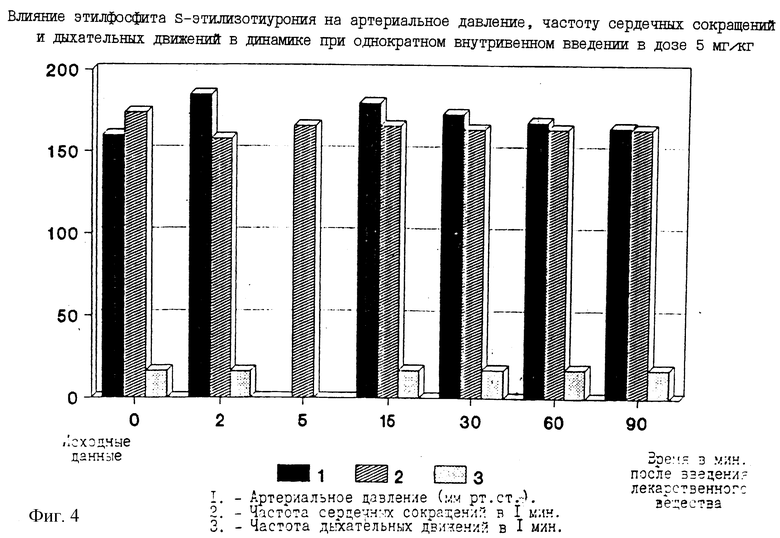
Этилфосфит S-этилизотиурония повышает артериальное давление на 15%. Продолжительность действия составляет 1,5 часа, соединение вызывает брадикардию, но не влияет на ЧДД (фиг. 4).
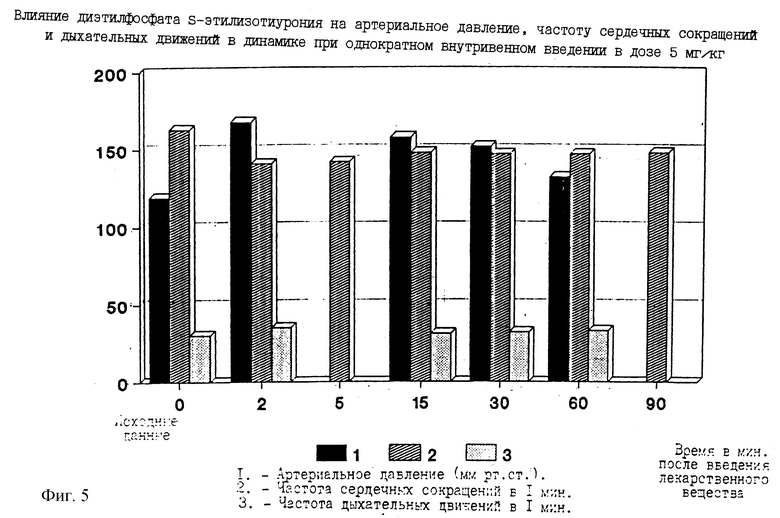
Диэтилфосфат S-этилизотиурония - одно из наиболее активных соединений. В изученной дозе повышает САД на 40%, увеличивает ЧДД (фиг. 5).
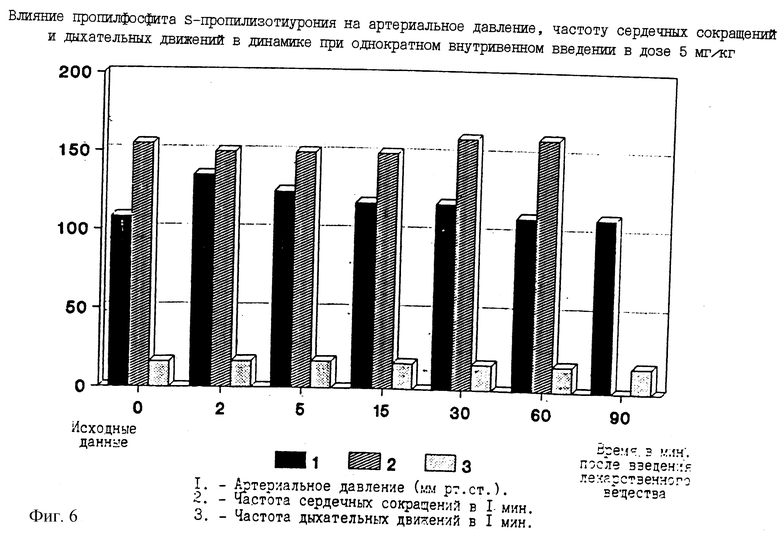
Пропилфосфит S-пропилизотиурония повышает артериальное давление на 24%. Гипертензивный эффект сохраняется в течение 1 часа, соединение вызывает умеренную тахикардию, но не влияет на ЧДД (фиг. 6).
Метафосфат S-изопропилизотиурония медленно повышает САД, максимальный эффект наблюдается только через 15 мин, но эффект сохраняется более 2 часов. Не влияет на ЧДД (фиг. 7).
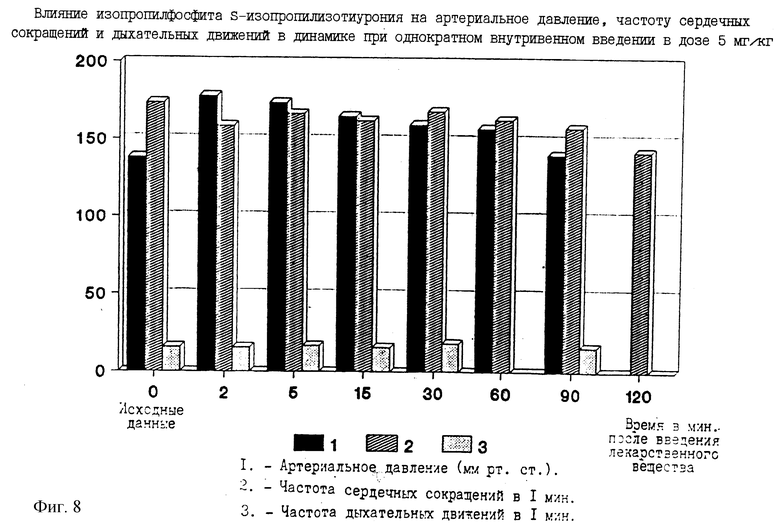
Изопропилфосфит S-изопропилизотиурония - одно из наиболее перспективных веществ, которое повышает САД почти на 30%, максимальный эффект достигается уже на 2-й мин после введения и сохраняется более 2-х часов. Отмечается транзиторная брадикардия, соединение не влияет на ЧДД (фиг. 8).
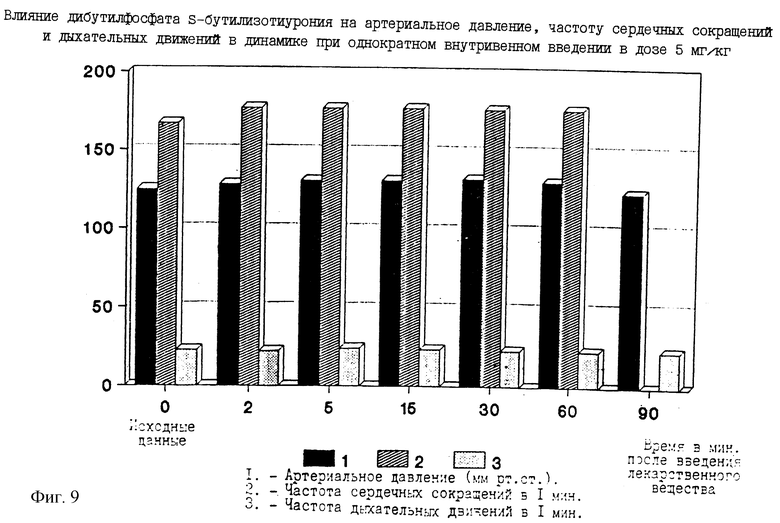
Дибутилфосфат S-бутилизотиурония слабо повышает артериальное давление. Гипертензивный эффект сохраняется в течение 1 часа (фиг. 9).
Изобутилфосфит S-изобутилизотиурония оказывает умеренное гипертензивное действие продолжительностью 2 часа, увеличивая при этом ЧСС и ЧДД (фиг. 10).
Далее приведены основные результаты экспериментов, подтверждающих возможность применения диэтилфосфата S-этилизотиурония по указанным в описании направлениям.
Эксперименты по изучению действия диэтилфосфата S-этилизотиурония на показатели системной гемодинамики проведены на 8 наркотизированных кошках массой 2-4 кг. Для наркотизации применяли уретан (внутрибрюшинно в виде 30% раствора из расчета 1-1,2 г/кг). С целью выявления периода максимальной эффективности и продолжительности действия препарата основные параметры системного кровообращения определяли до его введения (исходные данные), а также на 2, 15, 30 и 60-й минутах после введения диэтилфосфата S-этилизотиурония в дозе 5 мг/кг.
Системная гемодинамика оценивалась по совокупности следующих показателей: величины артериального давления (АД), частоты сердечных сокращений (ЧСС), минутного объема кровообращения (МОК), систолического объема сердца (СО), общего периферического сопротивления сосудов (ОПСС), работы левого желудочка (Алж).
Артериальное давление регистрировали у кошек в левой общей сонной артерии с помощью ртутного манометра. Для предупреждения свертывания крови вводили внутривенно 0,2-0,3 мл (1000-1500 ЕД) гепарина. Частоту сердечных сокращений подсчитывали по интервалу R-R электрокардиогаммы, запись которой осуществлялась двухканальным электрокардиографом ЭЛКАР-2 (модель 0-87). МОК рассчитывали по Ramirez A. A. et al. (1956). На основании данных о МОК, АД, центрального объема крови и ЧСС вычисляли СО сердца, Алж и ОПСС по формуле Wiggers C. G. (1947). Цифровой материал, полученный в экспериментах, подвергали статистической обработке с использованием программ для расчета t-критерия Стьюдента. Результаты сведены в таблицу 2.
Результаты опытов показали, что однократное внутривенное введение диэтилфосфата S-этилизотиурония в дозе 5 мг/кг вызывает быстрое и выраженное повышение АД. Уже на 2-й мин после введения препарата АД составляло 141% по отношению к исходному уровню и сохранялось на высоком уровне длительное время. На 60-й мин уровень АД снижался по сравнению с установленным на 30-й мин, но еще превосходил (на 11%) исходную величину. Различие величин, характеризующих уровень АД, в течение часа были существенны и статистически достоверны. Выраженность и длительность повышения АД зависели главным образом от возрастания ОПСС и в меньшей степени (на 2-й мин действия препарата) от возрастания МОК (табл. 2).
Уже на 2-й мин после введения диэтилфосфата S-этилизотиурония ОПСС составляло 135% по отношению к исходному уровню и сохранялось высоким на протяжении всего периода наблюдения. На 60-й минуте оно превосходило исходную величину на 58%. Следовательно, суммарный тонус сосудистого сопротивления после введения препарата возрастал (табл. 2). МОК на 2-й мин после введения препарата увеличился на 7%, а на 15-й и 30-й мин уменьшился на 11 и 22% соответственно. Такие изменения МОК определялись характером изменения под влиянием препарата - ЦОК, величиной венозного возврата крови к сердцу и как следствие этого СО сердца. Возрастание Алж было преходящим, так на 2-й и на 15-й мин после инъекции вещества оно превосходило исходную величину на 89% и 22%, а на 30-й мин возвратилось к исходному уровню. Полученные результаты свидетельствуют о том, что гипертензивный эффект, возникающий при однократном внутривенном введении диэтилфосфата S-этилизотиурония и сохраняющийся длительное время (до 1 часа), зависит главным образом от увеличения ОПСС и в меньшей степени (в основном в начальном периоде действия препарата) от возрастания МОК.
Известно, что адреномиметики практически не подавляют гипотензию, вызванную адреноблокаторами. Представляло интерес изучить влияние диэтилфосфата S-этилизотиурония при гипотензии, возникшей при введении известного α1-адреноблокатора - празозина (адверзутен). Адверзутен вводили однократно внутривенно в дозе 1 мг/кг. Результаты сведены в таблицу 3. На основании селективного места действия адверзутена существенно уменьшается периферическое сопротивление кровеносных сосудов, а следовательно, и уровень АД. После введения адверзутена уже на 5-й мин артериальное давление снижается на 51 мм рт. ст., на этом фоне введение диэтилфосфата S-этилизотиурония уже на 2-й мин увеличивает АД на 29 мм рт. ст. На 15-й и 30-й мин уровень АД был на 11,8 и 9,4% выше по сравнению с 5-й мин с момента введения адверзутена. Статистически достоверных изменений со стороны ЧСС и частоты дыхательных движений не наблюдали (за исключением 60-й мин с момента введения диэтилфосфата S-этилизотиурония, когда отмечалась брадикардия). На основании вышеизложенного можно сделать вывод о том, что диэтилфосфат S-этилизотиурония увеличивает АД и на фоне действия α1-адреноблокаторов, хотя и менее продолжительно, чем без их назначения.
В качестве экспериментальной модели геморрагического шока, близкой по своему течению к тяжелым клиническим формам, выбрана острая кровопотеря (3,2% массы тела животного), что составляет 45-47% от объема циркулирующей крови, в течение 3-5 мин. С целью выявления максимальной эффективности и продолжительности действия препарата основные параметры системного кровообращения определяли до кровопотери, через 30 мин после кровопускания, а также на 2, 10, 30 и 60 мин после внутривенного введения лекарственного средства. Результаты приведены в таблице 4.
В контрольной группе, состоящей из 8 фиксированных к станку животных, кровопотеря вызывала падение АД с 140,0±3,9 до 65,0±4,1 мм рт. ст., что составило 46% исходного уровня, ЧСС на 30-й мин от начала кровопотери увеличилась на 18%. МОК уменьшился со 102,8±4,5 до 44,0±5,2 мл/мин•кг, т.е. на 57% по сравнению с исходным.
Снижение АД на 30-й мин от начала острой кровопотери было обусловлено в основном за счет уменьшения МОК, который зависит, в свою очередь, от снижения ударного объема крови (до 36%) и центрального объема крови. Таким образом, постгеморрагическая гиповолемия приводит к снижению МОК, который не может быть компенсирован повышением ОПСС и учащением сердечных сокращений.
Расчеты Алж указывают на ее уменьшение в 6 раз.
На 2-й мин после введения изотонического раствора показатели системной гемодинамики мало чем отличались от тех же на 30-й мин от начала острой кровопотери, однако на 10-й и 30-й мин после введения 1 мл изотонического раствора натрия хлорида показатели системной гемодинамики прогрессивно ухудшались. Так, на 30 мин после инъекции раствора АД снижалось на 13% по сравнению с 30-ой мин от начала кровопускания. ЧОС уменьшилась на 7%, а МОК и СО уменьшились на 11 и 8% соответственно, Алж уменьшилась наполовину, а ОПСС увеличилось на 8%. Дальнейшее снижение МОК, обусловленное уменьшением производительности левого желудочка, приводило к гибели животных.
Однократное внутривенное введение диэтилфосфата S-этилизотиурония в дозе 5 мг/кг при геморрагическом шоке быстро и выраженно повышает АД. Так, уже на 2-й мин после инъекции лекарственного вещества АД увеличилось на 88% (по сравнению с 30-й мин с момента кровопотери) и этот эффект сохраняется в течение всего срока наблюдения. На 2-й мин после введения диэтилфосфата S-этилизотиурония отмечается достоверное урежение ЧСС, что можно объяснить как рефлекторное влияние на сердце в результате резкого повышения АД. Диэтилфосфат S-этилизотиурония оказывает двухфазное влияние на МОК. Первоначально МОК увеличивается на 19% с последующим его снижением на 30-й и 60-й мин после введения лекарственного средства. Следует, однако, отметить, что в контрольной группе с введением 1 мл изотонического раствора на 30-й и 60-й мин выявлено такое же снижение МОК. СО достоверно увеличился только на 2-й мин после инъекции препарата. Алж существенно увеличилась на 2-й и 10-й мин. ОПСС достоверно увеличено на протяжении всего времени наблюдения.
Анализируя изменение показателей системной гемодинамики под влиянием диэтилфосфата S-этилизотиурония, можно сделать вывод о том, что вещество увеличивает АД в начальном периоде за счет возрастания МОК и ОПСС, а в позднем за счет увеличения ОПСС.
Изучено влияние диэтилфосфата S-этилизотиурония на фоне артериальной гипотензии, вызванной известным ганглиоблокатором - гексонием. Гексоний вводили однократно внутривенно в дозе 10 мг/кг. Стимуляция седалищного и блуждающего нервов проводилась электроимпульсатором ЭМ-1 надпороговым прямоугольным импульсным током длительностью 1 м•сек, продолжительностью раздражения 10 сек и частотой 20 имп/сек (периферический отрезок блуждающего нерва) и 300 имп/сек (центральный конец седалищного нерва). Результаты приведены в таблице 5. Через 2 мин после введения гексония АД снизилось на 46%. Введение диэтилфосфата S-этилизотиурония уже на 2-ой мин повышает АД на 61 мм рт. ст., причем достоверное увеличение АД сохраняется в течение всего срока наблюдения. ЧСС изменялась в сторону брадикардии, однако эти изменения статистически недостоверны. Частота дыхательных движений не изменялась. Ганглиоблокирующие свойства при введении диэтилфосфата S-этилизотиурония полностью сохраняются, о чем свидетельствует отсутствие изменений уровня АД при повторных (на 2, 15, 30 и 60 мин) раздражениях периферического отрезка блуждающего и центрального конца седалищного нервов.
Можно сделать вывод, что диэтилфосфат S-этилизотиурония быстро восстанавливает уровень АД после гипотонии, вызванной ганглиоблокаторами, и поддерживает его на протяжении длительного времени.
Было изучено также влияние диэтилфосфата S-этилизотиурония в дозе 5 мг/кг на основные показатели кислотно-щелочного состояния (КЩС) и газового состава крови при геморрагическом шоке в опытах на кошках, наркотизированных внутрибрюшинным введением этаминала натрия (нембутала) в дозе 40 мг/кг. Кровопотерю вызывали кровопусканием из общей сонной артерии в количестве 3,2% массы животного, что приблизительно соответствует 45-47% объема циркулирующей крови. Кровопускание осуществляли в течение 3-5 мин. Показатели напряжения кислорода и углекислого газа в артериальной (РаО2, РаСО2) и смешанной венозной 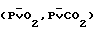 крови. рНа и рН исследовали микрометодом Аструпа. Содержание гемоглобина (Нв) определяли цианогемоглобиновым методом. Газовый состав крови и рН приведены в соответствии с температурой тела животного. Содержание бикарбонатных ионов [HCO3 -], показатели сдвига буферных оснований (BE) рассчитывали с помощью линейки Северинхауза. С целью упрощения расчеты проводили на ЭВМ модели GM-1403-02 по ранее составленной программе на языке Фортран. Показатели КЩС и газового состава крови исследовали в исходном состоянии, на 30-й мин с момента начала острой кровопотери, а также на 2-й, 10-й, 30-й и 60-й минутах после введения лекарственных веществ. Вещество вводили однократно внутривенно на 30-й мин с момента кровопускания.
крови. рНа и рН исследовали микрометодом Аструпа. Содержание гемоглобина (Нв) определяли цианогемоглобиновым методом. Газовый состав крови и рН приведены в соответствии с температурой тела животного. Содержание бикарбонатных ионов [HCO3 -], показатели сдвига буферных оснований (BE) рассчитывали с помощью линейки Северинхауза. С целью упрощения расчеты проводили на ЭВМ модели GM-1403-02 по ранее составленной программе на языке Фортран. Показатели КЩС и газового состава крови исследовали в исходном состоянии, на 30-й мин с момента начала острой кровопотери, а также на 2-й, 10-й, 30-й и 60-й минутах после введения лекарственных веществ. Вещество вводили однократно внутривенно на 30-й мин с момента кровопускания.
Контрольная группа (n=8). Кошкам вводили по 1 мл изотонического раствора натрия хлорида.
Результаты экспериментов показали, что у контрольных кошек с острой кровопотерей на 30-й мин после кровопускания изменения КЩС артериальной крови носили двоякий характер, у 5 из 7 кошек отмечался метаболический и дыхательный ацидоз, а у двух - метаболический ацидоз с компенсированным дыхательным алкалозом. рН артериальной крови уменьшился в среднем с 7,313±0,015 в исходном состоянии до 7,284±0,033 к 30-й мин от начала кровопотери. На 40-й и 60-й минутах после кровопускания отмечалось дальнейшее снижение рНа до 7,242±0,056 и 7,152±0,072 соответственно. Более выраженное снижение рН наблюдалось со стороны венозной крови. Так, у 7 кошек из 8 к 30-й мин после кровопотери рН снижался, а у одной не претерпевал существенных изменений. 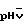 достоверно уменьшался с 7,284±0,011 в исходном состоянии до 7,184±0,028, 7,127±0,049 и 7,081±0,049 соответственно на 30-й, 40-й и 60-й минутах после кровопускания (p<0,05).
достоверно уменьшался с 7,284±0,011 в исходном состоянии до 7,184±0,028, 7,127±0,049 и 7,081±0,049 соответственно на 30-й, 40-й и 60-й минутах после кровопускания (p<0,05).
После острой кровопотери метаболические показатели КЩС артериальной и венозной крови на весь период наблюдения достоверно уменьшались. Содержание бикарбонатных ионов в артериальной крови на 30-й, 40-й и 60-й минутах после кровопотери снизилось соответственно на 25%, 27% и 40% по сравнению с исходными данными (Р<0,01). Параллельно с этим было обнаружено и достоверное уменьшение BE а с - 6,97±0,70 ммоль/л в исходном состоянии до - 10,61±0,86 ммоль/л на 30-й мин после кровопотери (Р<0,01). В дальнейшем к 30-й и 60-й минутам от начала кровопускания данный показатель уменьшился соответственно на 87,7% и 143%. Аналогичные изменения [НСО3 -] и [BE] выявлены со стороны венозной крови. Так, на 30-й мин после кровопотери содержание бикарбонатных ионов [НСО3 -] было на 14,6% ниже контрольного.
Дефицит буферных оснований достоверно возрастал к 30-й, 40-й и 60-й минутам после острой кровопотери соответственно на 55%, 99% и 130% по сравнению с исходным (Р<0,01). Таким образом, на ранних этапах после массивной острой кровопотери по нашим результатам наиболее частой формой нарушения КЩС является метаболический ацидоз. Это соответствует и данным литературы.
На 30-й мин после острой кровопотери отмечалось снижение PaCO2 и некоторое увеличение 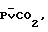 что приводило к увеличению артериовенозного градиента РCО2 в сравнении с исходным уровнем. Вполне понятно, что наблюдаемое в динамике острой кровопотери уменьшение градиента существенно ухудшало условия газообмена в легких и тканях и приводило к резкому нарастанию метаболического и респираторного ацидоза. Степень оксигенации артериальной крови в контрольной группе достаточно высока, тогда как РО2 венозной крови при этом достоверно снижалось.
что приводило к увеличению артериовенозного градиента РCО2 в сравнении с исходным уровнем. Вполне понятно, что наблюдаемое в динамике острой кровопотери уменьшение градиента существенно ухудшало условия газообмена в легких и тканях и приводило к резкому нарастанию метаболического и респираторного ацидоза. Степень оксигенации артериальной крови в контрольной группе достаточно высока, тогда как РО2 венозной крови при этом достоверно снижалось.
Группа с введением диэтилфосфата S-этилизотиурония (n=6). Препарат вводили в дозе 5 мг/кг.
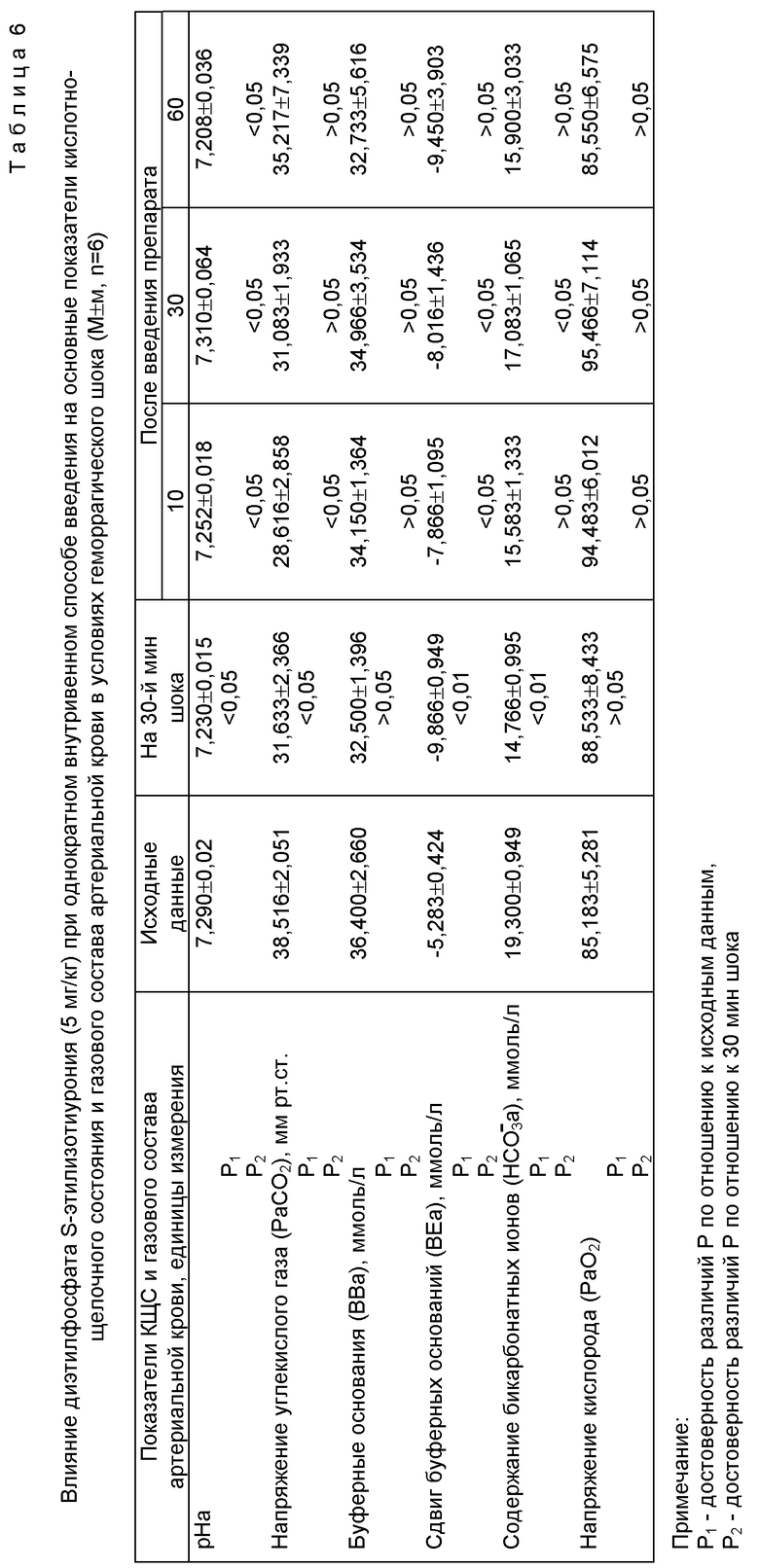
Из таблицы 6 следует, что диэтилфосфат S-этилизотиурония у кошек с геморрагическим шоком корригирует метаболический ацидоз, вызванный кровопотерей, увеличивая при этом рН артериальной крови с 7,230±0,015 на 30-й мин с момента кровопускания до 7,252±0,018 и 7,310±0,064 соответственно на 10-й и 30-й минутах после инъекции диэтилфосфата S-этилизотиурония.
Аналогично изменениям рН отмечались и изменения дефицита буферных оснований, который на 10-й и 30-й минутах после введения лекарственного вещества достоверно уменьшился соответственно на 20% и 18% по сравнению с величинами, наблюдаемыми на 30-й мин шока (табл. 6). В среднем содержание бикарбонатных ионов артериальной крови на 10-й и 30-й мин после введения диэтилфосфата S-этилизотиурония увеличивалось соответственно на 5% и 16% по сравнению с исходными величинами (табл. 6).
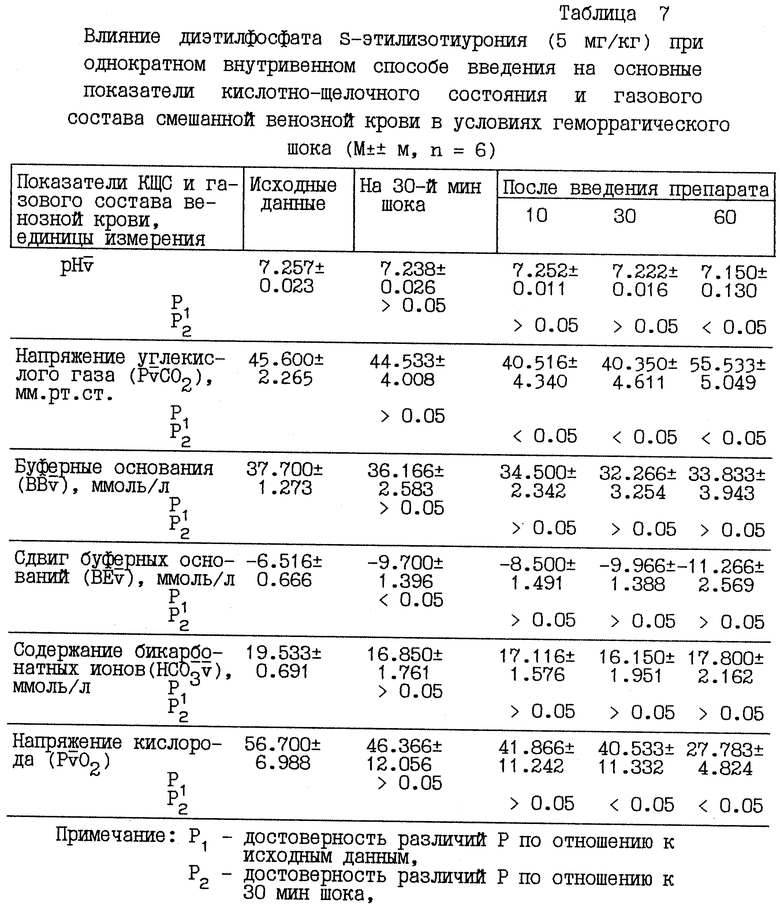
Такие же изменения наблюдались и со стороны основных показателей кислотно-щелочного состояния смешанной венозной крови, однако эти изменения оказались статистически недостоверными.
Парциальное напряжение углекислого газа артериальной и венозной крови по сравнению с 30-й мин после кровопускания уменьшилось на 10-й и 30-й минутах после инъекции диэтилфосфата S-этилизотиурония. Так, на 10-й мин оно снизилось на 9% (табл. 6, табл. 7). Парциональное давление кислорода в артериальной и венозной крови под действием диэтилфосфата S-этилизотиурония изменялось по-разному: в артериальной крови оно имело тенденции к увеличению, а в венозной к снижению, однако эти вариации оказались статистически недостоверными.
Анализируя данные о влиянии этирона и диэтилфосфата S-этилизотиурония на кислотно-щелочной баланс и газовый состав крови в условиях геморрагического шока, можно сделать вывод, что диэтилфосфат S-этилизотиурония эффективнее корригирует метаболический ацидоз, влияя, по-видимому, не только на увеличение содержания бикарбонат ионов, но и путем нарастания фосфатного буфера, так как молекула диэтилфосфата S-этилизотиурония, по сравнению с этироном, содержит диэтилфосфат.
Можно предположить также, что диэтилфосфат S-этилизотиурония влияет на показатели КЩС крови путем освобождения организма от конечных продуктов метаболизма: в частности, от молочной кислоты за счет более активного включения ее в циклы Кори и Кребса, поддерживая при этом сопряженность окисления и фосфорилирования.
В следующем цикле опытов изучали влияние диэтилфосфата S-этилизотиурония на сердечно-сосудистую систему собак. АД измеряли двумя способами: регистрировали на хвостовой артерии с помощью пьезодатчика на приборе для измерения давления фирмы Ugo Bazile или в бедренной артерии с помощью катетера, предварительно заполненного гепарином. Электрокардиограмма регистрировалась в трех стандартных отведениях на мингографе-82.
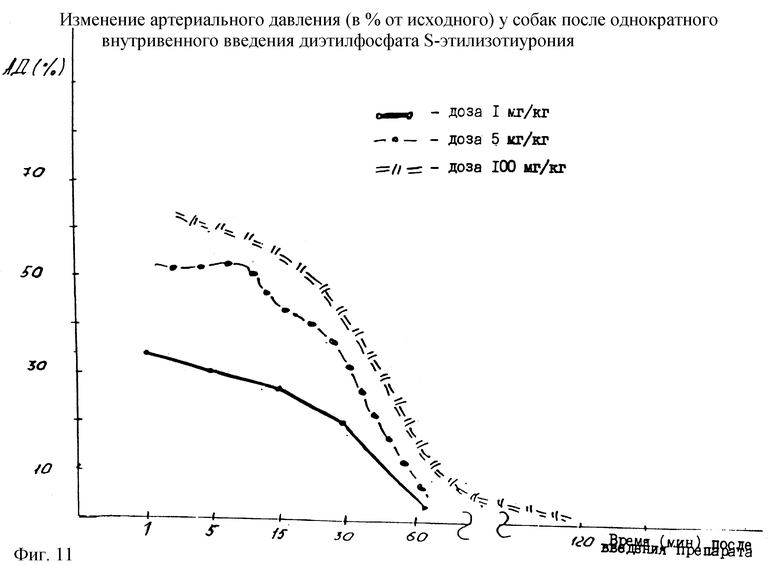
На фиг. 11 представлены данные по подбору оптимальной дозы препарата при внутривенном способе введения. Диэтилфосфат S-этилизотиурония вводили в дозах 1 мг/кг (n=5), 5 мг/кг (n=18) и 100 мг/кг (n=8). Как видно из чертежа, диэтилфосфат S-этилизотиурония во всех примененных дозах оказывает выраженную гипертензивную реакцию. Оптимальной дозой является по-видимому доза 5-10 мг/кг. На электрокардиограмме при исследовании всех вышеназванных доз препарата никаких патологических изменений не выявлено. Отмечается только развитие брадикардической реакции, которая развивается уже с первых минут после введения, достигая в среднем 25-30% от исходного уровня. Максимальная величина этой реакции наблюдается на 30-40 мин после начала опыта и сохраняется до 60-й мин наблюдения.
Следует особо отметить тот факт, что степень выраженности гипертензивной реакции у собак с низким уровнем артериального давления (гипотоников) значительно выше, чем у собак с высоким исходным уровнем артериального давления (гипертоников). По этой причине дальнейшее изучение велось раздельно для нормотоников и гипотоников.
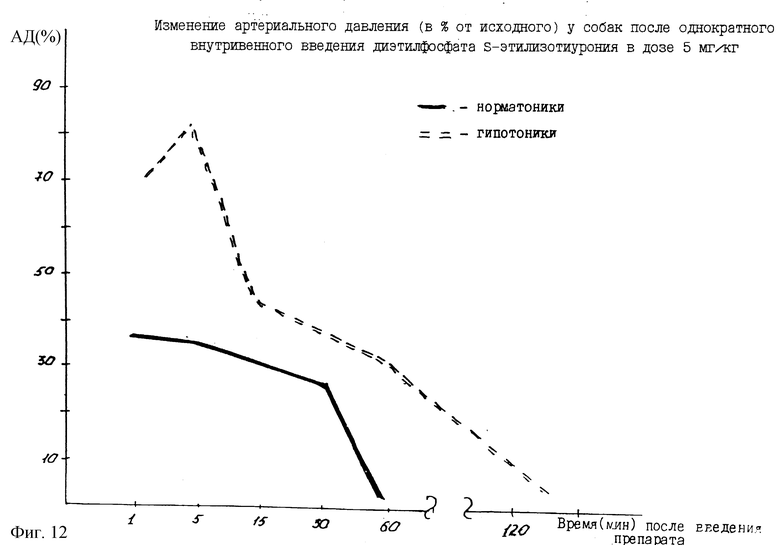
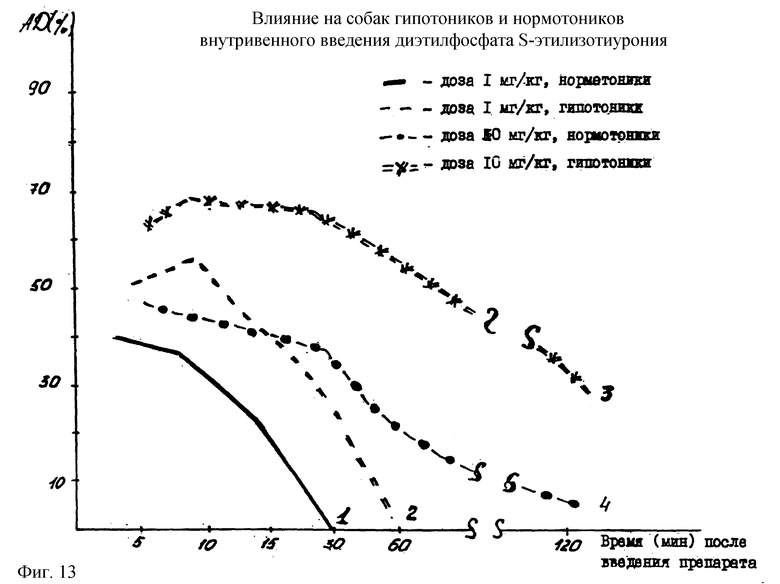
На фиг. 12 и 13 приведены показатели АД при введении различных доз диэтилфосфата S-этилизотиурония. Как видно из чертежей, подтверждено, что гипертензивная реакция у собак с низким уровнем артериального давления сильнее и продолжительнее, а оптимальная доза диэтилфосфата S-этилизотиурония при внутривенном способе введения составляет 5-10 мг/кг.
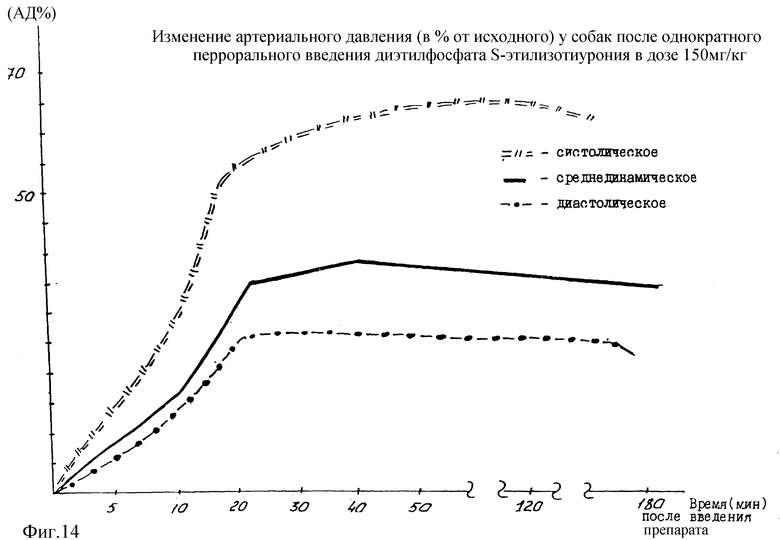
На фиг. 14 приведены показатели АД в опытах на собаках при пероральном способе введения диэтилфосфата S-этилизотиурония. Показано, что в этом случае количественый эффект повышения АД сохраняется, а время действия препарата существенно увеличивается.
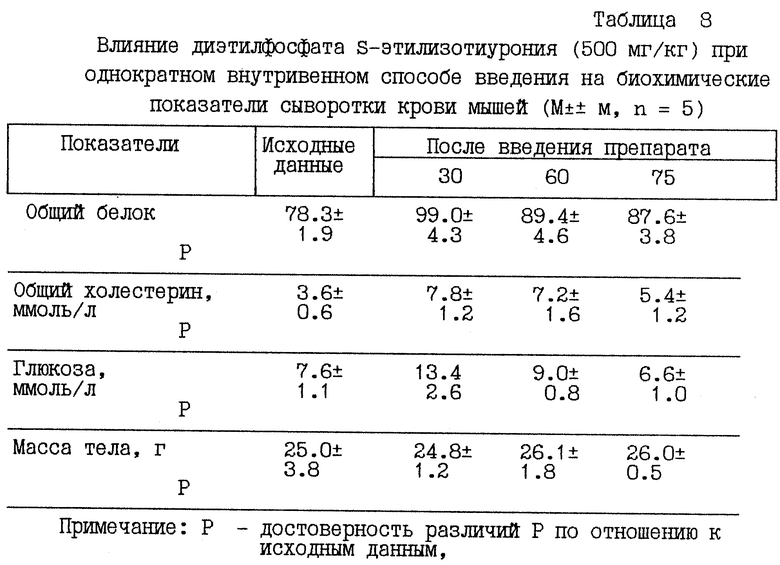
В опытах на мышах линии F1 (C57BlxCBA) было оценено функциональное состояние организма по биохимическим тестам при введении диэтилфосфата S-этилизотиурония при внутривенном способе введения в дозе 500 мг/кг однократно и в дозе 100 мг/кг в хроническом эксперименте в течение 30 дней подряд. В остром эксперименте кровь брали через 30, 60 и 75 мин после введения препарата. В хроническом эксперименте кровь исследовали ежедневно через 1 час после введения препарата. Сроки исследования 1, 7, 14 и 21 сутки после введения препарата. Оценивали состояние белкового, липидного и углеводного обмена, для чего определяли концентрацию общего белка, общего холестерина и глюкозы в сыворотке крови мышей по общепринятым методикам. Общий белок определяли биуретовым методом, общий холестерин - по методу Ильке, глюкозу - оксидазным методом.
Кровь у мышей получали после быстрой декаптации, исследуемый материал отобран в одно и то же время суток в один и тот же сезон года.
Кровь для получения сыворотки собирали в центрифужные пробирки, ставили в термостат на 30-40 мин, образовавшийся сгусток обводили иглой, затем помещали в холодильник на 1 час при температуре +4oС, после охлаждения центрифугировали при 3000 об/мин в течение 10-15 мин. Полученную сыворотку без признаков гемолиза отбирали в чистую пробирку. Все количественные показатели биохимических характеристик крови были получены с помощью спектрофотометра СФ-26. Предварительно были построены калибровочные кривые для определения общего белка и общего холестерина. Полученные данные сведены в таблицы 8 и 9.
В результате изучения выяснено, что после введения диэтилфосфата S-этилизотиурония в дозе 500 мг/кг наблюдаются достоверные повышения концентрации общего белка, холестерина и глюкозы через 30 мин, которые в дальнейшем имеют тенденцию к нормализации.
В связи с тем что печень включается во все биохимические процессы, происходящие в организме, и является местом образования белковых компонентов крови, можно предположить, что диэтилфосфат S-этилизотиурония в дозе 500 мг/кг оказывает влияние на функциональное состояние печени. Повышенный уровень общего белка возможно связан с нарушением регуляторных процессов синтеза белка крови печенью, а также с повреждением паренхимы.
Таким образом, можно сделать следующий вывод, что введение диэтилфосфата S-этилизотиурония в дозе 500 мг/кг приводит к изменению показателей белкового, липидного и углеводного обмена, что очевидно связано с недостаточностью компенсаторных возможностей печени и снижением функциональных способностей. Эти изменения выходят за пределы физиологических приспособительных реакций и приводят к изменениям, лежащим на грани патологии, однако указанные изменения не сопровождаются длительными изменениями функционального состояния, изменения носят обратимый характер.
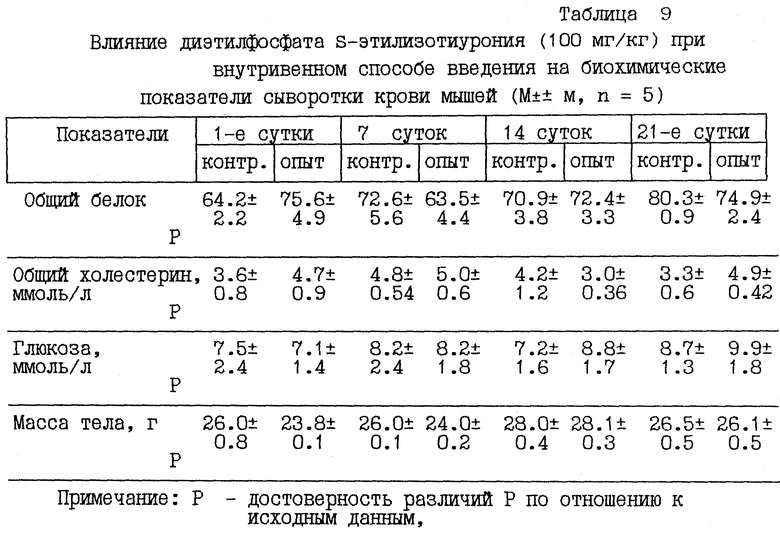
В условиях хронического эксперимента показано, что в дозе 100 мг/кг диэтилфосфата S-этилизотиурония колебания изученных параметров не выходят за пределы физиологических колебаний и не вызывают наблюдаемых изменений со стороны биохимических показателей.
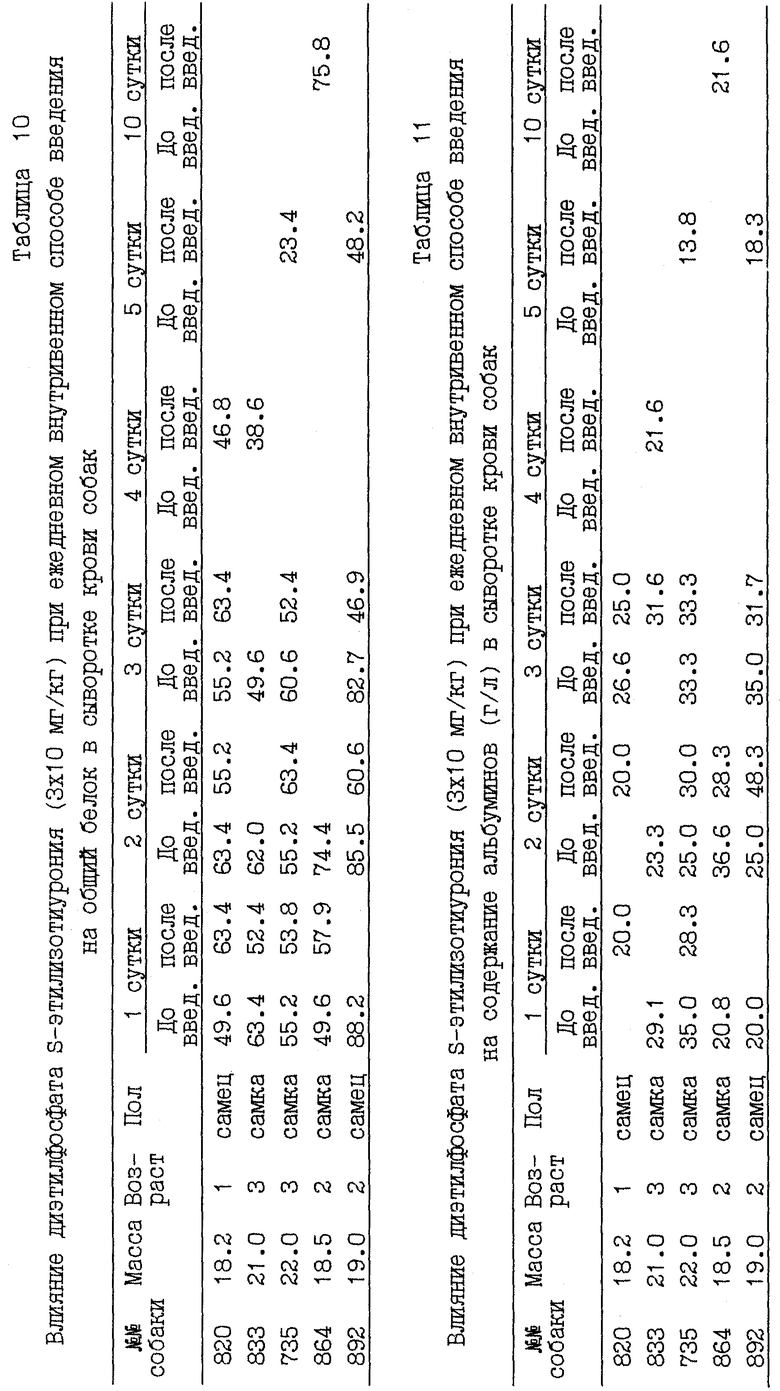
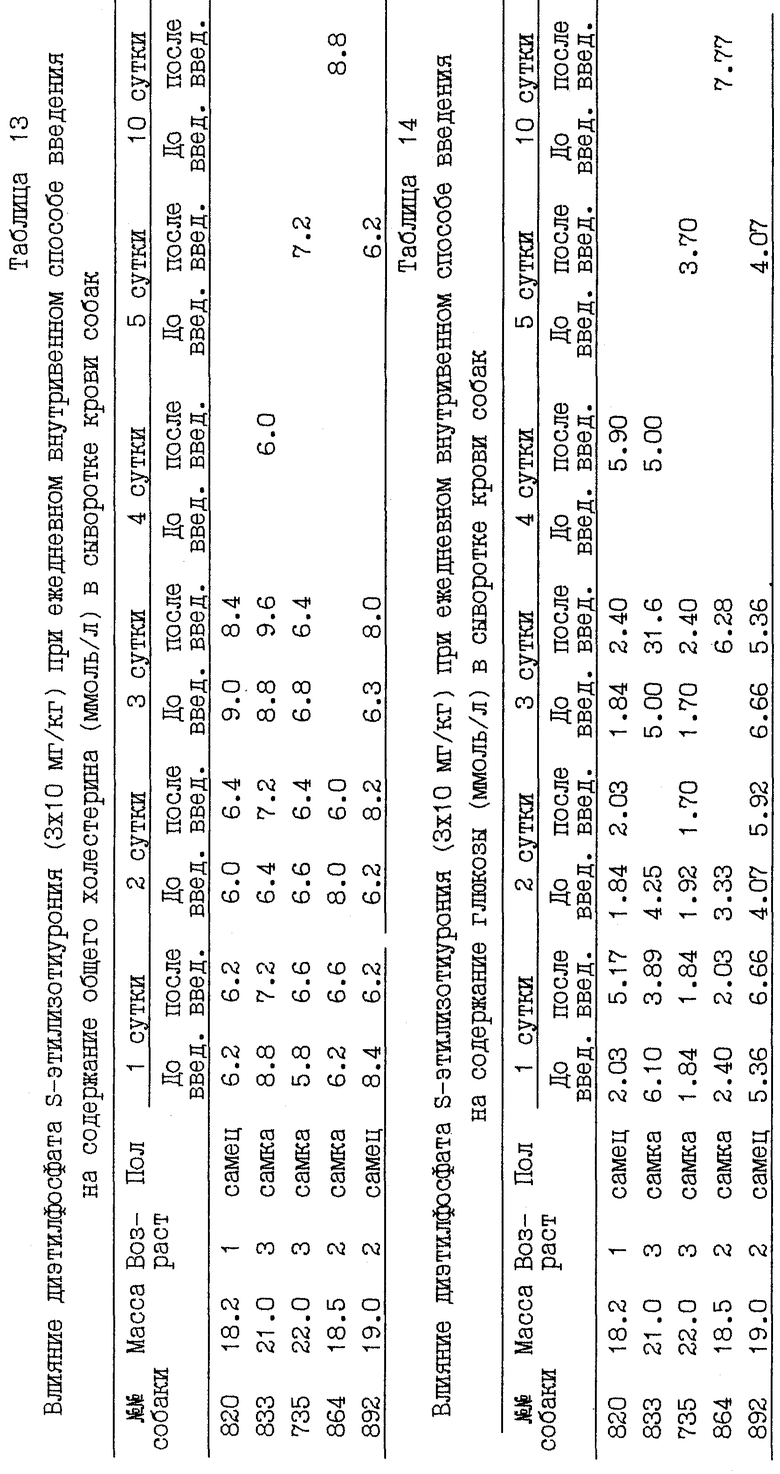
В опытах на собаках было оценено функциональное состояние организма по биохимическим тестам при введении диэтилфосфата S-этилизотиурония в виде 10% раствора для инъекций внутривенно в дозе 10 мг/кг ежедневно в одно и тоже время суток в течение 3 дней подряд. Кровь исследовали ежедневно через 1 час после введения препарата на протяжении 3 суток и после введения на 4, 5 и 10 сутки. Оценивали состояние белкового, липидного и углеводного обмена, для чего определяли концентрацию общего белка, альбуминов, глобулинов, общего холестерина и глюкозы в сыворотке крови собак по общепринятым методикам. Общий белок определяли биуретовым методом, общий холестерин - по методу Ильке, глюкозу - оксидазным методом. Результаты сведены в таблицы 10-14.
Уровень общего белка после введения препарата имел волнообразные колебания с тенденцией к понижению на 4-е и 5-е сутки, также волнообразно изменялся уровень альбуминов и глобулинов, уровень общего холестерина и глюкозы имел незначительные колебания, не выходящие за пределы колебаний, свойственных для здоровых собак.
Таким образом, на основании изучения общетоксического действия и биохимических показателей при ежедневном трехдневном эксперименте по внутривенному введению препарата в дозе 10 мг/кг в виде 10% раствора можно сделать вывод о том, что препарат, кроме специфического антигипо-тензивного эффекта, не оказывает существенного влияния на состояние здоровья собак, не выявлено признаков интоксикации или каких-либо существенных отклонений изученных показателей по сравнению с исходными данными, не отмечена индивидуальная чувствительность животных на внутривенное введение препарата.
В результате проведенного патоморфологического изучения внутренних органов экспериментальных животных (мыши, собаки), подвергавшихся однократным и повторным воздействиям диэтилфосфата S-этилизотиурония в среднесмертельных и сублетальных дозах, установлено, что данный препарат в условиях проведенных опытов вызывает в ранние сроки наблюдения умеренно выраженные признаки расстройства гемодинамики в виде расширения просветов и полнокровие преимущественно мелких и средних сосудов артериального и венозного русла в основном в печени, миокарде, легких, селезенке и, в меньшей мере, в почках. Расстройство кровообращения носит обратимый характер и, как правило, нормализуется через 7-10 суток после прекращения курса воздействия препарата. Каких-либо выраженных воспалительных, дистрофических или некробиотических изменений со стороны внутренних органов во всех экспериментах не наблюдалось. В ряде случаев отмечены признаки компенсаторно-приспособительных реакций со стороны печени (пролиферация клеток Купфера, гиперхромия цитоплазмы и ядер гепатоцитов).
| название | год | авторы | номер документа |
|---|---|---|---|
| ЛЕКАРСТВЕННОЕ ПРОТИВОШОКОВОЕ СРЕДСТВО | 1996 |
|
RU2142796C1 |
| СПОСОБ ЛЕЧЕНИЯ ШОКА | 1989 |
|
RU2012333C1 |
| КАРДИОТОНИЧЕСКОЕ И ГИПЕРТЕНЗИВНОЕ СРЕДСТВО, ДЛИТЕЛЬНО ПОВЫШАЮЩЕЕ ДАВЛЕНИЕ, И ЛЕКАРСТВЕННЫЕ ФОРМЫ НА ЕГО ОСНОВЕ | 1999 |
|
RU2181286C2 |
| АНТИГИПОТЕНЗИВНОЕ СРЕДСТВО | 2007 |
|
RU2338538C1 |
| ЩЕЛОЧНЫЕ СОЛИ АМИДОВ ОРОТОВОЙ КИСЛОТЫ И АМИНОКИСЛОТ, ОБЛАДАЮЩИЕ ГИПЕРТЕНЗИВНЫМ ЭФФЕКТОМ | 1995 |
|
RU2086543C1 |
| АНТИГИПОТЕНЗИВНОЕ СРЕДСТВО | 2007 |
|
RU2353614C1 |
| АНТИГИПОТОНИЧЕСКОЕ СРЕДСТВО | 2011 |
|
RU2506082C2 |
| СОПОЛИМЕР L-ЛИЗИНА С L-ГЛУТАМИНОВОЙ КИСЛОТОЙ, СОДЕРЖАЩИЙ ДОФАМИНОВЫЕ БОКОВЫЕ ГРУППЫ, ОБЛАДАЮЩИЙ ПРОЛОНГИРОВАННОЙ ГИПОТЕНЗИВНОЙ АКТИВНОСТЬЮ И КОМПЕНСАТОРНЫМ ЭФФЕКТОМ ПРИ ГЕМОРРАГИЧЕСКОМ ШОКЕ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1986 |
|
SU1469826A1 |
| СПОСОБ ПРЕДУПРЕЖДЕНИЯ НЕБЛАГОПРИЯТНЫХ ГЕМОДИНАМИЧЕСКИХ ЭФФЕКТОВ КАРБОДИОКСИПЕРИТОНЕУМА ПРИ ЛАПАРОСКОПИЧЕСКИХ ХОЛЕЦИСТЭКТОМИЯХ | 2002 |
|
RU2249452C2 |
| СПОСОБ СНИЖЕНИЯ НЕЖЕЛАТЕЛЬНЫХ ПОБОЧНЫХ ЭФФЕКТОВ ПРЕПАРАТА Б-190 | 2013 |
|
RU2575576C2 |





Изобретение может быть использовано в фармации и медицине для производства препаратов, влияющих на артериальное давление. Заявлено средство, содержащее в качестве действующего вещества S-алкилизотиуроний формулы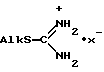
где Alk - разветвленный или неразветвленный С1-С4-алкил, а x- - анион фосфорсодержащей кислоты. Изобретение расширяет ассортимент средств гипертензивного действия. Новое средство лишено нежелательных побочных эффектов, присущих адреномиметикам, проявляющим то же действие. 2 з.п. ф-лы, 14 табл., 14 ил.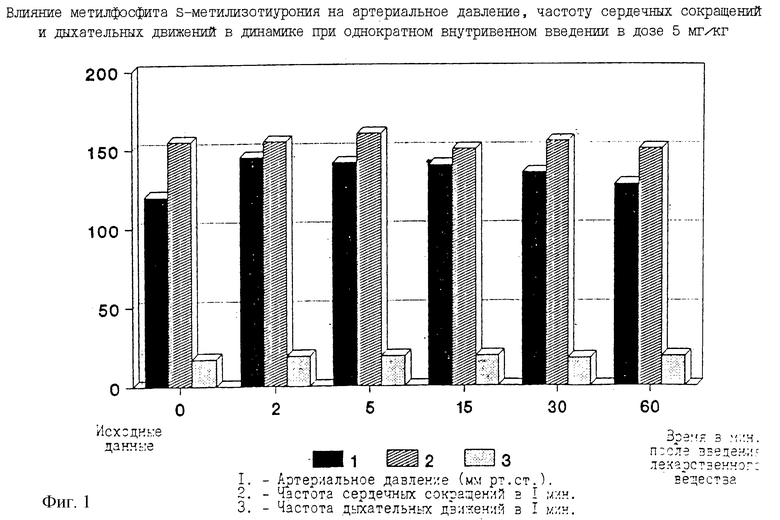
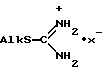
где Alk - разветвленный или неразветвленный С1-С4 - алкил;
x- - анион фосфорсодержащей кислоты.
| СПОСОБ ЛЕЧЕНИЯ ШОКА | 1989 |
|
RU2012333C1 |
| ЛЕКАРСТВЕННОЕ ПРОТИВОШОКОВОЕ СРЕДСТВО | 1996 |
|
RU2142796C1 |
| СПОСОБ ЛЕЧЕНИЯ ОЖОГОВОГО ШОКА | 1992 |
|
RU2039555C1 |
| US 4216230 А, 05.08.1980. | |||
Авторы
Даты
2002-08-20—Публикация
1997-09-19—Подача