Изобретение относится к химии полимеров и медицине, а именно к сополимеру L-лизина с L-глутаминовой кислотой, содержащему дофаминовые боковые группы, и способу его получения.
Целью изобретения является создание сополимера L-лизина с L-глутаминовой кислотой, обладающего гипотензивной прологированной активностью и компенсаторным эффектом при геморрагическом шоке.
П р и м е р 1. Синтез трет-бутилоксикарбонилдофамина (БОК-дофамина) и карбоната БОК-дофамина проводят по схемам:
A. HCl·NH2-(CH2) OH+(C2H5)3N+
OH+(C2H5)3N+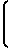
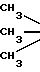 C-O-
C-O-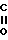
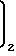 O ___→
O ___→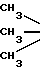 C-O-
C-O-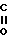 -NH-(CH2)
-NH-(CH2)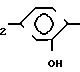 OH
OH
Б. 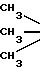 C-O-
C-O-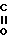 -NH-(CH2)
-NH-(CH2)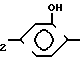 OH+(C2H5)3N+COCl2___→
OH+(C2H5)3N+COCl2___→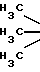 C-O-
C-O-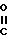 -NH-(CH2)
-NH-(CH2)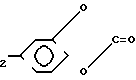
А. Синтез БОК-дофамина.
1,89 г (0,01 моль) хлоргидрата дофамина растворяют в 30 мл изопропанола в токе N2. К раствору добавляют 2,8 мл (0,02 моль) триэтиламина и раствор 2,5 г пирокарбоната в 5 мл изопропанола, а затем сразу еще 1,4 мл триэтиламина. Смесь перемешивают 2 ч при 20оС. Полноту протекания реакции контролируют методом тонкослойной хроматографии [пластинки Силуфол, система метанолхлороформ (8:2), проявление нингидрином]
После исчезновения пятна дофамина на хроматограмме из раствора отгоняют в вакууме легколетучие компоненты. Остаток растворяют в этилацетате и промывают 5%-ным водным раствором KHSO4 до тех пор, пока в растворе этилацетата не останется один продукт. Полноту отмывания контролируют методом ТСХ. Раствор сушат над MgSO4 и отгоняют растворитель.
Остаток кристаллизуют из смеси этилацетат-гексан (1:2). Выход перекристаллизованного трет-бутилоксикарбонилдофамина 2 г ( ≈ 79% от расчетного), т.пл. 137-138оС.
Найдено, C 61,35; 61,17; H 7,69; 7,88, N 5,42; 5,48.
C13H19O4N (БОК-дофамина).
Вычислено, C 61,64; H 7,56; N 5,53.
Б. Синтез карбоната БОК-дофамина.
1,40 г (0,0058 моль) БОК-дофамина растворяют в 30 мл сухого тетрагидрофурана. Раствор охлаждают до 0оС и одновременно добавляют раствор 0,6 г (0,006 моль) фосгена, растворенного в 1,4 г безводного бензола ( ≈ 30%-ный раствор), и 1,4 мл (0,01 моль) триэтиламина (d204=0,726 г/см3). Раствор при перемешивании оставляют на 12 ч. Током азота отдувают избыток фосгена.
На стеклянном фильтре отделяют осадок хлоргидрата триэтиламина. Из фильтрата в вакууме удаляют тетрагидрофуран. Сухой остаток перекристаллизовывают из гексана. Выход карбоната БОК-дофамина 1,10 г (≈ 62%), т.пл. 94-96оС.
Найдено, C 60,81; 60,54; H 6,43; 5,97; N 4,96; 4,88.
C14H17O5N.
Вычислено, С 60,20; H 6,13; N 5,01.
Продукт хроматографически однороден [ТСХ, пластинки Силуфол, система хлороформ-метанол (98: 2) или гексан этилацетат (3:8), проявление нингидрином]
Строение карбоната БОК-дофамина подтверждено ИК-спектроскопией: при переходе от БОК-дофамина к карбонату БОК-дофамина наблюдаются (значительные), изменения в области 2000-1800 см-1 и в области 3700-3500 см-1, которые могут быть объяснены замещением гидроксильных групп на карбонатную в бензольном кольце.
П р и м е р 2. Получение сополимера.
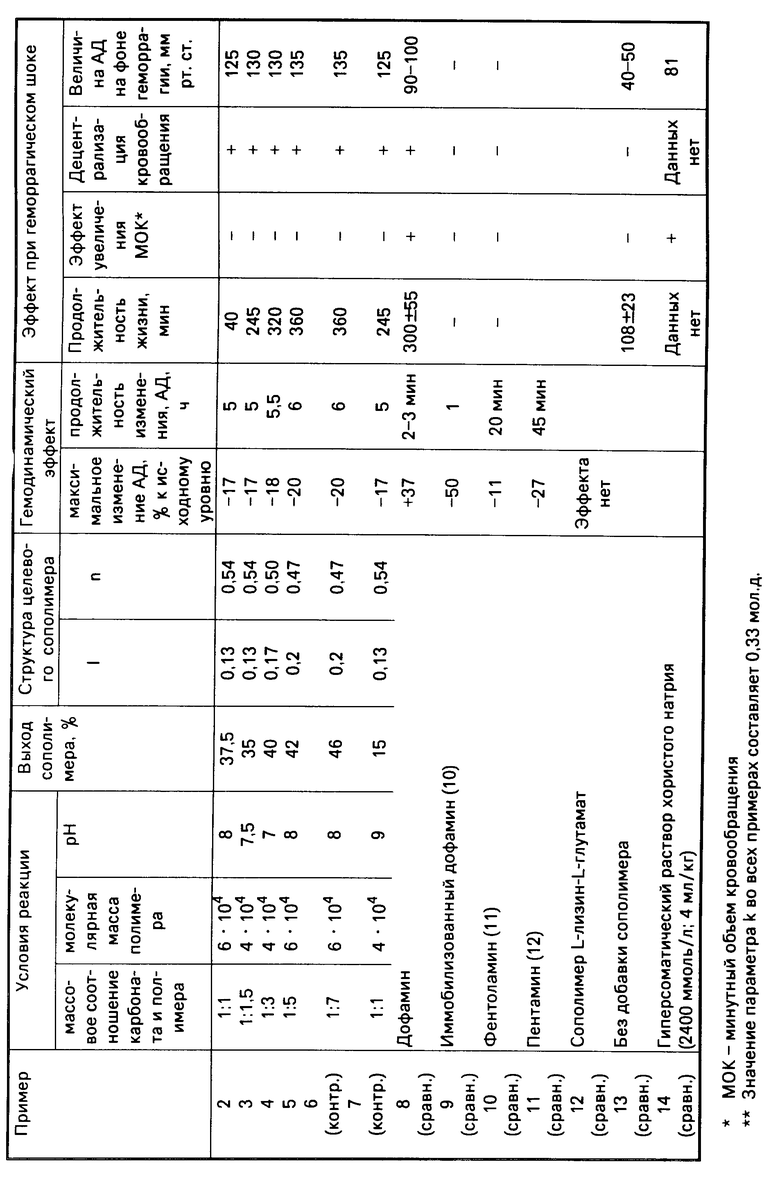
0,2 г сополимера L-лизина с L-глутаминовой кислотой с мол. м. 6 .104 растворяют в 10 мл 5%-ного водного раствора бикарбоната натрия. К этому раствору добавляют раствор 0,2 г карбоната БОК-дофамина в 5 мл диметилформамида. Смесь выдерживают при перемешивании 24 ч. Затем прикапывают концентрированную соляную кислоту до рН 1. Подкисление ведут в токе азота. Раствор выдерживают 5 ч в токе азота. За это время рН изменяется до 2,5. С помощью 20% -ного раствора NaOH рН доводят до 7,0, после чего раствор диализуют против воды до исчезновения ионов Cl- (по реакции с AgNO3) и лиофилизуют. Выход сополимерного продукта ≈ 0,1 г. С помощью гельхроматографии на сефадеке G-75 определяют молекулярную массу полученного сополимерного продукта, она равна 6 ˙ 104. Из спектров кругового дихроизма следует, что присоединилось 6,3 ˙ 10-4 моль дофамина на 1 г исходного сополимера, содержащего 0,33 мол.д. L-глутаминовой кислоты и 0,67 мол.д. L-лизина. Значения k, l и n в сополимере, полученном указанным путем, составляют 0,33; 0,13; 0,54. Данные по примерам 3-14, сравнительные данные и свойства описываемых сополимеров приведены в таблице.
Определение гемодинамического эффекта проводили на 5 наркотизированных (800 мг/кг уретана и 800 мг/кг оксибутирата натрия) кошках и 9 ненаркотизированных крысах. Опыты на кошках выполняют в условиях искусственной вентиляции легких. В яремную вену (для введения испытуемых веществ) и сонную артерию [для регистрации уровня артериального давления (АД) электроманометром] вводят полиэтиленовые катетеры. Крысам катетеры вживлялись в бедренную артерию и яремную вену за 1-2 сут до проведения хронических экспериментов.
Как в острых (на наркотизированных животных), так и в хронических экспериментах действие сополимера L-лизина с L-глутаминовой кислотой, содержащего дофаминовые боковые группы, оценивались по сравнению с эффектами аналогов по структуре и по эффекту.
Дофамин вводили в дозе 3-5 мг/кг. Через 1-2 с после введения фиксировали повышение уровня АД. При этом средний прирост АД составлял 37 ± 7% от исходного уровня. Гипертензивная фаза действия дофамина продолжалась 2-3 мин и сменялась снижением артериального давления. Во всех случаях к восьмой минуте наблюдения уровень АД стабилизировался на величинах, соответствующих исходным. Сополимер испытан на тех же группах животных, что и дофамин.
Предварительно в трех контрольных экспериментах исследовали эффект сополимера L-лизина с L-глутаминовой кислотой с мол.м. 4 ˙ 104-6 ˙ 104 в дозах 5,15 и 25 мг/кг, не содержащего дофамина. Влияния сополимера на уровень системного АД не обнаружено.
Описываемый сополимер с дофаминовыми боковыми группами вводили внутривенно в дозе 10-25 мг/кг (или 2-5 мг/кг в расчете на активное начало). Через 7-10 мин после введения соединения развивалось стойкое снижение уровня АД, не сопровождающееся изменениями частоты сердечных сокращений. Уровень АД оставался сниженным на протяжении нескольких часов (при дозе 10-25 мг/кг от 3 до 5-7 ч).
Данные таблицы показывают, что полимерное производное дофамина по величине гипотензивного эффекта находится на уровне, а по продолжительности значительно превышает действие типичных представителей гипотензивных соединений: α-адреноблокаторов (фентоламин) и ганглиоблокаторов (пептамин), чем достигнуто значительное увеличение продолжительности действия препарата.
Необходимость использования карбоната трет-бутилоксикарбонилдофамина определяется тем, что при таком способе присоединения (за гидроксильную группу) не затрагивается NH2-группа, необходимая для проявления биологических свойств.
Результаты контрольной группы животных показали типичные для тяжелого геморрагического шока нарушения гемодинамики. Системное АД после кровопотери устанавливалось и поддерживалось на критическом уровне. Наблюдалась сильная гипотензия, что являлось следствием прогрессирующего снижения МОК из-за уменьшения систолического объема сердца, достаточного для поддержания стабильных показателей гемодинамики. Компенсаторного увеличения общего периферического сосудистого сопротивления у животных контрольной группы не отмечалось. После кровопотери развивалась централизация кровообращения, которая ко второму часу увеличивалась на 50% Перераспределение уменьшенно МОК обеспечивалось за счет резкого ограничения кровотока в бассейне брюшной аорты. Наступавшая затем декомпенсация кровообращения при отсутствии фармакологической коррекции ограничивала продолжительность жизни животных на уровне 108 ± 23 мин (на 4 животных).
Во второй группе (14 животных) кошкам через 15 мин после кровопотери внутривенно непрерывно вводили дофамин. При этом достигалась стабилизация АД на уровне 90-100 мм рт.ст. преимущественно за счет увеличения производительности сердца. Начиная с третьего часа наблюдения отмечалась брадикардия, что обеспечивало длительное поддержание систолического объема на стабильном уровне вплоть до периода декомпенсации. В отличие от изменения регионарного кровотока в контрольной группе у этих животных на протяжении 5 ч доля кровотока в спланхическом ретоке относительно не изменялась, а в бассейне каудальной аорты снижалась до 33% от исходного значения. В последующем усиливалась централизация кровообращения, что свидетельствовало о срыве механизмов компенсации. Продолжительность жизни животных этой группы была в 4,3 раза больше, чем в контроле.
В третьей группе (5 животных) вводился заявленный сополимер L-лизина с L-глутаминовой кислотой, содержащий дофаминовые боковые группы.
Введение осуществляли в количестве 2,5 мг/кг однократно через 15 мин после стандартной кровопотери. Через 30-90 мин от момента введения сополимера отмечалось восстановление АД до уровня 125-135 мм рт.ст. (исходное АД до кровопотери составляло 145-160 мм рт.ст.).
Установившийся уровень АД поддерживался в течение 4-6 ч за счет возрастания общего периферического сосудистого сопротивления в 1,3-1,5 раза без увеличения МОК.
Если в ответ на кровопотерю наблюдалось преимущественное кровоснабжение органов и тканей головы и грудной клетки, то после введения сополимера заявленной структуры реакция централизации нивелировалась. Наблюдалось относительное увеличение (на 40-45%) кровотока в бассейне брюшной аорты. Оптимизация кровотока в спланхническом регионе сочеталась с ограничением МОК в бассейне каудальной аорты.
Период компенсации после однократного введения сополимера заявленной структуры в дозе 2,5 мг/кг составлял 4-6 ч. Таким образом, продолжительность жизни животных в сравнении с контролем увеличивалась в 2-3 раза. Более слабый эффект компенсации был достигнут при капельном введении дофамина в количестве 12 мкг/кг мин, таким образом, за 240-360 мин вводили в 1,8-2 раза большее количество активного начала, чем в случае введения заявленного сополимера.
Полученный результат позволяет заключить, что биотрансформация полимерного соединения дофамина в организме существенно отличается от дофамина-мономера.
| название | год | авторы | номер документа |
|---|---|---|---|
| СТАТИСТИЧЕСКИЕ СОПОЛИМЕРЫ В КАЧЕСТВЕ НИЗКОТОКСИЧНЫХ ВЕЩЕСТВ, ОБЛАДАЮЩИХ ПРОЛОНГИРОВАННЫМ ГИПОТЕНЗИВНЫМ ДЕЙСТВИЕМ, И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1989 |
|
SU1690368A1 |
| СРЕДСТВО, ВЛИЯЮЩЕЕ НА АРТЕРИАЛЬНОЕ ДАВЛЕНИЕ | 1997 |
|
RU2187309C2 |
| РАСТВОР ДЛЯ ИНФУЗИЙ | 2019 |
|
RU2708389C1 |
| АНТИГИПОТОНИЧЕСКОЕ СРЕДСТВО | 2011 |
|
RU2506082C2 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИИШЕМИЧЕСКОЙ, ГИПОТЕНЗИВНОЙ, ПРОТИВОАРИТМИЧЕСКОЙ И НООТРОПНОЙ АКТИВНОСТЬЮ | 2002 |
|
RU2216322C1 |
| ПОЛИФУНКЦИОНАЛЬНЫЙ КРОВЕЗАМЕНИТЕЛЬ ДЛЯ ЛЕЧЕНИЯ КРОВОПОТЕРИ И ШОКА | 1998 |
|
RU2136291C1 |
| ПЛАЗМОЗАМЕЩАЮЩИЙ РАСТВОР | 2014 |
|
RU2582219C2 |
| ФРАГМЕНТ ДНК ИЗ ESCHERICHIA COLI, ОПРЕДЕЛЯЮЩИЙ ПОВЫШЕННУЮ ПРОДУКЦИЮ L-АМИНОКИСЛОТ (ВАРИАНТЫ), И СПОСОБ ПОЛУЧЕНИЯ L-АМИНОКИСЛОТ | 1999 |
|
RU2175351C2 |
| СПОСОБ АНЕСТЕЗИОЛОГИЧЕСКОГО ПОСОБИЯ ПРИ ХИРУРГИЧЕСКОМ ЛЕЧЕНИИ СКОЛИОЗА | 2006 |
|
RU2305542C1 |
| ОДНО- И ДВУХВАЛЕНТНЫЕ СОЛИ N-(5-ГИДРОКСИНИКОТИНОИЛ)-L-ГЛУТАМИНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩИЕ ПСИХОТРОПНЫМ (АНТИДЕПРЕССИВНЫМ И АНКСИОЛИТИЧЕСКИМ), НЕЙРОПРОТЕКТОРНЫМ, ГЕРОПРОТЕКТОРНЫМ И ПРОТИВОИНСУЛЬТНЫМ ДЕЙСТВИЕМ | 2006 |
|
RU2314293C1 |
Изобретение относится к химии полимеров и может быть использовано в медицине. Изобретение позволяет создать полимерный физиологически активный препарат, обладающий пролонгированным гипотензивным действием и компенсаторным эффектом при геморрагическом шоке. Это достигается новой структурой вещества общей формулы 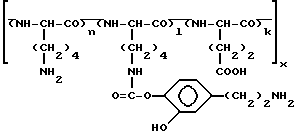 где l 0,13 20; n 0,47 0,54, к: (l + n) 0,33 0,67, с мол.м. 4·104-6·104, а также способом его получения путем обработки 1 мас.ч. сополимера L-лизина с L глутаминовой кислотой 1 5 мас.ч. карбоната трет-бутилоксикарбонильного производного дофамина формулы
где l 0,13 20; n 0,47 0,54, к: (l + n) 0,33 0,67, с мол.м. 4·104-6·104, а также способом его получения путем обработки 1 мас.ч. сополимера L-лизина с L глутаминовой кислотой 1 5 мас.ч. карбоната трет-бутилоксикарбонильного производного дофамина формулы 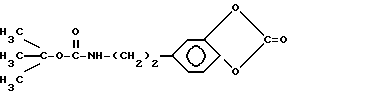 в водном растворе при pH 7 8. 2 с.п.ф-лы, 1 табл.
в водном растворе при pH 7 8. 2 с.п.ф-лы, 1 табл.
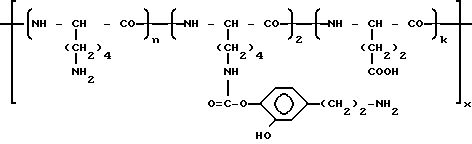
где h 0,47 0,54;
L 0,13 0,20;
k (l + n) 0,33 0,67,
с мол. мас. 4 · 104 6 · 104, обладающий пролонгированной гипотензивной активностью и компенсаторным эффектом при геморрагическом шоке.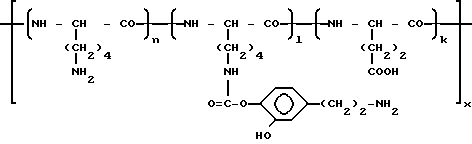
где n 0,47 0,54;
l 0,13 0,20;
k (l + n) 0,33 0,67,
заключающийся в обработке 1 мас. ч. сополимера 67 мол. L-лизина с 33 мол. L-глутаминовой кислоты в водном растворе при pH 7 8 1 5 мас. ч. карбоната трет-бутилоксикарбонильного производного дофамина формулы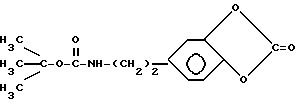
| Рожанская Н | |||
| И | |||
| и др | |||
| Фармакология кардиотропных средств | |||
| М., 1984, с.145. |
Авторы
Даты
1995-11-20—Публикация
1986-05-30—Подача