Изобретение относится к новому производному бензимидазола, обладающего антиаллергической активностью, и лекарственному средству, содержащему указанное производное бензимидазола в качестве активного ингредиента.
При лечении болезней, относящихся к аллергии типа I, таких как поллиноз, крапивница, атонический дерматит, аллергический ринит и астма, до сих пор часто использовали антигистамины и стероиды. Однако до сих пор остаются проблемы в отношении их клинической полезности. Вышеуказанные болезни, относящиеся к аллергии, побуждаются иммунной реакцией специфического антигена с антителами IgE и развиваются до хронического состояния через воспаление пораженной части или повреждение ткани. Предполагалось, что во время этого процесса различные химические медиаторы являются взаимно тесно связанными с патологическим прогрессом. На основании характеристик фармакологического действия считается, что среди них гистамин принимает участие в основном в начальной стадии патологического прогресса. Считается, что это является причиной того, почему остается проблема в отношении клинической полезности антигистаминов. С другой стороны, стероиды, которые используют в основном в серьезных случаях, проявляют фармакологическую активность в ингибировании различных процессов иммуно-воспалительных ответных реакций различным образом и, как считается, проявляют высокий уровень эффективности. Однако при использовании стероидов возникает проблема серьезных побочных действий и имеется много ограничений в их применении пероральным введением или повторным введением. Таким образом, в области лечения болезней, относящихся к аллергии типа I, очень желательна разработка лекарственного средства, имеющего новый механизм действия и высокий уровень эффективности.
В последние годы сообщалось, что вещество Р, которое представляет собой нейропептид, действует в качестве медиатора промотирования аллергических симптомов и принимает большое участие в воспалительных симптомах, особенно в хронической фазе (TIPS, 81, 24 (1987); Am. J. Respir. Crit. Care Med., 151, 613 (1995); J. Allergy Clin. Immunol., 92, 95 (1993)). Поэтому полагают, что антагонист вещества Р способен эффективно лечить аллергические симптомы в хронической фазе (особенно, хроническое воспаление).
Вещество Р является членом семейства нейрокининов и, известно, что оно принимает разнообразное участие в активации макрофагов или лимфоцитов и в иммунитете и воспалении в качестве фактора регуляции продуцирования цитокина (ИЛ1, ФНТ, ИЛ6) и оно вызывает симптомы воспаления, такие как повышение проницаемости сосудов, утечки плазмы и стимуляции секреторной железы. Кроме того, оно функционирует в качестве медиатора (передатчика) боли от периферии к центру и регулирует систему передачи допамина и адреналина в головном мозге.
В соответствии с этим полагают, что антагонист вещества Р эффективен не только в качестве антиаллергического агента, но также в качестве аналгетиков или психомиметиков.
Кроме того, полагают, что лекарственное средство, обладающее не только антагонистической активностью против вещества Р, но также антигистаминовой активностью, эффективно для лечения широкого ряда аллергических симптомов, простирающихся от острой фазы до хронической фазы, и, таким образом, ожидается, что оно является лекарственным средством, которое имеет клинически высокие результаты лечения.
В результате проведения экстенсивных исследований авторы данного изобретения обнаружили, что производные бензимидазола данного изобретения обладают антагонистической активностью против вещества Р и, кроме того, что среди соединений данного изобретения многие обладают также антигистаминовой активностью.
Бензимидазолы, обладающие антигистаминовой активностью, уже были описаны, например, в патентах Японии JP-A-59-199679, JP-A-58-79983, Европейских патентах ЕР-232937В, ЕР-144101В и патенте США 4219559. Однако соединения данного изобретения не включаются в число таких описанных бензимидазолов. Кроме того, в таких ссылках известного уровня техники ничего не говорится об антагонистической активности против вещества Р.
Таким образом, было обнаружено, что соединения данного изобретения являются превосходящими соединениями в качестве антиаллергических средств и они не только полезны в качестве активных ингредиентов для профилактических или лечебных средств для поллиноза, крапивницы, атопического дерматита, аллергического ринита и астмы/и так далее, но эффективны также против других, относящихся к веществу Р, болезней, например глазных болезней, таких как конъюнктивит и весенний катар глаз; воспалительных болезней, таких как хронический ревматоидный артрит; болей, таких как мигрень, головная боль, зубная боль и продолжительная тупая боль, сопровождающая различные болезни; желудочно-кишечных болезней, таких как неспецифический язвенный колит и болезнь Крона, и психических болезней, таких как депрессия и дистимия. Данное изобретение было выполнено на основе этих открытий.
Данное изобретение предлагает производное бензимидазола формулы (I) или его соль: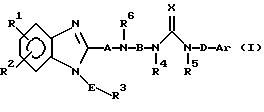
где А представляет одинарную связь или C1-2-алкиленовую группу (эта алкиленовая группа может быть необязательно замещена C1-4-алкильной группой), R6 представляет C1-4-алкильную группу (эта алкильная группа может быть необязательно замещена фенильной группой), В представляет С2-3-алкиленовую группу (эта алкиленовая группа может быть необязательно замещена C1-4-алкильной группой), Х представляет атом кислорода, атом серы или NR7 (где R7 представляет нитрогруппу, цианогруппу или С1-4-алкоксигруппу), каждый из R1 и R2, которые не зависят друг от друга, представляет атом водорода, атом галогена, C1-4-алкильную группу или C1-4-алкоксигруппу, Е представляет С1-2-алкиленовую группу (эта алкиленовая группа может быть необязательно замещена C1-4-алкильной группой), R3 представляет фенильную группу (эта фенильная группа может быть необязательно замещена атомом галогена, C1-4-алкильной группой или C1-4-алкоксигруппой), C1-4-алкоксигруппу или бензилоксигруппу, каждый из R4 и R5, которые не зависят друг от друга, представляет C1-4-алкильную группу (эта алкильная группа может быть необязательно замещена фенильной группой), D предоставляет C1-2-алкиленовую группу (эта алкиленовая группа может быть необязательно замещена C1-4-алкильной группой) и Ar представляет фенильную группу (эта фенильная группа может быть необязательно замещена атомом галогена, C1-4-алкильной группой, C1-4-алкоксигруппой или трифторметильной группой), способ его получения и фармацевтическая композиция, содержащая его в качестве активного ингредиента.
Теперь будут описаны заместители, относящиеся к соединению данного изобретения.
В этом описании "н" означает нормальный, "изо" означает изостроение, "втор" означает вторичный, "трет" означает третичный, "цикло" означает циклический, "Me" означает метил, "Et" означает этил, "Bu" означает бутил, "Ph" означает фенил и "Bn" означает бензил.
C1-2-алкиленовая группа включает метилен и этилен.
С2-3-алкиленовая группа включает этилен и триметилен.
C1-4-алкильная группа может быть линейной, разветвленной или циклической и включает метил, этил, н-пропил, изопропил, циклопропил, н-бутил, изобутил, втор-бутил, трет-бутил и циклобутил.
С1-4-алкоксигруппа может быть линейной, разветвленной или циклической и включает метокси, этокси, н-пропокси, изо-пропокси, циклопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси и циклобутокси.
Атом галогена включает фтор, хлор, бром и йод.
Теперь будут подробно описаны А, В, D, Е, Ar, X, R1, R2, R3, R4, R5 и R6 в соединении (I) данного изобретения.
Конкретные примеры А включают одинарную связь, СН2, СНМе, СН2СН2 и СН2СНМе, предпочтительно одинарную связь и CH2.
Конкретные примеры В включают СН2СН2, СН2СНМе, СНМеСН2, СНМеСНМе, СН2СН2СН2, СНМеСН2СН2, СН2СНМеСН2, СН2СН2СНМе, СНМеСНМеСН2, СНМеСН2СНМе, СН2СНМеСНМе и СНМеСНМеСНМе, предпочтительно СН2СН2 и СН2СН2СН2.
Конкретные примеры D включают СН2, СНМе, СН2СН2 и СН2СНМе, предпочтительно СН2, СНМе и СН2СН2.
Конкретные примеры Е включают СН2, СНМе, СН2СН2 и СН2СНМе, предпочтительно СН2 и СН2СН2.
Конкретные примеры Аr включают фенил, 2-фторфенил, 3-фторфенил, 4-фторфенил, 2-хлорфенил, 3-хлорфенил, 4-хлорфенил, 2-бромфенил, 3-бромфенил, 4-бромфенил, 2-иодфенил, 3-иодфенил, 4-иодфенил, 2-трифторметилфенил, 3-трифторметилфенил, 4-трифторметилфенил, 2-метилфенил, 3-метилфенил, 4-метилфенил, 2-метоксифенил, 3-метоксифенил, 4-метоксифенил, 2,3-дифторфенил, 2,4-дифторфенил, 2,5-дифторфенил, 2,6-дифторфенил, 3,4-дифторфенил, 3,5-дифторфенил, 2,3-дихлорфенил, 2,4-дихлорфенил, 2,5-дихлорфенил, 2,6-дихлорфенил, 3,4-дихлорфенил, 3,5-дихлорфенил, 2,3-дибромфенил, 2,4-дибромфенил, 2,5-дибромфенил, 2,6-дибромфенил, 3,4-дибромфенил, 3,6-дибромфенил, 2,3-дииодфенил, 2,4-дииодфенил, 2,5-дииодфенил, 2,6-дииодфенил, 3,4-дииодфенил, 3,5-дийодфенил, 2,3-бис(трифторметил)фенил, 2,4-бис(трифторметил)фенил, 2,5-бис(трифторметил)фенил, 2,6-бис(трифторметил)фенил, 3,4-бис-(трифторметил)фенил, 3,5-бис(трифторметил)фенил, 2,3-диметилфенил, 2,4-диметилфенил, 2,5-диметилфенил, 2,6-диметилфенил, 3,4-диметилфенил, 3,5-диметилфенил, 2,3-диметоксифенил, 2,4-диметоксифенил, 2,5-диметоксифенил, 2,6-диметоксифенил, 3,4-диметоксифенил, 3,5-диметоксифенил и 2-хлор-5-трифтор-метилфенил, предпочтительно фенил, 2-хлорфенил, 2-метокси-фенил, 3,5-диметилфенил, 3,5-бис(трифторметил)фенил, 3,5-диметоксифенил, 2, 5-дихлорфенил и 2-хлор-5-трифторметилфенил.
Конкретные примеры Х включают атом кислорода, атом серы, N-CN, N-NO2, N-OMe, N-OEt и N-OBu, предпочтительно атом кислорода.
Конкретные примеры каждого из R1 и R2 включают атом водорода, фтор, хлор, бром, йод, метил, этил, н-пропил, изопропил, циклопропил, н-бутил, изобутил, втор-бутил, трет-бутил, циклобутил, метокси, этокси, н-пропокси, изопропокси, циклопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси и циклобутокси, предпочтительно атом водорода.
Конкретные примеры R3 включают фенил, 4-фторфенил, 4-хлорфенил, метокси, этокси и бензилокси, предпочтительно 4-фторфенил и этокси.
Конкретные примеры каждого из R4 и R5 включают атом водорода, метил, этил, н-пропил, изопропил, циклопропил, н-бутил, изобутил, втор-бутил, трет-бутил, циклобутил и бензил, предпочтительно атом водорода, метил и бензил.
Конкретные примеры R6 включают атом водорода, метил, этил, н-пропил, изопропил, циклопропил, н-бутил, изобутил, втор-бутил, трет-бутил, циклобутил и бензил, предпочтительно атом водорода, метил и бензил.
Следующие соединения могут быть указаны в качестве предпочтительных соединений среди соединений формулы (I) данного изобретения.
(1) Соединение формулы (I) или его соль, где А представляет одинарную связь, СН2, СНМе, CH2H2 или СН2СНМе, В представляет CH2CH2, СН2СНМе, СНМеСН2, CHMeCHMe, CH2CH2CH2, СНМеСН2СН2, CH2CHMeCH2, СН2СН2СНМе, СНМеСНМеСН2,
СНМеСН2СНМе, СН2СНМеСНМе или CHMeCHMeCHMe, D представляет CH2, СНМе, СН2СН2 или СН2СНМе, Е представляет СН2, СНМе, СН2СН2 или СН2СНМе, Аr представляют фенил, 2-фторфенил, 3-фторфенил, 4-фторфенил, 2-хлорфенил, 3-хлорфенил, 4-хлорфенил, 2-бромфенил, 3-бромфенил, 4-бромфенил, 2-иодфенил, 3-иодфенил, 4-иодфенил, 2-трифторметилфенил, 3-трифторметилфенил, 4-трифторметилфенил, 2-метилфенил, 3-метилфенил, 4-метилфенил, 2-метоксифенил, 3-метоксифенил, 4-метоксифенил, 2,3-дифторфенил, 2,4-дифторфенил, 2,5-дифторфенил, 2,6-дифторфенил, 3,4-дифторфенил, 3,5-дифторфенил, 2,3-дихлорфенил, 2,4-дихлорфенил, 2,5-дихлорфенил, 2,6-дихлорфенил, 3,4-дихлорфенил, 3,5-дихлорфенил, 2,3-дибромфенил, 2,4-дибромфенил, 2,5-дибромфенил, 2,6-дибромфенил, 3,4-дибромфенил, 3,5-дибромфенил, 2,3-дииодфенил, 2,4-дииодфенил, 2,5-дииодфенил, 2,6-дииодфенил, 3,4-дииодфенил, 3,5-дииодфенил, 2,3-бис(трифторметил)фенил, 2,4-бис(трифторметил)фенил, 2,5-бис(трифторметил)фенил, 2,6-бис(трифторметил)фенил, 3,4-бис(трифторметил)фенил, 3,5-бис(трифторметил)фенил, 2,3-диметилфенил, 2,4-диметилфенил, 2,5-диметилфенил, 2,6-диметилфенил, 3,4-диметилфенил, 3,5-диметилфенил, 2,3-диметоксифенил, 2,4-диметоксифенил, 2,5-диметоксифенил, 2,6-диметоксифенил, 3,4-диметоксифенил, 3,5-диметоксифенил или 2-xлop-5-тpифтop-метилфенил, Х представляет атом кислорода, атом серы, N-CN, N-NO2, N-OMe, N-OEt или N-OBu, каждый из R1 и R2 представляет атом водорода, фтор, хлор, бром, йод, метил, этил, н-пропил, изопропил, циклопропил, н-бутил, изобутил, втор-бутил, трет-бутил, циклобутил, метокси, этокси, н-пропокси, изопропокси, циклопропокси, н-бутокси, изобутокси, втор-бутокси, трет-бутокси или циклобутокси, R3 представляет фенил, 4-фторфенил, 4-хлорфенил, метокси, этокси или бензилокси, каждый из R4 и R5 представляет атом водорода, метил, этил, н-пропил, изопропил, циклопропил, н-бутил, изобутил, втор-бутил, трет-бутил, циклобутил или бензил и R6 представляет атом водорода, метил, этил, н-пропил, изопропил, циклопропил, н-бутил, изобутил, втор-бутил, трет-бутил, циклобутил или бензил.
(2) Соединение или его соль по вышеуказанному пункту (1), где Х представляет атом кислорода.
(3) Соединение или его соль по выше указанному пункту (2), где каждый из R1 и R2 представляет атом водорода.
(4) Соединение формулы (I) или его соль, где А представляет одинарную связь или СН2, В представляет СН2СН2 или CH2CH2CH2, D представляет СН2, СНМе или CH2CH2, E представляет СН2 или СН2СН2, Аr представляет фенил, 2-хлорфенил, 2-метоксифенил, 3,5-диметилфенил, 3,5-бис(трифторметил)фенил, 3,5-диметоксифенил, 2,5-дихлорфенил или 2-хлор-5-трифторметилфенил, Х представляет атом кислорода, каждый из R1 и R2 представляет атом водорода, R3 представляет 4-фторфенил или этокси, каждый из R4 и R5 представляет атом водорода, метил или бензил и R6 представляет атом водорода, метил или бензил.
(5) Соединение или его соли по вышеуказанному пункту (4), где Е представляет CH2 и R3 представляет 4-фторфенильную группу.
(6) Соединение или его соль по вышеуказанному пункту (5), где Аr представляет 3,5-бис(трифторметил)фенил.
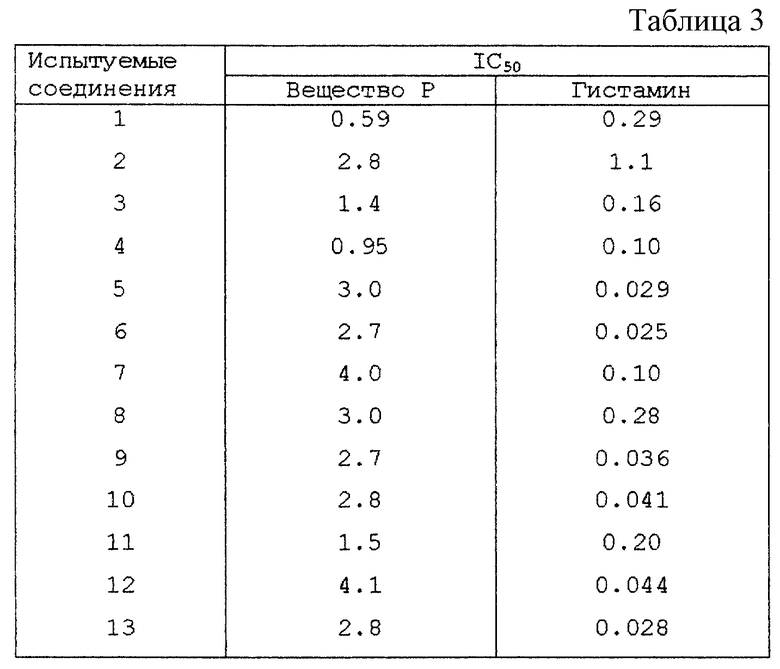
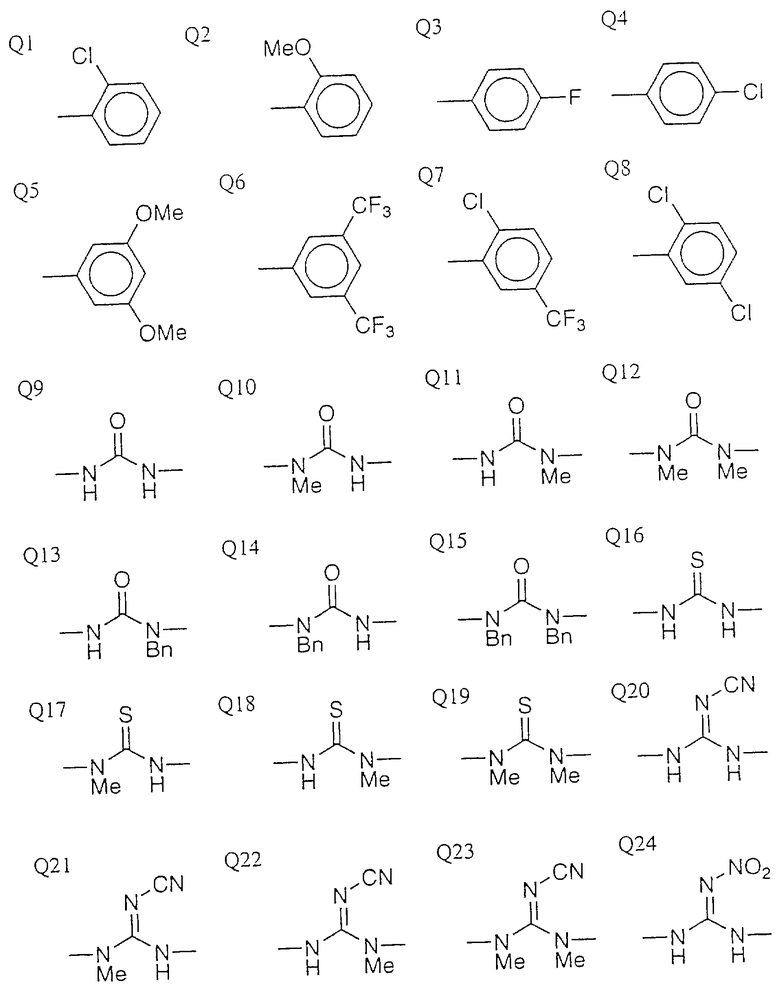
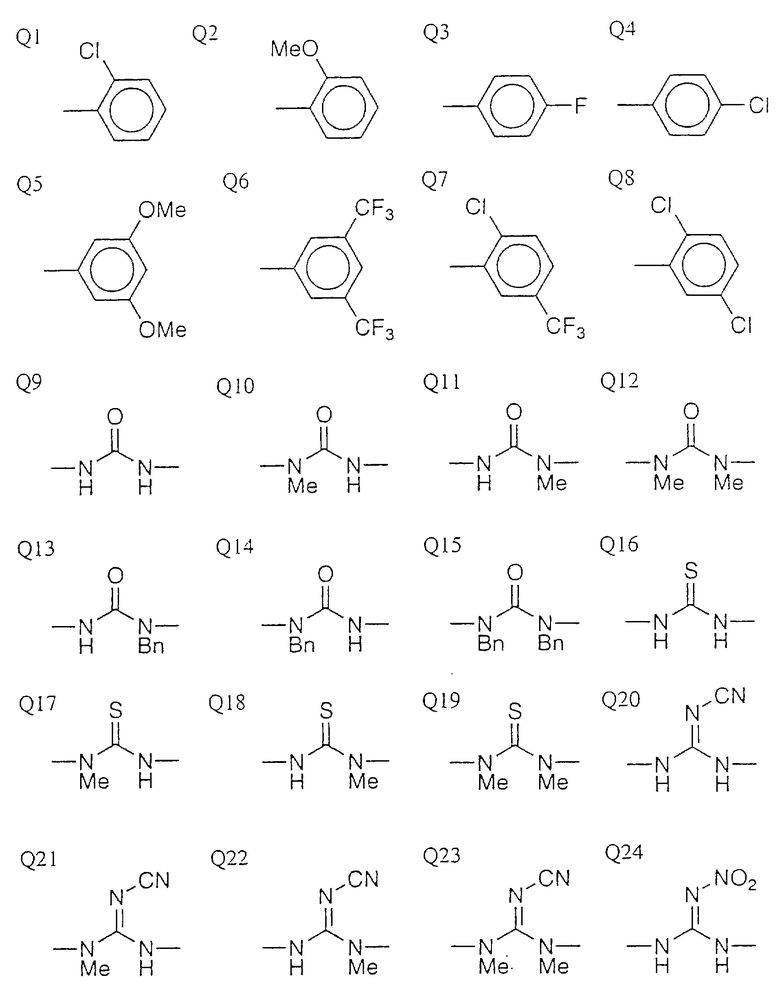
Типичные соединения среди производных бензимидазола формулы (Iа), как соединения данного изобретения, представлены в таблице 3, но должно быть понятно, что данное изобретение ни в коем случае не ограничивается такими конкретными соединениями, приведенными в конце описания, где Q1 - Q43 представляют группы формул.
Соединение формулы (I) данного изобретения можно использовать для цели данного изобретения либо в его свободной форме, либо в форме фармакологически приемлемой соли. Такая кислотно-аддитивная соль может, например, быть солью минеральной кислоты (такой как гидрохлорид, гидробромид, сульфат, гидросульфат, нитрат, фосфат, гидрофосфат или дигидрофосфат), солью органической кислоты (такой как формиат, ацетат, пропионат, сукцинат, малонат, оксалат, малеат, фумарат, малат, цитрат, тартрат, лактат, глутамат, аспартат, пикрат или карбонат) или сульфонатом (таким как метансульфонат, бензолсульфонат или толуолсульфонат).
Далее будут описаны способы получения соединений данного изобретения.
Производные бензимидазола формулы (I), как соединения данного изобретения, можно получить способами, представленными реакционными схемами (1) - (7) (см. в конце описания).
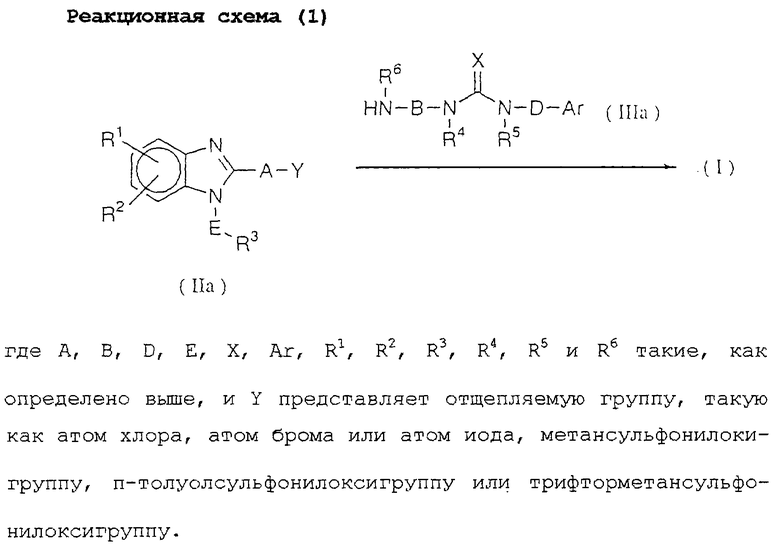
Реакционная схема (1) представляет собой способ получения соединения данного изобретения реакцией соединения (IIа) с соединением (IIIa).
Эту реакцию проводят обычно в присутствии или отсутствии неорганического основания или органического основания.
Неорганическое основание включает карбонаты металлов, такие как карбонат калия, карбонат натрия, карбонат лития, бикарбонат калия и бикарбонат натрия, гидроксиды металлов, такие как гидроксид лития, гидроксид натрия и гидроксид калия, гидриды металлов, такие как гидрид натрия, гидрид калия и н-бутиллитийгидрид, алкоксиды металлов, такие как метоксид натрия, этоксид натрия и трет-бутоксид калия, и амиды металлов, такие как амид натрия, диизопропиламид лития, гексаметилдисилазид лития, гексаметилдисилазид натрия, и 2,2,6,6-тетраметилпиперидид.
Органическое основание включает, например, триметиламин, триэтиламин, пиридин и диизопропилэтиламин.
Растворителем для реакции может быть любой растворитель, пока он не будет вовлечен в реакцию, им может быть, например, растворитель типа углеводорода, такой как бензол, толуол или гексан, растворитель типа простого эфира, такой как тетрагидрофуран, диэтиловый эфир или 1,4-диоксан, растворитель типа амида, такой как формамид, N,N-диметилацетамид, N,N-диметилформамид или N-метилпирролидон, растворитель типа спирта, такой как метанол, этанол или пропанол, растворитель галогенсодержащего типа, такой как хлороформ, метиленхлорид или этиленхлорид, другой растворитель, такой как ацетонитрил или диметилсульфоксид, вода или смесь таких растворителей. Однако реакцию можно проводить в отсутствии растворителя.
Температура реакции может быть в диапазоне от -78oС до точки кипения растворителя, используемого для реакции.
Молярное отношение исходных материалов необязательно может быть твердо установленным, но соединение (IIIa) можно использовать в количестве от 0,8 до 10 молей на моль соединения (IIа).
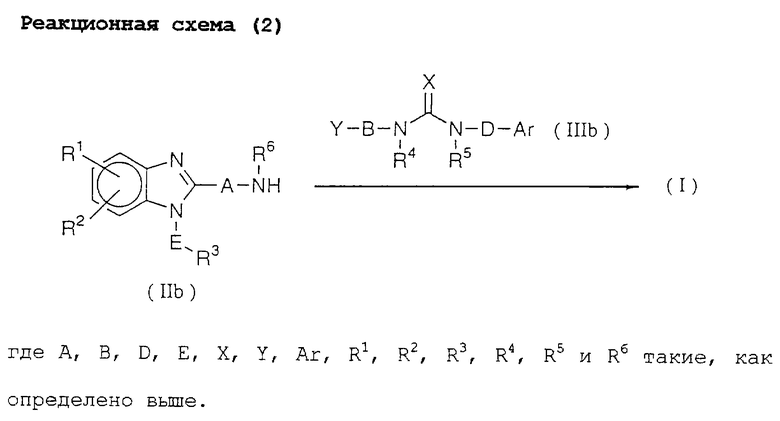
Реакционная схема (2) представляет собой способ получения соединения данного изобретения реакцией соединения (IIb) с соединением (IIIb).
Эту реакцию можно проводить в условиях, аналогичных реакционной схеме (1).
Молярное отношение исходных материалов необязательно может быть твердо установленным, но соединение (IIb) можно использовать в количестве от 0,8 до 10 молей на моль соединения (IIIb).
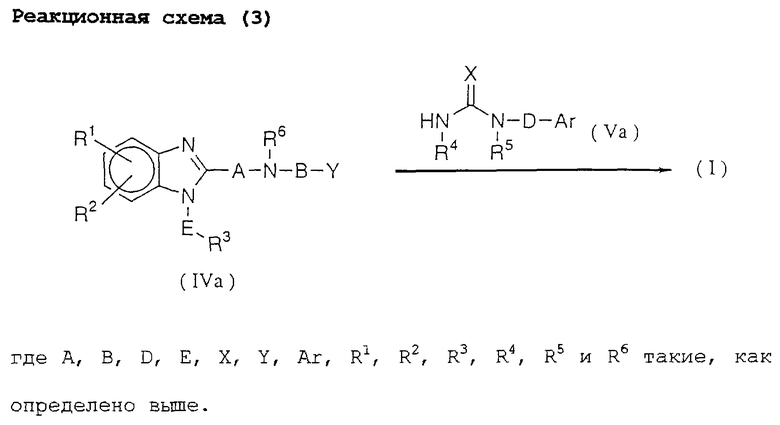
Реакционная схема (3) представляет собой способ получения соединения (I) данного изобретения реакцией соединения (IVa) с соединением (Va).
Эту реакцию можно проводить в условиях, аналогичных реакционной схеме (1).
Молярное отношение исходных материалов необязательно может быть твердо установленным, но соединение (Va) можно использовать в количестве от 0,8 до 1,5 моль на моль соединения (IVa).
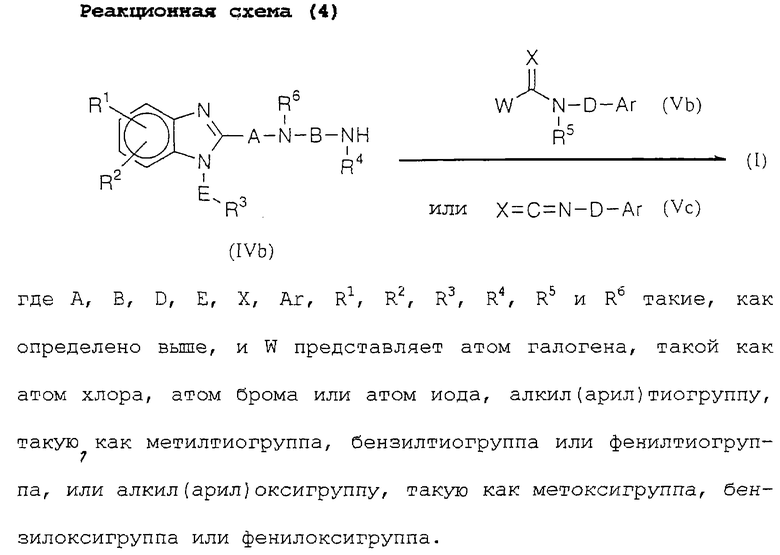
Реакционная схема (4) представляет собой способ получения соединения (I) данного изобретения реакцией соединения (IVb) с соединением (Vb) или соединением (Vc). (Когда используют соединение (Vc), R5 в соединении (I) будет атомом водорода).
Эту реакцию можно осуществлять нагреванием или охлаждением соединения (IVb) и соединения (Vb) или соединения (IVb) и соединения (Vc) в растворителе или в отсутствии растворителя, ее можно проводить в условиях, аналогичных реакционной схеме (1).
Молярное отношение исходных материалов необязательно может быть твердо установленным, но соединение (Vb) или соединение (Vc) можно использовать в количестве от 0,8 до 1,5 моль на моль соединения (IVb).
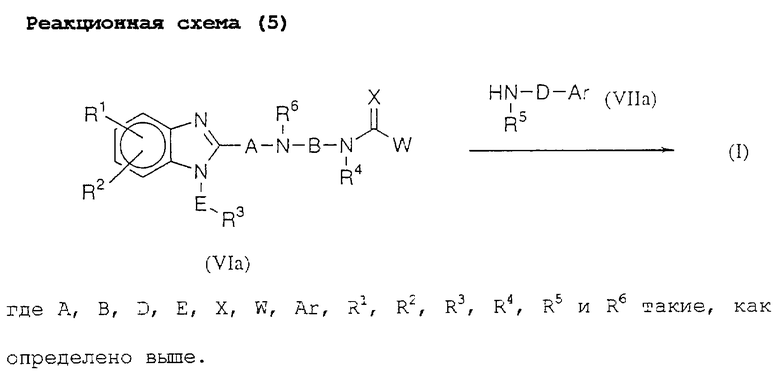
Реакционная схема (5) представляет собой способ получения соединения (I) данного изобретения реакцией соединения (VIa) с соединением (VIIa).
Эту реакцию можно осуществлять нагреванием или охлаждением соединения (VIa) и соединения (VIIa) в растворителе или в отсутствии растворителя, ее можно проводить в условиях, аналогичных реакционной схеме (1).
Молярное отношение исходных материалов необязательно может быть твердо установленным, но соединение (VIa) можно использовать в количестве от 0,8 до 1,5 моль на моль соединения (VIIa).
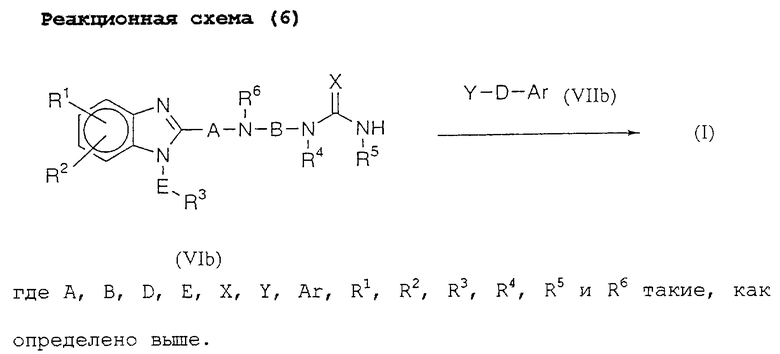
Реакционная схема (6) представляет собой способ получения соединения (I) данного изобретения реакцией соединения (VIb) с соединением (VIIb).
Эту реакцию можно проводить в условиях, аналогичных реакционной схеме (1).
Молярное отношение исходных материалов необязательно может быть твердо установленным, но соединение (VIb) можно использовать в количестве от 0,8 до 1,5 моль на моль соединения (VIIb).
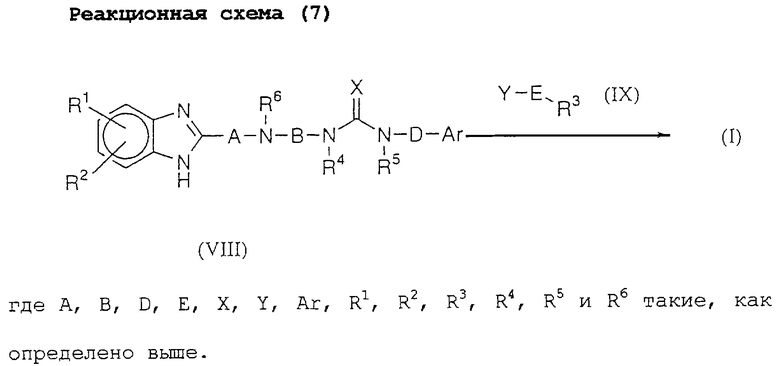
Реакционная схема (7) представляет собой способ получения соединения (I) данного изобретения реакцией соединения (VIII) с соединением (IX).
Эту реакцию можно проводить в условиях, аналогичных реакционной схеме (1).
Молярное отношение исходных материалов необязательно может быть твердо установленным, но соединение (IX) можно использовать в количестве от 0,8 до 1,5 моль на моль соединения (VIII).
Теперь будут описаны способы получения исходных материалов для соединений данного изобретения.
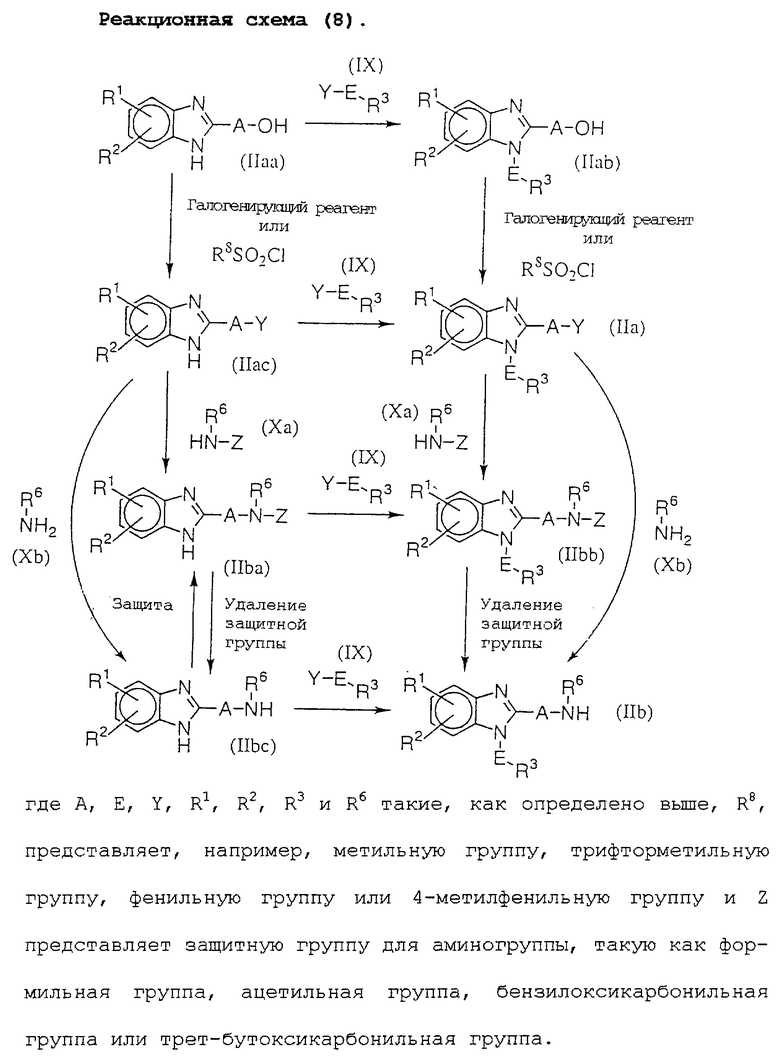
Среди исходных материалов для соединений данного изобретения соединение (IIа) и соединение (IIb) можно получить способами, показанными реакционной схемой (8).
Соединение (IIа) можно получить конденсацией соединения (IIaa) с соединением (IX) для получения соединения (IIab) с последующим галогенированием (галогенирующим реагентом может быть хлорирующий реагент, такой как пентахлорид фосфора, тионилхлорид, сульфурилхлорид, хлор-трифенилфосфин или тетрахлорид углерода-трифенилфосфин, бромирующий реагент, такой как трибромид фосфора, пентабромид фосфора, тионилбромид, сульфурилбромид, бром-трифенилфосфин или тетрабромид углерода-трифенилфосфин, или иодирующий реагент, такой как иодтрифенилфосфин, или реакцией его с R8SO2Cl или галогенированием соединения (IIaa) или реакцией его с R8SO2Cl для получения соединения (IIас) с последующей конденсацией его с соединением (IX).
Соединение (IIb) можно получить реакцией соединения (IIа) с соединением (Хb) или реакцией соединения (IIа) с соединением (Ха) для получения соединения (IIbb) с последующим удалением защитной группы, или реакцией соединения (IIас) с соединением (Ха) для получения соединения (IIba) с последующей реакцией его с соединением (IX) для получения соединения (IIbb) с последующим удалением защитной группы, или сначала проведением удаления защитной группы для получения соединения (IIbc) с последующей реакцией его с соединением (IX), или реакцией соединения (IIас) с соединением (Хb) для получения соединения (IIbc) с последующей реакцией его с соединением (IX), или защитой его для получения соединения (IIba) с, последующей реакцией его с соединением (IX) для получения соединения (IIbb) с последующим удалением защитной группы.
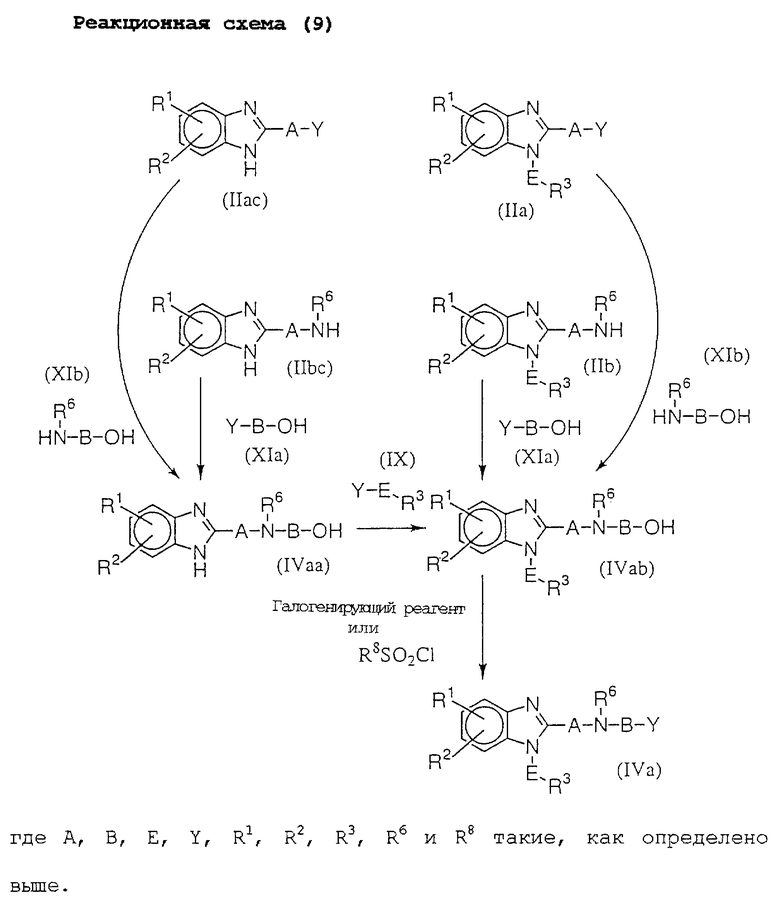
Среди исходных материалов для соединений данного изобретения соединение (IVa) можно получить способами, показанными на реакционной схеме (9).
Соединение (IVa) можно получить реакцией соединения (IIа) с соединением (XIb) или реакцией соединения (IIb) с соединением (XIа) для получения соединения (IVab) с последующим галогенированием его или реакцией его с R8SO2Cl, или реакцией соединения (IIас) с соединением (XIb), или реакцией соединения (IIbc) с соединением (ХIа) для получения соединения (IVaa) с последующей реакцией его с соединением (IX) для получения соединения (IVab) с последующим галогенированием его или реакцией его с R8SO2Cl.
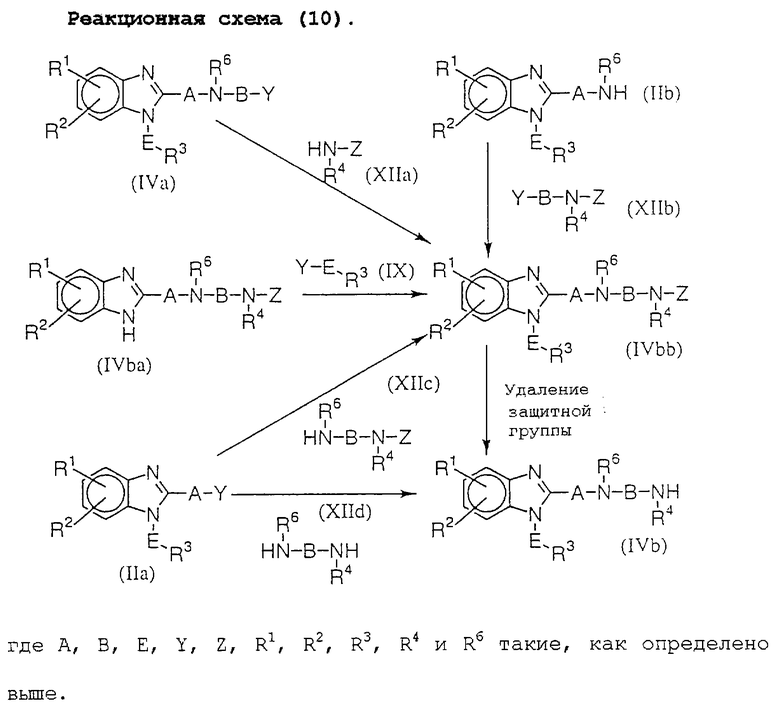
Среди исходных материалов для соединений данного изобретения соединение (IVb) можно получить способами, показанными на реакционной схеме (10).
Соединение (IVb) можно получить удалением защитной группы соединения (IVbb) или реакцией соединения (IIа) с соединением (XIId), Промежуточный продукт (IVbb) можно получить реакцией соединения (IIb) с соединением (XIIb), реакцией соединения (IVa) с соединением (XIIа), реакцией соединения (IVba) с соединением (IX) или реакцией соединения (IIа) с соединением (XIIc).
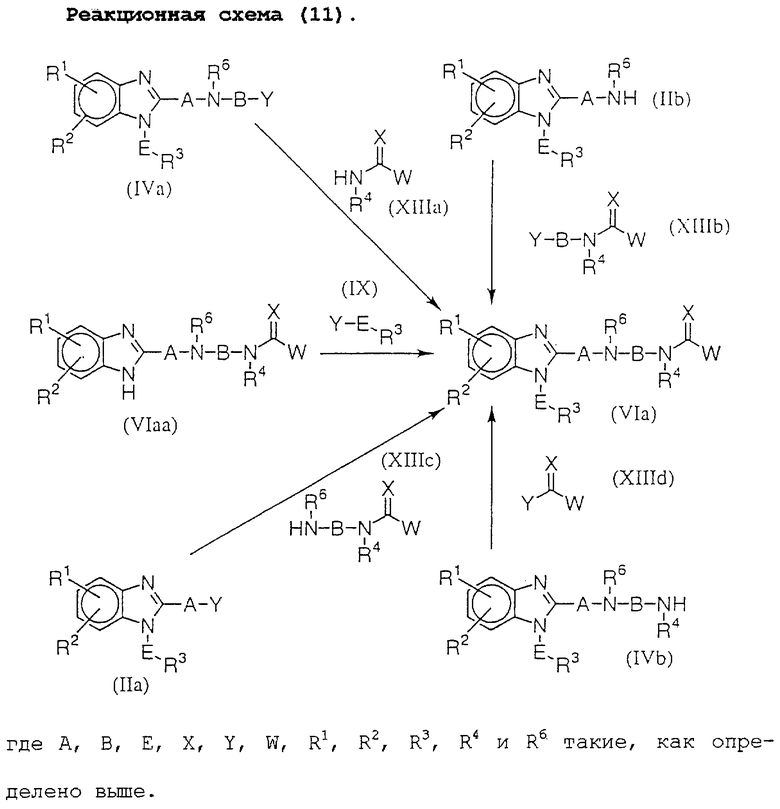
Среди исходных материалов для соединений данного изобретения соединение (VIa) можно получить способами, показанными на реакционной схеме (11).
Соединение (VIa) можно получить реакцией соединения (IIb) с соединением (XIIIb), реакцией соединения (IVa) с соединением (XIIIa), реакцией соединения (VIaa) с соединением (IX), реакцией соединения (IIа) с соединением (XIIIc) или реакцией соединения (IVb) с соединением (XIIId).
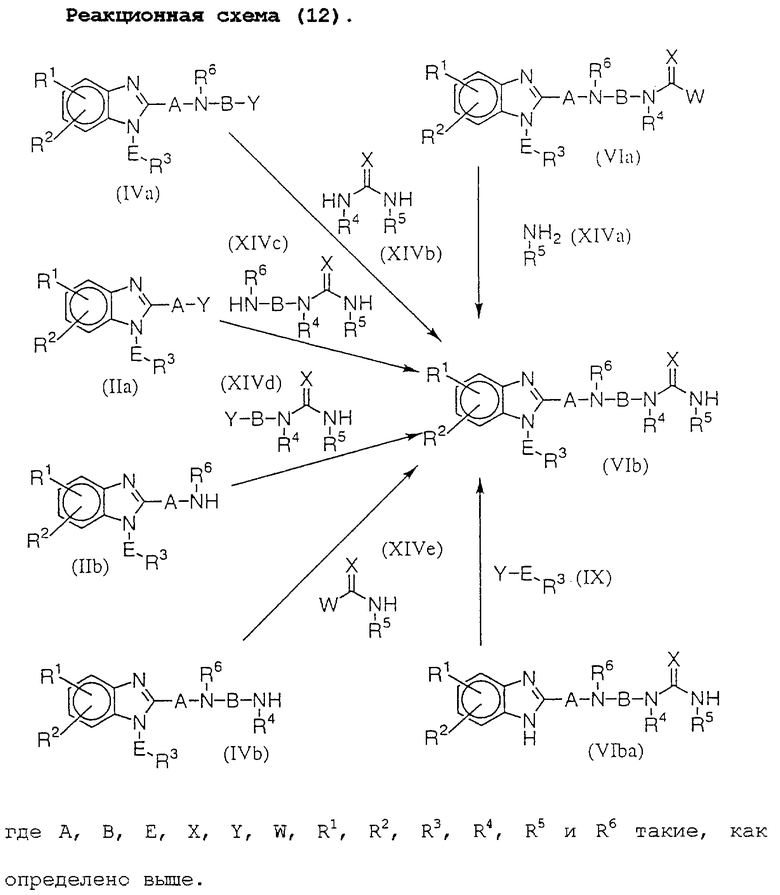
Среди исходных материалов для соединений данного изобретения соединение (VIb) можно получить способами, показанными на реакционной схеме (12).
Соединение (VIb) можно получить реакцией соединения (VIa) с соединением (XIVa), реакцией соединения (IVa) с соединением (XIVb), реакцией соединения (IIа) с соединением (XIVc), реакцией соединения (IIb) с соединением (XIVd), реакцией соединения (IVb) с соединением (XIVe) или реакцией соединения (IVba) с соединением (IX).
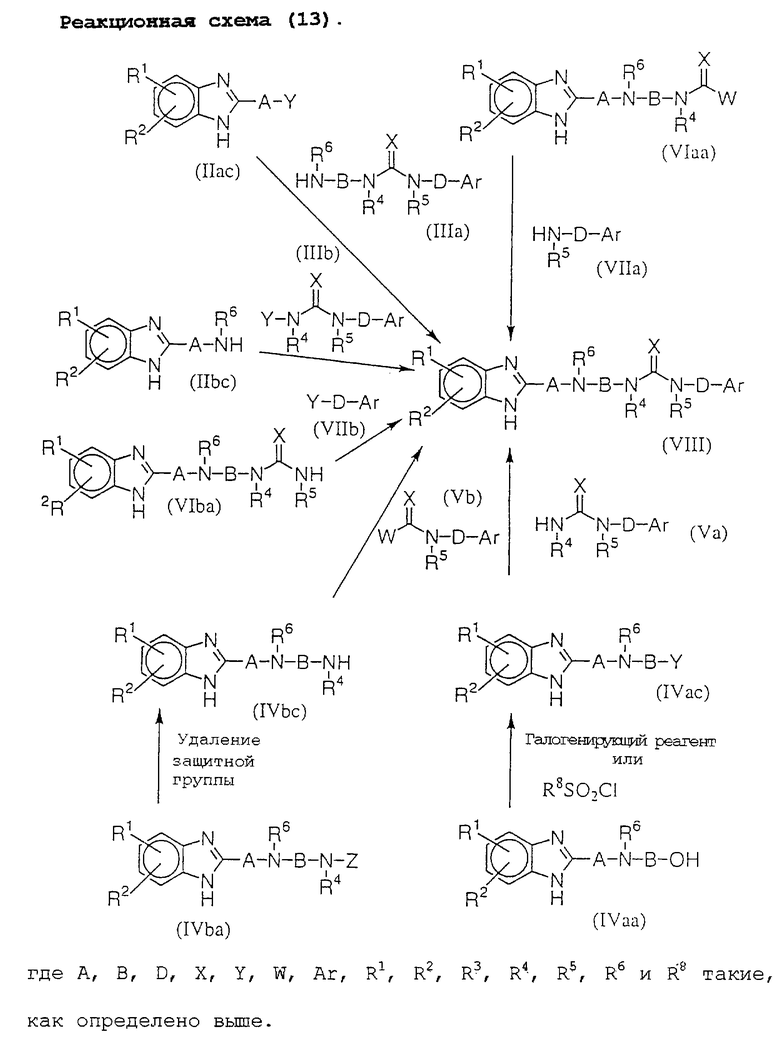
Среди исходных материалов для соединений данного изобретения соединение (VIII) можно получить способами, показанными на реакционной схеме (13).
Соединение (VIII) можно получить реакцией соединения (VIaa) с соединением (VIIa), реакцией соединения (IIас) с соединением (IIIa), реакцией соединения (VIba) с соединением (VIIb), реакцией соединения (IIbc) с соединением (IIIb), удалением защитной группы соединения (IVba) для получения соединения (IVbc) с последующей реакцией его с соединением (Vb) или галогенированием соединения (IVaa) или реакцией его с R8SO2Cl для получения соединения (IVac) с последующей реакцией его с соединением (Va).
Реакции следующих соединений, описанных на реакционных схемах от (8) до (13), т. е. (VIaa) и (VIIa), (IIас) и (IIIa), (IIbc) и (IIIb), (VIba) и (VIIb), (IVbc) и (Vb), (IVac) и (Va), (IVb) и (XIVe), (IIb) и (XIVd), (IIа) и (XIVc), (VIa) и (XIVa), (IVa) и (XIVb), (IVa) и (XIIIa), (IIb) и (XIIIb), (IIа) и (XIIIc), (IVb) и (XIIId), (IIас) и (XIb), (IIа) и (XIb), (IIbc) и (XIa), (IIb) и (XIa), (IIb) и (XIIb), (IVa) и (ХIIа), (IIа) и (XIIc), (IIа) и (XIId), (IIас) и (Ха), (IIа) и (Ха), (IIас) и (Хb), (IIа) и (Хb), (VIaa) и (IX), (VIba) и (IX), (IVba) и (IX), (IVaa) и (IX), (IIаа) и (IX), (IIас) и (IX), (IIbа) и (IX) и (IIbc) и (IX), можно проводить в условиях, аналогичных реакционной схеме (1). Реакции можно проводить также в отсутствии растворителя. Молярные отношения соединений необязательно могут быть твердо установлены, но они могут быть в диапазоне от 0,1:1 до 1:0,1.
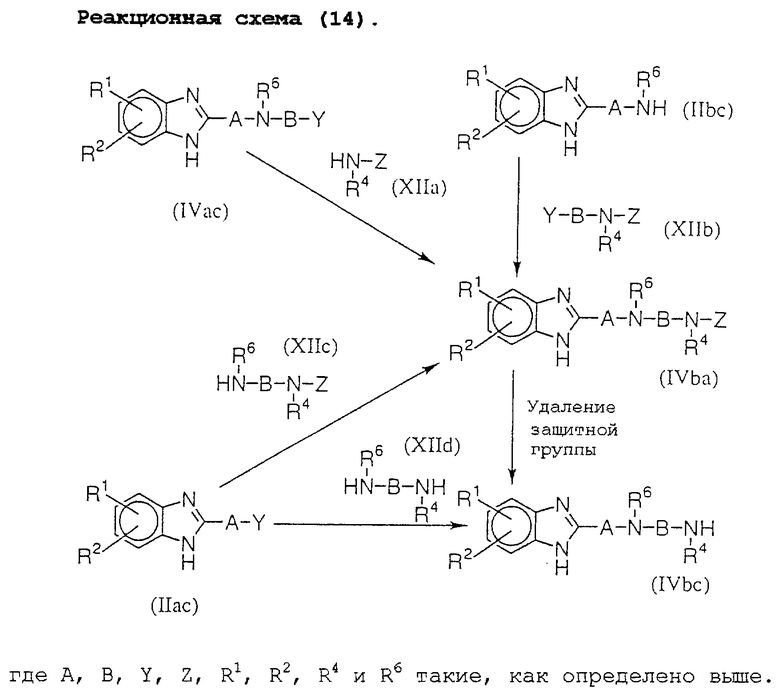
Промежуточные продукты (IVba), (IVbc), (VIaa) и (VIba), описанные в реакционных схемах от (10) до (13), могут быть получены способами, указанными на реакционных схемах от (14) до (16).
Соединение (IVba) можно получить реакцией соединения (IIbc) с соединением (XIIb), реакцией соединения (IVac) с соединением (XIIа) или реакцией соединения (IIас) с соединением (XIIc).
Соединение (IVbc) можно получить реакцией соединения (IIас) с соединением (XIId) или реакцией соединения (IIас) с соединением (XIIc) для получения соединения (IVba) с последующим удалением защитной группы.
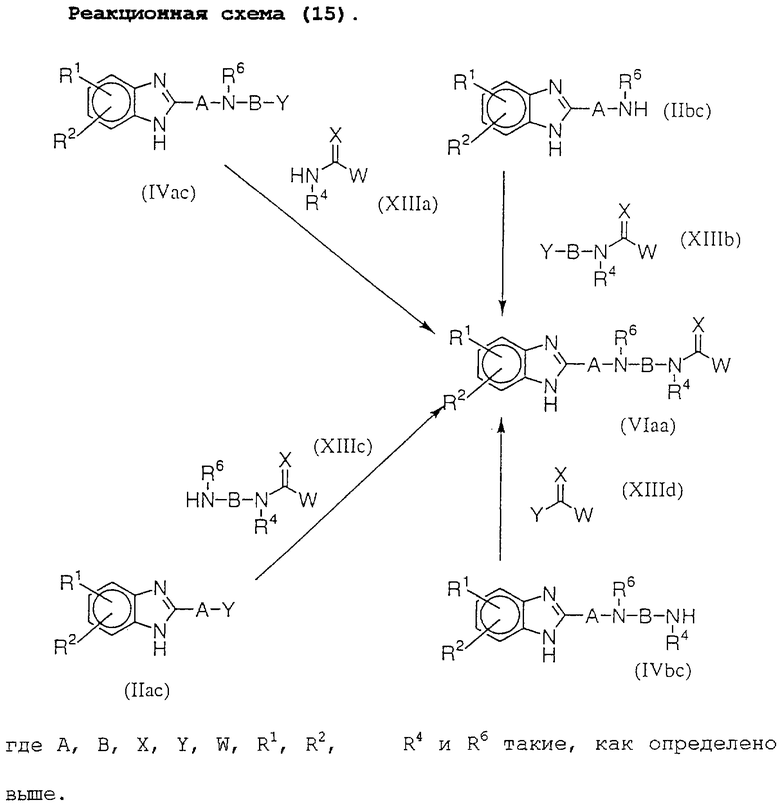
Соединение (VIaa) можно получить реакцией соединения (IIbc) с соединением (XIIIb), реакцией соединения (IVac) с соединением (XIIIa), реакцией соединения (IIас) с соединением (XIIIс) или реакцией соединения (IVbc) с соединением (XIIId).
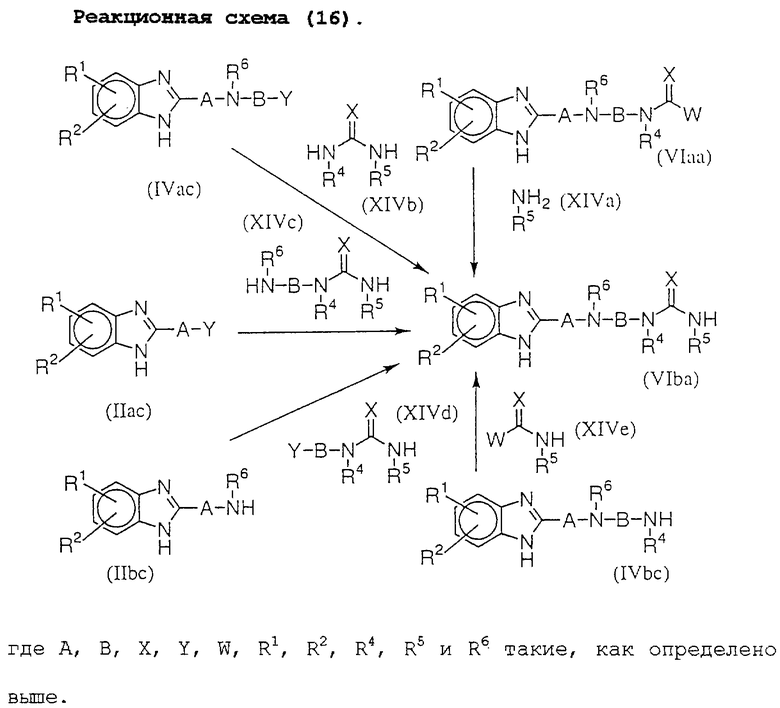
Соединение (VIba) можно получить реакцией соединения (VIaa) с соединением (XIVa), реакцией соединения (IVac) с соединением (XIVb), реакцией соединения (IIас) с соединением (XIVc), реакцией соединения (IIbс) с соединением (XIVd) или реакцией соединения (IVbc) с соединением (XIVe).
Реакции следующих соединений, описанных на реакционных схемах от (14) до (16), т. е. (IIас) и (XIIс), (IIас) и (XIId), (IIbc) и (XIIb), (IVac) и (XIIa), (IVac) и (XIIIa), (IIbc) и (XIIIb), (IIас) и (XIIIc), (IVbc) и (XIIId), (VIaa) и (XIVa), (IVac) и (XIVb), (IIас) и (XIVc), (IIbc) и (XIVd) и (IVbc) и (XIVe), можно проводить в условиях, аналогичных реакционной схеме (1). Кроме того, реакции можно проводить также в отсутствии растворителя. Молярные отношения соединений необязательно могут быть твердо установлены, но они могут быть в диапазоне от 0,1:1 до 1:0,1.
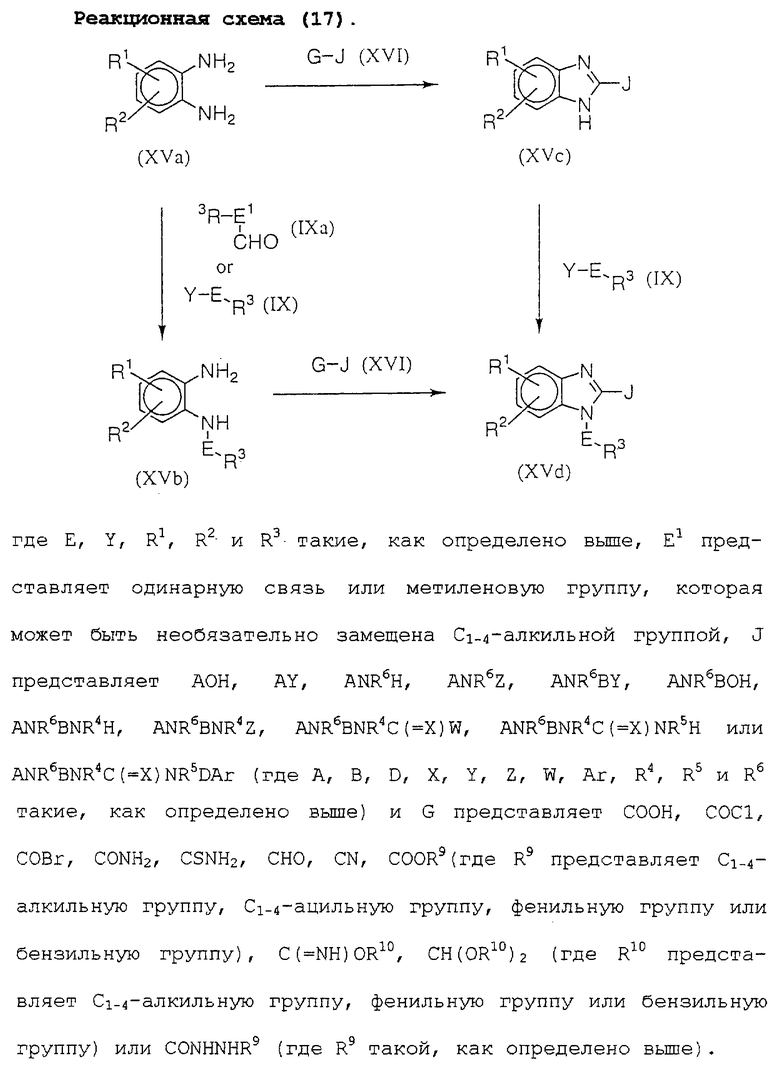
Способы, показанные на реакционной схеме (17), можно использовать как способы для получения структуры бензимидазола.
Производное бензимидазола формулы (XVc) можно получить конденсацией производного диаминобензола формулы (XVa) с соединением (XVI). Кроме того, производное бензимидазола формулы (XVd) можно получить конденсацией производного диаминобензола формулы (XVb) с соединением (XVI) или реакцией соединения (XVc) с соединением (IX). Промежуточный продукт (XVb) можно получить реакцией соединения (XVa) с соединением (IX) или конденсацией соединения (IХа) в восстанавливающих условиях.
Что касается условий получения, то ссылку можно сделать на способы, описанные, например, в J. Org. Chem., 28, 1931 (1963); J. Chem. Soc., 2238 (1953); J. Am. Chem. Soc., 77, 5652, 1955); J. Chem. Soc., 673 (1956); J. Am Chem. Soc. , 73, 5907 (1951); J. Am. Chem. Soc., 70, 2415 (1948); J. Chem. Soc. , 625 (1943); Khim. Geterotsikl. Soedin., 5, 684 (1982); J. Org. Chem., 56 (6), 2260 (1991); Synth. Commnn., 16(1), 35 (1986); Khim. Geterotsikl. Soedin. , 71 (1980); Chem. Soc. C., 20 (1967); Chim. Ther., 2, 95 (1967); J. Org. Chem. , 27, 2163 (1962); Chem. Pharm. Bull., 12, 773 (1964); J. Chem. Soc. , 2296 (1959); J. Am. Chem. Soc., 79, 4391 (1957); J. Chem. Soc., 1401 (1949).
Вышеуказанными способами соединения (IIаа), (IIас), (IIbc), (IIba), (IVac), (IVaa), (IVbc), (IVba), (VIaa), (VIba) и (VIII) можно получить непосредственно из соединения (XVa). Кроме того, соединения (IIab), (IIа), (IIb), (IIbb), (IVa), (IVab), (IVbb), (IVb), (VIa), (VIb) и (I) можно получить непосредственно из соединения (XVb).
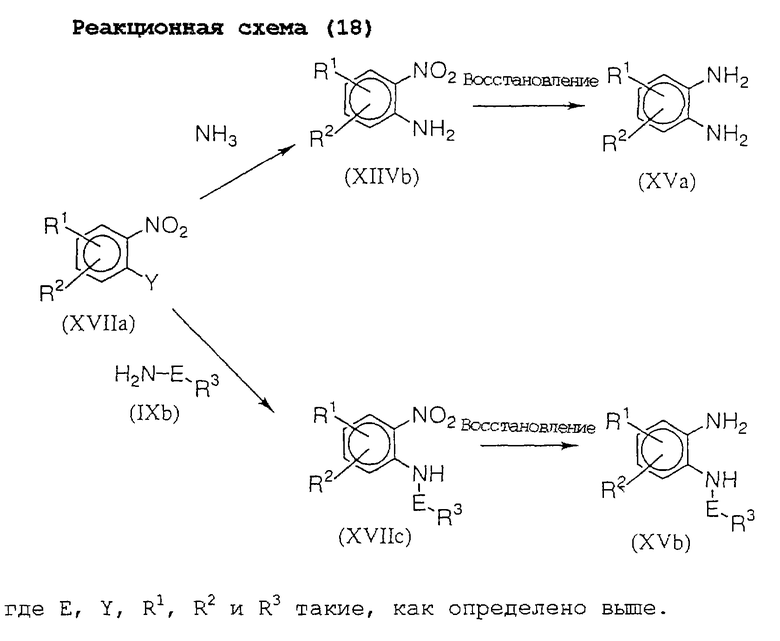
Для получения соединений (XVa) и (XVb) можно использовать способы, показанные на реакционной схеме (18).
Соединение (XVa) можно получить реакцией соединения (XVIIa) с аммиаком для получения соединения (XVIIb) с последующим его восстановлением. Кроме того, соединение (XVb) можно получить реакцией соединения (XVIIa) с соединением (IXb) для получения соединения (XVIIc) с последующим восстановлением его.
Как описано выше, авторами данного изобретения было обнаружено, что соединение формулы (I) данного изобретения представляет собой превосходное соединение в качестве сильного антиаллергического агента и его можно использовать не только в качестве активного ингредиента для профилактического или лечебного агента для поллиноза, крапивницы, атопического дерматита, аллергического ринита и астмы и так далее, но также в качестве эффективного средства против других болезней, относящихся к веществу Р, например, глазных болезней, таких как конъюнктивит и весенний катар глаз; воспалительных болезней, таких как хронический ревматоидный артрит; болей, таких как мигрень, головная боль, зубная боль и продолжительная тупая боль, сопровождающая различные болезни; желудочно-кишечные болезни, такие как неспецифический язвенный колит и болезнь Крона, и психические болезни, такие как депрессия и дистимия. Таким образом, данное изобретение предлагает фармацевтическую композицию, содержащую соединение данного изобретения в количестве, эффективном для лечения этих болезней.
Способом введения соединения данного изобретения может быть парентеральное введение, инъекции (гиподермическая, внутривенная, внутримышечная или внутрибрюшинная инъекция), мазь, суппозиторий или аэрозоль или пероральное введение таблеток, капсул, гранул, пилюль, сиропа, жидкости, эмульсии или суспензии.
Фармакологическая или ветеринарная композиция, содержащая соединение данного изобретения, содержит соединение данного изобретения в количестве от около 0,01 до 99,5%, предпочтительно от около 0,1 до 30%, считая на общую массу композиции.
Помимо соединения данного изобретения в композицию может быть введено другое фармаколически или ветеринарно активное соединение. Такая композиция может содержать несколько соединений данного изобретения.
Эффективная доза соединения данного изобретения обычно составляет от около 0,003 до 1,5 г, предпочтительно от около 0,01 до 0,6 г, для взрослого пациента в день, хотя его клиническая доза зависит от возраста, массы, восприимчивости и состояний пациента. Тем не менее, если необходимо, доза может быть вне вышеуказанного диапазона.
Соединения данного изобретения могут быть изготовлены в виде различных готовых препаративных форм, подходящих для введения в соответствии с фармацевтически общепринятыми способами.
А именно, таблетки, капсулы, гранулы или пилюли для перорального введения можно получить с использованием наполнителя, такого как сахар, лактоза, глюкоза, крахмал или маннит; связывающего вещества, такого так гидроксипропилцеллюлоза, сироп, аравийская камедь, желатин, сорбит, трагакант, метилцеллюлоза или поливинилпирролидон; дезинтегрирующего средства, такого как крахмал, карбоксиметилцеллюлоза или ее кальциевая соль, микрокристаллическая целлюлоза или полиэтиленгликоль; сшивающего агента, такого как тальк, стеарат магния или кальция или диоксид кремния; или смазывающего вещества, такого как лаурат натрия или глицерин.
Инъекции, растворы, эмульсии, суспензии, сиропы или аэрозоли можно получить с использованием растворителя для активного ингредиента, такого как вода, этиловый спирт, изопропиловый спирт, пропиленгликоль, 1,3-бутиленгликоль или полиэтиленгликоль; поверхностно-активного вещества, такого как эфир сорбитана и жирной кислоты, полиоксиэтилированный эфир сорбитана и жирной кислоты, полиоксиэтиленовый эфир жирной кислоты, полиоксиэтиленовый простой эфир гидрированного касторового масла или лецитин; суспендирующего агента, такого как производное целлюлозы, такое как натриевая соль карбоксиметил- или метилцеллюлозы, или натуральный каучук, такой как трагакант или аравийская камедь; или консерванта, такого как эфир параоксибензойной кислоты, хлорид бензалкония или соль сорбиновой кислоты.
Мази для чрескожного абсорбирования можно получить с использованием белого мягкого парафина, вазелинового масла, высшего спирта, мази макрогол, гидрофильной мази или наполнителя типа водного геля.
Суппозитории можно получить с использованием, например, какао-масла, полиэтиленгликоля, ланолина, триглицерида жирных кислот, кокосового масла или полисорбата.
Лучший способ осуществления примеров изобретения
Теперь данное изобретение будет описано с дальнейшими подробностями со ссылкой на примеры (включая примеры получения, примеры готовых препаративных форм и примеры испытания). Однако, должно быть понятно, что данное изобретение ни в коем случае не ограничивается этими конкретными примерами.
Символ "т. пл." означает "точку плавления".
ССЫЛОЧНЫЙ ПРИМЕР 1: N-Метил-N-(бензимидазол-2-ил)-N'-метил-N'-трет-бутоксикарбонил-1,3-пропилендиамин
Раствор, включающий 1,1 г 2-хлорбензимидазола и 1,6 г N,N'-диметил-1,3-пронилендиамина, нагревали при температуре от 120 до 130oС в течение двух часов. После охлаждения раствор разбавляли 50 мл хлороформа и промывали 30 мл 1 н. водного раствора карбоната калия. Его сушили над безводным сульфатом натрия и затем растворитель отгоняли при пониженном давлении. Полученный остаток растворяли в 50 мл хлороформа и к нему добавляли 5 г ди-трет-бутилдикарбоната. Смесь оставляли для стояния при комнатной температуре в течение одного часа и затем растворитель отгоняли при пониженном давлении. Полученный остаток перекристаллизовывали из диэтилового простого эфира, получая 2,1 г вышеидентифицированного соединения в виде бледно-коричневых кристаллов.
ССЫЛОЧНЫЙ ПРИМЕР 2: N-Метил-N-(бензимидазол-2-ил)-N'-метил-N'-трет-бутоксикарбонил-1,2-этилендиамин
Таким же способом, как в ссылочном примере 1, было получено 1,1 г вышеназванного соединения в виде бледно-коричневых кристаллов из 1,0 г 2-хлорбензимидазола и 4,0 г N,N'-диметил-1,2-этипендиамина.
ССЫЛОЧНЫЙ ПРИМЕР 3: N-Метил-N-(бензимидазол-2-ил)метил-N'-метил-N'-трет-бутоксикарбонил-1,3-пропилендиамин
2-Хлорметилбензимидазол в количестве 4,0 г добавляли при охлаждении льдом к раствору, включающему 5,0 г N,N'-диметил-1,3-пропилендиамина и 30 мл этанола, и смесь перемешивали в течение одного часа. Смесь после возвращения к комнатной температуре перемешивали в течение ночи, после чего растворитель отгоняли при пониженном давлении. К полученному остатку добавляли 50 мл воды и 50 мл хлороформа и карбонат калия добавляли до тех пор, пока смесь не становилась основной. Органический слой отделяли и сушили над безводным сульфатом калия и затем растворитель отгоняли при пониженном давлении. К полученному остатку добавляли 50 мл хлороформа и к этому раствору добавляли 8 г ди-трет-бутил-дикарбоната. Смесь перемешивали при комнатной температуре в течение одного часа и затем растворитель отгоняли при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат/этанол=9/1), получая 7,0 г вышеназванного соединения в виде коричневого маслянистого вещества.
ССЫЛОЧНЫЙ ПРИМЕР 4: N-Метил-N-(бензимидазол-2-ил)метил-N'-метил-N'-трет-бутоксикарбонил-1,2-этилендиамин
Таким же способом, как в ссылочном примере 3, было получено 6,5 г вышеназванного соединения в виде окрашенного в оранжевый цвет маслянистого вещества из 8,0 г N,N'-диметил-1,2-этилендиамина и 5,0 г 2-хлорметилбензимидазола.
ССЫЛОЧНЫЙ ПРИМЕР 5: N-Метил-N-(1-(4-фторбензил)бензимидазол-2-ил)-N'-метил-N'-трет-бутоксикарбонил-1,3-пропилендиамин
Раствор, включающий 1,0 г N-метил-N-(бензимидазол-2-ил)-N'-метил-N'-трет-бутоксикарбонил-1,3-пропилендиамина, 540 мг 4-фторбензилхлорида, 3 г карбоната калия и 20 мл диметилформамида, подвергали реакции при комнатной температуре в течение ночи при перемешивании. Затем его подвергали реакции при температуре от 50 до 60oС в течение 10 часов. Затем к нему добавляли 50 мл воды и смесь экстрагировали этилацетатом. Экстракт сушили над безводным сульфатом натрия (30 мл•3) и затем растворитель отгоняли при пониженном давлении. Полученный остаток очищали колоночной хроматографией на силикагеле (элюент: этилацетат), получая 1,4 г вышеназванного соединения в виде бесцветного маслянистого вещества.
ССЫЛОЧНЫЙ ПРИМЕР 6: N-Метил-N-(1-(4-фторбензил)бензимидазол-2-ил)-N'-метил-N'-трет-бутоксикарбонил-1,2-этилендиамин
Таким же способом, как в ссылочном примере 5, было получено 1,3 г вышеназванного соединения в виде бледно-желтого маслянистого вещества из 1,0 г N-метил-N-(бензимидазол-2-ил)-N'-метил-N'-трет-бутоксикарбонил-1,2-этилендиамина.
ССЫЛОЧНЫЙ ПРИМЕР 7: N-Метил-N-(1-(4-фторбензил)бензимидазол-2-ил)метил-N'-метил-N'-трет-бутоксикарбонил-1,3-пропилендиамин
Таким же способом, как в ссылочном примере 5, было получено 5,0 г вышеназванного соединения в виде бледно-желтого маслянистого вещества из 6,5 г N-метил-N-(бензимидазол-2-ил)метил-N'-метил-N'-трет-бутоксикарбонил-1,3-пропилендиамина.
ССЫЛОЧНЫЙ ПРИМЕР 8: N-Метил-N-(1-(4-фторбензил)бензимидазол-2-ил)метил-N'-метил-N'-трет-бутоксикарбонил-1,2-этилендиамин
Таким же способом, как в ссылочном примере 5, было получено 6,1 г вышеназванного соединения в виде бледно-желтого маслянистого вещества из 6,0 г N-метил-N-(бензимидазол-2-ил)метил-N'-метил-N'-трет-бутоксикарбонил-1,2-этилендиамина.
ПРИМЕР ПОЛУЧЕНИЯ 1: Гидрохлорид N-Метил-N-(1-(4-фтор-бензил) бензимидазол - 2 - ил) - N' - метил - N' - (3,5 - бис (трифторметил) бензиламинокарбонил)-1,3-пропилендиамина
Трифторуксусную кислоту в количестве 2 мл добавляли к 1,3 г N-метил-N-(1-(4-фторбензил)бензимидазол-2-ил)-N'-метил-N'-трет-бутоксикарбонил-1,3-пропилендиамина и смесь перемешивали при комнатной температуре в течение одного часа. Затем к ней добавляли 50 мл воды и 50 мл хлороформа и карбонат калия добавляли к ней до тех пор, пока смесь не становилась основной. Органический слой отделяли и сушили над безводным сульфатом натрия. Растворитель отгоняли при пониженном давлении, получая 970 мг бесцветного маслянистого вещества. К 300 мг этого маслянистого вещества добавляли 370 мг фенил N-(3,5-бис(трифторметил)бензил)карбамата и смесь нагревали и перемешивали при 120oС в течение двух часов. После охлаждения полученное маслянистое вещество очищали колоночной хроматографией на силикагеле (элюент:этилацетат/этанол = 9/1), получая 500 мг бесцветного маслянистого вещества. 250 мг Этого маслянистого вещества растворяли в 3 мл этанола и к нему добавляли 3 мл 28% смеси хлористо-водородная кислота-этанол. Растворитель отгоняли при пониженном давлении и остаток кристаллизовали из диэтилового простого эфира, получая 280 мг вышеназванного соединения в виде бесцветных кристаллов (т.пл. 170,0-172,0oС).
ПРИМЕР ПОЛУЧЕНИЯ 2: Гидрохлорид N-метил-N-(1-(4-фторбензил) бензимидазол-2-ил)-N'-метил-N'-(3,5-бис(трифторметил) бензиламиаминокарбонил)-1,2-этилендиамина
Таким же способом, как в примере получения 1, получали вышеназванное соединение виде бесцветных кристаллов из N-метил-N-(1-(4-фторбензил)бензимидазол-2-ил)-N'-метил-N'-трет-бутоксикарбонил-1,2-этилендиамина (т.пл. 182,0-185,0oС).
ПРИМЕР ПОЛУЧЕНИЯ 3: Гидрохлорид N-метил-N-(1-(4-фторбензил) бензимидазол-2-ил)метил-N'-метил-N'-(3,5-бис(трифторметил) бензиламинокарбонил)-1,3-пропилендиамина
Таким же способом, как в примере получения 1, получали вышеназванное соединение в виде бледно-желтого маслянистого вещества из N-метил-N-(1-(4-фторбензил)бензимидазол-2-ил)метил N'-метил-N'-трет-бутоксикарбонил-1,3-пропилендиамина.
ПРИМЕР ПОЛУЧЕНИЯ 4: Гидрохлорид N-метил-N-(1-(4-фтор-бензил) бензимидазол-2-ил)-метил-N'-метил-N'-(3,5-бис(трифторметил) бензиламинокарбонил)-1,2-этилендиамина
Таким же способом, как в примере получения 1, получали вышеназванное соединение в виде бесцветных кристаллов из N-метил-N-(1-(4-фторбензил)бензимидазол-2-ил)метил-N'-метил-N'-трет-бутоксикарбонил-1,2-этилендиамина (т.пл. 144,0-145,0oС).
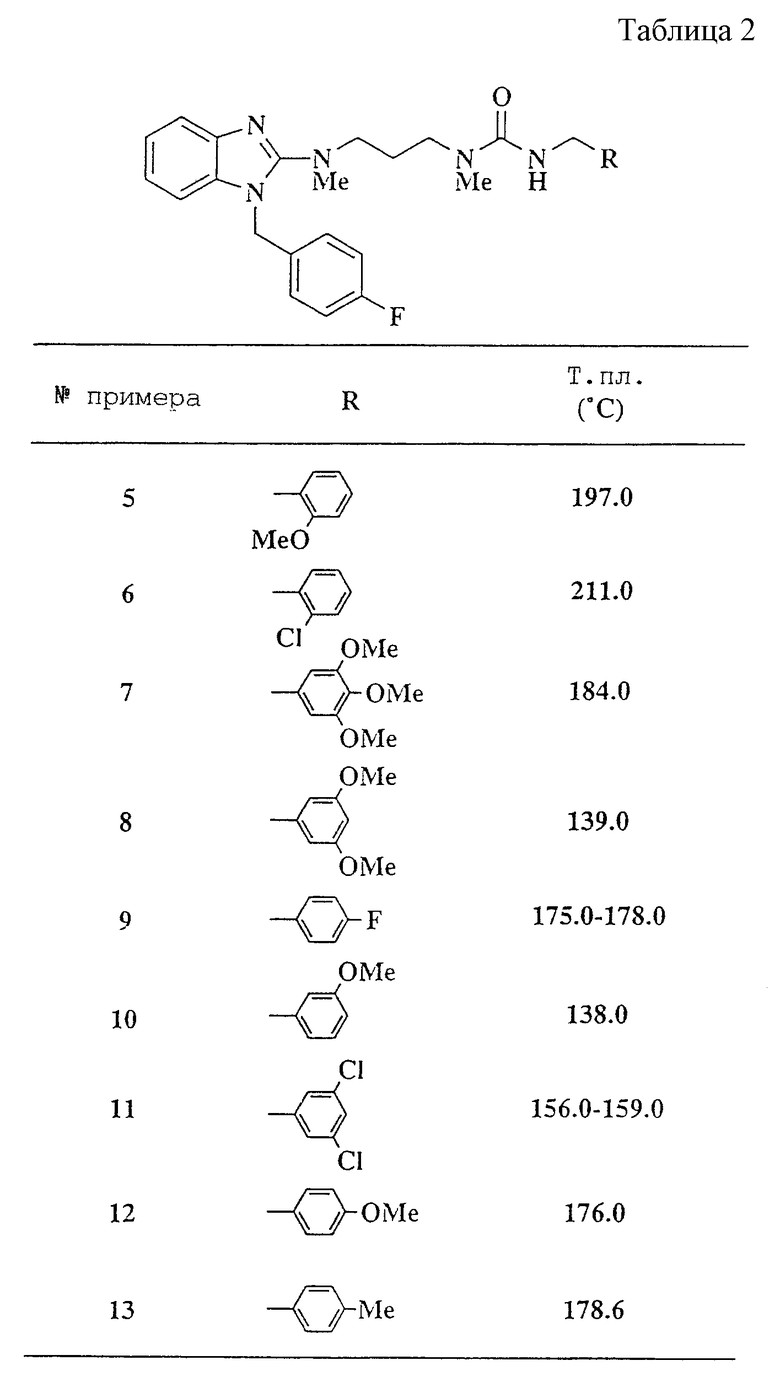
ПРИМЕРЫ ПОЛУЧЕНИЯ 5-13.
Таким же способом, как в примере получения 1, были получены соединения, приведенные в таблице 2, в форме их гидрохлоридов.
РЕЦЕПТУРНЫЙ ПРИМЕР 1: Таблетки, г:
Соединение данного изобретения - 10
Лактоза - 260
Микрокристаллическая целлюлоза - 600
Кукурузный крахмал - 350
Гидроксипропилцеллюлоза - 100
Карбоксиметилцеллюлоза-Са - 150
Стеарат магния - 30
Всего - 1500
Вышеуказанные ингредиенты смешивали общепринятым способом и превращали в 10000 покрытых сахаром таблеток, содержащих 1 мг активного ингредиента на таблетку.
РЕЦЕПТУРНЫЙ ПРИМЕР 2: Капсулы, г:
Соединение данного изобретения - 10
Лактоза - 440
Микрокристаллическая целлюлоза - 1000
Стеарат магния - 50
Всего - 1500
Вышеуказанные ингредиенты смешивали общепринятым способом и заполняли в желатиновые капсулы для получения 10000 капсул, содержащих 1 мг активного ингредиента на капсулу.
РЕЦЕПТУРНЫЙ ПРИМЕР 3: Мягкие эластичные капсулы, г
Соединение данного изобретения - 10
ПЭГ 400 - 479
Глицерид насыщенных жирных кислот - 1500
Масло перечной мяты - 1
Полисорбат 80 - 10
Всего - 2000
Вышеуказанные ингредиенты смешивали и затем заполняли в мягкие желатиновые капсулы 3 общепринятым способом для получения 10000 мягких эластичных капсул, содержащих 1 мг активного ингредиента на капсулу.
РЕЦЕПТУРНЫЙ ПРИМЕР 4: Мазь, г:
Соединение данного изобретения - 1,0
Жидкий парафин - 10,0
Цетанол - 20,0
Белый мягкий парафин - 68,4
Этилпарабен - 0,1
1-Ментол - 0,5
Всего - 100,0
Вышеуказанные ингредиенты смешивали общепринятым способом для получения 1% мази.
РЕЦЕПТУРНЫЙ ПРИМЕР 5: Суппозиторий, г:
Соединение данного изобретения - 1
Витерсол Н15* - 478
Витерсол W35* - 520
Полисорбат 80 - 1
Всего - 1000
* Фирменное, название соединения типа триглицерида
Вышеуказанные ингредиенты смешивали при расплавлении общепринятым способом и наливали в контейнер для суппозитория с последующим охлаждением и отверждением для получения 1000 штук суппозиторий по 1 г, содержащих по 1 мг активного ингредиента.
РЕЦЕПТУРНЫЙ ПРИМЕР 6: Инъекция
Соединение данного изобретения, мг - 1
Дистиллированная вода для инъекции, мл - 5
Всякий раз, когда требуется, инъекцию получают растворением соединения в дистиллированной воде.
ПРИМЕРЫ ИСПЫТАНИЙ
Ингибирующее действие на индуцированное веществом Р и гистамином сокращение выделенной подвздошной кишки морской свинки.
Соединение
Испытуемые соединения растворяли и разбавляли в 100% диметилсульфоксиде (ДМСО). Вещество Р (SP, Peninsula Laboratories или Peptide Institute) и дигидрохлорид гистамина (Wako Pure Chemicals) растворяли и разбавляли дистиллированной водой. Содержание ДМСО в ванне для органа не превышало 0,25% об. /об.
Способы
Самцов морских свинок Hartley (300-400 г) умерщвляли ударом в голову. Удаляли подвздошную кишку и полоски подвздошной кишки (15-20 мм) суспендировали при напряжении 0,5 г в ванне для органа на 20 мл, содержащей модифицированный раствор Тироде, который выдерживали при 30oС и аэрировали смесью 95%O2+5%СО2. Ответные реакции регистрировали изотонически. Ткани уравновешивали в течение 15 мин и затем получали постоянные ответные реакции на гистамин (1 мкМ). Затем получали индуцированное веществом Р (0,01 мкМ) или гистамином (0,1 мкН) сокращение после 5 мин инкубирования с испытуемыми соединениями или без них. Сократительные ответные реакции на вещество Р или гистамин с испытуемым соединением выражали как процент сократительных реакций без испытуемого соединения. IC50 было концентрацией испытуемого соединения, требуемой для предотвращения 50% сократительной ответной реакции, вызванной веществом Р или гистамином. Номера соединений испытуемых соединений соответствуют номерам примеров получения (см. табл.3)
Промышленная применимость
Соединения данного изобретения проявляют антагонистическую активность против, вещества Р и их можно использовать в качестве антиаллергических средств.
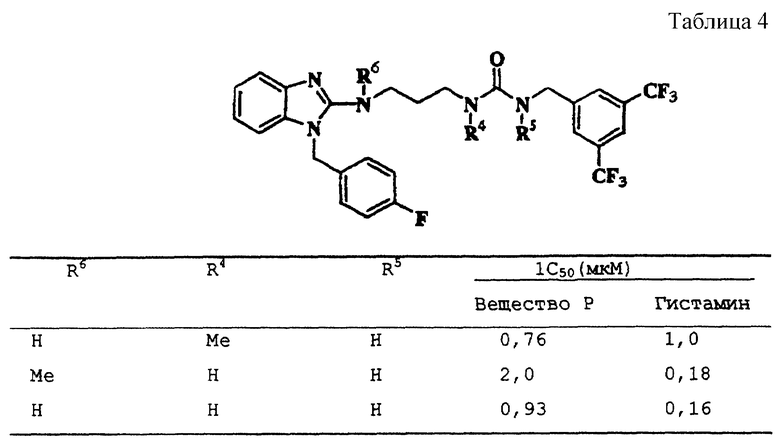
Пример получения
Пример 14 (см. табл.4)
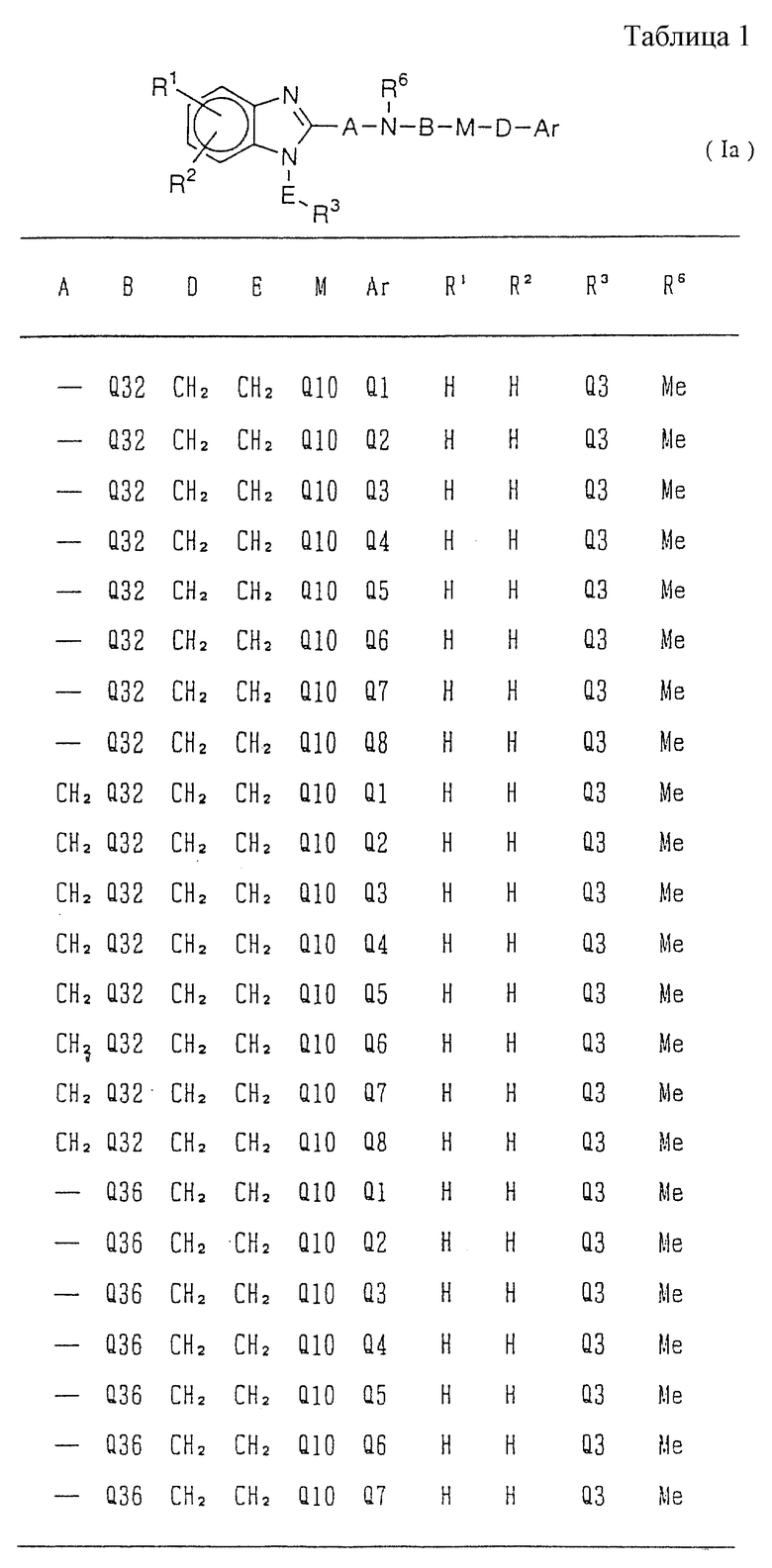



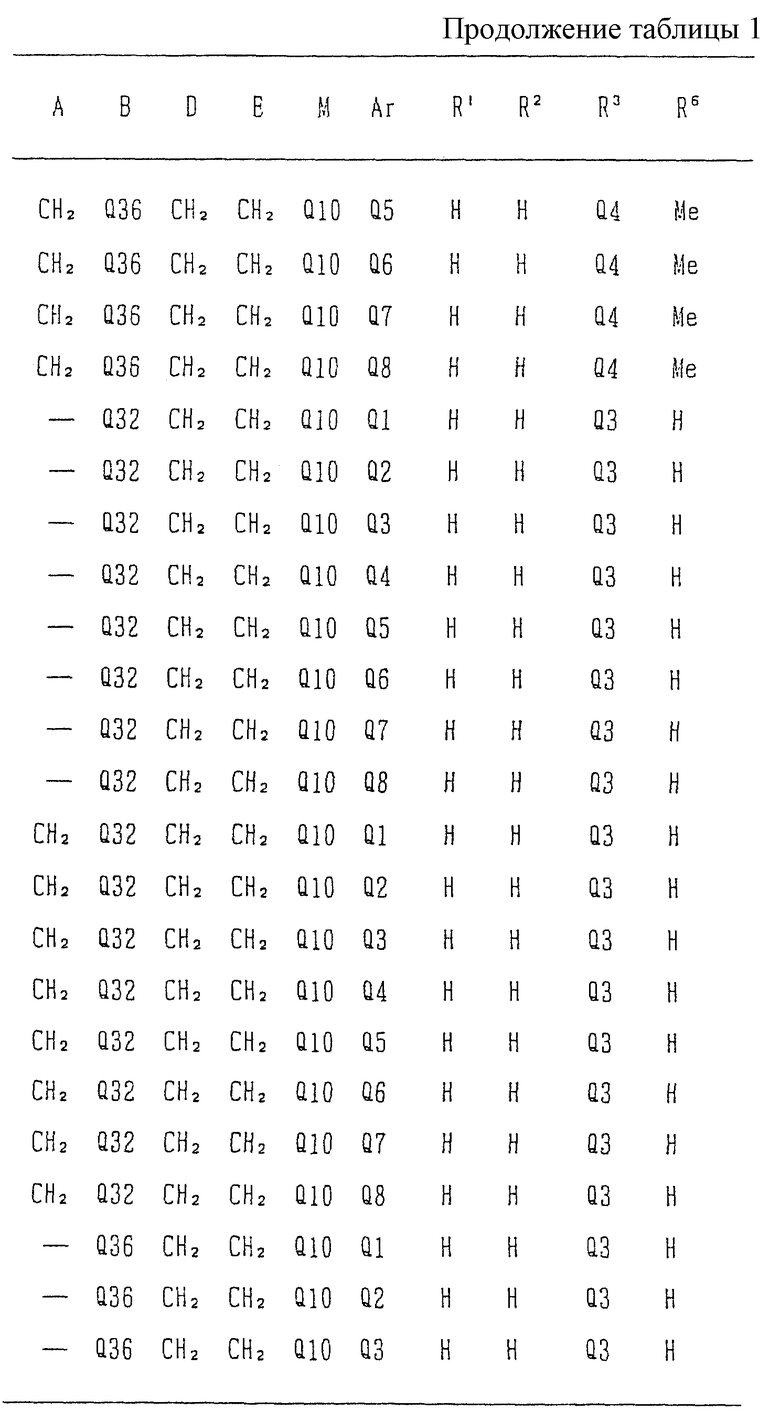
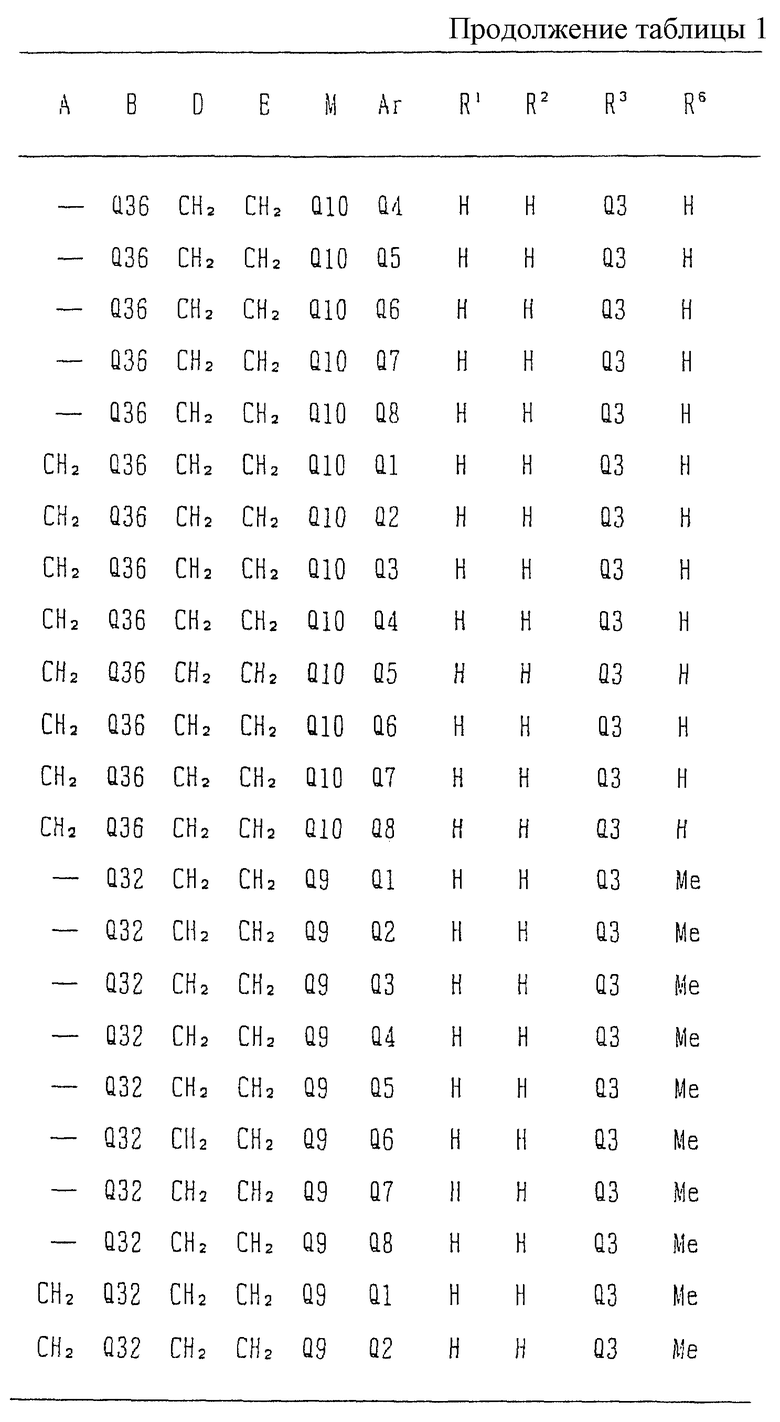
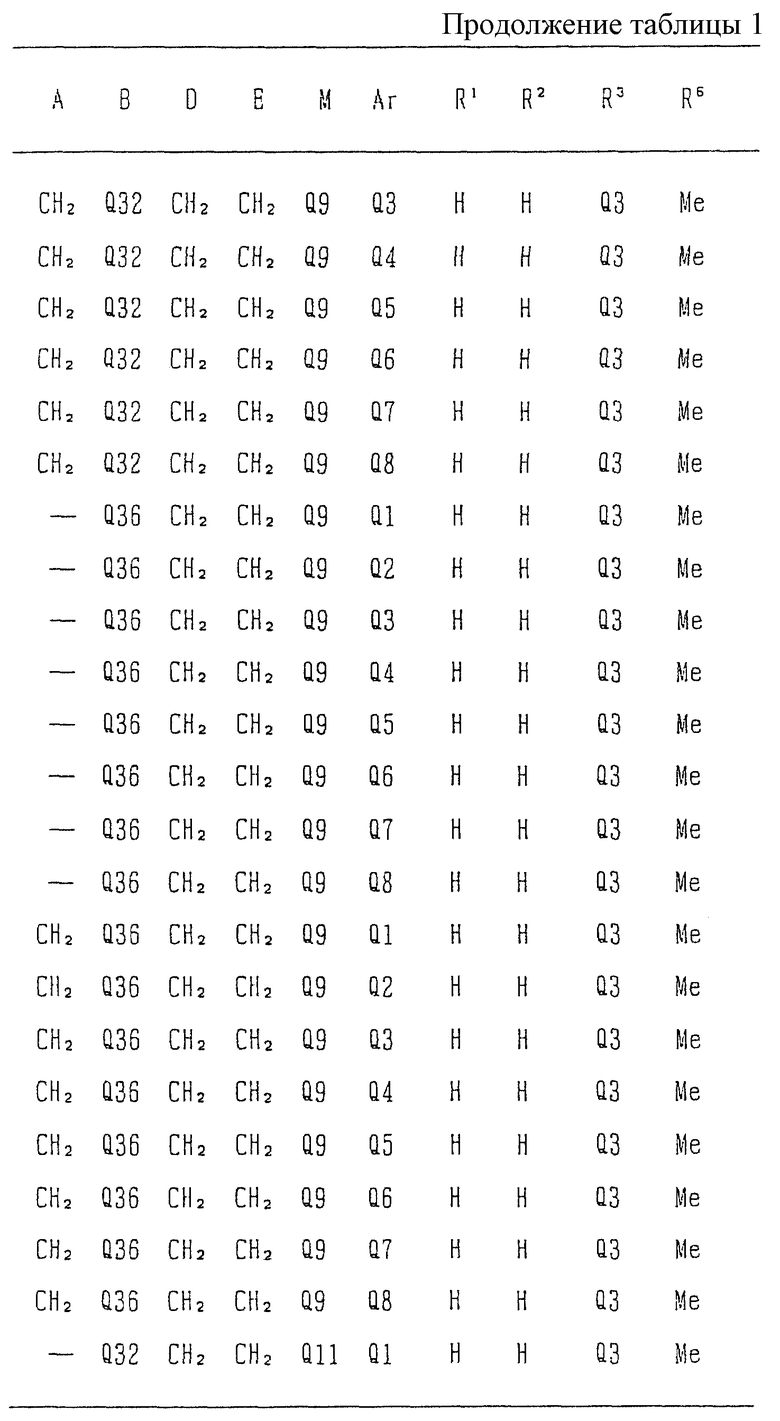
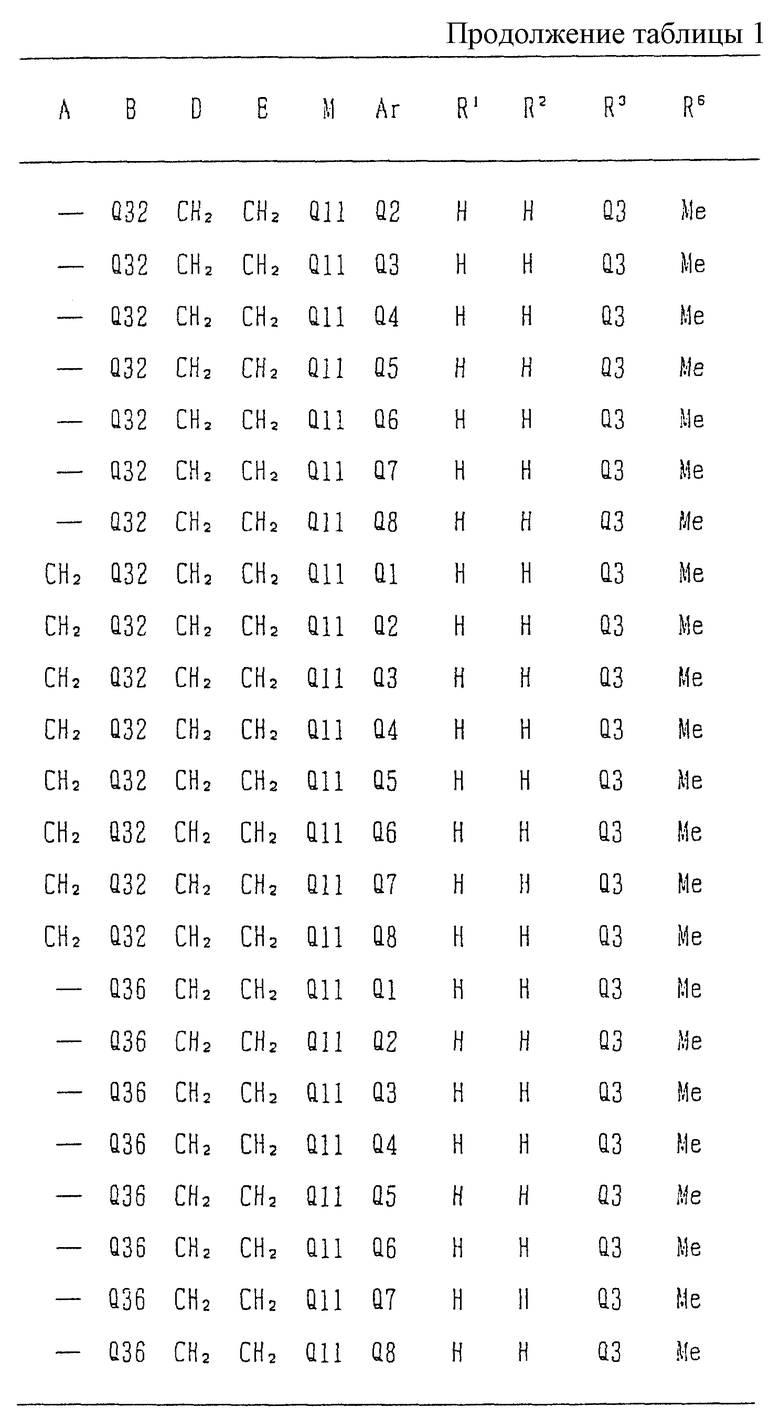
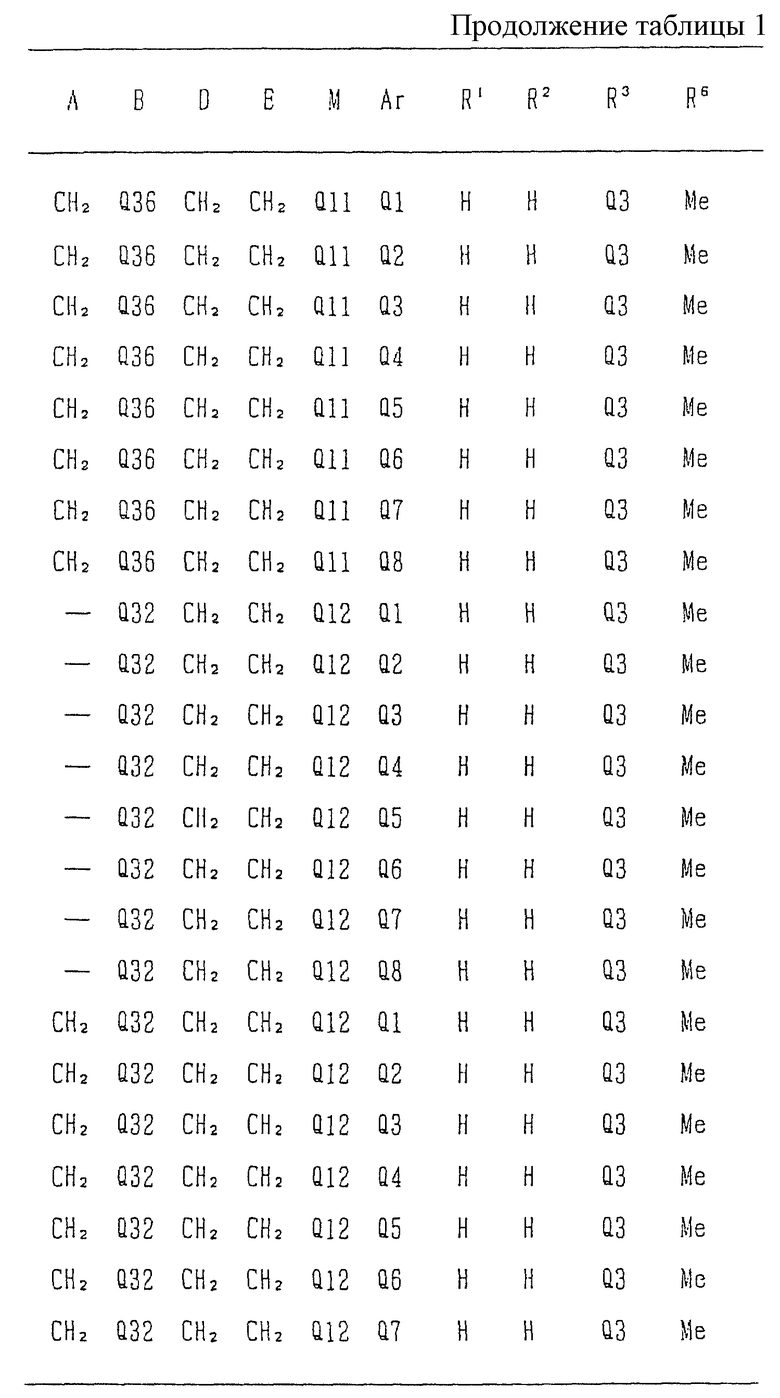
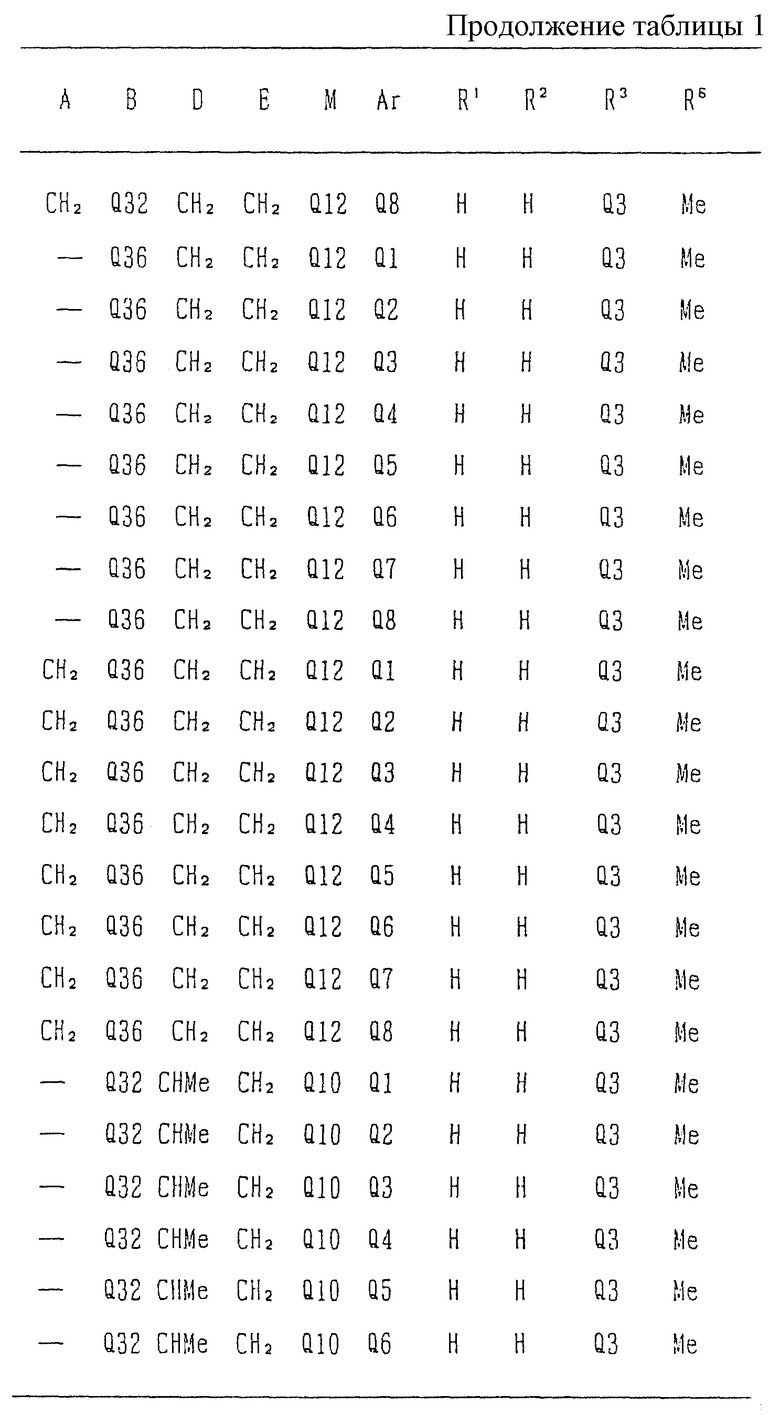
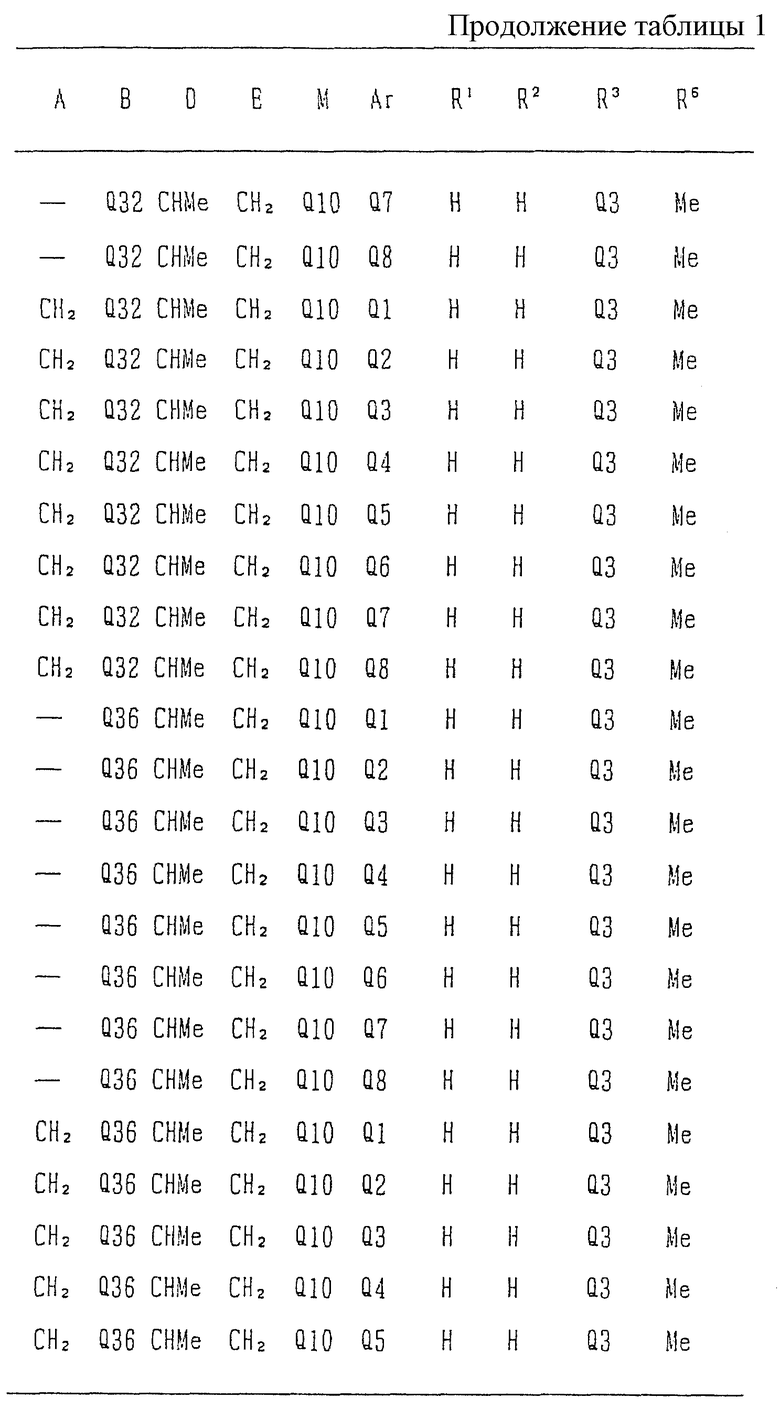
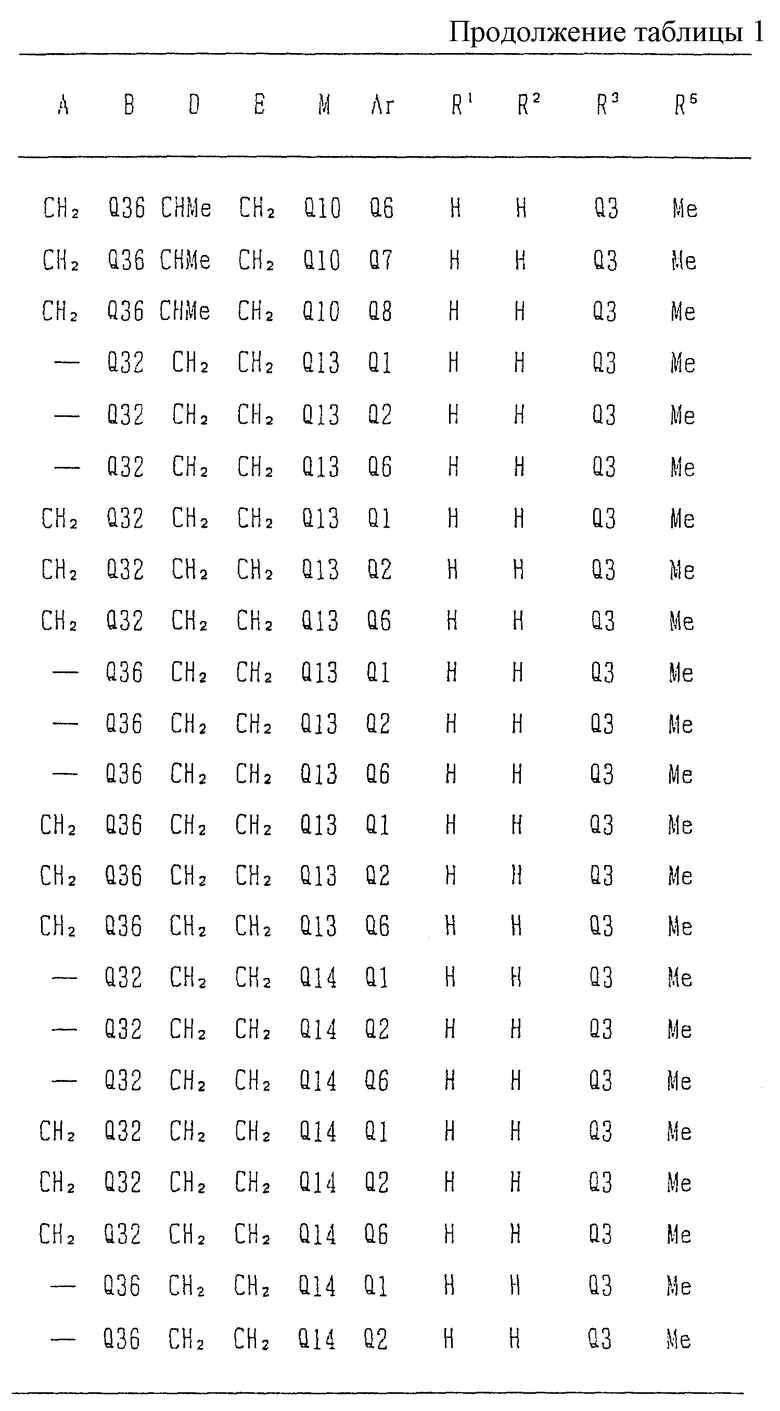

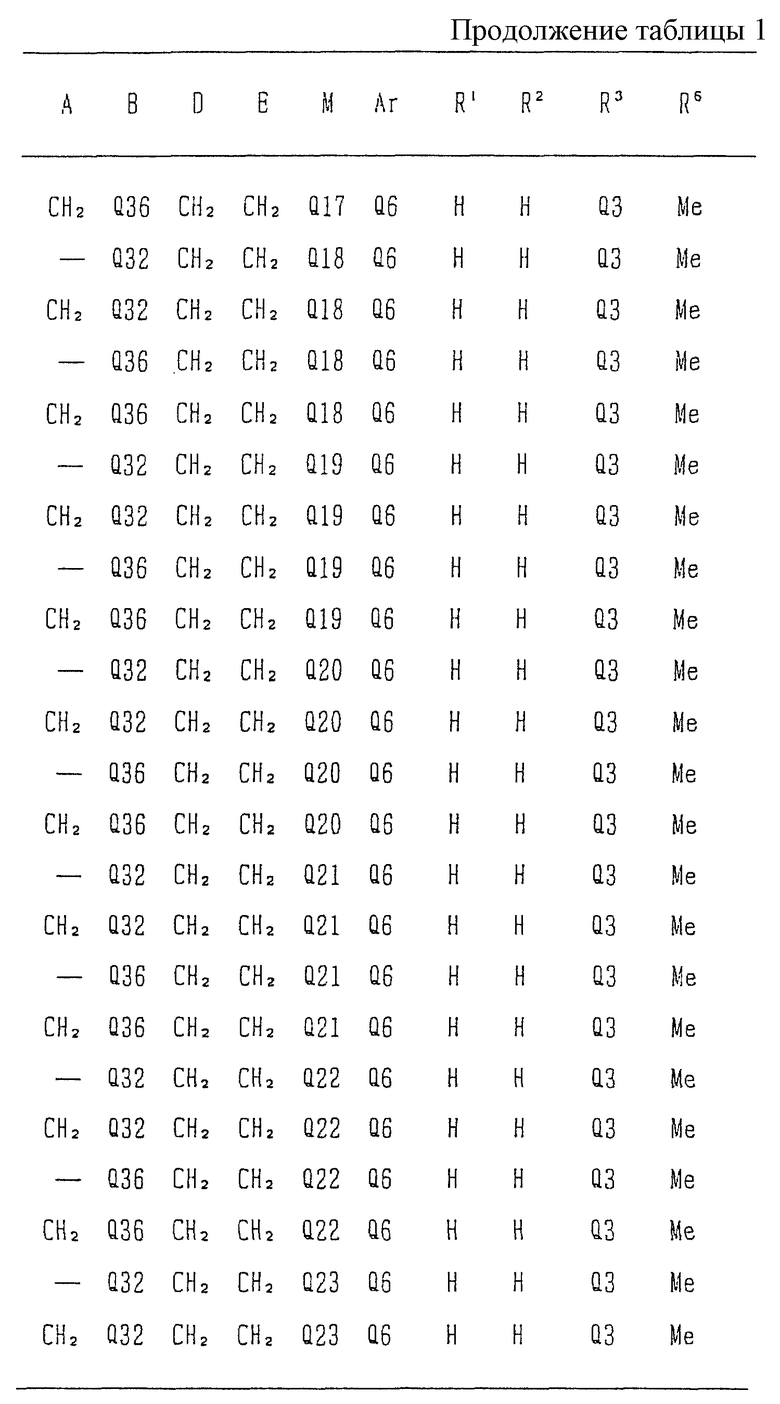
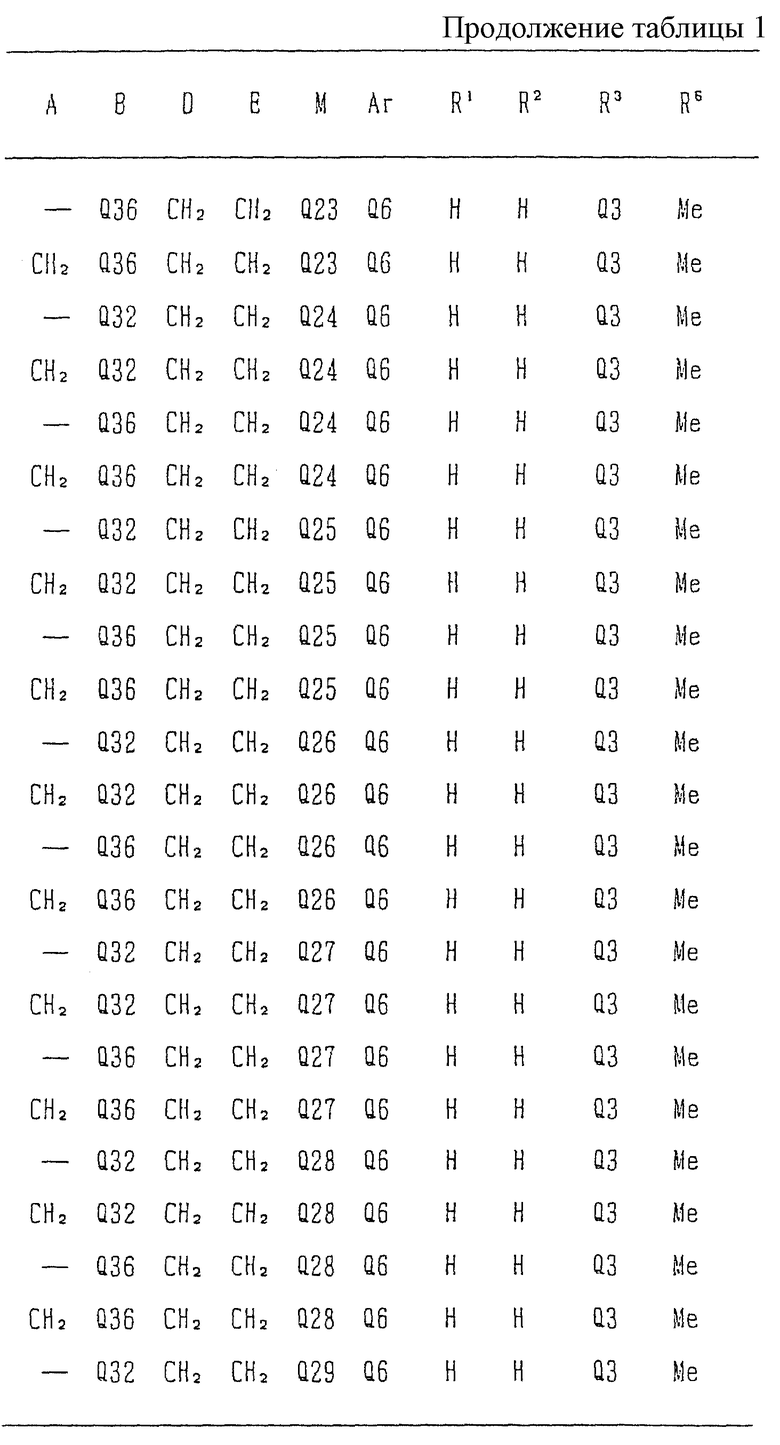
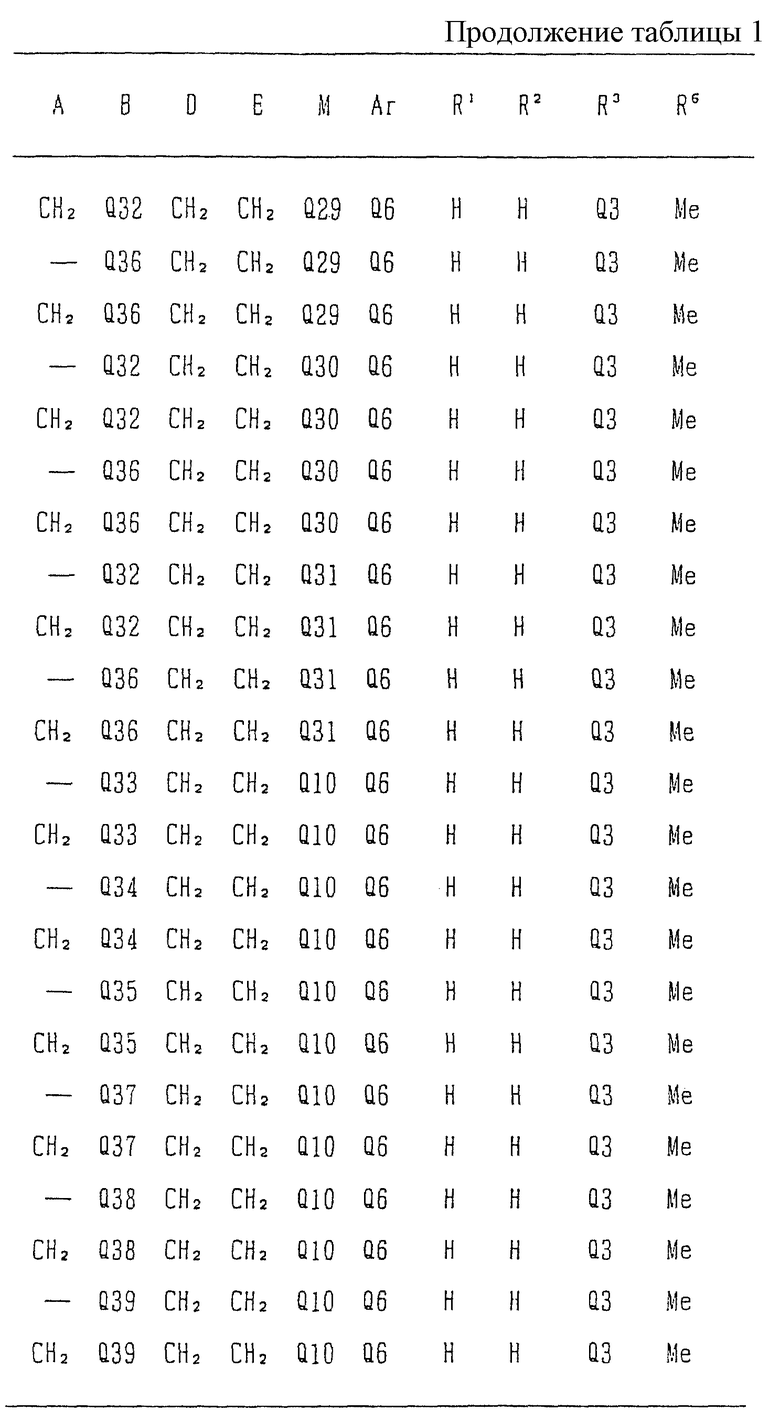
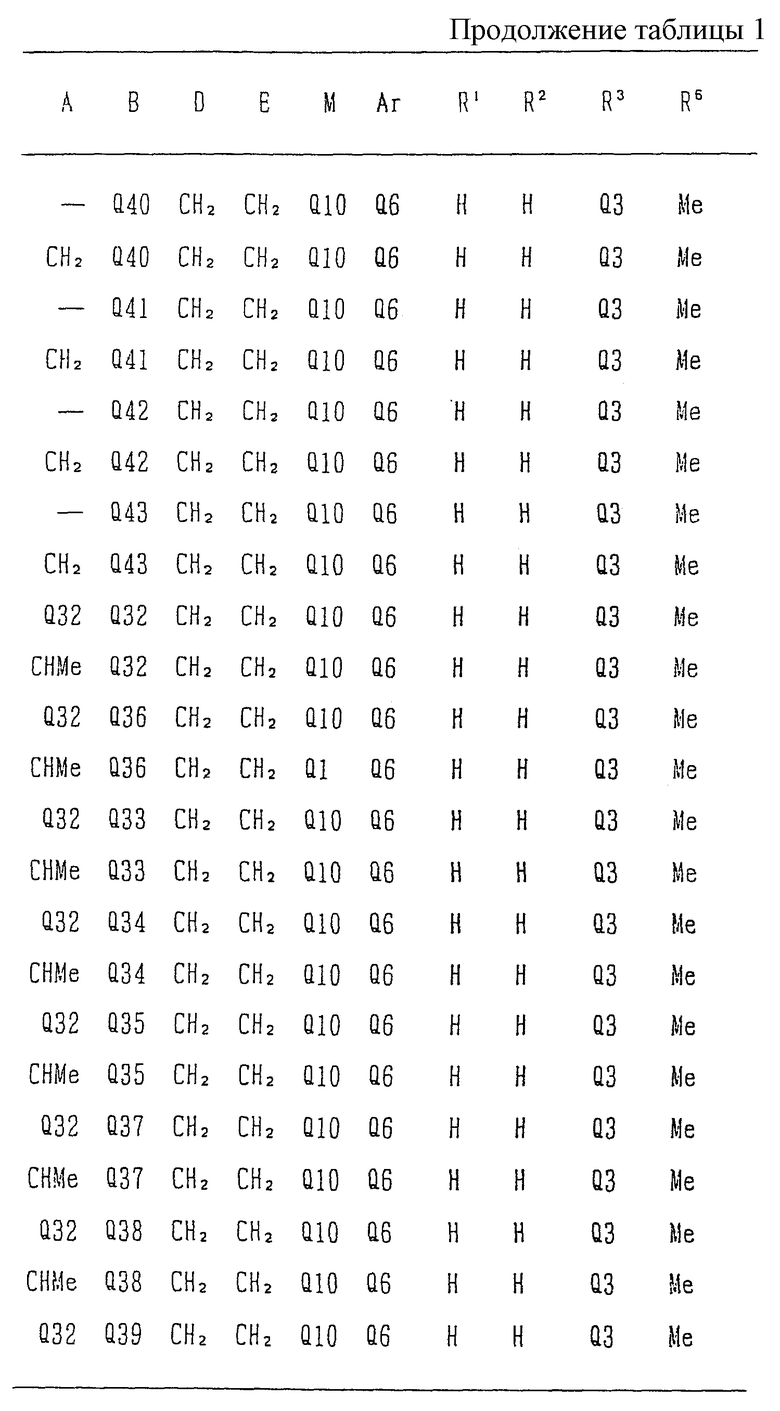
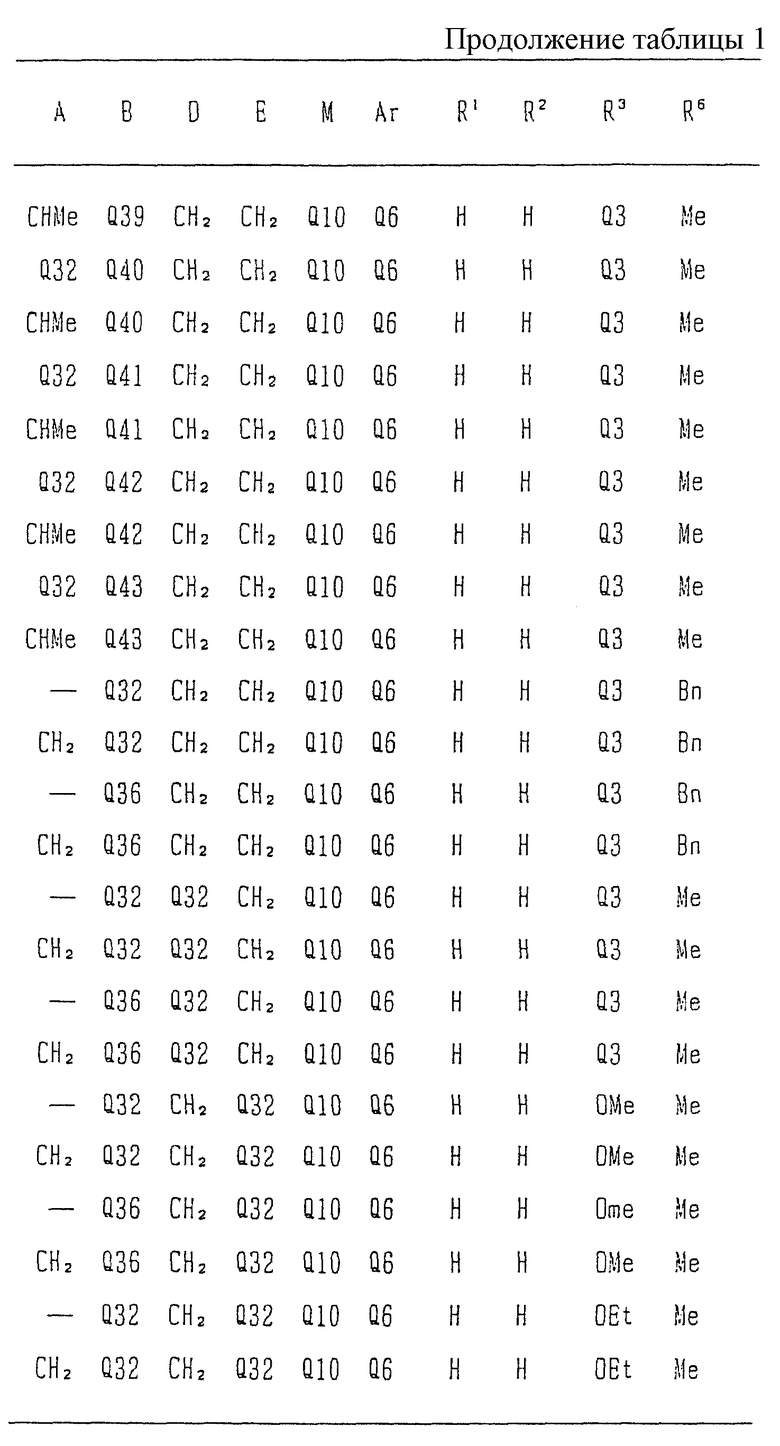



Изобретение относится к новому производному бензимидазола формулы (I), где А представляет одинарную связь или C1-2-алкиленовую группу; R6 - атом водорода или С1-4-алкильную группу; В - С2-3-алкиленовую группу; Х представляет атом кислорода, каждый из R1 и R2 - атом водорода; Е - C1-2-алкиленовую группу; R3 - фенильную группу (эта фенильная группа может быть необязательно замещена атомом галогена), каждый из R4 и R5, которые не зависят друг от друга, представляет атом водорода или С1-4-алкильную группу; D - C1-2-алкиленовую группу и Ar - фенильную группу (эта фенильная группа может быть необязательно замещена атомом галогена, C1-4-алкильной группой, C1-4-алкоксигруппой или трифторметильной группой). Также описывается средство, обладающее антагонистической активностью против вещества Р и антигистаминовой активностью. Изобретение может быть использовано в области химии и медицины. 2 с. и 4 з.п. ф-лы, 4 табл.
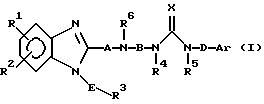
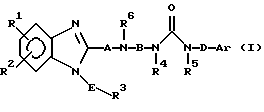
или его соль,
где А представляет одинарную связь или C1-2-алкиленовую группу;
R6 - атом водорода или C1-4-алкильную группу;
В - С2-3-алкиленовую группу;
Х - атом кислорода;
каждый из R1 и R2 - атом водорода;
Е - C1-2-алкиленовую группу;
R3 - фенильную группу (эта фенильная группа может быть необязательно замещена атомом галогена);
каждый из R4 и R5, которые не зависят друг от друга, представляет атом водорода или C1-4-алкильную группу;
D - C1-2-алкиленовую группу,
Ar - фенильную группу (эта фенильная группа может быть необязательно замещена атомом галогена, C1-4-алкильной группой, C1-4-алкоксигруппой или трифторметильной группой).
Приоритет по признакам
01.05.1997 по п. 1;
06.03.1998 по п. 1 (включая Ar представляет фенильную группу (эта фенильная группа может быть необязательно замещена атомом галогена, C1-4-алкильной группой, C1-4-алкокси группой).
| JP 9124609 А, 13.05.1997 | |||
| ПРОИЗВОДНЫЕ 5-(2-ИМИДАЗОЛИНИЛАМИНО)БЕНЗИМИДАЗОЛА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1994 |
|
RU2143430C1 |
| Петлеустановочное устройство | 1961 |
|
SU144101A1 |
| US 3962256 А, 08.06.1976. | |||
Авторы
Даты
2002-09-10—Публикация
1998-04-30—Подача