Изобретение относится к масс-спектрометру для макромолекул.
Ранее в масс-спектрометрии успешно использовалась различная техника для испарения и ионизации биологических макромолекул: бомбардировка быстрыми атомами (FAB) [1] , ионизация пучками электрических частиц (ESI) [2, 3] и лазерная десорбция/ионизация кристаллической решетки (MALDI) [4-7]. В способе MALDI макромолекулы с низким уровнем концентрации внедряются в кристаллическую решетку материала с высокой фотонной абсорбцией. Когда происходит воздействие лазером высокой интенсивности, кристаллическая решетка быстро нагревается и превращается в плазму. В процессе испарения импульс передается к макромолекулам, которые впоследствии ионизируются в плазме. Поскольку плазма в кристаллической решетке остывает быстро, большинство макромолекул остаются целыми. Ранее в масс-спектрометрах масса этих ионизированных макромолекул определялась методом измерения времени пролета (TOF) [3, 7, 8] , методом Фурье - преобразования ионно-циклотронного резонанса (FT-ICR) [2, 5, 6], а также с помощью одно- или мультиквадрупольного метода фильтрации масс [9, 10].
Недостатком имеющихся детекторов ионизированных частиц, используемых в масс-спектрометрии макромолекул, является сильное уменьшение эффективности ионизации для крупных макромолекул из-за уменьшения скорости частиц [11, 12] . В имеющихся детекторах для масс-спектрометрии ускоренная макромолекула испускает электрон в момент соударения с детектором, который впоследствии усиливается при помощи электронного умножителя. Эффективность эмиссии вышеуказанного электрона зависит от скорости воздействующей частицы, которая мала для крупных макромолекул. Этот недостаток эффективности детектора может компенсироваться в масс-спектрометрах при помощи увеличения потока макромолекул, однако ценой уменьшения общей чувствительности системы. Обычно в вышеуказанных масс-спектрометрах обнаружение макромолекул с массой, большей чем 50000 А.Е.М., неэффективно. С помощью FT-ICR техники можно обнаруживать значительно большие массы, хотя ценой большего времени интеграции порядка одной секунды, исключая приложения, где требуется высокая производительность.
Масс-спектрометрия используется в биологии при конструировании и определения белков при помощи измерения распределения массы белковых фрагментов [9, 13]. Масс-спектроскопия считается перспективной техникой для увеличения скорости и уменьшения стоимости конструирования молекул ДНК [2, 3, 5-8, 14]. Стандартной процедурой конструирования ДНК-последовательности является разделение кратных частей ДНК-фрагментов, приготовляемых согласно стратегии Maxam-Gilbert и Sanger, используя импульсный электрофорез геля [15, 16]. При такой технике ДНК-фрагменты разделяются по их длинам согласно их свойствам перемещаться в геле, к которому приложено электрическое поле. Пространственно разделенные полосы ДНК-фрагментов обычно записываются авторадиографической и флюоресцентной техникой.
Недостатком вышеизложенной техники электрофореза геля являются медленный темп упорядочения и слабое разрешение для очень больших ДНК-фрагментов. Недостатком масс-спектрометров для высокого темпа ДНК-упорядочения является низкая чувствительность ионизационного детектора ДНК-фрагментов, состоящих из более чем 100 оснований, делая недоступным увеличение темпа ДНК-упорядочения, которое возможно в масс-спектрометрии.
Краткое изложение изобретения
Предметом изобретения является масс-спектрометр для крупных макромолекул.
Далее предметом изобретения является прибор для измерения массы макромолекул с эффективным обнаружением независимой массы, т.е. позволяющий также измерять макромолекулы с очень большой массой.
Далее предметом изобретения является прибор для измерения массы макромолекул с эффективным обнаружением независимой массы, т.е. позволяющий также измерять макромолекулы в режиме подсчета единичной частицы.
Далее предметом изобретения является прибор для измерения массы макромолекул с детекторной системой, имеющей как высокое временное, так и пространственное разрешение.
Далее предметом изобретения является прибор, имеющий высокую производительность и высокую чувствительность к основной последовательности коротких и длинных ДНК-фрагментов.
Далее предметом изобретения является прибор, имеющий высокую производительность и высокую чувствительность к аминокислоте и малым и большим белкам.
Далее предметом изобретения является прибор, имеющий высокую производительность и высокую чувствительность определения малых и больших белков.
Далее предметом изобретения является прибор, имеющий высокую производительность и высокую чувствительность определения малых и больших полимеров.
Перечисленные возможности достигаются благодаря использованию фонон-чувствительного криогенного детектора частиц. В криогенном детекторе частиц поглощаемая кинетическая энергия ускоренных макромолекул преобразовывается в фононы (т. е. вибрация решетки детектора), которые преобразуются в электрические сигналы при помощи фононных сенсоров. Вышеуказанный фононный сенсор чувствителен только при криогенных температурах (т.е. температурах нескольких градусов Кельвина), где фон термических фононов незначителен.
В соответствии с вышеизложенным и в дальнейшем предметом изобретения является одна из реализации прибора - масс-спектрометр для определения времени полета частиц, когда макромолекулы разделяются по зависящей от массы скорости, которая пропорциональна квадратному корню из m, где m обозначает массу макромолекулы. Для одного времени эмиссии более тяжелые макромолекулы достигают детектора позднее, чем более легкие макромолекулы. Вышеуказанные криогенные детекторы частиц определяют время поступления макромолекулы на детектор в режиме подсчета одиночной частицы. Кинетическая энергия всех ускоренных макромолекул одинакова.
В другой реализации единичные или мультиквадропульные масс-спектрометры разделяют и анализируют массу макромолекул при помощи квадропульного метода фильтрации, при котором криогенный детектор частиц измеряет появившиеся макромолекулы. При такой реализации требуется очень малое количество макромолекул, т. к. используется вышеуказанный криогенный детектор частиц в режиме подсчета одиночной частицы.
В другой реализации макромолекулы пространственно разделяются при помощи постоянного магнитного поля в соответствии с их коэффициентом отношения массы к заряду, последовательно ускоряются и затем определяются детектором криогенных частиц.
В другой реализации макромолекулы десорбируются в порядке следования импульсов, пространственно разделяются при помощи постоянного магнитного поля в соответствии с их коэффициентом отношения массы к заряду, последовательно ускоряются и затем определяются детектором криогенных частиц с пространственным и временным разрешением. Исходя из пространственной и временной информации о макромолекуле и знания структуры эмиссии, время эмиссии макромолекулы может быть восстановлено и определена масса на основании времени полета частиц. Это приводит к параллельным действиям масс-спектрометра с высокой чувствительностью и производительностью.
В соответствии с вышеизложенным и в дальнейшем предметом изобретения является одна из реализаций криогенного детектора частиц, использующего кристаллическую подложку как абсорбентов, так и сверхпроводящие туннельные переходы, действующие в Giaever-режиме, фононных сенсоров. В другой реализации вышеуказанного криогенного детектора частиц, сверхпроводимость туннельных переходов Giaever-типа используется как в абсорбентах, так и в фононных сенсорах.
В другой реализации вышеуказанного криогенного детектора частиц фононная чувствительность туннельных переходов Giaever-типа расширяется при помощи осаждения сверхпроводящего туннельного перехода на поверхность большой области сверхпроводящей пленки, которая имеет сверхпроводящий энергетический промежуток, больший, чем соответствующая пленка, для того чтобы использовать эффект ловушки квазичастиц.
В другой реализации вышеуказанного криогенного детектора частиц кристаллический поглотитель покрывается сверхпроводником по краям фононных сенсоров.
В другой реализации вышеуказанного криогенного детектора частиц используются микрокаллориметры, состоящие из кристаллического поглотителя с низкой теплоемкостью и высокой терморезисторной чувствительностью, как фононный сенсор.
В другой реализации вышеуказанного криогенного детектора частиц используются микрокаллориметры, состоящие из кристаллического поглотителя с низкой теплоемкостью и высокочувствительными кинетическими термометрами в качестве фононных сенсоров.
В другой реализации вышеуказанного криогенного детектора частиц используются микрокаллориметры, где кристаллический поглотитель и термический фононный сенсор идентичны.
В другой реализации вышеуказанного криогенного детектора частиц кристаллический поглотитель покрывается сверхпроводниковыми гранулами, которые при сверхнизких температурах используются как фононные сенсоры.
В другой реализации вышеуказанного криогенного детектора частиц кристаллический поглотитель покрывается сверхпроводниковыми гранулами, которые используются как поглотители и фононные сенсоры.
Из вышеизложенного можно понять, что масс-спектрометр, являющийся предметом изобретения, имеет несколько преимуществ:
1) он позволяет определять массу макромолекулы независимо от ее массы, т.е. также очень крупных макромолекул;
2) позволяет определять массу макромолекулы в режиме подсчета одиночной частицы, т.е. включая очень высокую чувствительность;
3) тонко-пленочную технологию для производства фононных сенсоров, принимая во внимание высокое пространственное разрешение криогенного детектора, т. е. высокая производительность возможна за счет пространственного разделения макромолекулярных потоков и производства параллельных во времени измерений;
4) чувствительность и производительность определения ДНК-последовательностей может быть улучшена на несколько порядков;
5) чувствительность и производительность определения белковых последовательностей может быть улучшена на несколько порядков;
6) чувствительность и производительность определения белков может быть улучшена на несколько порядков;
7) чувствительность и производительность определения полимеров может быть улучшена на несколько порядков.
Краткое описание чертежей
В соответствии с вышеизложенным и в дальнейшем предмет изобретения будет пониматься и детально описываться со ссылками на сопутствующие чертежи, на которых
на фиг.1 показано схематическое представление фононного криогенного детектора частиц;
на фиг. 2 схематически представлена электрическая схема фононного криогенного детектора частиц по фиг.1;
на фиг.3 схематически представлено изобретение, использующее одноканальный криогенный детектор частиц, такой же, как в MULDI-TOF масс-спектрометре;
на фиг.4 - схематическое представление механической заслонки (прерывателя) как в MULDI-TOF масс-спектрометре по фиг.3;
на фиг. 5 - синхронизация лазерного тригера и механической заслонки (прерывателя) по фиг.4;
на фиг. 6 - синхронизация в случае трех макромолекул для реализации, представленной на фиг.3 и 4;
на фиг.7 - схематическое представление пространственной области криогенного детектора частиц, в которой макромолекулы поглощаются непосредственно фононным сенсором;
на фиг.8 схематически представлена альтернативная реализация криогенного детектора частиц, в котором макромолекулы поглощаются подложкой и опосредованно влияют на сенсор;
на фиг.9 схематически представлена альтернативная фиг.8 реализация криогенного детектора частиц, в котором фононный сенсор представляет из себя улавливающий слой как сверхпроводящий туннельный переход;
на фиг.10 представлены расчетные траектории макромолекул различной массы при альтернативной реализации с использованием многоэлементного криогенного детектора;
на фиг. 11 схематически представлен масс-спектрометр, который обеспечивает траектории макромолекул, изображенные на фиг.10; разделение макромолекул по массе происходит под действием постоянного магнитного поля и определяется с использованием многоэлементного криогенного детектора;
на фиг. 12 представлены результаты расчета, иллюстрирующие зависимость мощности пространственного разрешения от ускоряющего напряжения для реализации на фиг.11;
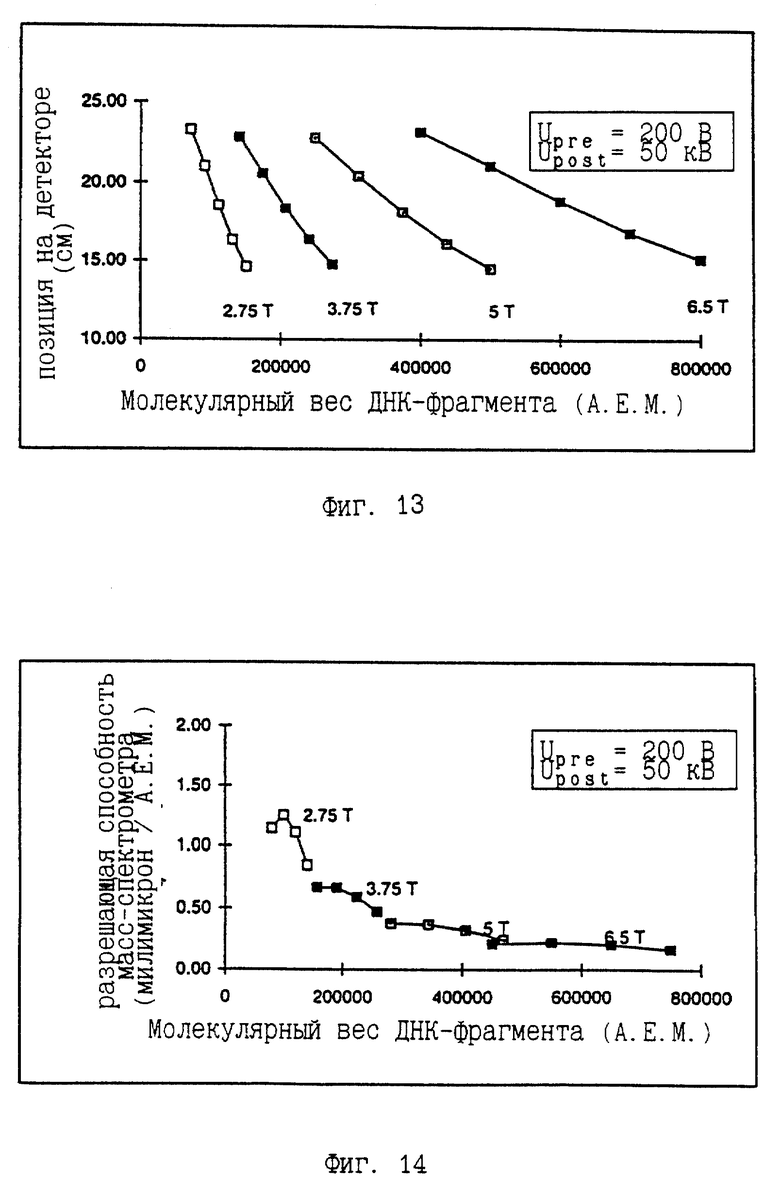
на фиг. 13 представлены результаты расчета, иллюстрирующие зависимость пространственного разделения массы от молекулярного веса макромолекул по фиг.11;
на фиг. 14 представлены результаты расчета, иллюстрирующие зависимость разрешающей способности при разделении массы от молекулярного веса макромолекул по фиг.11;
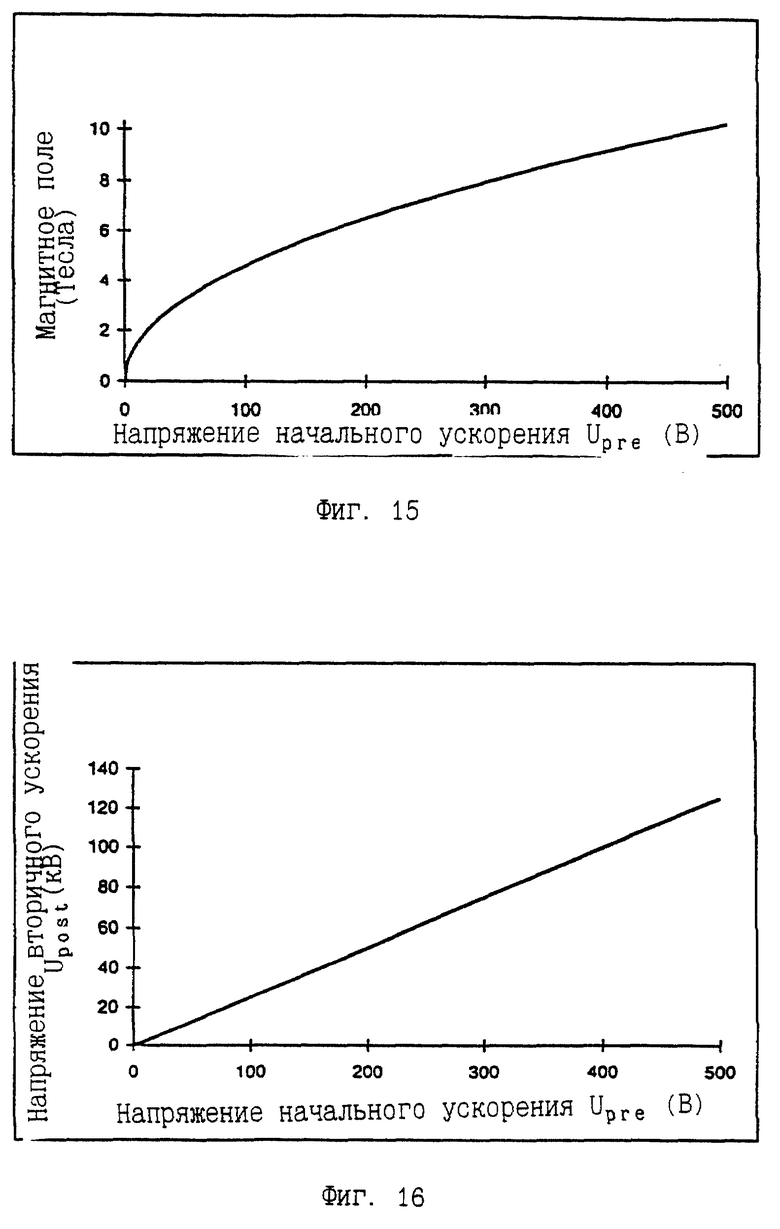
на фиг. 15 представлены результаты расчета, иллюстрирующие зависимость напряженности магнитного поля от ускоряющего напряжения для определения макромолекул, согласно воплощению по фиг.11 в соответствии с различием по массам по фиг.10;
на фиг. 16 представлены результаты расчета, иллюстрирующие зависимость пост-ускоряющего напряжения от начального ускоряющего напряжения для определения макромолекул по фиг.11 и согласно фиг.10;
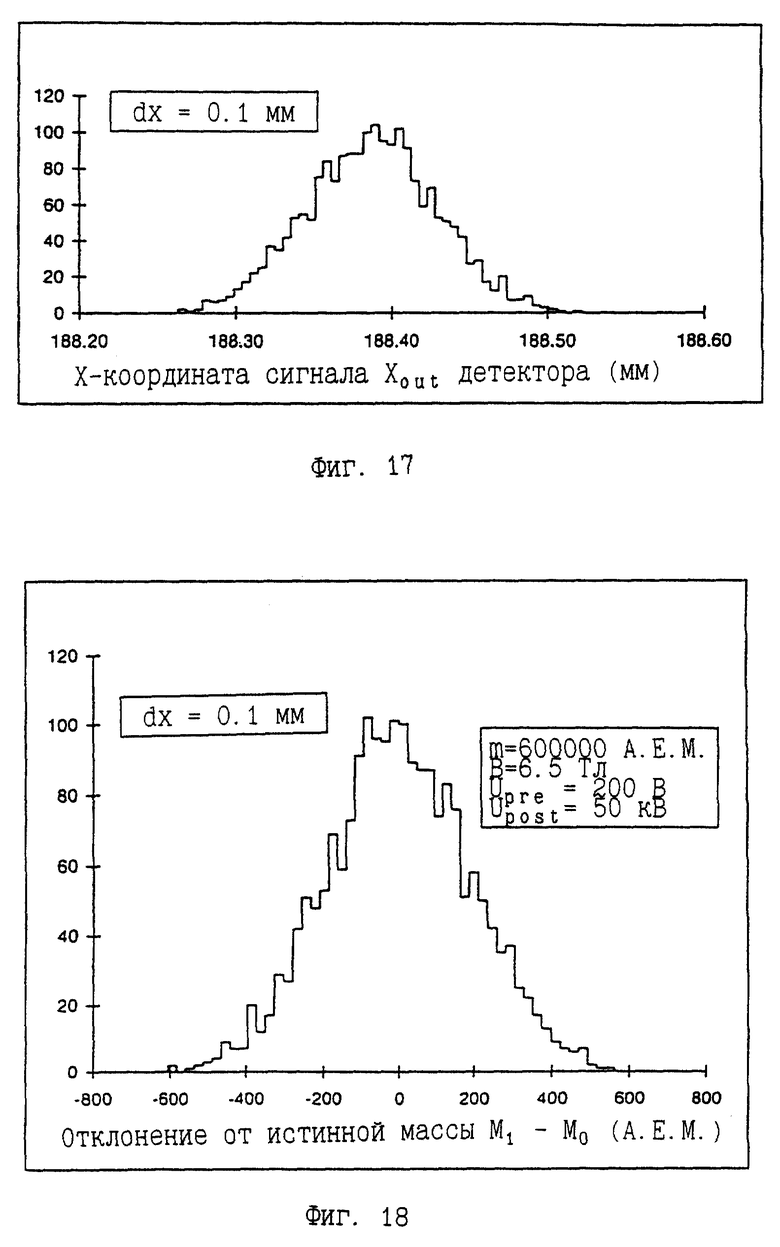
на фиг.17 представлены результаты расчета, по методу Монте-Карло иллюстрирующие разрешающую способность предлагаемого оборудования по фиг.7, 8 или 9, использованные в воплощении по фиг.11;
на фиг.18 представлены результаты расчета, по методу Монте-Карло иллюстрирующие разрешающую способность при определении массы, как определено по фиг.17;
на фиг.19 - импульсный режим работы, воплощение по фиг.11;
на фиг.20 представлены результаты расчета, по методу Монте-Карло иллюстрирующие время пробега частиц, по воплощениям, изображенным на фиг.7, 8 или 9, использующие воплощение по фиг.11;
на фиг.21 представлены результаты расчета, по методу Монте-Карло иллюстрирующие возможность определения массы частиц с учетом фиг.20;
на фиг. 22 представлены результаты расчета, иллюстрирующие зависимость эффективности определения массы частиц в зависимости от импульсного режима эмиссии, показанного на фиг.19 и 11;
на фиг. 23 представлены результаты расчета, иллюстрирующие зависимость эффективности определения массы частиц с помощью пространственного криогенного детектора, показанного на фиг.11;
на фиг. 24 представлены результаты расчета, иллюстрирующие зависимость эффективности определения массы частиц при использовании импульсного режима эмиссии, представленного на фиг.19;
на фиг.25 схематически представлен образец, используемый для определения ДНК-последовательности в масс-спектрометре, изображенном на фиг.11.
Детальное описание
Схема криогенного детектора частиц, представленная на фиг.1, содержит поглотитель частиц, обозначенный цифрой 1, на котором размещается детектор фононов 2. В реализации, представленной на фиг.1, этот датчик фононов представляет из себя сверхпроводящий туннельный переход, состоящий из верхнего слоя 3 толщиной около 100 нм, разделительной оксидной прослойки 4 в несколько нм и нижнего слоя 5 толщиной около 100 нм. Сверхпроводящий туннельный переход хорошо известен, как фотонный детектор q-частиц и рентгеновских лучей [17-20]. Имеются другие реализации криогенного фононного детектора [19]: сверхпроводящие переходные термометры, близкие к полупроводниковым термисторам, закрывающимся при критической температуре Тc, сверхпроводящие кинетические индукционные термометры и сверхпроводящие перегреваемые гранульные и точечные. В основном требуется, чтобы фононные сенсоры были чувствительны к энергии воздействия около 10 Кэв и времени воздействия не более 100 нсек. Криогенные детекторы частиц работают при температурах нескольких градусов Кельвина, где фон термически возбужденных фононов пренебрежимо мал. Принцип действия фонон-чувствительного криогенного детектора частиц в масс-спектрометрии макромолекул следующий (см. на фиг.1.). Макромолекула 6, которая ускоряется до кинетической энергии порядка 10 Кэв за счет электрического поля масс-спектрометра, порождает фононы 7. Фононы проходят сквозь поглотитель частиц 1 и в конечном итоге преобразуются в фононном сенсоре в электрический сигнал. Чувствительность криогенных детекторов частиц к поглощаемым ионизированным частицам с энергией в несколько Кэв показана в [21] другими авторами [19] . Новизной предлагаемого изобретения является возможность использования криогенных детекторов частиц в масс-спектрометрии макромолекул. Криогенный детектор частиц, представленный на фиг.1, обладает уникальным свойством определять не только ионизированные частицы, но и определять с такой же или даже большей чувствительностью неионизированные частицы, передавая кинетическую энергию к кристаллической решетке поглотителя частиц. Эффективность захвата фононов увеличивается при внедрении в глубь подложки, к примеру, монокристалла кремния на глубину порядка 10 мкм, для того чтобы локализовать плотность фононов в окрестности фононного сенсора.
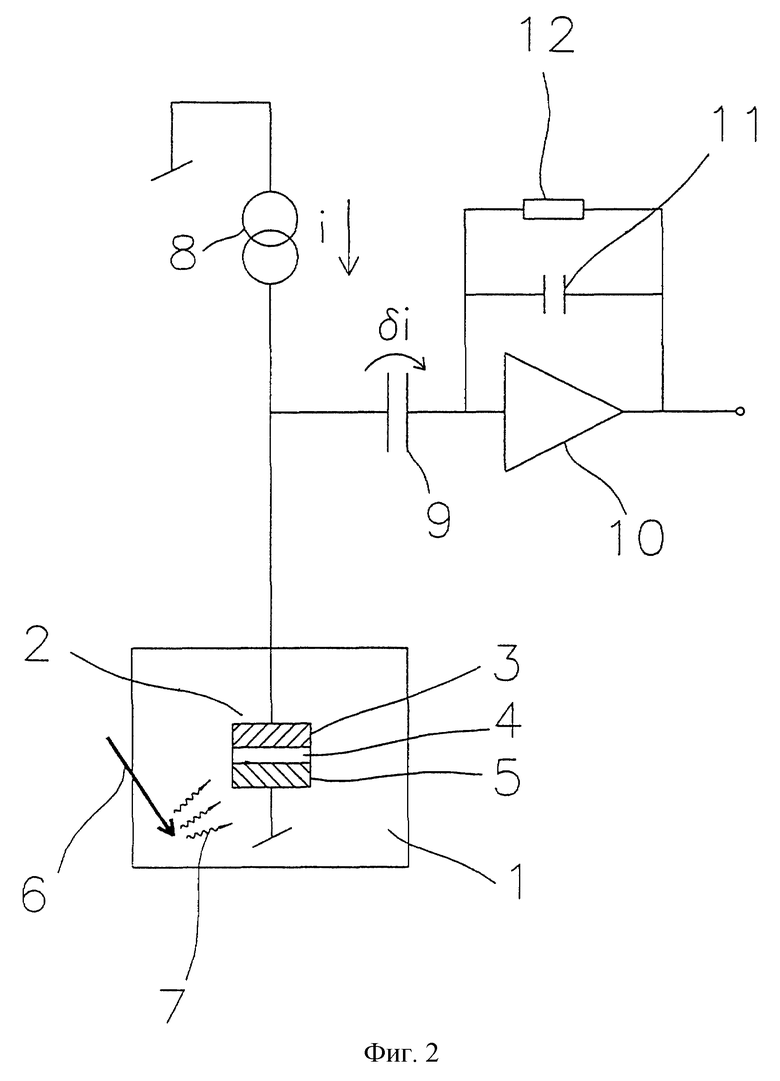
На фиг.2 показана электронная схема, в которой в качестве фононного сенсора использован сверхпроводящий туннельный переход. Фононы 7, возникшие за счет абсорбции макромолекул 6, распространяются сквозь абсорбер 1, в который входят сверхпроводящие слои 3 и 5. Фононы с энергией, большей, чем Cooper-пара, разбивают Cooper-пару и производят избыточные квазичастицы (электрический сигнал возбужденного состояния в сверхпроводнике). Два сверхпроводных слоя 3 и 5 находятся на разных энергетических уровнях, что приводит к изменению тока i, который поддерживается источником 8. Поток избыточных квазичастиц проходит через изолирующий слой 4. Так как фононы 7 и связанные с ними избыточные квазичастицы разрушаются за время порядка нескольких мксек, то поток избыточных квазичастиц di будет двигаться через конденсатор 9. С изменением чувствительности предусилителя, который состоит из операционного усилителя 10, конденсатора 11 и сопротивления 12, поток избыточных квазичастиц di интегрируется, и изменения будут пропорциональны числу фононов 7, абсорбированных детектором фононов 2. К сожалению, макромолекулы также могут быть абсорбированы детектором фононов и вызвать сигнал, который будет противоположен сигналу криогенного детектора фононов.
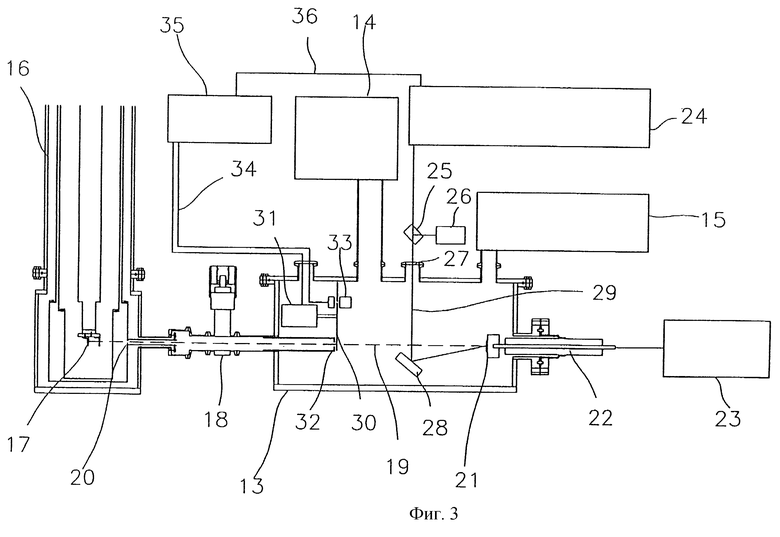
На фиг.3 показана реализация макромолекулярного масс-спектрометра с криогенным детектором частиц, использующим в основном технологию MALDI-TOF. В камере 13 турбонасосом системы 14 создается вакуум около 10-8 мБар, который контролируется вакуумной измерительной системой 15. Криостат 16 с криогенным детектором частиц 17 присоединен к холодной трубке, связанной с вакуумным приемником 13 через элемент 18. Поток макромолекул 19 проходит в вакуумном приемнике 13 холодную область, попадает в криостат 16 в виде серии небольших порций 20 в холодных областях криостата. Поток макромолекул 19 производится с помощью выбросов макромолекул из образца 21 за счет высоковольтного устройства 22, которое связано с высоковольтным источником мощности 23 и при помощи облучения лазерным потоком 29, исходящим из лазерного источника 24. Лазер может быть типа UV-лазер или инфракрасный лазер. Лазерный луч 29, выходящий от лазерного источника 24, разделяется с помощью делителя 25. Одна часть луча используется для измерения мощности лазера с помощью измерителя 26, а другая часть направляется в вакуумный приемник 13 через окно 27. В вакуумном приемнике лазерный луч 29 направляется на образец 21 с помощью зеркала 28. Проба содержит кристаллическую решетку светочувствительного кристаллораствора (например, цианистая кислота или -циано-4-гидрокси-цианистая кислота [12] ), в котором макромолекулы растворены в соотношении 104:1. Мощность лазера, обычно несколько МДж/нсек, поглощается решеткой, которая разрывается и разворачивается, превращаясь в электрическую плазму. Расширение атомной решетки передает импульс макромолекулам, которые испаряются и впоследствии заряжаются в зависимости от характеристик плазмы. Благодаря электрическому полю в вакуумном приемнике, для создания которого ток подается по высоковольтному щупу 22, макромолекулы заряжаются таким же зарядом, как и на щупе. Затем макромолекулы ускоряются в направлении к передающей трубке 32, в криостате 16 проходят охлаждающий клапан 20 и достигают криогенный детектор частиц 17. Разность по времени между запуском лазерного импульса и прибытием сигнала на криогенный детектор частиц характеризует массу макромолекулы. Так как криогенный детектор частиц - очень чувствительное устройство, то свет и остаточный поток макромолекул не должны попадать в криостат. Для предотвращения этого на входе передающей трубки 32 устанавливается механический заслон 30. В одной из реализаций заслона имеется мотор 31, который вращает диск с прорезью. Так же имеется световой диод, световая детекторная система 33 и электронная управляющая система 35, определяющая положение прорези и посылающая синхронизирующий сигнал 36 лазеру 24.
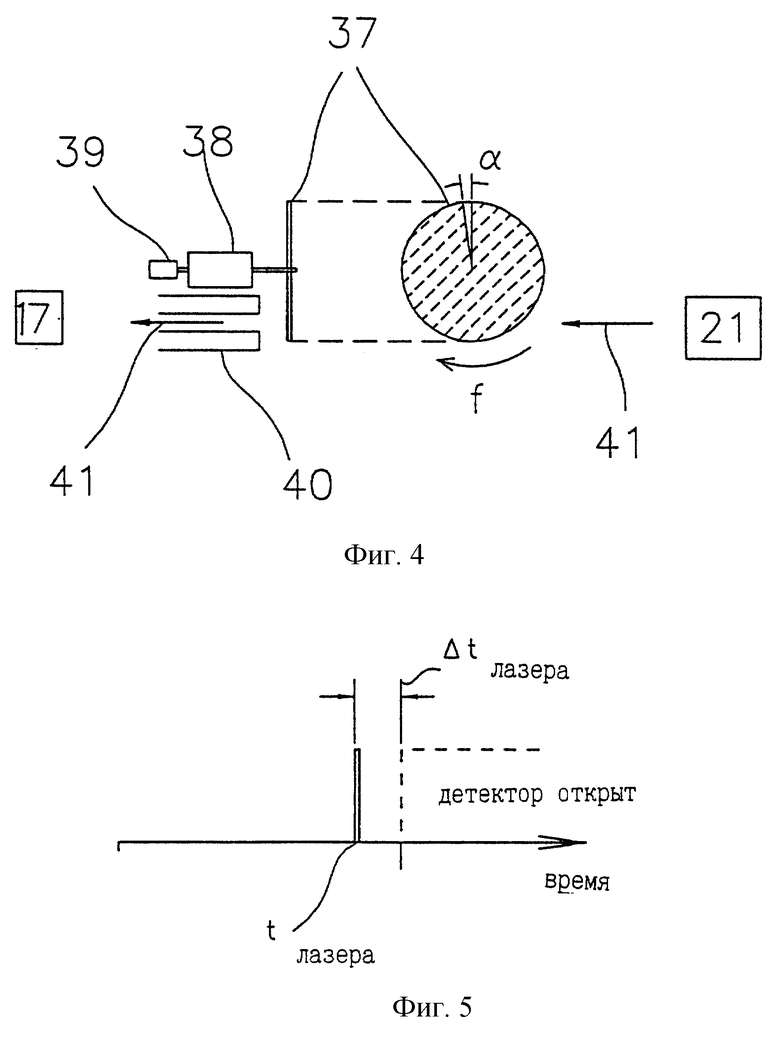
На фиг.4 представлена практическая реализация такого механического заслона: мотор 38 вращает диск 37 с прорезью на угол alfa (обычно 5-10o) и частотой вращения f (обычно 50-100 Гц). Положение вращающейся прорези контролируется преобразователем 39. Ускоренные макромолекулы 41 от источника 21 будут попадать в трубку 40, которая связывает вакуумный приемник с креостатом, только когда прорезь 37 находится напротив входа трубки. При правильно выбранной синхронизации работы лазера и заслона на криогенный детектор частиц 17 попадут только определенной величины макромолекулы. Как показано на фиг.5, электронная управляющая система механического заслона должна быть такой, чтобы сигнал тригера tlaser поступал к лазеру за интервал времени Δ tlaser до открытия заслона 37 у трубки 40. Детектор настраивается на определенный диапазон молекулярных масс в зависимости от угла alfa на диске заслона и скорости вращения f диска. На фиг.6 показаны временные интервалы включения заслона для движения макромолекул до детектора для установки по фиг. 3. Так как кинетическая энергия пропорциональна mv2, где m - масса, v - скорость макромолекулы, то время пролета пропорционально m1/2. Заштрихованная область на фиг.6, определяющая временной период 10 мксек в этом примере, связана с диапазоном макромолекулярных масс, которые не достигают детектора.
Для увеличения эффективности в другой реализации изобретения используется криогенно-детекторная матрица, позволяющая определить время взаимодействия и точку контакта ускоренной макромолекулы с поверхностью детектора. Так как многие реализации криогенных детекторов используют пленочное покрытие и литографическую технику, то мелкомасштабная структура покрытия, порядка милимикрон, будет обеспечивать пространственное разрешение для определения позиции контакта. Такая реализация изобретения является предпочтительной. Макромолекулы пространственно разделяются в магнитном поле в соответствии с их удельным зарядом, а масса исходя из позиции столкновения макромолекулы с криогенно-детекторной матрицей. Если использовать другой вариант реализации изобретения с применением импульсной эмиссионной техники, то масс-спектрометр становится высоко-параллельным инструментом, позволяющий одновременно определять широкий диапазон масс за короткое время в несколько мксек. Такая реализация криогенно-детекторной матрицы представляется впервые и будет детально обсуждаться в дальнейшем.
Криогенно-детекторная матрица (Cryogenic Detector Array), (CDA), используемая в изобретении, состоит из N фононных сенсоров 43 D1...DN с электронными каналами 45, расположенными на подложке 42 (см. фиг.7-9). В реализации многоэлементного криогенного детектора, показанной на фиг.7, ускоренные макромолекулы 46 абсорбируются непосредственно фононным сенсором 43, в котором образуются фононы 47 и сразу же преобразуются в электрический сигнал. Преимуществом этой реализации является высокая эффективность преобразования фонон - заряд и быстрота обработки сигнала. Однако фононный сенсор с большой поверхностью, которая требуется, технологически трудно изготовить (например, в случае сверхпроводящего туннельного проводника). Альтернативой вышеописанной реализации будет использование большого числа фононных сенсоров небольшого размера, к которым, однако, будет подводиться большое число электронных каналов. Следовательно, реализация криогенно-детекторной матрицы по фиг.8 предпочтительнее ранее описанной. Ускоренные макромолекулы 46 поглощаются поглотителем частиц, производят фотоны 47, которые распространяются сквозь поглотитель и преобразуются в электронные сигналы фононным сенсором 43. Когда используется чистый одиночный кристалл, например, кристалл кремния, то фононы распространяются баллистически на большое расстояние и будут фиксироваться более чем одним фононным сенсором. В вышеописанной реализации в качестве фононных сенсоров используются сверхпроводящие туннельные переходы, в которых электронный сигнал пропорционален числу абсорбированных фононов и высота импульса пропорциональна расстоянию между туннельными переходами. Следовательно, точное определение точки абсорбции макромолекулы может быть произведено при помощи расчета центроида при другой высоте импульса. Альтернативой вышеописанной реализации по фиг.8 будет реализация, показанная на фиг.9, в которой дополнительный сверхпроводящий слой 44 располагается над сверхпроводящим туннельным переходом. Материал этого сверхпроводящего слоя выбирается таким, чтобы энергетический порог Δ сверхпроводящего слоя был бы больше, чем порог соответствующего перехода, для того чтобы произошел захват квазичастиц [22]. Квазичастицы, возникающие под воздействием фононов 47, будут распространяться в сверхпроводящем слое 44 за счет диффузии и в конце концов проникнут в нижний слой сверхпроводящего туннельного перехода (см. фиг. 1). Затем они будут проникать сквозь оксидную перегородку и производить детекторный сигнал, как описано выше. Реализация по фиг.9 улучшает эффективность детектирования фононов по сравнению с реализацией по фиг.8. Вычисления, представленные ниже, показывают, что требования пространственно-временного разрешения к криогенно-детекторной матрице (CDA) технически реализуемы: реализация изобретения в виде определенной модели представляется в следующем параграфе. Модель обеспечивает пространственное разрешение dx=0.1 мм и временное разрешение dt= 100 нсек, что позволяет определять массу с точностью до 100 А.Е.М. при общей массе 600000 А.Е.М. В этих расчетах использовалась криогенно-детекторная матрица длиной 10 см и содержащий 100 фононных сенсоров. Другие реализации фононных сенсоров были упомянуты выше при обсуждении фиг.1.
Предпочтительной реализацией изобретения является масс-спектрометр с криогенно-детекторной матрицей, рассмотренной выше и с возможностью расчета траекторий макромолекул. Рассмотрим фиг.10: макромолекулы ионизируются, выбиваются из образца, сначала ускоряются в 51, затем проходя магнитное поле 50 разделяются по траекториям. Траекториями являются окружности, радиус которых зависит от удельного заряда (отношение заряда макромолекулы к ее массе) каждой молекулы. Впоследствии макромолекула электростатически ускоряется за счет разности потенциалов U1-U2 и сталкивается с криогенно-детекторной матрицей 53. Точка столкновения и время столкновения макромолекулы и датчика определяется для каждой молекулы (режим единичного подсчета молекул). Обратим внимание на то, что одним из главных улучшений предлагаемого изобретения является возможность определения массы высокомолекулярных макромолекул. В дальнейшем представляются и обсуждаются специальные расчеты, выполненные по предлагаемой реализации. В соответствии с этими расчетами масса порядка 106 А.Е.М. определялась с точностью до 100 А.Е.М. Кроме того, масс-спектрометр мог работать в квазинепрерывном режиме с мощностью цикла в 10%. Так как использовался режим единичного подсчета молекул, требовалось незначительное количество макромолекул, обычно не более находящихся в 10-15 молей.
Предлагаемая реализация высокопроизводительного масс-спектрометра с криогенно-детекторной матрицей схематически показана на фиг.11. Имеются два основных элемента конструкции: магнит, состоящий из двух прямоугольных сверхпроводных катушек 48, и криогенно-детекторная матрица 53, заключенная в сверхпроводящую оболочку 52. Магнит создает постоянное магнитное поле В, параллельное оси Z. Все элементы конструкции находятся в вакуумной системе и охлаждаются комбинированной криогенной установкой 60. Т1 - рабочая температура сверхпроводящего магнита, Т2 - рабочая температура криогенного детектора, охлаждаемого дополнительным криостатом 58, Т3 - рабочая температура предусилителя.
Анализируемый образец помещается в камеру 51, где макромолекулы ионизируются и выбиваются при помощи механизма 67, подведенного через межслойное соединение 66. Механизмом 67 может быть лазерный луч в случае применения MALDI-техники или капилляры при ESI-технике. Ионизированные макромолекулы сначала ускоряются до кинетической энергии около 100 эв и попадают в сепаратор масс 50, находящийся внутри магнита с магнитным полем несколько Tesla. Напряженность магнитного поля зависит от диапазона значений разделяемых масс. Камера 51 и сепаратор масс 50 находятся под высоковольтным напряжением U1, поддерживаемым источником 65 через межслойное соединение 64. Сверхпроводящий магнит состоит из двух прямоугольных сверхпроводных катушек 48, разделенных прокладкой 49 из сверхпроводящего материала для магнитных полей, в положении когда сепаратор масс параллелен оси z. Магнит охлаждается криостатом 60, подключенным через соединение 61 и имеет рабочую температуру Т1. Устройство 73 обеспечивает криогенную жидкость креостату по каналу 72. Ток для сверхпроводящего магнита поступает от источника 63 по кабелю 62.
Под действием магнитного поля В магнита макромолекулы движутся по окружностям с радиусами, пропорциональными удельному заряду макромолекулы. После прохождения половины окружности разделенные молекулы попадают в зону действия электрического поля и затем внедряются в криогенно-детекторную матрицу 53. Кинетическая энергия макромолекул в момент контакта с криогенно-детекторной матрицей е•(U2-U1), где е - единица заряда, U1 - электрический потенциал сепаратора и U2 - электрический потенциал криогенного детектора частиц, который обычно заземлен. Для того чтобы защитить криогенный детектор частиц от сильного магнитного поля, его помещают в магнитную камеру 52, также изготовленную из сверхпроводящего материала. Криогенно-детекторная матрица 53 расположена на холодной панели 54, которая охлаждается криостатом 58 до рабочей температуры Т2 матрицы 53. Криостат 58 подсоединяется к основному криостату 60, если оба используют 3Не. Криостат управляется системой температурного контроля и насосом 69, подключенным через устройство 68. Криогенно-детекторная матрица передает сигналы электронному предусилителю 56, который может быть охлажден до рабочей температуры Т3 через канал охлаждения 57 от криостата 60. Выход предусилителя подключен через соединение 70 к системе усвоения данных 71.
В последующем оценивается реакция предложенной высокопроизводительной системы на различные варианты управляющих параметров, которые иллюстрируются результатами расчетов. В основном будет использоваться двумерный машинный код [23] , позволяющий рассчитывать электрические и магнитные поля и определять траектории макромолекул в этих полях. Траектории макромолекулы вычисляются по пространственно-временной информации на любом временном шаге. Если не оговорено специально, то при расчетах используются следующие параметры: геометрические - по фиг.10, где наиболее удобными размерами являются внутренние размеры сепаратора масс 50 (64 см•32 см), масса макромолекул - от М= 400000 А.Е.М. до М=800000 А.Е.М., напряженность магнитного поля В=6.5 Tesla, напряжение для первичного ускорения Upre=200 В, напряжение для вторичного ускорения Upost=50 кВ. Пространственное разрешение детектора dх=0.1 мм, разрешение по времени - 100 нсек. Два последних значения типичны для криогенных детекторов частиц и технически реализуемы. Для расчетов, в которых масса макромолекулы была зафиксирована, использовалось значение М= 600000 А.Е.М.
Разделение макромолекул по массе производится за счет магнитного поля В и напряжения для первичного ускорения Upre. Напряжение для вторичного ускорения Upost требуется для предания макромолекулам достаточно высокой кинетической энергии порядка 10 кВ, для того чтобы их можно было фиксировать криогенно-детекторной матрицей, увеличение Upost облегчает определение макромолекул, однако из фиг.12 очевидно, что макромолекулы фокусируются в небольшой области криогенно-детекторной матрицы, тем самым уменьшая пространственное разрешение детектора. На фиг.13 показаны диапазоны значений для различных значений интенсивности магнитного поля. Для данного значения магнитного поля диапазон масс макромолекул, достигающих криогенно-детекторную матрицу, является ограниченным из-за ограниченного входного окна сепаратора масс, фиг.10. Как видно из фиг.13, большее магнитное поле производит больший диапазон значений масс, которые можно определять одновременно криогенно-детекторной матрицей. Однако из-за того, что эти массы распределяются на высоте 10 см, разрешение пространственного разделения масс уменьшается для увеличения масс, как показано на фиг.14. Однако, как видно из фиг. 14, при увеличении масс макромолекул разделение масс улучшается. Магнитное поле напряженностью 6.5 Т может быть легко достигнуто, однако при этом сравнительно большая область детектора будет технологически неактивна. Хорошее однородное магнитное поле требуется для того, чтобы корректировать небольшие неоднородности, учитывая две важные калибровочные кривые: пространственная калибровочная кривая Мx-cal(х) и временная калибровочная кривая Мt-cal(t). Для того чтобы получить хорошее разрешение важно иметь устойчивое по времени магнитное поле на короткий и длинный период.
Другим критическим фактором, от которого зависит хорошее разрешение высокопроизводительного масс-спектрометра, является качество ионизации макромолекулярного потока, поступающего в сепаратор (см. 65 на фиг.10). Этот поток должен иметь хорошую коллимированность и моноэнергетичность. Желательно, чтобы высококачественный поток легко получался при высоком Upre. Три управляющих магнитным полем параметра В, Uprе и Upost не могут, однако, выбираться независимо один от другого при заданном диапазоне измеряемых масс и определенном расположении криогенно-детекторной матрицы. На фиг.15 показана зависимость напряженности магнитного поля В от Upre для диапазона измеряемых масс от 400000 А.Е.М. до 800000 А.Е.М. На фиг.16 показана зависимость напряжения для вторичного ускорения Upost как функция напряжения для первичного ускорения Upre для того же диапазона измеряемых масс. Если, например, напряжение для первичного ускорения Upre=400 В, то напряженность магнитного поля В= 8 Т (фиг.15) и напряжение для вторичного ускорения Upost=100 кВ (фиг.16) позволяют измерять массы в диапазоне от 400000 А.Е.М. до 800000 А.Е.М. при вышеуказанном местоположении криогенно-детекторной матрицы. Преимущество предлагаемой в изобретении реализации состоит в том, что, не меняя расположения матрицы, можно измерять массу макромолекул, условно говоря, без ограничений диапазона масс, изменяя только магнитное поле. Дополнительно напряжение для первичного и вторичного ускорения могут быть выбраны так, чтобы оптимизировать производительность.
Масса макромолекулы может быть определена непосредственно по мощности пространственного разрешения криогенно-детекторной матрицы (см. фиг.14). В этой конкретной расчетной модели способность пространственного разделения макромолекулы криогенно-детекторной матрицей составляет 0.2 мкм/А.Е.М. (см. фиг. 14). Если необходимо определить массу макромолекулы с разрешением, скажем, 100 А. Е.М. (такое потребуется, если измерять массу больших ДНК-фрагментов ДНК-последовательности, где в основном масса основания макромолекул 300 А. Е.М.), потребуется пространственное разрешение криогенно-детекторной матрицы около 25 мкм. Так же потребуется около 4000 индивидуальных детекторов, для криогенно-детекторной матрицы размером 10 см, если воспользоваться реализацией по фиг.7. Когда используется реализация, показанная на фиг.8, 9, то можно получить пространственное разрешение dx=0.1 мм с расстоянием между фононными сенсорами 1 мм. Далее потребуется только 100 фононных сенсоров на площадку 10 см. Метод Монте-Карло был применен для исследования разрешающей способности различных реализаций изобретения. "Истинные" значения Хstop 2000 макромолекул массой М0=600000 А.Е.М. были рендомизированы по гауссовому распределению (FWHM) с разрешением dx=0.1 мм, имитируя выходную информацию Xout. На фиг. 17 показано распределение по х-координате выходного сигнала Xout криогенно-детекторной матрицы. Расчетные траектории соответствующих молекул использовались для вычисления калибровочной кривой Мx-cal(х). На основании полученных данных была определена масса макромолекулы M1. На фиг. 18 показано распределение ошибки расчета массы M1-М0. Полученное значение ошибки определения масс около 500 А.Е.М. будет недостаточно для определения ДНК-последовательности. Однако увеличение точности определения масс может быть получено за счет применения стратегии "подлетного времени" и реализации импульсного режима эмиссии высокопроизводительного масс-спектрометра. Этому будет посвящен следующий параграф.
Для определения "подлетного времени" в масс-спектрометре измеряют разность между моментом начала эмиссии частицы tstart и временем столкновения частицы с детектором tstop. Так как обычно в нашей расчетной модели подлетное время составляет 5 мсек, то эмиссировать частицы можно каждые Т2=10 мсек с продолжительностью импульса, скажем, T1=100 нсек. При таких условиях циклическая загрузка детектора будет t1/(T1+T2) порядка 10-5 и, соответственно, низкая производительность устройства. Идея режима оперативного подсчета частиц состоит в том, чтобы выполнять несколько измерений подлетного времени параллельно, способствуя определению пространственных траекторий в магнитном поле. Эмиссионные импульсы показаны на фиг.19. Время столкновения частицы с детектором tstop фиксируется криогенно-детекторной матрицей, однако момент начала эмиссии частицы tstart необходимо определить. Это делается с использованием пространственных траекторий движения частицы следующим образом. Как показано на фиг.19, макромолекулы эмиссируются в течение времени T1 и не эмиссируются в течение Т2. Такой эмиссионный импульс может исходить или из лазера (MALDI-схема), или от электроннооптических систем. В дальнейшем потребуется знание двух кривых: пространственной калибровочной кривой Мx-cal(х) и временной калибровочной кривой Мt-cal(t). Начальной точкой расчета являются два выходных сигнала криогенно-детекторной матрицы:
Xout=Xstop+dX,
tout=tstop+dt,
где Xstop, tstop - местоположение и время контакта макромолекулы и криогенного детектора частиц, соответственно,
dX, dt - отклонения от истинного положения макромолекулы в пространстве и времени, соответственно, зависящие от пространственно-временного разрешения криогенно-детекторной матрицы. По значению Xout определяется первое приближение массы Mi, используя пространственную калибровочную кривую Мx-cal(х):
M1=Mx-cal (Xout).
Подставляя это значение M1 в инвертированное М-1 t-c al(t) -временной калибровочной кривой, получим первое приближение t1 начала эмиссии частицы:
t1=tout-М- 1 t-саl(M1).
Теперь, зная, что макромолекула должна эмитироваться от каждого импульса, можно установить соответствующее число циклов эмиссии N (см. фиг. 19):
N=1+t1/(T1+Т2)
и получить второе приближение t2 начала эмиссии частицы:
t2=(N-1)(T1+Т2)+Т2/2.
Значение t2, к сожалению, определяется с точностью до значения T1. Используя снова временную калибровочную кривую, находим окончательно массу макромолекулы М2 методом TOF
М2=Mt-cal (tout-t2).
В представленном методе (TOF) точность определения массы макромолекулы определяется длительностью эмиссионного импульса T1 и временным разрешением dt криогенно-детекторной матрицы. В импульсном режиме пространственное разрешение dx криогенно-детекторной матрицы используется только для определения числа импульсов N. На фиг.20 представлено распределение Монте-Карло для времени столкновения частицы с детектором tstop, полученное при длительности эмиссионного импульса T1=0.5 мксек и временном разрешении криогенно-детекторной матрицы dt=100 нсек.
На фиг. 21 представлено распределение восстанавливаемых значений масс методом TOF. Это распределение получено следующим образом: при расчете по методу Монте-Карло каждый случай характеризовался соответствующими значениями Xout (фиг. 17) и tstop (фиг.20). Используя метод восстановления масс (TOF), описанный выше, было установлено значение массы макромолекулы М2 по двум калибровочным кривым. Распределение ошибки определения массы М2-М0 имеет центральный пик в области 100 А.Е.М. (с учетом условий FWHM) и связан с точностью определения числа импульсов N. Кроме того, два пика по краям графика связаны с ложным определением доверительных границ эмиссионных циклов, что приводит к "утечке" значений t1. Причина этих "утечек" - ограниченное пространственное разрешение dx криогенно-детекторной матрицы и малое значение паузы Т2 в последовательности импульсов. Увеличение Т2 уменьшает число ошибочных случаев. Однако циклическая загрузка детектора будет сокращаться. На фиг. 22 эффективность определения массы в зависимости от циклической загрузки детектора при двух значениях пространственного разрешения детектора dx представлена в виде отношения случаев определения массы к случаям некорректного определения массы.
Точность измерения массы M1 может быть повышена за счет увеличения пространственного разрешения криогенно-детекторной матрицы (т.е. определяя соответствующие значения dt меньшими) (см. фиг.23). Точность определения распределения массы М2 может быть повышена за счет уменьшения продолжительности действия эмиссионного импульса T1 (см. фиг.24). Однако в последнем случае точность измерения массы будет сильно зависеть от временного разрешения криогенно-детекторной матрицы. Вычисления вышеописанной точности расчета массы было получено в предположении, что ионизация начального потока макромолекул, поступающих в сепаратор, приводит к тому, что все макромолекулы имеют кинетическую энергию 200 эВ. К сожалению, это не совсем так для реального устройства и это будет одной из главных технологических задач при конструировании вышеуказанного предлагаемого изобретения.
В частности, рассмотрим применение предлагаемого изобретения для исследования ДНК-последовательности. Цепочка ДНК-последовательностей определяется четырьмя базовыми последовательностями ДНК-альфабет, А (аденин), G (гуанин), Т (тимин), С (цитозин). В молекулярных биологических лабораториях пробы, содержащие цепочки ДНК-последовательностей, приготавливают в соответствии с Sanger или Maxam-Gilbert методиками. Например, используя методику Sanger, четыре пробы одинаковых частей ДНК, могут быть помечены как А, G, Т и С, каждая из которых содержит информацию, связанную с расположением основных специфических частей ДНК-молекулы. Обычно макромолекулы сортируют в соответствии с их длинами для каждой из четырех проб с использованием техники гель-электрофореза. Макромолекулы смешивают в гель, который помещают в электрическое поле. При заданной протяженности цепочки короткие фрагменты смешиваются быстрее, чем длинные фрагменты, которые направляют в сепаратор. Главным недостатком гель-электрофореза является большое время (порядка нескольких часов), требуемое для перемешивания макромолекул в геле. Обычно хорошее оборудование лаборатории может подготовить порядка 10000 проб в день.
Наиболее быстрый метод разделения ДНК-фрагментов связан с использованием масс-спектрометрии. Как было показано выше, предлагаемое изобретение может анализировать большие ДНК-фрагменты массой 600000 А.Е.М. с разрешением порядка 100 А.Е.М. В дальнейшем анализируются пробы, эквивалентные человеческому геному, содержащие 3.109 проб, которые оценивают по предлагаемому методу. Так как используется криогенно-детекторная матрица работающих в режиме единичного подсчета частиц, то интенсивная нагрузка детектора будет предотвращена. Следовательно, только небольшое число макромолекул будет достигать многоэлементного детектора за заданное время. Детектор частиц позволяет идентифицировать каждый набор значений (Xstop, tstop), уникальный для импульсного эмиссионного цикла. Таким образом, тяжелые молекулы в случае ранней эмиссии будут достигать криогенного детектора частиц позднее, чем легкие молекулы в случае поздней эмиссии. Они никогда не достигнут того же положения на детекторе, так как уникальная траектория зависит от удельного заряда. Одно из усовершенствований предлагаемой реализации состоит в том, что заряженные макромолекулы могут разделяться при помощи управляющих параметров. Если поместить ДНК-фрагменты для анализа, как показано на фиг.25, то эмиссия каждой пробы может быть выполнена синхронно с эмиссионным импульсом масс-спектрометра. Каждое измеряемое криогенно-детекторной матрицей значение массы связано с определенной пробой. Мы снова выберем диапазон измерения масс между 400000 А.Е.М. и 800000 А.Е.М. и примем точность определения массы для выбранных проб Δm<300 А.Е.М. Вследствие имеющегося разрешения системы мы предполагаем, что 100 случаев потребуется для определения массы однозначно. Внутри заданного диапазона масс выбранный образец содержит 1300 оснований, которые могут быть реконструированы для четырех выбранных проб A, G, Т и С, изображенных на фиг.25. Для того чтобы удовлетворительно определить массу по значениям (Хstop, tstop), только одна макромолекула должна попадать на детектор в заданную точку за определенное время. Заданная проба будет анализироваться 100 раз. Если выбрать продолжительность эмиссионного импульса 100 мксек, то можно восстановить последовательность из 1300 оснований заданных стандартных ДНК за 100•4•100 μsec=40 мсек. Следующие четыре пробы будут связаны с популяцией макромолекул, смещенных на 1300 оснований. Потребуется 40 мсек для определения этих 1300 оснований последовательностей. В 1 сек машина имеет возможность определять 3.25•104 оснований, или, другими словами, число оснований человеческого генома, содержащего 3•109 оснований, может быть установлено за 9.2•104 сек, т.е. за 25 часов. Если одна из последовательностей человеческого генома с одним единичным гель-электрофорезным аппаратом имеет возможность создавать 10000 оснований в день, то потребуется 800 лет для таких расчетов. Однако разделение последовательностей является только первым шагом для определения ДНК-последовательностей. Биологическое производство последовательностей человеческого генома в лабораторных условиях потребует более нескольких часов. Тем не менее массив образцов может быть произведен и сохранен, как показано на фиг.25, различными лабораториями параллельно и анализироваться при помощи предлагаемого изобретения за очень короткое время.
Полный подсчет ДНК потребует также немногого: простой массив, как показано на фиг.25, должен состоять из 3•109/1300=2.3•104 проб, которые могут быть представлены в виде массива 1500•1500 проб. В нашем примере 4 пробы, определяемые как A, G, Т и С, содержат полностью 1300 макромолекул со средней массой 600000 А. Е. М. Общая масса макромолекул, достигающая криогенно-детекторную матрицу за один эмиссионный цикл составляет (1300/4)•(600000 А.Е. М. Так как анализ каждой пробы выполняется 100 раз для получения хорошей оценки значения массы, то предыдущее значение необходимо умножить на 100. Кроме того, так как эффективность выхода и ионизации макромолекул составляет не более, чем 10-4, полученное число необходимо умножить на 104. Следовательно, каждая полученная проба (1 А.Е.М.=1.66•10-24г) содержит:
количество ДНК в образце = 104•100•(1300/4)•600000 А.Е.М.=0.32•10-9 г.
Произведение числа проб и образцового массива (2.3•106) дает полное число ДНК:
общее число ДНК = 2.3•106•0.32•10-9г=0.74•10-3г.
Теперь давайте оценим размер образцового массива. Каждая проба содержит раствор ДНК с концентрацией 10-4, т.е. растворенная масса будет 3.2•10-4 г. Если для примера мы возьмем плотность раствора, равную плотности воды, то масса будет соответствовать объему 3.2•10-6 см3, или, альтернативно, радиус пробы составит 91 мкм. Пробы могут располагаться на расстоянии 0.2 мм друг от друга. Общий размер массива образца, следовательно, будет:
общий размер= (1500•0.2 мм)•(1500•0.2 мм)=30 см•30 см.
Общее число ДНК, аккумулированных криогенным детектором при анализе человеческого генома, описанного выше, будет составлять 4•10-10 г, которые соответствуют толщине пленки 7.4 нм для криогенного детектора длиной 10 см и молекулярного пучка толщиной 1 мм. Полимерная пленка такой толщины не будет препятствием для фононной чувствительности криогенного детектора.
Изобретение было использовано для вышеописанных вычислений. Описанное изобретение может быть применено также для протеинов, пептидов, полимеров и других макромолекул.
Представленные здесь формы конструкции изобретения могут иметь другие применения. Представленная реализация не имеет в виду отметить все возможные эквивалентные формы изобретения. Понятно, что используемые здесь термины являются скорее описательными, чем ограничивающими, и что различные изменения могут быть сделаны без ущемления сути изобретения.
| название | год | авторы | номер документа |
|---|---|---|---|
| МЁССБАУЭРОВСКИЙ СПЕКТРОМЕТР С РЕГИСТРАЦИЕЙ КОНВЕРСИОННЫХ ЭЛЕКТРОНОВ ПРИ СУБГЕЛИЕВЫХ ТЕМПЕРАТУРАХ | 2016 |
|
RU2620771C1 |
| МАСС-СПЕКТРОМЕТР ДЛЯ ИССЛЕДОВАНИЯ МАКРОМОЛЕКУЛ | 2006 |
|
RU2332748C1 |
| Сверхпроводящий акустический детектор ионизирующего излучения | 1979 |
|
SU820438A1 |
| Металл-Диэлектрик-Металл-Диэлектрик-Металл фотодетектор | 2020 |
|
RU2749575C1 |
| Биомолекулярный сенсор с микроэлектронным генератором электромагнитной волны | 2020 |
|
RU2749698C1 |
| Устройство для детектирования ионизирующих излучений | 1980 |
|
SU936705A1 |
| Активный сверхпроводящий детектор | 2022 |
|
RU2801961C1 |
| СПОСОБ АНАЛИЗА МАКРОМОЛЕКУЛ БИОПОЛИМЕРОВ | 1994 |
|
RU2124783C1 |
| ДЕТЕКТОР ТЕРАГЕРЦОВОГО ИЗЛУЧЕНИЯ НА ДЖОЗЕФСОНОВСКОЙ ГЕТЕРОСТРУКТУРЕ | 2010 |
|
RU2437189C1 |
| ЭЛЕКТРОХИМИЧЕСКИЙ СЕНСОР И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2009 |
|
RU2502992C2 |











Изобретение относится к исследованию макромолекул для определения массы макромолекул, включая белки, большие пептиды, длинные ДНК-фрагменты и полимеры. Техническим результатом является расширение временного и простанственного разрешения. Кинетическая энергия электростатически ускоренной и заряженной частицы поглощается в криогенном детекторе частиц, излучая при этом фононы, которые определяются фононным сенсором. Макромолекулы детектируются в режиме подсчета каждой частицы, независимо от их масс. В одной из реализаций масс-спектрометр содержит одноканальный криогенный детектор частиц. В другой реализации масс-спектрометр содержит пространственно распределенный многоканальный криогенный детектор частиц. Масс-спектрометр содержит вакуумный сосуд, в котором находится магнит, разделитель массы, проводящий элемент и фонон-чувстивтельный криогенный многоэлементный детектор частиц. Криогенный многоэлементный детектор частиц содержит абсорбент и определенное число фононных сенсоров. Масс-сепаратор размещается в магнитном поле магнита вместе с проводящим элементом, на который подается электрический потенциал U1, изолированный от магнита. Криогенный многоэлементный детектор заземлен и имеет электрический потенциал U2. Макромолекулы ускоряются под действием разности потенциалов U1-U2 и достигают криогенный многоэлементный детектор частиц с кинетической энергией, пропорциональной разности U1-U2. Масса макромолекулы определяется на основании пространственно-временной информации, поступающей от криогенного многоэлементного детектора частиц. 29 з.п. ф-лы, 25 ил.
| Nuclear instrument and methods in physics research, vol | |||
| ДИФФЕРЕНЦИАЛЬНАЯ ТЕРМИОННАЯ ЛАМПА | 1920 |
|
SU294A1 |
| Арматура для железобетонных свай и стоек | 1916 |
|
SU259A1 |
| СПОСОБ АНАЛИЗА МАТЕРИАЛОВ МЕТОДОМ ВТОРИЧНОЙ ИОННОЙ МАСС-СПЕКТРОМЕТРИИ И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1985 |
|
SU1306396A1 |
| ПЕЧАТАЮЩЕЕ УСТРОЙСТВО | 0 |
|
SU360676A1 |
Авторы
Даты
2002-09-10—Публикация
1995-07-31—Подача