Изобретение относится к области аналитической химии и химической технологии и может быть использовано для изучения аналитических свойств, для тестирования и определения ионов Со, Си и Zn.
Известен способ определения некоторых металлов в сточных водах с помощью сорбентов на основе силохрома С-80, химически модифицированного различными органическими реагентами [1].
Известен способ физической адсорбции 4-(2-тиазолилазо)-резорцина, иммобилизованный на поверхности силохрома С-120 (СГ-ТАР), который используется для определения палладия и урана в руде, катализаторе с сорбционным концентрированием и определением методом спектроскопии диффузного отражения [2] .
Известны способы концентрирования и разделения металлов путем контактирования растворов, содержащих ионы металлов с модифицированным силикагелем [4-6].
Наиболее близким является способ определения меди и кобальта с использованием в качестве индикаторных порошков гидрофобных силикагелей, нековалентно иммобилизированных или модифицированных 1-нитрозо-2-нафтолом, при этом сорбент используется в системах непрерывного проточного анализа [3].
Все вышеуказанные способы трудоемки, длительны, методы определения ионов металлов не избирательны и менее чувствительны.
Задача предлагаемого изобретения - расширение ряда модифицированных сорбентов и изучение их сорбционных свойств.
Технический результат в создании эффективных подвижных фаз для разделения ионов металлов и гетерогенных катализаторов нового типа.
Указанный технический результат достигается тем, что получают модифицированный сорбент путем иммобилизации реагентов на гидрофобный носитель за счет физической сорбции.
Иммобилизованный реагент начинает работать как сорбент для концентрирования микрокомпонентов и реагент для их тестирования и количественного определения.
Сущность предлагаемого изобретения в том, что в качестве органического реагента используют 2 карбокси 21-гидpoкco-51cyльфoфopмaзилбeнзoл (цинкон), растворенный в водно-ацетоновой среде (1:1), иммобилизованный за счет физической сорбции на силикагель марки КСК 2, 5. Иммобилизованный реагент начинает работать как сорбент для концентрирования микрокомпонентов и реагент для их тестирования и количественного определения.
Конкретный пример выполнения.
Приготовление растворов.
Готовят по ГОСТу из соответствующих металлов особой чистоты стандартные растворы Со (II), Сu (II), Zn (II) с концентрацией 0,1 мг/мл, 2 карбокси 21-гидроксо-5'сульфоформазилбензола - 1•10-3 М в водно-ацетоновой среде.
Получение (синтез) модифицированного сорбента.
Навеску силикагеля (СГ) в конической колбе обрабатывают 1М H2SО4 (на 1 г СГ 2 мл Н2SО4), затем разбавляют водой до слабокислой реакции, туда же вводят ацетоновый раствор 2 карбокси 21-гидpoкco-51cyльфoфopмaзилбeнзoлa, периодически взбалтывая для установления равновесия. Модифицированный сорбент СГ-21-гидpoкco-51-cyльфoфopмaзилбeнзoл переносят в воронку Бюхнера, промывают водой и высушивают на воздухе до воздушно-сухого состояния.
Определение ионов металлов.
В колбы с притертыми пробками вводят 1 г модифицированного сорбента СГ-21-гидроксо-51сульфоформазилбензол, создавая различные значения рН буферным раствором, туда же вводят определенное количество раствора ионов цинка, меди, кобальта и разбавляют водой до 15 мл, затем измеряют рН фильтрата и коэффициент диффузного отражения сорбента (Р).
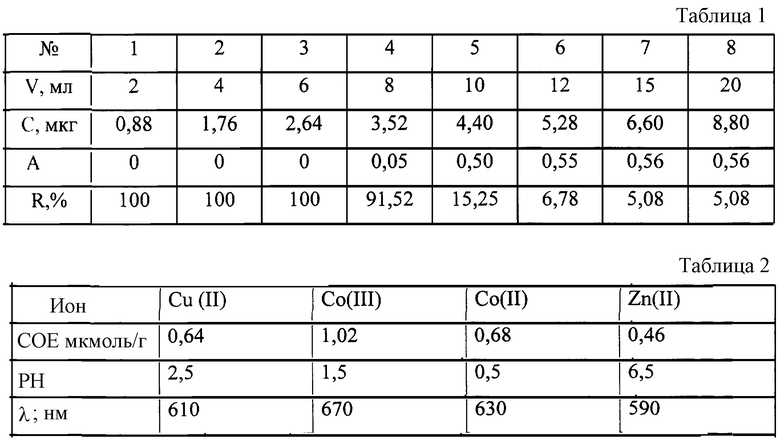
Количество реагента, закрепленного на носителе, определяют в статическом режиме. В табл.1 приведены результаты анализа сорбционной способности, 2 карбокси 21-гидроксо-51-сульфоформазилбензола на силикогеле.
Результаты анализа сорбционной способности 2 карбокси 21-гидроксо-51cyльфoфopмaзилбeнзoлa на силикогеле даны в табл.1.
По количеству поглощенного реагента рассчитывают емкость сорбента. Для насыщения сорбента достаточно 10 мл 0,001 М раствора 2 карбокси 21-гидpoкco-51сульфоформазилбензола. Полученный комплексообразующий реагент имеет емкость по 2 карбокси 21-гидpoкco-51cyльфoфopмaзилбeнзoлy 10 мкмоль на 1 г сорбента. Оптимальной областью сорбции 2 карбокси 21-гидроксо-51сульфоформазилбензола является рН от 2 до 4.
Оптимальное время установления равновесия для комплексов меди - 5 минут, кобальта -10 мин, цинка - 20 мин.
Емкость модифицированного сорбента СГ- 2 карбокси 21-гидpoкco-51сульфоформазилбензол по ионам Сu, Со, Zn определяется методом насыщения. Данные приведены в табл.2.
Из данных следует, что 0,5 г сорбента СГ-2 карбокси 21-гидроксо-51сульфоформазилбензола максимально сорбирует 15 мкг Zn2+; 20 мкг Сu2+; 20 мкг Со2+; 30 мкг Сo3+
Тест-реакция на Со, Cu и Zn и количественное определение
Реакция на кобальт в сильнокислой среде (рН 1,0) сопровождается возникновением сине-зеленой окраски на поверхности СГ-2 карбокси 21-гидроксо-51сульфоформазилбензола, на медь в присутствии уксусно-ацетатного буферного раствора (рН 2) образуется синее окрашивание, а при рН>6 в слабощелочной среде ионы цинка окрашивают поверхность СГ-2 карбокси 21-гидроксо -51сульфоформазилбензола в фиолетовый цвет. В пробирку с притертой пробкой для тест-реакций помещают 10 мл анализируемой пробы. В качестве анализируемой пробы служит модельный раствор, состоящий из 20 мкг ионов кобальта, меди и цинка соответственно, который подкисляют H2SO4, вводят 0,5 г модифицированного сорбента и встряхивают 10 мин. В сильнокислой среде комплекс меди разрушается, ионы цинка не образуют комплекс при этих значениях рН, в ионы кобальта окрашивают СГ-2 карбокси 21-гидроксо-51cyльфoфopмaзилбeнзoл в сине-зеленый цвет. Предел обнаружения кобальта 0,02 мкг.
В пробирку для тест-реакций помещают 10 мл пробы, вводят уксусно-ацетатную буферную смесь с рН 2, туда же приливают 0,05 М раствор цитрат-ионов для связывания ионов кобальта и встряхивают 5 мин. Этот маскирующий агент не препятствует образованию синего комплекса, характерного для ионов меди, тогда как остальные ионы маскируются. Пределы обнаружения меди 0,005 мг/мл.
В нейтральной или слабощелочной среде Zn(II) образует с СГ-2 карбокси 21-rидpoкco-51cyльфoфopмaзилбeнзoл комплекс фиолетового цвета, не разрушаемый в присутствии цитратов и тиосульфатов. Предел обнаружения 0,03 мг/мл.
Тест-реакция на ионы Рb2+, Fe3+ и Ni2+, их количественное определение.
Реакция на свинец в слабокислой среде (рН 4,5) сопровождается возникновением фиолетовой окраски на поверхности СГ-2 карбокси 21-гидpoкco-51сульфоформазилбензола, на железо - в нейтральной среде (рН 6), образуется желтое окрашивание, а в сильно-щелочной среде (рН 11) ионы никеля окрашивают поверхность СГ-2 карбокси 21-гидpoкco-51cyльфoфopмaзилбeнзoлa в малиновый цвет.
В пробирку с притертой пробкой для тест-реакций помещают 10 мл анализируемой пробы (модельный раствор, состоящий из 20 мкг ионов Рb2+, Fe3+ и Ni2+ соответственно), туда же вводят 0,5 г полученной новой фазы СГ-2 карбокси 21-гидроксо-51сульфоформазилбензол и встряхивают 30 мин.
При рН 6,0 (в нейтральной среде) ионы никеля не окрашивают поверхность модифицированного сорбента т. е. не образует комплекс, а Рb2+ цитратами связываются в прочный бесцветный комплекс. Предел обнаружения ионов железа 0,03 мкг. При этом поверхность СГ-2 карбокси 21-гидpoкco-51-сульфоформазилбензол окрашивается в желтый цвет.
В пробирку для тест-реакции помещают 10 мл пробы, 0,5 г СГ-2 карбокси 21-гидроксо-51сульфоформазилбензола, туда же вводят аммиачно-хлоридный буферный раствор с рН>10 и 0,02 М раствор фторида натрия для связывания ионов железа (III) и встряхивают 10 мин. Новая фаза модифицированного сорбента окрашивается в малиновый цвет, характерный для комплекса Ni2+ с 2 карбокси 21-гидpoкco-51cyльфoфopмaзилбeнзoлoм. Предел обнаружения 0,007 мг/мл.
Для обнаружения ионов Рb2+ железо связываем в бесцветный фторидный комплекс (Fe F6)3-, рН 4 создаем введением ацетатного буферного раствора, при этом поверхность Сг-2 карбокси 21-гидpoкco-51cyльфoфopмaзилбeнзoлa окрашивается в фиолетовый цвет. Предел обнаружения 0,05 мкг/мл.
Таким образом, учитывая все вышеизложенное, можно сделать вывод о преимуществах предложенного способа:
- получена новая фаза СГ-2 карбокси 21-гидpoкco-51cульфоформазилбензола за счет иммобилизации 2 карбокси 21-гидроксо-51cульфоформазилбензола на поверхности силикагеля КСК,
- установлена оптимальная кислотность сорбции 2 карбокси 21-гидроксо-51cульфоформазилбензол на силикагеле: рН 2-4,
- статистическая обменная емкость сорбента по реагенту составляет 10 мкмоль/г,
- установлен порядок сорбируемости ингредиентов, оптимальный эффект достигается при предварительной сорбции органического реагента, затем иона металла,
- определено время установления равновесия для комплексов меди кобальта и цинка поверхности твердой фазы,
- найдены оптимальные условия сорбции каждого иона и емкость по ионам,
- проведен сравнительный анализ оптических свойств комплексов Zn, Сu, Со, Рb, Fe и Ni на СГ-2 карбокси 21-гидpoкco-51cyльфoфopмaзилбeнзoл и в растворе.
Новая форма СГ-2 карбокси 21-гидpoкco-51cyльфoфopмaзилбeнзoлa позволяет сочетать концентрирование с последующим определением в концентрате ионов указанных металлов методов спектроскопии диффузного отражения.
Источники информации
1. Брыкина Г.Д., Крысина Л.С., Смирнов И.П. и т.д. Журнал аналитической химии, 1989, т. 44, 12, с. 2186-2189.
2. Иванов В.М., Кузнецова О.В. Журнал аналитической химии, 1995, т. 50, 5, с. 498-504.
3. Максимова И.М., Моросанова Е.И. Журнал аналитической химии, 1994, т. 49, 6, с. 602-606; 4, с. 1210.
4. Г. В. Лисичкин. Модифицированные кремнеземы в сорбции, катализе и хроматографии. М.: Химия, 1986, стр. 171-175.
5. В. Риман. Ионообменная хроматография в аналитической химии. М.: Мир, 1973.
6. С. Д. Татаева, Крамина С.В. Способ совместного определения ионов металлов в объектах окружающей среды, пат. 99109746/28, 27.02.2001.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ СОВМЕСТНОГО ОПРЕДЕЛЕНИЯ ИОНОВ МЕТАЛЛОВ В ОБЪЕКТАХ ОКРУЖАЮЩЕЙ СРЕДЫ | 1999 |
|
RU2173455C2 |
| СПОСОБ КОНЦЕНТРИРОВАНИЯ И ОПРЕДЕЛЕНИЯ ИОНОВ ХРОМА И МАРГАНЦА В БИОСУБСТРАТАХ | 2005 |
|
RU2292545C2 |
| СПОСОБ КОНЦЕНТРИРОВАНИЯ И ОПРЕДЕЛЕНИЯ МЕДИ, СВИНЦА И КАДМИЯ | 2008 |
|
RU2361660C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ЦИНКА (II) | 2012 |
|
RU2518967C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОБАЛЬТА (II) | 2008 |
|
RU2374638C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КОБАЛЬТА (II) | 2011 |
|
RU2456592C1 |
| СПОСОБ ИЗВЛЕЧЕНИЯ КАДМИЯ ИЗ СТОЧНЫХ И ПРИРОДНЫХ ВОД | 2009 |
|
RU2417952C1 |
| СПОСОБ ГРУППОВОГО ИЗВЛЕЧЕНИЯ CU, FE И ZN ИЗ ПРИРОДНЫХ И ПИТЬЕВЫХ ВОД | 2001 |
|
RU2224032C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПАЛЛАДИЯ | 2001 |
|
RU2187566C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ МЕДИ | 2001 |
|
RU2201592C2 |
Изобретение относится к области аналитической химии и химической технологии и может быть использовано для разделения, тестирования и определения ионов Со, Cu и Zn. Раствор, содержащий ионы металлов, контактируют с модифицированным силикагелем, на котором иммобилизован цинкон (2 карбокси 2'-гидроксо-5'сульфоформазилбензол), растворенный в водно-ацетоновой среде (1:1). Определение ионов проводят спектроскопией диффузного отражения. Технический результат заключается в создании эффективных подвижных фаз для разделения ионов металлов и гетерогенных катализаторов. 2 табл.
Способ концентрирования и разделения ионов металлов из растворов, включающий их контактирование с модифицированным гидрофобным силикагелем и последующее определение ионов в концентрате, отличающийся тем, что контактирование проводят с силикагелем, содержащим иммобилизованный 2 карбокси 2'-гидроксо-5'сульфоформазилбензол, а определение ионов осуществляют методом спектроскопии диффузного отражения.
| ЛИСИЧКИН Г.В | |||
| Модифицированные кремнеземы в сорбции, катализе и хроматографии | |||
| - М.: Химия, 1986, с.171-175 | |||
| КОМПЛЕКСНОЕ СОЕДИНЕНИЕ И СПОСОБ ИЗВЛЕЧЕНИЯ ЖЕЛАЕМЫХ ИОНОВ ИЗ РАСТВОРА С ИСПОЛЬЗОВАНИЕМ ЭТИХ СОЕДИНЕНИЙ | 1993 |
|
RU2116828C1 |
| ГЕТЕРОГЕННЫЙ КОМПЛЕКСООБРАЗУЮЩИЙ СОРБЕНТ | 1998 |
|
RU2141377C1 |
Авторы
Даты
2002-11-10—Публикация
2001-02-26—Подача