Изобретение относится к фармацевтической промышленности, касается способа получения биологически активных веществ из ламинарии и может применяться при лечении запоров и интоксикаций тяжелыми металлами.
Известен способ получения полисахаридов из морской капусты Laminaria saccharina L. (ламинария сахаристая) и L. japonica Aresch. (ламинария японская) сем. Laminariaceae (ламинариевые), произрастающих в Дальневосточном бассейне (Авторское свидетельство СССР 1275810, кл. А 61 К 35/78, 1984 "Способ получения полисахаридов, обладающих слабительным действием" /Зинченко В.В., Макаревич И. Ф. , Чушенко В.Н., Оболенцева Г.В., Ставрова Р.Ф., Бакай С.И., Бирюк В. А. ). Полисахариды получают путем измельчения, промывки слоевищ морской капусты, экстракции горячей водой при 80oС методом настаивания или противоточной перколяции, отделения экстракта от сырья, упаривания экстракта до соотношения 1:0,8-1:1,2, прибавления к горячему экстракту 96%-ного этилового спирта в соотношении экстракт:этанол 1:1. Затем образовавшуюся смесь отстаивают, отделяют нижний слой взвеси, центрифугируют и после отделения маточного раствора осадок промывают 96%-ным этиловым спиртом. Промытый осадок сушат, измельчают. Выход готового продукта составляет 5,6% к исходному сырью. Полученный комплекс полисахаридов с аминокислотами, известный под названием "Ламинарид", ранее выпускался на Харьковском производственном химико-фармацевтическом объединении (ХПХФО "Здоровье трудящимся") и применялся как препарат слабительного действия.
Недостатками указанного способа являются: а) получение только одного продукта из водорослей (полисахаридов), при этом отходами производства являются ценные вещества - маннит, альгинат натрия; б) низкий выход полисахаридов (5,6% к сырью), в) неполное осаждение полисахаридов этанолом за счет недостаточного количества этанола, г) потеря этанола при добавлении его к горячему концентрированному экстракту для осаждения полисахаридов; д) невысокая степень чистоты целевых продуктов.
Описан способ одновременного получения маннита, водорастворимого полисахаридного комплекса, ламинарана, фукоидана, альгината натрия, обладающих слабительным, гиполипидемическим, радионуклидсвязывающим, гепатозащитным, противоязвенным действием, из беломорской ламинарии (смеси двух видов ламинарии L. saccharina L. и L. digitata L.) (Патент Российской Федерации 2028153, кл. А 61 К 35/80, 1995 "Способ получения биологически активных веществ из ламинарии" /Макарова Р.Н., Самокиш И.И., Компанцев В.А., Кайшева Н. Ш. и др.). Способ осуществляют путем измельчения сырья, последовательного экстрагирования 90-96%-ным этанолом, горячей водой и 1,5% раствором карбоната натрия; этанольное извлечение концентрируют и кристаллизуют из него маннит; из водного экстракта 96%-ным этанолом осаждают водорастворимый полисахаридный комплекс (аналог "Ламинарида"); при этом оставшийся спиртовый маточный раствор упаривают и 80% этанолом осаждают ламинаран и фукоидан, для разделения последних полученный осадок обрабатывают 0,4%-ным раствором соляной кислоты и добавляют 0,5 моль/л раствор цетавлона для переведения кислых полисахаридов в осадок, экстракт обрабатывают этанолом (для осаждения ламинарана), а оставшийся осадок вновь растворяют в 0,4%-ном растворе соляной кислоты и обрабатывают 70% этанолом (фукоидан); из карбонатного извлечения после предварительной обработки концентрированной серной кислотой, раствором карбоната натрия получают альгинат натрия.
Согласно данному способу, сначала проводят сушку сырья при температуре 50oС, после чего освобождают его от механических примесей, затем сырье измельчают и проводят экстракцию различными растворителями. Выход целевых продуктов (% к исходному сырью) составляет: маннит - 7,85, полисахаридно-белковый комплекс ("Ламинарид") - 12,60, ламинаран - 4,53, фукоидан - 2,14, альгинат натрия - 12,41. Данный способ получения биологически активных веществ из ламинарии близок к заявляемому и выбран за прототип.
Недостатками указанного способа являются: а) относительно низкий выход целевых продуктов, б) длительность процесса сушки вещества, в) невысокая степень чистоты полученных веществ, г) трудоемкость и нецелесообразность раздельного получения отнотипных по структуре фракций веществ ("Ламинарид", ламинаран, фукоидан ), обладающих одним видом биологического действия (слабительный эффект), д) большой расход лимитированных и дефицитных растворителей (этилового спирта, цетавлона), необходимых для получения, очистки и разделения ламинарана, фукоидана.
Целью изобретения является комплексная переработка беломорских водорослей Северного бассейна (СБ) - ламиинарии сахаристой для одновременного получения маннита, полисахаридно-белкового комплекса ("Ламинарид СБ") и альгината натрия, повышение выхода, степени чистоты и растворимости целевых продуктов, упрощение способа получения, повышение комплексообразующей и слабительной активности целевых продуктов.
Поставленная цель достигается тем, что способ одновременного получения маннита, "Ламинарид СБ", альгината натрия, обладающих слабительным и детоксицирующим действием, из ламинарии сахаристой осуществляют путем измельчения сырья, обезжиривания его хлороформом в массо-объемном соотношении сырье: хлороформ 1:20 в течение 1,5 ч (для удаления липофильных пигментов), последовательного экстрагирования 90-96%-ным этанолом, горячей водой и 1,5%-ным раствором карбоната натрия; этанольное извлечение фильтруют, диализуют через целлофановую мембрану в течение 2 ч, концентрируют и кристаллизуют из него маннит; водный экстракт, содержащий преимущественно полисахариды ("Ламинарид СБ", ламинаран, фукоидан), трехкратно охлаждают при температуре 4oС в течение 1 ч, деализуют через целлофановую пленку в течение 6 ч, упаривают, осаждают из него с помощью 90%-ного этанола суммарный полисахаридно-белковый препарат "Ламинарид СБ"; сушат способом лиофильной сушки при температуре -13oС в течение 70 мин; из карбонатного извлечения после предварительной обработки концентрированной серной кислотой, раствором карбоната натрия, трехкратного охлаждения при температуре 4oС в течение 1 ч, последующего диализа через целлофановую пленку в течение 6 ч и обработки 96%-ным этанолом осаждают альгинат натрия, который затем сушат способом лиофильной сушки пери температуре -13oС в течение 50 мин.
Согласно заявляемому способу, сырье - слоевища ламинарии сахаристой - обезжиривают хлороформом для того, чтобы удалить различные липофильные вещества - фосфолипиды, гликолипиды, липопротеиды. Липиды составляют основу внеклеточной мембраны, покрывающей наружные стенки эпидермиса слоевища растения. От количества этих липидов зависит проницаемость клеток и их органоидов для различных растворителей (Муравьева Д.А. Фармакогнозия. М.: Медицина, 1991, с. 22, 124-125). Поэтому удаление липофильных веществ облегчает доступ экстрагентов к действующим веществам, содержащимся в клетках. Кроме того, обезжиривание сырья приводит к получению веществ более светлых тонов. Так, например, если "Ламинарид", полученный по способу-прототипу, представляет собой порошок серовато-желтого цвета, то "Ламинарид СБ", полученный по заявляемому способу, порошок светло-розового цвета, альгинат натрия - тонкие пластинки светло-оранжевого и белого цвета соответственно.
Многократное охлаждение растворов полисахаридного комплекса снижает их вязкость, т.е. наблюдается криолиз полисахаридов (Влияние низких температур на технологические характеристики растворов растительного полисахаридного комплекса / Н.Е.Чернов, И.П.Городецкий, Д.В.Рыбачук и др.// Тезисы докладов Республиканской научной конференции "Актуальные вопросы поиска и технологии лекарств". Харьков, 1981, с. 83-84). При этом скорость сушки растительных веществ увеличивается по сравнению с сушкой без предварительного замораживания. Длительное высушивание препаратов полисахаридов нецелесообразно, т.к. приводит к значительному ухудшению растворимости сухого препарата.
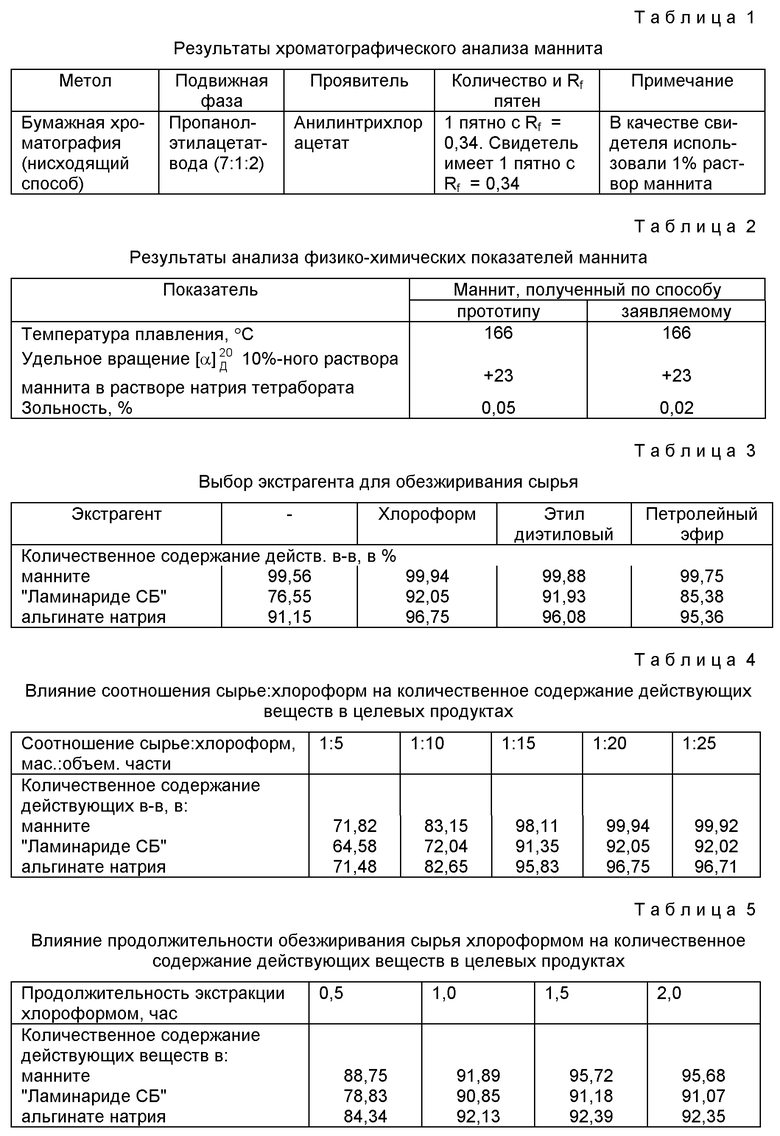
Диализ полисахаридных растворов через целлофановую пленку позволяет очистить полисахариды от балластных веществ, имеющих более крупные размеры, чем целевые продукты. Так, например, если записать УФ-спектр поглощения альгината натрия в растворе до и после диализа (см. чертеж), то можно заметить, что после диализа (кривая 2) спектр имеет более выраженный максимум поглощения с большей величиной оптической плотности, чем до диализа (кривая 1).
Для оценки эффективности связывания полисахаридами ионов металлов используется показатель комплексообразующей способности (КС), который характеризует число мг ионов металла, связанное 1 г полисахарида (Давидюк Л.П., Вшивкова Г.Ф. Сравнительное изучение комплексообразующей способности пектинов разного происхождения /Бюллетень гос. Никитского ботанического сада", - Ялта: ГНБС, 1981. - Вып.3 (46). - С. 98-101). Содержание ионов металла, связанное с полисахаридами, определяли методом обратного комплексонометрического титрования (Компанцев В.А., Кайшева Н.Ш., Гокжаева Л.П., Сизова Н.М. Определение комплексообразующей способности пектинов и пектиносодержащих препаратов/ Охрана окружающей среды. - М.: НИИТЭХИМ, 1991. - С. 25-27).
Полученные целевые продукты были подвергнуты качественному и количественному анализу.
1. Маннит
Идентификацию полученного маннита проводили методом бумажной хроматографии (табл.1).
Подлинность маннита подтверждали следующими качественными реакциями:
1) 0,5 г препарата растворяют в 1 мл воды. К раствору прибавляют 5 мл реактива (приготовление реактива: к 2 мл 10% раствора сульфата меди (II) прибавляют 10% раствор аммиака до получения прозрачного раствора темно-синего цвета, затем раствор разбавляют водой до 20 мл). Раствор хорошо встряхивают, выпадает осадок (маннит).
2) 0,5 г препарата помещают в колбу вместимостью 50 мл, прибавляют 3 мл ангидрида уксусного, 1 мл пиридина и нагревают на кипящей водяной бане в течение 15 мин, часто встряхивая. Реакционную смесь охлаждают, добавляют 29 мл охлажденной воды, перемешивают и дают постоять в течение 5 мин; выпадает осадок - маннит-гексаацетата, который собирают на стеклянной фильтр Шотта, перекристаллизовывают из эфира и высушивают при температуре 60oС в течение 1 ч. Температура плавления остатка от 119 до 123oС.
Результаты анализа физико-химических показателей маннита приведены в таблице 2.
Количественное содержание маннита определяли методом обратной иодометрии в присутствии индикатора крахмала. Титрование проводили до появления зеленой окраски раствора. Содержание маннита по способу-прототипу составило 99,56%; по заявляемому способу - 99,94%,
Таким образом, по приведенным методам идентификации и определения количественного содержания маннита препарат, полученный заявляемым способом, обладает высокой степенью чистоты и может использоваться как лекарственный препарат.
II. "Ламинарид СБ"
Идентификацию компонентов "Ламинарида СБ" проводили с помощью следующих реакций:
2 г препарата помещают в коническую колбу вместимостью 100 мл, прибавляют 100 мл воды, перемешивают (раствор А).
1) к 5 мл раствора А прибавляют 5 мл спирта 95%, перемешивают; появляются хлопьевидные сгустки светло-коричневого цвета, выпадающие в осадок (полисахариды);
2) К 10 мл раствора А прибавляют 0,5 г натрия цитрата, перемешивают. К полученному раствору прибавляют 5 мл кислоты хлористоводородной разведенной, образуется гелеобразный осадок (альгиновая кислота);
3) 5 мл раствора А дают характерную реакцию на кальций с оксалатом аммония; образуется белый осадок оксалата кальция.
4) 8 мл раствора дают характерную реакцию на натрий с цинк-уранилацетатом в уксуснокислой среде; образуется желтый кристаллический осадок;
5) 15 мл раствора А нагревают на водяной бане с 8 мг нингидрина в течение 8 мин, образуется сине-фиолетовое окрашивание раствора (аминокислоты);
6) cнимают спектр поглощения в видимой области 4 мл раствора В, полученного при количественном определении. Наблюдается только I максимум поглощения при длине волны 460 нм (восстанавливающие сахара);
7) для идентификации ламинарана и фукоидана препарат гидролизовали 4 моль/л раствором серной кислоты при температуре 100oС в течение 6 ч с последующей нейтрализацией гидролизата карбонатом бария. Гидролизат анализировали методом бумажной хроматографии (нисходящий способ) в системе растворителей: н-бутанол-пиридин-вода (6: 4: 3). Проявитель - кислый анилинфталат. На хроматограмме обнаружено 2 пятна с Rf=0,15 (фукоза) и Rf=0,16 (глюкоза). В качестве свидетелей использованы 1% растворы фукозы и глюкозы;
8) к 5 мл раствора А прибавляют 1 мл концентрированной соляной кислоты и 5 мл ацетона, появляется малиновое окрашивание раствора; максимум поглощения при 550 нм (фукоидан);
9) к 5 мл раствора А добавляют 1 мл концентрированной серной кислоты и 5 мл 1% раствора цистеина; появляется желтое окрашивание раствора; имеется два максимума поглощения при 400 и 427 нм (фукоидан).
10) К 5 мл раствора А добавляют 1 мл концентрированной серной кислоты и 5 мл 1% раствора тиогликолевой кислоты; появляется желто-зеленое окрашивание раствора (фукоидан).
Для определения количественного содержания восстанавливающих сахаров в "Ламинариде СБ" к 0,3 г препарата прибавляют 15 мл 10% раствора кислоты серной и кипятят в колбе со шлифом, соединенной с обратным холодильником в течение 3 ч. Содержимое колбы охлаждают и количественно переносят в мерную колбу на 50 мл, доводят объем раствора водой до метки и перемешивают. 10 мл полученного раствора помещают в стакан и последовательно нейтрализуют по универсальной индикаторной бумаге: сначала 1 моль/л раствором натра едкого, затем 10% раствором кислоты серной и, наконец, 1 моль/л раствором натра едкого. Раствор фильтруют, переносят в мерную колбу на 25 мл и доводят объем раствора водой до метки. В мерную колбу на 25 мл помещают 1 мл 1% раствора кислоты пикриновой, 3 мл 20% раствора натрия карбоната и 1 мл полученного раствора. Колбу с содержимым погружают в кипящую водяную баню на 10 мин, затем охлаждают до комнатной температуры и доводят объем раствора водой до метки (раствор В). Измеряют оптическую плотность полученного раствора В при 460 нм.
Содержание восстанавливающих сахаров в "Ламинариде" (прототип) составило 76,55%, в "Ламинариде СБ" (заявляемый способ) 92,05%, т.е. в последнем случае содержание восстанавливающих сахаридов превышает в 1,2 раза.
Таким образом, в результате анализа "Ламинарида СБ" идентифицированы полисахариды, аминокислоты, неорганические ионы, установлено высокое содержание редуцирующих сахаров и показано соответствие полученного "Ламинарида СБ" препарату "Ламинарид".
III. Альгинат натрия
Идентификацию альгината натрия проводили следующими реакциями:
1) к 5 мл 0,5% раствора препарата приливают 1 мл разведенной кислоты хлористоводородной, образуется гелеобразный осадок (альгиновая кислота);
2) к 5 мл 0,5% раствора альгината натрия приливают 1 мл 2% раствора хлорида кальция, образуется гелеобразный осадок (отличие от камедей, производных целлюлозы);
3) к 5 мл 0,5% раствора альгината натрия приливают 2,5 мл насыщенного раствора аммония сульфата; осадок не образуется (отличие от агара, крахмала, производных целлюлозы, желатина);
4) к 5 мл 0,5% раствора альгината натрия приливают 5 мл 10% раствора натрия цитрата и 3 мл кислоты соляной концентрированной, образуется студенистый осадок (кислота альгиновая);
5) 5 мл 2% раствора альгината натрия дают характерную реакцию на натрий с цинк-уранилацетатом в уксуснокислой среде; образуется желтый кристаллический осадок.
Для количественного определения альгината натрия навеску препарата растворяют в 0,1 н. растворе едкого натра, доводят объем раствора 0,1 н. раствором едкого натра до 100 мл. В пробирку отмеривают 0,5 мл полученного раствора. В пробирку отмеривают 0,5 мл полученного раствора, 0,25 мл 0,5% спиртового раствора карбазола, 5,5 мл сернокислого раствора мочевины и борной кислоты; пробирку с раствором кипятят на водяной бане в течение 15 мин, охлаждают и измеряют оптическую плотность раствора при 520 нм.
Содержание альгината натрия, полученного по способу-прототипу, составляет 91,15%, а по заявляемому способу 96,75%.
Таким образом, полученные результаты анализа подтверждают подлинность и высокое количественное содержание альгината натрия.
Нами изучена зависимость выхода целевых продуктов от ряда технологических параметров (табл.3).
Как следует из таблицы 3, наилучшими экстрагентами для обезжиривания слоевищ ламинарии являются хлороформ и диэтиловый эфир, но последний ввиду высокой взрыво- и огнеопаности, использовать нецелесообразно.
Как видно из таблицы 4, наибольшее количественное содержание действующих веществ обеспечивается при массо-объемном соотношении слоевищ ламинарии и хлороформа 1 : 20.
Как следует из таблицы 5, максимальное содержание действующих веществ в выделенных фракциях достигается при обработке сырья хлороформом в течение 1,5 ч.
Нами изучено влияние природы мембраны на степень диализа по значениям оптической плотности диализуемого раствора (Д1) и диализата (Д2). Степень диализа (d) рассчитана по формуле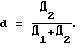
Результаты приведены в таблице 6. В этой же таблице приведены значения комплексообразующей способности (КС) очищенных путем диализа веществ.
Как показывают данные таблицы 6, наибольшая скорость диализа характерна для веществ через пленки из ацетата целлюлозы, при этом КС наименьшая; по-видимому, это связано с прохождением через пленки не только биологически активных веществ, но и примесей, которые снижают КС. При диализе через поливинилхлоридные пленки, несмотря на большую КС (в сравнении с целлюлозной пленкой), степень диализа относительно невысокая; возможно, что пленкой задерживаются не только примеси, но и действующие вещества. Наиболее оптимальным материалом диализной мембраны является целлофан: при высокой КС, вещества проявляют относительно высокую степень диализа.
Как показывают результаты, представленные в таблице 7, оптимальной продолжительностью диализа является для всех целевых продуктов 6 ч, кроме маннита (для него 2 ч).
Как следует из таблицы 8, оптимальной температурой охлаждения экстрактов является 4oС; при этом температуре достигаются максимальные выходы и растворимость целевых продуктов, сокращаются продолжительность сушки препаратов. При 4oС вязкость экстрактов снижается, что облегчает процессы диализа, фильтрации. Вязкость растворов определялась по времени истечения на вискозиметре ВПЖ-1 при 20oС.
Результаты, приведенные в таблице 9, показывают, что оптимальная продолжительность охлаждения достигается в течение 1 ч.
Как видно из таблицы 10, оптимальная повторность охлаждения составляет 3.
Лиофильная сушка препаратов проводилась в аппарате Долина, состоящем из камеры и конденсатора. Камера работает под глубоким вакуумом. Для оттаивания конденсата и подогрева камеры вмонтированы электроспирали. Вещества раскладывают на противни из нержавеющей стали и ставят сушить в металлической этажерке. Перед загрузкой противней с веществами в конденсаторе при помощи компрессорно-конденсаторного аппарата доводят температуру до отрицательных значений. Процесс сушки препаратов начинается при остаточном давлении в вакуум-сушильной камере 200-250 мкм, а после сушки давление составляет 50 мкм. Высушивание препаратов методом лиофильной сушки позволяет ускорить процесс сушки и избежать деструкцию действующих веществ. Нами подобраны оптимальные условия лиофилизации препаратов.
Как следует из таблицы 11, оптимальная температура сушки составляет для целевых продуктов -13oС: при этом достигается минимальная продолжительность сушки и максимальное содержание действующих веществ.
В способе-прототипе подтверждено, что оптимальной концентрацией этанола для осаждения ламинарана и фукоидана является концентрация в пределах 80-96% (в целях экономии спирта использовался 80% спирт), для осаждения "Ламинарида" используется 90-96% этанол. Поэтому при применении этанола в концентрации 90% осаждаются и "Ламинарид СБ" и нейтральные сахара - ламинаран и фукоидан, что наряду с другими причинами объясняет более высокий выход фракции "Ламинарид СБ" и снижение расхода спирта. Кроме того, нет необходимости разделять указанные вещества, т.к. все они ("Ламинарид СБ", ламинаран, фукоидан) обладают слабительным действием, при этом ламинаран и фукоидан не представляют интереса как детоксиканты металлов.
Благодаря обезжириванию исходных слоевищ ламинарии хлорформом, диализу экстрактов через целлофановые мембраны, а также лиофильной сушке препаратов, обеспечивающей сохранность целевых продуктов, последние обладают более выраженной КС, чем продукты, полученные по способу-прототипу. Результаты определения КС приведены в таблице 12.
Как следует из таблицы 12, "Ламинарид СБ" и альгинат натрия, полученные по заявляемому способу, обладают более выраженной детоксицирующей способностью, чем по способу-прототипу, в 1,4 раза. По-видимому, это объясняется высокой степенью очистки и высоким выходом целевых продуктов в заявляемом способе за счет обезжиривания исходного сырья, диализа экстрактов, охлаждения экстрактов и лиофильной сушкой, препятствующей разложению полисахаридов.
Заявляемый способ получения маннита, полисахаридно-белкового комплекса "Ламинарид СБ", альгината натрия поясняется следующими примерами конкретного выполнения.
Пример 1
Беломорские водоросли Северного бассейна (Laminaria saccharina L.) высушивают при 50oС в сушильном шкафу, затем освобождают их от механических примесей, моллюсков. Далее отвешивают 100 г водорослей с точностью ±0,02 г, измельчают на лабораторном измельчителе до размера частиц 3 мм, помещают в колбу со шлифом вместимостью 3 л, приливают 2 л хлороформа, колбу закрывают пробкой и выдерживают сырье с хлороформом в течение 1,5 ч. Затем хлороформное извлечение темно-зеленого цвета отделяют от сырья процеживанием через марлю (5 слоев). Колбу с сырьем помещают в вытяжной шкаф для удаления остатков хлороформа. Далее сырье переносят с помощью 600 мл 90%-ного этилового спирта в аппарат Сокслета и проводят экстракцию при температуре кипения этанола в течение 3 ч. Полученный спиртовый экстракт фильтруют на воронке Бюхнера под вакуумом, после чего диализуют через целлофановую мембрану в течение 2 ч. Для диализа используют прибор, в котором имеется два отсека, разделенных между собой целлофановой мембраной, края которой закреплены на внутренней стороне корпуса с помощью какого-либо водостойкого клея. В один отсек через отверстие прибора сверху помещается диализуемый спиртовый экстракт, который диализуется через мембрану в другой отсек (диализатор). Затем полученный диализат упаривают до образования сгущенного экстракта (около 30 мл), после чего концентрат кристаллизуют при температуре 4oС в холодильнике. Выпавшие кристаллы маннита двукратно очищают перекристаллизацией из спиртового раствора. Чистые кристаллы маннита фильтруют через бумажный фильтр и сушат при температуре 60oС в вакуум-сушильном шкафу. Выход маннита составляет 9,54 г или 9,54% к сырью.
Целевой продукт - маннит - представляет собой кристаллы белого цвета, без запаха, хорошо растворимые в воде и кипящем спирте, малорастворимые в холодном спирте, нерастворимые в эфире. КС полученного маннита составляет 7,85 мг Рв2+/г.
Далее водоросли, оставшиеся после извлечения маннита, "сушат" под тягой для удаления остатков спирта, после чего их загружают в колбу вместимостью 2 л и заливают 1 л горячей (температура 80oС) воды. Нагревание смеси проводят на электроплитке при температуре 80oС. Экстракцию проводят в течение 0,5 ч двукратно. Полученные горячие водные экстракты отделяют от жома процеживанием через 5 слоев марли, объединяют, фильтруют под вакуумом на воронке Бюхнера через двойную капроновую ткань. Объединенный профильтрованный экстракт помещают в холодильник и выдерживают в нем при температуре 4oС в течение 1 ч, после чего экстракт вынимают из холодильника и выдерживают до тех пор, пока температура экстракта не достигнет комнатной. Затем еще дважды экстракт охлаждают при тех же условиях. Далее проводят диализ экстракта через целлофановую пленку в течение 6 ч. Полученный диализат упаривают в колбе Вюрца под вакуумом при остаточном давлении 0,3 атм и температуре 70oС до плотности 1,05-1,06 г/см3 (примерно 1/7 от первоначального объема). Полученный водный концентрат обрабатывают двукратным объемом 90%-ного этанола, что позволяет осадить "ламинарид СБ" вместе с ламинараном и фукоиданом. Выпавший осадок полисахаридно-белкового комплекса фильтруют на воронке Бюхнера под вакуумом через двойную капроновую ткань. Осадок трехкратно промывают на воронке 96%-ным этанолом; сушат способом лиофильной сушки в аппарате Долина при температуре в барокамере -13oС в течение 70 мин. Выход полисахаридно-белкового комплекса "Ламинарид СБ" составляет 19,52 г или 19,52% к сырью.
Целевой продукт полисахаридно-белковый комплекс "Ламинарид СБ" представляет собой аморфный порошок светло-розового цвета, без запаха. Практически нерастворим в спирте. В воде умеренно растворим с образованием мутного слизистого раствора (1 г препарата растворяется в 45 мл воды при 20oС). КС "Ламинарида СБ" составляет 1920 мг Рв2+/г.
Оставшийся жом водорослей помещают в колбу вместимостью 3 л, приливают 2 л 1,5% раствора карбоната натрия и экстрагируют на водяной бане при температуре 50oС в течение 1 ч. Водно-щелочной экстракт далее декантируют с жома и фильтруют под вакуумом на воронке Бюхнера. Затем водно-щелочной экстракт обрабатывают примерно 100 мл концентрированной (99,95%) серной кислоты путем медленного добавления небольших порций кислоты (примерно по 5 мл) и экстракту. При этом выделяется осадок альгиновой кислоты, который отделяют фильтрованием на воронке Бюхнера. Этот осадок переносят количественно в колбу вместимостью 3 л, добавляют 300 мл 1,5%-ного раствора карбоната натрия, перемешивают, осадок альгиновой кислоты переходит в раствор альгината натрия. Раствор альгината натрия трехкратно охлаждают в холодильнике при температуре 4oС в течение 1 ч (после каждого охлаждения в холодильнике выдерживают раствор альгината натрия до тех пор, пока его температура не достигнет комнатной). Далее раствор альгината натрия диализуют через целлофановую мембрану в течение 6 ч. Альгинат натрия осаждают из полученного диализата путем добавления к нему 1,5 л 96%-ного этанола. Образующийся осадок фильтруют на воронке Бюхнера под вакуумом, после чего сушат способом лиофильной сушки в аппарате Долина при температуре в барокамере -13oС в течение 50 мин.
Выход альгината натрия составляет 21,83 г или 21,83% к сырью.
Целевой продукт - альгинат натрия - представляет собою тонкие пластинки белого цвета, без запаха, слизистого вкуса, растворимый в воде (при 20oС 1 г препарата растворяется в 15 мл воды), нерастворимый в спирте. КС альгината натрия составляет 2435 мг Рв2+/г.
Маточные спиртовые растворы подвергаются обработке с целью регенерации из них спирта.
Пример 2
Беломорские водоросли подготавливают к экстракции как описано в примере. Отвешивают 100 г водорослей, измельчают на лабораторном измельчителе до 3 мм, помещают в колбу со шлифом вместимостью 3 л, приливают 2,5 л хлороформа, колбу закрывают пробкой и выдерживают сырье с хлороформом в течение 2,0 ч. Отделение хлороформного извлечения, экстракцию маннита 90% этанолом проводят аналогично примеру 1. Спиртовый экстракт диализуют через целлофановую мембрану в течение 3 ч. Проведение диализа, выделение, очистка и сушка кристаллов маннита аналогично примеру 1. Выход маннита составляет 9,52 г или 9,52% к сырью. КС маннита составляет 7,81 мг Рв2+/г.
Далее экстракцию жома водой, процеживание экстракта проводят как описано в примере 1. Полученный экстракт после фильтрации четырехкратно охлаждают при температуре 2oС в течение 1,5 ч (после каждого охлаждения в холодильнике выдерживают экстракт до тех пор, пока его температура не достигнет комнатной). Затем диализуют экстракт через целлофановую мембрану в течение 7 ч. Выделение из диализата "Ламинарида СБ" проводится 90%-ным этанолом аналогично описанию в примере 1. Препарат сушат способом лиофильной сушки в аппарате Долина при температуре в барокамере -20oС в течение 70 мин. Выход "Ламинарида СБ" составил 19,32 г или 19,32% к сырью. КС "Ламинарида СБ" составляет 1900 мг Рв2+/г; растворимостью в воде при 20oС: 1 г препарата растворим в 45 мл воды.
Извлечение альгината натрия проводят аналогично примеру 1, но в отличие от него раствор альгината натрия (после обработки серной кислотой и карбонатом натрия) четырехкратно охлаждают при температуре 2oС в течение 1,5 ч; диализ проводят через целлофановую мембрану в течение 7 ч; сушку альгината натрия осуществляют при температуре -20oС в течение 70 мин. Выход альгината натрия 21,63 г или 21,63% к сырью. КС альгината натрия 2430 мг Рв2+/г. Растворимость в воде при 20oС: 1 г препарата растворим в 15 мл воды.
Пример 3
Подготовку сырья - слоевищ ламинарии - к экстракции, извлечение из него маннита, проводят аналогично примеру 1, но, в отличие от него для обезжиривания к 100 г водорослей приливают 1,5 л хлороформа и выдерживают с ним 1 ч; диализ спиртового экстракта через целлофановую мембрану проводят в течение 1 ч. Выход маннита составляет 8,31 г или 8,31% к сырью. КС маннита составляет 5,63 мг Рв2+/г.
Извлечение из оставшегося жома "Ламинарида СБ" осуществляют аналогично примеру 1, но в отличие от него водный экстракт охлаждают двукратно при температуре 10oС в течение 0,5 ч; экстракт диализуют через целлофановую мембрану в течение 5 ч; сушат препарат способом лиофильной сушки при температуре -11oС в течение 80 мин. Выход "Ламинарида СБ" составил 18,15 г или 118,15% к сырью. КС "Ламинарида СБ" составляет 1832 мг Рв2+/г; растворимость в воде при 20oС: 1 г препарата растворим в 70 мл воды.
Извлечение альгината натрия проводят аналогично примеру 1, но в отличие от него охлаждение раствора альгината натрия осуществляют двукратно при температуре 10oС в течение 0,5 ч; диализ проводят через целлофановую мембрану в течение 5 ч; сушку альгината натрия осуществляют при температуре -11oС в течение 65 мин. Выход альгината натрия 19,71 г или 19,71% к сырью. КС альгината натрия 2386 мг Рв2+/г. Растворимость в воде при 20oС: 1 г препарата растворим в 20 мл воды.
Экспериментальная биологическая часть
Изучение слабительного действия целевых продуктов осуществлялось путем регистрации суточной массы кала после перорального введения вещества в дозе 200 мг/кг в объеме 3 мл водного раствора в опытах на 42 белых крысах массой 200-220 г линии Вистар. Результаты биологических испытаний приведены в таблице 13. Представленные результаты изучения слабительного действия показали идентичность биологического действия маннита и альгината натрия, полученных обоими способами, с незначительным преобладанием слабительного эффекта целевыми продуктами по заявляемому способу (преобладание активности составляет для маннита 4,2%, для альгината натрия 4,9%). "Ламинарид СБ", полученный заявляемым способом, на 73% превышает слабительный эффект, вызываемый "Ламинаридом", полученный по способу-прототипу. Возможно, что это связано с наличием во фракции "Ламинарида СБ" дополнительных полисахаридов (ламинарана, фукоидана) и высоким количественным содержанием действующих веществ.
Таким образом, заявляемый способ обеспечивает следующий положительный эффект:
1. Обеспечивается комплексная переработка ламинарии сахаристой, произрастающей в Белом море Северного бассейна, при которой получают одновременно 3 продукта: маннит, полисахаридно-белковый комплекс "Ламинарид СБ", альгинат натрия. При этом полученные вещества могут иметь самостоятельное применение: а) маннит как осмотический диуретик для понижения внутричерепного давления и уменьшения отека мозга, при острой почечно-печеночной недостаточности (Машковский М.Д. Лекарственные средства: В 2-х томах. Т.1 10-е изд. стер. - М. : Медицина, 1986. - С.493-494), а также как слабительные препарат; б) "Ламинарид СБ" как выраженный детоксикант тяжелых металлов и как слабительный препарат; в) альгинат натрия аналогично "Ламинариду СБ", а также как стимулятор регенерации ран различной этиологии и как плазмозамещающее средство. Но наиболее широкое применение альгинат натрия имеет в технологии лекарственных форм как гелеобразователь, солюбилизатор, связывающее вещество, при производстве таблеток, стабилизатор суспензий и эмульсий, пленкообразователь, растворитель и др. (Properties of alginates (by R.H. Mc Dowell). - Alginate Industries Limited, London).
Ламинаран и фукоидан нецелесообразно выделять в качестве самостоятельных веществ, поскольку они, как и "Ламинарид СБ", проявляют слабительное действие и для применения в других целях не представляют интереса.
2. Повышение выхода целевых продуктов. Так, если в способе-прототипе выход маннита, "Ламинарида" и альгината натрия составляет соответственно (% к сырью): 7,85; 12,60; 12,41, то в заявляемом способе эти величины достигают следующих значений (соответственно): 9,54; 19,52; 21,83. Таким образом, увеличение выхода целевых продуктов по заявляемому способу составляет: для маннита - в 1,2 раза, для "Ламинарида СБ" - в 1,55 раза, для альгината натрия - в 1,76 раза. Повышение выхода целевых продуктов можно объяснить многократным охлаждением растворов полисахаридов и лиофильной сушкой препаратов, что исключает разрушение макромолекул полимеров. Кроме того, повышение выхода "Ламинарида СБ", по-видимому, связано с соосаждением с ним ламинарана и фукоидана.
Обезжиривание слоевищ ламинарии хлороформом способствует разрушению и извлечению различных липидов, образующих клеточные мембраны; при этом усиливается доступ различных растворителей - экстрагентов к действующим веществам внутри клетки, что также способствует повышению выхода действующих веществ.
3. Повышение степени чистоты целевых продуктов. Это подтверждается высоким количественным содержанием действующих веществ: так, например, если в целевых продуктах, полученных по способу-прототипу, содержание действующих веществ составило соответственно (%) в: манните - 99,56; "Ламинариде" - 76,55; альгинате натрия - 91,15, то в заявляемом способе эти значения составили соответственно 99,94; 92,05; 96,75. Кроме того, очистка препаратов повысила и КС (мг Рв2+/г): КС целевых продуктов, полученных по способу-прототипу, составила для маннита 5,71, "Ламинарида" 1380, альгината натрия 1725, а для полученных по заявляемому способу, соответственно 7,85; 1920; 2435. Превышение КС составило для всех продуктов в 1,4 раза. Полученный "Ламинарид СБ" отличается более светлыми тонами окраски - светло-розовый (по прототипу - серовато-желтый), альгинат натрия - белый (по прототипу - светло-оранжевый).
Повышение степени чистоты обусловлена несколькими причинами: а) обезжиривание сырья способствует освобождению экстрактов от липофильных пигментов, которые могут связываться с полисахаридами, снижая их КС; б) диализ экстрактов через целлофановые мембраны позволяет освободить экстракты от различного рода примесей. Спектр поглощения альгината натрия, представленный на чертеже, подтверждает влияние диализа на очистку вещества: кривая диализата имеет четкий максимум поглощения с более высокой величиной оптической плотности, чем до диализа; в) использование низких температур при лиофилизации препаратов позволяет избежать деструкцию целевых продуктов и образование низкомолекулярных фрагментов, "загрязняющих" препараты.
Обладая высокой чистотой, все три целевых продукта могут использоваться как лекарственные препараты, и даже для инъекционного применения (маннит, альгинат натрия).
4. Упрощение способа комплексной переработки ламинарии за счет: а) исключения трудоемкого раздельного получения ламинарана и фукоидана, б) сокращения продолжительности сушки препаратов: для "Ламинарида" и альгината натрия, полученных по способу-прототипу, продолжительность высушивания составляет соответственно 180 и 135 мин, а для веществ, полученных по заявляемому способу, соответственно 70 и 50 мин, т.е. сокращается продолжительность высушивания в 2,6 и 2,7 раза; в) сокращение и исключение расхода лимитированных и дефицитных экстрагентов (эталона, цетавлона, кислоты соляной) в связи с исключением раздельного давления ламинарана и фукоидана.
5. Повышение растворимости "Ламинарида СБ" и альгината натрия благодаря применению многократного охлаждения экстрактов. Как показывают данные таблицы 8, растворимость "Ламинарида СБ" и альгината натрия увеличивается в 1,9 раза.
6. Повышение КС целевых продуктов в 1,4 раза. Это позволяет рекомендовать "Ламинарид СБ" и альгинат натрия в качестве детоксикантов при интоксикациях тяжелыми металлами. Это действие препаратов особенно ценно, если учесть их основное назначение (слабительный и плазмозамещающий эффекты соответственно). "Ламинарид СБ", вызывая опорожнение ЖКТ, а альгинат натрия, оказывая плазмозаменяющее действие, могут быстро вывести из ЖКТ и крови (соответственно) ионы тяжелых металлов.
7. Повышение слабительного действия. "Ламинарид СБ", маннит и альгинат натрия, полученные по заявляемому способу, превосходят слабительное действие аналогичных препаратов, выделенных по способу-прототипу, соответственно на 73; 4,2 и 4,9%. Возможно, что это преимущество связно с высоким количественным содержанием действующих веществ.
8. Достаточная сырьевая база. Ламинария сахаристая образует ежегодные многотоннажные сырьевые запасы в Белом море Северного бассейна. Государственная фармакопея СССР XI (ГФ СССР. XI изд.Вып.2. Общие методы анализа. Лекарственное растительное сырье. - М.: Медицина, 1990. - Ст. 83) в качестве производящих растений рекомендует два вида ламинарии - л. сахаристую и л. японскую как наиболее богатые источники полисахаридов, а ламинария пальчаторассеченная (L. digitata), применяемая по способу-прототипу, не является официальным видом сырья из-за меньшего содержания действующих веществ. Поэтому в заявляемом способе L. digitata не используется.
Заявляемый способ позволит применительно к условиям Мурманского научно-технического центра "Экобиотек-Мурманск" переработать беломорскую ламинарию. При этом будут исключены расходы, связанные с транспортировкой и хранением сырья, т.к. сырье будет добываться и перерабатываться в Мурманске.
9. Морская капуста издавна применяется как пищевой продукт, поэтому продукты ее переработки совершенно нетоксичны и биосовместимы с организмом человек.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ МЕДИЦИНСКОГО ОЧИЩЕННОГО АЛЬГИНАТА НАТРИЯ | 2001 |
|
RU2197249C1 |
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ ИЗ ЛАМИНАРИИ | 1991 |
|
RU2028153C1 |
| СПОСОБ КОМПЛЕКСНОЙ ПЕРЕРАБОТКИ ФУКУСОВЫХ ВОДОРОСЛЕЙ (ВАРИАНТЫ) | 2006 |
|
RU2337571C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕДИЦИНСКОГО ОЧИЩЕННОГО ПЕКТИНА | 1996 |
|
RU2116075C1 |
| ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ ДЕТОКСИЦИРУЮЩЕЙ АКТИВНОСТЬЮ | 2001 |
|
RU2191590C1 |
| СПОСОБ КОМПЛЕКСНОЙ ПЕРЕРАБОТКИ БУРЫХ ВОДОРОСЛЕЙ С ПОЛУЧЕНИЕМ ПРЕПАРАТОВ ДЛЯ МЕДИЦИНЫ И КОСМЕТОЛОГИИ | 2003 |
|
RU2240816C1 |
| СПОСОБ ПОЛУЧЕНИЯ МОДЕЛЕЙ БИОЛОГИЧЕСКИХ МЕМБРАН | 2001 |
|
RU2202835C1 |
| СПОСОБ ПОЛУЧЕНИЯ ВОДОРАСТВОРИМЫХ ПОЛИСАХАРИДОВ, ОБЛАДАЮЩИХ ГЕПАТОПРОТЕКТОРНОЙ АКТИВНОСТЬЮ, ИЗ ЛИСТЬЕВ ЖЕНЬШЕНЯ | 1999 |
|
RU2157231C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДЕТОКСИКАНТОВ ТЯЖЕЛЫХ МЕТАЛЛОВ | 2001 |
|
RU2195274C1 |
| Способ комплексной переработки бурых водорослей | 2018 |
|
RU2676271C1 |
Изобретение относится к фармацевтической промышленности. Ламинарию сахаристую измельчают. Обезжиривают хлороформом в массо-объемном соотношении сырье : хлороформ 1:20 в течение 1,5 ч. Затем последовательно экстрагируют 90-96%-ным этанолом, горячей водой и 1,5%-ным раствором карбоната натрия. Этанольное извлечение фильтруют, диализуют через целлофановую мембрану в течение 2 ч, концентрируют и кристаллизуют из него маннит. Водный экстракт трехкратно охлаждают при температуре 4oС в течение 1 ч. Диализуют через целлофановую пленку в течение 6 ч, упаривают, осаждают из него с помощью 90%-ного этанола суммарной полисахаридно-белковый комплекс. Сушат способом лиофильной сушки при температуре -13oС в течение 70 мин. Из карбонатного извлечения после предварительной обработки концентрированной серной кислотой раствором карбоната натрия осаждают альгинат натрия, который затем сушат способом лиофильной сушки при температуре -13oС в течение 50 мин. Изобретение позволяет упростить процесс и повысить активность продукта. 1 ил., 13 табл.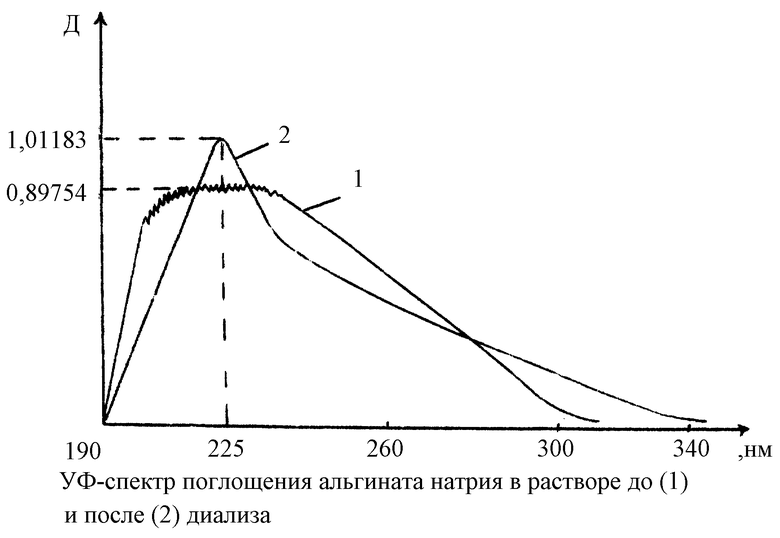
Способ получения биологически активных веществ из ламинарии для медицинских целей, отличающийся тем, что сырье обезжиривают хлороформом в массообъемном отношении сырье: хлороформ 1: 20 в течение 1,5 ч, затем проводят его последовательную экстракцию этанолом, водой и щелочным раствором, полученные экстракты диализуют через целлофановую мембрану в течение 2, 6 и 6 ч соответственно, причем водный и щелочной экстракты до стадии диализа трехкратно выдерживают при 4oС по часу с промежуточным самопроизвольным доведением температуры до комнатной, водный диализат обрабатывают 90%-ным спиртом этиловым, осаждая полисахаридно-белковый комплекс, содержащий восстанавливающие сахара, вместе с фукоиданом и ламинараном, а из щелочного диализата осаждают альгинат натрия, осадки сушат методом лиофильной сушки при -13oС в течение 70 и 50 мин соответственно.
| СПОСОБ ПОЛУЧЕНИЯ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ ИЗ ЛАМИНАРИИ | 1991 |
|
RU2028153C1 |
| СПОСОБ ПЕРЕРАБОТКИ БУРЫХ ВОДОРОСЛЕЙ | 1998 |
|
RU2132622C1 |
| Промысловые водоросли СССР | |||
| Справочник | |||
| / Под ред | |||
| В.Б.Возжинской | |||
| - М.: Пищевая промышленность, 1971, с | |||
| Мяльно-трепальный станок для обработки тресты лубовых растений | 1922 |
|
SU200A1 |
Авторы
Даты
2002-12-20—Публикация
2001-07-16—Подача