Настоящее изобретение относится к составам и способам лечения эректильной дисфункции полового члена (такой, как мужская эректильная импотенция) и, в частности, к составам и способам, эффективным при лечении эректильной дисфункции при их местном нанесении на половой член.
Предпосылки настоящего изобретения
Обычно импотенцию характеризуют как невозможность развития и поддержания эрекции, достаточной для завершения полового акта. Многие мужчины страдают некоторой степенью импотенции, являющейся результатом психологических и физиологических причин. Причины импотенции многочисленны. К ним относится атония, возникшая вследствие паралича двигательных нервов (нервов, возбуждающих эрекцию) без каких-либо признаков поражения центральной нервной системы. Наоборот, импотенция может быть паретической, как результат поражения центральной нервной системы, особенно спинного мозга. С другой стороны, импотенция может быть психологической и зависеть от психических комплексов или психической нестабильности. Причина может быть и симптоматической, вызванной каким-либо другим нарушением типа повреждения нервов в области промежности, за счет чего сенсорная часть рефлекса эрекции блокируется (см., например, патент США 4801587).
К специфическим физиологическим расстройствам, которые могут быть причиной эректильной дисфункции полового члена, или мужской импотенции, и при которых наравне с психологическими причинами можно использовать настоящее изобретение, относятся, например, заболевания сосудов таза, сахарный диабет, неврогенные расстройства, побочные действия приема лекарственных средств, операции и травмы тазовой области и т.п.
Один широко используемый вариант лечения импотенции состоит в применении имплантатов, которые, по существу, являются внутренними протезами. Однако имплантаты часто предусматривают хирургическое вмешательство, они являются дорогостоящими и не всегда эффективными средствами.
Другой важный способ лечения мужской импотенции предусматривает использование лекарственных средств. Поскольку эрекция непременно включает расширение артерий полового члена, то часто патофизиологическую причину импотенции можно лечить с помощью сосудорасширяющих средств. Имеются определенные достижения в клинических и экспериментальных исследованиях по разработке новых и лучших лекарственных средств и способов их доставки и такие исследования продолжаются. Эти научные исследования являются предметом нескольких статей и опубликованных патентов, включая, например, следующие патенты США: 4801587 - Voss, et al.; 5256652 - El-Rashidy; 5336678 - Cavallini; 5583144 - Kral; 5475535 - Place, et al.; 5482039 - Place; 5451609 - Bellamy, et al.; 5242391 - Place, et al.; 5145852 - Virag; 5399581 - Laragh; 5270323 - Milne, et al.; 5236904 -Gerstenberg, et al.; 4127118 - Latorre; 5565466 - Gioco, et al.; 5492911 - Stief; 5594032 - Gonzalez-Cadavid, et al.; 5488059 - Buhl; 5439938 - Snyder, et al.
Хотя заинтересовавшемуся читателю следует непосредственно обратиться к указанным выше патентам и литературе, обсуждаемой или цитируемой в них, а также к обсуждаемой ниже литературе, приведем их краткий обзор.
Патент США 5583144 основан на использовании пипероксана для лечения эректильной импотенции, в патенте раскрыто его местное применение. В патенте описана смесь пипероксана с простагландинами, в частности с простагландином Е2 (ПГЕ2). Составы для местного применения включают гели (в том числе гидрогели), мази, кремы и т. д., но каких-либо деталей не приведено.
Однако в целом патентами выявлено, что местное или трансдермальное применение лекарственных средств непригодно или не является предпочтительным: 5451609 (инъекции внутрь пещеристого тела); 5242391 (уретральное введение); 5145582 (простагландин E1 с папаверином); 5399581 (энтеральное введение), 5270323; 5236904 (инъекции внутрь пещеристого тела) и 4127118 (инъекционное введение).
К патентам, раскрывающим местнодействущие (трансдермальные) лекарственные средства, относятся патенты США 5256652 ('652) и 5336678 ('678). В патенте '678 указано местное применение 0,1-10% миноксидила. Патентовладельцы делят лекарственные средства для лечения нарушений эрекции на три класса:
1) оральные средства, например йохимбин;
2) инъекционные средства внутрь пещеристого тела полового члена, например простагландин E1 (ПГЕ1);
3) местнодействующие лекарственные средства, например нитроглицерин.
В патенте '652 описан состав для местного применения, который содержит агент, усиливающий поглощение, и (необязательно) сосудосуживающий агент и блокатор α-рецепторов. Циклодекситрин, в частности гидроксипропил-β-циклодекстрин, является таким усиливающим поглощение агентом.
В патенте '652 содержится ссылка на патент США 4311707 ('707), раскрывающий местное применение простагландинов, включая их предполагаемое использование для лечения импотенции. В указанном патенте '652 обсуждается и патент США 4801857 ('857), в котором раскрывается мазь, используемая местно для лечения импотенции.
Следует сделать ссылки на другие патенты, которые могут представлять интерес. К ним относятся патенты США: 5587167 (состав с экстрактом корня женьшеня, применяемый местно для профилактики и лечения преждевременной эякуляции); 5565466 (корректировка сексуальной реакции человека посредством орального, подслизистого, внутриносового или ректального применения сосудорасширяющих средств); 5492911 (линсидомин в инъекциях сам по себе или в комбинации с простагландинами); 5447920 (косметический состав, включающий продукт гидроксипропил-β-циклодекстрина); 5594032 (агенты неместного назначения, индуцирующие синтетазу оксида азота); 5448059 (инъекции соединения пиридилгуанидина в пещеристое тело полового члена или его трансдермальное применение) и 5439938 (ингибиторы синтетазы оксида азота, местное применение).
Трансдермальное применение простагландинов было предметом научных исследований. В докладе под названием "Аспекты трансдермального применения простагланднов" (International Journal of Pharmaceutics, 74:229-236, 1991) Watkinson A. C. с соавторами было изучено in vitro проницаемость сквозь кожу человека простагландинов E1, E2, F1α и F2α и влияние скорости поглощения при использовании усиливающих агентов - Азона и Транскутола (2-этоксиэтоксиэтанола). Было установлено, что предварительное нанесение на кожу указанных усиливающих агентов способствует поступлению лекарственного средства. Однако в случае ПГЕ1 это усиление было не столь значительным, как в случае ПГЕ2. При предварительной обработке примерно 10% смесью Азона и Транскутола наибольшее усиление было выявлено спустя 48 часов.
Несмотря на то, что проводилось изучение местного применения нитроглицерина, миноксидила, папаверина и простагландина E1 (ПГЕ1), их эффективность, как отражено в научной литературе, недостаточна. Anderson с соавторами в работе "Лечение импотенции местным применением нитратов" (Ann. Pharmacotherapy, 27:1203-1205, 1993) приводит обзор ранней литературы и делает вывод, что в ней содержится недостаточно доказательств эффективности местного применения. В работе "Местное применение простагландина E1 для лечения нарушений эрекции" (J. Urol, 158:1828-1830, 1995а) Kim и MсVary сообщают, что только у 20% пациентов (2 из 10), получавших местно гель с содержанием 0,4% ПГЕ1, эрекция была средней устойчивости. Носитель этого местноприменяемого геля не описан. Авторы делают вывод, что гель ПГЕ1 вызывает значительное увеличение диаметра артерии пещеристого тела, создает максимум систолической скорости кровотока и, как оказалось, он обладает высокой толерантностью при применении на область гениталий и предплечья. Однако результаты местного поглощения не были убедительными. Далее отмечается, что "Гель простагландина E1 может быть перспективен в более высоких концентрациях в сочетании с разными агентами, усиливающими кожное воздействие, или с другими местнодействующими средствами". Считается, что дальнейшее изучение будет непременно проведено.
В другом исследовании значительное усиление эректильной реакции наблюдалось после местного применения 0,5% ПГЕ1 и устойчивой эрекции, согласующейся со степенью проникновения, достигли 67% пациентов. Однако по окончании стимуляции эрекция не сохранялась (Montorsi, et al., Drugs 50 (3): 465-479, 1995а; Intern. J. Impotence Res., 7:10. 1995b). Ни в одном из этих сообщений не отмечено каких-либо побочных действий, вызванных применением ПГЕ1. Было сделано предположение, что для достижения положительной динамики может стать необходимым увеличение степени проникновения активного агента сквозь кожу и/или в ткани пещеристого тела.
Для случая папаверина была исследована местная аппликация на половой член 133-500 мг водного геля, содержащего 7, 15 или 20% папаверингидрохлорида (Kim и соавторы, J. Urol., 158:361-365, 1995b). У пациентов с повреждениями спинного мозга 15 и 20% лекарственные составы увеличивали диаметр артерий пещеристого тела полового члена (почти на 36%) и максимум систолического кровотока (почти на 26%). Однако, хотя у 3 из 17 прошедших такое лечение пациентов наблюдалось некоторое распухание полового члена и эрекция, подобным же образом они реагировали и на аппликацию геля плацебо. Тем не менее, после геля папаверина эрекция длилась дольше, хотя этот результат не является статистически важным.
Gomaa с соавторами (British Med. Journal 312:1512-5, 1995) сообщил, что местнодействующий лекарственный состав ("крем"), содержащий три активных ингредиента (3% аминофиллин, 0,25% изосорбид динитрат и 0,05% мезилат) эффективен для лечения эректильной дисфункции.
В кратком обзоре (Becher с соавторами "Двойное контролируемое вслепую с помощью плацебо испытание местного применения простагландина E1 при эректильной дисфункции"), представленном на симпозиуме по эректильной дисфункции, состоявшемся в Сан-Франциско (США) в феврале 1997 года, сообщается, что в трех предварительных исследованиях на 51 пациентах, страдающих импотенцией, использовалось три разных состава. У 33% испытуемых (5 из 15) была реакция на лекарственный состав, содержащий 2 мг ПГЕ1 (в сравнении с 13%, реагировавшими на плацебо); у 61% (11 из 18) была реакция на лекарственный состав, содержащий 4 мг ПГЕ1 (в сравнении с 39%, реагировавшими на плацебо) и у 66% (12 из 18) была реакция на лекарственный состав, содержащий 4 мг ПГЕ1 и нитроглицерин (в сравнении с 39%, реагировавшими на плацебо). В этих исследованиях у одного пациента возникло кожное высыпание и у одного пациента был случай снижения давления. Составы, используемые в этих испытаниях, не описаны.
Linet с соавторами (The New England J. of Medicine, 334(14):873-877; April 4, 1996) описал исследование, касающееся эффективности и безопасности инъекционного введения алпростадила внутрь пещеристого тела полового члена для лечения эректильной дисфункции у мужчин. Помимо других побочных эффектов, 54 из 235 мужчин (23%) испытывали боль в половом члене. Алпростадил представляет собой синтетический простагландин Ei. В сопроводительной редакционной статье (L. Lipschultz, стр. 913-14) исследование, проведенное Linet, характеризуется как "наиболее перспективное из до сих пор предпринятых исследований, охватывающее многочисленные лечебные учреждения по инъекции единственного лекарственного средства (сноска опущена). Не неожиданно авторами было обнаружено, что алпростадил обеспечивает существенно лучшую эрекцию, чем плацебо, и что эта реакция зависит от дозы". В этой редакционной статье объясняется далее, что из исследованных 577 мужчин 69% прошли полное 6-месячное испытание; 87% сообщили о том, что указанные инъекции вызвали достаточную сексуальную активность. 31% испытуемых, которые не завершили это исследование, были недовольны отсутствием эффективности. У 683 мужчин отмечались побочные действия, а 50% сообщали о болезненности полового члена. В различных исследованиях с применением алпростадила из-за сильных болей прервали терапию 17%, а еще 22% испытывали боли - от слабой до умеренной. Доктор Lipschultz делает вывод, что инъекции внутрь пещеристого тела полового члена представляют собой хорошо адаптированный и эффективный способ лечения эректильной дисфункции, в то время как "другие пути введения алпростадила типа лечебной уретральной системы (ссылка опущена) и местнодействующего лекарственного геля10 еще не дали подобных результатов". Ссылка 10 относится к упомянутой выше статье Kim и McVary (1995a).
В еще более недавней научной работе, проведенной Padma-Nathan с соавторами и посвященной лечению эректильной дисфункции алпростадилом, использовался трансуретральный механизм доставки (The New England J. of Medicine, 336 (10:1-7, January 2, 1997). В этом эксперименте на 996 мужчинах почти 88% полностью завершили трехмесячный курс лечения. Было установлено, что трансуретральное введение алпростадила эффективно для 69% мужчин, получавших этот препарат. Однако во время клинического испытания о боли в половом члене (характеризующейся как умеренная) сообщили почти 36% мужчин, в то время как из-за этой боли прекратило испытание более 2%. При лечении в домашних условиях сообщения о боли в половом члене поступали после 10,8% введений алпростадила, и эти сообщения были сделаны почти 33% мужчин. Авторы работы ссылаются (см. стр. 6) на другие способы доставки лекарственного средства, в том числе содержащий простагландин Е2 интрауретральный крем, который наносится на уретральный проход. Из 20 испытуемых мужчин в 30% случаев поступали сообщения о сильной степени распухания полового члена. Также авторы считают предварительное исследование, проведенное Kim и McVary по трансдермальному применению ПГЕ1 для создания устойчивой эрекции, неудавшимся. Это, по-видимому, связано с недостаточным переносом этого лекарственного средства сквозь кожный покров.
Из патента США 4861764, принадлежащего Carlos M. Samour и Stefanous Daskalakis (и в целом соотнесенного с предметом заявки), известно, что 1,3-диоксоланы и 1,3-диоксаны, в том числе, например, 2-н-пентил-, 2-н-гептил-, 2-н-нонил-, 2-н-ундецил-, пентилен-1,5-бис-1,3-диоксоланы, 2-н-нонил-, 2-н-ундецил-, 2-(2',6'-диметил-2'-гептадиенил)-1,3-диоксаны, пригодны в качестве агентов, усиливающих чрезкожное поглощение, используемых для увеличения проницаемости сквозь кожу терапевтических агентов.
Как описано ранее в частично соотнесенном с заявкой патенте США 5527797, принадлежащем Eisenberg и Samour, указанные выше 1,3-диоксаны, 1,3-диоксоланы и другие алкил- или алкенилзамещенные соединения общей формулы R-X (где R представляет собой С5-С28 алкил или алкенил; Х представляет собой 1,3-диоксан, 1,3-диоксолан; 5-, 6-, 7- или 8-членный лактам; циклоалкиленкарбонат, -СООН, -ОН; -COOR' (R' представляет собой низший алкил или незамещенный низший алкил); -(ОСН2СН2)n-ОН (где n -целое число от 1 до 20); -OC(О)R', R'OC(О)-; -C(О)N(R')2; ацетали и полуацетали можно использовать как нерастворимые в воде или в значительной степени нерастворимые в воде липидные модификаторы рогового слоя эпидермиса с целью усиления передачи заряженных молекул через кожный покров при ионофорезе.
Недавно опубликованный патент США 5620980, принадлежащий С. Samour и также в целом соотнесенный с настоящей заявкой, раскрывает использование 1,3-диоксоланов и 1,3-диоксанов в лекарственном местнодействующем составе, содержащем миноксидил, для лечения выпадения волос.
В описанных выше работах не содержится указаний, которые могли бы заставить практикующих врачей понять или поверить, что 1,3-диоксоланы и 1,3-диоксаны или ацетали будут пригодны для усиления проникновения простагландинов, особенно простагландина E1 (ПГЕ1) или любого иного сосудорасширяющего средства или другого лекарственного средства, используемого при лечении эректильной дисфункции. На самом деле, по предыдущим исследованиям применение этих соединений, усиливающих проницаемость кожного покрова, вместе с ПГЕ1, фентоламином, празолином и т.п. можно рассматривать как свидетельство противоположного.
Например, хотя известно, что диоксаны и диоксаланы представляют собой агенты, усиливающие проницаемость, не следует ожидать доставки аваскулярным способом повышенных уровней лекарственного средства непосредственно на нужное место глубоко под кожей. Предполагается, что в высокой степени васкуляризованная дерма удалит лекарственное средство быстро, еще прежде, чем это средство сможет проникнуть в расположенные глубже целевые ткани; в нашем случае это - само пещеристое тело и спонгиоза. Более того, пещеристое тело полового члена покрыто плотной тканью - белочной оболочкой, чьи "барьерные" свойства существенно отличны от аналогичных свойств самой кожи.
Далее, слой рогового эпидермиса на головке полового члена, являющейся тем местом, где благодаря его соединению с указанным выше пещеристым телом наиболее желательно максимальное поглощение, фактически не обладает основными "барьерными" свойствами кожи. Поскольку 1,3-диоксаны, 1,3-диоксаланы и ацетали хорошо известны как агенты, усиливающие проницаемость кожи, механизм действия которых состоит во временном разрыве слоя рогового эпидермиса, то не следует ожидать, что проникновение терапевтически активных количеств лекарственных средств сквозь неороговевшую структуру этого органа усилится.
Хотя это конкретно не касается указанных выше сведений о местнодействующих лекарственных составах для лечения эректильной дисфункции, ПГЕ1 в значительной степени нерастворим в воде. Попытки увеличить его растворимость, повышая рН системы, имеют ограниченное применение, так как при рН выше рК свободной кислоты стабильность ПГЕ1 снижается.
Следовательно, предметом настоящего изобретения является обеспечение простагландинового состава, пригодного для местной доставки при лечении эректильной дисфункции полового члена.
Связанный с ним предмет изобретения состоит в обеспечении местнодействующего лекарственного состава трансдермальной доставки, который более эффективен, чем известные лекарственные составы, и более прост в применении, чем инъекционные лекарственные составы или имплантаты.
Еще одним предметом настоящего изобретения является обеспечение для лечения эректильной дисфункции полового члена такого местнодействующего лекарственного состава, при трансдермальной доставке активного агента которого указанный состав можно наносить только на головку полового члена.
КРАТКОЕ ИЗЛОЖЕНИЕ НАСТОЯЩЕГО ИЗОБРЕТЕНИЯ
Приведенные выше цели настоящего изобретения, которые так же, как и другие его цели, станут более очевидны из приведенного ниже детального описания, достигаются использованием состава для местного трансдермального нанесения на половой член нуждающихся в этом пациентов. Указанный состав содержит:
(а) фармакологически эффективное количество простагландина E1;
(б) эффективное количество соединения, усиливающего чрезкожную проницаемость, которое выбирают из группы, включающей С6-С20-гидрокарбилгруппу, замещенный 1,3-диоксан, 1,3-диоксалан и ацеталь;
(в) фармацевтически эффективный носитель, содержащий:
(i) смесь этилового спирта и воды, пригодную для того, чтобы сделать указанные компоненты (а) и (б) растворимыми;
(ii) смесь изопропилового спирта и воды, пригодную для того, чтобы сделать указанные компоненты (а) и (б) растворимыми; или
(iii) смесь пропиленгликоля с этанолом или изопропиловым спиртом или с обоими указанными спиртами;
(г) эффективное для гелеобразования количество гелеобразующего агента; и, необязательно,
(д) снимающее раздражение эффективное количество метанола.
Согласно другому аспекту настоящее изобретение обеспечивает способ лечения эректильной дисфункции полового члена пациента, нуждающегося в этом. Этот способ состоит в местном нанесении на область гениталий этого пациента состава, содержащего: фармакологически эффективное количество простагландина E1 в присутствии эффективного количества соединения, усиливающего чрезкожную проницаемость и отобранного из группы, включающей С6-С20-гидрокарбилгруппу, замещенный 1,3-диоксан, 1,3-диоксалан и ацеталь, причем указанный простагландин E1 и соединение, усиливающее чрезкожную проницаемость, растворяют в фармакологически приемлемом водно-спиртовом носителе, содержащем этиловый спирт и воду, изопропиловый спирт и воду, или в неводном носителе, содержащем этиловый спирт и/или изопропиловый спирт; и загуститель, количество которого способно удержать на половом члене пациента простагландин E1, и соединение, усиливающее чрезкожную проницаемость.
Согласно воплощению настоящего изобретения местнодействующий состав наносят только на головку полового члена.
ДЕТАЛЬНОЕ ОПИСАНИЕ И ПРЕДПОЧТИТЕЛЬНЫЕ ВОПЛОЩЕНИЯ
Составы и способ настоящего изобретения можно применять для лечения любого из состояний, лежащих в основе эректильной дисфункции полового члена или мужской импотенции, в том числе, например, заболевания сосудов таза, сахарный диабет, неврогенные расстройства, операции тазовой области, побочные действия приема других лекарственных средств, травма и психологические проблемы.
Составы по настоящему изобретению предназначены для местного неинвазивного нанесения на область гениталий, главным образом на половой член, на весь половой член целиком или предпочтительно непосредственно на его головку. Помимо этого, указанный состав можно наносить на мошонку и/или промежность. Одно главное преимущество настоящего изобретения состоит в том, что указанный состав эффективен даже при нанесении только на головку полового члена; другое преимущество состоит в снижении таких побочных эффектов, как чувство жжения или боль.
Термин "неинвазивный" означает, что лечение не требует прокола кожи, хирургического смещения ткани или любого другого вида хирургического вмешательства, включая трансуретральное применение.
Активным ингредиентом лекарственного состава по настоящему изобретению является простагландин E1 (ПГЕ1) [11,15-дигидрокси-9-оксопрост-13-ен-1-оевая кислота; 3-гидрокси-2-(3-гидрокси-1-октенил)-5-оксоциклопентагептаноевая кислота] , известный как сосудорасширяющее средство. Однако можно использовать и другие простагландины, такие как простагландин Е2 (ПГЕ2), или простагландинмиметики или другие лекарственные средства, пригодные для лечения эректильных дисфункций полового члена, например папаверин (1-[3,4-диметоксифенил)метил] -6,7-диметоксиизохинолин), диоксилин, этаверин (1-[(3,4-диэтоксифенил)метил] -6,7-диэтоксиизохинолин), фентоламин (3-([4,5-дигидро-1Н-имидазол-2-ил)метил] (4-метилфенил)аминофенол), празосин (1-(4-амино-6,7-диметокси-2-хиназолинил)-4-(2-фуранилкарбонил)пиперазин), моноксидил, нитроглицерин, α-блокаторы, доноры оксида азота и пептиды. Особенно предпочтительны смеси ПГЕ1 с фентоламином или празосином; например смеси с соотношением ПГЕ1 и фентоламина или празосина от 1:200 до 1:1, предпочтительно от 1:100 до 1:5, более предпочтительно от 1:50 до 1:10.
Как правило, количество активного ингредиента, которое следует применить, будет зависеть от таких факторов, как тип имеющегося нарушения, степень его тяжести, возраст пациента, количество и тип усиливающего агента. Обычно приемлемые результаты для большинства пациентов обеспечивает ПГЕ1 в количестве от примерно 25 мг до примерно 4 мг на каждую аппликацию, предпочтительно от примерно 50 мг до примерно 2,5 мг ПГЕ1, более предпочтительно от примерно 125 мг до примерно 1,5 мг ПГЕ1). Следовательно, в составы для местного применения необходимо включать ПГЕ1 в количествах примерно от 0,001 до 5,0% от общего веса состава (если иного не оговорено, то все используемые здесь проценты, процентные количества и соотношения являются весовыми), предпочтительно от 0,05 до 1,5%, более предпочтительно - примерно от 0,05 до 1,0%. При использовании ПГЕ1 в сочетании с другим активным ингредиентом (таким, как фентоламин или празосин) общее количество активных ингредиентов может совпадать с указанными выше пределами. Аналогично, если фентоламин или празосин используют вместо ПГЕ1, то количество активного ингредиента может совпадать с указанными выше пределами.
Проникновение активного ингредиента сквозь кожу может быть увеличено до требуемого уровня, если в состав включить эффективное количество соединения, усиливающего чрезкожную проницаемость. Это соединение представляет собой 2-замещенный 1,3-диоксолан формулы (I):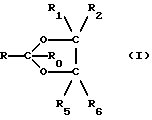
или 1,3-диоксан формулы (II):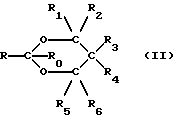
или ацеталь (в том числе полуацеталь) формулы (III):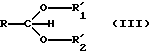
где R представляет собой С6-С20 алифатическую группу,
каждый из R1, R2, R3, R4, R5 и R6 независимо представляет собой водород или С1-С4-алифатическую группу,
каждый из R'1 и R'2 независимо представляет собой C1-C4-алифатическую группу.
Предпочтительно, чтобы R представлял собой С6-С12-алифатическую группу, особенно С7-С10-алифатическую группу. Указанная алифатическая группа может представлять собой разветвленную или неразветвленную алкильную или алкенильную группу, такую, например, как н-гексил, н-гептил, н-октил, н-нонил, н-децил, н-ундецил, н-додецил, н-гексадецил, н-октадецил, 2-метилоктил, 4-этилдецил, 8-метилдецил, н-октенил, н-стеарил и им подобные. Особенно предпочтительны такие неразветвленные алкильные группы, как н-гептил, н-октил, н-нонил и н-децил.
C1-C4 алифатическая группа может представлять собой, например, метил, этил, н-пропил, изопропил, н-бутил, трет-бутил, этенил и им подобные. Предпочтительными алифатическими группами для R1-R6 и для R'1 и R'2 являются алкильные группы, особенно алкилы, имеющие от 1 до 6 атомов углерода, главным образом - этил. Предпочтительно, чтобы все R1-R6 могли представлять собой водород.
Количество соединения, усиливающего проницаемость, следует подбирать таким, чтобы с учетом таких факторов, как побочные эффекты, носитель и тому подобные, обеспечивалась необходимая скорость доставки активного соединения. Обычно указанное соединение в количестве примерно от 0,5 до 25% от веса всего состава, предпочтительно от примерно 2 до примерно 15%, главным образом примерно от 3 до 10% должно обеспечивать стабильность и эффективность состава.
Обычно указанные составы приготавливают в виде гелей, главным образом водно-спиртовых. Однако и другие формы, такие как, например, лосьоны, кремы, муссы, аэрозоли, мази, смазки и т. п., можно использовать при условии, что указанный лекарственный состав при его нанесении на гениталии останется на своем месте (т.е. не будет стекать) в течение времени, достаточного для распределения этого состава по всей поверхности полового члена пациента, а предпочтительно - только по головке полового члена.
Помимо приведенных выше различных форм состава, составы для применения могут находиться в любой из известных форм доставки лекарственных средств, включая, например, однократную лекарственную форму и лекарственную форму многократного использования (т. е. лекарственная форма многократного использования в одной упаковке или контейнере), а также нерасфасованные лекарственные средства. В качестве примеров однократной лекарственной дозы можно отметить, например, шприц-тюбик, капсула геля, блистерная упаковка и им подобные. Нерасфасованные лекарственные средства можно сохранять, например, в тубах, бутылях, банках, помпах, аэрозольных контейнерах и подобных емкостях, изготовленных из стекла, в емкостях с металлическим или пластиковым покрытием. Опять-таки, приготовление лекарственного состава и упаковка фармацевтических продуктов понятны в пределах имеющегося в этой области опыта.
Также в границах настоящего изобретения и в некоторых случаях для увеличения стабильности (например, внешний вид состава, к примеру, разделение фаз; химическая стабильность ингредиентов) нужно обеспечить, чтобы указанный состав существовал в двух или более частях (обычно в двух), причем, чтобы соединение, усиливающее проницаемость, находилось отдельно по крайней мере от простагландинового (ПГЕ1) компонента - в отдельном контейнере или в отдельной части того же контейнера. Состав из двух частей, перемешиваемый непосредственно перед использованием, особенно удобен, если усиливающим агентом является ацеталь формулы (III) и 1,3-диоксоланы и 1,3-диоксаны. В связи с этим ацетали и в меньшей степени диоксоланы и диоксаны подвержены гидролизу при предпочтительно кислом рН указанного состава (например, рН от примерно 5 до примерно 6). Таким образом, сохранение усиливающего агента вплоть до использования отдельно от остальных ингредиентов состава должно в значительной степени предотвратить гидролиз усиливающего агента (если таковой имеет место). При применении в двух частях, когда усиливающий агент содержится отдельно от ПГЕ1, предпочтительно, чтобы указанный усиливающий агент смешивали с ПГЕ1 и с другими компонентами до нанесения на область гениталий.
Поэтому, поскольку сохранять необходимый лекарственный состав из ингредиентов обычно удобнее как цельный состав, в нашем случае часто возникает практическое ограничение относительно хранения состава или относительно срока хранения. То есть оптимальное значение рН, обеспечивающее стабильность ПГЕ1, - относительно низкое и оно составляет примерно 5, в то время как диоксан, диоксолан и, главным образом, ацеталь-агенты, усиливающие чрезкожную проницаемость, наиболее стабильны при более высоком значении рН, обычно 6 или более. Таким образом, отдельный лекарственный состав будет обычно ограничивать стабильность одного из своих компонентов или их обоих в большей или меньшей степени в зависимости от значения рН, присущего данному составу. Поэтому, вероятно, более желательно, чтобы ПГЕ1 и усиливающий агент(ы) находились в отдельных составах или в отдельных ячейках одного и того же контейнера, где значение рН каждого из них оптимизировано с точки зрения его стабильности, причем перемешивать эти ингредиенты следует непосредственно перед использованием состава. Аналогично, если активный ингредиент включает празосин, то состав должен быть неводным, т.е. спиртовым (этанол и/или изопропанол) и пропиленгликольным, или вплоть до применения состава празосин следует хранить отдельно от водной среды.
Кроме того, на стабильность ПГЕ1 может влиять его физическая форма и, главное, наблюдается, что обычно он более стабилен в твердом состоянии, чем в растворе. Таким образом, что касается стабильности при хранении состава из двух частей, то одна из его частей должна содержать предпочтительно твердый, т. е. кристаллический ПГЕ1, который для получения единого готового для немедленного использования состава следует растворить и перемешать с жидкими ингредиентами второй части. При таких условиях кристаллический ПГЕ1 может сохранять стабильность при замораживании на период почти до 2 лет.
Однако пределы настоящего изобретения предусматривают также, что вначале на гениталии (например, на головку полового члена, или на тело полового члена, или на всю зону полового члена, включая мошонку) наносят усиливающий агент, а затем, обычно в пределах 30 мин, предпочтительно в течение 15 мин, наносят ПГЕ1 (вместе с любым другим компонентом лекарственного средства) и другие части указанного состава.
Более того, людям, квалифицированным в этой области, должно быть ясно, что с учетом растворимости, стабильности продукта, легкости применения и т. п. факторов фармацевтически приемлемый носитель может содержаться в цельном составе или в его части только с усиливающим агентом и с ПГЕ1 или с тем и другим вместе.
В таких условиях ПГЕ1 плохо растворим в воде, но полностью растворим в этаноле. Более того, указанная растворимость практически не снижается при добавлении используемого в настоящем изобретении водонерастворимого усиливающего агента.
Следовательно, в качестве носителя для ПГЕ1 и соединений, усиливающих проницаемость, предпочтителен водный или неводный спиртовой носитель, содержащий количество спирта (главным образом, этанола и/или изопропанола), достаточное для растворения по существу водонерастворимого ПГЕ1 и для смешивания с указанным усиливающим агентом. Однако обычно, в зависимости от количества усиливающего агента и ПГЕ1 в конкретном лекарственном составе, этот водно-спиртовой носитель может содержать от примерно 10 до примерно 90% этанола или изопропилового спирта, предпочтительно от примерно 60 до примерно 80% этанола и примерно от 45 до 55% изопропанола. Могут быть также использованы смеси этанола и изопропанола при соотношениях, обеспечивающих необходимую растворимость ПГЕ1 и совместимость с указанным усиливающим агентом.
Общее количество водного или неводного спиртового носителя будет зависеть от количества ПГЕ1, других активных ингредиентов, количества и типа усиливающего агента и от формы конкретного лекарственного состава (например, гель, крем, мазь и т.п.). Обычно водный или неводный спиртовой носитель можно использовать в количествах от примерно 70 до примерно 90%.
В предпочтительных составах, используемых в форме геля, загуститель (типа гидроксипропилцеллюлозы) следует включать как гелеобразующий агент. Однако возможно применение и любого другого фармацевтически приемлемого загустителя/гелеобразующего агента. Например, можно обратить внимание на другие эфиры целлюлозы, полимерные загустители (например, полимеры акриловой кислоты, загустители Carbopol® и т.д., ксантановая смола, гуаровая смола) наравне с неорганическими загустителями/гелеобразующими агентами. Количество загустителя не является особо критичным и его можно подбирать таким, чтобы были обеспечены консистенция или вязкость целевого продукта, позволяющие его свободное нанесение на гениталии, но чтобы этот продукт не стал настолько водянистым или рыхлым, что он останется на том участке, куда был нанесен. В связи с этим часто может быть предпочтительным, чтобы при нанесении указанного состава на гениталии пациент стоял. Обычно желаемый эффект обеспечивает загуститель в количестве до примерно 5% от веса всего состава, например от 0,1 до примерно 2% (в зависимости от молекулярного веса загустителя).
Хотя составы по настоящему изобретению обычно не имеют побочных эффектов или имеют незначительные побочные эффекты (главным образом, боль в половом члене), некоторая часть пациентов из генеральной совокупности может испытывать незначительный дискомфорт типа ощущения жжения, в особенности при нанесении состава на тело полового члена. При нанесении состава на головку полового члена склонность возникновения ощущений жжения снижается. В этом состоит еще одно преимущество настоящего изобретения, а именно указанные составы более эффективны при нанесении исключительно на головку полового члена. Как отмечалось выше, была неожиданной эффективность указанного состава при нанесении исключительно на головку полового члена (неороговевшую ткань) из-за доказанного воздействия усиливающих агентов, таких как диоксолановый, диоксановый и ацетальный агент.
В любом случае, особенно, если указанный состав предназначен для нанесения на половой член целиком и/или на область гениталий, он должен включать (и это входит в границы настоящего изобретения) незначительное количество мягкого местного анестезирующего средства или агента, снимающего чувство жжения, или противозудного агента (например, до примерно 5%, главным образом до примерно 3%, т.е. от примерно 0,1 до примерно 2%). Хотя известно много таких агентов, удовлетворительные результаты были достигнуты при использовании ментола. Можно использовать и другие мягкие местные анестезирующие средства, такие как, например, хлорбутанол, камфара, бензиловый спирт и т.п.
Для лечения эректильной дисфункции и при предпочтительном нанесении на головку полового члена предпочтительное количество наносимого лекарственного состава составляет от примерно 0,1 до примерно 1 мл, предпочтительно примерно от 0,1 до 0,5 мл, более предпочтительно примерно от 0,2 до 0,5 мл. Для случая такого предпочтительного применения указанные количества активного ингредиента в лекарственном составе составляют в процентных долях примерно от 0,001 до 5,0%, предпочтительно от 0,05 до 1,5%, более предпочтительно от 0,05 до 1,0%.
Для типичного, характерного для настоящего изобретения лекарственного состава в форме геля, содержащего 0,5% ПГЕ1 и 5% 2-н-нонил-1,3-диоксолана, могут подходить дозировки (в зависимости от подразумеваемого назначения и зоны нанесения) от примерно 0,1 до примерно 0,5 мл, предпочтительно примерно от 0,2 до 0,3 мл, например такая, как 0,25 мл.
Ниже (см. таблицу) приведены типичные лекарственные составы спиртовых (неводных) гелей и водно-спиртовых гелей согласно настоящему изобретению, причем в интервалах, обозначенных как "широкий", "промежуточный" и "предпочтительный", указаны количества в весовых частях.
Хотя рН указанных составов сложно измерить из-за кислой природы простагландина E1, они склоны обладать средней кислотностью. Как правило, в составах по настоящему изобретению использование агентов, меняющих рН (например, кислот или оснований), не является предпочтительным.
Особенным преимуществом предпочтительных составов по настоящему изобретению является то, что они остаются стабильными при разделении фаз и распаде продукта в широком диапазоне условий хранения. Например, лекарственные составы водного и неводного спиртового гелей, описанные выше, сохраняют стабильность в диапазоне по крайней мере от -18oС до примерно 10oС в течение срока от нескольких месяцев до нескольких лет в зависимости от температуры хранения. Чем ниже эта температура, тем выше стабильность. В пределах указанного диапазона температур определенная концентрация ПГЕ1 остается на уровне более 80% от его исходной концентрации. При более низких температурах, которые в некоторых случаях могут вызвать разделение фаз ПГЕ1, указанный состав можно вернуть в исходное состояние путем оттаивания. Следовательно, часто предпочтительно, чтобы эти составы вплоть до их использования были заморожены. Другим главным преимуществом настоящего изобретения является тот факт, что благодаря увеличению эффективности ПГЕ1 можно использовать незначительное количество активного ингредиента, тем самым уменьшая вероятность раздражения или других побочных эффектов. Хотя составы по настоящему изобретению эффективны без дополнительных вспомогательных средств, в некоторых случаях можно достичь лучшей эрекции (т.е. большей приспособленности для половых сношений), главным образом тогда, когда нанесение указанного состава непосредственно и только на голову полового члена сочетают с местным трансдермальным нанесением активного ингредиента (как это описано выше) и с помощью механического венозного жгута (типа резиновой ленты) или иного зажимающего устройства. Подобные устройства хорошо известны. В контексте настоящего изобретения предполагается, что помощь механического зажимающего устройства, накладываемого на основание тела полового члена или около него, может увеличить эффективность активного ингредиента за счет того, что указанный активный ингредиент более эффективно направляется ко входу в пещеристое тело полового члена.
Отсылочный пример 1
Согласно настоящему изобретению был приготовлен приведенный ниже водно-спиртовой гель, %:
Простагландин E1 - 0,1
2-н-нонил-1,3-диоксолан - 5,0
Гидроксипропилцеллюлоза - 1,0
Растворитель (этанол/вода:70/30) - до 100
Для получения прозрачного раствора 2-н-нонил-1,3-диоксолан добавляют к растворителю (этанол/вода) при перемешивании. Потом добавляют при перемешивании твердый (кристаллический) ПГЕ1 (коммерчески доступный из ряда различных источников) и оставляют для растворения. После этого добавляют гидроксипропилцеллюлозу (порошок) при непрерывном перемешивании до тех пор, пока не будет отмечено равномерное гелеобразование.
Перемешивание проводят при комнатной температуре, но при необходимости его можно осуществлять и при более низкой температуре. Также при необходимости для смешивания ингредиентов в условиях уменьшенного сдвига перемешивание можно осуществить с помощью вальцовой мельницы.
Отсылочный пример 2
Согласно настоящему изобретению был приготовлен приведенный ниже водно-спиртовой гель, %:
Простагландин E1 - 0,5
2-н-нонил-1,3-диоксолан - 5,0
Гидроксипропилцеллюлоза - 1,0
Растворитель (этанол/вода:70/30) - До 100
Отсылочный пример 3
Согласно настоящему изобретению был приготовлен приведенный ниже водно-спиртовой гель, %:
Простагландин E1 - 0,5
2-н-нонил-1,3-диоксолан - 5,0
Гидроксипропилцеллюлоза - 1,0
Ментол - 0,5
Растворитель (этанол/вода:70/30) - До 100
Отсылочный пример 4
Согласно настоящему изобретению был приготовлен приведенный ниже водно-спиртовой гель, %:
Простагландин E1 - 0,1
2-н-нонил-1,3-диоксолан - 5,0
Гидроксипропилцеллюлоза - 1,0
Ментол - 0,5
Растворитель (этанол/вода:70/30) - До 100
Отсылочный пример 5
Согласно настоящему изобретению был приготовлен приведенный ниже водно-спиртовой гель, %:
Простагландин E1 - 0,1
2-н-нонил-1,3-диоксолан - 5,0
Гидроксипропилцеллюлоза - 1,0
Ментол - 0,5
Растворитель (этанол/вода:50/50) - До 100
Пример 1
а) 0,25 мл геля, описанного в отсылочном примере 4, нанесли на головку полового члена 57-летнего человека. Некоторое распухание наблюдалось в течение 30 мин.
б) В другом случае 0,25 мл геля, описанного в отсылочном примере 2, нанесли на головку полового члена того же мужчины. Некоторое распухание наблюдалось в течение 20 мин. Полная нестимулируемая эрекция наблюдалась в течение 30 мин и она продолжалась в течение 1 ч.
в) В другом случае 0,25 мл геля, описанного в отсылочном примере 3, нанесли на головку полового члена этого же мужчины. Некоторое распухание наблюдалось в течение 30 мин. Полная эрекция наблюдалась при наглядной стимуляции 45 мин после нанесения геля.
г) В двух различных случаях тому же мужчине на головку полового члена наносили 0,25 мл геля плацебо, т.е. геля, не содержащего простагландин E1. Ни в одном из этих случаев не наблюдалось никакого распухания или эрекции, даже при наглядной стимуляции.
Пример 2
0,25 мл геля, описанного в отсылочном примере 2, нанесли на головку полового члена 44-летнего мужчины. Он почувствовал, что приток крови или увеличение полового члена было больше, чем обычно наблюдаемое при половом акте.
Пример 3
а) 0,5 мл геля, описанного в отсылочном примере 4, нанесли на головку полового члена 47-летнего мужчины. Этот человек сообщил о приятном ощущении от того, что всегда несколько часов после применения геля возникала частичная эрекция - даже после смывания указанного геля с поверхности кожи.
б) В другом случае этому же мужчине на головку полового члена нанесли 0,25 мл геля, описанного в отсылочном примере 5, при этом были получены аналогичные позитивные результаты.
Пример 4
Состав из отсылочного примера 1 изучали при клинических испытаниях под контролем плацебо на 34 пациентах, страдающих импотенцией. В качестве плацебо использовался лекарственный состав, описанный в отсылочном примере 1 и 2, но не содержащий простагландин Е1. Лекарственный состав исследовали путем нанесения на половой член таких его объемов, которые содержали бы 0,5 мл ПГЕ1 (доза А) или 1,0 мл ПГЕ1 (доза Б). Эрекция наблюдалась у 8 из 12 мужчин (67%), получивших дозу А и у 7 из 10 мужчин (70%), получавших дозу Б, причем при получении геля плацебо эрекция наблюдалась только у 2 из 12 мужчин.
| название | год | авторы | номер документа |
|---|---|---|---|
| СРЕДСТВО КОРРЕКЦИИ МУЖСКИХ СЕКСУАЛЬНЫХ ДИСФУНКЦИЙ | 2008 |
|
RU2421211C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ИНДУЦИРОВАНИЯ ЭРЕКЦИИ У МУЖЧИН (ВАРИАНТЫ) | 1992 |
|
RU2098120C1 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ СИЛДЕНАФИЛ ИЛИ АЛПРОСТАДИЛ, МИНОКСИДИЛ ИЛИ ЭУФИЛЛИН, ТЕСТОСТЕРОН ИЛИ ЙОХИМБИН И ЛИПОСОМЫ ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ | 2010 |
|
RU2482847C2 |
| ИСПОЛЬЗОВАНИЕ ИНГИБИТОРОВ СGМР-ФОСФОДИЭСТЕРАЗЫ ДЛЯ ЛЕЧЕНИЯ ИМПОТЕНЦИИ | 1996 |
|
RU2181288C2 |
| СПОСОБ ЛЕЧЕНИЯ ЭРЕКТИЛЬНОЙ ДИСФУНКЦИИ У ПАЦИЕНТОВ, ПЕРЕНЕСШИХ РАДИКАЛЬНУЮ ПРОСТАТЭКТОМИЮ ИЛИ БРАХИТЕРАПИЮ | 2020 |
|
RU2741204C2 |
| СПОСОБ КОРРЕКЦИИ ЭРЕКТИЛЬНОЙ ДИСФУНКЦИИ У БОЛЬНЫХ САХАРНЫМ ДИАБЕТОМ | 2001 |
|
RU2201250C2 |
| СПОСОБ ЛЕЧЕНИЯ ЭРЕКТИЛЬНОЙ ДИСФУНКЦИИ "JULIA" | 2015 |
|
RU2609054C1 |
| Способ лечения эректильной дисфункции | 2016 |
|
RU2622757C1 |
| ЛЕКАРСТВЕННЫЕ ФОРМЫ, ПОЛЕЗНЫЕ ДЛЯ ЛЕЧЕНИЯ МУЖСКОЙ И ЖЕНСКОЙ ИМПОТЕНЦИИ | 2007 |
|
RU2440127C2 |
| ЛЕКАРСТВЕННЫЕ ФОРМЫ, ПОЛЕЗНЫЕ ДЛЯ ЛЕЧЕНИЯ МУЖСКОЙ И ЖЕНСКОЙ ИМПОТЕНЦИИ | 2003 |
|
RU2313357C2 |

Изобретение относится к медицине, конкретно к средствам для лечения эректильной импотенции или другой эректильной дисфункции полового члена. Сущность изобретения заключается в составе на основе простагландина E1 для местного трансдермального нанесения на половой член, изобретение также относится к способу лечения указанных нарушений. Техническим результатом изобретения является обеспечение местнодействующего лекарственного состава трансдермальной доставки, который более эффективен, чем известные лекарственные составы, и более прост в применении, чем инъекционные лекарственные составы или имплантаты. 3 с. и 17 з.п. ф-лы, 1 табл.
| КОЛОДЦЕВ СТОЯКОВ коксовых ПЕЧЕЙ | 0 |
|
SU277720A1 |
| US 5583144, 10.12.1996 | |||
| US 4311707, 19.01.1982 | |||
| US 5620980, 15.04.1997. | |||
Авторы
Даты
2003-02-20—Публикация
1998-06-15—Подача