Изобретение относится к использованию тетрациклических производных, которые являются мощными и селективными ингибиторами гуанозин-3',5'-циклофосфат-специфической фосфодиэстеразы (cGMP-специфической PDE), в лечении импотенции.
Импотенция может быть охарактеризована как потеря половой активности у мужчин в совершении полового акта и может проявляться в неспособности достижения эрекции полового члена или эякуляции, либо того и другого. Более конкретно, эректильная импотенция или дисфункция может быть охарактеризована как неспособность достижения или поддержания эрекции, необходимой для полового акта. Утверждают, что ее распространенность увеличивается с возрастом и составляет от 2 до 7% мужского населения в возрасте до 50 лет и в интервале от 18 до 75% в возрасте между 50 и 80 годами.
Сообщения о правильно контролируемых клинических испытаниях у мужчин встречаются редко, и эффективность перорально вводимых препаратов низка. Хотя и было показано, что много различных препаратов вызывают эрекцию полового члена, их эффективность ограничивается способами введения - инъекцией непосредственно в половой член, а именно интрауретральной или интракавернозальной (i. e.) инъекцией, а они не пригодны при эректильной дисфункции. Современное лечение основано на i.e. инъекции вазоактивных веществ, хорошие результаты сообщены при введении феноксибензамина, пентоламина, папаверина и простагландина E1 в моно-режиме или в комбинации; однако введение некоторых из этих агентов сопровождается болью, приапизмом и фиброзом полового члена. Было показано, что активны также активаторы калиевых каналов (КСО) и вазоактивный кишечный полипептид (VIP), однако стоимость и проблемы стабильности ограничивают применение последнего. Альтернативой i.e. введению является наложение на половой член повязки с тринитратом глицерина (GTN), что является эффективным, но вызывает побочные эффекты как у партнера, так и у партнерши.
В качестве альтернативы фармакологическому вмешательству для достижения эрекции были использованы разнообразные протезы полового члена. Получены хорошие краткосрочные результаты, но возможность инфекции и ишемии, особенно у мужчин с диабетом, не позволяют этому виду лечения стать первостепенным.
Соединения по данному изобретению являются мощными ингибиторами гуанозин-3', 5'-циклофосфат-специфической фосфодиэстеразы (cGMP PDE). В заявке GB 9514464.8, которая является документом о приоритете для настоящей заявки, описывается синтез соединений по данному изобретению и их использование для лечения импотенции. В заявке W095/19978, которая не была опубликована к дате приоритета настоящей заявки, также описывается синтез соединений по данному изобретению и их использование в лечении других болезней, связанных с ингибированием cGMP PDE. Соединения могут быть представлены следующей общей формулой (I):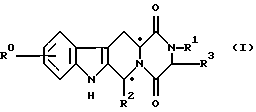
и их соли и сольваты (например, гидраты), в которых;
R0 означает атом водорода, галоида или C1-6-алкил;
R1 означает атом водорода, C1-6-алкил, С2-6-алкенил, С2-6-алкинил, галоидсодержащий C1-6-алкил, С3-8-циклоалкил, С3-8-циклоалкилсодержащий C1-3-алкил, арилсодержащий С1-3-алкил или гетероарилсодержащий С1-3-алкил;
R2 означает произвольно замещенное моноциклическое ароматическое кольцо, выбранное из группы, состоящей из бензола, тиофена, фурана и пиридина, или произвольно замещенное бициклическое кольцо,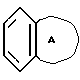
присоединенное к остальной молекуле через один из углеродных атомов бензольного кольца, где сочлененное кольцо А является 5- или 6-членным кольцом, которое может быть насыщенным либо частично, или полностью ненасыщенным и включает атомы углерода и произвольно один или два гетероатома, выбранные из группы, состоящей из атома кислорода, серы и азота; и
R3 означает атом водорода или С1-3-алкил или R1 и R3 вместе означают 3- или 4-членную алкильную или алкенильную цепь.
Соответствующие индивидуальные соединения по этому изобретению для лечения эректильной дисфункции включают:
цис-2,3,6,7,12,12а-гексагидро-2-(4-пиридилметил)-6-(3,4-метилендиоксифенил) - пиразино[2',1':6,1]пиридо[3,4-b]индол-1,4-дион;
цис-2,3,6,7,12,12а-гексагидро-6-(2,3-дигидробензо[b] фуран-5-ил)-2-метилпиразино [2',1':6,1]пиридо[3,4-b]индол-1,4-дион;
цис-2,3,6,7,12,12а-гексагидро-6-(5-бром-2-тиенил)-2-метилпиразино[2',1': 6,1] пиридо[3,4-b]индол-1,4-дион;
цис-2,3,6,7,12,12а-гексагидро-2-бутил-6-(4-метилфенил)-пиразино[2', 1': 6,1]пиридо [3,4-b]индол-1,4-дион;
(6R, 12aR)-2,3,6,7,12,12а-гексагидро-2-изопропил-6-(3,4-метилендиоксифенил)-пиразино [2',1':6,1]пиридо[3,4-b]индол-1,4-дион;
(6R, 12aR)-2,3,6,7,12,12а-гексагидро-2-циклопентил-6-(3,4-метилендиоксифенил)-пиразино [2',1':6,1]пиридо[3,4-b]индол-1,4-дион;
(6R, 12aR)-2,3,6,7,12,12а-гексагидро-2-циклопропилметил-6-(4-метоксифенил)-пиразино[2',1':6,1]пиридо[3,4-b]индол-1,4-дион;
(6R, 12aR)-2,3,6,7,12,12а-гексагидро-6-(3-хлор-4-метоксифенил)-2-метилпиразино [2',1':6,1]пиридо[3,4-b]индол-1,4-дион;
(6R, 12aR)-2,3,6,7,12,12а-гексагидро-2-метил-6-(3,4-метилендиоксифенил)-пиразино[2',1':6,1]пиридо[3,4-b]индол-1,4-дион;
(6R, 12aR)-2,3,6,7,12,12а-гексагидро-6-(3,4-метилендиоксифенил)пиразино [2',1':6,1]пиридо[3,4-b]индол-1,4-дион;
(5аR, 12R, 14аS)-1,2,3,5,6,11,12,14а-октагидро-12-(3,4-метилендиоксифенил)-пирроло[1",2":4',5']пиразино[2',1':6,1] пиридо[3,4-b]индол-1,4-дион;
цис-2,3,6,7,12,12а-гексагидро-2-циклопропил-6-(3,4-метилендиоксифенил)-пиразино[2',1':6,1]пиридо[3,4-b]индол-1,4-дион;
(3S, 6R, 12aR)-2,3,6,7,12,12а-гексагидро-3-метил-6-(3,4-метилендиоксифенил)-пиразино[2',1':6,1]пиридо[3,4-b]индол-1,4-дион;
и их физиологически приемлемые соли и сольваты (например, гидраты).
Специфическими соединениями по данному изобретению являются:
(6R, 12аR)-2,3,6,7,12,12а-гексагидро-2-метил-6-(3,4-метилендиоксифенил)пиразино[2',1':6,1]пиридо[3,4-b]индол-1,4-дион (соединение А); и
(3S, 6R, 12аR)-2,3,6,7,12,12а-гексагидро-2,3-диметил-6-(3,4-метилендиоксифенил)-пиразино[2',1':6,1]пиридо[3,4-b]индол-1,4-дион (соединение В);
и их физиологически приемлемые соли и сольваты (например, гидраты).
Неожиданно было обнаружено, что соединения формулы (I) и, в частности, соединения А и В пригодны для лечения эректильной дисфункции. Более того, соединения могут вводиться перорально, устраняя тем самым недостатки, связанные с i.e. введением. Таким образом, настоящее изобретение связано с использованием соединений формулы (I) и, в частности, соединений А и В или их фармацевтически приемлемой соли или фармацевтического состава, содержащего каждый объект, в производстве медикамента для лечебной или профилактической обработки эректильной дисфункции у млекопитающих мужского пола, включая человека.
Фармацевтически приемлемые соли соединений формулы (I) и, в частности, соединений А и В, которые содержат основный центр, являются кислотоприсоединяемыми солями, образуемыми при взаимодействии с фармацевтически приемлемыми кислотами. Примеры включают гидрохлоридную, гидробромидную, сульфатную или бисульфатную, фосфатную или кислую фосфатную, ацетатную, бензоатную, сукцинатную, фумаратную, малеатную, лактатную, цитратную, тартратную, глюконатную, метансульфонатную, бензолсульфонатную или п-толуолсульфонатную соли. Соединения формулы (I) и, в частности, соединения А и В могут также образовывать фармацевтически приемлемые соли с металлами, в частности со щелочными металлами, с основаниями. Примеры включают натриевые и калиевые соли.
Показано, что соединения по настоящему изобретению являются мощными и селективнми ингибиторами cGMP-специфической PDE. В настоящее время неожиданно было обнаружено, что человеческое кавернозное тело содержит три различных PDE фермента. Далее неожиданно было обнаружено, что преобладающей PDE является cGMP PDE. Вследствие селективного ингибирования PDE V соединениями по данному изобретению они могут повышать уровни cGMP, которые, в свою очередь, могут способствовать релаксации ткани кавернозного тела и последующей эрекции полового члена.
Хотя соединения по данному изобретению вначале рассматривались как средства для лечения эректильной дисфункции или половой дисфункции мужчин, они могут также оказаться полезными в лечении женской половой дисфункции, включая оргазменную дисфункцию, связанную с клиторальными нарушениями.
Обычно у мужчин предпочтительным путем введения соединений по данному изобретению является пероральное введение как наиболее удобное и позволяющее избежать недостатков, связанных с i.e. введением. В обстоятельствах, при которых реципиент страдает от расстройства глотания или от нарушения абсорбции лекарства при пероральном применении, препарат может вводиться парентерально, например подъязычно или трансбуккально.
Для введения человеку при лечебной и профилактической обработке упомянутых выше нарушений пероральная доза соединения формулы (I) и, в частности, соединений А и В обычно будет находиться в интервале 0,5-800 мг в день для среднего взрослого пациента (70 кг). Таким образом, для типичного взрослого пациента таблетки или капсулы содержат 0,2-400 мг активного соединения в соответствующем фармацевтически приемлемом наполнителе или носителе для введения в виде однократной или многократной дозы один или несколько раз в день. Дозы для трансбуккального или подъязычного введения обычно будут находиться в интервале 0,1-400 мг в виде однократной дозы, если это необходимо. На практике врач определит необходимый дозовый режим, который будет наиболее подходящим для данного пациента, и он будет изменяться в зависимости от возраста, веса и чувствительности пациента. Упомянутые выше дозы являются типичными для обычного случая, однако в особых случаях они могут быть ниже или выше дозового интервала, что входит в сферу действия этого изобретения.
Для использования на человеке соединения формулы (I) и, в частности, соединения А и В могут быть введены как таковые, но обычно их вводят в смеси с фармцевтическим носителем, выбранным с учетом предполагаемого пути введения и стандартной фармацевтической практики. Например, соединение может быть введено перорально, трансбуккально или подъязычно в виде таблеток, содержащих наполнители, такие как крахмал или лактоза, либо в оболочке или в капсулах как таковое, или в смеси с наполнителями, или в виде эликсиров или суспензий, содержащих ароматизаторы или красители. Такие жидкие препараты могут быть получены с использованием фармацевтически приемлемых добавок, таких как суспендирующие агенты (например, метилцеллюлоза, полусинтетический глицерид, такой, как витепсол, или смеси глицеридов, такие как смесь косточкового абрикосового масла и эфиров PEG-6 (полиэтиленгликоля-6) или смеси PEG-8 и глицеридов, содержащих остатки каприловой/каприновой кислот).
При использовании в ветеринарии соединение формулы (I) и, в частности, соединение А или В, либо их нетоксичная соль вводится в соответствующей приемлемой лекарственной форме в соответствии с обычной ветеринарной практикой, и ветеринарный хирург определяет дозовый режим и путь введения, который более всего подходит для отдельного животного мужского пола.
Таким образом, изобретение включает фармацевтический состав для лечебной и профилактической обработки эректильной дисфункции у млекопитающих мужского пола, включая человека, состоящий из соединения формулы (I) и, в частности, соединения А и В или их фармацевтически приемлемой соли вместе с фармацевтически приемлемым разбавителем или носителем.
В дальнейшем предоставляется процесс приготовления фармацевтического состава для лечебной и профилактической обработки эректильной дисфункции у млекопитающих мужского пола, включая человека, состоящий в получении лекарственной формы из соединения формулы (I) и, в частности, соединения А или В, или их фармацевтически приемлемой соли и фармацевтически приемлемого разбавителя или носителя.
Изобретение предоставляет также способ обработки млекопитающего мужского пола, включая человека, с целью лечения или предотвращения эректильной дисфункции, который включает обработку упомянутого млекопитающего мужского пола эффективным количеством соединения формулы (I) и, в частности, соединения А или В либо их фармацевтически приемлемой соли или фармацевтическим составом, включающим каждый объект.
Более того, изобретение включает использование соединения формулы (I) и, в частности, соединения А или В, либо их фармацевтически приемлемой соли или фармацевтического состава, включающего каждый объект, в производстве медикамента для лечебной или профилактической обработки эректильной дисфункции у млекопитающего мужского пола, включая человека.
Соединение формулы (I) и, в частности, соединение А или В могут также использоваться в комбинации с другими терапевтическими агентами, которые могут оказаться полезными в лечении эректильной дисфункции, в основном, так, как здесь было описано. Поэтому в другом аспекте изобретение предоставляет комбинацию соединения формулы (I) и, в частности, соединения А или В с другим терапевтически активным агентом.
Упомянутая выше комбинация может быть использована в виде фармацевтической лекарственной формы, и поэтому фармацевтические составы, включающие комбинацию, как упомянутая выше, с фармацевтически приемлемым разбавителем или носителем, составляют следующий аспект изобретения.
Индивидуальные компоненты такой комбинации в раздельных фармацевтических лекарственных формах могут также вводиться или последовательно, или одновременно.
Специалисты без затруднений определят дозы известных терапевтических агентов для использования их в комбинации с соединением по данному изобретению.
Соединения по данному изобретению могут быть получены любым подходящим способом, известным специалистам, или следующими способами, которые составляют часть настоящего изобретения. Способ был, в основном, описан ранее в документе о приоритете настоящего изобретения GB 9514464.8 и в WO 95/19978. Таким образом, способ получения соединения формулы (I) включает обработку соединения формулы (II)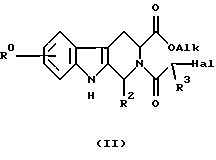
(в котором Alk означает C1-6-алкил, например метил или этил, Hal означает атом галоида, например хлора) первичным амином R1NH2 в подходящем растворителе, таком как спирт (например, метанол или этанол), или в смеси растворителей обычно при температуре от 20oС до температуры кипения (например, около 50oС).
Соединение формулы (II) может быть легко получено обработкой соединения формулы (III) соединением формулы (IV)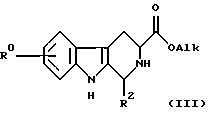
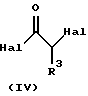
в подходящем растворителе, таком как галоидуглеводород (например, трихлорметан или дихлорметан) или простой эфир (например, тетрагидрофуран), предпочтительно в присутствии основания, такого как органический амин (например, триалкиламин, такой как триэтиламин) или карбонат, либо бикарбонат щелочного металла (например, NаНСО3). Реакция легко проходит при температуре от -20oС до +20oС (например, при 0oС).
Соединение формулы (I) может быть легко получено из соединения формулы (III) в две стадии через стадию образования соединения формулы (II), выделенного без очистки.
Соединения формулы (I) могут быть получены в виде индивидуальных энантиомеров в две стадии из соответствующего энантиомера формулы (III) или в виде смесей (например, рацематов) пар либо цис-, либо трансизомеров из соответствующих смесей пар либо цис-, либо трансизомеров формулы (III).
Индивидуальные энантиомеры соединений по данному изобретению могут быть получены из рацематов путем разделения с использованием методов разделения рацемических смесей на составляющие их энантиомеры, с использованием методов известных специалистам, например HPLC (ЖХВР, жидкостной хроматографии высокого разрешения) на колонке с хиральным сорбентом, таким как гиперсилнафтилмочевина.
Соединение формулы (III) может быть легко получено из алкилового эфира триптофана формулы (V)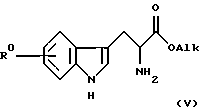
(где Alk такой, как описано ранее) или его соли (например, гидрохлорида) и альдегида R2CHO. Реакция может быть легко проведена в подходящем растворителе, таком, как галоидуглеводород (например, дихлорметан) или в ароматическом углеводороде (например, толуоле) в присутствии кислоты, такой, как трифторуксусная кислота. Реакцию удобно проводить при температуре от -20oС до температуры кипения, получая соединение формулы (III) в одну стадию. Реакцию можно проводить также в таком растворителе, как ароматический углеводород (например, бензол или толуол), при кипении с использованием насадки Дина-Старка для улавливания образующейся воды.
В реакции образуется смесь цис- и трансизомеров, которые могут быть либо индивидуальными энантиомерами, либо рацематами, состоящими из пар цис- или трансизомеров в зависимости от того, использовался ли в качестве исходного вещества рацемический или энантиомерный алкиловый эфир триптофана. Индивидуальные цис- и трансизомеры могут быть легко выделены из их смеси фракционной кристаллизацией или хроматографией (например, колоночной флеш-хроматографией) с использованием соответствующих растворителей и элюентов. Подобным образом пары цис- и трансизомеров могут разделяться хроматографией (например, колоночной флеш-хроматографией) с использованием соответствующих элюентов. Оптически чистый трансизомер может быть легко превращен в оптически чистый цисизомер с использованием подходящих способов эпимеризации. Один из таких способов включает обработку трансизомера или смеси (например, смеси в соотношении 1: 1) цис- и трансизомеров метанольным или водным раствором хлористого водорода при температуре от 0oС до температуры кипения раствора. Затем смесь подвергают хроматографии (например, колоночной флеш-хроматографии) для того, чтобы разделить образующиеся диастереоизомеры, или в процессе использования водного хлористого водорода желаемый цисизомер выпадает в осадок в виде гидрохлорида, который затем может быть отделен фильтрацией.
Фармацевтически приемлемые соли, образующиеся при добавлении кислоты к соединению формулы (I) и, в частности, к соединению А или В, которые содержат основный центр, могут быть получены обычным способом. Например, раствор свободного основания может быть обработан соответствующей кислотой либо в неизмененном виде, либо в подходящем растворе, и образующуюся соль выделяют или фильтрацией, или упариванием растворителя в вакууме. Фармацевтически приемлемые соли, образующиеся присоединением основания, могут быть получены аналогичным образом путем обработки раствора соединения А или В соответствующим основанием. Оба типа солей могут образовываться или взаимопревращаться с использованием ионообменных смол.
Соединения по данному изобретению могут быть выделены в ассоциации с молекулой растворителя путем кристаллизации из или упаривания соответствующего растворителя.
Синтезы соединений А и В и промежуточных соединений для использования в этом изобретении иллюстрируются следующими примерами. Примеры описаны ранее в документе о приоритете заявки GB 9514464.8, и номера соответствующих промежуточных соединений или номера Примеров приведены здесь в скобках рядом с номером промежуточного соединения или Примера настоящего изобретения.
При описании примеров здесь использованы следующие сокращения: МеОН (метанол) и ЕtOН (этанол).
Промежуточное соединение 1 (54)
Метиловый эфир (1R,3R)-1,2,3,4-тетрагидро-1-(3,4-метилендиоксифенил)-9H-пиридо[3,4-b]индол-3-карбоновой кислоты, цисизомер
К перемешиваемому раствору метилового эфира D-триптофана (11 г) и пипероналя (7,9 г) в безводном дихлорметане (400 мл), охлажденном до 0oС, добавляли по каплям трифторуксусную кислоту (7,7 мл) и раствор оставляли при температуре окружающей среды. Через 4 суток желтый раствор разбавляли хлористым метиленом (200 мл) и промывали насыщенным водным раствором бикарбоната натрия, затем водой (3х200 мл) и сушили над сульфатом натрия. Органический слой упаривали при пониженном давлении и остаток, содержащий два геометрических изомера, очищали флеш-хроматографией, элюируя смесью дихлорметан/этилацетат (97/3), получая первым продукт, названный в заголовке (6,5 г), Т. пл. 154oС.
Промежуточное соединение 2 (83)
Метиловый эфир (1R,3R)-1,2,3,4-тетрагидро-2-(2-хлорпропионил)-1-(3,4-метилендиоксифенил)-9Н-пиридо[3,4-b]индол-3-карбоновой кислоты
К раствору (R)-(+)-2-хлорпропионовой кислоты (191 мкл, 2,2 ммоль) в безводном дихлорметане (30 мл) добавляли дициклогексилкарбодиимид (0,45 г, 2,2 моль). Затем добавляли промежуточное соединение 1 (0,7 г, 2 ммоль) и смесь перемешивали при комнатной температуре в течение 20 часов. Образующийся осадок дициклогексилмочевины удаляли фильтрацией, фильтрат упаривали в вакууме и сырой продукт очищали флеш-хроматографией, элюируя смесью толуол/этилацетат (95/5). Полученное масло кристаллизовали из смеси эфир/гексан, получая соединение, названное в заголовке, в виде бледно-желтых кристаллов (0,74 г). Т. пл. 126-128oС.
Пример 1 (78) (соединение А)
(6R, 12aR)-2,3,6,7,12,12а-Гексагидро-2-метил-6-(3,4-метилендиоксифенил)-пиразино[2',1':6,1]пиридо[3,4-b]индол-1,4-дион
a) К перемешиваемому раствору промежуточного соединения 1 (0,5 г) и бикарбоната натрия (0,14 г) в безводном хлороформе (20 мл) добавляли по каплям хлорацетилхлорид (0,27 мл) при 0oС. Полученную смесь перемешивали 1 час при той же температуре и разбавляли хлороформом (20 мл). Затем при перемешивании к смеси прибавляли по каплям воду (10 мл), после чего прибавляли насыщенный раствор бикарбоната натрия. Органический слой промывали водой до нейтральной реакции и сушили над сульфатом натрия. После упаривания растворителя в вакууме получали метиловый эфир (6R,12aR)-1,2,3,4-тетрагидро-2-хлорацетил-1-(3,4-метилендиоксифенил)-9H-пиридо[3,4-b]индол-3-карбоновой кислоты в виде масла, которое кристаллизовали из эфира, получая твердое вещество (0,38 г, т. пл. 233oС), использованное без дополнительной очистки на следующей стадии.
b) К перемешиваемой суспензии хлорацетильного производного (0,37 г) в метаноле (20 мл) добавляли при комнатной температуре раствор метиламина (33% в этаноле), образующуюся смесь нагревали при 50oС в атмосфере азота в течение 16 часов. Растворитель удаляли при пониженном давлении, остаток растворяли в дихлорметане (50 мл). После промывания водой (3х20 мл) сушили над сульфатом натрия и упаривали досуха. Остаток очищали флеш-хроматографией, элюируя смесью дихлорметан/метанол (99/1) и перекристаллизовывали из изопропанола, получая соединение, названное в заголовке, в виде белых кристаллов (0,22 г). Т. пл. 302-303oС.
Анализ для C22H19NaO4. Вычислено, %: С 67,86; Н 4,92; N 10,79. Найдено, %:
С 67,77; Н 4,92; N 10,74.
[α]
Пример 2 (117) (соединение В)
(3S, 6R, 12aR)-2,3,6,7,12,12а-Гексагидро-2,3-диметил-6-(3,4-метилендиоксифенил)-пиразино[2',1':6,1]пиридо[3,4-b]индол-1,4-дион
К перемешиваемому раствору промежуточного соединения 2 (0,3 г, 0,68 ммоль) в тетрагидрофуране (30 мл) прибавляли при комнатной температуре раствор метиламина (33% в этаноле) (0,68 мл) и полученный раствор нагревали при кипении в токе азота в течение 6 дней. Растворитель удаляли при пониженном давлении, остаток растворяли в дихлорметане (50 мл). После промывания водой (2,25 мл) органическую фазу сушили над сульфатом натрия и упаривали досуха, сырой продукт очищали флеш-хроматографией, элюируя смесью дихлометан/метанол (99/1). Полученное масло кристаллизовали из метанола, получая соединение, названное в заголовке, в виде белых кристаллов (40 мг). Т. пл. 307-309oС.
Анализ для С23Н21N3O4. Вычислено, %: С 68,47; Н 5,25; N 10,42. Найдено, %:
С 68,35; Н 5,33; N 10,42.
[α]
Аналогично получали следующее соединение.
Пример 3
(3S, 6R, 12aR)-2,3,6,7,12,12а-Гексагидро-3-метил-6-(3,4-метилендиоксифенил)пиразино[2',1':6,1]пиридо[3,4-b]индол-1,4-дион
Получали в виде белых кристаллов, используя аммиак в качестве основания. Т. пл. 319-321oС.
Анализ для C22H19N3O4. Вычислено, %: С 67,86; Н 4,92; N 10,79. Найдено, %:
С 67,86; Н 5,17; N 10,72.
[α]
Соединения А и В включены в состав лекарственных форм, подробные сведения о которых приведены ниже.
Таблетки для перорального применения А.
Прямое прессование
1. - мг/таблетку
Активный ингредиент - 50,0
Кросповидон USNF - 8,0
Стеарат магния Ph Eur - 1,0
Лактоза безводная - 141,0
Активный ингредиент просеивали и смешивали с наполнителями. Образующуюся смесь прессовали в таблетки.
2. - мг/таблетку
Активный ингредиент - 50,0
Двуокись кремния коллоидная - 0,5
Кросповидон - 8,0
Додецилсульфат натрия - 1,0
Стеарат магния Ph Eur - 1,0
Микрокристаллическая целлюлоза USNF - 139,5
Активный ингредиент просеивали и смешивали с наполнителями. Образующуюся смесь прессовали в таблетки.
В. Влажная грануляция
1. - мг/таблетку
Активный ингредиент - 50,0
Поливинилпирролидон - 150,0
Полиэтиленгликоль - 50,0
Полисорбат 80 - 10,0
Стеарат магния Ph Eur - 2,5
Кроскармеллоза-натрий - 25,0
Двуокись кремния коллоидная - 2,5
Микрокристаллическая целлюлоза USNF - 210,0
Поливинилпирролидон, полиэтиленгликоль и полисорбат 80 растворяли в воде. Образующийся раствор использовали для грануляции активного ингредиента. После высушивания гранулы просеивали, затем экструдировали (штамповали) при повышенной температуре и давлении. Экструдат измельчали и/или просеивали, затем смешивали с микрокристаллической целлюлозой, кроскармеллоза-натрием, коллоидной двуокисью кремния и стеаратом магния. Образующуюся смесь прессовали в таблетки.
2. - мг/таблетку
Активный ингредиент - 50,0
Полисорбат 80 - 3,0
Лактоза Ph Eur - 178,0
Крахмал ВР - 45,0
Прежелатинизированный кукурузный крахмал ВР - 22,5
Стеарат магния - 1,5
Активный ингредиент просеивали и смешивали с лактозой, крахмалом и прежелатинизированным кукурузным крахмалом. Полисорбат 80 растворяли в очищенной воде. Прибавляли соответствующие объемы раствора полисорбата 80 и порошки гранулировали. После высушивания гранулы просеивали и смешивали со стеаратом магния. Затем гранулы прессовали в таблетки.
Таблетки с другой интенсивностью действия могут быть получены путем изменения соотношения активного ингредиента и наполнителей.
Таблетки с пленочным покрытием
Таблетки, описанные выше, были покрыты пленкой.
Покрывающая суспензия - % весовой
Опадри белый  - 13,2
- 13,2
Очищенная вода Ph Eur - до 100,0* Опадри белый - это запатентованный материал, полученный фирмой Colorcon Limited, Великобритания, который содержит гидроксипропилметилцеллюлозу, диоксид титана и триацетин.
Опадри белый - это запатентованный материал, полученный фирмой Colorcon Limited, Великобритания, который содержит гидроксипропилметилцеллюлозу, диоксид титана и триацетин.
* В конечном продукте вода не определяется. Максимальный теоретический вес твердых веществ, нанесенных при покрытии, составил 20 мг/таблетку. Таблетки покрывали пленкой, используя покрывающую суспензию и обычное оборудование для нанесения покрытия.
Капсулы
1. - мг/капсулу
Активный ингредиент - 50,0
Лактоза - 148,5
Поливинилпирролидон - 100,0
Стеарат магния - 1,5
Активный ингредиент просеивали и смешивали с наполнителями. Наполняли смесью твердые желатиновые капсулы размера 1, используя соответствующее оборудование.
2. - мг/капсулу
Активный ингредиент - 50,0
Микрокристаллическая целлюлоза - 233,5
Додецилсульфат натрия - 3,0
Кросповидон - 12,0
Стеарат магния - 1,5
Активный ингредиент просеивали и смешивали с наполнителями. Наполняли смесью твердые желатиновые капсулы размера 1, используя соответствующее оборудование.
Другие дозы могут быть получены путем изменения соотношения активного ингредиента и наполнителя, наполняемого веса и, если необходимо, изменения размера капсулы.
3. - мг/капсулу
Активный ингредиент - 50,0
Лабрафил M1944CS - до 1,0 мл
Активный ингредиент просеивали и смешивали с лабрафилом. Наполняли смесью мягкие желатиновые капсулы, используя соответствующее оборудование.
Ингибирующее действие на cGMP-PDE
Активность соединений настоящего изобретения в отношении cGMP-PDE измеряли, используя одностадийный анализ, адаптированный Wells и др. (Wells J. N. , Baird C.E., Wu Y.J., Yardman J.G. Biophys. Acta 384, 430 (1975)). Реакционная среда содержала 50 мМ трис-HCI, рН 7,5, 5 мМ ацетат магния, 250 мкг/мл 5'-нуклеотидазы, 1 мМ EGTA (этиленгликоль-бис-(-(β-аминоэтил)-N,N,N', N'-тетрауксусную кислоту) и 0,15 мкМ 8-[H3]-cGMP. Использованный фермент представлял собой человеческую рекомбинантную PDEV (ICOS, Сиэттл, США).
Соединения по данному изобретению растворяли в ДМСО (диметилсульфоксиде), конечная концентрация не превышала 2%. Время инкубации составило 30 минут, тотальное превращение субстрата не превышало 30%.
Значения IC50 (50%-ной ингибирующей концентрации) для изученных соединений определяли по кривым зависимости эффекта от концентрации, используя обычные интервалы концентраций от 10 нМ до 10 мкМ. Тесты с другими PDE с использованием стандартной методологии показали также, что соединения по данному изобретению обладают высокой селективностью по отношению к cGMP-специфической PDE.
Измерения уровней cGMP
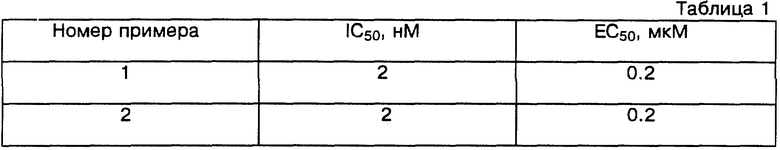
Клетки гладкой мышцы крысиной аорты (RSMC), полученные в соответствии с Chamley et al. Cell Tissue Res. 177, 503-522 (1977), использовали между десятым и двадцать пятым пассажем при слиянии в 24-ячеечных культуральных сосудах. Культуральную среду удаляли и заменяли PBS (физиологическим раствором, забуференным фосфатом) (0,5 мл), содержащим тестируемое соединение в соответствующей концентрации. Через 30 минут при 37oС частицы гуанилатциклазы стимулировали добавлением ANF (атриального натрийуретического фактора) (100 нМ) в течение 10 минут. В конце инкубации среду удаляли и проводили две экстракции добавлением 65% этанола (0,25 мл). Два этанольных экстракта объединяли и упаривали досуха, используя вакуумную систему Speed-vac. После ацетилирования измеряли содержание cGMP с помощью сцинтилляционного иммуноанализа (AMERSHAM). Показано, что соединения по настоящему изобретению, как правило, имеют значение IC50 менее 500 нМ и значение EC50 менее 5 мкМ. Данные теста in vitro для репрезентативных соединений по данному изобретению приведены в таблице.
Приведенные выше данные демонстрируют способность соединений-субъектов по данному изобретению ингибировать активность cGMP PDE и, следовательно, их применимость в лечении эректильной дисфункции, в основном, так, как здесь было описано.
Изобретение относится к области медицины. Предложены соединения формулы (I)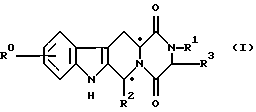
(6R, 12aR)-2,3,6,7,12,12a-гексагидро-2-метил-6-(3,4-метилендиоксифенил)-пиразино[2', 1': 6,1] пиридо[3,4-b] индол-1,4-дион; и (3S,6R,12aR)-2,3,6,7,12,12a-гексагидро-2,3-диметил-6-(3,4-метилендиоксифенил)-пиразино[2',1':6,1]пиридо[3,4-b]индол-1,4-дион и их физиологически приемлемые соли и сольваты для лечения импотенции. Предложен также способ лечения и профилактики эректильной дисфункции с помощью указанных соединений, а также фармацевтических составов на их основе. Предложен способ получения фармацевтических составов. Предложенные соединения более активны, чем известные в этой области. 9 c. и 4 з.п. ф-лы, 1 табл.
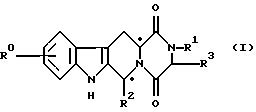
и его соли и сольваты (например, гидраты),
где R0 означает атом водорода, галоида или C1-6-алкил;
R1 означает атом водорода, C1-6-алкил, С2-6-алкенил, С2-6-алкинил, галоидсодержащий C1-6-алкил, С3-8-циклоалкил, С3-8-циклоалкилсодержащий С1-3-алкил, арилсодержащий С1-3-алкил или гетероарилсодержащий С1-3-алкил;
R2 означает произвольно замещенное моноциклическое ароматическое кольцо, выбранное из группы, состоящей из бензола, тиофена, фурана и пиридина, или произвольно замещенное бициклическое кольцо,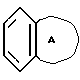
присоединенное к остальной молекуле посредством одного из углеродных атомов бензольного кольца, где сочлененное кольцо А является 5- или 6-членным кольцом, которое может быть насыщенным или частично либо полностью ненасыщенным и включает углеродные атомы и произвольно один или два гетероатома, выбранные из группы, состоящей из атома кислорода, серы и азота;
R3 означает атом водорода или С1-3-алкил, или R1 и R3 вместе означают 3- или 4-членную алкильную или алкенильную цепь,
имеющее использование в производстве медикамента для лечения и профилактики эректильной дисфункции у млекопитающих мужского пола, включая человека.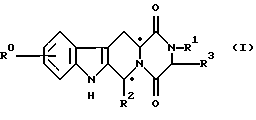
и его солей и сольватов (например, гидратов),
где R0 означает атом водорода, галоида или C1-6-алкил;
R1 означает атом водорода, C1-6-алкил, С2-6-алкенил, С2-6-алкинил, галоидсодержащий C1-6-алкил, С3-8-циклоалкил, С3-8-циклоалкилсодержащий С1-3-алкил, арилсодержащий С1-3-алкил или гетероарилсодержащий С1-3-алкил;
R2 означает произвольно замещенное моноциклическое ароматическое кольцо, выбранное из группы, состоящей из бензола, тиофена, фурана и пиридина, или произвольно замещенное бициклическое кольцо,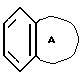
присоединенное к остальной молекуле посредством одного из углеродных атомов бензольного кольца, где сочлененное кольцо А является 5- или 6-членным кольцом, которое может быть насыщенным или частично либо полностью ненасыщенным и включает углеродные атомы и произвольно один или два гетероатома, выбранные из группы, состоящей из атома кислорода, серы и азота;
R3 означает атом водорода или С1-3-алкил, или R1 и R3 вместе означают 3- или 4-членную алкильную или алкенильную цепь.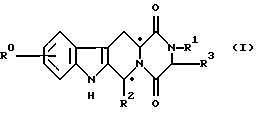
и его соли и сольваты (например, гидраты),
где R0 означает атом водорода, галоида или C1-6-алкил;
R1 означает атом водорода, C1-6-алкил, С2-6-алкенил, С2-6-алкинил, галоидсодержащий C1-6-алкил, С3-8-циклоалкил, С3-8-циклоалкилсодержащий С1-3-алкил, арилсодержащий С1-3-алкил или гетероарилсодержащий С1-3-алкил;
R2 означает произвольно замещенное моноциклическое ароматическое кольцо, выбранное из группы, состоящей из бензола, тиофена, фурана и пиридина, или произвольно замещенное бициклическое кольцо,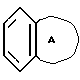
присоединенное к остальной молекуле посредством одного из углеродных атомов бензольного кольца, где сочлененное кольцо А является 5- или 6-членным кольцом, которое может быть насыщенным или частично либо полностью ненасыщенным и включает углеродные атомы и произвольно один или два гетероатома, выбранные из группы, состоящей из атома кислорода, серы и азота;
R3 означает атом водорода или С1-3-алкил, или R1 и R3 вместе означают 3- или 4-членную алкильную или алкенильную цепь.
| US 3917599 А, 04.11.1975 | |||
| US 5382585 А, 17.01.1995 | |||
| ТРИЦИКЛИЧЕСКИЕ АЗОТСОДЕРЖАЩИЕ СОЕДИНЕНИЯ И ПРОИЗВОДНЫЕ ТЕТРАГИДРОХИНОЛИНА ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ | 1991 |
|
RU2023712C1 |
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
Авторы
Даты
2002-04-20—Публикация
1996-07-11—Подача