Изобретение касается, прежде всего, композиции в виде микрокапсул или имплантатов, содержащих эксципиент или смесь полимерных или сополимерных биоразлагаемых эксципиентов с характеристической вязкостью, составляющей от 0,5 дл/г до 1,6 дл/г СНCl3, и, по меньшей мере, одно активное вещество. Изобретение касается также композиции в виде микрокапсул или имплантатов, содержащих, по меньшей мере, один биоразлагаемый полимер или сополимер высокой молекулярной массы и, по меньшей мере, одно водорастворимое активное вещество, имеющее высокую удельную поверхность. Такие композиции используются для достижения равномерного высвобождения активного вещества в течение длительного периода, который может составлять более трех месяцев.
Такие композиции и, в частности, микрокапсулы находят основное применение в аптечном деле, но также могут использоваться в других областях, в частности в агрохимии, т.е. в фитосанитарной области.
Значение введения активных начал в виде композиций с прогрессивным высвобождением известно давно как в отношении обычных фармацевтических препаратов, например стероидов, пептидов или протеинов (см., например, патент US 3773919, Boswell), так и препаратов фитосанитарного назначения. Принятые составы могут иметь форму микрочастиц, в которых активное начало вводится в биоразлагаемый полимер или сополимер, такой как сополимер полиактидекогликолид (ПЛГА).
Оказывается, что, в частности, когда хотят добиться сравнительно постоянного, во всяком случае, непрерывного, высвобождения, способ, квалифицируемый, например, как "однофазный", в европейском патенте ЕР 58481, необходимы полимеры типа ПЛГА со сравнительно низким молекулярным весом, следовательно, малой вязкости. В этой связи можно привести европейские патенты ЕР 21234 (см. пример 8. В. 2., в котором описывается сополимер с характеристической вязкостью 0,5 дл/г), ЕР 52510, в котором сополимер с вязкостью 0,38 дл/г в гексаизофторпропаноле (ГФИП) тестируется in vivo, ЕР 26599, в котором в качестве примера описываются полимеры, имеющие вязкость от 0,12 до 0,20 дл/г и заявлены полимеры, имеющие вязкость от 0,08 до 0,30 дл/г. Описанные в этих патентах полимеры представлены как приводящие к композициям с постоянным высвобождением. Композиции патента ЕР 26599 могут, например, содержать факторы контроля плодовитости.
Впрочем, важно отметить в этой связи, что при процедуре противопоставления относительно европейского патента ЕР 58481, которая еще не закончена на день подачи настоящей заявки, заявитель ограничил главный пункт изобретения полимерами малой вязкости (менее 0,3 или 0,5 дл/г), которые, согласно заявителю, являются единственными, способными обеспечить высвобождение однофазного типа.
В то же время, когда требуется добиться более длительного периода высвобождения, например, более одного месяца, появляются более сложные проблемы, а решение, предлагаемое, например, патентом ЕР 0302582, заключается в смешивании нескольких типов микрокапсул, состоящих из полимеров различной вязкости.
Итак, заявитель констатировал, что некоторые полимеры высокой вязкости могут подойти для получения композиций с прогрессивным пролонгированным высвобождением. Было также отмечено, что использование некоторых полимеров приводит к композициям, имеющим однофазный профиль высвобождения в течение длительного времени и без начального периода, не включающего высвобождение ("dead period"). Это особенно справедливо в отношении полимеров, имеющих характеристическую вязкость, предпочтительно, по меньшей мере, равную 0,5 дл/г в СНCl3 и еще более предпочтительно, по меньшей мере, равную 0,6 или 0,7 дл/г. Однако характеристическая вязкость этих полимеров в принципе не превышает 1,6 дл/г в СНCl3 и может быть ниже 1,4 или 1,2 дл/г. Названные полимеры будут представлять собой, предпочтительно, ПЛГА с отношением лактид/гликолид от 40/60 до 90/10 и, предпочтительно, около 75/25.
Полимеры по изобретению могут быть получены обычными методами, в частности, раскрытием лактидных или гликолидных циклов. Такой способ описан, например, в американском патенте US 3773919.
В настоящем изобретении можно также использовать смесь полимеров с различной высокой вязкостью, но предпочтение отдают композициям, содержащим только один полимер или сополимер.
Таким образом, изобретение касается, прежде всего, композиции в виде микрокапсул или имплантатов, содержащих эксципиент или смесь биоразлагаемых полимерных или сополимерных эксципиентов с характеристической вязкостью в интервале от 0,5 дл/г до 1,6 дл/г в СНCl3 и активное вещество или смесь активных веществ, причем микрокапсулы или имплантаты могут высвобождать активное вещество или смесь активных веществ в течение длительного периода: по меньшей мере, 1 месяца, предпочтительно, по меньшей мере, 2 месяцев и еще более предпочтительно, по меньшей мере, 3 месяцев.
Под микрокапсулой подразумевают также микросферу, микрочастицу, нанокапсулу, наносферу или наночастицу. Под полимером понимают полимер, сополимер или некую смесь этих веществ. Наконец, пол активным веществом понимают активное вещество, одну из его солей или один из его предшественников или некую смесь этих соединений.
Соли активных веществ, которые могут использоваться для композиций по изобретению, включают, в частности, соли, получаемые из органических кислот, таких как уксусная, яблочная, винная, щавелевая, фумаровая, лимонная, молочная, стеариновая, памоиновая, метансульфоновая и р-толуолсульфоновая кислоты, или из неорганических кислот, таких как соляная, серная, фосфорная или бромистоводородная кислоты. Предпочтительно, используют водорастворимый продукт, получаемый солеобразованием в виде катиона, например, с уксусной кислотой. Можно, однако, использовать нерастворимую соль, например памоат.
В частности, изобретение касается композиции в виде микрокапсул или имплантатов, содержащих эксципиент или смесь биоразлагаемых полимерных или сополимерных эксципиентов и активное вещество или смесь активных веществ, причем названные микрокапсулы или названные имплантаты могут высвобождать активное вещество или смесь активных веществ в течение продолжительного периода, который может достигать 3 месяцев или более, причем профиль высвобождения оказывается практически однофазным, а названная композиция отличается тем, что:
- или когда композиция находится в виде микрокапсул:
- либо вязкость названных полимеров или сополимеров составляет от 0,7 дл/г до 1,6 дл/г в СНCl3, а способ получения названных микрокапсул не включает стадию плавления названных микрокапсул,
- либо вязкость названных полимеров или сополимеров составляет от 0,5 дл/г до 1,6 дл/г в СНCl3, а названные полимеры или сополимеры имеют гидрофильный характер,
- или когда композиция находится в виде имплантатов, вязкость названных полимеров или сополимеров составляет от 0,5 дл/г до 1,6 дл/г в СНCl3.
Предпочтительно, вязкость полимеров или сополимеров для композиций по изобретению, по меньшей мере, равна 0,9 дл/г в СНCl3.
Полимеры или сополимеры, которые могут использоваться для данного изобретения, могут, в частности, быть такими полимерами, как полимеры молочной кислоты, гликолевой кислоты, лимонной кислоты или яблочной кислоты, или же другими биосовместимыми полимерами, такими как поли-β-гидроксимасляная кислота, сложные полиортоэфиры, полиортокарбонаты, сложные полиэфиры α-цианоакриловой кислоты, алкиленполиоксалаты, такие как триметилен- или тетраметиленполиоксалат, полиаминокислоты и т.д. Они могут также быть сополимерами, такими как ПЛГА, полистирол, полиметакриловая кислота, сополимеры метакриловой кислоты и акриловой кислоты, полиаминокислотами, полимерами малеинового ангидрида, этилцеллюлозой, нитроцеллюлозой, ацетилцеллюлозой и т. д. Все эти полимеры или сополимеры могут быть использованы по отдельности или в смеси. ПЛГА содержат обычно от 40 до 90% лактида и от 10 до 60% гликолида. Предпочтительно, используют D,L-ПЛГА и более предпочтительно D,L-ПЛГА, полученные из 70-80% D,L-лактида и 20-30% гликолида. Особенно для изобретения подходит ПЛГА, синтезируемый из 75% D,L-лактида и 25% гликолида.
Другим особенно предпочтительным для изобретения полимером является L-ПЛГА, получаемый из L-лактида и гликолида. По сравнению с D,L-ПЛГА такой же вязкости, L-ПЛГА обеспечивает более медленное высвобождение и является альтернативой D,L-ПЛГА более высокой вязкости.
Вообще, предпочтение отдается гидрофильным полимерам или сополимерам. Так, обычно, вместо ПЛГА, получаемого раскрытием цикла гидрофобными инициаторами, типа лаурилового спирта, предпочитают такие, которые получают раскрытием цикла гидрофильными инициаторами, типа молочной кислоты или гликолевой кислоты.
Пол гидрофильным полимером или сополимером подразумевают полимер или сополимер, концевая цепь которого полярна (например, эта концевая цепь имеет на конце кислотную функцию), в отличие от гидрофобного полимера или сополимера, концевая цепь которого является неполярной (например, эта концевая цепь является алифатической цепью).
Кислотный индекс, соответствующий числу миллиэквивалентов КОН, необходимых на грамм полимера для нейтрализации свободной кислотности, представляется параметром, в наибольшей степени коррелирующим с гидрофильным или гидрофобным характером полимера или сополимера. Кислотный индекс может быть измерен в случае, когда, вследствие природы мономера, концевые цепи полимеров или сополимеров могут содержать свободную кислотную функцию.
В целом, заявитель установил, что гидрофильные полимеры дают лучший профиль высвобождения. Так, кислотный индекс для полимеров по изобретению будет составлять, предпочтительно, по меньшей мере, 1 или, лучше, 1,2 и еще более предпочтительно 1,5 или 2.
Содержание активного вещества ("core loading") в микрокапсулах по изобретению, т.е. отношение массы чистого инкапсулированного пептида к общей массе микрокапсулы, обычно составляет от 0 до 20%, предпочтительно, от 2 до 15%. Для ацетата трипторелина содержание будет, предпочтительно, меньше или равно 10% и еще более, предпочтительно, от 4 до 8% для форм, обеспечивающих высвобождение за период около 3 месяцев. Для ацетата ланреотида содержание, предпочтительно, составляет от 10 до 20%.
Для имплантатов содержание активного вещества составляет обычно от 0 до 30%, предпочтительно, от 15 до 25%.
Стадия инкапсулирования может представлять собой так называемую стадию коацервации, такую как описано, например, в американском US 3773919 или европейском ЕР 52510 патентах.
Можно также использовать так называемый способ плавления-экструзии, такой как описано в европейском патенте ЕР 58481 или американском патенте US 5225205, при этом получаемые продукты затем при необходимости измельчаются согласно обычным методам для получения микрокапсул.
В то же время, можно использовать водорастворимое активное начало, такое как растворимая соль пептида, например ацетат. Можно также использовать нерастворимую соль растворимой молекулы, такую как соль кислоты жирного ряда с пептидом, например памоат пептида, такой как описан в английском патенте GВ 2209937.
Композиции, получаемые плавлением-экструзией с использованием полимеров по изобретению, могут также иметь вид имплантатов и использоваться в этом виде.
Эти имплантаты являются, предпочтительно, небольшими имплантатами (амниимплантаты или микроимплантаты) диаметром порядка 1 мм, например от 0,8 до 1,2 мм. Длина этих имплантатов может составлять, например от 10 до 35 мм, например, порядка 25 мм. Эти имплантаты дают очень интересные результаты при низких дозах активного вещества, например, порядка 3 мг ацетата трипторелина на имплантат. Такие имплантаты могут высвобождать активное вещество в течение периода времени, который может достигать 3 месяцев и более.
Кроме того, выяснено, что конфигурация активного начала может также иметь влияние на диффузию этого вещества. В частности, когда активное начало может быть получено в кристаллическом или аморфном виде, выбор той или иной формы имеет значение.
В заявке на патент ЕР 709085 описываются микрокапсулы, содержащие полимер и водорастворимое и аморфное активное вещество. В ней, в частности, идет речь о важности получения частиц активного вещества малой крупности и, предпочтительно, крупностью, менее 10 мкм. В этой заявке, однако, не описан способ получения названных частиц и нет никакого упоминания о влиянии удельной поверхности частиц активного начала на профиль высвобождения композиций, содержащих эти частицы. Заявитель же использует уже с 1986 г. микрокапсулы, содержащие аморфное активное вещество, ацетат трипторелина, выпускаемый под названием Decapeptyl 3,75 мг, крупность частиц которого составляет всего около 8 мкм. Но он отметил, что крупность частиц не является единственным решающим параметром, способствующим пролонгированному высвобождению, которое может продолжаться более 3 месяцев.
Вопрос об аморфном характере, в принципе, не ставится для таких веществ, как пептиды или протеины, способ получения которых, особенно лиофилизация, приводит в большинстве случаев к аморфному веществу, как в случае Decapeptyl 3,75 мг.
В литературе широко описано это явление, в частности, можно привести следующие статьи: Hsu, С. С. et al.. Pharmaceutical Reserch, 12(1), 69-77 (1995) или Towns, J.K., Journal of Chromatography, A, 705(1), 115-27 (1995).
Изобретение касается также композиции в виде микрокапсул или имплантатов, содержащих, по меньшей мере, один биоразлагаемый полимер или сополимер, предпочтительно, высокой молекулярной массы, и, по меньшей мере, одно водорастворимое активное вещество, имеющее высокую удельную поверхность. В частности, названная удельная поверхность выше 2 м2/г, предпочтительно, выше 3 м2/г. Более предпочтительно, названная удельная поверхность выше 5 м2/г или 10 м2/г. Еще более предпочтительно, названная удельная поверхность выше 20 м2/г и, предпочтительно, выше 30 м2/г.
Изобретение касается, предпочтительно, вышеуказанных композиций, в которых водорастворимое активное вещество является пептидом или протеином.
Оно касается также вышеуказанных композиций, для которых вязкость полимера или сополимера составляет от 0,5 до 1,6 дл/г в СНCl3 и, предпочтительно, от 0,9 до 1,6 дл/г в СНCl3. В частности, можно выбирать для использования полимеры или сополимеры с вязкостью от 0,7 до 1,3 дл/г в СНCl3 и еще более предпочтительно, полимеры или сополимеры с вязкостью от 0,9 до 1,3 дл/г. Особенно подходят полимеры ПЛГА. Предпочтительно, названные ПЛГА получают из 40-90% лактида и 10-60% гликолида и более предпочтительно из 70-80% лактида и 20-30% гликолида. Предпочтительно, водорастворимые активные вещества, вводимые в микрокапсулы или имплантаты, являются протеинами или пептидами.
Композиции, содержащие активное вещество с высокой удельной поверхностью, являются, предпочтительно, такими, для которых вязкость полимера или сополимера составляет от 0,5 до 1,6 дл/г в СНCl3 и в которых полимер или сополимер является гидрофильным, причем кислотный индекс этого последнего выше 1 мэкв КОН на грамм полимера или сополимера и, предпочтительно, выше 1,2, более предпочтительно, 1,5 мэкв, даже 2 мэкв КОН на грамм полимера или сополимера.
Изобретение касается, кроме того, композиций в виде микрокапсул или имплантатов, содержащих активное вещество с высокой удельной поверхностью, отличающихся тем, что полимер или сополимер является ПЛГА, предпочтительно, ПЛГА, получаемым из 70-80% лактида и 20-30% гликолида, причем вязкость названного ПЛГА составляет от 0,5 до 1,6 дл/г в СНCl3, а активное вещество, вводимое в микрокапсулы или имплантаты, является протеином или пептидом.
Эти микрокапсулы или имплантаты обеспечивают однофазный профиль высвобождения, при котором начальный пик (или по-английски "burst") уменьшен по сравнению с некоторыми другими препаратами, использующими полимер более низкого молекулярного веса, так что они обеспечивают высвобождение активного вещества в течение продолжительного периода действия, который может составлять более трех месяцев.
Другими словами, заявитель обнаружил, что свойства высвобождения, особенно высвобождения однофазного типа, композиций в виде микрокапсул или имплантатов, в частности, композиций на основе ПЛГА, и содержащих в качестве активного вещества пептид или протеин, значительно повышаются, если присутствует, по меньшей мере, один из следующих признаков:
а) полимер или сополимер является ПЛГА, имеющим вязкость в хлороформе выше 0,5 дл/г, предпочтительно, выше 0,9 дл/г и ниже 1,6 дл/г;
б) полимер или сополимер является ПЛГА, получаемым из 70-80% лактида и 20-30% гликолида;
в) полимер или сополимер является гидрофильным и имеет, предпочтительно, кислотный индекс выше 1 мэкв КОН и более предпочтительно, выше 1,2, даже 1,5 мэкв КОН на грамм полимера или сополимера;
г) активное вещество, предпочтительно, пептид или протеин, имеет высокую удельную поверхность выше 2 м2/г, предпочтительно, выше 10 м2/г, более предпочтительно, выше 20 м2/г и даже выше 30 м2/г;
причем эти признаки могут при необходимости комбинироваться с использованием L-ПЛГA вместо D,L-ПЛГА.
С учетом известного уровня техники заявитель полагает, что признак г) очень важен сам по себе и может успешно комбинироваться с другими признаками а), б) или в). В частности, можно комбинировать признак г) со следующими признаками: только а), только б), только в), а) и б) вместе, а) и в) вместе, б) и в) вместе или а), б) и в) вместе. Предпочтительно, комбинируют признак г), по меньшей мере, с признаком в).
Среди активных веществ, которые можно использовать для различных аспектов изобретения, можно, в частности, привести протеины и пептиды. Названные активные вещества могут быть выбраны, например, в группе, состоящей из следующих веществ: трипторелин или одна из его солей, в частности ацетат трипторелина, ланреотид или одна из его солей, в частности ацетат ланреотида, октреотид или одна из его солей (такая как описанная, например, в европейском патенте ЕР 29579), в частности ацетат или памоат октреотида, соединение, обладающее активностью LH-RH, такое как трипторелин, гозерелин, лейпрорелин, бузерелин или их соли, антагонист LH-RH, антагонист GPIIb/IIIa, соединение, обладающее активностью, подобной антагонисту GPIIb/llla, эритропоэтин (ЭПО) или один из его аналогов, различные α-интерфероны, β- или γ-интерферон, соматостатин, производное соматостатина, такое как описано в европейском патенте ЕР 215171, аналог соматостатина, такой как описанный в американском патенте US 5552520 (этот патент сам содержит перечень других патентов, в которых описаны аналоги соматостатина и содержание которых включено в виде ссылки в настоящую заявку), инсулин, гормон роста, фактор высвобождения гормона роста (GRF), пептид высвобождения гормона роста (GHRP), эпидермальный фактор роста (EGF), меланоцитостимулирующий гормон (MSH), гормон высвобождения тиреотропина (TRH) или одна из его солей или производных, тиреоидстимулирующий гормон (TSH), лютеинизирующий гормон (LH), фолликулостимулирующий гормон (FSH), паратиреоидный гормон (РТН) или одно из его производных, гидрохлорид лизоцима, пептид, связанный с паратиреоидным гормоном (РТНrр), N-концевой фрагмент пептида (положение 1 --> 34) человеческого гормона РТН, вазопрессин или одно из его производных, окситоцин, кальцитонин, производное кальцитонина с активностью, подобной активности кальцитонина, пептид, связанный с геном кальцитонина (CGRP), глюкагон, пептид, аналогичный глюкагону (GLP), гастрин, пептид высвобождения гастрина (GRP), секретин, панкреозимин, холецистокинин, ангиотензин, лактоген плаценты человека, хорионический гонадотропин человека (HCG), энкефалин, производное энкефалина, стимулирующий фактор колоний (CSF), эндорфин, киоторфин, интерлейкины, например Интерлейкин 2, туфцин, тимопоэтин, тимостимулин, гуморальный тимусный фактор (THF), сывороточный тимусный фактор (FTS), производное сывороточного тимусного фактора (FTS), тимозин, тимусный фактор X, фактор опухолевого некроза (TNF), мотилин, бомбезин или одно из его производных, таких как описанные в американском патенте US 5552520 (этот патент сам содержит перечень других патентов, в которых описаны производные бомбезина, и которые вводятся в виде ссылки в настоящую заявку), пролактин, нейротензин, динорфин, церулеин, вещество Р, урокиназа, аспаргиназа, брадикинин, калликреин, фактор роста нервной ткани, фактор свертывания крови, полимиксин В, колистин, грамицидин, бацитрацин, пептид, стимулирующий белковый синтез, антагонист эндотелина или одна из его солей или производных, вазоактивный интестинальный полипептид (VIР), адренокортикотропный гормон (АСТН) или один из его фрагментов, фактор роста, полученный из тромбоцитов (PDGF), костный морфогенетический протеин (BMP), полипептид, активирующий гипофизарную аденилатециклазу (РАСАР), нейропептид Y (NPY), пептид YY (PYY), полипептид гастроингибитор (GIP), и полинуклеотиды, в частности двухцепочечные РНК (дцРНК), такие как описанные в заявке на патент ЕР 0300680 или французский патент 2622586.
Под дцРНК подразумевают, предпочтительно, комплекс полиадениловой кислоты и полиуридиловой кислоты, называемый также поли (А)-поли (U) или Poly-adenur®. Могут использоваться по изобретению другие дцРНК, в частности комплекс полиинозиновой кислоты с полицитидиловой кислотой, известный также под названием поли (1)-поли (С), а также эти же комплексы, модифицированные путем введения уридиловой кислоты в цепь полицитидиловой кислоты, такой как вещество Ampligen® фирмы HEMISPHERx (для описания этих веществ обращаться, в частности, к заявке на европейский патент ЕР 0300680). Используемая дцРНК может представлять собой, например, смесь дцРНК, таких как определенные выше. Предпочтительно, дцРНК получают по способу, описанному во французском патенте 2622586.
Высокая удельная поверхность может быть получена для указанных выше активных веществ, если они являются водорастворимыми или стали водорастворимыми, например, посредством солеобразования или прививки на их структуре водорастворимой цепочки. Это справедливо, в частности, для указанных выше пептидов и протеинов. Любое другое водорастворимое активное вещество или одна из солей или предшественников и, в частности, соли, получаемые с уксусной кислотой, также может использоваться специалистом в данной области для этого признака изобретения, если он посчитает это целесообразным.
По одному из предпочитаемых признаков изобретения пептид или протеин с высокой удельной поверхностью выбирают из группы, состоящей из ацетата трипторелина, ацетата ланреотида или ацетата октреотида.
Под пептидом и/или протеином подразумевают в настоящей заявке как сами пептид и/или протеин, так и фармакологически активные фрагменты, соли или производные этих пептидов или протеинов.
Водорастворимое активное вещество, такое как используемое для изготовления микрокапсул или имплантатов по изобретению, и, в частности, ацетат трипторелина, ацетат ланреотида, ацетат октреотида, гозерелин, лейпрорелин, бузерелин или их соли, получают, предпочтительно, по способу, состоящему, главным образом, из двух стадий:
- стадия лиофилизации, включающая быстрое охлаждение разбавленного раствора водорастворимого вещества в среде с температурой ниже -50oС и, предпочтительно, ниже -70oС;
- при необходимости, стадия измельчения; предпочтительно, эта стадия включает ультразвуковое измельчение.
Под разбавленным раствором активного вещества подразумевают раствор, имеющий концентрацию названного активного вещества ниже половины концентрации насыщения и, предпочтительно, ниже четверти названной концентрации насыщения в случае, когда она, по меньшей мере, равна 200 г/л. Этот способ позволяет получать активное вещество, имеющее высокую удельную поверхность.
Под быстрым охлаждением нужно подразумевать приведение в контакт со средой с низкой температурой, вызывающей мгновенное замерзание раствора водорастворимого вещества.
Для лиофилизации можно, например, замораживать раствор в чашке, помещенной в сосуд с жидким азотом, перед проведением собственно процесса лиофилизации.
Предпочтительно, для получения максимальной удельной поверхности быстрому охлаждению раствора предшествует микронизация раствора активного вещества. Когда раствор активного вещества предварительно микронизирован, достаточно температуры низкотемпературной среды ниже -50oС.
Например, для получения очень высокой удельной поверхности можно выбрать атомизацию раствора путем его распыления через атомизатор на металлическую пластину с низкой температурой. Температура пластины составляет, предпочтительно, ниже -50oС и более предпочтительно, ниже -70oС, даже -80oС или -120oС. Эта температура может быть достигнута, например, путем быстрого охлаждения металлической пластины в среде с очень низкой температурой, такой как, например, жидкий азот. По предпочтительному варианту изобретения металлическая пластина является полой, а раствор распыляется с помощью атомизатора внутри названной пластины.
Возможны другие способы замораживания, например атомизация раствора активного вещества в ванне с предварительно охлажденным веществом, не являющимся растворителем названного активного вещества. В качестве нерастворителя предпочитают сжиженный газ, как, например, жидкий азот.
Другая возможность заключается в замораживании активного вещества на охлаждаемой вращающейся чашке ("drumfreezing"). Как указывалось выше, этому замораживанию предшествует микронизация раствора активного вещества.
При применении способа замораживания в чашке к активному веществу для получения микрокапсул или имплантатов с пролонгированным высвобождением по изобретению удельная поверхность активного вещества после лиофилизации, но перед измельчением, составляет, предпочтительно, более 2 м2/г. Предпочтительно, удельная поверхность активного вещества составляет более 3 м2/г, даже 5 м2/г.
Если необходима удельная поверхность выше 10 м2/г, предпочтительно прибегнуть к способу, включающему стадию микронизации. Предпочтительно, удельная поверхность, получаемая для активного вещества после лиофилизации, составляет более 15 м2/г. Еще более предпочтительно, эта удельная поверхность выше 20 м2/г, даже 30 м2/г.
Для изменения получаемых удельных поверхностей можно изменять условия замораживания раствора активного вещества за счет различных параметров, таких как, например, скорость замораживания или концентрация раствора.
Удельная поверхность активного вещества является благоприятным фактором для достижения высвобождения в течение длительного периода действия, в частности в случае микрокапсул. Действительно, как уже указывалось, частицы активного вещества такой же крупности, но другой удельной поверхности, дают с тем же полимерным эксципиентом совершенно другие результаты.
Предметом изобретения являются, следовательно, также способы, такие как описанные выше, применяемые к биологически активному водорастворимому веществу. Они касаются также биологически активного вещества, такого как получаемое по этим способам, имеющего высокую удельную поверхность.
В частности, изобретение касается ацетата трипторелина, ацетата ланреотида или ацетата октреотида, такого как получаемый по этим описанным выше способам, или двухцепочечной РНК, предпочтительно, комплекс полиадениловой кислоты с полиуридиловой кислотой, такой как получаемый по этим способам.
Как указано выше, композиции по изобретению находят применение, предпочтительно, в фармацевтической области. Фармацевтические композиции могут быть введены пациенту различными путями; однако, предпочитаемым путем является подкожная или внутримышечная инъекция. Микрокапсулы по изобретению могут быть вначале суспендированы в подходящем носителе, предназначенном для инъекции, таком как водный раствор хлорида натрия или водный раствор маннита.
Кроме специально отмеченных случаев, все используемые здесь технические и научные термины имеют то же значение, что и обычно понимаемое средним специалистом в области, к которой относится это изобретение. Также, все приведенные здесь публикации, заявки на патент, все патенты и все прочие ссылки включены в качестве справки.
Приводимые ниже примеры представлены для иллюстрации вышеназванных способов и не должны рассматриваться как ограничение объема изобретения.
ПРИМЕРЫ.
Для всех этих примеров характеристическая вязкость (IV) измерялась по обычным методам измерения времени течения, таким как описанные, например, в "Европейской Фармакопеи", 1997 г. , стр.17-18 (метод капиллярной трубки). Если не указано иное, вязкость измерялась в хлороформе при концентрации 0,1% при 25oС или в гексафторизопропаноле при концентрации 0,5% при 30oС. Удельная поверхность активного вещества при ее измерении определялась по так называемому методу В.Е.Т. (поглощение монослоя азота на активном веществе), который хорошо известен специалисту.
Для нижеследующих примеров "модифицированным" пептидом называют пептид, который был подвергнут лиофилизации по изобретению, в отличие от "немодифицированного" пептида, который лиофилизовался обычным способом (без резкого охлаждения при низкой температуре).
Пример 1.
16,120 г "немодифицированного" ацетата трипторелина растворяют в 554 мл воды. Раствор замораживают в чашке, помещенной в жидкий азот, затем лиофилизуют.
Получают, таким образом, 15,18 г "модифицированного" ацетата трипторелина при выходе 91,34 %. Это соединение имеет удельную поверхность 4,7 м2/г против 0,8 м2/г до лиофилизации.
Затем проводят ультразвуковое измельчение ацетата трипторелина: 15 минут достаточно для получения частиц крупностью менее 10 мкм для модифицированного пептида (тогда как 30 минут необходимы для получения такого гранулометрического состава с немодифицированным пептидом).
Затем проводят стадию инкапсулирования по метолу коацервации, такому как описанный в европейском патенте EP 52510 и американском патенте US 3773919, используя 3,378 г этого модифицированного и измельченного ацетата трипторелина и раствор 7,30% D,L-ПЛГА (D,L-ПЛГА состоит из 75% D,L-лактида и 25% гликолида, характеристическая вязкость в хлороформе = 0,70 дл/г, кислотный индекс = 1,61 мэкв КОН/г) в дихлорметане. 390 мл силиконового масла добавляли для образования микрокапсул по способу коацервации. Эти микрокапсулы извлекали после погружения в гептановую ванну (22 л) и фильтрации на мембране 10 мкм.
Пример 2.
0,338 г немодифицированного ацетата трипторелина крупностью, равной 8 мкм после ультразвукового измельчения в течение 30 минут, добавляли при перемешивании в раствор 7,30% D,L-ПЛГA в дихлорметане (ПЛГА эквивалентен тому, который описан в примере 1). Добавляли 40 мл силиконового масла для образования микрокапсул, которые затем осаждались в гептановой ванне (2 л), после чего фильтровались на мембране 10 мкм.
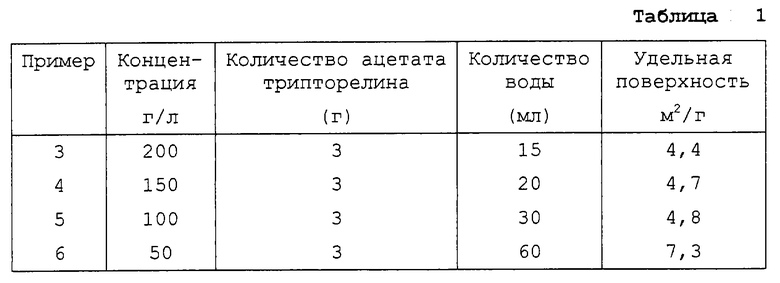
Примеры 3-6.
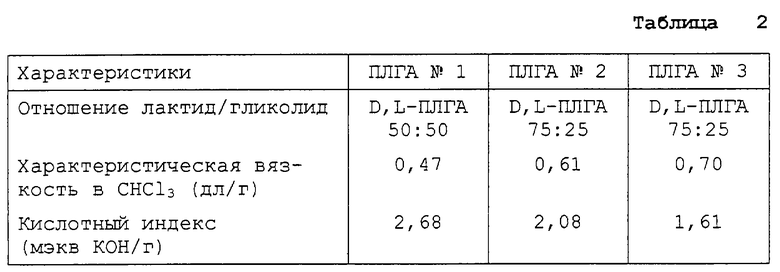
0,338 г модифицированного ацетата трипторелина в соответствии с условиями, описанными в приводимой ниже табл. 1, добавляли после ультразвукового измельчения в раствор с 7,30% смеси 33,3%/ 33,3%/ 33,3% трех D,L-ПЛГА (с характеристиками, описанными в приводимой ниже табл. 2) в дихлорметане. Добавляли 40 мл силиконового масла для образования микрокапсул, которые затем осаждались в гептановой ванне (2 л), после чего фильтровались на мембране 10 мкм.
Удельная поверхность исходного ацетата трипторелина (немодифицированного) составляет 0,8 м2/г.
Физико-химические характеристики трех смешиваемых полимеров приведены в табл. 2.
Пример 7.
22,560 г немодифицированного ацетата ланреотида растворяют в 752 мл воды. Раствор замораживают в чашке, помещенной в жидкий азот, после чего лиофилизуют. Получают 21,75 г модифицированного ацетата ланреотида с удельной поверхностью, равной 4,4 м2/г, с выходом 96,41%.
Затем проводят стадию инкапсулирования по методу коацервации, такому как описанный в европейском ЕР 52510 и американском US 3773919 патентах, используя 7,5 г этого модифицированного и измельченного ацетата трипторелина и 3,7%-раствор D,L-ПЛГА (D,L-ПЛГА состоит из 50% D,L-лактида и 50% гликолида, характеристическая вязкость в ГФИП = 0,55 дл/г) в дихлорметане. Добавляли 650 мл силиконового масла для образования микрокапсул по способу коацервации. Эти микрокапсулы извлекались после погружения в гептановую ванну (30 л) и фильтрования на мембране 10 мкм.
Примеры 8 и 9.
Получили микрокапсулы из ацетата трипторелина с D,L-ПЛГА (D,L-ПЛГА состоит из 75% D,L-лактида и 25% гликолида) различных средневесовых молекулярных весов (Mw). Использовали способ получения, описанный в примере 1 с ацетатом трипторелина с удельной поверхностью, равной 4,7 м2/г.
Физико-химические параметры примеров 8 и 9 приведены в табл. 3.
Пример 10.
Микрокапсулы изготавливали по способу, описанному в примере 1 с D,L-ПЛГА (D, L-ПЛГА состоит из 75% D,L-лактида и 25% гликолида; молекулярный вес, определяемый в THF: 80100; вязкость в хлороформе: 0,75 дл/г, кислотный индекс = 0,40 мэкв КОН/г) с гидрофобной тенденцией.
Пример 11.
Микрокапсулы изготовляли по способу, описанному в примере 1, из L-ПЛГА (L-ПЛГА состоит из 75% L-лактида и 25% гликолида; молекулярный вес в THF: 99260; вязкость в хлороформе: 0,78 дл/г, кислотный индекс = 1,80 мэкв КОН/г) с кристаллической тенденцией.
Пример 12.
К четырем весовым частям порошка D,L-ПЛГА (ПЛГА состоит из 75% лактида и 25% гликолида; молекулярный вес, определяемый в THF: 103810; характеристическая вязкость в хлороформе: 0,82 дл/г) добавляют одну весовую часть ацетата трипторелина.
Разбивают комочки просеванием через сито с размером ячеек 400 мкм, перемешивают в течение 20 минут со скоростью 42 оборота в минуту и экструдируют смесь при 120oС на шнековом экструдере через фильеру диаметром 1 мм. После чего охлаждают на воздухе и калибруют вытягиванием (вытяжная машина) до конечного диаметра 0,85 мм.
Определяют содержание смеси на единицу длины (мм) и дозируют микроимплантаты с 3 мг трипторелина, нарезая кусочки материала после экструзии расчетной длины (в данном случае, 24 мм). Наконец, проверяют вес каждого микроимплантата.
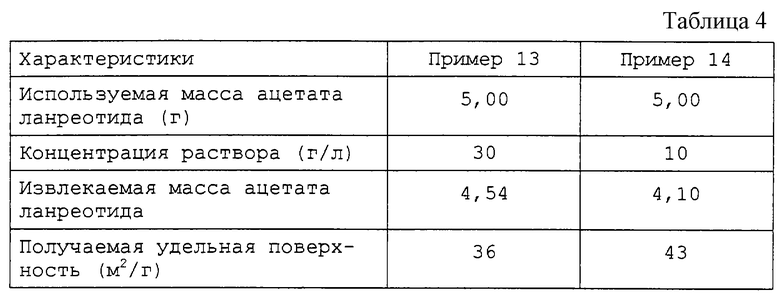
Примеры 13 и 14.
Используют для этих двух примеров ту же последовательность операций:
5 г ацетата ланреотида растворяют в воде для получения раствора выбранной концентрации (например, для получения концентрации 30 г/л, добавляют 167 мл стерильной воды). Этот раствор атомизируют с помощью распылителя 500 мл, струя которого регулируется в целях получения как можно более маленьких капелек. Получаемые капельки впрыскивают в чашку, дно которой контактирует с жидким азотом. Предварительно вводят в чашку два температурных датчика для того, чтобы следить за изменением температуры материала.
После замораживания продукта чашку вводят в лиофилизатор, температура пластины которого составляет около -54oС.
Температура материалов и пластины уравновешивается в течение 1 часа. После этого переходят к фазе сублимации (температура пластины устанавливается на уровне 20oС, а давление в ванне 100 мкбар). Эта фаза длится около 30 часов. Средняя конечная температура материала составляет 13oС. Последующая вторичная сушка (давление в ванне 50 мкбар) длится около 24 часов. Средняя конечная температура материала составляет 20oС.
В табл. 4 приводятся характеристики используемых реагентов и получаемых материалов.
Полученный ранее ацетат ланреотида с удельной поверхностью 43 м2/г (пример 14) вводится в микрокапсулы по следующему способу:
0,782 г ацетата ланреотида взвешивают в стеклянной трубке. 15 мл дихлорметана добавляют к соли пептида. Измельчение пептида осуществляют ультразвуком с помощью ультразвукового генератора, оборудованного усилителем и датчиком с плоским или погруженным концом (частота = 50 Гц, мощность 250 Вт; измельчение длится около 15 мин).
После этого осуществляют стадию инкапсулирования по методу коацервации, как описано в европейском ЕР 52510 и американском US 3773919 патентах, используя 0,782 г измельченного ацетата ланреотида и раствор 4 г D,L-ПЛГА 50:50 (IV= 0,48 дл/г в СНCl3) в 35 мл дихлорметана. Добавляют 34,2 мл силиконового масла для образования микрокапсул по способу коацервации. Эти микрокапсулы извлекали после погружения в гептановую ванну (2,5 л) и фильтрования на мембране 10 мкм.
Получаемые микрокапсулы могут после этого быть высушены в вакууме, расфасованы по флаконам и лиофилизованы с эксципиентами (например, с балластом или поверхностно-активным веществом) для хранения в нормальных условиях и облегчения суспендирования микрокапсул.
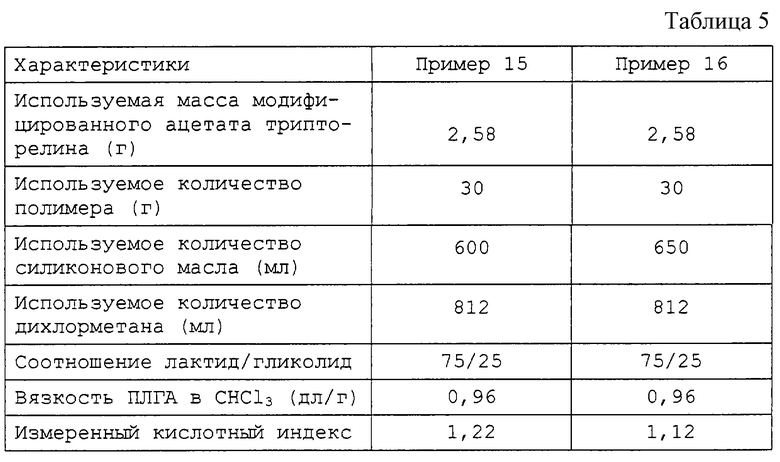
Примеры 15 и 16.
Для обоих примеров используют схему действий, аналогичную схеме примера 1. В этих примерах используют тот же пептид. Характеристики, касающиеся используемого ПЛГА, количеств взятого пептида (для этих примеров, модифицированный ацетат трипторелина) и параметры получения микрокапсул приведены в табл. 5.
Исследование профилей высвобождения микрокапсул по изобретению.
Для иллюстрации значения микрокапсул по изобретению было проведено исследование их профилей высвобождения in vivo.
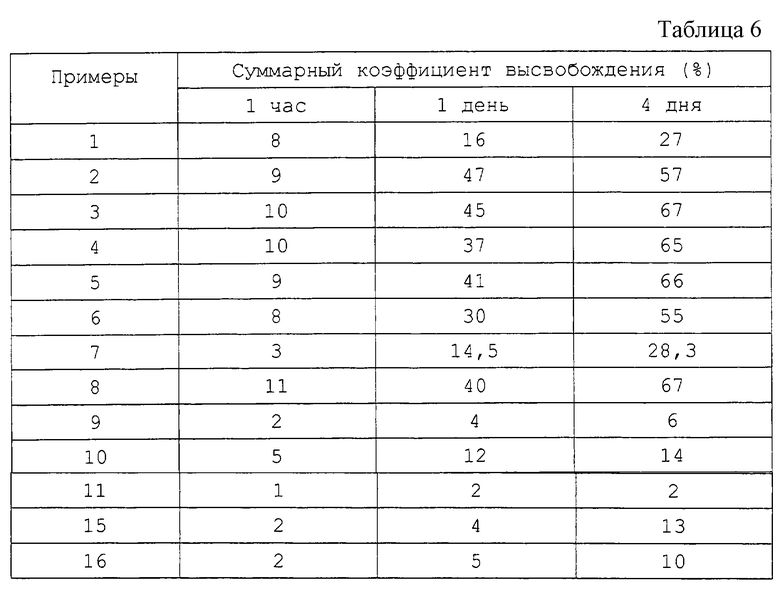
Для каждого из примеров 1-11 и 15-16 измеряют высвобождение трех контрольных образцов приблизительно по 25 мг микрокапсул (около 20 мг для примера 7), помещаемых в 4 мл 0,9%-раствора хлорида натрия. Экстрагируют через 1 час, 1 день и 4 дня высвобождения в растворе, поддерживаемом при температуре 37oС.
Количество трипторелина измеряют посредством жидкостной хроматографии высокой разрешающей способности (HPLC) по отношению к интервалу эталонирования в виде градиента в системе трифторуксусной кислоты (TFA).
Для получения стандартного интервала эталонирования для трипторелина готовят раствор Т1 следующим образом: контрольную пробу около 7,5 мг эталонного ацетата трипторелина помещают в колбу 50 мл; доливают до 50 мл раствором уксусной кислоты 0,1%. Из раствора T1 готовят растворы Т2 и Т3, действуя следующим образом: для T2 отбирают 10 мл раствора T1 и доливают до 20 мл раствором уксусной кислоты 0,1%. Для раствора Т3 отбирают 1 мл раствора T1 и доливают до 50 мл раствором уксусной кислоты 0,1%.
Ланреотид измеряют таким же способом посредством жидкостной хроматографии высокой разрешающей способности. Для получения стандартного интервала эталонирования для ланреотида готовят раствор T'1 следующим образом: контрольную пробу около 16,5 мг эталонного ацетата трипторелина помещают в колбу 50 мл; доливают до 50 мл раствором уксусной кислоты 0,1%. Из раствора T'1 готовят растворы T'2, Т'3, Т'4 и T'5, действуя следующим образом: для Т'2 отбирают 10 мл раствора T'1 и доливают до 25 мл раствором уксусной кислоты 0,1%. Для раствора Т'3 отбирают 5 мл раствора T'1 и доливают до 25 мл раствором уксусной кислоты 0,1%. Раствор T'4 получают разбавлением 2 мл раствора T'1 в растворе уксусной кислоты 0,1% для получения общего объема 25 мл, а раствор Т'5 - разбавлением 1 мл раствора T'1 в растворе уксусной кислоты 0,1% для получения общего объема 25 мл.
Высвобождаемое количество ацетата трипторелина или ацетата ланреотида определяют в процентах по отношению к исходно присутствующему количеству (100%) ацетата трипторелина или ацетата ланреотида, который служит эталоном.
В табл. 6 приведены результаты лабораторных испытаний.
Результаты испытаний in vivo демонстрируют хорошую корреляцию с результатами испытаний in vitro. В качестве примера, микрокапсулы из примера 1 с дозой 1,2 мг/кг вводились внутримышечно крысам. Замеры в плазме показали, что содержание трипторелина оставалось постоянно выше 0,1 нг/мл в течение более 90 дней. Такие же исследования, проводимые с микрокапсулами из примера 2, показали, что содержание тестостерона оставалось постоянно ниже 1 нг/мл в течение более 90 дней. В то же время микрокапсулы из примера 9 также вводились внутримышечно крысам с дозой 1,2 мг/кг, а замеры в плазме показали, что содержание трипторелина оставалось постоянно выше 0,1 нг/мл в течение более 90 дней.
Микрокапсулы из примера 12 испытывались in vivo следующим образом: общая доза 3 мг трипторелина вводилась внутримышечно 6 собакам Beagles (вес около 12 кг) в мышцу задней лапы каждого животного. Замеры в плазме показали, что содержание трипторелина оставалось постоянно выше 0,1 нг/мл в течение более 90 дней.

Изобретение относится к композициям в виде микрокапсул или имплантатов. Композиции содержат эксципиент или смесь биоразлагаемых полимерных или сополимерных эксципиентов с характеристической вязкостью от 0,5 до 1,6 дл/г в СНСl3. В качестве активного вещества композиции содержат протеин или пептид. Композиции обеспечивают высвобождение указанного активного вещества в течение длительного периода, который может достигать 3 месяцев или более, и имеют практически однофазный профиль высвобождения активного вещества без начального периода. 4 с. и 20 з.п. ф-лы, 6 табл.
Приоритет по пунктам:
18.04.1997 по п.2;
25.03.1998 по пп.1, 3-11, 19-24;
17.04.1998 по пп.12-18.
| DE 4041563 А, 25.06.1992 | |||
| Способ лечения неврологических проявлений позвоночного остеохондроза | 1977 |
|
SU709085A1 |
| КОНВЕЙЕР ДЛЯ ПРОДОЛЬНОГО ТРАНСПОРТИРОВАНИЯ ШТУЧНЫХ ИЗДЕЛИЙ ЦИЛИНДРИЧЕСКОЙ ФОРМЫ | 0 |
|
SU384752A1 |
| Промышленная технология лекарств | |||
| / Под ред | |||
| проф | |||
| В.И.Чуешова | |||
| - Харьков: Укр | |||
| ФА "Основа", т.2, 1999, с.383-414. | |||
Авторы
Даты
2003-02-20—Публикация
1998-04-17—Подача