Изобретение относится к медицине, а именно к нефроурологии.
Известна клиническая картина и динамика течения острой и хронической почечной недостаточности, сопровождающейся синдромом уремии. При синдроме уремии основными показателями интоксикации являются концентрация мочевины (характеризующая задержку азотистых веществ во внеклеточной жидкости) и креатинина (обладающего высокой стабильностью в крови). [Родоман В.Е., Максимов В. И. Внепочечное очищение организма от азотистых шлаков при урологических заболеваниях, сопровождающихся хронической почечной недостаточностью, Урология. 1999, 6, с. 51-54]. Эффективность лечения этого контингента больных во многом зависит от методов детоксикации [Энтеросорбция / Под ред. Н.А.Белякова Л. 1991, с. 210-211]. Применение активных методов лечения почечной недостаточности, прежде всего гемодиализа, не решает всех медицинских проблем. Поэтому в нефрологической и реанимационной практике особо выделяют задачи оказания помощи больным с уремией на додиализном этапе лечения с целью удлинения додиализного промежутка и оказания помощи инкурабельным больным, которым противопоказаны активные методы терапии. Использование желудочно-кишечного тракта как викарного (заместительного) органа в выведении уремических токсинов и метаболической коррекции почечной недостаточности достаточно давно известна. Экспериментально и клинически доказано, что при кишечном диализе из организма можно удалять мочевину, креатинин и мочевую кислоту [Sparks R.E. - Kidney int., 1975, v. 7, p. S-373-s-376]. Через желудочно-кишечный тракт самопроизвольно выводятся уремические токсины и гормоны [Zeig S. , Friadman E.A. - In: Sordents and Their Clinical Application. Ed. C. Giordano. New York, 1980, p. 275-294]. Проведение кишечного диализа достигается путем приема внутрь сорбентов либо бактериальных ферментов, усиливающих переработку азотистых соединений. До сих пор в нефроурологической практике используются твердые углеродсодержащие матрицы энтеросорбентов и гипертонические растворы для выведения уремических токсинов, действие которых основано на ионном обмене. Недостатком твердых таблетированных форм энтеросорбентов является низкая текучесть в просвете кишки, резко снижающая контакт энтеросорбента с токсинами, раздражающее действие на слизистую оболочку кишки и низкая способность связывания и выведения уремических токсинов. Недостатком ионных гипертонических растворов является их неспособность связывать уремические токсины, способность вызывать диарею и гиперсекрецию токсинов в просвет кишки, создавая ионный дисбаланс в организме.
Известна элиминация азотистых веществ через желудочно-кишечный тракт при использовании per os твердого окисленного крахмала, обладающего сродством к хитозану. Недостатком сорбента является значительное усиление перистальтики кишки, появление диареи. Характерна избирательная адсорбция мочевины и аммиака, концентрация креатинина и мочевины в сыворотке крови не снижается. [1) Giordano С., Esposito R., Pluvio M. - Proc. Europ. Dialys. Transplant. Ass. , 1973, v. 10, p. 136-140. 2) Inoshito К. - Nephron, 1981, v. 28, р. 305-307. 3) Man N. К., Druenke Т., Paris J. et al. - Proc. Europ. Dialis. Transplant. Ass., 1973, v. 10, p. 143-151].
На сегодняшний день наибольшей эффективностью при выведении уремических токсинов обладает гранулированная марка угля СКН в дозе 0,8-1,5 г/кг (60-120 г/сут) в сутки. В течение нескольких месяцев наблюдается уменьшение симптомов уремической гастроэнтеропатии и достоверное снижение уровня креатинина с 1,02±0,09 ммоль/л до 0,81±0,07 ммоль/л, что позволяет существенно отсрочить диализную терапию [Шостак Г.Д., Рябов С.И., Лукичев Б.Г. и др. Пероральные сорбенты в терапии хронической почечной недостаточности. Терапевтический архив, том LVI, 7, 1984, с. 58-63]. Недостатком данного сорбента является то, что при назначении малых доз сорбента (30-60 г/сут) последний вызывает тошноту и рвоту, а при больших дозах (120-150 г/сут) приводит к запору и развитию частичной кишечной непроходимости. Хорошо известно, что сорбенты типа СКН практически не поглощают мочевину сыворотки крови. [Николаев В.Г., Стрелко В.В. Гемосорбция на активированных углях. Киев, 1979].
Известно экспериментальное исследование, в котором моделирование заболевания воспроизводилось одномоментным удалением обеих почек, а в качестве энтеросорбента использовался природный цеолитсодержащий туф (клиноптилолит) [патент РФ 94016980, МПК 6 А 61 К 33/00, 10.05.96]. Энтеросорбент вводят per os и через желудочный зонд в количестве 500-600 мг/мл. Пероральная терапия природным цеолитсодержащим туфом (клиноптилолитом) приводит к увеличению выживаемости нефрэктомированных животных в 1,9 раза. Недостатком применения природного цеолитсодержащего туфа является низкая способность снижать уровень креатинина и мочевины в крови. Клинический опыт показывает, что следует применять энтеросорбенты даже в случае отсутствия снижения или стабилизации показателей азотистого гомеостаза при наличии только положительной клинической динамики [Энтеросорбция / Под ред. Н.А.Белякова. Л. 1991, с. 223]
Наиболее близким техническим решением в снижении уремических токсинов является применение таблеток, содержащих хитозан. [Jing S.B., Li L., Ji D., Takiguchi Y., Yamaguchi T. Effect of chitosan on renal function in patients with chronic renal failure. J. Pharm. Pharmacol. 1997. - Vol. 49. 7. - P. 721-723]. Исследование проводилось на людях, страдающих хронической почечной недостаточностью (ХПН) и находящихся на постоянном управляемом гемодиализе. Пациенты были разделены на 2 группы. В 1 группе (контроль) находились люди на консервативном методе лечения ХПН. Во 2 группе (лечение) пациенты принимали per os таблетки, содержащие хитозан, по 450 мг/сут. Одна таблетка (140 мг) содержит 45 мг хитозана, 75 мг декстрана, экстракт дрожжей и протеин. Осмотр пациентов двух групп проводился 1 раз через каждые 4 недели. Во 2 группе через 12 недель отмечалось улучшение аппетита, сна и физической силы по сравнению с 1 группой. В лечебной группе после 4 недель по сравнению с контрольной группой произошло увеличение гемоглобина с 58,2±12,1 до 69,3±11,3 г/л, снижение мочевины с 79±19 до 54±19 мМ, креатинина с 1,049±0,565 до 0,867±0,261 мМ. Недостатком данного исследования является применение таблетированного препарата, обладающего низкой текучестью в просвете кишки, малой поверхностью соприкосновения с токсинами и раздражающим действием на слизистую кишки.
Поиск и разработка новых энтеросорбентов является одной из фундаментальных задач эфферентной медицины [Энтеросорбция / Под ред. Н.А.Белякова. Л. 1991, с. 336].
Наибольший интерес в настоящее время представляют водорастворимые и водонерастворимые препараты хитозана, дающие вязкие растворы и гели [Рогожин С. В. , Гамзазаде А.И., Скляр А.М., Леонова Е.Ю., Насибов С.М. Полимер-гомологи хитозана и сульфопроизводные на их основе, Матер. 1 всесоюз. науч.-техн. конф. : Производство и использование хитина и хитозана из панциря криля и других ракообразных. Владивосток, 1983. - С. 58-68; Роговина С.З., Акопова Т. А. , Зеленецкий С.Н.. Изучение экструзионного размола хитозана \ Тез. IV Всеросс. конф. Производство и применение хитина и хитозана. - М., 1995. - С. 27-28] . Новым направлением в исследовании хитозана является получение гелей [Moore G.K., Roberts G.A.T. Int. J. Biol. Macromol., 1980. - Vol. 2. - 73. - P. 78] , которые образуются при ацетилировании хитозана [Hirano S., Ohe Y. Agr. Biol. Chem., 1975. - Vol. 39. - P. 1337]. Хитозан как волокно усиливает прохождение пищевых масс по желудочно-кишечному тракту.
Морфологические и морфометрические исследования тканей и внутренних органов свидетельствуют о полной нетоксичности хитозановой диеты в течение длительного времени ее использования [Петров В.А., Тарасенко Г.А. Токсиколого-гигиеническая оценка хитозана из панциря камчатского краба в условиях хронического эксперимента. Матер. V конф. Новые перспективы в исследовании хитина и хитозана. - М. - Щелково, 1999. - С. 179-181].
Лечение гелевой формой мелкодисперсного хитозана синдрома уремии в патентных и литературных источниках не обнаружено.
Задача изобретения: введение в клиническую практику нового перорального сорбента, эффективного для консервативной терапии уремии различного генеза и оказания помощи инкурабельным больным с целью удлинения додиализного промежутка.
Задачу решают за счет того, что вводят гелевую форму мелкодисперсного хитозана перорально или через зонд по 4 мл на 1 кг массы тела через каждые 3 часа.
Сведения, подтверждающие возможность осуществления изобретения.
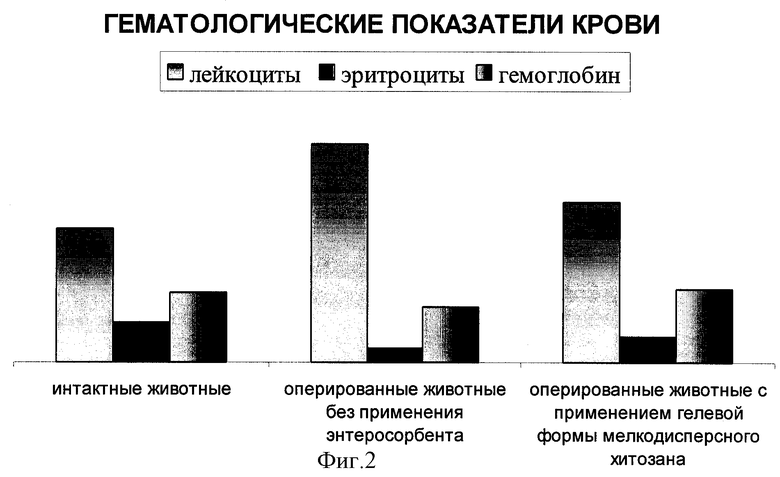
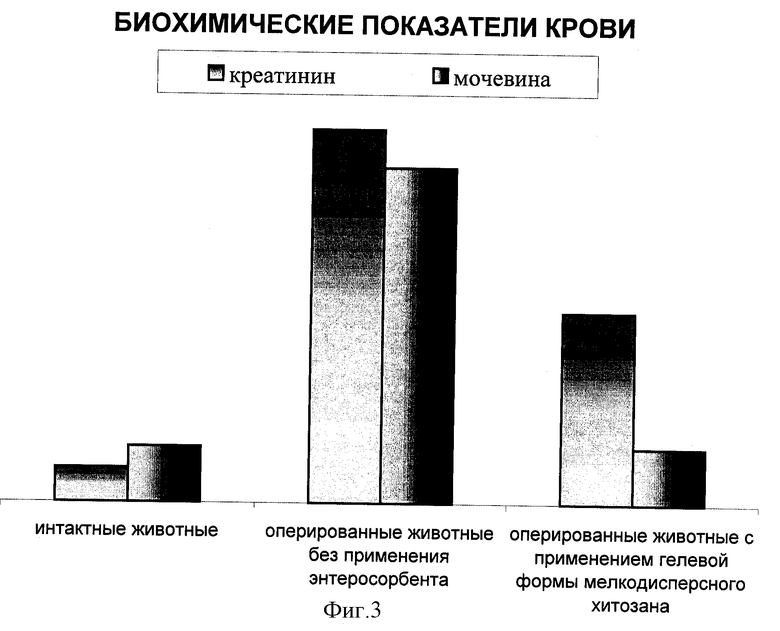
Для воспроизведения клинико-лабораторных признаков уремии использованы стандартные экспериментальные методы. Экспериментальное моделирование уремии проводилось на белых крысах-самцах популяции Wistar массой от 180 до 200 г. Операция проводилась в асептических условиях и заключалась в одномоментном двухстороннем изолированном удалении почек через лапаротомический разрез под нейролептанальгезией (внутрибрюшинное введение 0,4 мл кетамина) путем наложения шелковых лигатур на сосудистые ножки и мочеточники. Брюшная стенка зашивалась наглухо двумя рядами шелковых швов. В эксперименте оперировано 30 особей животных, из которых сформированы 3 группы. 1 группа (10 особей) - контроль: интактные животные, находящиеся на обычном вскармливании; 2 группа (10 особей) - контроль за выживаемостью и развитием уремической интоксикации без применения энтеросорбентов; 3 группа (10 особей) - эксперимент на выживаемость при развитии уремической интоксикации с применением гелевой формы мелкодисперсного хитозана. Лечебный эффект подтверждался выживаемостью животных (фиг. 1), общему состоянию животных, признаками уремической гастроэнтеропатии, гематологическими показателями крови (фиг.2), биохимическими сдвигами в сыворотки крови (фиг.3), патоморфологическими изменениями отделов кишки. В крови определяли количество лейкоцитов, эритроцитов, гемоглобина. В сыворотке крови определяли концентрацию креатинина и мочевины с использованием стандартных наборов реактивов ("Олвекс"). Животные 3 группы в период выживания получали гелевый хитозан (М.м. 180-200 кД, степенью деацитилирования 75%) в дозе по 4 мл/кг через каждые 3 часа. Кормление осуществлялось принудительно внутрижелудочно через зонд. Средняя суточная доза хитозана составляла 8 мл.
У животных 2 группы по сравнению с 1 группой отмечалось бурное нарастание внешних признаков эндотоксемии к концу первых суток, проявляющееся характерным запахом уратов, снижением двигательной активности, повышенной жесткостью, ломкостью и разрежением волосяного покрова. Период жизни этих животных составлял 47,2±0,5 часа. При использовании гелевой формы мелкодисперсного хитозана внешние признаки нарастания эндотоксемии проявились только к концу третьих суток, при этом не отмечалось появления жесткости и ломкости волосяного покрова. Применение данного объема препарата не вызывало изменения стула. Внешнее состояние животных этой группы указывает на снижение выделения уремических токсинов через кожный покров. Период жизни животных 3 группы составил 94,4±0,7 часов.
Объективно: - на вскрытии у животных 2 группы по сравнению с 1 группой отмечалась свободная жидкость в полости брюшины и низкая перистальтическая активность кишки (атония). При использовании гелевой формы мелкодисперсного хитозана в полости брюшины отсутствовала свободная жидкость. Содержимое кишки по сравнению со 2 группой составляло жидкую консистенцию с волокнами хитозана. Перистальтика кишки не нарушена. Данные гематологического исследования крови: у животных 2 группы отмечалось увеличение лейкоцитов с 2,0±0,16•109/л до 3,4±0,19•109/л, у оперированных животных при применении гелевой формы мелкодисперсного хитозана происходило снижение лейкоцитов до 2,4±0,12•109/л по сравнению со 2 группой. При анализе клеток красной крови и гемоглобина во 2 группе происходило снижение показателей эритроцитов с 6,1±0,16•1012/л до 2,l±0,14•1012/л и количества гемоглобина с 106±2,4 г/л до 83,7±2,7 г/л, что характерно для синдрома уремии. При использовании гелевых форм мелкодисперсного хитозана происходило увеличение эритроцитов до 3,9±0,07•1012/л и гемоглобина до нормальных показателей 112,2±2,35 г/л, по сравнению со 2 группой. Данные биохимического контроля показали, что содержание токсических метаболитов в сыворотке крови оперированных животных 2 группы растет: мочевина с 7,8±0,48 до 47,2±1,1 ммоль/л, креатинин с 0,096±0,007 до 1,05±0,041 ммоль/л, что свидетельствует о развитии интоксикации, характерной для уремии. У животных 3 группы, находящихся на вскармливании энтеросорбентом, показатели мочевины в терминальный период восстанавливались до исходного уровня (7,81±0,52 ммоль/л), а креатинин существенно понижался (0,54±0,017 ммоль/л).
Таким образом, применение гелевой формы мелкодисперсного хитозана существенно удлиняет продолжительность жизни животных (в 2 раза), проявляя лечебный эффект в увеличении количества гемоглобина, эритроцитов, лейкоцитов и снижении креатинина и мочевины сыворотки крови, способствует улучшению общего состояния экспериментального животного при синдроме экспериментальной уремии, что составляет положительный эффект при его использовании. Удлинение продолжительности жизни и выведение уремических токсинов из крови при использовании в качестве энтеросорбента гелевой формы мелкодисперсного хитозана делает возможным оказание консервативной помощи больным с уремией на додиализном этапе лечения и оказание помощи инкурабельным больным, которым противопоказаны активные методы терапии.
| название | год | авторы | номер документа |
|---|---|---|---|
| ЭНТЕРОСОРБЕНТ ДЛЯ ТЕРАПИИ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТИ | 1994 |
|
RU2097046C1 |
| СПОСОБ ЛЕЧЕНИЯ ДЕСТРУКТИВНОЙ ФОРМЫ ПАНКРЕАТИТА | 2001 |
|
RU2196587C1 |
| СПОСОБ УСТРАНЕНИЯ ФУНКЦИОНАЛЬНОГО ДУОДЕНОСТАЗА ПРИ ПАНКРЕОНЕКРОЗЕ | 2003 |
|
RU2240802C1 |
| СПОСОБ ЛЕЧЕНИЯ И ПРОФИЛАКТИКИ ТОКСИКОЗОВ БЕРЕМЕННЫХ ЖИВОТНЫХ | 1997 |
|
RU2136289C1 |
| СПОСОБ ВОССТАНОВЛЕНИЯ ФУНКЦИОНАЛЬНОГО ПОЧЕЧНОГО РЕЗЕРВА | 1993 |
|
RU2084248C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ СТЕПЕНИ УРЕМИЧЕСКОЙ ЭНЦЕФАЛОПАТИИ У БОЛЬНЫХ С ХРОНИЧЕСКОЙ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТЬЮ | 2004 |
|
RU2272562C1 |
| Способ лечения пациентов с хронической болезнью почек V стадии на диализном этапе | 2020 |
|
RU2753127C1 |
| СРЕДСТВО ДЛЯ ЛЕЧЕНИЯ НИЗКООБМЕННОГО ВАРИАНТА ЗАБОЛЕВАНИЯ СКЕЛЕТА У БОЛЬНЫХ С ХРОНИЧЕСКОЙ ПОЧЕЧНОЙ НЕДОСТАТОЧНОСТЬЮ | 2012 |
|
RU2485957C1 |
| СПОСОБ ЭНТЕРОСОРБЦИИ | 1997 |
|
RU2122868C1 |
| СПОСОБ УСТАНОВЛЕНИЯ УРЕМИЧЕСКОГО ГЕНЕЗА ПОЛИНЕВРОПАТИИ | 2006 |
|
RU2314527C1 |

Изобретение относится к медицине, а именно к нефроурологии, и касается лечения уремии. Для этого вводят гелевую форму мелкодисперсного хитозана перорально или через зонд по 4 мл на 1 кг массы тела через каждые 3 ч. Способ приводит к эффективной детоксикации при уремии различного генеза, в том числе у инкурабельных больных при удлинении додиализного промежутка, когда активные методы лечения противопоказаны. 3 ил.
Способ лечения уремического синдрома путем введения в желудочно-кишечный тракт энтеросорбентов, отличающийся тем, что для этого используют гелевую форму мелкодисперсного хитозана перорально или через зонд по 4 мл на 1 кг массы тела через каждые 3 ч.
| JING S.B | |||
| et al., - in J | |||
| Pharm Pharmacol., 1997, v | |||
| Способ смешанной растительной и животной проклейки бумаги | 1922 |
|
SU49A1 |
| РУЧНОЙ ПИТАТЕЛЬНЫЙ НАСОС | 1921 |
|
SU721A1 |
| БИО-, ГЕМОСОВМЕСТИМЫЕ СОРБЕНТЫ НА ОСНОВЕ СВЕРХСШИТЫХ ПОЛИМЕРОВ СТИРОЛА С МОДИФИЦИРОВАННОЙ ПОВЕРХНОСТЬЮ, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И СПОСОБ ПОЛУЧЕНИЯ МАТРИЦЫ СОРБЕНТА | 1996 |
|
RU2089283C1 |
| 2000 |
|
RU2156133C1 | |
| СПОСОБ ВЫВЕДЕНИЯ СВИНЦА И НИКЕЛЯ ИЗ ОРГАНИЗМА КОРОВ | 2000 |
|
RU2175234C1 |
| Способ размножения копий рисунков, текста и т.п. | 1921 |
|
SU89A1 |
| КОМАРОВ Б.А | |||
| и др | |||
| Новые перспективы в исследовании хитина и хитозана | |||
| Материалы Пятой конференции | |||
| - М.: Щелково, 1999, с | |||
| Раздвижной паровозный золотник с подвижными по его скалке поршнями между упорными шайбами | 1922 |
|
SU148A1 |
Авторы
Даты
2003-04-10—Публикация
2001-06-08—Подача