Текст описания в факсимильном виде (см. графическую часть). ТC
| название | год | авторы | номер документа |
|---|---|---|---|
| МЕЧЕНЫЕ РАДИОАКТИВНЫМ ИЗОТОПОМ ПЕПТИДЫ ДЛЯ ДИАГНОСТИКИ И ТЕРАПИИ | 1996 |
|
RU2171117C2 |
| СПОСОБ ПОЛУЧЕНИЯ ТИОЭФИРА ПЕПТИДА | 2010 |
|
RU2529998C2 |
| СОЕДИНЕНИЯ НА ОСНОВЕ ПЕПТИДОВ ДЛЯ НАПРАВЛЕННОЙ ДОСТАВКИ К РЕЦЕПТОРАМ ИНТЕГРИНОВ | 2002 |
|
RU2303042C2 |
| ПЕПТИДНЫЕ АНТАГОНИСТЫ ПЕПТИДНЫХ ГОРМОНОВ ИЗ СЕМЕЙСТВА КАЛЬЦИТОНИНА (КАЛЬЦИТОНИН ГЕН-РОДСТВЕННЫХ ПЕПТИДОВ (CGRP)) И ИХ ПРИМЕНЕНИЕ | 2013 |
|
RU2624016C2 |
| ПЕПТИДНЫЕ АНТАГОНИСТЫ ПЕПТИДНЫХ ГОРМОНОВ ИЗ СЕМЕЙСТВА КАЛЬЦИТОНИНА (CGRP) И ИХ ПРИМЕНЕНИЕ | 2017 |
|
RU2742826C2 |
| СПОСОБ УМЕНЬШЕНИЯ ОКИСЛИТЕЛЬНОГО ПОВРЕЖДЕНИЯ (ВАРИАНТЫ) | 2005 |
|
RU2376028C2 |
| КОНЪЮГАТЫ АНТАГОНИСТА ПЕПТИДА АНАЛОГА БОМБЕЗИНА | 2009 |
|
RU2523531C2 |
| СИНТЕТИЧЕСКИЕ ПЕПТИДНЫЕ АМИДЫ | 2007 |
|
RU2500685C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕПТИДА | 2008 |
|
RU2478105C2 |
| СИНТЕТИЧЕСКИЕ ПЕПТИДНЫЕ АМИДЫ И ИХ ДИМЕРЫ | 2007 |
|
RU2510399C2 |














































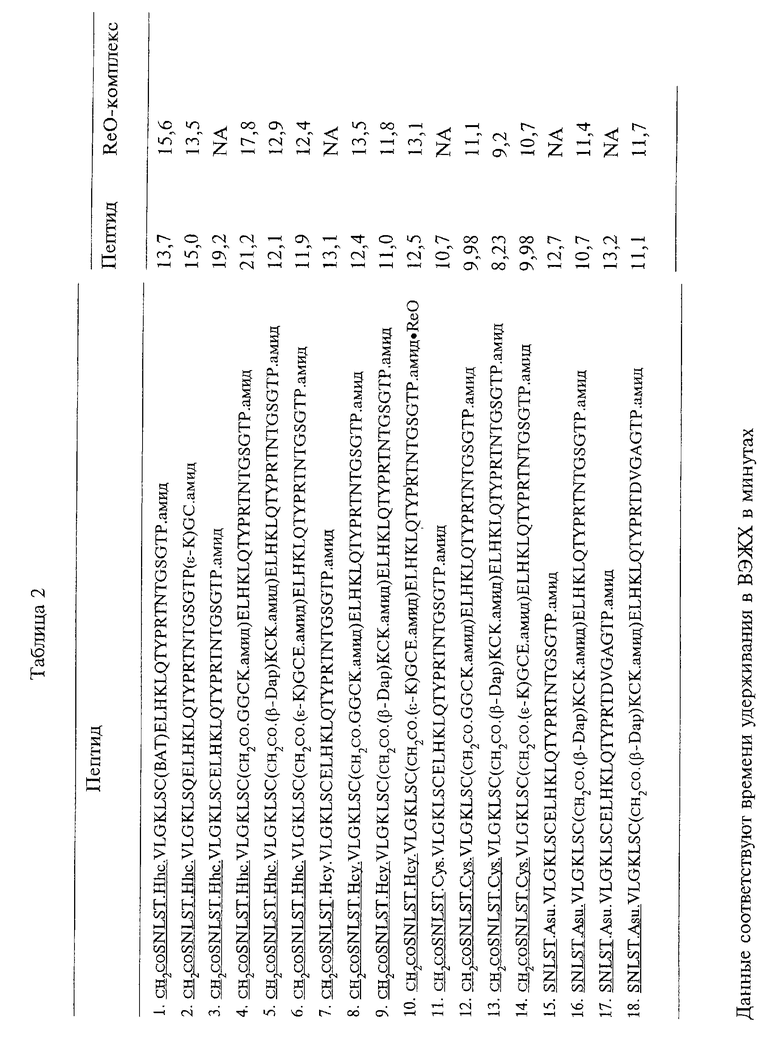








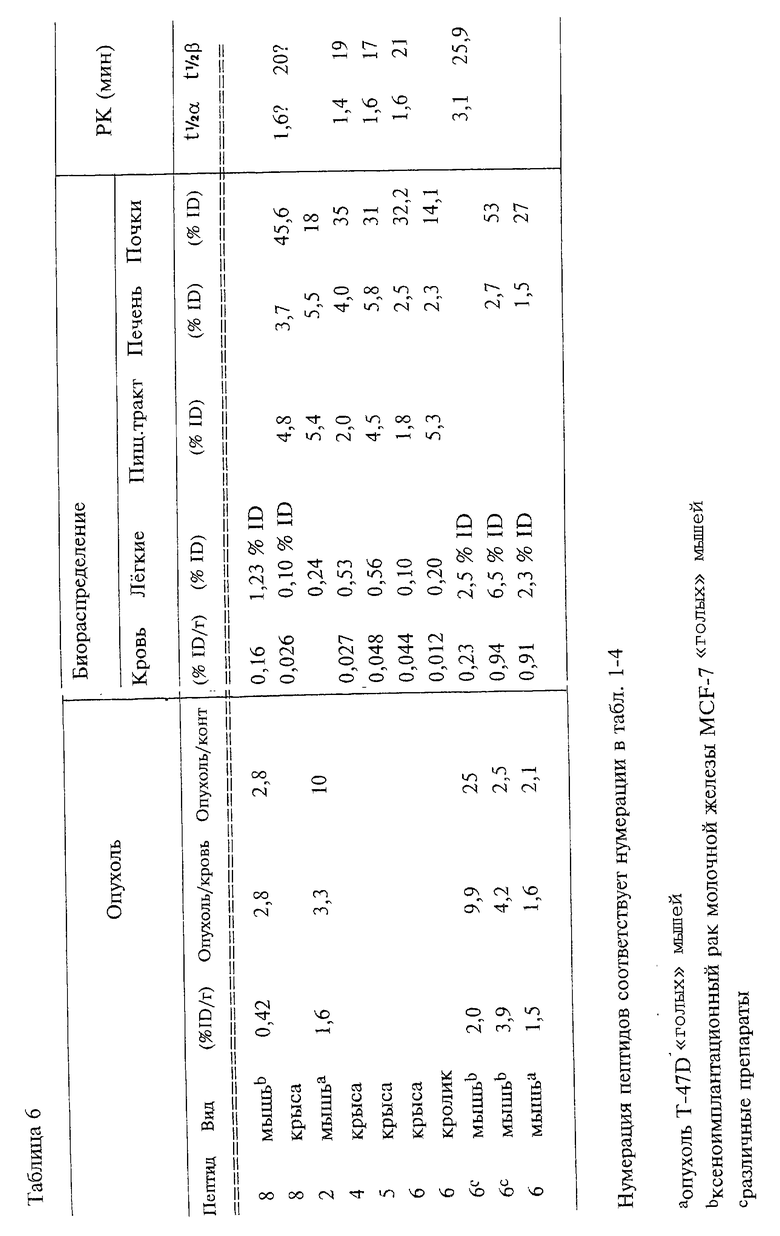









Изобретение относится к синтетическому связывающемуся с рецепторами кальцитонина соединению, имеющему молекулярную массу менее 10000 Д, которое представляет собой пептид, ковалентно соединенное с хелатором радиоактивного металла с образованием реагента, при этом упомянутый реагент проявляет аффинность по связыванию с рецептором кальцитонина, равную или превышающую аффинность связывания с упомянутым рецептором, характерную для нативного, помеченного радиоактивным йодом кальцитонина. Соединения могут быть помечены радиоактивным способом с помощью подходящего изотопа и использоваться в качестве радиодиагностических или радиотерапевтических средств для визуализации опухолей в теле млекопитающего. Описаны также сцинтиграфическое визуализирующее средство для определения локализации и характера опухоли, композиция для образования комплекса реагента с радиоактивным технецием или рением, радиотерапевтическое средство для сцинтиляционной визуализации, набор для получения радиофармацевтического препарата и способ получения описанного реагента. 9 с. и 5 з.п. ф-лы, 6 табл.
a) пептида, характеризующегося аминокислотной последовательностью
СН2СО. SNLST. Hhc. VLGKLSCELHKLQTYPRTNTGSGTP. амид (SEQ ID N0 : 9),
где хелатор встраивается в состав пептида по боковой аминокислотной цепи указанной последовательности,
b) пептида, включающего домен связывания с рецептором кальцитонина, который циклизован с помощью тиоэфирной связи;
c) пептида, включающего аминокислотную последовательность
CH2CO. SNLSTX - SEQ ID N0 : 10;
где X выбирается из группы, включающей остаток цистеина, остаток гомоцистеина и остаток гомогомоцистеина;
d) пептида, включающего аминокислотную последовательность:
СН2СО. Х1LSTХ2 - SEQ ID N0 : 11;
где X1 выбирается из группы, включающей остаток аланина, остаток глицина и остаток серина;
X2 выбирается из группы, включающей остаток цистеина, остаток гомоцистеина и остаток гомогомоцистеина, ковалентно соединенное с хелатором радиоактивного металла с образованием реагента, при этом указанный реагент проявляет аффинность по связыванию с рецептором кальцитонина, равную или превышающую аффинность связывания с указанным рецептором, характерную для нативного, помеченного радиоактивным йодом кальцитонина.
a) пептида, характеризующегося аминокислотной последовательностью
СН2СО. SNLST. Hhc. VLGKLSCELHKLQTYPRTNTGSGTP. амид (SEQ ID N0 : 9),
где хелатор встраивается в состав пептида по боковой аминокислотной цепи указанной последовательности;
b) пептида, включающего домен связывания с рецептором кальцитонина, который циклизован с помощью тиоэфирной связи;
c) пептида, включающего аминокислотную последовательность:
CH2CO. SNLSTX - SEQ ID N0 : 10;
где X выбирается из группы, включающей остаток цистеина, остаток гомоцистеина и остаток гомогомоцистеина;
d) пептида, включающего аминокислотную последовательность:
CH2CO. X1LSTX2 - SEQ ID N0 : 11;
где X1 выбирается из группы, включающей остаток аланина, остаток глицина и остаток серина;
X2 выбирается из группы, включающей остаток цистеина, остаток гомоцистеина и остаток гомогомоцистеина, ковалентно соединенное с хелатором радиоактивного металла с образованием реагента, при этом указанный реагент проявляет аффинность по связыванию с рецептором кальцитонина, составляющую не менее одной десятой от аффинности связывания с указанным рецептором, характерную для нативного, помеченного радиоактивным йодом кальцитонина.
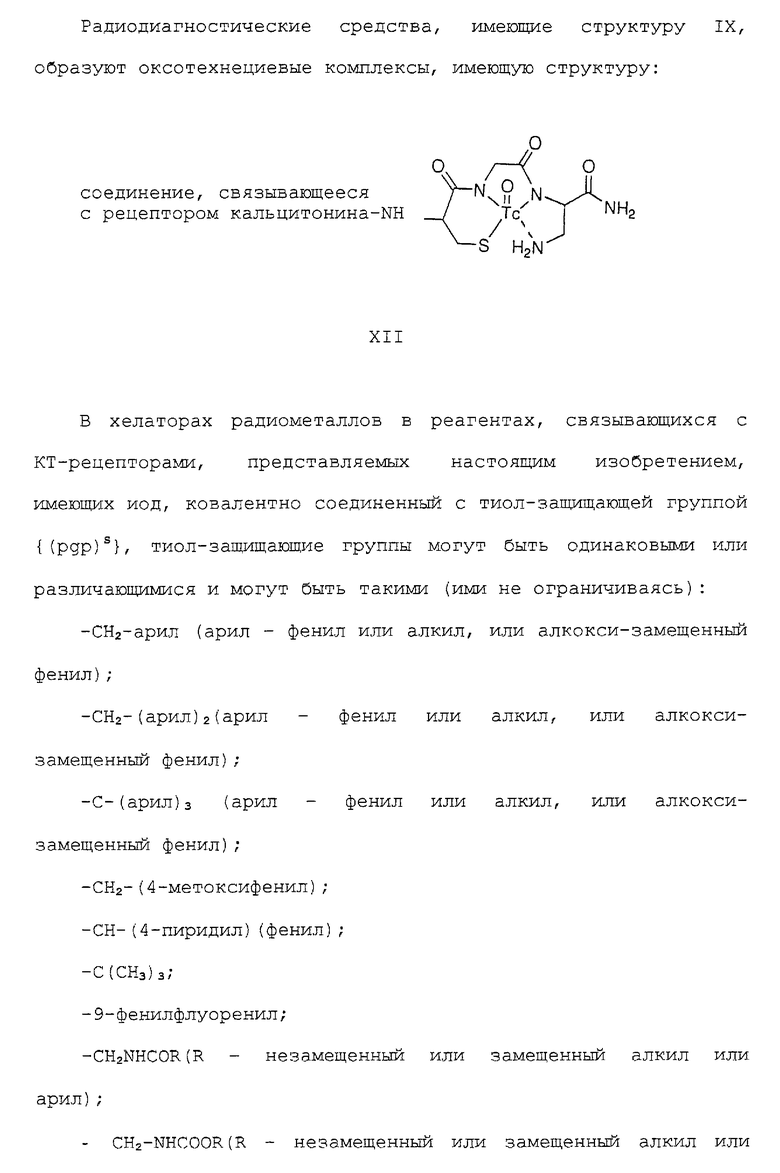
а) C(pgp)S-(aa)-C(pgp)S,
где (pgp)S - Н или тиолзащищающая группа;
(аа) - любая первичная α- или β-аминокислота,
b)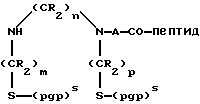
где каждый R независимо представляет собой Н, СН3 или С2Н5;
каждый из (рgр)S независимо представляет собой тиолзащищенную группу или Н;
m, n или р - независимо представляют собой 2 или 3;
А = линейный или циклический низший алкил;
с)
где каждый R независимо представляет собой Н, СН3 или С2Н5;
m, n или р - независимо представляют собой 2 или 3;
А = линейный или циклический низший алкил;
V = Н или -СО-пептид;
R' = Н или пептид;
при этом, что когда V = Н, то R' = пептид и когда R'= H, то V = -СО-пептид;
d)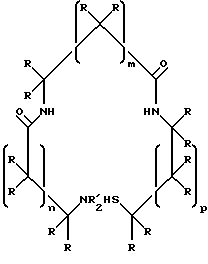
где n, m и р независимо представляют собой 0 или 1;
каждый R' независимо представляет собой Н, низший алкил, гидроксиалкил(С2-С4) или алкоксиалкил(С2-С4);
каждый R независимо представляет собой Н или R", где R" представляет собой замещенный или незамещенный низший алкил или фенил, не включающий тиоловую группу;
один из R или R' представляет собой L, при этом когда R' представляет собой L, то -NR'2 представляет собой амин, а L представляет собой бивалентную группу, связывающую хелатор с соединением;
е)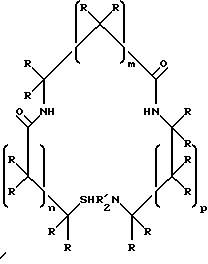
где n, m и р независимо представляют собой 0 или 1;
каждый R' независимо представляет собой Н, низший алкил, гидроксиалкил(C2-C4) или алкоксиалкил(С2-С4);
каждый R независимо представляет собой Н или R", где R" представляет собой замещенный или незамещенный низший алкил или фенил, не включающий тиоловую группу;
один из R или R' представляет собой L, при том, что когда R' представляет собой L, то -NR'2 представляет собой амин, а L представляет собой бивалентную группу, связывающую хелатор с соединением;
f)
(HOOCCH2)2 N (CR2) (CR2) N (CH2COOH) (CR2) (CR2) N (CH2COOH);
где каждый R независимо представляет собой Н, C1-C4-алкил или арил, а один R ковалентно соединен с бивалентным линкером;
g)
(HOOCCH2)2 N (CR2) (CR2) N (СН2СООН);
где каждый R независимо представляет собой Н, С1-С4 алкил или арил, а один R ковалентно соединен с бивалентным линкером;
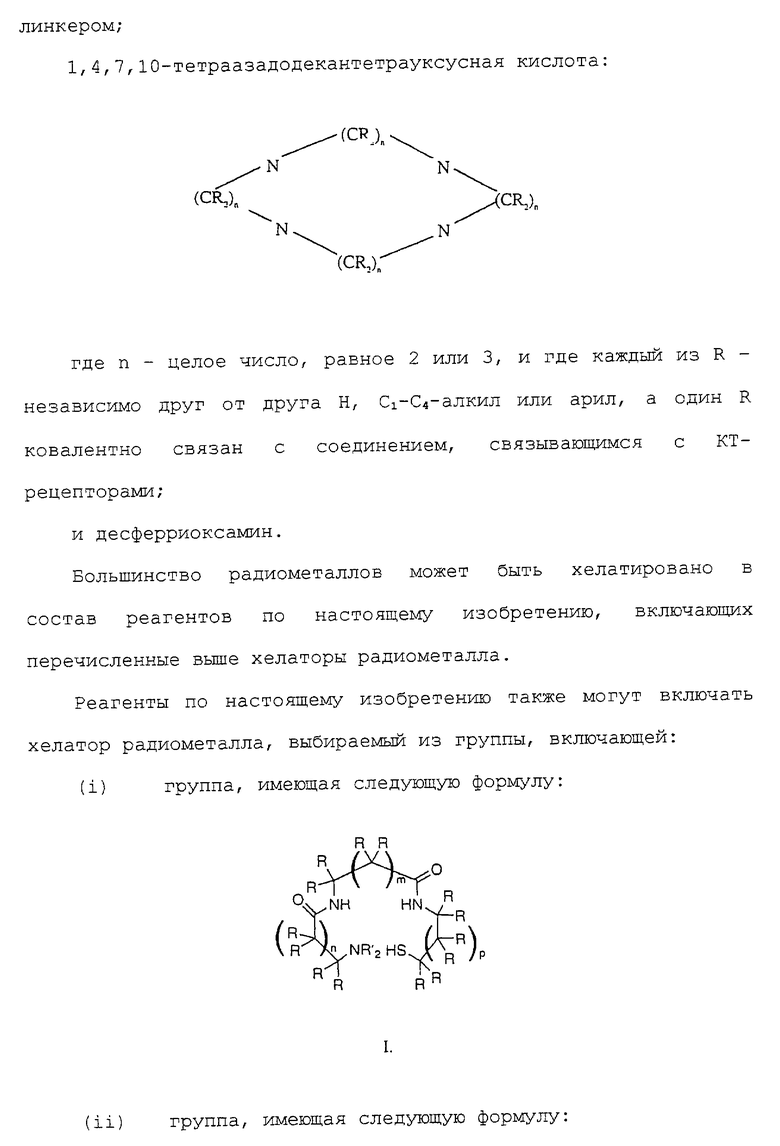
h) 1,4,7,10-тетраазадодекантетрауксусная кислота;
i)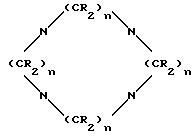
где n - целое число, равное 2 или 3;
каждый R независимо представляет собой Н, С1-С4-алкил или арил, а один R ковалентно соединен со связывающимся с рецепторами кальцитонина соединением;
j) десферриоксиамин.
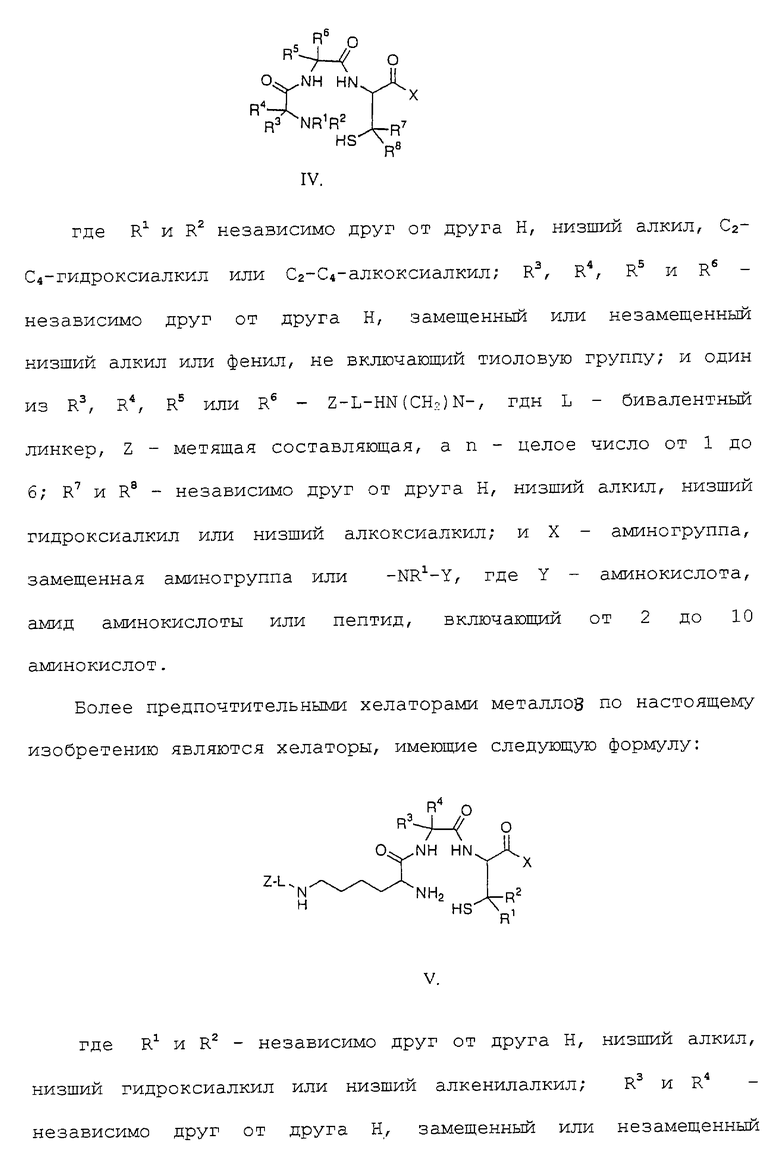
A-CZ (B) - { C(R1R2)} n - X,
где А представляет собой Н, НООС, H2NOC, (аминокислота или пептид)-NHOC, (аминокислота или пептид)-ООС или R4;
В представляет собой Н, SH, -NHR3, -N(R3)-(аминокислота или пептид) или R4;
Х представляет собой Н, SH, -NHR3, -N(R3)-(аминокислота или пептид) или R4;
Z представляет собой Н или R4;
R1, R2, R3 и R4 - независимо представляют собой Н или с прямой или разветвленной цепью или циклический низший алкил;
n представляет собой 0, 1 или 2;
(аминокислота) представляет собой любую первичную α- или β-аминокислоту, не имеющую тиоловой группы;
(пептид) представляет собой пептид, включающий 2-10 аминокислот;
где В представляет собой -NHR3 или -N(R3)-(аминокислота или пептид); Х представляет собой SH; n представляет собой 1 или 2;
где Х представляет собой -NHR3 или -N(R3)-(аминокислота или пептид), В представляет собой SH; n представляет собой 1 или 2;
где В представляет собой Н или R4; А представляет собой НООС, H2NOC, (аминокислота или пептид)-NHOC, или (аминокислота или пептид)-ООС; Х представляет собой SH; n представляет собой 0 или 1;
где А представляет собой Н или R4, далее где В представляет собой SH, Х представляет собой -NHR3 или -N(R3)-(аминокислота или пептид) и где Х представляет собой SH, В представляет собой -NHR3 или -N(R3)-(аминокислота или пептид); n представляет собой 1 или 2;
где Х представляет собой Н или R4, А представляет собой НООС, H2NOC, (аминокислота или пептид)-NHOC или (аминокислота или пептид)-ООС; В представляет собой SH;
где Z представляет собой метил, Х представляет собой метил, А представляет собой НООС, H2NOC, (аминокислота или пептид)-NHOC, или (аминокислота или пептид)-ООС; В представляет собой SH; n представляет собой 0;
где В представляет собой SH, Х не представляет собой SH и где Х представляет собой SH, В не представляет собой SH;
при этом тиоловая составляющая находится в восстановленной форме;
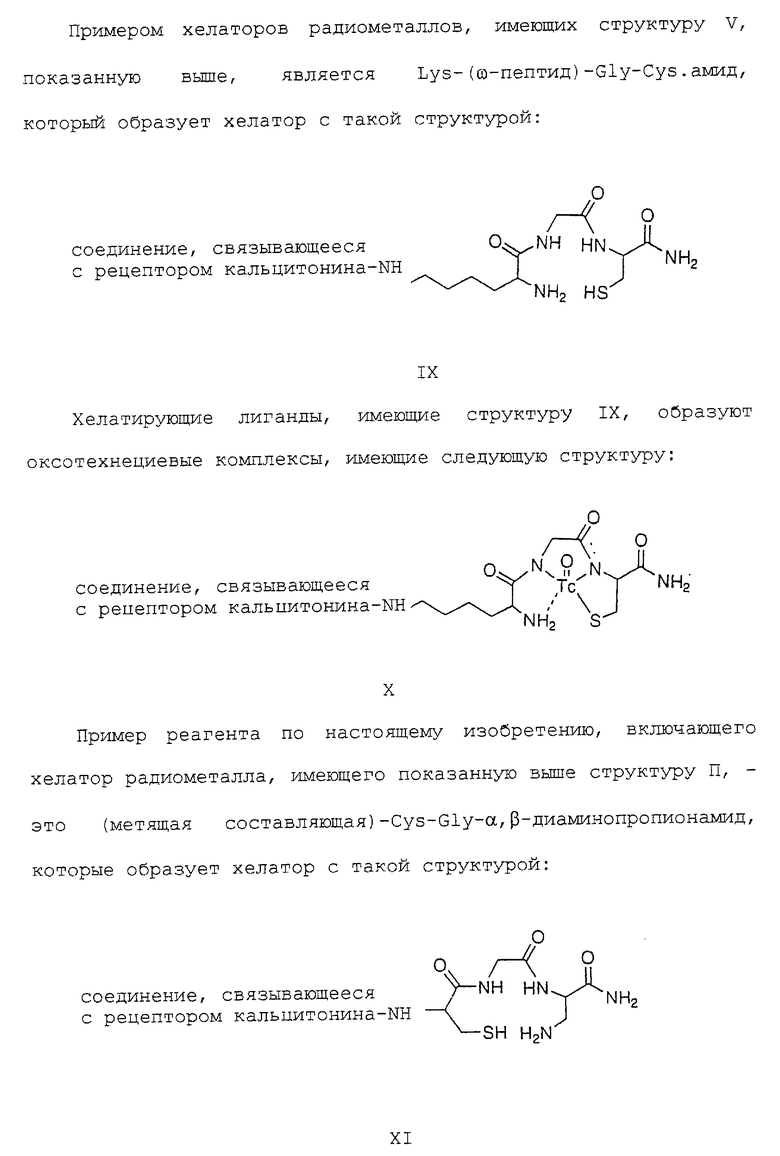
при этом указанный хелатор необязательно выбирают из группы, включающей
a) - (аминокислота)1-(аминокислота)2 { A-CZ(В)-{ С(R1R2)} n-X} ;
b) -{ A-CZ(В)-{ C(R1R2)} n-X} - (аминокислота)1-(аминокислота)2;
c) -(первичная α-, β- или β, γ-диаминокислота)-(аминокислота)1-{ A-CZ(В)-{ С(R1R2)} n-X} ;
d) { A-CZ(В)-{ С(R1R2)} n-X} -(аминокислота)1-(первичная α-, β- или β, γ-диаминокислота),
где (аминокислота)1 и (аминокислота)2 независимо представляют собой любые естественно встречающиеся, модифицированные, замещенные или измененные α или β аминокислоты, не включающие тиоловую группу; I
e) (аминокислота)1-(аминокислота)2-цистеин;
f) (аминокислота)1-(аминокислота)2-изоцистеин-;
g) (аминокислота)1-(аминокислота)2-гомоцистеин-;
h) (аминокислота)1-(аминокислота)2-пеницилламин-;
i) (аминокислота)1-(аминокислота)2-2-мepкaптoэтилaмин-;
j) (аминокислота)1-(аминокислота)2-2-мepкaптoпpoпилaмин-;
k) (аминокислота)1-(аминокислота)2-2-мepкaптo-2-метилпропиламин-; и
l) (аминокислота)1-(аминокислота)2 -3-меркаптопропиламин-; при этом карбоксильный конец или боковая цепь указанного хелатора ковалентно связана с соединением и (аминокислота)1 необязательно выбирается из группы, включающей α, β-диаминокислоту, имеющую свободный α-амин и β, γ-диаминокислоту, имеющую свободный β-амин;
m) -цистеин-(аминокислота)-(α, β- или β, γ-диаминокислота);
n) -изоцистеин-(аминокислота)-(α, β- или β, γ-диаминокислота);
о) -гомоцистеин-(аминокислота)-(α, β- или β, γ-диаминокислота);
р) -пеницилламин-(аминокислота)-(α, β- или β, γ-диаминокислота);
q) 2-меркаптоуксусная кислота- (аминокислота)-(α, β- или β, γ--диаминокислота);
r) 2- или 3-меркаптопропионовая кислота-(аминокислота)-(α, β- или β, γ-диаминокислота); и
s) 2-меркапто-2-метилпропионовая кислота-(аминокислота)-(α, β- или β, γ-диаминокислота);
при этом N-конец или боковая цепь указанного хелатора ковалентно связана с соединением;
t) -Gly-Gly-Cys-;
u) -Ala-Gly-Cys-;
v) - (ε -Lys)-Gly-Cys-;
w) - (δ-Orn)-Gly-Cys-;
x) - (γ-Dab)-Gly-Cys-;
у) - (β-Dap)-Lys-Cys-;
z) - (β-Dap)-Gly-Cys-;
aa) - Cys(BAT).
CH2COSNLST. Hhc. VLGKLSC (BAT) ELHKLQTYPRTNTGSGTP. амид (SEQ ID N0 : 4)
CH2COSNLST. Hhc. VLGKLSQELHKLQTYPRTNTGSGTP (ε -K) GC. амид
CH2COSNLST. Hhc. VLGKLSC(CH2CO. GGCK. амид)
ELHKLQTYPRTNTGSGTP. амид
CH2CO. SNLST. Hhc. VLGKLSC(CH2CO. (β-Dap)KCK. амид)
ELHKLQTYPRTNTGSGTP. амид
CH2CO. SNLST. Hhc. VLGKLSC(CH2CO. (ε-K)GCE. амид)
ELHKLQTYPRTNTGSGTP. амид
СН2СО. SNLST. Hey. VLGKLSC(CH2CO. GGCK. амид)
ELHKLQTYPRTNTGSGTP. амид
CH2CO. SNLST. Hey. VLGKLSC(CH2CO. (β-Dap)KCK. амид)
ELHKLQTYPRTNTGSGTP. амид
CH2CO. SNLST. Hey. VLGKLSC(CH2CO. (ε-K)GCE. амид)
ELHKLQTYPRTNTGSGTP. амид
СН2СО. SNLST. Cys. VLGKLSC(CH2CO. (GGCK. амид)
ELHKLQTYPRTNTGSGTP. амид
СН2СО. SNLST. Cys. VLGKLSC(CH2CO. (β-Dap)KCK. амид)
ELHKLQTYPRTNTGSGTP. амид
CH2CO. SNLST. Cys. VLGKLSC (CH2CO. (ε-K)GCE. амид)
ELHKLQTYPRTNTGSGTP. амид
SNLST. Asu. VLGKLSC(CH2CO. (β-Dap)KCK. амид)
ELHKLQTYPRTNTGSGTP. амид
SNLST. Asu. VLGKLSC(CH2CO. (β-Dap)KCK. амид)
ELHKLQTYPRTNTGSGTP. амид
CH2COSNLST. Hhc. VLGKLSCELHKLQTYPRTNTGSGTP. амид (SEQ ID N0 : 5);
CH2COSNLST. Hсy. VLGKLSCELHKLQTYPRTNTGSGTP. амид (SEQ ID N0 : 6);
CH2COSNLST. Cys. VLGKLSCELHKLQTYPRTNTGSGTP. амид (SEQ ID N0 : 7);
SNLST. Asu. VLGKLSCELHKLQTYPRTNTGSGTP. амид (SEQ ID N0 : 8).
CH2CO. SNLST. Hhc. VLGKLSC(CH2CO. (ε-К)GCE. амид)
ELHKLQTYPRTNTGSGTP. амид.
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| RU 94046010 А1, 20.10.1996 | |||
| Прибор для очистки паром от сажи дымогарных трубок в паровозных котлах | 1913 |
|
SU95A1 |
| US 5508020 А, 16.04.1996. | |||
Авторы
Даты
2003-05-27—Публикация
1998-05-01—Подача