Данное изобретение относится к аналитическому прибору для определения аналитов в жидких молочных продуктах, таких как молоко. Оно также относится к обнаружению и количественному определению аналитов в молоке с помощью этого аналитического устройства и к аналитическому набору, содержащему это аналитическое устройство.
В настоящее время гигиенические требования во многих странах вызывают необходимость регулярного контроля наличия в молочных продуктах различных веществ, таких как лекарственные препараты для животных и гормоны, которые обычно применяются при разведении крупного рогатого скота. По очевидным медицинским причинам этих веществ необходимо избегать в молочных продуктах, потребляемых человеком.
В других случаях желательно проводить испытания, которые делают возможным обнаружение эндогенных веществ в молоке, чтобы оптимизировать разведение скота. В частности, быстрое определение уровня гормонов в молоке дает возможность легко определять предпочтительные для репродукции фазы.
В других случаях ведется поиск надежных и удобных методов контроля источника молочных продуктов, полученных из молока различных видов животных. Т. е. поиск методов, которые дали бы возможность определять наличие белков, характерных для данного вида молока в отличие от других видов.
В литературе известны, кроме того, различные тесты для обнаружения аналитов в биологических жидкостях. В этих тестах обычно используют способы обнаружения с применением распознающего агента (рецептора или антитела), который специфично распознает аналит или аналог этого аналита, и метки (радиоактивного изотопа, фермента, флуоресцирующего агента); в данном описании эти агенты далее называются детекторы. В зависимости от избранных элементов метод называется радиоиммуноанализ (РИА), радиорецепторный анализ (РРА), иммуноферментный анализ с афинной хроматографией (EIA) и т.д. В принципе в этих тестах применяют, как минимум, комбинацию из двух вышеназванных элементов (детекторов), позволяющую получить в результате величину, отражающую количество присутствующего аналита.
Следует заметить, что в зависимости от выбранного метода обнаружения, изотоп может присоединяться либо к распознающему агенту, либо к аналиту или к аналогу аналита при условии его распознавания распознающим агентом. Существуют способы, в которых распознающий агент или аналит или аналог аналита содержит изначально (по своей сути) изотоп (например, радиоактивный аналит).
В случае молочных продуктов наиболее широко описаны тесты по обнаружению аналитов, относящиеся к обнаружению антибиотиков. Действительно, хорошо известно, что антибиотики используются для лечения некоторых инфекционных заболеваний у молочного скота. Однако по очевидным медицинским требованиям молоко, предназначенное в пищу человеку, в принципе не должно содержать никаких следов антибиотиков. Более того, концентрация пенициллина 0,005 межд. ед. /млн. или менее может оказывать вредное влияние в процессе производства молочных продуктов, таких как сыр, йогурт и т.д.
Можно представить себе множество ситуаций. В первом случае, например, чтобы обнаружить антибиотики на ферме перед погрузкой на транспорт, приоритет будет за чрезвычайно быстрым (менее 5 минут) и простым тестом. Также можно представить себе применение подобного быстрого теста, когда, например, применявшийся при лечении антибиотик известен и, кроме того, когда этот искомый антибиотик может быть обнаружен с помощью национального эталона. В этом втором случае, когда акцент не делается на скорости, важным является обнаружение большинства, если не всех антибиотиков с помощью национальных (федеральных) эталонов.
Это вызвано тем, что законами некоторых стран утверждены совершенно конкретные стандарты качества. Например, американские власти требуют, чтобы концентрация в молоке шести следующих антибиотиков не превышала конкретных значений: пенициллин, 5 частей на миллиард, ч/млрд.; ампициллин, 10 ч/млрд.; амоксициллин 10 ч/млрд. ; клоксациллин 10 ч/млрд.; цефапирин, 20 ч/млрд.; цефтиофур, 50 ч/млрд. Европейским Союзом, в свою очередь, также утверждены стандарты качества: пенициллин, 4 ч/млрд.; амоксициллин 4 ч/млрд.; ампициллин, 4 ч/млрд.; клоксациллин 30 ч/млрд.; диклоксациллин 30 ч/млрд.; оксациллин 30 ч/млрд.; цефапирин, 10 ч/млрд.; цефтиофур, 100 ч/млрд.; цефхинон (cefquinone) 20 ч/млрд.; нафциллин 30 ч/млрд.; цефазолин 50 ч/млрд.
Следовательно, было бы полезно иметь доступный тест, позволяющий обнаружить большинство антибиотиков. Кроме того, можно полагать, что в отсутствие теста, сочетающего в себе все характеристики: скорость, чувствительность и простоту, - для молочной промышленности было бы полезно иметь тест, который бы позволял наилучшее сочетание этих трех параметров, даже если он не полностью отвечает им.
В патенте США 4239852 описан микробиологический способ обнаружения в молоке антибиотиков, содержащих цикл β-лактама. По этому способу образец молока сначала термостатируют в присутствии частей клеток микроорганизма с высокой чувствительностью к антибиотикам, и особенно Bacillus stearothermophilus, а затем в присутствии антибиотика, "меченого" радиоактивным изотопом или ферментом. Термостатирование проводят в условиях, позволяющих антибиотикам, если они присутствуют в образце, и меченому антибиотику связываться с частями клеток.
После термостатирования части клеток выделяют из смеси и затем отмывают. Затем определяют, количество меченого антибиотика, связанного с частями клеток и сравнивают с эталоном. Количество меченого антибиотика, связанного с частями клеток, обратно пропорционально концентрации антибиотика, имеющегося в анализируемом образце молока.
Этот способ требует очень точных манипуляций, особенно на стадии выделения частей клеток из смеси. Кроме того, в своем наиболее чувствительном варианте этот способ использует антибиотик, меченый радиоактивным изотопом (14С или 125I). В этом случае количественное определение антибиотика, присутствующего или иным образом оказавшегося в молоке, требует применения специального прибора, например, такого как сцинтилляционный счетчик. Далее, работа с радиоактивными веществами, даже в очень малых количествах, не совсем безопасна для человека, осуществляющего анализ.
В Европейской патентной заявке 593112 описан другой способ, позволяющий определять антибиотики в молоке. Этот способ использует белок, выделенный из чувствительного к антибиотику микроорганизма, такого как Bacillus stearothermophilus. Этот белок дополнительно метят ферментом, таким как пероксидаза.
Испытание проводят следующим образом: образец молока термостатируют в пробирке в присутствии меченого белка; после термостатирования молоко переносят в другую пробирку, на стенках которой иммобилизован эталонный антибиотик (антибиотик сравнения); проводят второе термостатирование, а затем удаляют содержимое из пробирки; стенки этой второй пробирки трижды промывают промывным раствором, который в свою очередь выливают, а затем остатки из второй пробирки переносят на лист промокательной бумаги; во вторую пробирку затем добавляют окрашивающее вещество, ее снова термостатируют, а затем добавляют раствор, замедляющий процесс проявления цвета; окрашивание пробирки сравнивают с окрашиванием стандартного образца антибиотика, с которым параллельно проводят идентичное испытание. Количество меченого белка, иммобилизованного на подложке, и, следовательно, интенсивность окрашивания обратно пропорциональны количеству антибиотика, присутствующему в анализируемом образце молока.
Согласно Примеру 1 этой патентной заявки, этот тест дает возможность обнаруживать пенициллин G вплоть до концентрации порядка 5 ч/млрд., позволяет обнаруживать амоксициллин (5 ч/млрд.), ампициллин (10 ч/млрд.), цефапирин (5 ч/млрд.) и цефтиофур (5 ч/млрд.).
Однако испытание это очень утомительно, особенно для неспециалистов. Действительно, этот тест содержит много стадий, включая стадии переноса жидкости и остатков из одной емкости в другую, и ряд стадий отмывания. Точное число и вид стадий, требующихся при этом испытании, очень сильно зависит от знания исполнителем ноу-хау эксперимента.
Кроме того, для интерпретации результата требуется параллельное проведение двух испытаний, что увеличивает и еще более усложняет операции.
Раскрыты также другие типы ферментативных способов, которые позволяют определять низкие концентрации антибиотиков в молоке (J.M. Frere et al., Antimicrobial Agents and Chemotherapy, 18(4), 506-510 (1980), и патенты, Европейский патент ЕР 85667 и ЕР 468946), которые основаны на применении специфического фермента, а именно, растворимой внеклеточной D-аланин-D-аланинкарбосипептидазы, продуцируемой Actinomadura R39 (обозначен в данном описании "фермент R39"). Фермент R39 обладает специфичной активностью в отношении гидролиза групп D-аланин-D-аланина различных пептидов и также может гидролизовать некоторые тиоэфиры.
Кроме того, фермент R39 реагирует с антибиотиками, содержащими цикл β-лактама, очень быстро и практически необратимо, образуя эквимолярный неактивный комплекс фермент-антибиотик.
В самом последнем варианте этого теста (Европейский патент ЕР 468946) заданный объем образца жидкости для испытания термостатировали с заданным количеством фермента R39 в условиях, которые позволяют β-лактам-содержащему антибиотику, возможно, присутствующему в образце, реагировать с ферментом, образуя эквимолекулярный комплекс, неактивный и практически не распадающийся обратно.
Затем заданное количество тиоэфирного субстрата термостатируют с продуктом, полученным на первой стадии в условиях, при которых субстрат может гидролизоваться остаточным ферментом R39, который не образовал комплекс с антибиотиком в ходе первого термостатирования. Количество образовавшегося при этом меркаптоалкановой кислоты затем определяют методом колориметрии с помощью реагента, вызывающего окрашивание за счет реакции со свободной SH-группой меркаптоалкановой кислоты. Интенсивность окрашивания сравнивают со стандартом, заранее установленным с помощью образцов, содержащих известные количества антибиотиков. Количественное определение можно проводить с помощью измерений на спектрофотометре; в случае молока может возникнуть необходимость предварительно осветлять образец.
Ясно, что этот тест содержит меньшее число стадий и более прост для проведения, чем тест, описанный в Европейской патентной заявке 593112. Однако он ограничивается определением антибиотиков, содержащих цикл β-лактама, и ограниченными пределами определения, доступными в случае фермента R39. С учетом этого этот тест нельзя применять в случае других рецепторов антибиотиков, и нельзя непосредственно взять за основу для обнаружения других аналитов в молоке.
Учитывая, что имеющиеся тесты все еще имеют различные недостатки, заявитель поставил целью поиск новых методов детектирования аналитов в жидких молочных продуктах, причем от искомых методов требовалось, чтобы они позволяли обнаруживать различные виды аналитов надежно, предпочтительно, во время сбора на ферме. Заявитель, следовательно, разработал метод, который позволяет получать очень быстро, надежный и чувствительный (точный) результат при ограниченном числе стадий, не требующих никаких специальных ноу-хау. Кроме того, заявитель разработал метод, дающий результат, который легко можно обнаружить визуально и который, кроме того, поддается количественному расчету с помощью измерительных приборов.
Заявитель открыл, что этих целей можно достигнуть с помощью нового аналитического устройства (анализатора), которое позволяет с легкостью определять наличие аналитов в жидких молочных продуктах, особенно, в молоке, приведенного на фиг.1 - 3.
Данное изобретение, следовательно, представляет аналитическое устройство, которое позволяет определять наличие аналитов в жидких молочных продуктах с помощью тангенциальной капиллярной миграции указанного молочного продукта. Аналитическое устройство по изобретению включает твердую подложку (1), которая имеет первый и второй конец и на которой укреплены следующие мембраны последовательно, начиная с первого конца:
- мембрана (2), позволяющая очищать анализируемую жидкость,
- мембрана (3), на которой иммобилизуются одно или более захватывающих веществ, и
- поглощающая мембрана (4),
характеризующиеся тем, что мембрана (2) способна задерживать вещества, находящиеся в молочном продукте, которые препятствуют миграции аналитов, возможно, присутствующих в молочном продукте, и детекторов, применяемых согласно технологии, через аналитическое устройство во время тангенциальной капиллярной миграции образца после того, как первый конец аналитического устройства погружен в анализируемый молочный продукт.
В соответствии с конкретной формой воплощения изобретения аналитическое устройство (анализатор) по данному изобретению дополнительно имеет мембрану (5), на которую нанесен, по меньшей мере, один детектор, способный быстро растворяться в присутствии указанного молочного продукта. Согласно этому конкретному варианту изобретения мембрану (5) следует поместить перед мембраной (3). Ее можно поместить, например, или перед мембраной (2) на первом конце устройства, или между мембраной (2) и мембраной (3), или над или под мембраной (2).
Концы различных мембран, имеющихся в аналитическом устройстве по данному изобретению, наложены друг на друга, так чтобы обеспечить непрерывную миграцию молочного продукта из одной зоны в другую. Предпочтительно, чтобы мембрана (3) была расположена так, чтобы ее ближний конец находился ниже мембраны (2), а ее дальний конец ниже мембраны (4). Мембраны могут, но не обязательно, соприкасаться друг с другом с помощью клейкой полимерной пленки (6). В этом случае клейкую полимерную пленку выбирают так, чтобы не вызывать миграции жидкости через аналитическое устройство.
Вариант с покрытием аналитического прибора клейкой полимерной пленкой имеет два преимущества: она обеспечивает действительный контакт в точке совмещения (наложения) мембран и представляет собой защитную пленку. Клейкая полимерная пленка (6) может либо покрывать мембраны (2), (3), (4) и (5) полностью, или частично покрывать отдельные мембраны. Предпочтительно, чтобы клейкая полимерная пленка не покрывала первые несколько миллиметров первого конца, чтобы сделать возможной более быструю миграцию жидкости через мембрану (2) аналитического устройства.
На фигурах 1-3 даны примеры аналитических устройств по данному изобретению. На фигурах 1а, 2 и 3 показан вид спереди (фронтальный), а на фигуре 1b дан продольный разрез.
Твердая подложка (основание) (1) аналитического устройства по данному изобретению сделана из стекла или пластика, предпочтительно, из пластика. В том случае, когда основание сделано из пластика, его толщина обычно составляет 0,05-1 мм, предпочтительно 0,1-0,6 мм. Мембраны закреплены на твердой подложке (1) с помощью клея.
Мембрана (2) может быть различных типов. С одной стороны, она должна удерживать вещества в молочном продукте, препятствующие аналиту, возможно, присутствующему в молочном продукте, и детекторам, применяемым согласно изобретению, мигрировать через аналитическое устройство. С другой стороны, она должна обеспечивать быструю миграцию аналитов и детекторов через аналитическое устройство при сохранении активности этих аналитов и детекторов во время этой миграции. Примерами, не ограничивающими мембраны, позволяющие получать такой результат по изобретению, являются Cytosep 1663 и Leukosorb LK4 (выпускаемые Pall Gelman Sciences), GF/D, GF/DVA, 17 CHR (выпускаемые Whatmann) и стекловолокно типа (выпускаемое GF141 Alstrom).
Предпочтительно применяемая мембрана Leukosorb представляет собой мембрану из нетканого полиэфирного волокна и предназначена для удерживания лейкоцитов при клиническом анализе крови, мочи, слюны и спинномозговой жидкости. Удерживание лейкоцитов осуществляют фильтрованием жидкости при поперечном прохождении через мембрану.
Заявитель неожиданно открыл, что мембраны этого типа также позволяют осуществлять очень важную функцию обнаружения аналитов в молочном продукте с помощью аналитических устройств по данному изобретению, а именно, удерживать вещества, содержащихся в молочных продуктах, которые мешают нормальному проведению теста по определению методом тангенциальной капиллярной быстрой миграции молочного продукта через указанные аналитические устройства, и при этом допускают быструю миграцию аналитов и детекторов.
Для наиболее эффективного осуществления этой функции мембрана (2) должна быть достаточно длинной, чтобы удалять все вещества в молочном продукте, мешающие миграции аналитов и детекторов через аналитическое устройство.
Мембрана (3) должна допускать возможность иммобилизации одного или более захватывающих веществ и быстрой миграции молочного продукта после прохождения через мембрану (2). Предпочтительно, чтобы мембрана (3) была укреплена на непористом основании полиэфирного типа. Примерами, не ограничивающими пригодные по данному изобретению мембраны, являются нитроцеллюлозные мембраны с высокой капиллярной скоростью, такие как мембраны Hi-Flow (поставляемые Millipore), предпочтительно мембраны Hi-Flow типа SX или ST. Эти мембраны обеспечивают оптимальный результат в сочетании с мембранами (2), описанными выше.
Одно или более захватывающих веществ иммобилизуются на мембране (3). Тип иммобилизованного захватывающего вещества, зависит, конечно, от способа обнаружения, (детектирования) аналитов; захватывающие вещества способны селективно иммобилизовать, по меньшей мере, один из компонентов жидкости, мигрирующей через аналитическое устройство, такой, например, как один из детекторов или продукт, полученный в результате образования комплекса этого аналита, или аналога этого аналита, с, по меньшей мере, одним детектором, или же продукт, получающийся при образовании комплекса двух или более детекторов. Захватывающее вещество также может быть одним из детекторов. Захватывающие вещества сконцентрированы на участке или на нескольких четко определенных участках мембраны (3), таких как диски или тонкие полоски, или любая другая пригодная конфигурация. Какая бы конфигурация не была выбрана, она должна обеспечить четкое считывание результатов.
Что касается ее размеров, мембрана (3) должна быть достаточно длинной, чтобы на ней могли разместиться все захватывающие вещества в количествах, требуемых в соответствии со способом детектирования.
Тип мембраны, употребляемой в качестве мембраны (4), имеет наименьшее значение при условии, что она способна абсорбировать и хранить жидкость после прохождения ею предыдущих мембран. Мембрана (4) достаточно велика для того, чтобы можно было абсорбировать жидкость после прохождения через мембрану (3), но, с практической точки зрения, также и для того, чтобы с аналитическим устройством было легче работать.
Аналитическое устройство по изобретению может включать мембрану (5), на которой осаждается, по меньшей мере, один детектор. Мембрана (5) должна допускать миграцию молочного продукта, и в то же время растворение и выделение детектора (или детекторов) при прохождении молочного продукта. Не ограничивающиеся этими примерами мембраны, пригодные для этой цели, суть: мембраны из стекловолокна на полимерной основе, такие как Т5NМ-мембраны (выпускаемые Millipore), F075-14 или мембраны F075-17 или GF/C (выпускаемые Whatman), мембрана Cytosep 1663 (выпускаемая Pall Gelman Sciences), мембраны из полиэфирного волокна на полимерной основе, такие как мембраны Accuwick (фирмы Pall Gelman Sciences), целлюлозная бумага 3 мм (фирмы Whatman) или мембраны типа Release Matrix PT-R2 (фирмы Advances Micro Devices). Предпочтительно применять мембрану из полиэфирного волокна на полимерной основе, такую как мембраны Accuwick. Мембрана (5) достаточной длины, чтобы удерживать нужное количество детектора.
Аналитическое устройство по данному изобретению изготавливается способами, известными специалистам. Панели можно делать, например, используя промышленно доступные ламинаторы. Захватывающие вещества наносятся на мембрану (3) в виде растворов до или после сборки панелей. Эти растворы можно наносить очень точно с помощью промышленных устройств, таких как аппарат на платформе BioJet Quanti-3000 X-Y фирмы BioDot, Inc. Эти нанесенные растворы мгновенно упариваются, например, если поместить в ток горячего воздуха. При больших масштабах производства также можно изготавливать рулоны. Затем панели и рулоны с нанесенными на них заданными захватывающими веществами разрезают на полосы, причем каждая из этих полос представляет собой аналитическое устройство по изобретению.
Когда аналитическое устройство (анализатор) включает мембрану (5), детектор(ы) могут наноситься на нее перед сборкой панелей или рулонов с помощью простого погружения мембраны (5) в раствор, содержащий детектор(ы). Или же реагент(ы) можно наносить после сборки панелей или рулонов способом, подобным таковому, применяемому для нанесения захватывающих веществ на мембраны (3).
В одном варианте изобретения устройство помещают в пластиковый корпус с двумя отверстиями: первое в виде углубления (плоской чаши) расположено точно над мембраной (2) и позволяет анализировать жидкость; второе отверстие представляет собой окно, через которое можно наблюдать за результатом на мембране (3). В этом случае анализатор не содержит клеящую полимерную пленку (6).
Анализатор по данному изобретению позволяет определять наличие аналитов в жидком молочном продукте, особенно молоке. Следовательно, данное изобретение предоставляет способ обнаружения аналитов в жидком молочном продукте, использующий анализатор по данному изобретению и детекторы, и включающий следующие стадии:
а) обеспечение контакта определенного объема молочного продукта с анализатором по данному изобретению, причем этот контакт имеет место на первом конце анализатора;
б) тангенциальная миграция, за счет капиллярности, молочного продукта через анализатор так, что аналиты и детекторы, которые могут быть в молочном продукте, постепенно проходят через мембрану (2), затем мембрану (3), и таким образом, что компоненты молочного продукта, которые не удерживаются мембранами (2) и (3) удерживаются мембраной (4), и
в) определение связывания (фиксации) с мембраной (3).
Способ по данному изобретению позволяет обнаруживать аналиты в жидком молочном продукте таком, например, как молоко, сыворотка, пахта и т.д. Данное изобретение связано более конкретно с обнаружением аналитов таких, как лекарственные вещества, применяемые в ветеринарии, гормоны или белки, которые могут находиться в молоке.
Детекторы, применяемые в соответствии со способом по изобретению, могут отличаться как количественно, так и по природе в зависимости от способа осуществления изобретения, который сам по себе основан на практическом опытном методе обнаружения. В способе по данному изобретению используется, по меньшей мере, два детектора. Первый детектор представляет собой распознающий агент, способный специфично распознавать аналит и называемый ниже "определитель". Второй детектор представляет собой метку и называется ниже "маркер". Следует заметить, что, в зависимости от выборного способа воплощения, некоторые детекторы могут находиться на мембране (3) или на мембране (5). В зависимости от определяемого аналита и применяемых детекторов, может оказаться необходимым добавить один или более детектор перед стадией контактирования молочного продукта с анализатором по изобретению и выдерживать эту смесь в условиях термостатирования, при которых возможно образование комплекса между детекторами и аналитом или аналогом аналита. В зависимости от выбранного способа определитель и маркер могут связываться друг с другом или быть отдельным веществом. С другой стороны, может быть ряд определителей и/или маркеров.
Определитель позволяет обнаруживать наличие искомого типа аналита за счет его способности распознавать специфично этот аналит или его аналог. Это может быть рецептор, способный образовывать селективно устойчивый и практически необратимый комплекс с аналитом или его аналогом, или моноклональное или поликлональное антитело, характеристичное по отношению к аналиту или к аналогу аналита. Для обнаружения антибиотиков определитель можно выбирать из специфичных поликлональных или моноклональных антител или из рецепторов, полученных из микроорганизмов, чувствительных к антибиотикам, таких как рецепторы, полученные из вида Bacillus (Bacillus stearothermophilus, Bacillus subtilis, Bacillus licheniformis и т.д.), или вида Actinomycetes (Actinomadura R39 и т.д.).
Согласно предпочтительному способу воплощения данного изобретения применяется определитель, который содержит рецептор, чувствительный к антибиотикам с β-лактамовым циклом, таковой рецептор получают из Bacillus licheniformis, например, рецептор BlaR или рецептор BlaR-CTD. Выделение и аминокислотная последовательность белка BlaR описаны в Y. Zhu et al., J.Bacteriol, 1137-1141 (1990); рецептор BlaR-CTD представляет собой карбокситерминальный участок BlaR, выделение и аминокислотная последовательность которого описаны в В. Joris et al., FEMS Microbiology Letters, 107-114 (1990).
Применение рецепторов BlaR или BlaR-CTD по данному изобретению для обнаружения антибиотиков с циклом β-лактама имеет значительные преимущества перед применявшимися до сих пор распознающими агентами. Действительно, рецепторы BlaR и BlaR-CTD способны очень быстро образовывать комплексы с большим количеством антибиотиков и делать это при температуре термостатирования более низкой, чем требуемая для известных распознающих агентов, таких, например, как рецепторы, полученные из Bacillus stearothermophilus.
Второй вид применяемого детектора представляет собой маркер, который делает возможной визуализацию и прямое или косвенное определение аналитов в молочном продукте. Маркеры, которые можно использовать по изобретению, могут быть корпускулярными, флуоресцентными, радиоактивными, люминесцентными или ферментативными. Предпочтительно выбирать такой корпускулярный маркер (частицу), который дает легко обнаруживаемый визуальный сигнал, даже присутствуя в малых количествах. В качестве не ограничивающих примеров можно упомянуть коллоидные частицы металлов (платины, золота, серебра и т.д.), коллоидные частицы селена, углерода, серы, теллура, а также окрашенные синтетические коллоидные частицы латекса. Коллоидные частицы золота с диаметром 1-60 нм особенно предпочтительны; они дают четко видимое интенсивное розово-красное окрашивание.
Маркер дает возможность определять присутствие аналита в образце молочного продукта за счет его связывания с одним или более детекторов, с аналитом или с аналогом аналита.
Связывание маркера с детектором можно осуществлять известными специалистам методами. Когда применяется корпускулярный маркер, метку можно ввести либо непосредственной адсорбцией на частицах либо опосредованно, с помощью химического прикрепляющего агента ("якоря"), такого, например, как комплекс биотин/антибиотин. Это связывание может осуществляться либо до стадии контактирования молочного продукта с анализатором по изобретению, либо во время миграции молочного продукта через анализатор по изобретению.
По одному конкретному варианту изобретения применяют третий тип детектора, называемый далее в описании "эталон". Он представляет собой вещество, известное количество которого добавляют к анализируемому образцу, и которое фиксируется специфичным захватывающим веществом, иммобилизованном на мембране (3). Эталон дает полосу, интенсивность которой служит стандартом при количественном определении аналита.
Что касается контактирования молочного продукта с анализатором по изобретению (стадия а) способа), его осуществляют, помещая анализатор по данному изобретению в сосуд, на дне которого находится анализируемый образец. Анализатор помещают практически вертикально в сосуде, так что первый конец устройства соприкасается со смесью.
В варианте изобретения, где анализатор помещен в пластиковый корпус (коробку), коробку ставят горизонтально, и контактирование осуществляется за счет того, что аликвоту образца для анализа помещают в отверстие (щель) в форме плоской чаши, расположенной над мембраной (2).
Что касается стадии миграции б), то жидкость оставляют мигрировать за счет капиллярности через анализатор по изобретению. Жидкость, которая мигрирует за счет капиллярных сил через анализатор по изобретению, сначала встречает мембрану (2), которая позволяет задерживать вещества в молочном продукте, которые предотвращают миграцию аналитов, возможно, присутствующих в молочном продукте, и детекторов через анализатор. Затем аналиты и детекторы мигрируют через мембрану (3), на которой иммобилизовано одно или более захватывающих веществ. Захватывающие вещества селективно иммобилизуют, по меньшей мере, один из компонентов, присутствующих в анализируемой жидкости. Согласно одному конкретному варианту изобретения применяют захватывающее вещество, расположенное на конце миграционного пути жидкости через мембрану (3) и способное фиксировать все маркеры, которые не были задержаны предыдущими захватывающими веществами. Это захватывающее вещество позволяет исчерпывающе дополнить количественную информацию, полученную благодаря предыдущим захватывающим веществам.
Определение фиксации на мембране (3) (стадия с) способа) осуществляется просто определением наличия маркеров в этой зоне. Такое определение возможно простым способом, визуально. Однако, если требуется точное измерение интенсивности наблюдаемых сигналов, можно применять инструмент, способный измерять интенсивность наблюдаемого сигнала. Когда применяется эталон, он фиксируется с помощью специфичного захватывающего вещества, образуя внутренний эталон для измерения интенсивности наблюдаемых сигналов.
Интерпретация полученного результата зависит от применяемого способа определения, а именно, от используемых детекторов и захватывающих веществ.
По сравнению со способами обнаружения аналитов в молоке, описанными ранее в литературе. Способ по данному изобретению имеет следующие преимущества. Во-первых, этот способ очень быстрый и чрезвычайно прост в исполнении: он включает практически две простых операции, не требующих специального экспериментального ноу-хау. Далее, качественная и количественная оценка результата дается немедленно и не требует специальных дополнительных операций, таких, например, которые требуются, когда определение проводят с помощью маркеров красителей и/или ферментов. Кроме того, данный способ можно непосредственно применять для обнаружения различных типов аналитов. Наконец, в варианте воплощения способа с использованием эталона результат может быть прямо рассчитан и интерпретирован, и нет необходимости проводить один или более сравнительных анализов.
Данное изобретение также представляет аналитический набор для обнаружения аналитов в молочном продукте, содержащий анализатор по данному изобретению. Если нужно, аналитический набор по данному изобретению может также включать детекторы для добавления в образец перед тем, как молочный продукт соприкоснется с анализатором.
Примеры, представленные ниже, иллюстрируют различные аспекты и формы воплощения способа по данному изобретению, не ограничивая, однако, его объем.
Пример 1. Изготовление анализаторов. Общие операции.
1.1. Сборка мембранных панелей
Сначала собирают панели размером 300•76,2 мм с применением ламинатора типа Clamshell laminator (фирмы BioDot, Inc.) следующим способом:
Вырезают пластиковый прямоугольник для подложки (основания) типа ArCare 8565 (фирмы Adhesive Research) с размерами 300•76,2 мм (твердая подложка (1)). Затем вырезают прямоугольник из мембраны Leukosorb LK4 (фирмы Pall Gelman Sciences), отмеряя 300•20 мм (мембрана (2)), прямоугольник 300•25 мм из мембраны Hi-Flow SX (выпускаемой Millipore) (мембрана (3)), прямоугольник 300•40 мм из 3 мм-вой целлюлозной мембраны (выпускаемой Whatman) (мембрана (4)) и прямоугольник 300•0,8 мм из мембраны Accuwick (выпускаемой Pall Gelman Sciences) (мембрана (5)).
Мембраны (2) и (4), затем (5), затем (3) последовательно укладывают в специальное место нижней полуформы ламинатора. Твердую подложку (1), покрытую адгезивом, в свою очередь, помещают на верх аппарата, адгезивом наружу. Мембраны, расположенные в нижней полуформе, контактируют с клейкой подложкой, когда ламинатор закрывают; мембраны удерживаются точно на месте за счет того, что вакуумный насос откачивает воздух. Когда вакуум убирают, получают панель, состоящую из твердой подложки (1) с закрепленными на ней мембранами (2), (3), (4) и (5).
1.2. Нанесение захватывающих веществ на мембрану (3)
Нанесение захватывающих веществ на мембрану (3) осуществляют до или после сборки в соответствии с Примером 1.1.
Готовят водный раствор, содержащий захватывающие вещества. Его наносят на мембрану (3) мембранной платы, изготовленной в Примере 1.1, с помощью аппарата BioJet X-Y Platform Quanti-300 фирмы Bio-Dot, Inc.
Нанесенные растворы мгновенно упариваются, когда панель (пластину) целиком помещают на одну минуту в ток горячего (60o) воздуха в импульсном режиме.
1.3. Нанесение меток на мембрану (5)
а) Перед сборкой в соответствии с Примером 1.1.
Готовят водный раствор, содержащий вещество для метки. Погружают в этот раствор мембрану (5). Затем дают раствору стечь и сушат мембрану в течение ночи при комнатной температуре в вакууме 0,5 бар.
б) После сборки в соответствии с Примером 1.1.
Осуществляют операцию, описанную в Примере 1.2 для нанесения захватывающих веществ.
1.4. Покрытие клейкой полимерной пленкой (6)
Вырезают прямоугольник из клейкой пленки типа ArCare 7759 (выпускаемой Adhesive Research) размером 300•20 мм для частичного покрытия и 300•71,2 мм для покрытия всех мембран.
Панель, полученную согласно Примеру 1.1, помещают в нижнюю полуформу ламинатора, а клейкую пленку - на верх ламинатора адгезивом наружу. Клейкая полимерная пленка соприкасается с мембранной панелью, когда аппарат закрывают.
1.5. Разрезание на полосы
Панели (пластины), полученные после сборки, разрезают на полосы с помощью устройства гильотинного типа или с помощью ротационной установки (выпускаемой BioDot, Kinematic or Akzo). Полосы с краев отбрасывают, остальные полосы готовы к использованию.
Чтобы сохранить их, аналитические устройства (анализаторы) помещают в светонепроницаемый, герметически закрытый контейнер в присутствии осушителя (Silgelac, Франция).
1.6. Изготовление в пластиковом корпусе
Анализатор помещают в пластиковый корпус с двумя отверстиями: первое, в виде углубления (плоская чаша) расположено над мембраной (2) и позволяет принимать анализируемую жидкость; второе представляет собой окно, позволяющее визуализацию мембраны (3).
Пример 2. Обнаружение антибиотиков, содержащих (в молекуле) β-лактамный цикл, в молоке с применением фермента R39.
2.1. Определитель
Определитель, применяемый в этом примере, представляет собой растворимую внеклеточную D-аланин-D-аланинкарбоксипептидазу, продуцируемую Actinomadura R39, получаемую по методике, описанной J.-M. Frere et al., Antimicrobial Agents and Chemotherapy, 18(4), 506-510 (1980).
2.2. Связывание определителя с маркером
2.2.1. Биотинилирование определителя
Проводят диализ 250 мкл водного раствора фермента R39 с концентрацией 1 мг/мл в течение 24 часов против 500 мл буфера HNM (ГЭПЭС (HEPES) 10 мМ, рН 8, NaCl 10 мМ, MgCl 5 мМ). К этому диализованному раствору фермента R39 затем добавляют 2 мл бикарбонатного буфера (0,1 М бикарбоната натрия, рН 9) и 250 мкл раствора N-гидроксисукцинимидного эфира 6-(биотинамидо)-капроновой кислоты с концентрацией 5 мг/мл в ДМФА. Этот раствор осторожно перемешивают с помощью мешалки LABINCO для пробирок с вращающейся осью (выпускаемой VEL, Бельгия) со скоростью 2 оборота/минута в течение 3 часов при комнатной температуре и в темноте. Полученный таким образом раствор подвергают диализу против буфера (ГНМ) HNM (HEPES 100 мМ, рН 8, NaCl 100 мМ, MgCl2 50 мМ) в течение 24 часов. Таким образом получают раствор биотинилированного фермента R39, который разбавляют буфером HNM-BSA (ГНМ-БСА) (HEPES 500 мМ, рН 8, NaCl 500 мМ, MgCl2 250 мМ, BSA 10 мг/мл) до концентрации 100 мкг фермента R39 на мл буфера. Этот раствор хранят при -20oС.
2.2.2. Маркер
Что касается применяемого маркера, он состоит из частиц золота диаметром 40 нм, на которые нанесены антитела козы к биотину в виде суспензий в 2 мМ водном растворе тетрабората с рН 7,2, стабилизированном 0,1% азида натрия (выпускается British Biocell (Ref. GAB40)). Оптическая плотность этих суспензий при 520 нм составляет, примерно, 10 и концентрация белка, примерно, 24 мкг/мл.
2.2.3. Связывание биотинилированного определителя с маркером
Раствор А для быстрого анализа.
Раствор биотинилированного фермента R39, приготовленный в Примере 2.2.1, разводят 25-кратно буфером ГНМ-БСА (HNM-BSA) (HEPES 500 мМ, рН 8, NaCl 500 мМ, MgCl2 250 мМ, BSA 10 мг/мл). При комнатной температуре смешивают 17,5 объемных частей этого разбавленного раствора биотинилированного фермента R39, 9,27 объемных частей суспензии частиц золота в качестве метки для фермента R39 и 6 объемных частей эталонной суспензии частиц золота (см. Пример 2.3).
Раствор Б для чувствительного (точного) анализа
Раствор биотинилированного фермента R39, приготовленный в Примере 2.2.1, разбавляют в 50 раз буфером ГНМ-БСА (HNM-BSA) (HEPES 500 мМ, рН 8, NaCl 500 мМ, MgCl2 250 мМ, BSA 10 мг/мл). При комнатной температуре смешивают 17,5 объемных частей этого разбавленного раствора биотинилированного фермента R39, 9,27 объемных частей суспензии частиц золота в качестве метки для фермента R39 и 6 объемных частей эталонной суспензии частиц золота (см. Пример 2.3).
2.3. Эталон
В качестве эталона берут частицы золота размером 40 нм, на которые нанесены антитела козы к кроличьему иммуноглобулину. Эти частицы выпускает British Biocell (Ref. GAB40) в виде суспензий в 2 мМ водном растворе тетрабората натрия, с рН 7,2, стабилизированной 0,1% азида натрия. Оптическая плотность этой суспензии при 520 нм составляет, примерно 3, а концентрация белка равна, примерно 6 мкг/мл.
2.4. Захватывающие вещества
2.4.1. Первое захватывающее вещество
8 мл раствора, содержащего 213 мг человеческого гамма-глобулина (G4386, Sigma) и 8,6 мг гидрохлорида 2-иминотиолана (Aldrich, 33056-6) в натрий-карбонатном буфере (100 мМ, рН 9) термостатируют при 25oС в течение одного часа.
Дополнительно 20 мл раствора, содержащего 119,8 мг цефалоспорина С и 54 мг сульфосукцинимидил-4-(N-малеимидометил)циклогексан-1-карбоксилата (sSMCC, 22322 Pierce) в натрий-карбонатном буфере (100 мМ, рН 9) термостатируют при 25oС в течение одного часа.
Затем смешивают два приготовленных выше раствора. рН полученного раствора доводят до 7,1, добавляя 3 мл NaH2PO4 500 мМ, и раствор термостатируют при 25oС в течение двух часов. Смесь, полученную после термостатирования, трижды подвергают диализу против 1 литра натрий-фосфатного буфера (10 мМ, рН 7,5). Полученный раствор фильтруют через фильтр 0,22 мкм, затем делят на аликвоты и замораживают при -20oС до использования.
Когда надо использовать, аликвоты размораживают и добавляют к ним пищевой краситель перед нанесением на мембрану для того, чтобы в любой момент указать точное положение осадка и характер траектории.
Первое захватывающее вещество позволяет фиксировать определители, связанные в избытке по сравнению с количеством антибиотика в образце.
2.4.2. Второе захватывающее вещество
В качестве второго захватывающего вещества применяют буфер раствора кроличьего иммуноглобулина (Sigma I 5006) с концентрацией иммуноглобулина 0,5 мг/мл в буфере 10 мМ фосфата натрия, рН 7,5, содержащем человеческий гамма-глобулин 5 мг/мл. Это второе захватывающее вещество задерживает эталон, когда жидкость мигрирует через анализатор (аналитическое устройство).
2.5. Аналитическое устройство
Применяются аналитические устройства, содержащие мембраны (2), (3) и (4), собранные в соответствии с описанием в Примере 1.1. На проксимальной стороне мембраны (3) этих устройств находится захватывающее вещество, описанное в Примере 2.4.1, а на дальней (дистальной) стороне находится захватывающее вещество, описанное в Примере 2.4.2. Захватывающие вещества были нанесены в соответствии с процедурой, описанной в Примере 1.2.
2.5.1. Тест 1 - быстрый тест
Готовят семь проб молока, содержащего 0; 2; 4; 5; 6; 8 и 10 г/млрд., соответственно, пенициллина G. Каждый из этих растворов затем анализируют следующим образом.
Берут аликвоту 200 мкл пробы молока и 32,8 мкл раствора А, приготовленного как в Примере 2.2.3, и помещают в пробирку Эппендорфа. Эту смесь термостатируют при 47oС в течение 3 минут. Затем аналитическое устройство (анализатор) ставят вертикально в пробирку Эппендорфа так, что первый конец анализатора соприкасается со смесью. Смесь оставляют мигрировать через анализатор, тогда как установку термостатируют при 47oС в течение 2 минут.
Ниже в таблице А даны результаты, полученные для 7 опытных образцов (проб). Величина интенсивности в интервале от 0 до 10 относится к определяемой (детектируемой) полосе, при этом 10 относится к наиболее интенсивной полосе, а 0 к наименее интенсивной полосе. По этой шкале значение 6 относится к полосе сравнения (эталонной). Интенсивность сигнала, наблюдаемого в первой определяемой полосе, обратно пропорциональна количеству пенициллина G в образце.
В этом примере тест считается положительным, если интенсивность первой полосы ниже интенсивности эталонной полосы. Результаты, приведенные в таблице 1, указывают, что этот тест позволяет обнаруживать за 5 минут до 4 г/млрд. пенициллина G в пробе молока.
2.5.2. Тест 2 - чувствительный тест
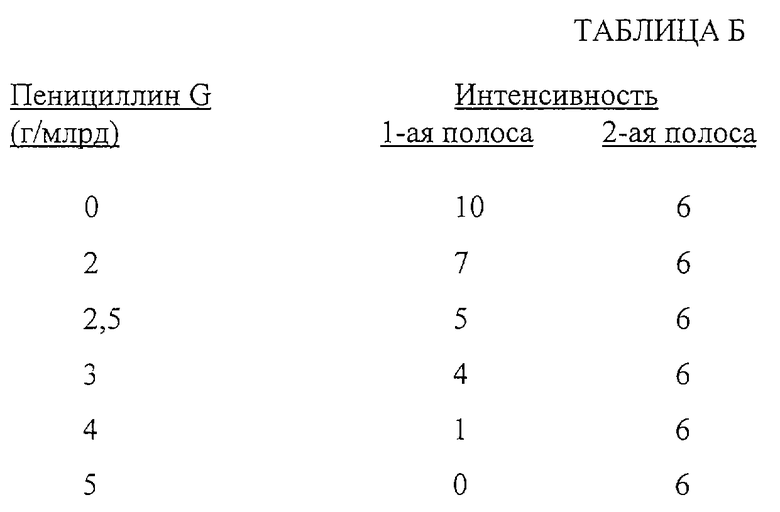
Готовят шесть проб молока, с содержанием пенициллина G 0; 2; 2,5; 3; 4 и 5 г/млрд. , соответственно. Каждый из этих растворов затем анализируют следующим образом.
Берут аликвоту 200 мкл пробы молока и 32,8 мкл раствора Б, приготовленного как в Примере 2.2.3, и помещают в пробирку Эппендорфа. Эту смесь термостатируют при 47oС в течение 5 минут. Затем аналитическое устройство помещают в пробирку Эппендорфа так, чтобы его первый конец соприкасался со смесью. Смесь оставляют мигрировать через анализатор, пока вся установка термостатируется при 47oС в течение 2 минут.
Ниже в таблице Б приведены результаты, полученные для 7 опытных образцов (проб). Значения интенсивности от 0 до 10 относятся к определяемой полосе, при этом 10 относится к наиболее интенсивной полосе, а 0 к наименее интенсивной полосе. По этой шкале значение 6 относится к полосе сравнения (эталонной). Интенсивность сигнала первой определяемой полосы обратно пропорциональна количеству пенициллина G в молоке.
В этом примере тест считается положительным, если интенсивность первой полосы ниже, чем полосы сравнения (эталона). Результаты, приведенные в таблице 2, показывают, что этот тест позволяет за 7 минут обнаруживать до 2,5 г/млрд. пенициллина G в пробе молока.
Пример 3. Определение в молоке антибиотиков с β-лактамным циклом с применением BlaR.
В этом примере показано обнаружение в молоке антибиотиков с циклом β-лактама, контроль которых проводят органы здравоохранения. Тест, описанный в этом примере, использует рецептор BlaR-CTD, связанный с золотыми гранулами, являющимися меткой, и подложку, которая в случае аналитического устройства представляет собой твердую основу (опору), на которой фиксируются мембраны.
3.1 Связывание BlaR-CTD (определитель) с золотыми гранулами (маркер)
3.1.1. Биотинилирование BlaR-CTD
3,79 мл раствора распознающего агента BlaR-CTD с концентрацией 6,6 мг/мл вводят в натрий-фосфатный буфер, 20 мМ, рН 7. Затем к этому раствору BlaR-CTD добавляют 41,71 мл бикарбонатного буфера (0,1 М бикарбоната натрия, рН 9) и 2 мл раствора эфира 6-(биотинамидо)-капроновой кислоты и N-гидроксисукцинимида, содержащий 2,23 мг/мл такого же бикарбонатного буфера. Этот раствор осторожно перемешивают на мешалке LABINCO для пробирок на оси вращения (выпускаемой VEL, Бельгия) со скоростью 2 оборота в минуту в течение 2 часов при комнатной температуре в темноте. 2,5 мл раствора буфера Tris, 1 М рН 8 термостатируют с реакционной смесью в тех же условиях в течение 30 минут. Полученный таким образом раствор подвергают диализу против буфера HNM (HEPES 100 мМ, рН 8, NaCl 100 мМ, MgCl2 50 мМ) в течение 24 часов. Таким образом получают биотинилированный раствор BlaR-CTD, который разводят буфером HNM-BSA (HEPES 500 мМ, рН 8, NaCl 500 мМ, MgCl2 250 мМ, BSA 10 мг/мл) до концентрации 250 мкг биотинилированного BlaR-CTD на мл буфера. Этот раствор хранят при -20oС.
3.1.2. Агент, применяемый в качестве метки
В качестве метки используют частицы золота размером 40 нм, на которые нанесены антитела козы к биотину в виде суспензий в 2 мМ-ном водном растворе тетрабората натрия, с рН 7,2, стабилизированном 0,1% азида натрия (выпускается British Biocell (Ref. GAB40). Оптическая плотность этих суспензий при 520 нм составляет, примерно 10, а концентрация белка равна, примерно 24 мкг/мл.
3.1.3. Связывание биотинилированного BlaR-CTD с золотыми гранулами
Раствор биотинилированного BlaR-CTD, приготовленный в Примере 3.1.1, разбавляют в 114,7 раз буфером HNM-BSA (HEPES 500 мМ, рН 8, NaCl 500 мМ, MgCl2 250 мМ, BSA 10 мг/мл). При комнатной температуре смешивают 22,5 объемных частей этого разбавленного биотинилированного раствора BlaR-CTD, 7,5 объемных частей буфера HNM-BSA, 9,27 объемных частей суспензии частиц, применяемой в качестве метки для биотинилированного BlaR-CTD, и 6 объемных частей эталонной суспензии частиц золота (см. ниже. Пример 3.1.4).
3.1.4. Независимый эталон (стандарт)
В этом тесте применяется эталонное вещество (вещество сравнения), дающее полосу, интенсивность которой позволяет быстро количественно определять антибиотик в образце.
Для этой цели применяют частицы (гранулы) золота размером 40 нм, на которые нанесены антитела козы к кроличьему иммуноглобулину. Эти частицы выпускает British Biocell (Ref. GAB40) в виде суспензий в 2 мМ-ном водном растворе тетрабората натрия с рН 7,2, стабилизированном 0,1% азида натрия. Оптическая плотность этих суспензий при 520 нм составляет, примерно 3, а концентрация белка около 6 мкг/мл.
3.2. Захватывающие вещества
3.2.1. Первое захватывающее вещество - антибиотик сравнения (эталонный)
8 мл раствора, содержащего 213 мг человеческого гамма-глобулина (G4386, Sigma) и 8,6 мг гидрохлорида 2-иминотиолана (Aldrich, 33056-6) в натрий-карбонатном буфере (100 мМ, рН 9) термостатируют при 25oС в течение одного часа.
Отдельно в течение одного часа термостатируют при 25oС 20 мл раствора, содержащего 119,8 мг цефалоспорина С и 54 мг сульфосукцинимидил - 4-(N-малеимидометил)циклогексан-1-карбоксилата (sSMCC, 22322 Pierce) в натрий-карбонатном буфере (100 мМ, рН 9).
Затем смешивают два приготовленных, как указано выше, раствора. рН полученного раствора доводят до 7,1 добавлением 3 мл NaH2PO4 500 мМ, и раствор термостатируют при 25oС в течение двух часов. Смесь, полученную после термостатирования, подвергают трехкратному диализу против 1 литра натрий-фосфатного буфера (10 мМ, рН 7,5). Полученный раствор фильтруют через фильтр 0,22 мкм, затем делят на аликвотные части и замораживают при -20oС до момента использования.
В момент применения аликвоты размораживают и добавляют к ним пищевой краситель перед нанесением на мембрану, чтобы в любой момент указать точное положение осадка и характер траектории.
Первое захватывающее вещество позволяет фиксировать BlaR-CTD, связанный с золотыми гранулами, присутствующими в избытке по сравнению с имеющимся в образце антибиотиком.
3.3.2. Второе захватывающее вещество - вещество, способное фиксировать независимый эталон
В качестве второго захватывающего вещества применяют раствор кроличьего иммуноглобулина (Sigma I 5006) с концентрацией иммуноглобулина 0,5 мг/мл в буфере 10 мМ фосфата натрия, рН 7,5, содержащем человеческий гамма-глобулин 5 мг/мл. Это второе захватывающее вещество задерживает независимый стандарт, когда жидкость мигрирует через аналитическое устройство.
3.3. Аналитическое устройство (анализатор)
Применяются анализаторы, включающие мембраны (2), (3) и (4), собираемые в соответствии с процедурой, описанной в Примере 1.1. На проксимальной стороне мембраны (3) этих устройств нанесено захватывающее вещество, описанное в Примере 3.2.1, а на дистальной (дальней) стороне - захватывающее вещество, описанное в Примере 3.2.2. Захватывающие вещества наносятся в соответствии с описанием в Примере 1.2.
3.4. Определение антибиотиков в молоке
3.4.1. 3-минутный тест - быстрый тест
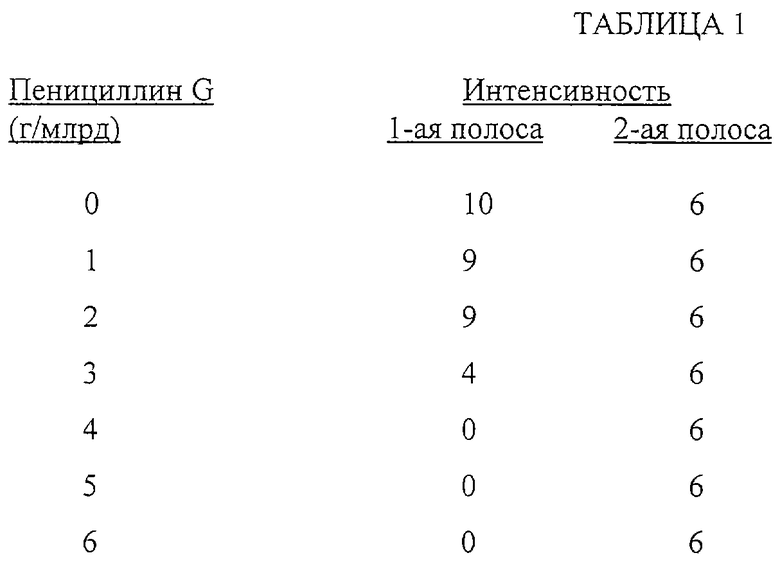
Готовят 7 проб молока, содержащего, соответственно, 0; 1; 2; 3; 4; 5 и 6 г/млрд. пенициллина G. Каждый из этих растворов анализируют следующим образом.
Берут аликвоту 200 мкл пробы молока и 45,27 мкл раствора, приготовленного в Примере 3.1.3, и помещают в стеклянный сосуд. Эту смесь термостатируют при 47oС в течение 1 минуты. Берут аналитическое устройство и ставят вертикально в стеклянный сосуд, так чтобы первый конец его соприкасался со смесью, а второй конец опирался о стенку стеклянного сосуда. Смесь оставляют мигрировать через аналитическое устройство, тогда как весь комплект термостатируют при 47oС в течение 2 минут.
Ниже в таблице 1 приведены результаты, полученные для 7 опытных образцов. Значение интенсивности от 0 до 10 относится к определяемым полосам, причем 10 относится к наиболее интенсивной полосе, а 0 к наименее интенсивной полосе. По этой шкале значение 6 относится к полосе сравнения (эталон). Интенсивность сигнала, наблюдаемого для первой определяемой полосы, обратно пропорциональна количеству пенициллина G в образце.
В этом примере тест считается положительным, если интенсивность первой полосы ниже таковой второй полосы. Результаты, приведенные в таблице 1, показывают, что этот тест позволяет обнаруживать за 3 минуты менее 4-х г/млрд. пенициллина G в пробе молока.
Проводились анализы других антибиотиков с циклом β-лактама в тех же условиях. Этот тест, осуществляемый за 3 минуты, позволяет обнаруживать в пробе молока амоксициллин вплоть до 5 г/млрд. , ампициллин вплоть до 5 г/млрд. , клоксациллин при содержании менее 10 г/млрд., диклоксациллин с концентрацией менее 20 г/млрд., оксациллин с концентрацией менее 20 г/млрд. и цефапирин с концентрацией до 20 г/млрд.
3.4.2. Пятиминутный тест
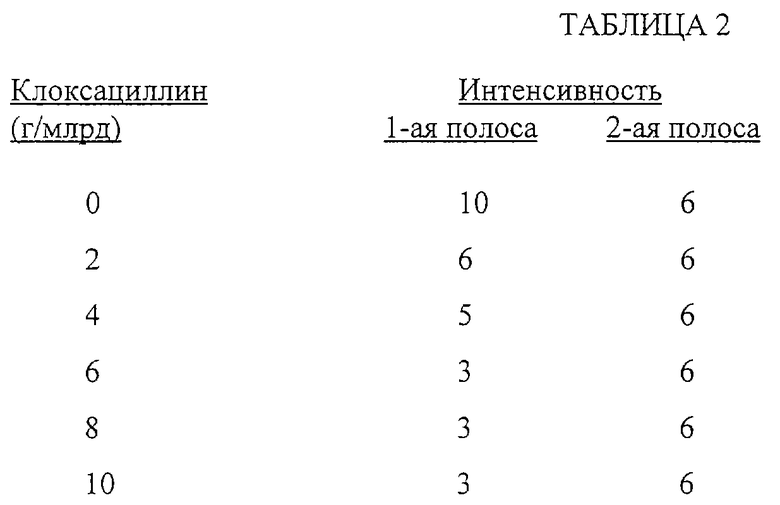
Готовят шесть проб свежего молока с содержанием, соответственно, 0; 2; 4; 6; 8 и 10 г/млрд., клоксациллина. Каждый из этих растворов затем анализируют следующим образом.
Берут аликвоту 200 мкл пробы молока и 45,27 мкл раствора, приготовленного, как в Примере 3.1.3, и помещают в стеклянный сосуд. Эту смесь термостатируют при 47oС в течение 3 минут. Берут аналитическое устройство и ставят вертикально в стеклянный сосуд, так чтобы первый конец аналитического устройства соприкасался со смесью, а второй конец опирался о стенку стеклянного сосуда. Смесь оставляют мигрировать через аналитическое устройство, пока весь комплект термостатируют при 47oС в течение 2 минут.
Ниже в таблице 2 приводятся результаты, полученные для 6 опытных образцов. Величина интенсивности от 0 до 10 относится к определяемым полосам, причем 10 относится к наиболее интенсивной полосе, а 0 к наименее интенсивной полосе. По этой шкале значение 6 относится к полосе сравнения (эталонной). Интенсивность сигнала, наблюдаемого в случае первой полосы, обратно пропорциональна количеству клоксациллина в образце.
В этом примере тест считается положительным, если интенсивность первой полосы ниже таковой второй полосы. Результаты, приведенные в таблице 2, показывают, что этот тест позволяет обнаруживать за 5 минут менее 4 г/млрд. клоксациллина в молоке.
Проведены были также испытания других содержащих β-лактамный цикл антибиотиков в тех же условиях. Этот тест, длящийся 5 минут, позволяет определять в пробе молока пенициллин G с содержанием до 3 г/млрд., амоксициллин с содержанием до 4 г/млрд., ампициллин с концентрацией до 4 г/млрд., диклоксациллин с концентрацией до 8 г/млрд. , оксациллин с концентрацией до 8 г/млрд., цефапирин с концентрацией до 16 г/млрд., цефтилфур с содержанием до 100 г/млрд., цефхинон с концентрацией ниже 20 г/млрд. и цефазолин с концентрацией до 60 г/млрд.
Этот тест особенно пригоден при сортировке перед перевозкой молоковозами их содержимого на хранение.
3.4.3. 9-минутный тест
Готовят шесть проб свежего молока, содержащего, соответственно 0; 4; 6; 8; 10 и 12 г/млрд. цефапирина. Каждый из этих растворов затем анализируют следующим образом. Берут аликвоту 200 мкл пробы молока и 45,27 мкл раствора, приготовленного в Примере 3.1.3, и помещают в стеклянный сосуд. Эту смесь термостатируют при 47oС в течение 7 минут. Берут аналитическое устройство и ставят вертикально в стеклянный сосуд, так чтобы его первый конец соприкасался со смесью, а второй конец опирался о стенку стеклянного сосуда. Смесь оставляют мигрировать через аналитическое устройство, пока весь комплект термостатируется при 47oС в течение 2 минут.
Ниже в таблице 3 приводятся результаты, полученные для 6 опытных образцов. Значение интенсивности от 0 до 10 относится к определяемой полосе, при этом 10 относится к наиболее интенсивной полосе, а 0 относится к наименее интенсивной полосе. По этой шкале значение 6 относится к полосе сравнения (эталона). Интенсивность сигнала, наблюдаемого в первой полосе, обратно пропорциональна количеству цефапирина в образце.
В этом примере тест считается положительным, если интенсивность первой полосы ниже таковой второй полосы. Приведенные в таблице 3 результаты показывают, что этот тест позволяет определять за 9 минут до 6 г/млрд. цефапирина в пробе молока.
Также были проведены анализы других антибиотиков с β-лактамным циклом в тех же условиях. Этот тест, осуществляемый 9 минут, позволяет обнаруживать в пробе молока пенициллин G до 3 г/млрд., амоксициллин до 4 г/млрд., ампициллин до 4 г/млрд., клоксациллин до 4 г/млрд., диклоксациллин до 8 г/млрд., оксациллин до 8 г/млрд., цефтиофур до 80 г/млрд., цефхинон менее 20 г/млрд., нафциллин до 20 г/млрд. и цефазолин до 45 г/млрд.
Этот тест, следовательно, проводящийся в течение 9 минут позволяет обнаруживать все антибиотики, в настоящее время контролируемые европейскими властями и делать это вплоть до законных предельных концентраций, установленных властями.
3.4.4. 20-минутный тест
Готовят шесть проб свежего молока с содержанием, соответственно 0; 20; 30; 40; 50 и 60 г/млрд. цефтиофура. Каждый из этих растворов затем анализируют следующим образом.
Берут аликвоту 200 мкл пробы молока и 45,27 мкл раствора, приготовленного в Примере 3.1.3, и помещают в стеклянный сосуд. Эту смесь термостатируют при 47oС в течение 18 минут. Аналитическое устройство ставят вертикально в стеклянный сосуд, так чтобы первый конец анализатора соприкасался со смесью, а второй конец опирался о стенку стеклянного сосуда. Смесь оставляют мигрировать через аналитическое устройство, пока весь комплект термостатируется при 47oС в течение 2 минут.
Ниже в таблице 4 приводятся результаты, полученные для 6 опытных образцов. Значение интенсивности от 0 до 10 относится к определяемой полосе, при этом 10 относится к наиболее интенсивной полосе, а 0 к наименее интенсивной полосе. По этой шкале значение 6 относится к полосе сравнения (эталону). Интенсивность сигнала, наблюдаемого для первой определяемой полосы, обратно пропорциональна количеству цефтиофура в образце.
В этом примере тест считается положительным, если интенсивность первой полосы ниже, чем таковая второй полосы. Приведенные в таблице 4 результаты показывают, что этот тест позволяет обнаруживать за 20 минут до 30 г/млрд. цефтиофура в молоке.
Следовательно, этот 20-минутный тест позволяет обнаруживать с помощью единственного теста все антибиотики, мониторинг которых в настоящее время проводят европейские и американские власти, причем делать это вплоть до законных предельных концентраций, установленных этими властями.
Пример 4. Применение аналитического устройства в пластиковом корпусе.
Применяется аналитическое устройство, описанное в Примере 1.6. В этом случае контактирование образца (пробы) с аналитическим устройством осуществляют, помещая термостатированную смесь в отверстие в форме резервуара (углубления), предназначенного для этой цели.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ОПРЕДЕЛЕНИЯ АНТИБИОТИКОВ, СОДЕРЖАЩИХ β-ЛАКТАМНЫЙ ЦИКЛ, В ЖИДКОСТИ БИОЛОГИЧЕСКОГО ПРОИСХОЖДЕНИЯ И АНАЛИТИЧЕСКИЙ НАБОР ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ | 1999 |
|
RU2213973C2 |
| СПОСОБ ИММУНОХРОМАТОГРАФИЧЕСКОГО АНАЛИЗА ДЛЯ ДЕТЕКТИРОВАНИЯ АНАЛИТОВ В ОБРАЗЦЕ | 2010 |
|
RU2420740C1 |
| СПОСОБ ИММУНОХРОМАТОГРАФИЧЕСКОГО ОПРЕДЕЛЕНИЯ АНТИБИОТИКОВ В МОЛОКЕ И МОЛОЧНЫХ ПРОДУКТАХ | 2009 |
|
RU2406090C2 |
| Способ цветометрического и тест-определения тетрациклина и доксициклина в молоке и молочных продуктах | 2016 |
|
RU2673822C2 |
| СПОСОБ СОРБЦИОННО-ХРОМАТОГРАФИЧЕСКОГО ОПРЕДЕЛЕНИЯ ТЕТРАЦИКЛИНА В МОЛОКЕ И МОЛОЧНЫХ ПРОДУКТАХ | 2013 |
|
RU2566422C2 |
| СРЕДСТВО ДИАГНОСТИКИ ДЛЯ ОБНАРУЖЕНИЯ И/ИЛИ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ АНАЛИТОВ, ПРИСУТСТВУЮЩИХ В ПРОБЕ | 2018 |
|
RU2799444C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ДЛЯ ОПРЕДЕЛЕНИЯ АНАЛИТА В ОБРАЗЦЕ | 2019 |
|
RU2791099C2 |
| СПОСОБ ОПРЕДЕЛЕНИЯ КАЧЕСТВА МОЛОКА И МОЛОЧНЫХ ПРОДУКТОВ | 2007 |
|
RU2361203C1 |
| УДЛИНЕННАЯ МНОГОСЛОЙНАЯ ИНДИКАТОРНАЯ ТЕСТ-ПОЛОСКА ДЛЯ ИЗМЕРЕНИЯ КОНЦЕНТРАЦИИ АНАЛИТА И СПОСОБ ИЗМЕРЕНИЯ КОНЦЕНТРАЦИИ АНАЛИТА | 1997 |
|
RU2198406C2 |
| СПОСОБ ДЕМИНЕРАЛИЗАЦИИ МОЛОЧНЫХ ПРОДУКТОВ И ИХ ПРОИЗВОДНЫХ (ВАРИАНТЫ) | 1997 |
|
RU2192749C2 |





Изобретение относится к аналитическому устройству для определения аналитов в жидком молочном продукте с помощью капиллярной миграции указанного молочного продукта, включающему твердую подложку, имеющую первый и второй конец, на которой укреплены последовательно, начиная с первого конца: мембрана для очистки анализируемой жидкости, мембрана, на которой иммобилизованы одно или несколько захватывающих веществ, и абсорбирующая мембрана. Изобретение также относится к способу обнаружения и количественного определения аналитов в жидком молочном продукте с помощью указанного аналитического устройства и аналитического набора, содержащего указанное аналитическое устройство. Это позволяет получить средства для надежного обнаружения различных видов аналитов. 4 с. и 19 з.п. ф-лы, 6 табл., 3 ил.
| УСТРОЙСТВО для ГРАДУИРОВКИ АКСЕЛЕРОМЕТРОВ В УДАРНОМ РЕЖИМЕ | 0 |
|
SU408222A1 |
| WO 9615453 A, 23.05.1996 | |||
| WO 9610177 A, 04.04.1996. | |||
Авторы
Даты
2003-06-10—Публикация
1998-10-06—Подача