Область техники
Настоящее изобретение относится к средству иммунохроматографической диагностики для соответствующего, одновременного и специфического обнаружения и/или количественного определения множества аналитов, присутствующих в основном в жидкой пробе, содержащему:
- по меньшей мере одну реакционную смесь, содержащую биологические молекулы распознавания и/или конкурирующие лиганды, помеченные по меньшей мере одной молекулой визуализации; и
- по меньшей мере одну систему извлечения в виде твердой подложки, на которой оказываются закрепленными конкурирующие лиганды и/или молекулы распознавания в разных и известных местах извлечения таким образом, чтобы посредством локализации упомянутых мест извлечения на упомянутой подложке идентифицировать упомянутые аналиты, присутствующие в упомянутой пробе.
Технологические предпосылки
В настоящее время все больше проявляется интерес к средствам диагностики, обеспечивающим соответствующее, одновременное и специфическое обнаружение и/или количественное определение присутствующих в пробе аналитов, в частности, в области производства продуктов питания, а также в области медицины.
Действительно, мы постоянно сталкиваемся с новыми проблемами в области здравоохранения, против которых необходимо разрабатывать быстрые и эффективные решения диагностики для обеспечения соответствующего лечения. Например, каждый год в мире около 60 000 интоксикаций человека связаны с токсинами, производимыми водорослями (включая цианотоксины пресной воды), с общей смертностью около 1,5%. Морские токсины (называемые также фикотоксинами) вырабатываются некоторыми видами фитопланктона и могут накапливаться в различных морских организмах, в частности, в рыбе, крабах или в фильтрующих двухстворчатых организмах (моллюсках), таких как мидии, устрицы, морские гребешки и петушки. Если человек потребляет загрязненные моллюски в больших количествах, он может подвергнуться серьезной интоксикации. Следовательно, очень важно располагать быстрыми и эффективными средствами диагностики для обнаружения морских биотоксинов, например, посредством анализа крови или мочи.
Вышеупомянутые средства диагностики можно также использовать для обнаружения и количественного определения вирусов, ответственных за самые разные патологии. Такие средства диагностики позволяют: (1) получить доказательство вирусного происхождения наблюдаемых клинических симптомов и диагностировать соответствующие вирусы (например, гепатитов или герпеса) и отслеживать биологическое развитие инфекции (например, через определение количества вируса в крови: VIH, VHB, VHC); (2) отслеживать биологические развитие инфекции (например, VIH или гепатита В); (3) принимать терапевтическое решение и судить об эффективности антивирусного лечения (например, при лечении цитомегаловирусной инфекции при помощи ганцикловира); (4) предупреждать передачу вирусных инфекций при переливании крови или пересадке органов и тканей; (5) оценивать иммунологическое состояние (например, в случаях краснухи); (6) исследовать сывороточные маркеры в популяции (например, при оценке общей заболеваемости или при эпидемиологических исследованиях). Как правило, медицинская диагностика должна охватывать максимальный объем отслеживаемых параметров, чтобы назначить оптимальное лечение и тип ухода для пациента, что ограничивает, в частности, часто неизученные побочные явления.
Кроме того, в области производства продуктов питания и, в частности, в молочной промышленности мониторинг и контроль продуктов требуют осуществления тестов как можно раньше на стадии их производства. В идеале эти тесты необходимо проводить на месте производства сырья или на месте его переработки. Эти тесты мониторинга, называемые также «скрининговыми тестами», предусмотрены для обнаружения присутствия и определения количества некоторых аналитов, в том числе химических контаминантов (например, остатки антибиотиков или токсины), протеинов (например, аллергены) или патогенов (например, вирусы, паразиты или бактерии). Возрастающее число санитарных норм и стремление к лучшему мониторингу продуктов питания требуют увеличения числа тестируемых аналитов, а также как можно более точного знания их классов (идентификация семейств, классов или отдельного соединения) и их количеств по отношению к максимально допустимым пределам в каждой матрице. Кроме того, поскольку молоко поступает из самых разных мест в мире, представляется трудным точно определить контаминанты, которые можно найти в молоке, в зависимости от места производства, настолько практические процессы различаются от одного места планеты к другому. Действительно, происхождение пищевых продуктов, а также соответствующие локальные практические методы производства не всегда известны, что вынуждает производить отслеживание соединений в широком и как можно более широком спектре, охватывающем все, что может находиться в анализируемой пробе.
В частности, агропромышленной сектор заинтересован в средстве диагностики, позволяющем предусмотреть в ходе одной операции анализ соединений, принадлежащих к разным классам, которые могут иметь в корне различающиеся физико-химические свойства, внутри одного семейства аналитов или нет, и присутствующих одновременно в данной пробе. Например, тип и число антибиотиков, которые можно вводить животным, могут варьировать в зависимости от того, идет ли речь о терапевтическом или профилактическом применении, в зависимости от вида животного, от микроба, с которым необходимо бороться, от ветеринарных практик, от действующего законодательства, от имеющихся в наличии средств или от географических регионов. В случае некоторых специальных видов лечения можно использовать смесь медикаментов. Как правило, врач использует антибиотики отдельно или в комбинации среди имеющихся в продаже в зависимости от его оценки наилучшей эффективности.
Основным классами антибактериальных и антибиотических средств являются: пенициллины, цефалоспорины, тетрациклины, сульфамиды, аминогликозиды и аминоциклитолы, макролиды, хлорамфениколы или другие пептиды, ионофоры, нитрофураны, хинолоны, карбадоксы и т.д., причем каждый из этих классов объединяет очень широкую совокупность химически различающихся соединений.
Присутствие таких молекул в молочных продуктах может иметь определяющее негативное последствие для рентабельности промышленного процесса, предполагающего ферментацию (сыр, йогурт,…) свежего молока.
Кроме того, часто интенсивное использование антибиотиков в ветеринарии и в сельскохозяйственном производстве может стать причиной появления бактериальных штаммов, которые становятся стойкими к антибиотикам. В целях охраны здоровья человека и принятия соответствующих законов многие страны установили максимально допустимые уровни (МДУ) содержания остатков антибиотиков в пищевых продуктах. Эти МДУ фиксируют границу между положительной пробой и отрицательной пробой, то есть между отбракованным образцом и принятым образцом.
Важно, чтобы методы мониторинга с применением средства диагностики: (1) могли охватывать одновременное обнаружение максимума соединений, при этом тесты отслеживания предпочтительно и логически должны быть мультианалитными тестами, (2) позволяли распознавать классы, к которым принадлежат соединения, найденные в положительной пробе, чтобы напрямую приходить к адекватному методу подтверждения, и (3) не могли давать результатов типа «ложного отрицательного», так как они не войдут в анализ и не будут впоследствии подтверждены.
Уровень техники
Средство диагностики, указанное во вступлении, известно. Действительно, в известном документе ЕР1712914 раскрыто средство иммунохроматографической диагностики для соответствующего, одновременного и специфического обнаружения и/или количественного определения множества аналитов, присутствующих в основном в жидкой пробе, содержащее:
- по меньшей мере одну реакционную смесь, содержащую биологические молекулы распознавания и/или конкурирующие лиганды, помеченные по меньшей мере одной молекулой визуализации; и
- по меньшей мере одну систему извлечения в виде твердой подложки, на которой оказываются закрепленными конкурирующие лиганды и/или молекулы распознавания в разных и известных местах извлечения, чтобы посредством локализации упомянутых мест извлечения на упомянутой подложке идентифицировать упомянутые аналиты, присутствующие в упомянутой пробе.
В частности, в этом известном документе предложено средство диагностики, позволяющее обнаруживать одновременно все соединения, которые могут принадлежать по меньшей мере к двум разным классам аналитов, и характеризовать класс, к которому действительно принадлежит обнаруженное соединение, причем с установлением технической и практической совместимости для объединения в один способ по меньшей мере двух механизмов обнаружения, при этом работа одного из них не должна мешать работе другого. Кроме того, средство диагностики согласно документу ЕР1712914 доказывает техническую возможность мультианалитной дозировки, которая может происходить быстро, например, за менее чем 10 минут, и в ходе одного и того же этапа анализа на основании одной исходной пробы.
Практически, способ применения средства диагностики согласно документу ЕР1712914 характеризуется следующими этапами:
- введение в контакт заранее определенной реакционной среды с характеризуемой пробой для получения раствора, который инкубируют при 50°С в течение 3 минут;
- смачивание вышеупомянутой системы извлечения полученным раствором и инкубация в течение 3 минут;
- количественная и качественная интерпретация результата на системе извлечения при помощи считывающего оптического устройства.
Согласно этому известному документу, именно позиционирование элементов извлечения (конкурирующих лигандов) позволяет идентифицировать тип заражения. Например, согласно примеру из документа ЕР1712914, соответствующему одновременной дозировке тетрациклинов, β-лактамов и сульфамидов, каждый элемент извлечения располагают в виде линий захвата, каждую из которых располагают последовательно одна за другой относительно направления миграции жидкости (соответствующей реакционной смеси, введенной в контакт с пробой). Согласно предпочтительному признаку этого средства диагностики, зоны захвата, содержащие элементы извлечения β-лактамов, тетрациклинов и сульфадиметоксинов, располагают соответственно на первом, на втором и на третьем уровнях, если рассматривать направление миграции жидкости.
Интерпретация результатов, полученных при помощи такого средства диагностики, должна происходить в обратном порядке и основана на принципе конкуренции, который использует распознавание искомых соединений по отношению к конкурирующему лиганлу и/или к биологической молекуле распознавания. Можно рассмотреть несколько случаев, когда элементами извлечения, закрепленными на системе извлечения, являются конкурирующие лиганды:
- либо искомое соединение присутствует в пробе и свяжется с биологическими молекулами распознавания, присутствующими в реакционной смеси, которые, следовательно, не смогут больше связываться с конкурирующими молекулами, закрепленными на системе извлечения. В этом случае результат будет положительным и будет иметь отсутствующую метку;
- либо искомое соединение отсутствует в пробе, следовательно, присутствующие в реакционной смеси биологические молекулы распознавания смогут свободно связываться с конкурирующими молекулами, закрепленными на системе извлечения. В этом случае результат будет отрицательным и будет иметь присутствующую метку.
К сожалению, средство диагностики согласно документу ЕР1712914 обеспечивает обнаружение и/или количественное определение только ограниченного числа аналитов, присутствующих в пробе, и, следовательно, не может реально рассматриваться как средство мультианалитной диагностики. В частности, средство диагностики согласно документу ЕР1712914 позволяет обнаруживать соединения, принадлежащие только к трем разным классам антибиотиков, а именно к β-лактамам, тетрациклинам и сульфамидам.
Следовательно, даже если β-лактамы, тетрациклины и сульфамиды действительно образуют классы аналитов, которые можно рассматривать как разные, описанное в этом документе известное средство позволяет обнаруживать только антибиотики. Таким образом, это известное средство диагностики не позволяет обнаруживать и/или количественно определять такие аналиты, как антибактериальные средства, токсины, гормоны, патогены, адюльтеранты или аллергены.
Действительно, в рассматриваемых отраслях, таких как агропромышленной сектор или медицина, существует потребность в наиболее полном анализе, который предпочтительно позволяет идентифицировать максимум соединений. Более практичным и экономичным является осуществление только одного комплексного теста при помощи одной пробы, чем производить отдельный тест для каждого соединения или для небольшой группы соединений, а именно для 2 или 3 соединений максимум, как это происходит со средством диагностики согласно документу ЕР1712914.
Как было указано выше, в этом известном документе представлена система извлечения, имеющая зоны захвата (закрепленные элементы извлечения) в виде линий, расположенных одна за другой и перпендикулярно к направлению миграции жидкости, и техническая несовместимость проявляется, когда специалист в данной области пытается расположить большее число зон захвата одновременно на системе извлечения, по причине (1) ограниченного размера тестовых зон, (2) большего количества реактивов, наносимых на последовательные линии (что способствует фоновому шуму и более значительной перекрестной реактивности), и (3) недостаточной точности во время интерпретации результатов при визуальном или инструментальном анализе, который является длительным и сложным. Это затрудняет и даже делает невозможным разграничение различных зон захвата и, следовательно, не позволяет отличать различные аналиты друг от друга.
В публикации Тарановой (Taranova et al.) сделана попытка устранить недостатки решения по документу ЕР1712914 за счет объединения иммунохроматографии и технологии «микрорешеток». Действительно, чтобы увеличить число аналитов, которые можно обнаружить/количественно определить в ходе одного теста, в документе Тарановой предложено располагать места извлечения на твердой подложке в соответствии с двухмерной матричной компоновкой. Таким образом, твердая подложка средства иммунохроматографической диагностики согласно документу Тарановой имеет микрорешетку, состоящую из 32 антигенов (конкурирующих лигандов), закрепленных в виде точек (мест извлечения). К сожалению, средство диагностики согласно этому известному документу позволяет обнаруживать и количественно определять только четыре аналита, а именно амфетамин, бензоилэкгонин, метамфетамин и морфин, которые считаются наркотиками. Действительно, согласно документу Taranova et al., на твердой подложке предусмотрены восемь мест извлечения в виде точек для обнаружения и количественного определения одного аналита. В частности, для обнаружения и/или количественного определения данного аналита на твердой подложке закрепляют восемь точек, содержащих специфические для этого аналита антигены (конкурирующие лиганды), при этом восемь точек, позволяющих идентифицировать данный аналит, располагают вдоль оси, перпендикулярной к направлению миграции жидкости. Следовательно, согласно этому документу, речь идет не о 32 разных антигенах, которые позволили бы обнаружить 32 разных аналита, закрепленных на твердой подложке, а только о четырех разных антигенах, которые воспроизведены восемь раз и которые являются специфическими для четырех разных аналитов. Таким образом, идентификация аналитов происходит в ходе одной операции, при этом восемь мест извлечения, расположенных вдоль оси, перпендикулярной к направлению миграции жидкости, являются идентичными, то есть содержат антигены, специфические только для одного аналита. Согласно этому известному документу, компоновка мест извлечения в виде точек представляет собой ряды точек, при этом каждый ряд соответствует данному аналиту, а не реальную двухмерную матричную компоновку.
Таким образом, известные средства иммунохроматографической диагностики сталкиваются на этой стадии с серьезным ограничением для эффективности, которое характеризуется отсутствием быстрого и практичного реально мультианалитного теста, обеспечивающего обнаружение и/или количественное определение аналитов, которое является:
- специфическим, то есть позволяющим различать аналиты разных классов, и
- универсальным, то есть применимым для большинства веществ, анализируемых в областях агропромышленного сектора и медицинской диагностики, таких как остатки медикаментов (например, антибиотиков и антибактериальных средств), токсины, гормоны, патогены, адюльтеранты или аллергены.
Задача изобретения
Изобретение призвано преодолеть недостатки известных решений и предложить более быстрое, более практичное, более экономичное и более эффективное средство диагностики, обеспечивающее обнаружение и/или количественное определение аналитов, которое является:
- специфическим, то есть может различать аналиты разных классов, и
- универсальным, то есть применимым для большинства веществ, анализируемых в областях агропромышленного сектора и медицинской диагностики, таких как остатки медикаментов (например, антибиотиков и антибактериальных средств), токсины, гормоны, патогены, адюльтеранты или аллергены,
при этом обнаружение и/или количественное определение происходит в ходе одного этапа и менее чем за 15 минут.
В частности, заявленное средство диагностики позволяет обнаруживать/количественно определять по меньшей мере 5 разных классов аналитов, предпочтительно по меньшей мере 10 разных классов аналитов, предпочтительно по меньшей мере 15 разных классов аналитов, присутствующих в пробе, при этом классами аналитов являются остатки медикаментов (например, антибиотиков или антибактериальных средств), токсины, гормоны, патогены, адюльтеранты или аллергены, причем менее чем за 15 минут и в ходе одного этапа. Чтобы решить эту задачу, согласно изобретению, предусмотрено средство иммунохроматографической диагностики для соответствующего, одновременного и специфического обнаружения и/или количественного определения множества аналитов, присутствующих в основном в жидкой пробе, содержащее:
- по меньшей мере одну реакционную смесь, содержащую биологические молекулы распознавания и/или конкурирующие лиганды, помеченные по меньшей мере одной молекулой визуализации; и
- по меньшей мере одну систему извлечения в виде твердой подложки, на которой закреплены конкурирующие лиганды и/или биологические молекулы распознавания в разных и известных местах извлечения, которые расположены в соответствии с двухмерной матричной компоновкой таким образом, чтобы посредством локализации упомянутых мест извлечения на упомянутой подложке идентифицировать упомянутые аналиты, присутствующие в упомянутой пробе,
при этом упомянутое средство диагностики отличается тем, что:
а) упомянутая двумерная матричная компоновка определена по системе координат, имеющей первую координату Х и вторую координату Y, при этом каждое место извлечения, закрепленное на упомянутой твердой подложке, позволяет идентифицировать отдельный аналит,
b) для обнаружения и/или количественного определения данного аналита присутствует диагностическая пара, состоящая из конкурирующего лиганда и биологической молекулы распознавания, при этом упомянутая биологическая молекула распознавания находится в упомянутой реакционной смеси, и упомянутый конкурирующий лиганд закреплен по меньшей мере в одном месте извлечения или наоборот;
c) упомянутая по меньшей мере одна молекула визуализации является молекулой, обнаруживаемой при флуоресценции; и
d) упомянутая реакционная смесь находится в емкости, при этом упомянутая емкость является отдельной от упомянутой системы извлечения.
Под термином «аналит» в рамках настоящего изобретения следует понимать соединение, которое подлежит обнаружению и/или количественному определению в целях диагностики, в частности, в областях агропромышленного сектора и медицины.
Под терминами «класс аналитов» в рамках настоящего изобретения следует понимать группу из нескольких аналитов, которые имеют сходные биологические и химические свойства. Например, медикаментозные остатки можно разделить на различные классы, такие как пенициллины, цефалоспорины, тетрациклины, сульфамиды, аминогликозиды, аминоциклитолы, макролиды, хинолоны, ионофоры, карбадоксы, нитрофураны и фениколы. В частности, пенициллины являются антибиотиками, имеющие общий принцип действия (биологическое свойство) и имеют сходную химическую структуру (химическое свойство).
Под терминами «соответствующее обнаружение и/или количественное определение» в рамках настоящего изобретения следует понимать обнаружение и/или количественное определение всех представляющих интерес аналитов с использованием только одного заявленного средства диагностики.
Под терминами «одновременное обнаружение и/или количественное определение» в рамках настоящего изобретения следует понимать обнаружение и/или количественное определение всех представляющих интерес аналитов после одинакового промежутка времени.
Под терминами «специфическое обнаружение и/или количественное определение» в рамках настоящего изобретения следует понимать обнаружение и/или количественное определение всех представляющих интерес аналитов отдельно, чтобы можно было точно идентифицировать обнаруженный и/или количественно определенный аналит.
Под терминами «диагностическая пара» в рамках настоящего изобретения следует понимать две взаимодополняющие молекулы, предназначенные для обнаружения и/или количественного определения данного аналита, при этом упомянутые две молекулы являются биологической молекулой распознавания и конкурирующим лигандом. Обнаружение и/или количественное определение данного аналита основано на принципе конкуренции в соответствии с двумя возможными ситуациями:
- либо биологическая молекула распознавания находится в реакционной смеси, и конкурирующий лиганд закреплен на твердой подложке;
- либо конкурирующий лиганд находится в реакционной смеси, и биологическая молекула распознавания закреплена на твердой подложке.
Под терминами «биологические молекулы распознавания» в рамках настоящего изобретения следует понимать природную или синтетическую молекулу, которая может специфически связываться с представляющим интерес аналитом.
Под терминами «конкурирующие лиганды» в рамках настоящего изобретения следует понимать молекулу, которая может специфически связываться с биологическими молекулами распознавания и которая, следовательно, вступает в конкуренцию с рассматриваемым аналитом при связывании с биологическими молекулами распознавания.
Под терминами «место извлечения» в рамках настоящего изобретения следует понимать место, в котором будут закреплены биологические молекулы распознавания или конкурирующие лиганды. В случае, когда в месте извлечения закреплены биологические молекулы распознавания, искомый аналит (если он присутствует) или конкурирующий лиганд (если искомый аналит отсутствует) будет специфически связан, захвачен и, следовательно, перестанет мигрировать. В случае, когда в месте извлечения закреплены конкурирующие лиганды, биологические молекулы искомого аналита будут специфически связаны, извлечены и, следовательно, перестанут мигрировать, причем если представляющий интерес аналит отсутствует.
Способ, применяемый для обнаружения и/или количественного определения, состоит в следующем:
- реакционную смесь вводят в контакт с пробой для получения жидкости;
- производят инкубацию при 30°С в течение 3 минут;
- конец системы извлечения, который находится на входе по направлению миграции, смачивают в жидкости (содержащей пробу и реакционную смесь);
- производят инкубацию в течение 10 минут при 30°С; и
- результат на системе извлечения интерпретируют качественно и/или количественно при помощи считывающего оптического устройства.
Направление миграции жидкости в рамках изобретения определяют в упомянутой системе координат, образующей матричную компоновку мест извлечения, закрепленных на системе извлечения в соответствии с изобретением, и, следовательно, определяют по координате Х и координате Y.
Обнаружение и/или количественное определение в соответствии с изобретением основано на принципе конкуренции, который использует распознавание искомых аналитов по отношению к конкурирующему лиганду и/или к биологической молекуле распознавания.
В зависимости от того, закреплены в местах извлечения конкурирующие лиганды или биологические молекулы распознавания, можно рассмотреть несколько случаев:
1) В случае, когда элементами извлечения являются конкурирующие лиганды,
- либо искомое соединение присутствует в пробе и будет в этом случае связываться с биологическими молекулами распознавания, присутствующими в реакционной смеси, которые, следовательно, не смогут свободно связаться с конкурирующими молекулами, закрепленными на системе извлечения. Результат будет положительным и будет иметь отсутствующую метку;
- либо искомое соединение отсутствует в пробе, и в этом случае присутствующие в реакционной смеси биологические молекулы распознавания могут свободно связаться с конкурирующими молекулами, закрепленными на системе извлечения. Результат будет отрицательным и будет иметь присутствующую метку.
2) В случае, когда элементами извлечения являются биологические молекулы распознавания,
- либо искомое соединение присутствует в пробе и будет в этом случае входить в конкуренцию с присутствующими в реакционной смеси конкурирующими лигандами, чтобы связываться с биологическими молекулами распознавания, закрепленными на системе извлечения. Результат будет положительным и будет иметь отсутствующую или слабую метку;
- либо искомое соединение отсутствует в пробе, и в этом случае с биологическими молекулами распознавания, закрепленными на системе извлечения, могут связаться только конкурирующие лиганды. Результат будет отрицательным и будет иметь присутствующую метку.
В рамках настоящего изобретения неожиданно выяснилось, что заявленное средство иммунохроматографической диагностики, которое имеет вышеупомянутые признаки (а), (b), (c) и (d), является более эффективным и одновременно является специфическим и в то же время универсальным. В частности, оно позволяет обнаруживать и/или количественно определять по меньшей мере 5 разных классов аналитов, предпочтительно по меньшей мере 10 разных классов аналитов и еще предпочтительнее - по меньшей мере 15 разных классов аналитов, присутствующих в пробе, при этом классами аналитов являются медикаментозные остатки (например, антибиотиков или антибактериальных средств), токсины, гормоны, патогены, адюльтеранты или аллергены, причем менее чем за 15 минут и в ходе одного этапа. Следовательно заявленное средство диагностики является более практичным, более экономичным и более эффективным, чем известные в настоящее время средства диагностики, которые ограничены обнаружением и/или количественным определением менее пяти разных классов аналитов.
В частности, неожиданно было установлено, что помещение реакционной смеси в емкость отдельно от твердой подложки обеспечивает несколько преимуществ.
Во-первых, поскольку взаимодействие реакционной смеси с анализируемой пробой сосредоточено в отдельной емкости, контроль взаимодействия реакционной смеси с пробой является оптимизированным. Таким образом, можно с уверенностью сказать, что проба полностью прореагирует с реакционной смесью, прежде чем полученная жидкость (образованная реакционной смесью и пробой) войдет в контакт с твердой подложкой и, следовательно, с местами извлечения. Следовательно, отделение реакционной смеси в отдельной емкости от твердой подложки позволяет избежать получения ложных отрицательных результатов. Действительно, в случае, когда реакционная смесь закреплена на твердой подложке на входе элементов извлечения относительно направления миграции, как в документе Taranova et al., в основном жидкая проба входит в контакт непосредственно с реакционной смесью, закрепленной на твердой подложке, что приведет к немедленной миграции жидкости за счет капиллярности. В этом случае существует повышенный риск встречи пробы с местами извлечения до того, как взаимодействие с реакционной смесью станет полным, что приведет к ошибочному результату, то есть аналит реально присутствует в пробе, но не обнаруживается.
Во-вторых, отделение реакционной смеси в емкости обеспечивает лучший контроль качества анализируемой пробы. Действительно, с применением заявленного средства диагностики можно поместить в емкость определенный и точный объем пробы и убедиться, что весь этот объем пробы будет подвергнут анализу, в отличие от средства диагностики, раскрытого в документе Taranova et al. Действительно, с таким средством диагностики, то есть со средством, в котором реакционная смесь присутствует на твердой подложке на входе элементов извлечения относительно направления миграции жидкости, проба напрямую входит в контакт с твердой подложкой, погруженной в пробу, при этом полученная жидкость (образованная пробой и реакционной смесью) сразу же мигрирует за счет капиллярности. Таким образом, невозможно точно определить объем жидкости, который будет мигрировать на твердой подложке, что значительно затрудняет и даже делает невозможным определение объема пробы, который будет реально проанализирован. Этот отличительный признак заявленного средства диагностики позволяет уменьшить стандартные отклонения и добиться, таким образом, лучшей воспроизводимости по сравнению с известными средствами диагностики. Точное определение объема пробы, который будет проанализирован, позволяет также более адекватно определить состав реакционной смеси и особенно количество различных составляющих ее элементов. Следовательно, обнаружение или количественное определение данного аналита является значительным и надежным даже в одном экземпляре в отличие от документа Taranova et al. Действительно, согласно этому известному документу и как было указано выше, на твердой подложке необходимо предусмотреть восемь мест извлечения для обнаружения и количественного определения одного аналита. Следовательно, для надежного обнаружения и/или количественного определения одного и того же числа аналитов, например, четырех аналитов, твердая подложка в соответствии с изобретением должна содержать 4 места извлечения, тогда как твердая подложка согласно документу Taranova et al. должна содержать 32 места извлечения. Следовательно, при одинаковой площади твердой подложки заявленное средство диагностики позволяет обнаруживать и/или количественно определять 32 разных аналита.
В-третьих, отделение реакционной смеси в емкости позволяет увеличить число компонентов реакционной смеси. Действительно, как было указано выше, для обнаружения и/или количественного определения данного аналита присутствует диагностическая пара, состоящая из конкурирующего лиганда и биологической молекулы распознавания, при этом биологическая молекула распознавания находится в реакционной смеси, а конкурирующий лиганд закреплен по меньшей мере в одном месте извлечения, или наоборот. Таким образом, реакционная смесь содержит одну биологическую молекулу распознавания или один конкурирующий лиганд на каждый аналит. Следовательно, для обнаружения и/или количественного определения большого числа разных аналитов в реакционную смесь необходимо добавить большее число молекул распознавания или разных конкурирующих лигандов. При известном средстве диагностики, раскрытом в документе Taranova et al., число компонентов смеси ограничено имеющейся площадью на твердой подложке.
Кроме того, согласно изобретению, матричная двухмерная компоновка определена в системе координат, имеющей первую координату Х и вторую координату Y, при этом каждое место извлечения, закрепленное на упомянутой твердой подложке, обеспечивает идентификацию отдельного аналита. Этот признак значительно повышает также эффективность заявленного средства диагностики, которое позволяет обнаруживать и/или количественно определять большее число разных аналитов при идентичной площади подложки, например, позволяет повысить эффективность в восемь раз по сравнению со средством диагностики из документа Taranova et al.
Таким образом, согласно изобретению, при одной и той же координате Х несколько мест извлечения, каждое из которых содержит биологические молекулы распознавания или разные конкурирующие лиганды, расположены по разным координатам Y, что позволяет, при одной и той же координате Х, обнаруживать и/или количественно определять несколько разных аналитов. С другой стороны, наоборот, при одной и той же координате Y несколько мест извлечения, каждое из которых содержит биологические молекулы распознавания или разные конкурирующие лиганды, расположены по разным координатам Х, что позволяет обнаруживать и/или количественно определять несколько разных аналитов.
Кроме того, неожиданно было установлено, что использование молекулы визуализации, которую можно обнаружить при флуоресценции, позволяет улучшить предел обнаружения сигнала и, следовательно, уменьшить риск ложных отрицательных результатов за счет повышения чувствительности обнаружения и/или количественного определения. Следовательно, поскольку порог обнаружения является более низким, места извлечения могут быть меньшими, что позволяет выполнить твердую подложку, которая имеет больше мест извлечения при идентичной площади. Кроме того, поскольку обнаружение сигнала при флуоресценции является более чувствительным, в местах извлечения можно закрепить меньшее количество конкурирующих лигандов и/или биологических молекул распознавания, что дает ощутимое экономическое преимущество, а также уменьшает фоновой шум и снижает риск взаимодействий между механизмами обнаружения и/или количественного определения.
В заключение следует сказать, что заявленное средство диагностики дает лучший технический эффект по сравнению с существующими средствами диагностики и, в частности, по сравнению со средством диагностики, раскрытым в документе Taranova et al.
Таким образом, настоящее изобретение доказывает техническую и практическую совместимость для объединения в одном средстве диагностики большого числа (не менее 5, предпочтительно не менее 10 и предпочтительно не менее 15) механизмов обнаружения и/или количественного определения. Кроме того, в рамках настоящего изобретения доказана техническая возможность мультианалитной дозировки, которая может производится быстро, менее чем за 15 минут, предпочтительно за 13 минут, в ходе одного этапа анализа при помощи одной пробы. Действительно, заявленное средство диагностики не требует ни промывки, ни осуществления отдельного этапа маркировки молекул распознавания и/или конкурирующих лигандов, учитывая, что, согласно изобретению, реакционная смесь содержит молекулы распознавания и/или конкурирующие лиганды, связанные по меньшей мере с одной молекулой визуализации. Предпочтительно упомянутые места извлечения, закрепленные на упомянутой системе извлечения упомянутого заявленного средства диагностики, расположены в соответствии с двухмерной матричной компоновкой в виде точек, каждая из которых имеет диаметр, составляющий от 20 мкм до 2 мм, предпочтительно составляющий от 100 мкм до 500 мкм и еще предпочтительнее - от 250 мкм до 400 мкм.
Было доказано, что места извлечения в виде точек, каждая из которых имеет диаметр, составляющий от 20 мкм до 2 мм, предпочтительно составляющий от 100 мкм до 500 мкм и еще предпочтительнее - от 250 мкм до 400 мкм, позволяют закрепить по меньшей мере 5, предпочтительно по меньшей мере 10 и предпочтительно по меньшей мере 15 мест извлечения в одном экземпляре, в двойном экземпляре или в тройном экземпляре, предназначенных для контроля порога обнаружения, позволяющего подтвердить тест, и/или для калибровки с целью обнаружения и/или количественного определения, причем на системе извлечения, имеющей умеренный размер, для реализации обнаружения и/или количественного определения упомянутых 15 аналитов при помощи оптического устройства считывания.
Предпочтительно места извлечения, закрепленные на упомянутой системе извлечения упомянутого заявленного средства диагностики, расположены в соответствии с двухмерной матричной компоновкой в виде точек, при этом упомянутые точки присутствуют с плотностью от 62500 до 6,25 точек на см2, предпочтительно от 2500 до 100 точек на см2, предпочтительно от 400 до 150 точек на см2.
Предпочтительно матричная компоновка всех мест извлечения меньше или равна 3 см2, предпочтительно меньше или равна 2 см2 и предпочтительно меньше или равна 1 см2.
Предпочтительно первая координата Х определена на продольной оси длины упомянутой системы извлечения, и вторая координата Y определена на продольной оси ширины упомянутой системы извлечения.
Следует предусматривать минимальное расстояние промежутка между двумя точками, которое составляет от 20 мкм до 2 мм, предпочтительно от 100 мкм до 500 мкм и предпочтительно от 250мкм до 400 мкм вдоль координат Х и Y.
В частном варианте выполнения упомянутая система извлечения в соответствии с изобретением содержит по меньшей мере 5, предпочтительно по меньшей мере 10, предпочтительно по меньшей мере 15 отдельных мест извлечения, предназначенных для соответствующего, одновременного и специфического обнаружения и/или количественного определения по меньшей мере 5, предпочтительно по меньшей мере 10, предпочтительно по меньшей мере 15 разных аналитов, присутствующих в пробе, и по меньшей мере одно место извлечения, предназначенное для контроля и/или калибровки.
Предпочтительно упомянутый контроль и/или упомянутую калибровку производят при помощи независимой пары конкурирующий лиганд/молекула распознавания, в силу собственной (или синтетической) природы которой молекула контроля никогда не присутствует в пробе (например, специфическое антитело белка другого вида животного, отличного от того, из которого взята проба), или белка-носителя (например, коровьего серум-альбумина), химически модифицированного при помощи синтетического маркера (например, биотина или полигистидинового маркера или маркера c-myc).
В предпочтительном варианте выполнения заявленного средства диагностики, каждое из упомянутых мест извлечения расположено на упомянутой системе извлечения в двойном экземпляре, предпочтительно в тройном экземпляре. Выполнение в виде двойных или тройных экземпляров позволяет улучшить статистику и точность получаемых результатов.
Предпочтительно матричную компоновку мест извлечения, в которых закрепляют конкурирующие лиганды или молекулы распознавания, определяют по направлению миграции жидкости таким образом, чтобы место извлечения, в котором закреплены конкурирующие лиганды или биологические молекулы распознавания, предназначенные для обнаружения и/или количественного определения первого данного аналита, располагалось на входе места извлечения, в котором закреплены конкурирующие лиганды или биологические молекулы распознавания, предназначенные для обнаружения и/или количественного определения второго данного аналита, относительно направления миграции жидкости. Такая матричная компоновка позволяет еще больше снизить риск взаимодействий между различными механизмами обнаружения и/или количественного определения искомых аналитов.
Предпочтительно упомянутая система извлечения в виде твердой подложки содержит мембрану или набор мембран. Предпочтительно мембрана является мембраной из нитроцеллюлозы.
Предпочтительно упомянутая емкость является емкостью из стекла или пластика.
Предпочтительно упомянутые биологические молекулы распознавания являются антителами, предпочтительно первичными антителами, моноклональными или поликлональными, очищенными или не очищенными, и/или аптамерами, и/или GEPIs, и/или биологическими рецепторами.
Предпочтительно упомянутые конкурирующие лиганды являются аналогами искомых аналитов и/или молекулами, способными специфически закреплять упомянутые биологические молекулы распознавания.
В предпочтительном варианте выполнения заявленного средства диагностики упомянутые конкурирующие лиганды выбирают из группы, в которую входят медикаментозные вещества типа антибиотиков, гормоны, токсины, такие как афлатоксин, вирусы типа вируса Денге, бактерии типа L-monocytogenes, тяжелые металлы, адюльтеранты, аллергены и их смеси.
Предпочтительно упомянутая по меньшей мере одна молекула визуализации соединена с упомянутыми биологическими молекулами распознавания и/или с упомянутыми конкурирующими лигандами посредством химического и/или генетического связывания.
Под терминами «химическое и/или генетическое связывание» в рамках настоящего изобретения следует понимать соединение молекулы распознавания и/или конкурирующего лиганда с молекулой визуализации посредством химического и/или генетического изменения биологической молекулы распознавания и/или конкурирующего лиганда, то есть, следовательно, последние уже не находятся в своем природном состоянии, а в модифицированном виде или в виде комплексов.
Было установлено, что такое химическое и/или генетическое связывание молекулы визуализации с биологическими молекулами распознавания и/или с конкурирующими лигандами позволяет улучшить техническую и практическую совместимость, чтобы объединить в одном средстве обнаружения и/или количественного определения большее число (по меньшей мере 5, предпочтительно по меньшей мере 10, предпочтительно по меньшей мере 15) механизмов обнаружения и/или количественного определения, но чтобы работа одного из них не могла мешать работе одного из других механизмов. Действительно, реакционная смесь в соответствии с изобретением, которая имеет такую связь, позволяет уменьшить и даже устранить риск неспецифичности и взаимодействий между различными биологическими молекулами распознавания и/или различными конкурирующими лигандами, присутствующими в реакционной смеси, и тем самым - риск наблюдения ложных положительных и/или ложных отрицательных результатов, а также значительно уменьшить остаточную маркировку (фоновой шум), наблюдаемую на системе извлечения, когда такая связь отсутствует, и получить лучший контраст между маркировкой элементов извлечения и не зафиксированной твердой подложки (и получить, таким образом, лучший порог обнаружения).
В известном документе ЕР1712914, наоборот, утверждается, что не происходит никакой маркировки посредством химической модификации, чтобы максимально сохранить функции используемых рецепторов и антител, и, что, следовательно, биологические молекулы распознавания используются в своем максимально возможном естественном состоянии. Например, биологическую молекулу распознавания в качестве рецептора маркируют при помощи антитела, которое, в свою очередь, распознается белком-А (как правило, распознающим все типы антител), который связывают с коллоидным золотом. Согласно этому известному документу, с коллоидным золотом (молекула визуализации) связывают именно белок-А, а не биологическую молекулу распознавания.
Предпочтительно упомянутое химическое и/или генетическое связывание осуществляют при помощи по меньшей мере одной статической силы, по меньшей мере одной пептической связи, по меньшей мере одного репортерного гена или их комбинации.
В частном варианте выполнения упомянутую по меньшей мере одну молекулу визуализации выбирают из группы, в которую входят изотиоцианат флуоресцеина (FITC), фикоэритрин (РЕ), родамин В и их смеси.
Предпочтительно упомянутые аналиты выбирают из группы, в которую входят медикаментозные остатки, токсины, вирусы, бактерии, гормоны, тяжелые металлы, адюльтеранты, аллергены и их смеси. Среди медикаментозных остатков можно указать, в частности, антибиотики и антибактериальные средства. Нежелательные химические молекулы, адюльтеранты, могут также обнаруживаться в результате пассивного загрязнения при перемещении из емкости (например, из пластиковой упаковки).
В предпочтительном варианте выполнения упомянутыми аналитами являются медикаментозные остатки, которые выбирают из группы, в которую входят пенициллины, цефалоспорины, тетрациклины, сульфамиды, аминогликозиды, аминоциклитолы, макролиды, хинолоны, ионофоры, карбадоксы, нитрофураны, фениколы и их смеси.
Предпочтительно упомянутую пробу получают из молока, меда, мяса, яиц, цельной крови, сыворотки, мочи или других биологических жидкостей.
Под терминами «биологические жидкости» в рамках настоящего изобретения следует понимать любую органическую жидкость или телесную жидкость, производимую живым организмом.
Предпочтительно упомянутую пробу получают из молока. Было установлено, что обнаружение аналитов является более чувствительным, когда анализируемую пробу получают из молока, так как ингредиенты молока насыщают нитроцеллюлозную мембрану и уменьшают, таким образом, фоновый шум.
В частности, согласно изобретению, соответствующее, одновременное и специфическое обнаружение и/или количественное определение множества аналитов, присутствующих в пробе, осуществляют при помощи оптического устройства считывания.
В частном варианте выполнения места извлечения располагают в соответствии с трехмерной матричной компоновкой. Такая трехмерная матричная компоновка позволяет получить большее число мест извлечения на твердой подложке, имеющей аналогичную площадь, и, следовательно, обнаруживать и/или количественно определять соответственно и одновременно большее число представляющих интерес аналитов.
Предпочтительно трехмерную матричную компоновку определяют по системе координат, имеющей первую координату (Х) на продольной оси длины упомянутой системы извлечения, вторую координату (Y) на продольной оси ширины упомянутой системы извлечения и третью координату (Z) на продольной оси глубины упомянутой системы извлечения. В этом случае направление миграции жидкости (содержащей пробу и реакционную смесь) определяют в соответствии с упомянутой системой координат, определяющей матричную компоновку мест извлечения, закрепляемых на системе извлечения в соответствии с изобретением, и, следовательно, она протекает вдоль координаты Х, координаты Y и координаты Z.
Другие варианты выполнения заявленного средства диагностики представлены в прилагаемой формуле изобретения.
Объектом изобретения является также способ соответствующего, одновременного и специфического обнаружения и/или количественного определения множества аналитов, присутствующих в основном в жидкой пробе, содержащий следующие этапы:
- реакционную смесь заявленного средства диагностики вводят в контакт с пробой для получения жидкости;
- производят инкубацию при температуре, составляющей от 0 до 70°, предпочтительно от 10 до 60°С, предпочтительно от 20 до 50°С, предпочтительно от 20 до 40°С, предпочтительно от 25 до 35°С, предпочтительно 30°С в течение продолжительности, меньшей или равной 15 минутам, предпочтительно меньшей или равной 10 минутам, предпочтительно меньшей или равной 5 минутам, предпочтительно меньшей или равной 3 минутам, предпочтительно равной 3 минутам;
- один конец системы извлечения заявленного средства диагностики смачивают в жидкости;
- производят инкубацию при температуре, составляющей от 0 до 70°, предпочтительно от 10 до 60°С, предпочтительно от 20 до 50°С, предпочтительно от 20 до 40°С, предпочтительно от 25 до 35°С, предпочтительно 30°С в течение продолжительности, меньшей или равной 15 минутам, предпочтительно меньшей или равной 10 минутам, предпочтительно равной 10 минутам; и
- результат на системе извлечения интерпретируют качественно и/или количественно при помощи оптического устройства.
Заявленный способ основан на методах микрофлюидики и иммунохроматографии.
Объектом изобретения является также диагностический комплекс для соответствующего, специфического и одновременного обнаружения и/или количественного определения аналитов, присутствующих в пробе, включающий в себя заявленное средство диагностики и дополнительно содержащий оптическое устройство считывания съемной твердой подложки, содержащее:
- место для размещения упомянутой твердой подложки;
- оптический блок для анализа упомянутой твердой подложки, содержащий:
- первый источник света для излучения, с первой интенсивностью излучения и в первом диапазоне длины волны, первого светового пучка в направлении упомянутого места;
- систему получения изображений, содержащую оптический датчик для получения изображения зоны визуализации, при этом упомянутая зона визуализации включает в себя по меньшей мере часть упомянутого места;
- фильтр для фильтрования определенного диапазона длины волны, расположенный между местом и упомянутой системой получения изображений;
- средства связи для получения информации, относящейся к твердой подложке;
- средства выбора для:
- выбора из списка заранее определенных аналитов, соответствующих упомянутым местам извлечения, закрепленным на твердой подложке, набора аналитов, предназначенных для обнаружения и/или количественного определения, для упомянутой пробы при помощи этой же твердой подложки;
- средства обработки изображения для:
- определения на основании информации, относящейся к упомянутой считываемой твердой подложке, конечного числа участков упомянутого изображения, при этом каждый участок соответствует одному аналиту;
- получения данных, относящихся к интенсивности света, исходящего от упомянутых участков;
- средства определения для:
- вычисления интенсивности участка для каждого участка, соответствующего аналиту, выбранному из упомянутого набора аналитов;
- определения, на основании упомянутой интенсивности участка, информации по аналитам упомянутой пробы для каждого участка, соответствующего аналиту, выбранному из упомянутого набора аналитов;
- средства передачи, выполненные с возможностью передавать упомянутую информацию по аналитам упомянутой анализируемой пробы для каждого участка, соответствующего аналиту, выбранному из упомянутого набора аналитов.
Такое устройство в соответствии с изобретением позволяет считывать тестируемые зоны, в частности, с моментальным измерением флуоресценции или предпочтительно с измерением света, отраженного от тестируемых зон. Для обеспечения выбора тестируемых аналитов, соответствующих интересующим зонам на указателе, такое устройство, благодаря доступу к методу, содержащему информацию, относящуюся к указателю, позволяет сделать выбор из списка тестируемых аналитов. Действительно, необходимо осуществить выбор тестируемых аналитов до получения по ним результатов, чтобы точно сфокусироваться на аналитах, по которым необходимо узнать результаты теста, чтобы не обременять пользователя слишком большим количеством результатов. Получение пользователем доступа к слишком большому количеству результатов, которые не обязательно являются для него нужными, подвергает его риску потери объективности относительно его первоначальной цели анализа. Таким образом, благодаря средствам выбора, такое устройство позволяет пользователю выбрать тестируемые аналиты до считывания указателя. Средства выбора, связанные со средствами обработки изображения, позволяют средствам обработки изображения определять данные только по выбранным аналитам.
Преимуществом использования оптического считывателя в соответствии с изобретением для осуществления диагностики, касающейся набора представляющих интерес аналитов, является то, что оно не требует ни первого выбора различных типов тестовых полосок, ни введения в контакт каждой из этих полосок с тестируемым веществом и затем их помещения в оптический считыватель. Все это позволяет избегать сложного манипулирования тестовых полосок, которое занимает много времени и усложняет задачи логистики. Это обеспечивает также более простой, более быстрый и более целенаправленный анализ тестируемых аналитов, используя только результаты, выбранные в конце считывания полоски оптическим считывателем в соответствии с изобретением.
Предпочтительно набор аналитов является набором из нескольких аналитов.
Предпочтительно оптическое устройство дополнительно содержит:
- средства, позволяющие считывать профиль набора; и упомянутые средства выбора выполнены с возможностью осуществления упомянутого выбора аналитов на основании упомянутого профиля набора.
Предпочтительно каждый участок из упомянутого конечного числа участков упомянутого изображения, определенный средствами обработки изображения, соответствует упомянутому набору аналитов, предпочтительно каждому выбранному аналиту.
Предпочтительно упомянутые средства обработки изображения выполнены с возможностью определять также упомянутое конечное число участков упомянутого изображения на основании упомянутого профиля набора.
Предпочтительно упомянутый первый источник света выполнен с возможностью излучать упомянутый первый пучок напрямую в сторону упомянутого места, предпочтительно напрямую в сторону упомянутых мест извлечения, закрепленных на твердой подложке.
Предпочтительно упомянутая твердая подложка содержит места извлечения в виде точек, каждая из которых имеет диаметр, составляющий от 20 мкм до 2 мм, предпочтительно от 100 мкм до 500 мкм, предпочтительно от 250 мкм до 400 мкм.
Объектом изобретения является также диагностический комплекс для соответствующего, специфического и одновременного обнаружения и/или количественного определения аналитов, присутствующих в пробе, включающий в себя заявленное средство диагностики и дополнительно содержащий оптическое устройство считывания съемной твердой подложки, содержащее:
- место для размещения упомянутой твердой подложки;
- оптический блок для анализа упомянутой твердой подложки, содержащий:
- первый источник света для излучения, с интенсивностью излучения и в первом диапазоне длины волны, первого светового пучка в направлении упомянутого места;
- датчик интенсивности света для измерения интенсивности света, излучаемого упомянутым первым источником света;
- средство обратной связи для модулирования упомянутой интенсивности излучения упомянутого первого источника света в зависимости от интенсивности излучения, измеренной упомянутым датчиком интенсивности света, таким образом, чтобы упомянутый первый источник света излучал свет целевой интенсивности;
- систему получения изображений, содержащую оптический датчик для получения изображения зоны визуализации, при этом упомянутая зона визуализации включает в себя по меньшей мере часть упомянутого места;
- фильтр для фильтрования определенного диапазона длины волны, расположенный между местом и упомянутой системой получения изображений;
- средства обработки изображения для:
- определения конечного числа участков упомянутого изображения;
- получения данных, относящихся к интенсивности света, исходящего от упомянутых участков;
- средства определения для:
- вычисления, для каждого участка, интенсивности участка, и
- средства передачи, выполненные с возможностью передавать информацию, относящуюся к упомянутой интенсивности участка, для каждого участка.
Такое устройство в соответствии с изобретением позволяет считывать тестируемые зоны, в частности, с моментальным измерением флуоресценции или предпочтительно с измерением света, отраженного от тестируемых зон. Когда для тестируемых зон (или точек) используют метод флуоресценции или метод отраженного света, средство обратной связи позволяет гарантировать интенсивность света всегда с одинаковым возбуждением, что обеспечивает надежное моментальное измерение флуоресценции или отражения при любой температуре, с любым используемым источником энергии или при любом сроке службы и времени старения источника света. Использование средства обратной связи позволяет гарантированно иметь источник световой энергии с постоянной во времени и заранее определенной интенсивностью. Источник световой энергии с заранее определенной интенсивностью позволяет, в частности, гарантировать надежные количественные результаты. Предпочтительно средство обратной связи является электронным средством обратной связи. Например, датчик интенсивности света является фотодиодом.
Объектом изобретения является также диагностический комплекс для соответствующего, специфического и одновременного обнаружения и/или количественного определения аналитов, присутствующих в пробе, включающий в себя заявленное средство диагностики и дополнительно содержащий оптическое устройство считывания съемной твердой подложки, содержащее:
- место для размещения упомянутой твердой подложки;
- оптический блок для анализа упомянутой твердой подложки, содержащий:
- первый источник света для излучения, с интенсивностью излучения и в первом диапазоне длины волны, первого светового пучка в направлении упомянутого места;
- систему получения изображений, содержащую двухмерный оптический датчик для получения двухмерного изображения зоны визуализации, при этом упомянутая зона визуализации включает в себя по меньшей мере часть упомянутого места;
- фильтр для фильтрования определенного диапазона длины волны, расположенный между местом и упомянутой системой получения изображений;
- средства обработки упомянутого двухмерного изображения для:
- обнаружения контрольных зон упомянутого двухмерного изображения;
- определения конечного числа участков упомянутого изображения;
- позиционирования в каждом двухмерном изображении каждого участка в заранее определенное положение относительно упомянутых контрольных зон;
- получения данных, относящихся к интенсивности света, исходящего от упомянутых участков;
- средства определения для:
- вычисления, для каждого участка, интенсивности участка, и
- средства передачи, выполненные с возможностью передавать упомянутую интенсивность участка, для каждого участка.
Такое устройство в соответствии с изобретением обеспечивает одновременное считывание большого числа точек, благодаря двухмерному оптическому датчику и средствам обработки изображения и определения, позволяющим считывать данные аналитов для каждой из точек. Двухмерное изображение содержит участки, части, интересующие области, интересующие зоны, а также фрагменты изображений. Предпочтительно участки двухмерного изображения содержат множество пикселей. Предпочтительно каждый участок содержит по меньшей мере 20 пикселей, предпочтительно более 50 пикселей и еще предпочтительнее - более 200 пикселей.
Преимуществом такого заявленного устройства является возможность диагностики посредством непрерывного считывания при флуоресценции с максимальным устранением фонового шума, создаваемого источником света.
Другим преимуществом такого заявленного считывающего оптического устройства является возможность сканирования большого количества интересующих областей на одном указателе. В случае такого заявленного оптического устройства сканирование большого числа интересующих областей не требует предусматривать места для нескольких указателей. Применение нескольких указателей в одном оптическом считывателе для одновременного считывания нескольких указателей, чтобы охватить большое число интересующих областей при помощи одного оптического датчика, может стать причиной плохого размещения и смещения интересующих областей от одного измерения к другому для каждого из указателей, вводимых в оптический считыватель.
Объектом изобретения является также диагностический комплекс для соответствующего, специфического и одновременного обнаружения и/или количественного определения аналитов, присутствующих в пробе, включающий в себя заявленное средство диагностики и дополнительно содержащий оптическое устройство считывания съемной твердой подложки, содержащее:
- место для размещения упомянутой твердой подложки;
- устройство идентификации считываемой твердой подложки;
- средства связи для получения доступа к базе данных методов, относящихся к упомянутой считываемой твердой подложке, для получения информации, относящейся к твердой подложке;
- оптический блок для анализа упомянутой твердой подложки на основе параметров анализа, включенных в упомянутую информацию, относящуюся к твердой подложке, содержащий:
- первый источник света для излучения, с интенсивностью излучения и в первом диапазоне длины волны, первого светового пучка в направлении упомянутого места;
- систему получения изображений, содержащую оптический датчик для получения изображения зоны визуализации, при этом упомянутая зона визуализации включает в себя по меньшей мере часть упомянутого места;
- фильтр для фильтрования определенного диапазона длины волны, расположенный между местом и упомянутой системой получения изображений;
- средства обработки изображения для:
- считывания в информации, относящейся к упомянутой считываемой твердой подложке, информации, относящейся к конечному числу участков упомянутого изображения;
- получения данных, относящихся к интенсивности света, исходящего от упомянутых участков;
- средства определения для:
- вычисления, для каждого участка, интенсивности участка, и
- определения на основании упомянутой интенсивности участка и на основании информации, относящейся к упомянутой считываемой твердой подложке, данных аналита для каждого участка;
- средства передачи, выполненные с возможностью передавать упомянутую данную по аналиту, для каждого участка.
Такое устройство в соответствии с изобретением обеспечивает оптическое считывание указателя для анализа пробы с выбором автоматического метода считывания. Метод считывания предпочтительно включает в себя данные, касающиеся: версии метода, номера партии, предельной даты использования партии, типа используемого источника света, типа интересующей зоны (линия или точка), метода качественного (бинарного) или количественного анализа, параметров съемки изображений (время экспозиции, коэффициент увеличения,…), положений относительно контрольных точек (например, в декартовой системе координат), числа интересующих зон, числа реплик на аналит, матричной организации интересующих зон на подвижной твердой подложке, размеров интересующих зон (например, радиус), размера зоны вокруг интересующей зоны для учета фона, параметров калибровки, типа интерполяции данных или для количественного анализа пробы и, наконец, назначения интересующих зон в зависимости от аналита, который они позволяют обнаруживать и/или количественно определять.
Другие варианты выполнения заявленного диагностического комплекса представлены в прилагаемой формуле изобретения.
Объектом изобретения является также применение заявленного средства диагностики для соответствующего, одновременного и специфического обнаружения и/или количественного определения аналитов, присутствующих в пробе, предпочтительно по меньшей мере 5, предпочтительно по меньшей мере 10 и предпочтительно по меньшей мере 15 разных аналитов.
Объектом изобретения является также применение заявленного диагностического комплекса для соответствующего, одновременного и специфического обнаружения и/или количественного определения аналитов, присутствующих в пробе, предпочтительно по меньшей мере 5, предпочтительно по меньшей мере 10 и предпочтительно по меньшей мере 15 разных аналитов.
Другие варианты использования заявленного средства диагностики и заявленного диагностического комплекса представлены в прилагаемой формуле изобретения.
Другие отличительные признаки, детали и преимущества изобретения будут более очевидны из нижеследующего описания, представленного в качестве не ограничительного примера, со ссылками на прилагаемые чертежи.
Описание фигур
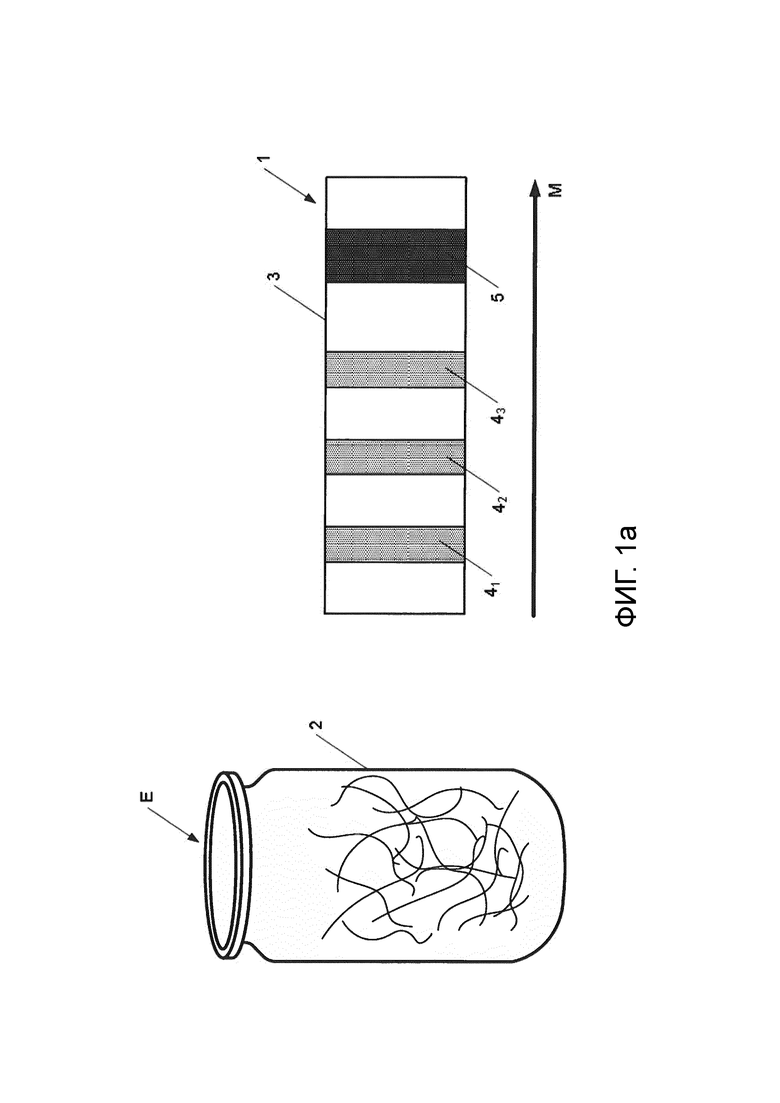
Фиг. 1а - схематичный вид средства диагностики согласно известному документу ЕР1712914.
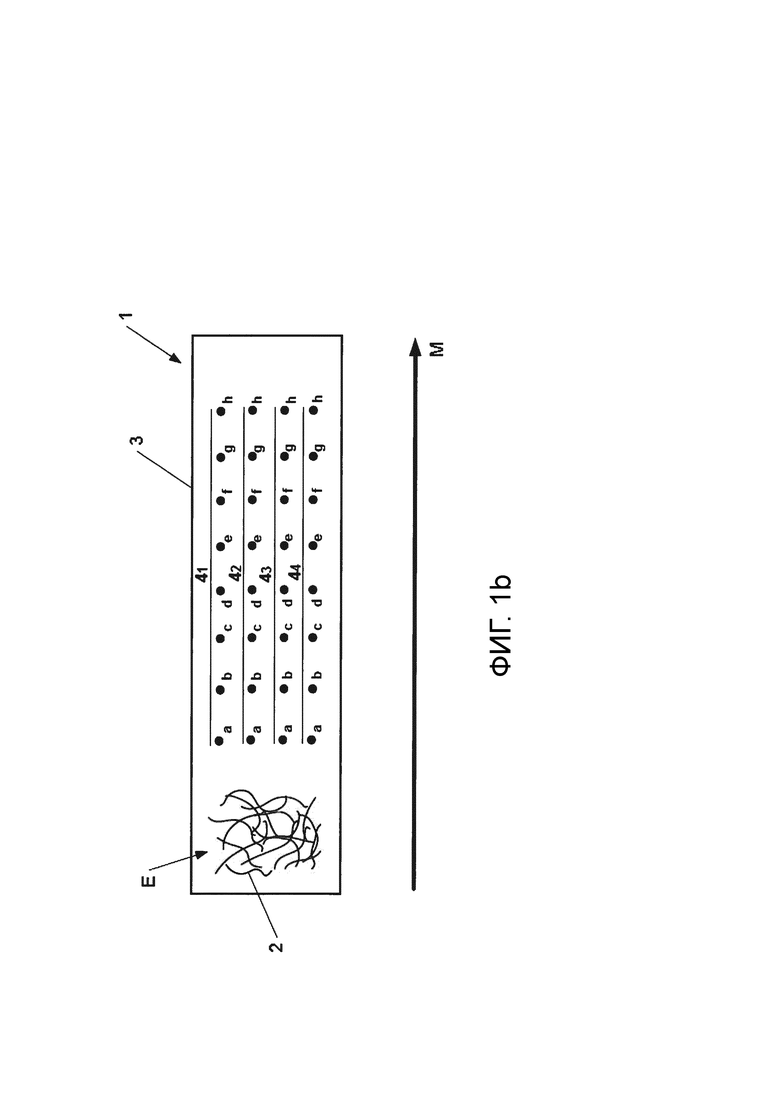
Фиг. 1b - схематичный вид средства диагностики согласно документу Taranova et al.
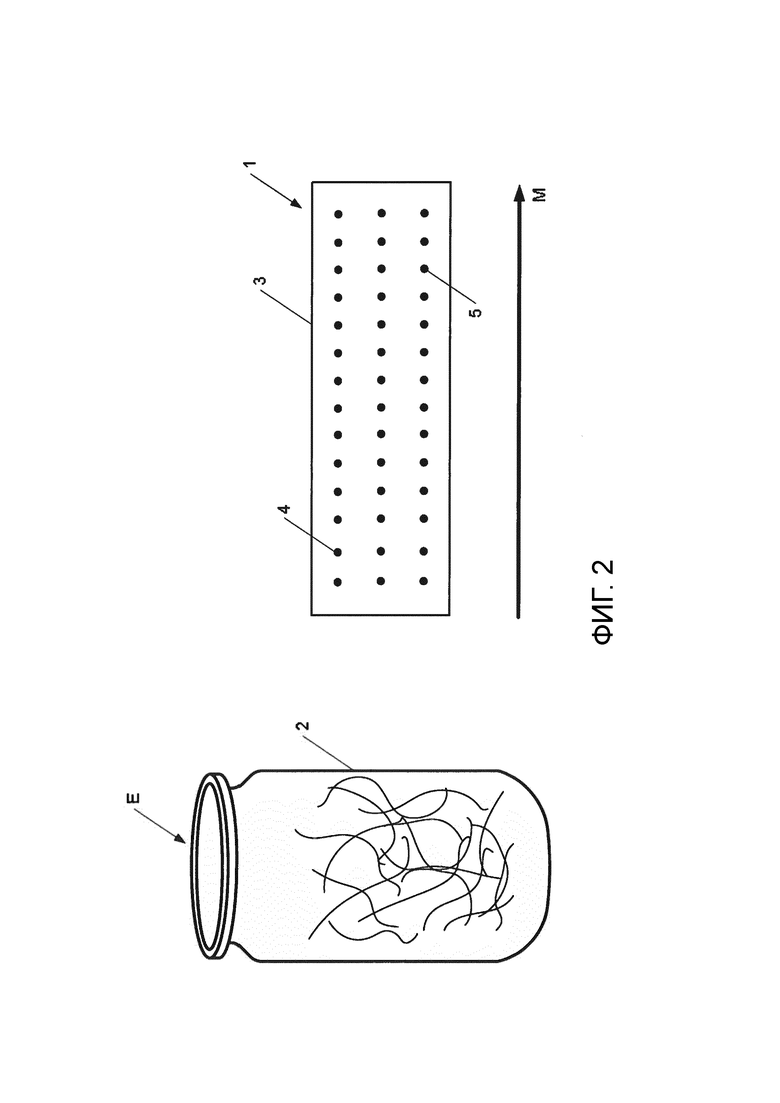
Фиг. 2 - схематичный вид заявленного средства диагностики.
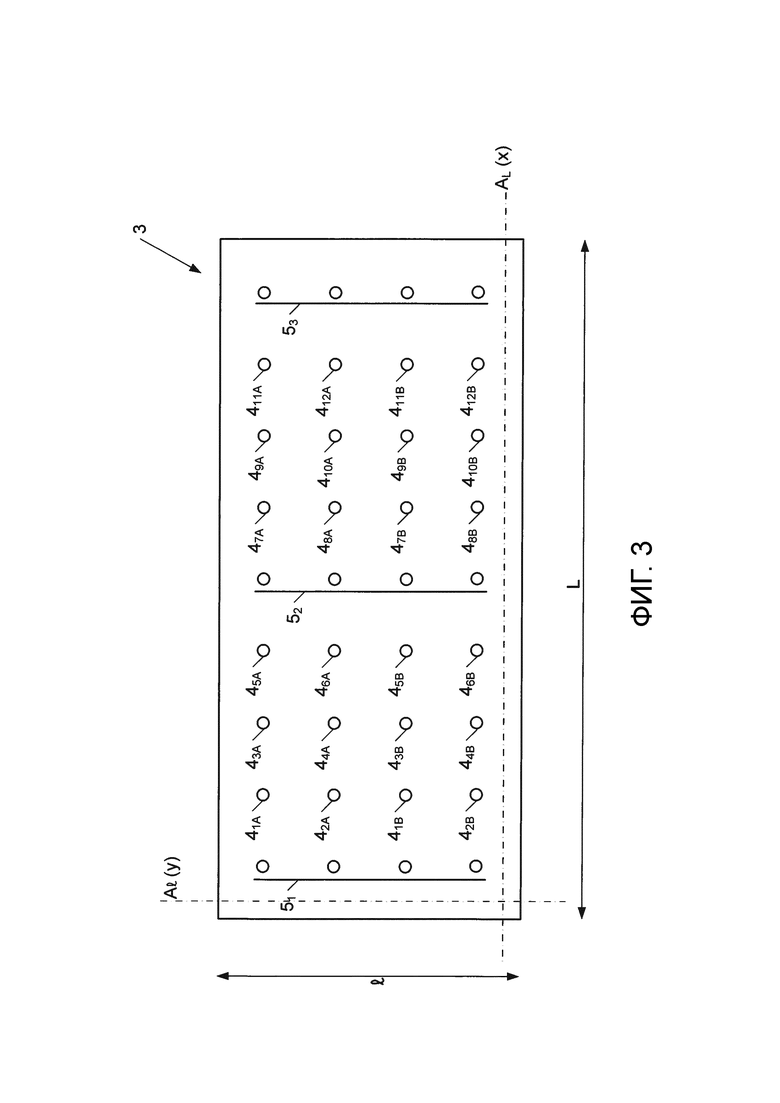
Фиг. 3 - схематичный детальный вид системы извлечения в соответствии с изобретением.
На фигурах идентичные или аналогичные элементы имеют одинаковые обозначения.
На фиг. 1а представлено средство 1 диагностики согласно известному документу ЕР1712914, где показано расположение элементов извлечения 41, 42, 43 и 5 на системе извлечения 3 в виде твердой нитроцеллюлозной подложки в случае одновременной дозировки β-лактамов 41, тетрациклинов 42 и сульфадиметоксина 43, при этом предусмотрена зона контроля 5, неподвижная относительно направления миграции М. Согласно этому известному документу, в отдельном сосуде предусмотрена реакционная смесь 2, с которой вводят в контакт тестируемую пробу Е.
На фиг. 1b представлено средство 1 диагностики согласно документу Taranova et al., где показано расположение элементов извлечения 41а, 41b, 41c, 41d, 41e, 41f, 41g, 41h, 42а, 42b, 42c, 42d, 42e, 42f, 42g, 42h, 43а, 43b, 43c, 43d, 43e, 43f, 43g, 43h, 44а, 44b, 44c, 44d, 44e, 44f, 44g, 44h на системе извлечения 3 в виде твердой нитроцеллюлозной подложки в случае одновременной дозировки амфетаминов (41а, 41b, 41c, 41d, 41e, 41f, 41g, 41h), бензоилэкгонина (42а, 42b, 42c, 42d, 42e, 42f, 42g, 42h), метамфетаминов (43а, 43b, 43c, 43d, 43e, 43f, 43g, 43h) и морфина (44а, 44b, 44c, 44d, 44e, 44f, 44g, 44h). Элементы извлечения 4 закреплены в виде точек в соответствии с двухмерной матричной компоновкой. Согласно документу Taranova et al., реакционная смесь 2 присутствует на упомянутой системе извлечения 3 в лиофилизированном виде на входе упомянутых элементов извлечения 4, закрепленных на упомянутой системе извлечения 3, относительно направления миграции М жидкости, содержащей тестируемую пробу Е на реакционной смеси 2. Согласно этому документу, элементы извлечения, расположенные в один ряд, то есть имеющие одну и ту же координату Y, являются специфическими для одного и того же аналита.
На фиг. 2 представлено заявленное средство 1 диагностики с показом позиционирования элементов извлечения 4 и 5 на системе извлечения 3 в виде твердой подложки относительно направления миграции М, при этом элементы извлечения 4 и 5 закреплены в виде точек в соответствии с двухмерной матричной компоновкой. Согласно изобретению, в отдельной емкости предусмотрена реакционная смесь 2, с которой вводят в контакт тестируемую пробу Е, чтобы получить жидкость, после чего систему извлечения 3 смачивают полученной жидкостью.
На фиг. 3 детально показана система извлечения 3 в соответствии с изобретением, на которой места извлечения 4 и 5 расположены в соответствии с двухмерной матричной компоновкой в виде точек определенного диаметра, при этом каждая из точек отделена от других минимальным расстоянием. Двухмерную матричную компоновку определяют в системе координат (Х;Y), которая имеет первую координату Х на продольной оси (АL) длины (L) упомянутой системы извлечения 3 и вторую координату Y на продольной оси (Al) ширины (l) упомянутой системы извлечения 3. Согласно предпочтительному варианту выполнения, система извлечения 3 содержит по меньшей мере 12 отдельных мест извлечения (41-412), предназначенных для соответствующего, одновременного и специфического обнаружения и/или количественного определения по меньшей мере 12 аналитов разных классов, присутствующих в пробе Е, и по меньшей мере три места извлечения 5, предназначенные для контроля порога обнаружения или служащие для калибровки. Кроме того, каждое из мест извлечения (41-412 и 51-53) расположено в двойном экземпляре (41А;41В-412А;412В).
Разумеется, настоящее изобретение ни в коем случае не ограничивается описанными выше вариантами выполнения, и в него можно вносить изменения, не выходя за пределы объема, определенного прилагаемой формулой изобретения.
Варианты выполнения изобретения - Примеры
Пример 1: Пример композиции буферного раствора для реакционной смеси и пример способа приготовления реакционной смеси
Таблица 1:
В этот буферный раствор добавляют молекулы распознавания и/или конкурирующие лиганды. После инкубации смеси в течение одной ночи при 4°С ее подвергают лиофилизации. Во время испытания в полученную таким образом реакционную смесь добавляют 250 мкл предназначенной для теста пробы.
Пример 2: Пример связывания молекул распознавания с флуорофором родамином В
В соответствии со способом, описанным в ЕР1712914А1, получают рецепторы «Бета» и «Тетра» и олигонуклеотиды ДНК.
Моноклональные антитела очищают на колонке белка-А или белка-G в зависимости от вида и от изотипа. Затем антитела хранят при -20°С в буферном растворе фосфата 10ммоль, NaCl 140ммоль, рН 7,4.
Используемый родамин В имеет остаток N-гидроксисукцинимид(NHS)-эфиров, особенностью которого является реагирование с аминогруппами белков с щелочным рН.
Молекулы распознавания (антитела и/или рецепторы) подвергают диализу в течение ночи в буферном растворе карбоната 50 ммоль, рН 8,5. Флуорофор растворяют в DMF до 5 мг/мл.
Молекулу распознавания и флуорофор (молекулу визуализации) оставляют в контакте друг и другом в молярном соотношении около 1/4 в течение часа в защищенном от света месте.
Наконец, химическую реакцию останавливают во время комплексного диализа при помощи буферного раствора фосфата 10 ммоль, рН 7,4.
Можно также осуществлять другие типы химического связывания с флуорохромами, имеющими малеимидные или карбоксильные группы.
Можно использовать другие типы флуорофоров, такие как FITC, Alexa, DyLight,…
Связывание молекул распознавания можно также производить с колориметрическими наночастицами (наночастицы золота, латекса, углерода…) как посредством ковалентного связывания, так и путем электростатической адсорбции.
Пример 3: Пример композиции реакционной смеси и пример элементов извлечения, закрепленных на системе извлечения
Таблица 2:
Пример 4: Пример испытания и полученные результаты
Пробу молока ввели в контакт с реакционной смесью (содержащей буферный раствор и молекулы распознавания и/или конкурирующие лиганды в лиофилизированном виде) в течение 3 минут при 30°С. Затем входной по направлению миграции конец системы извлечения погрузили в раствор (содержащий пробу и реакционную смесь). После инкубации в течение 10 минут при 30°С произвели считывание результатов при помощи оптического устройства.
Результаты приведены в таблице 3
Таблица 3:
(частей на миллиард; мкг/кг)
| название | год | авторы | номер документа |
|---|---|---|---|
| МИКРОФЛЮИДНЫЕ УСТРОЙСТВА И СПОСОБЫ ИХ ПОДГОТОВКИ И ПРИМЕНЕНИЯ | 2006 |
|
RU2423073C2 |
| ТВЕРДОЕ УСТРОЙСТВО ДЛЯ ПРОВЕДЕНИЯ МУЛЬТИАНАЛИТНЫХ АНАЛИЗОВ, СПОСОБ ЕГО ФОРМИРОВАНИЯ И СИСТЕМА, ВКЛЮЧАЮЩАЯ ТАКОЕ УСТРОЙСТВО | 1998 |
|
RU2168174C2 |
| УСТРОЙСТВО ДЛЯ АНАЛИЗОВ И СПОСОБ ВЫПОЛНЕНИЯ БИОЛОГИЧЕСКИХ АНАЛИЗОВ | 2009 |
|
RU2527686C2 |
| СПОСОБЫ И СИСТЕМЫ ДЛЯ ОБНАРУЖЕНИЯ | 2008 |
|
RU2480768C2 |
| СПОСОБ ГАРМОНИЗАЦИИ РЕЗУЛЬТАТОВ АНАЛИЗА | 2019 |
|
RU2817657C2 |
| СПОСОБЫ РЕТЕНТАТНОЙ ХРОМАТОГРАФИИ ДЛЯ РАЗДЕЛЕНИЯ АНАЛИТОВ В ОБРАЗЦЕ | 1998 |
|
RU2253116C2 |
| МУЛЬТИПЛЕКСНЫЕ АНАЛИЗЫ НА ОСНОВЕ АПТАМЕРОВ | 2013 |
|
RU2666989C2 |
| СИСТЕМЫ И МЕТОДЫ ОПТИМИЗАЦИИ ИСПОЛЬЗОВАНИЯ ОБРАЗЦА | 2012 |
|
RU2620922C2 |
| МОЛЕКУЛЯРНЫЙ ЗОНД | 1991 |
|
RU2107730C1 |
| ТЕСТ-СИСТЕМА С ИСПОЛЬЗОВАНИЕМ ЭЛЕМЕНТОВ НЕЭНЗИМАТИЧЕСКОГО РАСПОЗНАВАНИЯ АНАЛИЗИРУЕМОГО ВЕЩЕСТВА | 2005 |
|
RU2398235C2 |
Группа изобретений относится к иммунохроматографической диагностике. Раскрыт диагностический комплекс для одновременного и специфического обнаружения аналитов, присутствующих в пробе (E), включающий средство (1) иммунохроматографической диагностики для одновременного и специфического обнаружения множества аналитов, присутствующих в жидкой пробе (Е), содержащее по меньшей мере одну реакционную смесь (2), содержащую биологические молекулы распознавания и/или конкурирующие лиганды, помеченные по меньшей мере одной молекулой визуализации; по меньшей мере одну систему извлечения (3) в виде твердой подложки, на которой закреплены конкурирующие лиганды и/или биологические молекулы распознавания в разных и известных местах извлечения (4, 5); оптическое устройство считывания съемной твердой подложки (3). Также раскрыты способ обнаружения с использованием указанного комплекса и применение указанного комплекса для обнаружения классов аналитов в пробе. Группа изобретений обеспечивает быстрое, практичное, экономичное и эффективное средство диагностики. 3 н. и 8 з.п. ф-лы, 4 ил., 3 табл., 4 пр.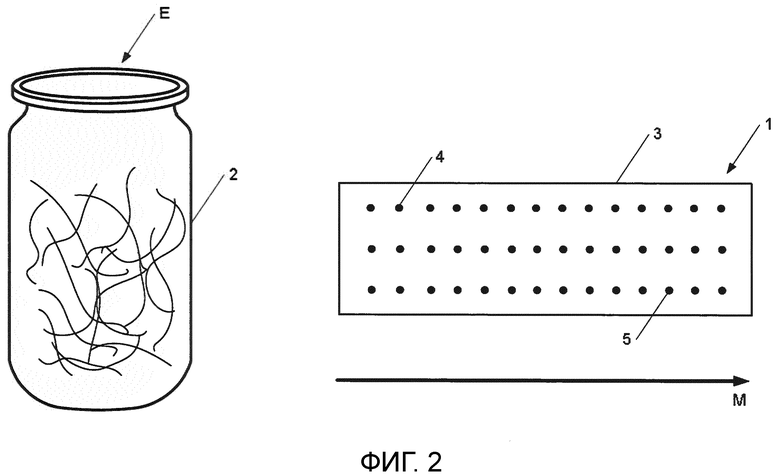
1. Диагностический комплекс для одновременного и специфического обнаружения аналитов, присутствующих в пробе (E), включающий средство (1) иммунохроматографической диагностики для одновременного и специфического обнаружения множества аналитов, присутствующих в жидкой пробе (Е), содержащее:
- по меньшей мере одну реакционную смесь (2), содержащую биологические молекулы распознавания и/или конкурирующие лиганды, помеченные по меньшей мере одной молекулой визуализации; и
- по меньшей мере одну систему извлечения (3) в виде твердой подложки, на которой закреплены конкурирующие лиганды и/или биологические молекулы распознавания в разных и известных местах извлечения (4, 5), которые расположены в соответствии с двухмерной матричной компоновкой таким образом, чтобы посредством локализации упомянутых мест извлечения (4, 5) на упомянутой подложке идентифицировать упомянутые аналиты, присутствующие в упомянутой пробе (Е),
где:
а) упомянутая двумерная матричная компоновка определена по системе координат, имеющей первую координату (Х) и вторую координату (Y), при этом для одной и той же координаты Х несколько мест извлечения содержат, каждое, биологические молекулы распознавания или разные конкурирующие лиганды, расположенные по разным координатам Y, и для одной и той же координаты Y несколько мест извлечения содержат, каждое, биологические молекулы распознавания или разные конкурирующие лиганды, расположенные по разным координатам Х;
b) для обнаружения данного аналита присутствует диагностическая пара, состоящая из конкурирующего лиганда и биологической молекулы распознавания, при этом упомянутая биологическая молекула распознавания находится в упомянутой реакционной смеси (2), и упомянутый конкурирующий лиганд закреплен по меньшей мере в одном месте извлечения (4), или наоборот;
c) упомянутая по меньшей мере одна молекула визуализации является молекулой, обнаруживаемой при флуоресценции; и
d) упомянутая реакционная смесь (2) находится в емкости, при этом упомянутая емкость является отдельной от упомянутой системы извлечения (3);
где диагностический комплекс дополнительно содержит оптическое устройство считывания съемной твердой подложки (3), содержащее:
- место для размещения упомянутой твердой подложки (3);
- оптический блок для анализа упомянутой твердой подложки (3), содержащий:
○ первый источник света для излучения, с первой интенсивностью излучения и в первом диапазоне длины волны, первого светового пучка в направлении упомянутого места;
○ систему получения изображений, содержащую оптический датчик для получения изображения зоны визуализации, при этом упомянутая зона визуализации включает в себя по меньшей мере часть упомянутого места;
○ фильтр для фильтрования определенного диапазона длины волны, расположенный между местом и упомянутой системой получения изображений;
- средства связи для получения информации, относящейся к твердой подложке (3);
- средства выбора для:
○ выбора из списка заранее определенных аналитов, соответствующих упомянутым местам извлечения, закрепленным на твердой подложке (3), набора аналитов, предназначенных для обнаружения упомянутой пробы при помощи этой же твердой подложки (3);
- средства обработки изображения для:
○ определения на основании информации, относящейся к упомянутой считываемой твердой подложке (3), конечного числа участков упомянутого изображения, при этом каждый участок соответствует одному аналиту;
○ получения данных, относящихся к интенсивности света, исходящего от упомянутых участков;
- средства определения для:
○ вычисления для каждого участка, соответствующего аналиту, выбранному из упомянутого набора аналитов, интенсивности участка;
○ определения, на основании упомянутой интенсивности участка, информации по аналитам упомянутой пробы для каждого участка, соответствующего аналиту, выбранному из упомянутого набора аналитов;
- средства передачи, выполненные с возможностью передавать упомянутую информацию по аналитам упомянутой анализируемой пробы для каждого участка, соответствующего аналиту, выбранному из упомянутого набора аналитов.
2. Диагностический комплекс по п. 1, отличающийся тем, что упомянутые места извлечения (4, 5) расположены в соответствии с двухмерной матричной компоновкой в виде точек, каждая из которых имеет диаметр, составляющий от 20 мкм до 2 мм.
3. Диагностический комплекс по п. 1 или 2, отличающийся тем, что упомянутая система извлечения (3) содержит по меньшей мере 15 разных аналитов, присутствующих в пробе, и по меньшей мере одно место извлечения, предназначенное для контроля и/или калибровки.
4. Диагностический комплекс по любому из пп. 1-3, отличающийся тем, что упомянутая система извлечения (3) выполнена в виде твердой подложки и содержит мембрану или набор мембран.
5. Диагностический комплекс по любому из пп. 1-4, отличающийся тем, что упомянутая по меньшей мере одна молекула визуализации связана с упомянутыми биологическими молекулами распознавания и/или с упомянутыми конкурирующими лигандами посредством связывания.
6. Диагностический комплекс по п. 5, отличающийся тем, что упомянутое связывание осуществляют при помощи по меньшей мере одной статической силы, по меньшей мере одной пептидной связи, по меньшей мере одного репортерного гена или их комбинации.
7. Диагностический комплекс по любому из пп. 1-6, отличающийся тем, что упомянутые аналиты выбирают из группы, в которую входят медикаментозные остатки, токсины, вирусы, бактерии, гормоны, тяжелые металлы, фальсифицирующие вещества, аллергены и их смеси.
8. Диагностический комплекс по п. 7, отличающийся тем, что упомянутыми аналитами являются медикаментозные остатки, которые выбирают из группы, в которую входят пенициллины, цефалоспорины, тетрациклины, сульфамиды, аминогликозиды, аминоциклитолы, макролиды, хинолоны, ионофоры, карбадоксы, нитрофураны, фениколы и их смеси.
9. Способ одновременного и специфического обнаружения множества аналитов, присутствующих в жидкой пробе (Е), включающий следующие этапы:
– обеспечение диагностического комплекса по любому из предшествующих пунктов;
- приведение в контакт реакционной смеси (2) диагностического комплекса с пробой (Е) для получения жидкости;
- производят инкубацию при температуре, составляющей от 0 до 70°, в течение продолжительности, меньшей или равной 15 мин;
- смачивают один конец системы извлечения (3) средства (1) диагностики в жидкости;
- производят инкубацию при температуре, составляющей от 0 до 70°, в течение продолжительности, меньшей или равной 15 мин; и
- результат на системе извлечения интерпретируют качественно при помощи оптического устройства считывания съемной твердой подложки (3).
10. Диагностический комплекс по любому из пп. 1-8, отличающийся тем, что оптическое устройство считывания съемной твердой подложки (3) дополнительно содержит:
- средства, позволяющие считывать профиль набора;
и тем, что упомянутые средства выбора выполнены с возможностью осуществления упомянутого выбора аналитов на основании упомянутого профиля набора.
11. Применение диагностического комплекса по любому из пп. 1-8 для одновременного и специфического обнаружения классов аналитов, присутствующих в пробе (Е).
| US 20120184462 A1, 19.07.2012 | |||
| US 20150087543 A1, 26.03.2015 | |||
| СПОСОБ ИММУНОХРОМАТОГРАФИЧЕСКОГО ОПРЕДЕЛЕНИЯ АНТИБИОТИКОВ В МОЛОКЕ И МОЛОЧНЫХ ПРОДУКТАХ | 2009 |
|
RU2406090C2 |
| WO 2017075649 A1, 11.05.2017. | |||
Авторы
Даты
2023-07-05—Публикация
2018-10-04—Подача