Изобретение относится к области медицины, а именно к физиологии укачивания организма, и может быть использовано для повышения резистентности организма к укачиванию.
Механизм действия большинства противорвотных препаратов заключается в успокаивающем действии на рвотный центр продолговатого мозга (подавлении возбуждения лабиринтного аппарата) в на хеморецепторную пусковую (триггерную) зону продолговатого мозга. При морской и воздушной болезни (при укачивании) наступает преимущественно перевозбуждение лабиринтного аппарата. Поэтому для лечения морской и воздушной болезни применяют лекарственные препараты, способные достаточно эффективно подавлять возбуждение лабиринтного аппарата. А те противорвотные препараты, которые способны успокаивать только пусковую (триггерную) зону продолговатого мозга, не излечивают от морской и воздушной болезни. В хеморецепторной пусковой (триггерной) зоне содержатся дофаминовые рецепторы. В рвотном же центре содержатся холинергические (мускариновые) и гистаминовые (H1) рецепторы.
Известен способ [1, с. 211 и 59] повышения резистентности организма к укачиванию путем предварительного введения (перорально или внутримышечно) лекарственного препарата в организм перед укачиванием, в котором в качестве лекарственного препарата используют нейролептические вещества из группы фенотиазина (наилучший - тиэтилперазин, или иначе торекан) и из группы бутирофенона (наилучшие - галоперидол и меторин), действующие преимущественно на дофаминергаческие системы триггерной зоны и в значительно меньшей степени действующие на рвотный центр продолговатого мозга.
Однако этот способ-аналог мало эффективен. Кроме того, для применения указанных лекарственных препаратов есть многочисленные противопоказания, и наблюдается высокая токсичность при их передозировке. Например, основные препараты группы бутирофенов (1, с. 59) являются сильными антипсихотическими средствами. При их применении часто наблюдаются экстрапирамидные растройства, поэтому лечение бутерофенонами обычно требует одновременного назначения противопаркинсонических средств.
Известен более эффективный способ-аналог [1, с. 309] повышения резистентности организма к укачиванию путем предварительного введения (перорально или внутримышечно) лекарственного препарата в организм перед укачиванием, в котором в качестве лекарственного препарата используют противогистаминные вещества (наилучшие и наименее безвредные - димедрол и дименгидренат), действующие преимущественно на гистаминовые рецепторы рвотного центра.
Главные недостатки - малая эффективност, наличие противопоказаний, вредные побочные действия. Например, используемые препараты могут вызывать интоксикацию, сухость во рту, затруднение дыхания, спутанность сознания, замедляют двигательные и психические реакции и др.
Известен еще более эффективный способ-аналог [1, с. 309] повышения резистентности организма к укачиванию путем предварительного введения (перорально или внутримышечно) лекарственного препарата в организм перед укачиванием, в котором в качестве лекарственного препарата используют холинолитик платифиллин (или фармацевтические композиции на его основе, например таблетки "Плавефин" [1, с. 243]), действующий преимущественно на холинергические рецепторы рвотного центра. В таблетке "Плавефин" (1, с. 243) содержится 5 мг платифиллина гидрохлорида, 50 мг папаверина гидрохлорида, 100 мг кофеина, 150 мг калия бромида. Применяют внутрь по 1 таблетке за 1 ч да поездки (до укачивания) и повторно через 3-5 ч.
Главные недостатки этого способа - малая эффективность, наличие противопоказаний, вредные побочные действия. Например, передозировка платифиллина может вызвать такие же явления, как передозировка атропина (сухость во рту, сердцебиение, расширение зрачков, тахикардию, атонию кишечника, возбуждение ЦНС и др.). Противопоказания - такие же, как для платифиллина (при глаукоме, органических заболеваниях печени и почек).
Известен более эффективный способ-прототип [1, с. 239] повышения резистентности организма к укачиванию путем предварительного введения (перорально или парентерально, например подкожно) лекарственного препарата в организм перед укачиванием, в котором в качестве лекарственного препарата используется холинолитик скополамин (или фармацевтические композиции на его основе, например таблетки "Аэрон" [1, с. 240]), действующий преимущественно на холинергические рецепторы рвотного центра и нашедший самое широкое применение для лечения морской и воздушной болезни. Препарат скополамин с этой целью применяют в разовой дозе 0,25-0,5 мг. Таблетки "Аэрон" содержат по 0,1 мг скополамина и 0,4 мг гиосциамина. Их применяют по 1-2 штуке за 6 ч до укачивания в затем по 1 штуке через каждые 6 ч укачивания.
Главными недостатками способа-прототипа, как и способов-аналогов, являются малая эффективность, наличие противопоказаний к применению (глаукома и др. ), нежелательные побочные действия (жажда, сухость во рту и горле, тахикардия, атония кишечника, затруднение мочеиспускания и др.), токсичность при передозировках.
Техническим результатом предлагаемого изобретения является увеличение эффективности и безопасности способа повышения резистентности организма к укачиванию.
Технический результат достигается тем, что в способе повышения резистентности организма к укачиванию, путем парентерального введения лекарственного препарата в организм, в качестве лекарственного препарата используют окисленный глутатион или фармацевтические композиции на его основе. Кроме того, технический результат достигается тем, что введение окисленного глутатиона осуществляют за 1-24 ч перед процедурой и в дозе 0,1-10 мг на 1 кг массы организма.
Фармацевтические композиции на основе окисленного глутатиона могут содержать фармацевтически приемлемые растворитель (физиологический раствор и другие), компонент, способный продлить пребывание глутатиона в окисленной форме (cis-диаминодихлор-платина и другие), активные компоненты, дополняющие лекарственное действие глутоксима (рибофлавин и другие).
Известно [2] об использовании окисленного глутатиона для лечения онкологических, инфекционных и гематологических заболеваний, при которых целесообразна стимуляция эндогенной продукции цитокинов и гемопоэтических факторов. Его лекарственная форма под названием "Глутоксим" прошла клинические испытания, разрешена Фармкомитетом к использованию в медицинской практике [3] и поставляется в специализированные аптеки Москвы и Санкт-Петербурга. Известны также фармацевтические композиции на основе окисленного глутатиона [4]. Но нет сведений об использовании окисленного глутатиона или фармацевтических композиций ва его основе для повышения резистентности организма к укачиванию.
Сравнение заявляемых способа и способа-прототипа позволило установить, что заявляемый способ отличается использованием в качестве лекарственного препарата вместо токсичных скополамина и гиосциамина безвредного окисленного глутатиона или фармацевтических композиций на его основе, в сделать вывод, что изобретение соответствует критерию "новизна".
При изучении других известных решений в данной области техники признаки, идентичные признакам, отличающим заявляемое изобретение от прототипа, выявлены не были, и поэтому оно соответствует критерию "изобретательский уровень".
Применение заявляемого изобретения для повышения резистентности организма к укачиванию и использование в нем известных препаратов и технологий обеспечивает ему критерий "промышленная применимость".
Предлагаемый способ осуществляют следующим образом.
За 1-24 ч перед процедурой укачивания осуществляют парентеральное (подкожное, внутримышечное, внутрибрюшинное) введение окисленного глутатиона (в дозе 0,1-10 мг на 1 кг массы организма). Затем проводят укачивание при заданных условиях эксперимента и регистрируют результаты укачивающего воздействия на организм.
Предлагаемый способ иллюстрируется следующим примером.
Опыты проведены на двух группах (опытной и контрольной) белых мышей линии SHR из питомника Рапполово, самцах, весом 18-20 г (возраст 40-65 дн.). За 24 ч до начала укачивания подопытным животным внутрибрюшинно ввели по 0,2 мл 0,1%-ного раствора окисленного глутатиона (глутоксима). Контрольным животным внутрибрюшинно ввели по 0,2 мл раствора Рингера. Для укачивания мышей был применен стенд типа центрифуги с реверсом. Параметры стенда: цикл прямого и обратного вращений - 5 с, соотношение величин прямого и обратного хода - 1:1 (по 1.2 оборота на каждый ход за 2.5 с), угловая скорость по достижении ее максимума - 1.2 об/с, пределы свободного перемещения мышей в секциях - 8-13 см от центра вращения. В каждом опыте в центрифугу помещали по 4 контрольные мыши (которым был введен физраствор Рингера) и по 4 подопытных мыши (которым был введен раствор Глутоксима). Контрольные мыши при указанных условиях утрачивали двигательную активность обычно через 13 мин после начала реверсивного укачивания.
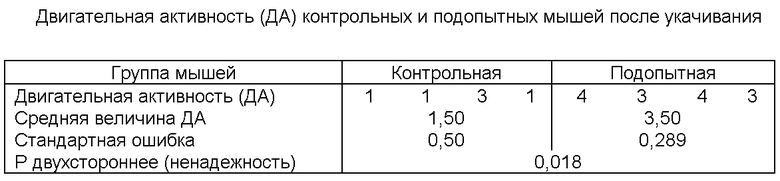
Реверсивное укачивание проводили в течение 15 мин. За 2 мин до его конца включали видеокамеру для записи (оценки двигательной активности мышей на 14-ой в 15-ой мин укачивания). Оценку двигательной активности (ДА) проводили в баллах: отсутствие активности - 1 балл, низкая активность - 2 балла, средняя активность - 3 балла, высокая активность - 4 балла.
Типичные результаты одного из опытов представлены в таблице.
Из данных таблицы следует, что реверсивное укачивание понижает двигательную активность (ДА) у контрольных мышей достоверно сильнее, чем у подопытных мышей, которым до укачивания ввели глутоксим. Средняя величина двигательной активности подопытных мышей была в 2,33 раза, т.е. на 133%, выше, чем у контрольных мышей (3,50:1,50=2,33). С повышением числа опытов достоверность различий возрастает.
Для достижения достаточного защитного эффекта против укачивания парентеральное введение окисленного глутатиона или фармацевтических композиций на его основе следует приводить за 1-24 ч перед укачивающим воздействием на организм и в дозе 0,1-10 мг окисленного глутатиона на 1 кг массы организма. Введение в организм более высоких доз окисленного глутатиона (свыше 10 мг/кг) не повышает защитного эффекта и поэтому нецелесообразно. При отклонениях от рекомендуемого диапазона времени предварительного введения в ту или другую сторону (или менее 1 ч, или более 48 ч), а также при отклонении от рекомендуемого диапазона вводимых доз в сторону уменьшения (менее 0,1 мг/кг) защитный эффект заметно уменьшается (более, чем на 25%).
Заявляемый способ может быть с успехом использован для повышения резистентности к укачиванию не только животных, но и человека. Введение окисленного глутатиона (внутримышечно, в дозе 0,1 мг на 1 кг массы человека, за 24 ч перед процедурой укачивания) в 2-3 раза повышает устойчивость человека к интенсивному укачиванию при заданных условиях эксперимента: первые признаки укачивания (тошнота и головокружение) наступают в 2-3 раза позже, чем без введения ему глутоксима.
По сравнению со способом-прототипом заявляемый способ более эффективен. В одинаковых условиях эксперимента заявляемый способ, где используется окисленный глутатион, позволяет повысить двигательную активность мышей на 133% (см. выше), тогда как способ-прототип, где используется скополамин, всего лишь на 40-92%.
Кроме того, по сравнению со способом-прототипом, где используется высокотоксичный скополамин (хранение по Списку А), в предлагаемом способе используется безвредный окисленный глутатион или фармацевтические композиции на его основе.
Повышение резистентности организма к укачиванию имеет большое значение прежде всего для обеспечения работоспособности экипажей в дорогостоящих и ответственных космических и авиационных полетах, а также различного вида плаваниях (надводных и подводных). Например, утрата работоспособности исполнителем полетного задания в космическом полете (из-за укачивания) может нанести экономический ущерб, оцениваемый сотнями тысяч долларов в час.
Источники информации
1. Машковский М. Д. Лекарственные средства. В 2-х томах. Т. 1. М.: Медицина, 1987. - 624 с.
2. Патент РФ (RU) 2089179 С1, Кл. МКИ: А 61 К 9/08, 1997 г. (Глутоксим).
3. Инструкция по медицинскому применению "Глутоксим Glutoxim, раствор глутоксима для инъекций"//Утверждено Фармакологическим государственным комитетом Минздрава России 01 июля 1999 года приказом 76.
4. Патент РФ (RU) 2144374 С1, Кл. МКИ: А 61 К 38/06, 1997 г. (Фармкомпозиции).
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОВЫШЕНИЯ УСТОЙЧИВОСТИ ОРГАНИЗМА К ПОВЫШЕННОМУ ДАВЛЕНИЮ ДЫХАТЕЛЬНОЙ ГАЗОВОЙ СРЕДЫ | 2002 |
|
RU2208452C1 |
| СПОСОБ ПОВЫШЕНИЯ РЕЗИСТЕНТНОСТИ ОРГАНИЗМА К ТЕПЛОВОМУ ВОЗДЕЙСТВИЮ | 2002 |
|
RU2206334C1 |
| СПОСОБ ПОВЫШЕНИЯ РЕЗИСТЕНТНОСТИ ОРГАНИЗМА К ГИПОТЕРМИЧЕСКОМУ ВОЗДЕЙСТВИЮ | 2002 |
|
RU2206335C1 |
| СПОСОБ НОРМАЛИЗАЦИИ СНА | 2002 |
|
RU2218933C2 |
| СПОСОБ ПОВЫШЕНИЯ ЭФФЕКТИВНОСТИ ВОСПРОИЗВОДСТВА ИКРЫ И ЧИСЛЕННОСТИ ОСЕТРООБРАЗНЫХ РЫБ | 2004 |
|
RU2262844C1 |
| Терапевтическая композиция и лекарственная форма на её основе | 2015 |
|
RU2629314C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ ЦИКЛОФЕРОНА МЕСТНОГО И НАРУЖНОГО ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ГНОЙНО-ДЕСТРУКТИВНЫХ ПОРАЖЕНИЙ СЛИЗИСТОЙ И КОЖИ, ОБЩЕСИСТЕМНЫХ ЗАБОЛЕВАНИЙ ПРИ ИММУНОДЕФИЦИТНЫХ СОСТОЯНИЯХ | 2008 |
|
RU2414221C2 |
| ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ ТИЛОРОНА МЕСТНОГО И НАРУЖНОГО ПРИМЕНЕНИЯ ДЛЯ ЛЕЧЕНИЯ ГНОЙНО-ДЕСТРУКТИВНЫХ ПОРАЖЕНИЙ СЛИЗИСТОЙ И КОЖИ, ОБЩЕСИСТЕМНЫХ ЗАБОЛЕВАНИЙ ПРИ ИММУНОДЕФИЦИТНЫХ СОСТОЯНИЯХ | 2008 |
|
RU2401104C2 |
| СПОСОБ ЛЕЧЕНИЯ РАЗЛИЧНЫХ ФОРМ ТУБЕРКУЛЕЗА ЛЕГКИХ, В ТОМ ЧИСЛЕ РЕЗИСТЕНТНЫХ К ПРОТИВОТУБЕРКУЛЕЗНОЙ ХИМИОТЕРАПИИ | 2001 |
|
RU2197984C1 |
| СПОСОБ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ УКАЧИВАНИЯ И СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ УКАЧИВАНИЯ (ВАРИАНТЫ) | 2019 |
|
RU2753952C2 |
Изобретение относится к медицине. Предложен способ повышения резистентности организма к укачиванию путем введения окисленного глутатиона. Способ обеспечивает эффективность воздействия при безвредности для организма. 1 з. п.ф-лы, 1 табл.
| СТИМУЛЯТОР ЭНДОГЕННОЙ ПРОДУКЦИИ ЦИТОКИНОВ И ГЕПОПОЭТИЧЕСКИХ ФАКТОРОВ И СПОСОБ ЕГО ИСПОЛЬЗОВАНИЯ | 1995 |
|
RU2089179C1 |
| EP 9605736, 11.12.1996 | |||
| МАШКОВСКИЙ М.Д | |||
| лекарственные средства | |||
| - М.: Медицина, 2001, т.1, с | |||
| Гидравлическая или пневматическая передача | 0 |
|
SU208A1 |
Авторы
Даты
2003-07-20—Публикация
2002-02-11—Подача