Изобретение относится к применению определенных солей моноалкиловых эфиров фумаровой кислоты индивидуально или в сочетании с диалкилфумаратом для получения микротаблеток в целях лечения псориатического артрита, нейродермита, псориаза и регионального энтерита (болезни Крона).
В европейской заявке ЕР-А-0188749 уже описаны производные фумаровой кислоты и содержащие их фармацевтические композиции для лечения псориаза. Из заявки DE-A-2530372 также известны фармацевтические композиции для лечения псориаза, которые содержат смесь фумаровой кислоты и других производных фумаровой кислоты. Доля свободной фумаровой кислоты в этих фармацевтических композициях является обязательной.
Далее, в заявке DE-A-2621214 описываются лекарственные средства для лечения псориаза, которые в качестве биологически активного вещества содержат моноэтиловый эфир фумаровой кислоты и его неорганические соли. Из публикации в Hautarzt, с.279-285 (1987) также известно применение солей кальция, цинка и магния моноэтилового эфира фумаровой кислоты, а также диметилового эфира фумаровой кислоты для лечения псориаза.
Наконец, в Европейском патенте ЕР 0312697 описываются фармацевтические композиции, которые содержат одно или несколько соединений, выбранных из солей кальция, магния, цинка и железа монометилового эфира фумаровой кислоты индивидуально или предпочтительно в смеси с (C1-C5)-алкилфумаратами. Препарат, описанный в примере 4 этого патента, содержит 87,5 мг моноэтилфумарата кальция, 120,0 мг диметилфумарата, 5,0 мг моноэтилфумарата магния и 3,0 мг моноэтилфумарата цинка, что соответствует 164 мг фумаровой кислоты. Препарат находится в форме устойчивых к действию желудочного сока таблеток и разрешен и выпускается в продажу в Германии под торговым названием фумадерм (Fumaderm®).
Уже во время фазы 3 клинических исследований и при последующем изучении маркетинга в отношении этого препарата установлено, что примерно 60% пациентов во время начальной фазы лечения с помощью фумадерма жалуются на нарушения в области желудочно-кишечного тракта в форме диареи, болей в желудке и присутствие чувства переполнения. В качестве другого побочного действия, кроме того, часто возникает так называемый прилив крови, а также расстройства зрения и чувство жара.
Хотя таблетки, как правило, относительно хорошо переносимы, однако, прежде всего в начале лечения всегда снова сталкиваются с указанными нарушениями. В процессе лечения часто снова появляются нежелательные побочные действия. Однако встречаются пациенты, у которых прием фумадерма вызывает тяжелые нарушения в области желудочно-кишечного тракта. Появляющиеся нарушения в области желудка и кишечника ухудшают соблюдение больным режима и схемы лечения и могут оказывать на пациентов отрицательное влияние до такой степени, что они являются отчасти причиной прекращения лечения.
Задачей настоящего изобретения является получение фармацевтической композиции, с помощью которой можно избежать указанных побочных действий, в особенности нарушений в области желудочно-кишечного тракта, при одновременном введении тех же самых, входящих в состав композиции фармацевтических веществ.
Исследования заявителя показали, что метилгидрофумарат, представляющий собой метаболит диметилфумарата, основной компонент препарата фумадерм, первоначально повышает стимулируемое эндотоксином выделение альфа-фактора некроза опухоли в человеческих мононуклеарных клетках периферической крови (periphere blood mononuclear cells=РВМС-клетки) и в изолированных моноцитах. При множественном повторном воздействии приходят к уменьшению повышения выделения альфа-фактора некроза опухоли, индуцируемого эндотоксином, следовательно, к эффекту привыкания.
Эта первоначальная индукция альфа-фактора некроза опухоли возможно ответственна за известное побочное действие препарата фумадерм, как нарушения в области желудочно-кишечного тракта или симптоматика прилива крови. Тенденция к уменьшению стимулируемого эндотоксином выделения альфа-фактора некроза опухоли после неоднократного воздействия метилгидрофумарата может быть объяснена эффектом привыкания, то есть уменьшением побочных действий при длительном лечении с помощью фумадерма. Соответственно этому целью дальнейших исследований являлось, прежде всего, ингибирование выделения альфа-фактора некроза опухоли с помощью других лекарственных средств и контролирование благодаря этому побочных действий при введении фумадерма.
Исследованиями неожиданно показано, что лекарственная форма биологически активных веществ в виде микротаблеток может значительно уменьшать нарушения в области желудочно-кишечного тракта. Поставленная задача решается согласно изобретению применением одной или нескольких солей моноалкиловых эфиров фумаровой кислоты общей формулы ,
,
в случае необходимости в смеси с диалкилфумаратом формулы ,
,
причем А означает двухвалентный катион из ряда Са, Мg, Zn или Fe или одновалентный катион из ряда Li, Na или К и n означает число 1 или 2 в зависимости от рода катиона и в случае необходимости обычных фармацевтических вспомогательных средств и носителей для получения фармацевтической композиции в форме микротаблеток или микропилюль для лечения псориатического артрита, нейродермита, псориаза и регионального энтерита Крона.
Величина или средний диаметр микропилюль или микротаблеток предпочтительно находится в пределах от 300 до 2000 мкм, в особенности в области от 500 до 1500 мкм и в наибольшей степени предпочтительно составляет 1000 мкм.
Микротаблетками или микропилюлями можно заполнять капсулы или пакетики и принимать в этой форме. Далее, сами микротаблетки или капсулы могут быть снабжены покрытием, устойчивым к действию желудочного сока. Это покрытие наносят обычными способами. В случае капсул речь может идти о твердых или мягких желатиновых капсулах.
Предпочтительные композиции согласно изобретению содержат кальциевую соль монометилового эфира фумаровой кислоты и/или кальциевую соль моноэтилового эфира фумаровой кислоты, в случае необходимости в смеси с диметилфумаратом. Общая масса биологически активных веществ при этом составляет 10-300 мг. Композиция в форме микротаблеток предпочтительно содержит 10-290 мас. частей моноалкилового эфира фумаровой кислоты (кальциевой соли) и 290-10 мас. частей диметилфумарата. Согласно другому варианту осуществления изобретения эта композиция, кроме того, может содержать 1-50 мас. частей цинковой соли моноалкилового эфира фумаровой кислоты.
Другая предпочтительная композиция в форме микротаблеток содержит 1-250 мас. частей моноалкилового эфира фумаровой кислоты (кальциевой соли), 250-10 мас. частей диметилфумарата, 1-50 мас. частей моноалкилового эфира фумаровой кислоты (магниевой соли) и 1-50 мас. частей моноалкилового эфира фумаровой кислоты (цинковой соли), причем общая масса биологически активных веществ составляет 30-300 мг.
Для системного начала лечения, а также, наоборот, для окончания лечения (постепенно снижающаяся дозировка) предпочтительна низкая дозировка. Она может состоять из 30 мг диметилфумарата, 20 мг моноэтилфумарата кальция и 3 мг моноэтилфумарата или монометилфумарата цинка. Для терапевтической дозировки после начальной фазы можно использовать, например, дозировку из 20 мг диметилфумарата, 87 мг моноэтилфумарата кальция и 3,0 мг моноэтилфумарата или монометилфумарата цинка.
Используемые согласно изобретению производные фумаровой кислоты получают, например, согласно способам, описанным в Европейском патенте ЕР 0312697.
Не вдаваясь в теоретические рассуждения, предполагают, что нарушения в области желудочно-кишечного тракта могут быть вызваны локальными раздражениями в эпителиальных клетках кишечника, которые индуцируют выделение альфа-фактора некроза опухоли. Вероятно, при приеме обычных таблеток входящие в состав таблетки вещества локально высвобождаются в кишечнике в слишком высокой концентрации, вследствие чего возникает местное раздражение слизистой оболочки кишечника. Из-за этого локального раздражения за короткий срок высвобождаются очень высокие концентрации альфа-фактора некроза опухоли, которые могут быть ответственны за желудочно-кишечные побочные действия. При введении устойчивых к действию желудочного сока микротаблеток в капсулах, по сравнению с этим, достигаются локально низкие концентрации биологически активных веществ в эпителиальных клетках кишечника. Микротаблетки из желудка постепенно, за счет перистальтики желудка, попадают в тонкий кишечник и тем самым происходит лучшее распределение биологически активных веществ.
Устойчивые к действию желудочного сока микротаблетки одинаковой дозировки, следовательно, распределяются уже в желудке и поэтому уже порциями попадают в кишечник, где биологически активные вещества высвобождаются в меньших дозах. Таким образом избегают локального раздражения эпителиальных клеток кишечника, так же как высвобождения альфа-фактора некроза опухоли. Отсюда, вероятно, следует лучшая переносимость микротаблеток желудком и кишечником по сравнению с обычными таблетками. Однако нельзя было ожидать, что лишь изменение галеновой формы препарата приведет к такого рода резкому уменьшению побочных действий.
Получение и принцип действия предлагаемых согласно изобретению микротаблеток поясняются с помощью следующих примеров.
Примеры получения
ПРИМЕР 1. Получение устойчивых к действию желудочного сока микротаблеток в капсулах, содержащих 87,0 мг моноэтилфумарата кальция, 120,0 мг диметилфумарата, 5,0 мг моноэтилфумарата магния и 3,0 мг моноэтилфумарата цинка, что соответствует, в целом, 164 мг фумаровой кислоты.
8,700 кг моноэтилфумарата кальция, 12,000 кг диметилфумарата, 0,500 кг моноэтилфумарата магния и 0,30 кг моноэтилфумарата цинка размельчают, интенсивно перемешивают и при соответствующих мерах предосторожности (дыхательная маска, перчатки, защитная одежда и т.д.) гомогенизируют с помощью сита 800. Готовят смесь вспомогательных веществ следующего состава: 18,00 кг производного крахмала (STA-RX® 1500), 0,30 кг микрокристаллической целлюлозы (Avicel® PH 101), 0,75 кг поливинилпирролидона (Kollidon® 120), 4,00 кг Primogel®, 0,25 кг коллоидальной кремневой кислоты (Aerosil®). Порошкообразную смесь смешивают со смесью биологически активных веществ, гомогенизируют с помощью сита 200, при использовании 2%-ного водного раствора поливинилпирролидона (Kollidon® K25) обычным образом перерабатывают в гранулят связующего и в высушенном состоянии смешивают с внешней фазой, которая состоит из 0,50 кг стеарата магния и 1,50 кг талька. Порошкообразную смесь затем обычным образом прессуют с получением выпуклых микротаблеток брутто-массой 10,0 мг и диаметром 2,0 мм. Вместо этих классических способов таблети-рования также можно использовать другие способы получения таблеток, как прямое таблетирование, а также получение твердых дисперсий способом плавления и способом распылительной сушки.
Устойчивое к действию желудочного сока покрытие можно наносить в классическом дражировочном котле путем напыления или при использовании вакуума, а также в аппаратуре с псевдоожиженным слоем. Для достижения устойчивости к действию желудочного сока в этом случае готовят, например, порционно раствор 2,250 кг гидроксипропилметилцеллюлозофталата (НРМСР, Pharmacoat® HP 50) в смеси следующих растворителей: 13,00 л ацетона, 13,50 л этанола (96%-ного денатурированного с помощью 2% кетона) и 1,50 л деминерализованной воды. К готовому раствору в качестве пластификатора добавляют 0,240 кг касторового масла и обычным образом порциями наносят на ядра таблеток.
По окончании высушивания затем в той же самой аппаратуре в качестве пленочного покрытия наносят суспензию следующего состава: 0,340 кг талька, 0,400 кг оксида титана(VI) Cronus RN 56, 0,324 кг красного лака Farblack L 86837, 4,800 кг 12,5%-ного эудражит Е (Eudragit E) и 0,120 кг полиэтиленгликоля 6000 (рН. 11 XI) в смеси растворителей следующего состава: 8,170 кг пропан-2-ола, 0,200 кг деминерализованной воды и 0,600 кг глицеринтриацетата (триацетин).
Устойчивые к действию желудочного сока микротаблетки затем вносят в разъемные твердые желатиновые капсулы в количестве до 500,0 мг массы нетто и закрывают.
ПРИМЕР 2. Получение устойчивых к действию желудочного сока микротаблеток в капсулах, содержащих 87,0 мг моноэтилфумарата кальция, 120 мг диметилфумарата, 5,0 мг моноэтилфумарата магния и 3,0 мг моноэтилфумарата цинка, что соответствует в целом 164 мг фумаровой кислоты.
8,700 кг моноэтилфумарата кальция, 12,000 кг диметилфумарата, 0,500 кг моноэтилфумарата магния и 0,30 кг моноэтилфумарата цинка размельчают, интенсивно перемешивают и при соответствующих мерах предосторожности (дыхательная маска, перчатки, защитная одежда и т.д.) гомогенизируют с помощью сита 800. Готовят смесь вспомогательных веществ следующего состава: 24,70 кг микрокристаллической целлюлозы (Avicel® PH 200), 3,00 кг натрийкроскармелозы (AC-Di-SOL-SD-711), 2,50 кг талька, 0,10 кг безводного диоксида кремния (Aerosil® 200) и 1,00 кг стеарата магния. Всю смесь вспомогательных веществ смешивают со смесью биологически активных веществ и перемешивают до получения гомогенной смеси. Порошкообразную смесь затем путем прямого таблетирования прессуют с получением выпуклых микротаблеток брутто-массой 10,0 мг и диаметром 2,0 мм. Вместо этих классических способов таблетирования также можно использовать другие способы получения таблеток, как получение твердых дисперсий способом плавления и способом распылительной сушки или таблетирование гранулятов связующих.
Устойчивое к действию желудочного сока покрытие можно наносить в классическом дражировочном котле путем напыления или при использовании вакуума, а также в аппаратуре с псевдоожиженным слоем. В этом случае, например, готовят раствор 0,94 г эудражит L (Eudragit® L) в изопропаноле, который дополнительно содержит 0,07 кг дибутилфталата. Этот раствор наносят путем опрыскивания ядер таблеток.
Затем готовят дисперсию из 17,32 кг эудражита (Eudragit® L D-55) и смеси 2,80 кг микроталька, 2,00 кг макрогеля 6000 и 0,07 кг диметикана в воде и наносят путем напыления на ядра.
Устойчивые к действию желудочного сока микротаблетки затем вносят в разъемные твердые желатиновые капсулы в количестве до 760,0 мг массы нетто и закрывают.
Примеры лечения
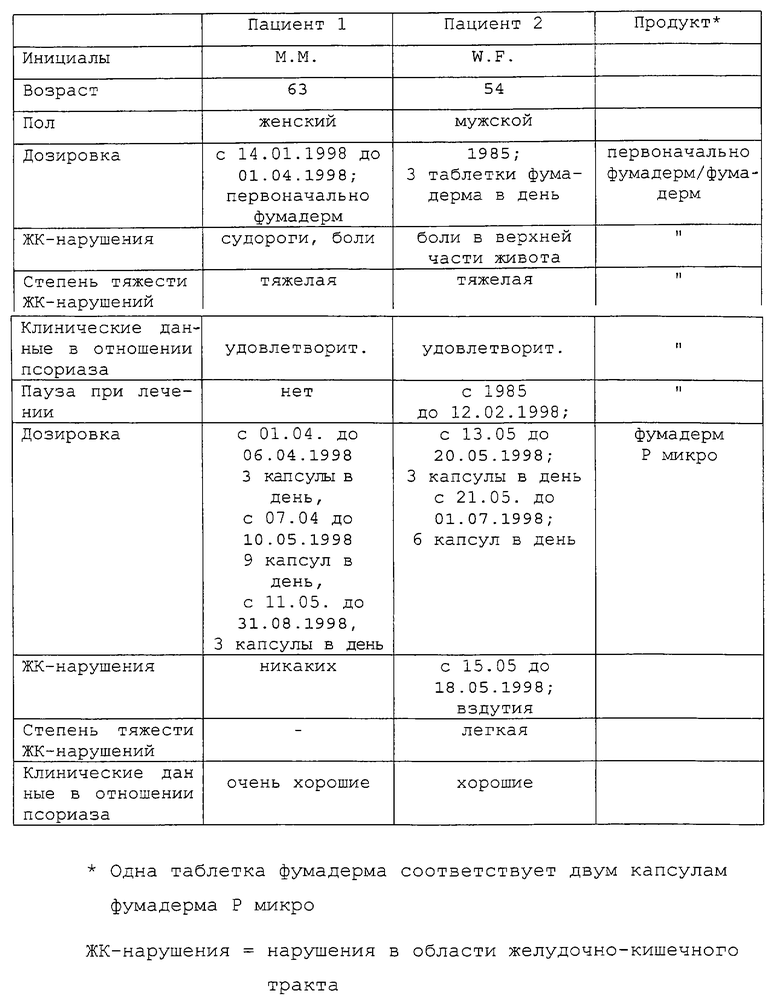
Согласно вышеприведенным примерам приготовили микротаблетки, содержащие те же самые 4 биологически активных вещества в таком же количественном составе, которые содержатся в торговом продукте фумадерм (Fumaderm®). Устойчивая к действию желудочного сока таблетка фумадерма соответствует примерно 102 устойчивым к действию желудочного сока микротаблеткам такого же состава. Для практического использования этими микротаблетками заполняют капсулы, как описано в вышеприведенных примерах. Две капсулы соответствуют одной таблетке фумадерма.
Для лучшего сравнения двух пациентов, которые страдали тяжелыми нарушениями в области желудочно-кишечного тракта при лечении таблетками фумадерма, лечили с помощью устойчивых к действию желудочного сока микротаблеток согласно настоящему изобретению. Эти пациенты после приема микротаблеток неожиданно больше не страдали нарушениями в области желудочно-кишечного тракта, наблюдаемыми при приеме обычной таблетки. Улучшения состояния в отношении псориаза достигали, как при лечении с помощью таблеток фумадерма, известных из уровня техники, при этом, смотря по обстоятельствам, для достижения клинического успеха достаточна меньшая доза при приеме в виде микротаблеток.
Результаты лечения представлены в таблице.
Из таблицы видно, что прием микротаблеток даже в повышенной дозе (9 капсул ежедневно) не вызывает никаких побочных действий или имеет следствием только незначительные побочные действия, в то время как уже более низкая дозировка торгового препарата фумадерм приводит к тяжелым нарушениям в области желудочно-кишечного тракта.
Из результатов лечения также видно, что микротаблетки в отношении своей эффективности для лечения псориаза по крайней мере идентичны торговому препарату, если не обладают улучшенным действием. Поэтому в целом предлагаемая согласно изобретению лекарственная форма производных фумаровой кислоты в виде микротаблеток показывает отчетливое улучшение по сравнению с лечением с помощью обычных таблеток.
Предложено: микротаблетки на основе алкиловых эфиров фумаровой кислоты общей формулы (1) или (2) для лечения псориатического артрита, нейродермита, псориаза и регионального энтерита Крона. Изобретение позволяет резко снизить побочные действия традиционных таблеток с заявленным активным ингредиентом в отношении желудочно-кишечного тракта и расширяет арсенал средств указанного назначения. 9 з.п.ф-лы, 1 табл.

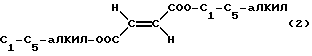
причем А означает двухвалентный катион, n=1 или 2.
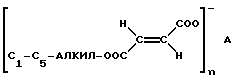
в случае необходимости, в смеси с диалкилфумкратом формулы
где А означает двухвалентный катион из ряда Са, Mg, Zn или Fe или одновалентный катион из ряда Li, Na или К;
n означает число 1 или 2 в зависимости от рода катиона,
в качестве биологически активных веществ в количестве 10-300 мг и фармацевтические вспомогательные вещества.
| US 4851439, 25.07.1989 | |||
| US 4959389, 25.09.1990 | |||
| ПЛАНЕТАРНАЯ КОРОБКА ПЕРЕДАЧ 5R2 | 2016 |
|
RU2621214C1 |
| DE 3834794, 19.04.1990 | |||
| Кузнечная нефтяная печь с форсункой | 1917 |
|
SU1987A1 |
| ПРОИЗВОДНЫЕ БЕНЗОЛАЛКАНОВОЙ КИСЛОТЫ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2110512C1 |
| US 4797287, 10.01.1989. | |||
Авторы
Даты
2003-08-20—Публикация
1999-10-08—Подача