Текст описания в факсимильном виде (см. графическую часть) Тк

































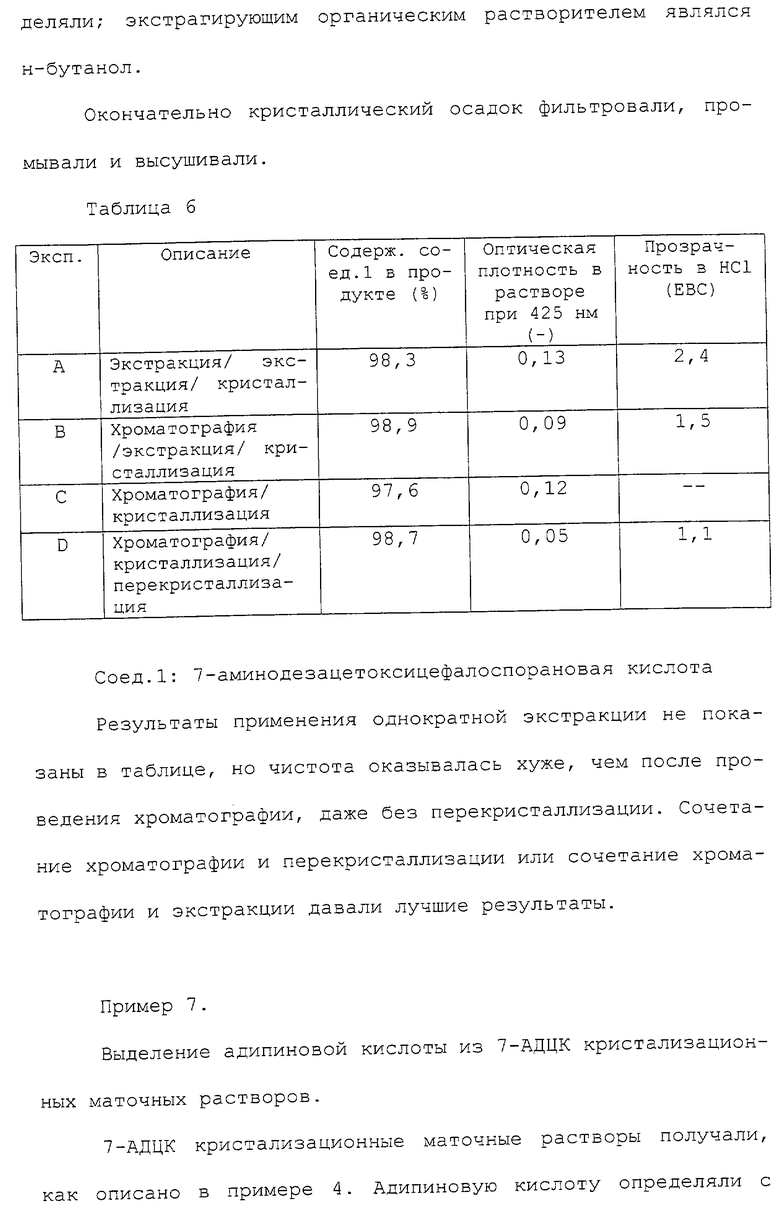

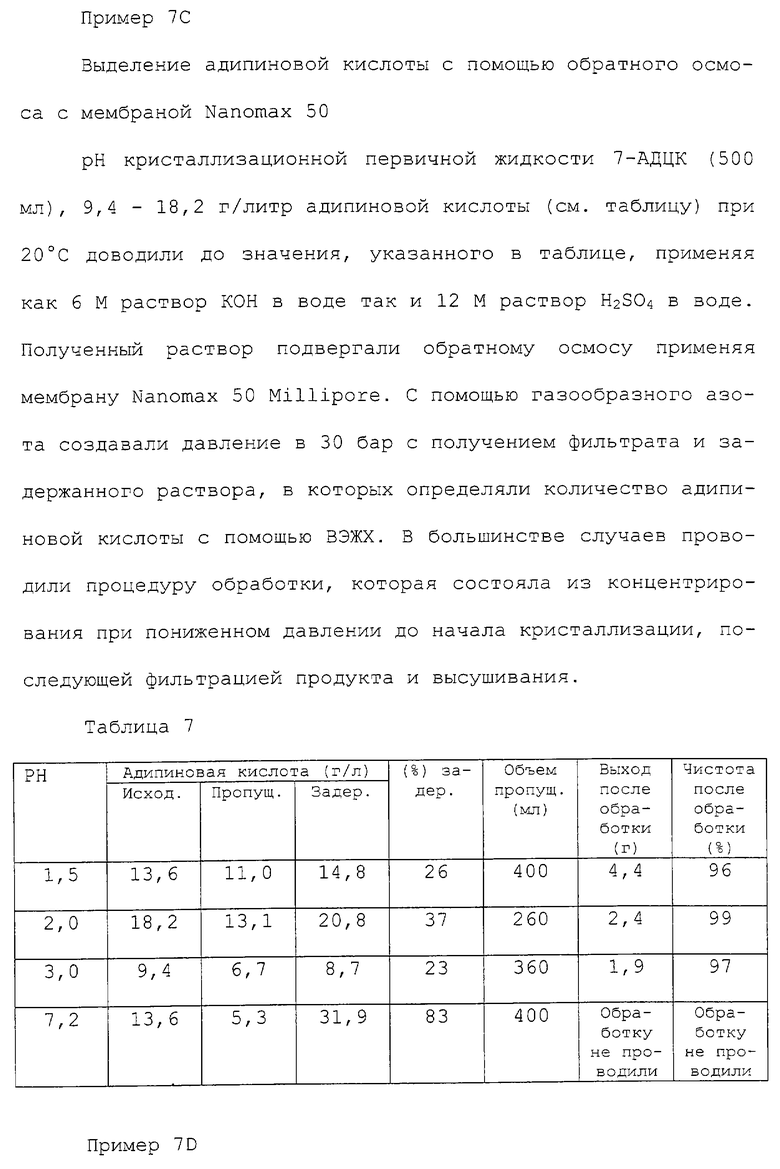

Изобретение относится к новому способу ферментативного получения цефалоспорина общей формулы (I), где R0 представляет собой водород или C1-3 алкокси; Y представляет собой СН2, кислород, серу или окисленную форму серы; R1 представляет собой любую из групп, выбранных из группы, включающей водород, гидрокси, галоген, насыщенный или ненасыщенный, прямой или разветвленный алкил (1-5 атомов углерода; необязательно замененных одним или несколькими гетероатомами), необязательно замещенный гидрокси, галогеном, арилом, алкокси (1-3 атома углерода) или ацилом; и т.д., и R2 выбран из группы, включающей адипил (1,4-дикарбоксибутан), сукцинил, глутарил, пимелил, суберил, 2-(карбоксиэтилтио)ацетил, 3-(карбоксиэтилтио)пропионил, высшие алкиловые насыщенные и высшие алкиловые ненасыщенные дикарбоновые кислоты, из сложной смеси, содержащей, помимо соединения общей формулы (I), 6-аминопенициллановую кислоту (6-АПК) и необязательно одно или несколько N-замещенных β-лактамовых соединений, включающий стадии: (а) подкисления сложной смеси до значения рН ниже 6,5 и выдерживания смеси при рН ниже указанного значения при температуре между 10oС и 150oС; и/или (б) необязательного взаимодействия сложной смеси с источником диоксида углерода; и (в) выделения из смеси, образуемой после стадий (а) и/или (б), производного цефалоспорановой кислоты формулы (I). Предложен также способ получения соединения формулы (II), где R0 представляет собой водород или C1-3 алкокси; Y представляет собой СН2, кислород, серу или окисленную форму серы; R1 представляет собой любую из групп, выбранных из группы, включающей водород, гидрокси, галоген, насыщенный или ненасыщенный, прямой или разветвленный алкил (1-5 атомов углерода; необязательно замененных одним или несколькими гетероатомами), необязательно замещенный гидрокси, галогеном, арилом, алкокси (1-3 атомов углерода) или ацилом; и т.д., включающий стадии выделения соединения формулы (I), где R0, Y и R1 имеют значения, указанные выше; и R2 выбран из группы, включающей адипил (1,4-дикарбоксибутан), сукцинил, глутарил, пимелил, суберил, 2-(карбоксиэтилтио)ацетил, 3-(карбоксиэтилтио)пропионил, высшие алкиловые насыщенные и высшие алкиловые ненасыщенные дикарбоновые кислоты, из сложной смеси, содержащей, помимо соединения общей формулы (I), 6-аминопенициллановую кислоту (6-АПК) и необязательно одно или несколько N-замещенных β-лактамовых соединений, путем: (а) подкисления сложной смеси до значения рН ниже 6,5 и выдерживания смеси при рН ниже указанного значения при температуре между 10oС и 150oС; и/или (б) необязательного взаимодействия сложной смеси с источником диоксида углерода; и (в) выделения из смеси, образуемой после стадий (а) и/или (б), производного цефалоспорановой кислоты формулы (I); (г) деацилирования соединения формулы (I) с получением конверсионного раствора, содержащего соединение формулы (II), и (е) выделения соединения (II) из раствора. Технический результат - новый способ получения цефалоспорина. 2 с. и 16 з.п.ф-лы, 14 табл.
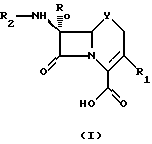

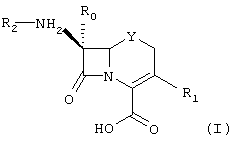
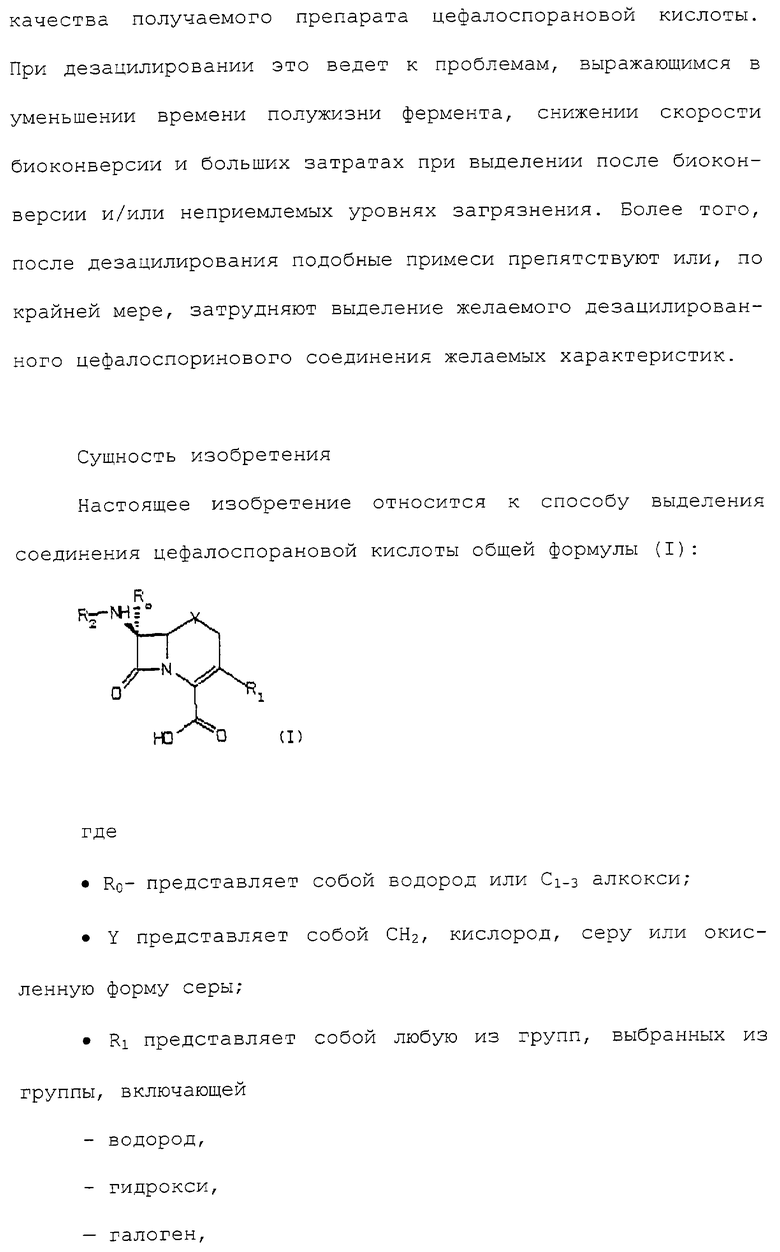
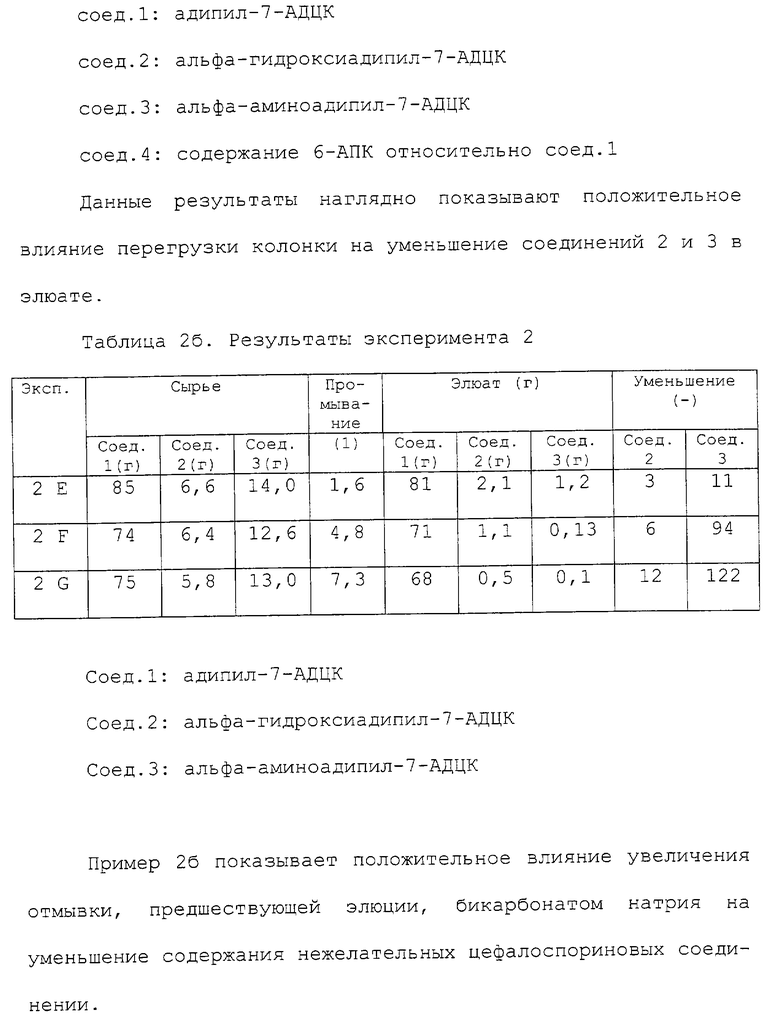
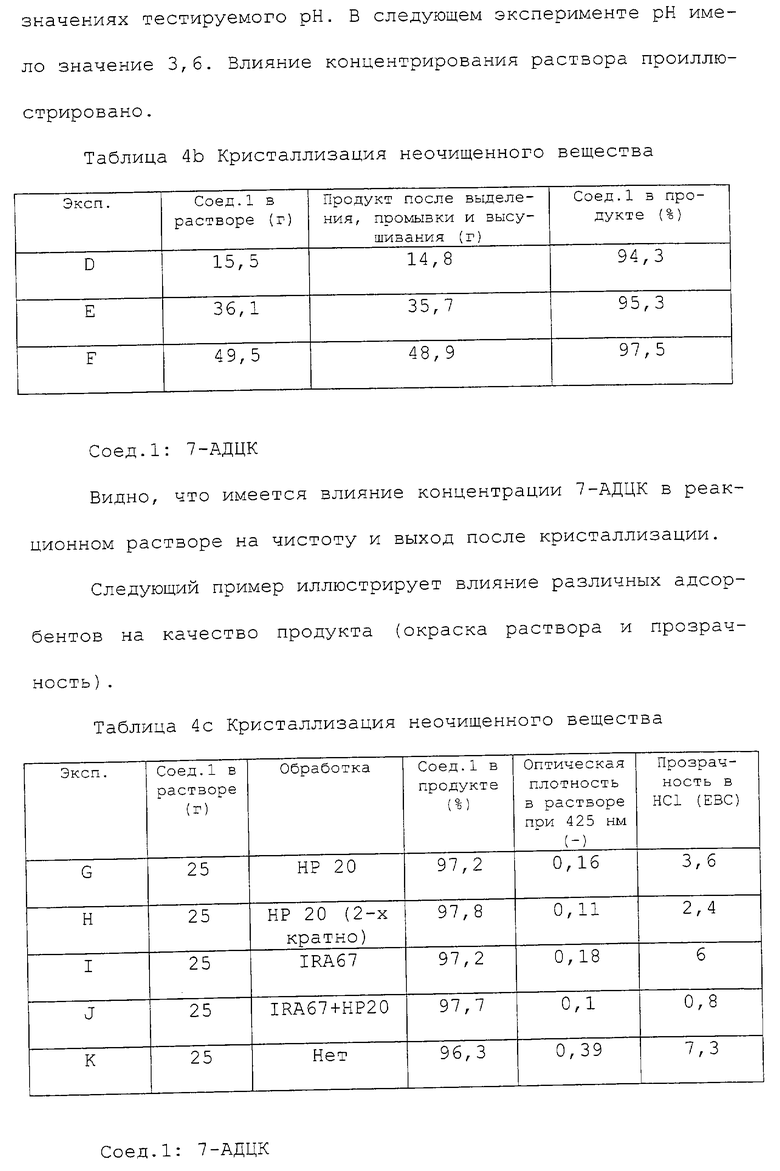
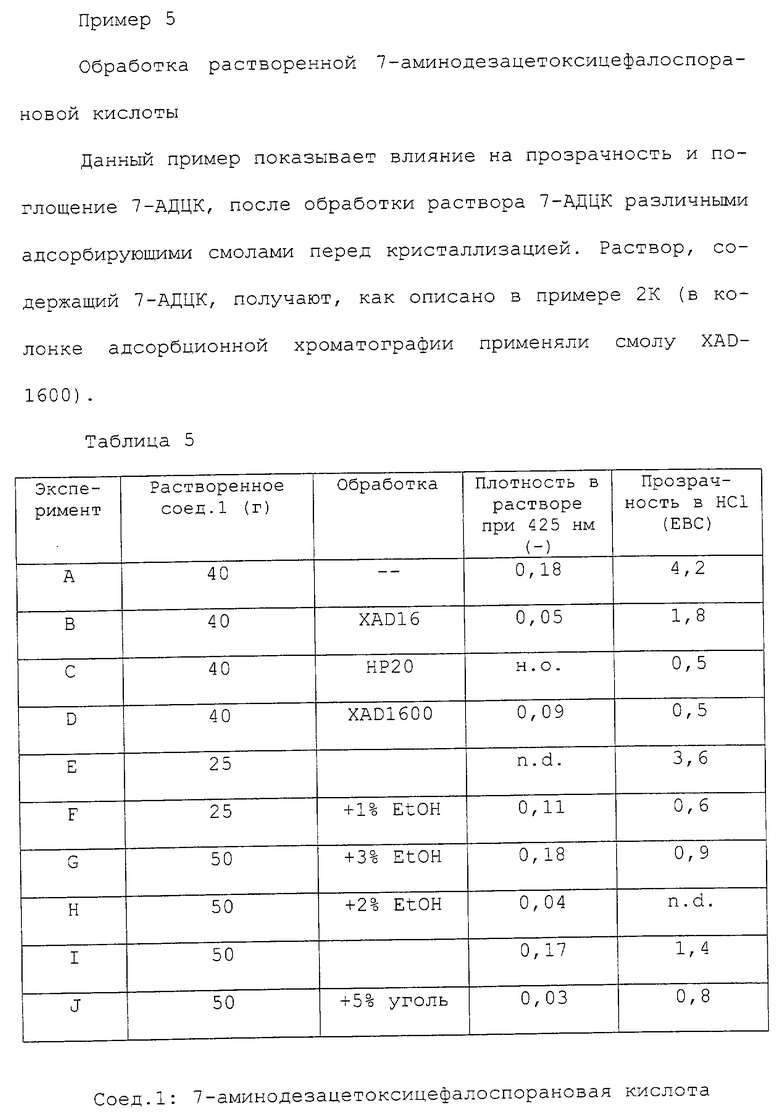
где R0 - водород или C1-3 алкокси;
Y - СН2, кислород, сера или окисленная форма серы;
R1 представляет собой любую из групп, выбранных из группы, включающей водород, гидрокси, галоген, насыщенный или ненасыщенный, прямой или разветвленный алкил (1-5 атомов углерода. необязательно замененных одним или несколькими гетероатомами), необязательно замещенный гидрокси, галогеном, арилом, алкокси (1-3 атома углерода) или ацилом; алкокси (1-3 атома углерода; необязательно замененных одним или несколькими гетероатомами), необязательно замещенный гидрокси или галогеном, или циклоалкил (3-8 атомов углерода), необязательно замещенный гидрокси, галогеном или амино; арил; гетероарил;
R2 выбран из группы, включающей адипил (1,4-дикарбоксибутан), сукцинил, глутарил, пимелил, суберил, 2-(карбоксиэтилтио)ацетил, 3-(карбоксиэтилтио)пропионил, высшие алкиловые насыщенные и высшие алкиловые ненасыщенные дикарбоновые кислоты, из сложной смеси, содержащей, помимо соединения общей формулы (I) 6-аминопенициллановую кислоту (6-АПК) и необязательно одно или несколько N-замещенных β-лактамовых соединений,
включающий стадии (а) подкисления сложной смеси до значения рН ниже 6,5 и выдерживания смеси при рН ниже указанного значения при 10 - 150°С и/или (б) необязательного взаимодействия сложной смеси с источником диоксида углерода и (в) выделения из смеси, образуемой после стадий (а) и/или (б), производного цефалоспорановой кислоты формулы (I).

где R0 - водород или C1-3 алкокси;
Y представляет собой СН2, кислород, серу или окисленную форму серы;
R1 представляет собой любую из групп, выбранных из группы, включающей водород, гидрокси, галоген, насыщенный или ненасыщенный, прямой или разветвленный алкил (1-5 атомов углерода. необязательно замененных одним или несколькими гетероатомами), необязательно замещенный гидрокси, галогеном, арилом, алкокси (1-3 атомов углерода) или ацилом, алкокси (1-3 атомов углерода, необязательно замененных одним или несколькими гетероатомами), необязательно замещенный гидрокси или галогеном, или циклоалкил (3-8 атомов углерода), необязательно замещенный гидрокси, галогеном или амино, арил, гетероарил, включающий стадии выделения соединения формулы (I)

где R0, Y и R1 имеют значения, указанные выше;
R2 выбран из группы, включающей адипил (1,4-дикарбоксибутан), сукцинил, глутарил, пимелил, суберил, 2-(карбоксиэтилтио)ацетил, 3-(карбоксиэтилтио)пропионил, высшие алкиловые насыщенные и высшие алкиловые ненасыщенные дикарбоновые кислоты, из сложной смеси, содержащей помимо соединения общей формулы (I) 6-аминопенициллановую кислоту (6-АПК) и необязательно одно или несколько N-замещенных β-лактамовых соединений, путем (а) подкисления сложной смеси до значения рН ниже 6,5 и выдерживания смеси при рН ниже указанного значения при 10 - 150°С и/или (б) необязательного взаимодействия сложной смеси с источником диоксида углерода и (в) выделения из смеси, образуемой после стадий (а) и/или (б), производного цефалоспорановой кислоты формулы (I); (г) деацилирования соединения формулы (I) с получением конверсионного раствора, содержащего соединение формулы (II), и (е) выделения соединения (II) из раствора.
| Привод к центробежному сепаратору | 1976 |
|
SU599854A1 |
| Способ силосования грубых кормов | 1978 |
|
SU810196A1 |
| Приспособление в пере для письма с целью увеличения на нем запаса чернил и уменьшения скорости их высыхания | 1917 |
|
SU96A1 |
| Способ выделения фермента, катализирующего превращение креатинина в креатин и фермента, катализирующего превращение креатина в саркозин и мочевину | 1972 |
|
SU532341A3 |
| СПОСОБ ФЕРМЕНТАТИВНОГО ПОЛУЧЕНИЯ ЦЕФАЛОСПОРИНА С | 1992 |
|
RU2094463C1 |
Авторы
Даты
2003-12-20—Публикация
1999-03-26—Подача