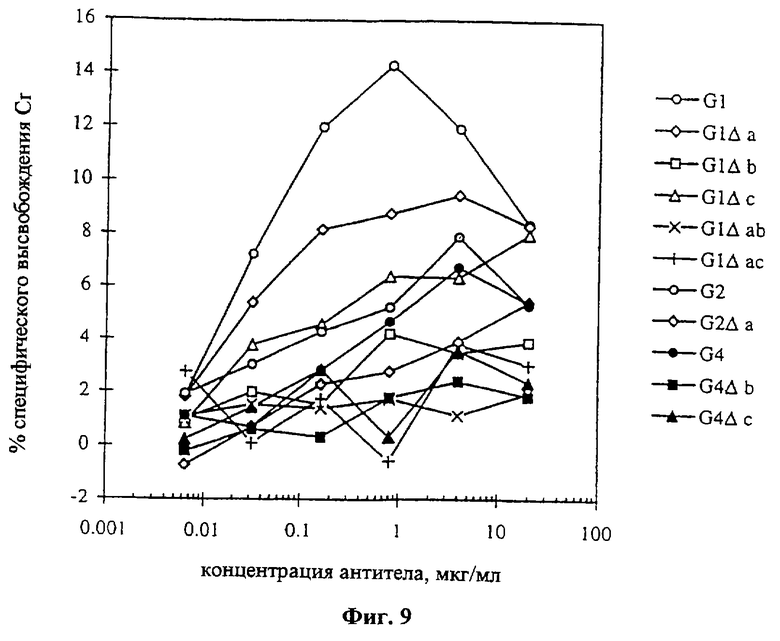
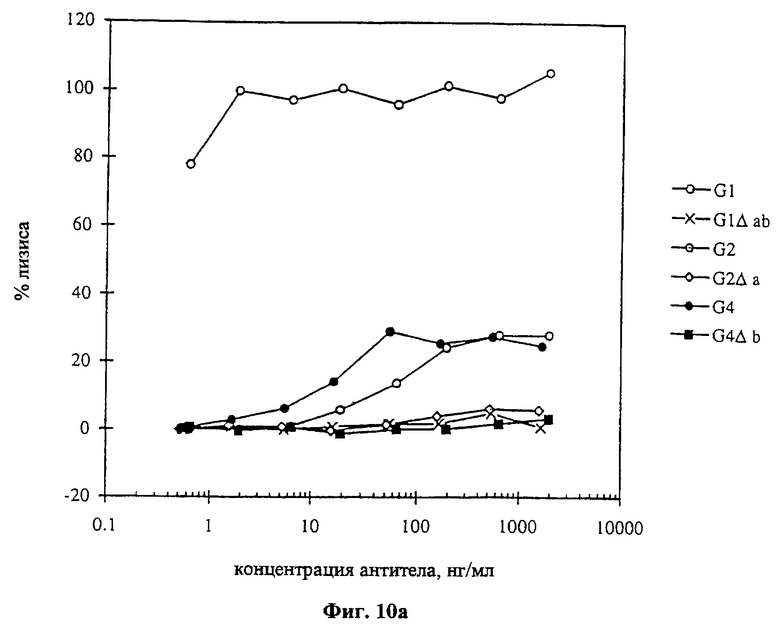
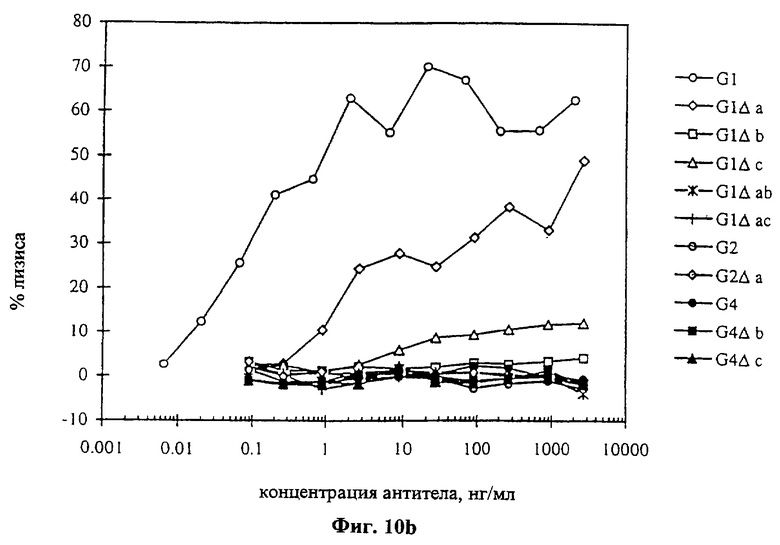
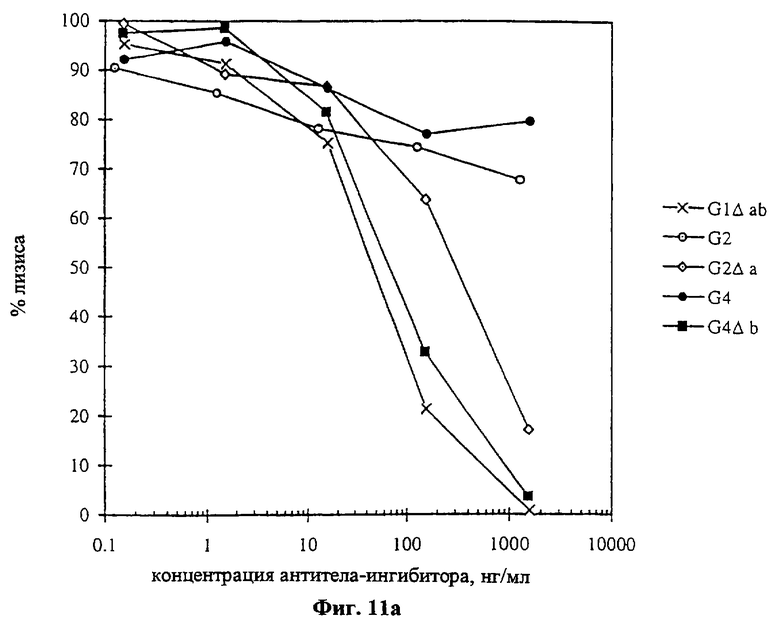
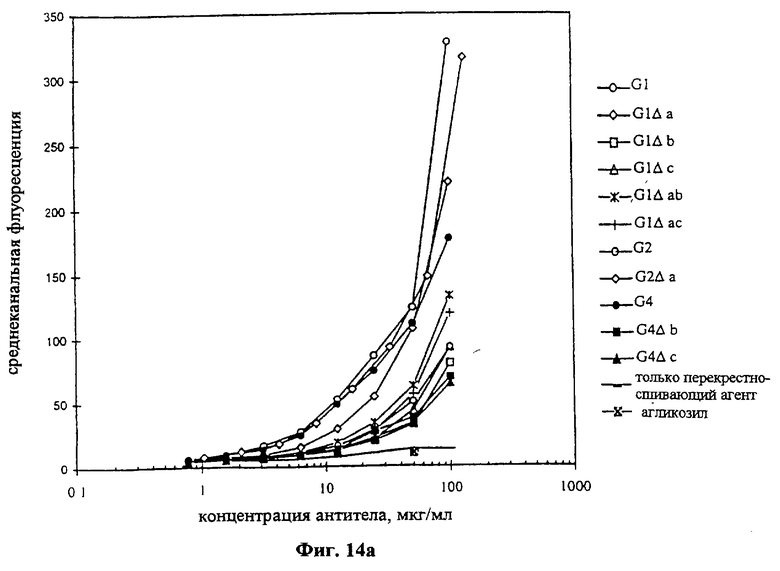
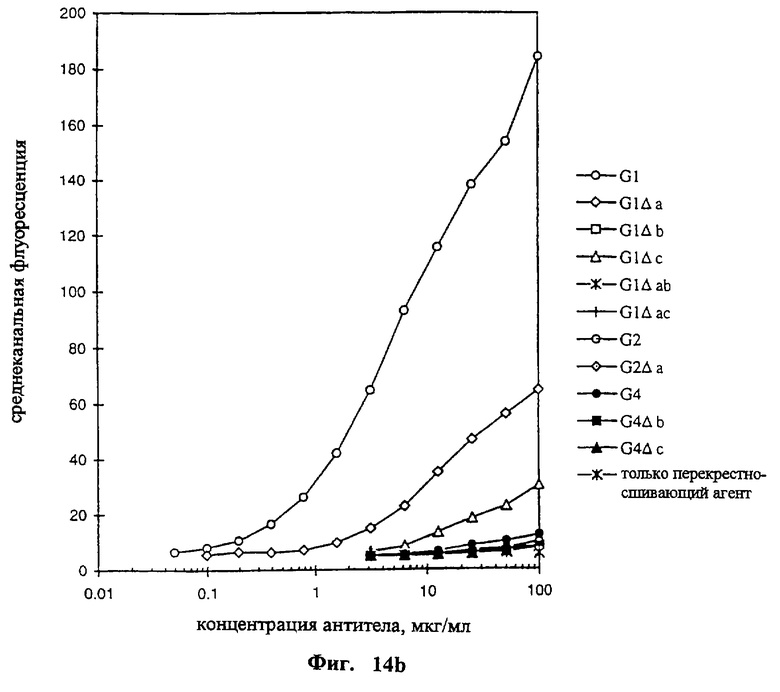
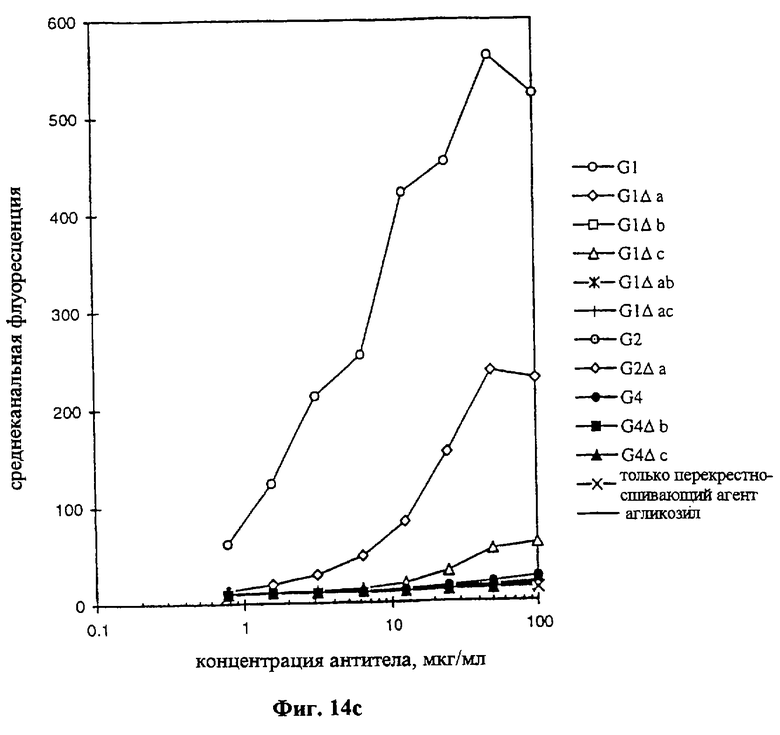
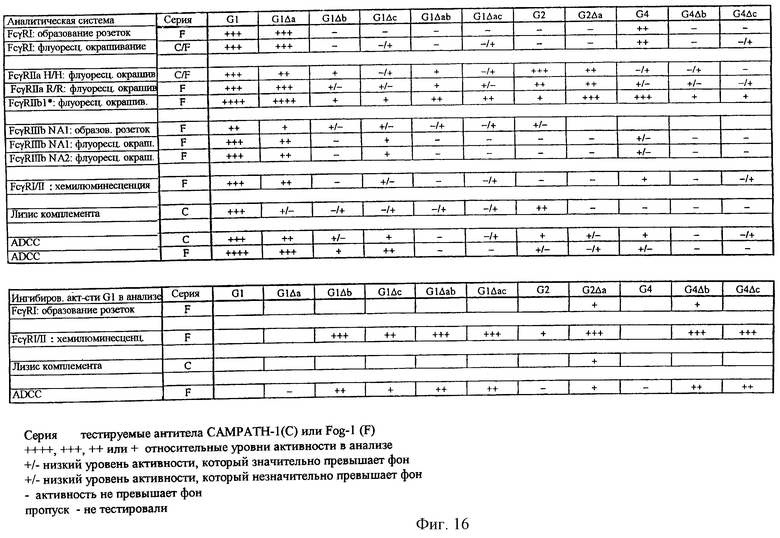
Текст описания в факсимильном виде (см. графическую часть).
Изобретение относится к группе новых соединений, являющихся связывающей молекулой, которая представляет собой рекомбинантное полипептидное антитело или адгезионную молекулу, включающую: (i) связывающий домен, способный связываться с молекулой-мишенью, и (ii) эффекторный домен, имеющий аминокислотную последовательность, в основном гомологичную всему константному домену тяжелой цепи иммуноглобулина человека или его части; где связывающая молекула способна связываться с молекулой-мишенью, не стимулируя при этом значительного комплементзависимого лизиса или клеточно-опосредованной деструкции мишени, и отличающаяся тем, что эффекторный домен обладает способностью специфически связываться с FcRn и/или FcγRIIb и представляет собой химерный домен, который происходит от доменов СН2 тяжелой цепи двух или более иммуноглобулинов человека, причем иммуноглобулины человека выбраны из IgGl, IgG2 и IgG4, и где химерный домен представляет собой домен СН2 тяжелой цепи иммуноглобулинов человека, который имеет следующие блоки аминокислот в заявленных положениях: 233Р, 234V, 235A, 236G, 327G, 330S и 331S в соответствии с системой нумерации EU и может являться, по меньшей мере, на 98% идентичным последовательности СН2 (остатки 231-340) из IgG1, IgG2 человека, имеющих указанные модифицированные аминокислоты; а также к выделенной нуклеиновой кислоте, содержащей нуклеотидную последовательность, кодирующую эффекторный домен связывающей молекулы; реплицируемому вирусу, содержащему эту аминокислоту; способу получения связывающей молекулы; способу связывания молекулы-мишени и фармацевтическому препарату, содержащему связывающую молекулу. 8 с. 16 з.п. ф-лы, 22 ил.
1. Связывающая молекула, которая представляет собой рекомбинантное полипептидное антитело или адгезионную молекулу, включающую (i) связывающий домен, способный связываться с молекулой-мишенью, и (ii) эффекторный домен, имеющий аминокислотную последовательность, в основном гомологичную всему константному домену тяжелой цепи иммуноглобулина человека или его части; где связывающая молекула способна связываться с молекулой-мишенью, не стимулируя при этом значительного комплементзависимого лизиса или клеточно-опосредованной деструкции мишени, отличающаяся тем, что эффекторный домен обладает способностью специфически связываться с FcRn и/или FcγRIIb и представляет собой химерный домен, который происходит от доменов СН2 тяжелой цепи двух или более иммуноглобулинов человека, причем иммуноглобулины человека выбраны из IgGl, IgG2 и IgG4, и где химерный домен представляет собой доменов СН2 тяжелой цепи иммуноглобулинов человека, который имеет следующие блоки аминокислот в заявленных положениях: 233Р, 234V, 235A и 236G и 327G, 330S и 331S в соответствии с системой нумерации EU.2. Связывающая молекула по п.1, в которой эффекторный домен выбран из G1Δac или G4Δc, как показано на фиг.17, необязательно включающий дополнительные модификации для придачи молекуле, по существу, нулевой аллотипии.3. Связывающая молекула по п.2, в которой эффекторный домен выбран из G1Δac или G4Δc, как показано на фиг.17.4. Связывающая молекула, которая представляет собой рекомбинантное полипептидное антитело или адгезионную молекулу, включающую (i) связывающий домен, способный связываться с молекулой-мишенью, и (ii) эффекторный домен, имеющий аминокислотную последовательность, в основном гомологичную всему константному домену тяжелой цепи иммуноглобулина человека или его части; где связывающая молекула способна связываться с молекулой-мишенью, не стимулируя при этом значительного комплементзависимого лизиса или клеточно-опосредованной деструкции мишени, и отличающаяся тем, что эффекторный домен обладает способностью специфически связываться с FcRn и/или FcγRIIb и
представляет собой химерный домен, который происходит от доменов СН2 тяжелой цепи двух или более иммуноглобулинов человека, причем иммуноглобулины человека выбраны из IgG1, IgG2 и IgG4, и где химерный домен представляет собой домен СН2 тяжелой цепи иммуноглобулинов человека, который имеет следующие блоки аминокислот в заявленных положениях: 233Р, 234V, 235A и в положении 236 аминокислота отсутствует, 327G, 330S и 331S в соответствии с системой нумерации EU, и является по меньшей мере на 98% идентичным последовательности СН2 (остатки 231-340) из IgG1 или IgG2 человека, имеющей указанные модифицированные аминокислоты.
5. Связывающая молекула по п.4, в которой эффекторный домен выбран из G1Δab или G2Δa, как показано на фиг.17, необязательно включающий дополнительные модификации для придачи молекуле, по существу, нулевой аллотипии.6. Связывающая молекула по п.5, в которой эффекторный домен выбран из G1Δab или G2Δa.7. Связывающая молекула по любому из предыдущих пунктов, в которой эффекторный домен происходит от первого домена СН2 тяжелой цепи иммуноглобулина человека, в котором по меньшей мере 1 аминокислота по меньшей мере в 1 области домена СН2 была модифицирована в соответствующую аминокислоту из второго, отличного домена СН2 тяжелой цепи иммуноглобулина человека, и в котором эффекторный домен имеет сниженный аффинитет к FcγRI, FcγRIIa или FcγRIII и сниженную способность опосредовать комплемент-зависимый лизис по сравнению с первым или вторым доменом СН2 тяжелой цепи иммуноглобулина человека.8. Связывающая молекула по п.7, где указанный эффекторный домен сохраняет аффинность по отношению к FcγRIIb.9. Связывающая молекула по любому из предыдущих пунктов, где указанный связывающий домен происходит от другого источника, отличающегося от источника эффекторного домена.10. Связывающая молекула по любому из предыдущих пунктов, где указанный связывающий домен способен связываться с любой из следующих молекул: с антигеном RhD эритроцитов; аллоантигеном НРА тромбоцитов; нейтрофильным антигеном; Т-клеточным рецептором; интегрином; коллагеном GMB; Der PI; HPA-la; VAP-1; ламинином; лютераном; гликопротеином VI тромбоцитов; гликопротеином 1а/IIа тромбоцитов.11. Связывающая молекула по п.10, где указанный связывающий домен выбирают из САМРАТН-1 и FOG1; ОКТ3; В2 (антитела против HPА-1а); VAP-1; мышиного антитела NC1 против α3 (IV); YTH12,5 (CD3); 2С7 (антитела против Der p I); антитела против ламинина; антитела против лютерана.12. Выделенная нуклеиновая кислота, содержащая нуклеотидную последовательность, кодирующую эффекторный домен связывающей молекулы по любому из предыдущих пунктов.13. Нуклеиновая кислота по п.12, где указанная нуклеотидная последовательность кодирует связывающую молекулу по любому из пп.1-11.14. Реплицируемый вектор, содержащий нуклеиновую кислоту по п.12 или по 13.15. Вектор по п.14, где указанная нуклеотидная последовательность операбельно связана с промотором.16. Клетка-хозяин, содержащая вектор по п.14 или 15 или трансформированная этим вектором.17. Способ получения связывающей молекулы по любому из пп.1-11, предусматривающий проведение стадии модификации нуклеотидной последовательности, кодирующей первый домен Сн2 тяжелой цепи первого иммуноглобулина человека, так, чтобы 2, 3 или 4 аминокислоты, по крайней мере, в 1 области указанного домена Сн2 соответствовали аминокислоте из домена Сн2 тяжелой цепи второго иммуноглобулина человека, где указанные области выбирают из 2 дискретных областей, с остатками под номерами 233-236 и 327-331, пронумерованными в соответствии с системой нумерации EU, и где в каждом случае указанный иммуноглобулин человека выбирают из IgG1, IgG2 и IgG4.18. Способ по п.17, где 2 аминокислоты в 1 области домена сн2 модифицированы так, что они соответствуют аминокислотам домена сн2 тяжелой цепи второго иммуноглобулина человека.19. Способ связывания молекулы-мишени, где способ включает контактирование указанной молекулы-мишени со связывающей молекулой по любому из пп.1-11.20. Способ по п.19, где молекулой-мишенью является FcγRIIb, связывание с которой приводит к ингибированию одного или нескольких эффектов: активации В-клеток; дегрануляции тучных клеток; фагоцитоза.21. Способ по п.19 для предупреждения, ингибирования или иного предотвращения каким-либо другим способом связывания второй связывающей молекулы с указанной молекулой-мишенью.22. Способ по п.21, где второй связывающей молекулой является антитело.23. Способ по п.21 или 22, где молекулу-мишень выбирают из антигена RhD эритроцитов; аллоантигена НРА тромбоцитов; нейтрофильного антигена; Т-клеточного рецептора; интегрина; коллагена ГБМ; Der PI; HPA-la; VAP-1; ламинина; лютерана; гликопротеина VI тромбоцитов; гликопротеина 1a/IIа тромбоцитов.24. Способ по любому из пп.20-23 для лечения пациента от расстройств, выбранных из реакции “трансплантат против хозяина”; реакции “хозяин против трансплантата”; отторжения трансплантированного органа; отторжения трансплантированного костного мозга; аутоиммунных заболеваний, таких как васкулиты, аутоиммунная гемолитическая анемия, аутоиммунная тромбоцитопения и артрит; аллоиммунных заболеваний, таких, как аллоиммунная тромбоцитопения плода/новорожденных; астмы и аллергии; хронических или острых воспалительных заболеваний, таких, как болезнь Крона; гемолитической болезни новорожденных; болезни Гудпасчера, серповидно-клеточной анемии, окклюзии коронарной артерии.25. Способ по любому из пп.19-24, где связывающую молекулу вводят пациенту или необязательно в том случае, когда этим пациентом является неродившийся ребенок, матери этого ребенка.26. Фармацевтический препарат, содержащий связывающую молекулу по любому из пп.1-12 или нуклеиновую кислоту по любому из пп.14-16, а также фармацевтически приемлемый носитель, применяемая при лечении заболеваний, указанных в п.24.