Изобретение относится к способу получения моноциклических кетонов С7-С20, более конкретно способу их получения путем жидкофазного окисления закисью азота (N2O) моноциклических алкенов формулы СnН2n-2, содержащих 7-20 атомов углерода.
Моноциклические кетоны С7-С20 являются важнейшими промежуточными продуктами в синтезе разнообразных органических соединений, в том числе дикарбоновых кислот и лактамов. Последние используются для производства различных полиамидных материалов, например найлона-8, найлона-12 и других.
Основным способом получения моноциклических кетонов является жидкофазное окисление соответствующих циклоалканов кислородом воздуха. Такое окисление может проводиться как в присутствии катализатора, так и без катализатора. В обоих случаях в качестве продуктов реакции образуется смесь циклических кетонов и спиртов. Например, при окислении циклододекана при 155-170°С и давлении 1-10 атм в присутствии борной кислоты образуется смесь циклододеканона и циклододеканола с суммарной селективностью около 90% при конверсии 5-20% [US Pat. №3419615, 1968, E.J. Inchalik et аl.]. При этом селективность по кетону не превышает 20%. Окисление циклододекана в смесь циклододеканона и циклододеканола может также проводиться с использованием в качестве катализатора солей Со или Мn при 90-150°С [GB Pat. №930842, 1963]. В патенте [US Pat. №3917708, 1975, A. Kuessner et al.] описан способ окисления циклических алканов C5-C12 в смесь соответствующих циклических кетонов и спиртов в присутствии солей Со, Мn, Сu, Fe, Ni. Процесс ведут при 130-160°С, давлении 5-25 атм и конверсии 3-6%.
Общим недостатком этих способов является образование, наряду с кетонами, значительных количеств циклических спиртов, а также резкое падение селективности реакции с увеличением конверсии.
В патенте GB Pat. 649, 680 (1951) заявлен способ окисления олефинов в карбонильные соединения закисью азота. Согласно этому способу, в частности, возможно получение циклооктанона путем окисления циклооктена.
Основным недостатком этого способа является возможность образования воспламеняемых смесей “циклоалкен - закись азота” при проведении процесса. Чтобы исключить взрывоопасность, авторы патента предлагают дополнительно вводить в реакционную смесь насыщенные углеводороды. Однако, как показали более поздние исследования, смеси насыщенных углеводородов с N2О почти столь же взрывоопасны, как и смеси олефинов [G. Panetier, A. Sicard, V Symposium on Combustion, 620 (1955); Б.Б. Брандт, Л.А. Матов, А.И. Розловский, В.С. Хайлов, Хим. пром., 1960, №5, с.67-73]. Поэтому насыщенные углеводороды, несмотря на их меньшую реакционную способность, не могут служить средством для исключения взрывоопасности.
Настоящий патент раскрывает способ получения моноциклических кетонов С7-С20 путем окисления моноциклических алкенов закисью азота, N2O, в присутствии инертного газа, который не имеет указанных недостатков. Согласно этому способу, реакцию ведут в присутствии инертного газа в условиях, когда циклоалкен присутствует в виде жидкой фазы, в которой реакция окисления протекает с высокой селективностью. Излишнее повышение температуры и/или давления N2O является нежелательньм, так как может приводить к понижению селективности за счет вклада газофазного окисления.
Взрывобезопасные условия работы по предлагаемому способу обеспечиваются добавлением в реакционную смесь инертного газа, не вступающего в реакцию с N2O, например азот, аргон, гелий, углекислый газ и т.д., либо их смесь. Роль инертного газа могут играть отходящие газы реакции или рециркулирующие газы. На разных стадиях процесса, в зависимости от соотношения "циклоалкен: закись азота", доля инертного газа, необходимая для обеспечения взрывобезопасной работы, может быть различной и создаваться путем его раздельной подачи. С точки зрения простоты и максимальной безопасности процесса целесообразно иметь такое разбавление закиси азота инертным газом, чтобы реакционная смесь была невзрывоопасной при любом содержании циклоалкена. Это условие выполняется, если содержание N2O в смеси с инертным газом составляет не более 25%. Применение такой смеси исключает возникновение взрывоопасных ситуаций на всех стадиях процесса.
Для уменьшения взрывоопасности в реакционную смесь могут добавляться ингибиторы горения, такие как трифторбромметан, дифторхлорбромметан, дибромтетрафторэтан и др.
В соответствии с данным изобретением окисление моноциклических алкенов в кетоны может быть осуществлено в широком интервале условий как в статическом, так и в проточном реакторе, который может быть изготовлен из стали, титана или другого подходящего материала. При этом могут быть использованы все известные технологические приемы, повышающие эффективность газожидкостных реакций.
В случае статического варианта процесса в автоклав при комнатной температуре загружают моноциклический алкен в таком количестве, чтобы при нагревании до температуры реакции он присутствовал в виде жидкой фазы. Затем подают смесь закиси азота с инертным газом, доводя давление до заданной величины. Количество закиси азота подбирают таким образом, чтобы ее давление при температуре реакции составляло 1,5-100 атм. Концентрацию инертного газа в смеси с закисью азота подбирают таким образом, чтобы она не превышала 99%. После этого реактор закрывают и нагревают до температуры реакции в области 20-350°С. Время реакции подбирается в зависимости от условий ее проведения, а также требований, предъявляемых к показателям процесса, и может изменяться от нескольких минут до нескольких десятков часов.
Предлагаемый процесс может осуществляться без растворителей. Однако возможно проведение процесса и с применением растворителей, которые могут выбираться из широкого круга веществ, применяемых в практике органического синтеза. Реакция с достаточно высокой скоростью протекает без катализатора, хотя может проводиться и в присутствии катализатора.
Предлагаемый способ получения моноциклических кетонов не предполагает высокой чистоты исходных реагентов. Так, закись азота может быть использована как в чистом виде, так и с примесями различных газов, не оказывающими вредного влияния на показатели процесса. Моноциклические алкены С7-С20 также могут содержать примеси других органических соединений, особенно, если они не содержат двойных связей С=С.
Сущность предлагаемого изобретения иллюстрируется следующими примерами.
Примеры 1-2.
Пример 1. Этот пример является сравнительным. В реактор объемом 100 см3, выполненный из нержавеющей стали и снабженный мешалкой (фирма Parr), заливают 25 см циклооктена (Aldrich, 99%). Реактор продувают закисью азота и затем доводят ее давление до 10 атм. Реактор герметично закрывают, нагревают до 220°С и выдерживают при этой температуре в течение 12 ч. Давление закиси азота при температуре реакции составляет 30 атм. После окончания реакции реактор охлаждают до комнатной температуры, измеряют давление и анализируют конечный состав газовой и жидкой фаз методами газовой хроматографии, хроматомасс-спектрометрии и ЯМР. Из полученных данных рассчитывают конверсию циклооктена (X) и селективность реакции по циклооктанону (S):
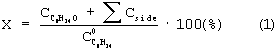
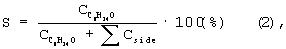
где 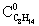 - начальная концентрация циклооктена;
- начальная концентрация циклооктена;  - концентрация циклооктанона в продуктах реакции; ∑Сside - суммарная концентрация побочных продуктов. В случае больших конверсии величина Х может быть рассчитана также по разнице между начальной и конечной концентрациями циклооктена:
- концентрация циклооктанона в продуктах реакции; ∑Сside - суммарная концентрация побочных продуктов. В случае больших конверсии величина Х может быть рассчитана также по разнице между начальной и конечной концентрациями циклооктена:
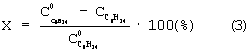
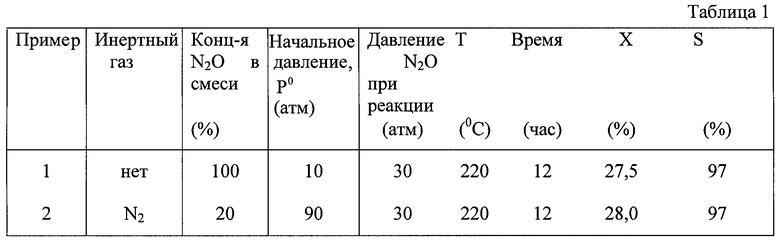
Конверсия циклооктена и селективность реакции по циклооктанону показаны в табл.1.
Пример 2 аналогичен примеру 1 с тем отличием, что вместо чистой закиси азота в реактор подают ее смесь с инертным газом - азотом, в которой концентрация N2O составляет 20% (табл.1). Начальное давление смеси в реакторе, Р0, устанавливают 90 атм. Давление закиси азота при температуре реакции составляет 30 атм.
Этот пример показывает, что реакция жидкофазного окисления моноциклических алкенов в циклические кетоны протекает с сохранением конверсии и высокой селективности при использовании в качестве окислителя смеси закиси азота с инертным газом.
Примеры 3-10.
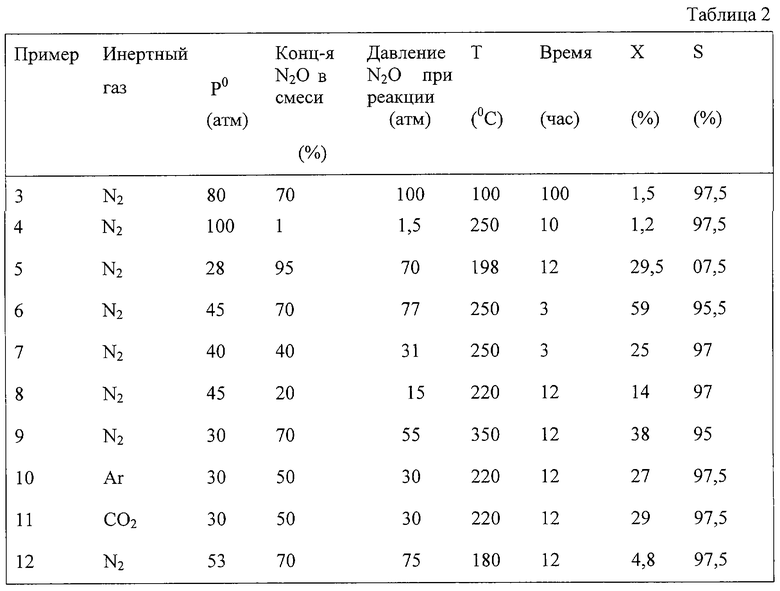
Примеры 3-10 показывают возможность проведения реакции с использованием смесей закиси азота с инертными газами различного состава (табл.2).
Пример 3 аналогичен примеру 2 с тем отличием, что для окисления используют смесь закиси азота с азотом, в которой концентрация N2O составляет 70%, и начальное давление в реакторе устанавливают 80 атм. Опыт проводят при 100°С в течение 100 ч. Давление N2О при температуре реакции составляет 100 атм.
Пример 4 аналогичен примеру 2 с тем отличием, что для окисления используют смесь закиси азота с азотом, в которой концентрация N2O составляет 1%, азота - 99%.
Начальное давление смеси в реакторе устанавливают 100 атм. Опыт проводят при 250°С в течение 10 ч. Давление N2O при температуре реакции составляет 1.5 атм.
Пример 5 аналогичен примеру 2 с тем отличием, что для окисления используют смесь закиси азота с азотом, в которой концентрация N2O составляет 95%, азота - 5%. Начальное давление смеси в реакторе устанавливают 28 атм. Опыт проводят при 198°С в течение 12 ч. Давление N2О при температуре реакции составляет 70 атм.
Пример 6 аналогичен примеру 2 с тем отличием, что концентрация N2O в смеси с азотом составляет 70%, и начальное давление смеси в реакторе устанавливают 45 атм. Опыт проводят при 250°С в течение 3 ч. Давление N2O при температуре реакции составляет 77 атм.
Пример 7 аналогичен примеру 6 с тем отличием, что концентрация N2O в смеси с азотом составляет 40%, а начальное давление смеси устанавливают 40 атм. Давление N2O при температуре реакции составляет 31 атм.
Пример 8 аналогичен примеру 2 с тем отличием, что начальное давление смеси N2O и азота в реакторе устанавливают равным 45 атм. Опыт проводят при 220°С в течение 12 ч. Давление N2O при температуре реакции составляет 15 атм.
Пример 9 аналогичен примеру 6 с тем отличием, что начальное давление в реакторе устанавливают 30 атм. Опыт проводят при 350°С в течение 2 ч. Давление N2O при температуре реакции составляет 55 атм.
Пример 10 аналогичен примеру 2 с тем отличием, что для окисления используют смесь закиси азота с аргоном, в которой концентрация N2O составляет 50%. Начальное давление в реакторе устанавливают 30 атм. Опыт проводят при 220°С в течение 12 ч. Давление N2O при температуре реакции составляет 30 атм.
Пример 11 аналогичен примеру 10 с тем отличием, что вместо аргона используют углекислый газ.
Пример 12 аналогичен примеру 6 с тем отличием, что начальное давление смеси в реакторе устанавливают 53 атм. Опыт проводят при 180°С в течение 12 ч. Давление N2O при температуре реакции составляет 75 атм.
Пример 13.
Этот пример является сравнительным. Опыт проводят аналогично примеру 6 с тем отличием, что в реактор загружают 3 мл циклооктена. При таком количестве весь циклооктен в условиях реакции находится в газовой фазе. Опыт проводят при 250°С в течение 3 ч, используя смесь закиси азота с азотом, в которой концентрация N2O составляет 70%. Начальное давление смеси в реакторе устанавливают 45 атм. В результате опыта конверсия циклооктена составила менее 1%. Это показывает, что при данных условиях реакция в газовой фазе практически не идет.
Примеры 14-15.
Эти примеры (табл.3) демонстрируют возможность проведения процесса в присутствии катализатора.
Пример 14 аналогичен примеру 12 с тем отличием, что реакцию ведут 6 ч в присутствии 0,2 г Fе2O3/SiO2 (2,8 мас.% Fе2O3). Катализатор готовят путем пропитки SiO2 раствором FеСl3, сушат при 110°С и прокаливают на воздухе при 500°С в течение 2 ч. Для окисления используют смесь закиси азота с азотом, в которой концентрация N2O составляет 70%. Начальное давление в реакторе устанавливают 53 атм. Опыт проводят при 180°С. Давление N2O при температуре реакции составляет 75 атм.
Пример 15 аналогичен примеру 14 с тем отличием, что реакцию ведут 5 ч в присутствии 0,5 г Ag/SiO2 (1 мас.% Ag). Катализатор готовят путем пропитки SiO2 раствором AgNO3, сушат при 110°С и прокаливают на воздухе при 500°С в течение 2 ч.

Примеры 16-19.
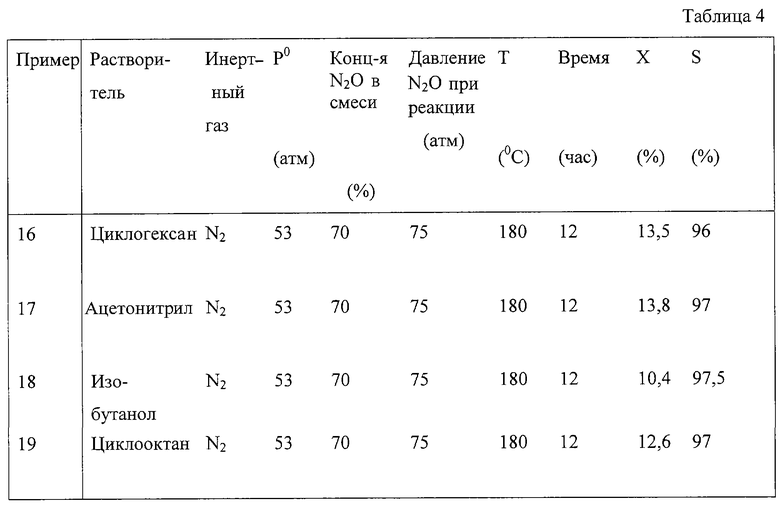
Эти примеры демонстрируют возможность окисления циклооктена в присутствии различных растворителей (табл.4).
Пример 16 аналогичен примеру 12 с тем отличием, что в реактор заливают 25 мл смеси циклооктена и циклогексана в объемном отношении 1:1.
Пример 17 аналогичен примеру 16 с тем отличием, что вместо циклогексана используют ацетонитрил.
Пример 18 аналогичен примеру 16 с тем отличием, что вместо циклогексана используют изобутиловый спирт.
Пример 19 аналогичен примеру 16 с тем отличием, что вместо циклогексана используют циклооктан.
Примеры 20-21.
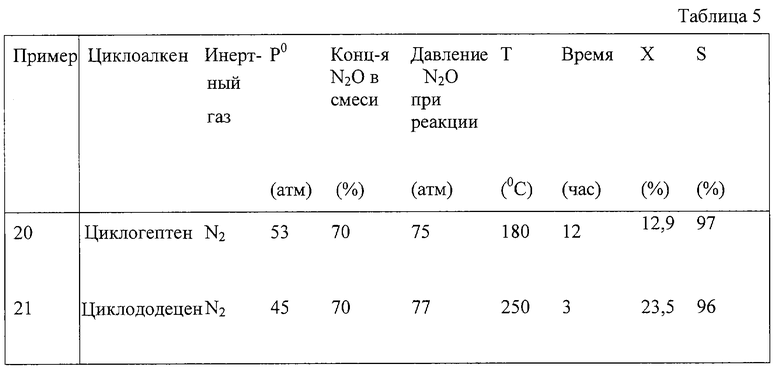
Примеры 20-21 показывают возможность окисления циклогептена и циклододецена в циклические кетоны с использованием смесей закиси азота с инертными газами (табл.5).
Пример 20 аналогичен примеру 12 с тем отличием, что вместо циклооктена используют циклогептен.
Пример 21 аналогичен примеру 6 с тем отличием, что вместо циклооктена используют циклододецен.
Примеры 2-12 и 14-21 показывают, что моноциклические алкены с высокой селективностью окисляются в соответствующие кетоны с помощью закиси азота, разбавленной инертным газом. Проведение процесса без использования инертного газа-разбавителя приводит к образованию взрывоопасных композиций циклоалкен-N2O в газовой фазе при заполнении реактора закисью азота, его разогреве или в условиях реакции. Например, проведение процесса по примеру 1 без добавления инертного газа приводит к образованию смесей, содержащих до 14,5% паров циклоалкена в закиси азота, взрывоопасность которых описана в работах [G. Panetier, A. Sicard, V Symposium on Combustion, 620 (1955); Б.Б. Брандт, Л.А. Матов, А.И. Розловский, В.С. Хайлов, Хим. пром., 1960, №5, с.67-73]. Проведение процесса в аналогичных условиях, но с использованием смеси N2O - инертный газ, в которой концентрация N2O составляет 20% (пример 2), позволяет исключить образование взрывоопасных смесей и обеспечить безопасность процесса.
Согласно предлагаемому способу, содержание закиси азота в смеси с инертным газом может изменяться в широких пределах, включая область концентраций N2O 25% и менее, в которой исключается возможность взрывоопасных ситуаций на всех стадиях процесса при любых композициях с циклоалкеном. Как показывают примеры 2 и 8, реакция окисления в этой области протекает с высокой эффективностью.
В настоящем изобретении предложен новый способ получения моноциклических кетонов С7-С20, основанный на реакции жидкофазного окисления моноциклических алкенов смесью закиси азота с инертным газом. Процесс обеспечивает высокую селективность, взрывобезопасность и является перспективным для промышленного применения.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ МОНОЦИКЛИЧЕСКИХ КЕТОНОВ | 2002 |
|
RU2227134C2 |
| СПОСОБ ПОЛУЧЕНИЯ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ | 2002 |
|
RU2227133C2 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛОПЕНТАНОНА | 2002 |
|
RU2227135C2 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 1-ПИРАЗОЛИНА | 2015 |
|
RU2598077C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛОГЕКСАНОНА | 2002 |
|
RU2205175C1 |
| СПОСОБ ПОЛУЧЕНИЯ ЦИКЛОГЕКСАНОНА ИЗ БЕНЗОЛА | 2002 |
|
RU2205819C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ | 2004 |
|
RU2270185C1 |
| СПОСОБ ВВЕДЕНИЯ КАРБОНИЛЬНЫХ ГРУПП В ПОЛИМЕРЫ | 2003 |
|
RU2230754C1 |
| СПОСОБ ПОЛУЧЕНИЯ КАРБОНИЛЬНЫХ СОЕДИНЕНИЙ С-С | 2015 |
|
RU2570818C1 |
| СПОСОБ МОДИФИЦИРОВАНИЯ ПОЛИМЕРОВ, СОДЕРЖАЩИХ ДВОЙНЫЕ УГЛЕРОД-УГЛЕРОДНЫЕ СВЯЗИ | 2003 |
|
RU2235102C1 |
Изобретение относится к способу получения моноциклических кетонов С7-С20. Способ заключается в реакции окисления моноциклических алкеновформулы СnH2n, содержащих 7-20 атомов углерода в цикле, в соответствующие моноциклические кетоны закисью азота в присутствии инертного газа-разбавителя, при температуре 100-3500С и давлении закиси азота 1,5-100 атм.Процесс обеспечивает высокую селективность по целевому продукту, взрывобезопасность работы и является перспективным для промышленного применения. 1 с. и 4 з. п. ф-лы, 5 табл.
| Металлобетонная смесь | 1977 |
|
SU649680A1 |
| J | |||
| Приспособление к пишущей машине для назначения и указания последней строки страницы | 1925 |
|
SU1951A1 |
| Способ получения 1,4-дизамещенных бутандионов-2,3 | 1974 |
|
SU504749A1 |
Авторы
Даты
2004-04-20—Публикация
2002-03-20—Подача