Изобретение относится к молекулярной биологии и биотехнологии и предназначено для анализа состава сложных биологических веществ и их смесей.
Известно устройство для детекции молекул, содержащее набор сенсоров, каждый из которых выполнен в виде ячейки, дно которой изготовлено из диэлектрика, ее объем заполняется раствором анализируемого вещества, а на поверхности диэлектрической крышки ячейки, обращенной в раствор, известным образом закреплены антилиганды. Дно ячейки заземлено, а крышка электрически соединена сигнальным проводом с источником сигнала и детектором сигнала (см. описание к патенту США № 6340568, фиг.1А [1].
В известном устройстве по сигнальному проводу передают электрические импульсы, которые через ячейку сенсора попадают на детектор. В случае осаждения молекул из анализируемого раствора на антилигандах изменяются диэлектрические свойства ячейки и по величине этих изменений судят о фиксации молекул на крышке ячейки.
Недостатком известного устройства является низкая чувствительность, так как ячейка сенсора содержит множество антилигандов и изменение диэлектрических свойств ячейки, обусловленное, например, присоединением одной молекулы, будет незначительным, не поддающимся измерению.
Известно устройство для детекции молекул, содержащее источник высокочастотного сигнала, соединенный с сенсором, подключенным к блоку обработки сигналов (см. [1], фиг.1В и 1С). Сенсор представляет собой измерительную ячейку, заполняемую раствором анализируемого вещества, на дне которой зафиксированы антилиганды, захватывающие молекулы одного сорта. Факт захвата определяется по изменению резонансной частоты ячейки.
Недостатком известного устройства является его низкая чувствительность, обусловленная тем, что, например, захват антилигандом одной молекулы аналита практически не изменит резонансную частоту ячейки, имеющей относительно большой объем.
Наиболее близким к заявляемому по своей технической сущности и достигаемому результату является устройство для детекции молекул, известное из описания к патенту US № 5891630. Известное устройство содержит набор сенсорных ячеек, соединенных с блоками детекции и регистрации. Каждая сенсорная ячейка представляет собой выполненное в диэлектрической пластине углубление, снабженное электродами, выполняющими роль обкладок конденсатора. В случае закрепления на антилигандах анализируемых молекул емкость конденсатора изменяется, что может быть определено с помощью блока детекции и зарегистрировано с помощью блока регистрации.
Заявляемый сенсор направлен на повышение чувствительности определения детектируемых молекул.
Указанный результат достигается тем, что сенсор для детекции молекул, макромолекул и макромолекулярных агрегатов выполнен в виде матрицы детектирующих ячеек, каждая из которых выполнена в виде двух электродов, размещенных на диэлектрической подложке, и по крайней мере одного электрода, размещенного над ними с зазором, заполненным диэлектриком, при этом все электроды размещены на расстоянии друг от друга от 1 до 10 характеристических размеров детектируемых частиц и подключены к источнику напряжения и блоку регистрации и обработки данных, при этом источник напряжения выполнен с возможностью изменения знака и величины напряжения, подаваемого на каждый из электродов.
Указанный результат достигается также тем, что на поверхность каждой ячейки нанесено покрытие, обеспечивающее преимущественную адсорбцию детектируемых частиц.
Указанный результат достигается также тем, что покрытие нанесено на участок подложки между расположенными на ней электродами и/или на поверхности одного или нескольких электродов каждой ячейки.
Указанный результат достигается также тем, что на каждую детектирующую ячейку нанесено покрытие с идентичными адсорбционными свойствами.
Размещение электродов на расстоянии друг от друга от 1 до 10 характеристических размеров детектируемых молекул позволяет обеспечить такой объем межэлектродного пространства (порядка 101-103 объема анализируемых молекул), что даже попадание в него одной отдельной макромолекулы приводит к измеримым изменениям диэлектрических свойств ячейки. Так как в сенсорных элементах предлагаемой нами конструкции величины межэлектродных зазоров составляют десятки нанометров, то даже небольшая разность потенциалов (1-100 мВ), приложенная к электродам, создает в межэлектродном пространстве поле напряженностью 107-108 В/м. Наложение модулированного поля такой интенсивности способно сильно поляризовать молекулы полиэлектролитов, каковыми является большинство биомолекул, и, при определенных условиях, способствовать разрушению молекулярных комплексов, характеризующихся низкой свободной энергией образования. Как известно, взаимодействие биомолекул с лигандами сложной структуры может быть неоднозначным. Одна и та же молекула (например, ДНК) может связываться со своим лигандом (например, олигонуклеотидом) несколькими, а иногда даже очень большим числом способов. С другой стороны, с данным лигандом могут связываться биомолекулы нескольких типов, которые имеют родственные структурные мотивы. Такие не совсем комплиментарные взаимодействия энергетически менее выгодны, чем полностью комплиментарные, однако кинетически они предпочтительнее, поэтому образуются в первую очередь. На практике образование таких комплексов проявляется в виде огромного числа ложнопозитивных сигналов и может быть устранено лишь в результате длительной и тонкой процедуры отжига, которая не всегда бывает успешной. Эта процедура заключается в длительной инкубации образовавшихся комплексов при температуре немного ниже температуры их разрушения. Поэтому возможность создания в межэлектродном пространстве значительных напряженностей позволяет ускорить процесс "правильной" фиксации детектируемых молекул. Кроме того, высокая напряженность поля может приводить к более сильной поляризации детектируемых молекул, а возникновение в межэлектродном промежутке диполей приводит к существенному изменению диэлектрических свойств в межэлектродном пространстве, что облегчает его измерение.
Выполнение ячейки в виде по крайней мере одного электрода, расположенного над двумя другими, которые размещены в плоскости подложки с зазором, заполненным диэлектриком, позволяет одновременно зафиксировать две проекции вектора диполя молекулы - на плоскость подложки и в плоскости, ей перпендикулярной, что является параметром, отражающим особенности строения данной молекулы. В частных случаях электроды, которые размещаются вне плоскости подложки, могут находиться над каждым из электродов, лежащих в плоскости подложки. Таким образом, предлагаемая ячейка может состоять либо из трех, либо из четырех электродов. Последний вариант позволяет использовать электромагнитные поля с большим числом вариантов ориентации вектора напряженности поля.
Выполнение источника напряжения с возможностью изменения знака и величины напряжения, подаваемого на каждый из электродов, позволяет создавать в межэлектродном промежутке переменное электрическое поле с различной частотой. При этом за счет третьего электрода вектор электрического поля может лежать не только в плоскости подложки, но и вне ее, т.е. изменять свое направление в плоскости, перпендикулярной подложке и оси электродов. Это позволяет регистрировать резонансное поглощение переменного электрического поля молекулами в межэлектродном пространстве и изменение направления вектора поляризации в зависимости от характера приложенного к электродам напряжения. Эти параметры отражают особенности строения детектируемых макромолекул. Учет этого фактора позволяет повысить соотношение сигнал/шум и дает дополнительную информацию о молекулах.
Наложение электрического поля высокой напряженности в плоскости, перпендикулярной плоскости подложки (за счет использования третьего электрода), способствует - в зависимости от направления вектора поля - адсорбции и десорбции заряженных детектируемых макромолекул на поверхности ячейки. При этом поля высокой напряженности, достигаемые за счет малости межэлектродного промежутка, способствуют не только диффузии несвязанных молекул к (или от) адсорбирующей поверхности, но также способны вызывать разрушение комплексов этих макромолекул с иммобилизованными на поверхности ячейки лигандами, если энергия образования таких комплексов невелика, которая присуща, как правило, комплексам, образовавшимся в результате не вполне комплементарного взаимодействия лигандов с макромолекулами.
В общем случае фиксация молекул в межэлектродном пространстве осуществляется за счет электрического взаимодействия между молекулами и электродами ячейки, на которые подано соответствующее напряжение.
В частных случаях на поверхность подложки между расположенными на ней электродами наносится покрытие, обеспечивающее адсорбцию определенного вида детектируемых молекул. Его нанесение позволяет обеспечивать либо специфичное, либо селективное связывание молекул либо одного вида, либо одного семейства, либо одного класса в зависимости от решаемой задачи. Указанное покрытие может наноситься не только на подложку между электродами, но и на боковые стенки ячейки. При этом оно может покрывать либо электроды, либо диэлектрик, находящийся между ними, либо и электроды и диэлектрик.
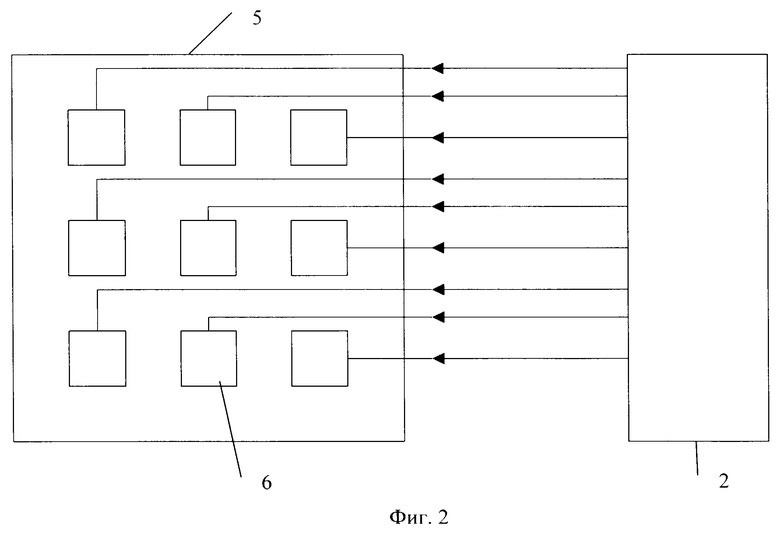
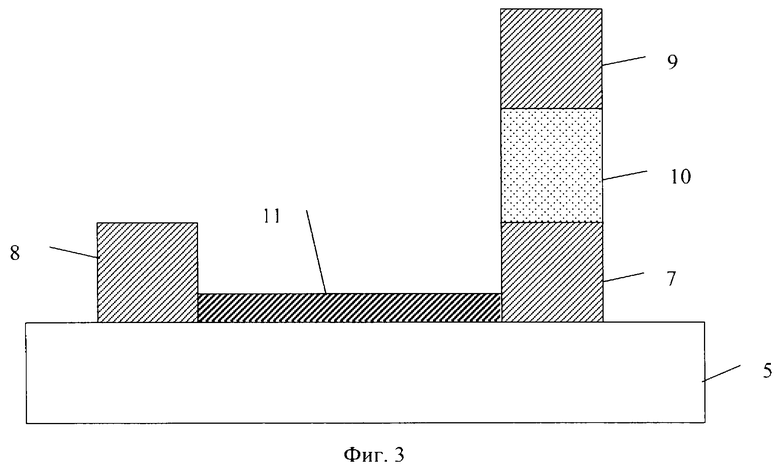
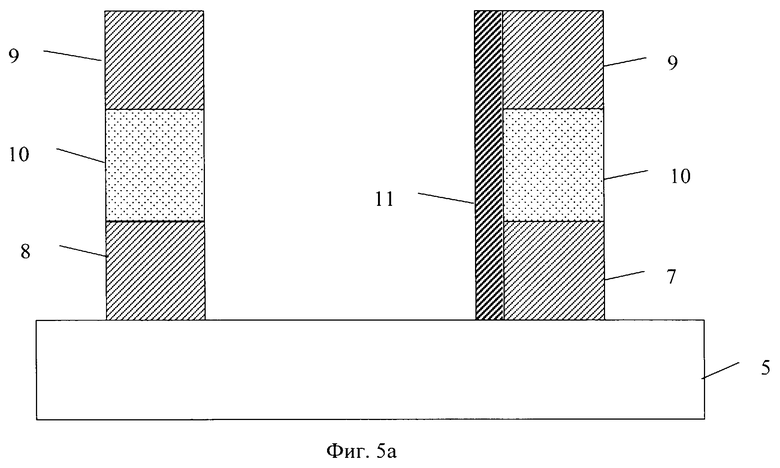
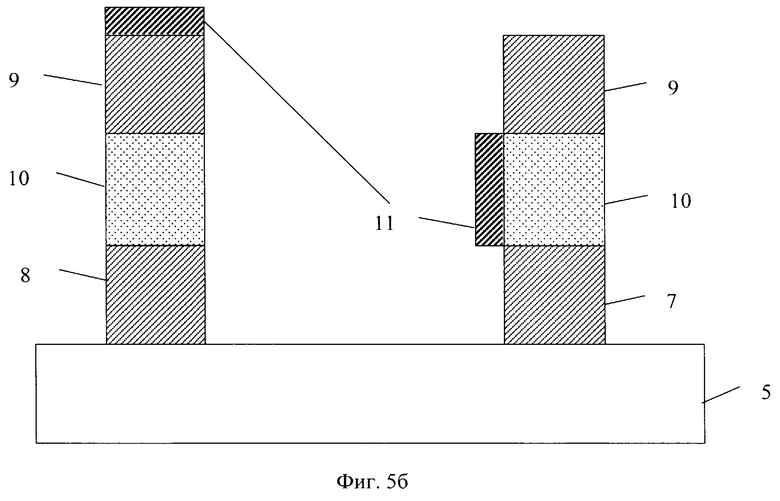
Сущность изобретения поясняется примерами его реализации и чертежами. На фиг.1 представлена принципиальная блок-схема устройства; на фиг.2 схематично представлено устройство с матрицей сенсоров; на фиг.3 - поперечный разрез одной из детектирующих ячеек с тремя электродами. На фиг.4 показан поперечный разрез частного варианта реализации ячейки с четырьмя электродами; на фиг.5а, б - варианты ячейки с нанесенным покрытием, обеспечивающим адсорбцию, на боковой стенке.
Устройство в наиболее общем виде содержит матрицу детектирующих ячеек 1, каждая из которых электрически соединена с источником напряжения 2, который соединен соответствующим образом с блоком регистрации и обработки 3, выход которого соединен с блоком управления 4. Выход блока управления соединен со входом источника напряжения.
В качестве источника напряжения может быть использован любой из числа известных, обеспечивающий требуемый алгоритм подачи напряжения на электроды. В качестве блоков управления, регистрации и обработки могут быть использованы компьютеры, снабженные соответствующим программным обеспечением. В частных случаях это может быть один компьютер, обеспечивающий совместную работу обеих программ. Блок регистрации и обработки может выводить получаемые результаты либо на монитор, либо на принтер, либо на устройство магнитной записи (на чертежах не показаны).
Матрица детектирующих ячеек выполнена в виде диэлектрической подложки 5, на которой размещаются детектирующие ячейки 6, каждая из которых соединена электрически с источником напряжения. Число ячеек может колебаться от нескольких сотен до несколько десятков тысяч, в зависимости от решаемых задач.
Каждая из ячеек в общем случае представляет собой размещенные на подложке два электрода 7 и 8, выполненные из любого подходящего электропроводного материала. Над одним из этих электродов размещен третий электрод 9 с зазором, заполненным диэлектриком 10, в качестве которого может быть использован любой из числа известных. В другом варианте реализации над каждым из электродов, размещенных на подложке (7 и 8), может быть размещен свой дополнительный электрод 9а, б с диэлектриком 10 ( см. фиг.4).
В частных случаях реализации поверхность подложки в межэлектродном промежутке или ее боковые стенки покрыты веществом 11, обеспечивающим адсорбцию определенного вида (класса) детектируемых молекул. В качестве покрытия могут быть использованы различные органические молекулы, например белки, фрагменты нуклеиновых кислот, их синтетических химических аналогов, низкомолекулярные органические вещества и т.д., которые предварительно функционализированы любым из известных способов.
Устройство работает следующим образом. Перед началом измерений система опрашивает все детектирующие ячейки 6 матрицы 1 и те из них, параметры которых не укладываются в заданные рамки, помечаются как "плохие" и данные в дальнейшем с них не считываются. Затем анализируемый раствор наносится на поверхность матрицы 1 детектирующих ячеек 6, в результате чего промежутки между электродами 7, 8 и 9 заполняются жидкостью. Это приводит к изменению физического состояния детектирующих ячеек 6, что проявляется в изменении их диэлектрической проницаемости. С помощью блока регистрации измеряют рассеяние энергии переменного электрического поля в каждой ячейке, что отражает ее мгновенный статус. Статус ячеек 6 может быть одним из перечисленных ниже:
I. "плохие", те о которых речь шла выше;
II. поврежденные, то есть те, которые стали неисправны в результате добавления анализируемого раствора;
III. пустые, те, что содержат только растворитель;
IV. заполненные молекулами низкомолекулярных соединений;
V. содержащие адсорбированные макромолекулы, неспецифичные для данного лиганда и поэтому не полностью комплементарно связанные с данным лигандом ("неправильное взаимодействие");
VI. содержащие адсорбированные макромолекулы, комплементарно связанные с данным лигандом ("правильное взаимодействие").
Ячейки 6 в состоянии I и II легко дискриминируются и далее не опрашиваются. Однако при правильной эксплуатации их число не должно быть велико и не они определяют основной уровень ошибок. Концентрация низкомолекулярных веществ (обычно 0,1-100 мМ) такова, что в объеме ячейки 6 будут находиться лишь их единичные молекулы, поэтому вероятность состояния IV невелика. Состояние VI также маловероятно в самом начале измерения, так как, во-первых, концентрация молекул, способных дать "неправильный" комплекс с данным лигандом, обычно на несколько порядков больше, чем тех, что дают полностью комплиментарный комплекс. Во-вторых, комплексы первого типа ("неправильные") кинетически более предпочтительны и образуются в первую очередь (см., например, Dai H. et al., Nucl. Acids Res. 2002, v.30, p. е86).
Наиболее представленными будут ячейки 6 в состояниях III и V (оптимальна такая концентрация аналита, когда их число примерно сравнимо). Поэтому следующим этапом анализа является процесс перевода ячеек 6 из состояния V в состояние VI. (То есть дать возможность "неправильным" комплексам разрушится, анализируемым молекулам продиффундировать к местам узнавания и там образовать правильные комплиментарные комплексы). При использовании стандартной технологии биочипов для этого используют отжиг (инкубацию чипа при повышенной температуре в течение нескольких часов с одновременной отмывкой). Однако конструкционные особенности предлагаемых ячеек 6 таковы, что они позволяют осуществлять отжиг по другой процедуре, которая описана ниже.
Так как в ячейках 6 предлагаемой нами конструкции величины межэлектродных зазоров составляют десятки нанометров, то даже небольшая разность потенциалов (1-100 мВ), приложенная к электродам, создает в межэлектродном пространстве поле напряженностью 107-108 В/м. Наложение модулированного поля такой интенсивности способно сильно поляризовать молекулы полиэлектролитов, каковыми является большинство биомолекул, и, при определенных условиях, способствовать разрушению молекулярных комплексов, характеризующихся низкой свободной энергией образования. Более того, для процессов, протекающих по сложному пути с несколькими примерно одинаковыми барьерами активации (а это как раз наш случай), направленное частотное воздействие может изменять путь и даже влиять на константу равновесия данного процесса (см., например, Astumian R.D., Robertson В. JACS, 1993, v.115, no. 24). Таким образом, переменное электрическое поле высокой напряженности, модулированное по амплитуде, частоте и направлению за счет приложения различных зарядов к электродам 7, 8 и 9 ячейки, вызывает дестабилизацию комплексов с низкой энергией образования, ускоряет массообмен ячейки 6 с окружающей жидкостью и, в конечном счете, сокращает процесс отжига, который в этом случае будет занимать несколько минут.
В наиболее предпочтительном варианте процедура отжига совмещена с процедурой регистрации за счет того, что источник напряжения 2 работает под управлением блока управления 4, который формирует команды на основании данных, получаемых от блока регистрации и обработки 3. Поэтому, в отличие от процедур, принятых в обычных технологиях, в данном случае не обязательно доводить отжиг до конца для получения надежного результата. Объединенная процедура отжига и регистрации может происходить по следующей схеме.
Источник напряжения 2 подает на электроды 7, 8 и 9 каждой ячейки 6 переменное напряжение, определенным образом модулированное по фазе и частоте. Порядок подачи напряжения и его параметры определяются экспериментально, на основании ранее проделанных измерений. Отклик каждой ячейки, выражающийся в поглощении подаваемой на нее энергии, в проявлении ею анизотропии диэлектрической проницаемости и т.п., отражает ее текущий статус. Этот отклик поступает в блок регистрации и обработки 3, который регистрирует данные от каждой ячейки независимо от остальных, причем этот процесс может быть либо параллельным, либо последовательным. Далее следует обработка полученных сигналов, которая происходит по алгоритму, основные особенности которого таковы:
i. Сигналы ячеек, чьи параметры лежат за пределами допустимых значений в течение всего предшествующего периода измерений, отбрасываются.
ii. Ячейки, чьи сигналы не превышают некого известного порогового значения, учитываются как свободные.
iii. Сигналы от ячеек, превышающие некое пороговое значение, интерпретируются как единичный сигнал и после умножения на особый коэффициент суммируются.
iv. Коэффициент, указанный в п.iii, рассчитывается с использованием процедур статистической механики с учетом следующих параметров: времени, в течение которого ячейка 6 находится в данном состоянии; температуры окружающей среды, частоты, фазы и интенсивности приложенного электрического поля; состава буферного раствора и т.д. Чем ближе время существования ячейки 6 в данном состоянии к среднему времени жизни комплекса "проба-мишень", которое ранее определено экспериментально, тем ближе значение указанного коэффициента к единице.
v. Информация о текущем состоянии матрицы (полученная на этапах i, ii и iii) хранится в оперативной памяти блока регистрации и обработки, обновляется в течение всего периода регистрации и используется в качестве исходных данных для блока управления и для расчета конечного результата измерений.
Блок управления 4 выдает источнику напряжения 2 инструкции о значениях параметров переменного напряжения (амплитудах, фазах и частотах), которое подается на электроды 7, 8 и 9 каждой из ячеек 6. Инструкции могут быть общими, а могут быть и индивидуальными для каждой ячейки. В начале процесса измерения инструкции выдаются на основании данных из базы, которая хранится в памяти блока управления 4. Далее, в процессе анализа, инструкции корректируются на основании данных, полученных на этапе v алгоритма блока обработки данных 4. Корректировка инструкций происходит таким образом, чтобы создать условия внутри ячеек 6, в которых время жизни комплиментарных комплексов "проба-мишень" имеет конечное, экспериментально измеряемое значение, и, как следствие, время жизни остальных комплексов много меньше.
Финальной точкой процесса измерения является появление стационарной картины в массиве обновляемых данных на этапе v алгоритма.
По окончании процесса измерения фактическая начальная концентрация анализируемого вещества в исходной смеси рассчитывается исходя из данных о количестве свободных ячеек и данных из массива, полученного на этапе v.
В частном случае описанный прибор используется для детекции макромолекулярных комплексов, имеющих строго детерминируемую структуру. К таким частицам можно отнести, например, большинство фагов и вирусов. В этом случае в качестве дополнительной информации, используемой для идентификации частицы, могут быть использованы количественные изменения параметров ячейки, которые происходят в результате единичного акта связывания. К таким параметрам можно отнести, например, частотную зависимость интенсивности рассеивания энергии переменного электрического поля, время релаксации диэлектрической поляризации и т.д.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ФОРМИРОВАНИЯ СТРУКТУРЫ | 2002 |
|
RU2205470C1 |
| СПОСОБ ПОЛУЧЕНИЯ ОБЪЕМНОЙ ПРОВОДЯЩЕЙ СТРУКТУРЫ | 2002 |
|
RU2205469C1 |
| СПОСОБ СЕКВЕНИРОВАНИЯ ДНК И УСТРОЙСТВО ДЛЯ ЕГО ОСУЩЕСТВЛЕНИЯ (ВАРИАНТЫ) | 2013 |
|
RU2539038C1 |
| СПОСОБ ИЗГОТОВЛЕНИЯ ОПТИЧЕСКОГО ВОЛНОВОДНОГО УСТРОЙСТВА | 2000 |
|
RU2183026C1 |
| СПОСОБ ДИАГНОСТИКИ РАКА МОЛОЧНОЙ ЖЕЛЕЗЫ И РАКА ЯИЧНИКОВ | 2017 |
|
RU2696114C2 |
| СПОСОБ РЕГИСТРАЦИИ РЕЗУЛЬТАТА РЕАКЦИИ ПОЛИМЕРИЗАЦИИ ДНК И УСТРОЙСТВО ДЛЯ ЕГО РЕАЛИЗАЦИИ | 2019 |
|
RU2724507C1 |
| ДЕТЕКЦИЯ ЦЕЛЕВОЙ ПОСЛЕДОВАТЕЛЬНОСТИ ПУТЕМ НАНОПОРОВОГО СЕНСОРНОГО ОБНАРУЖЕНИЯ СИНТЕТИЧЕСКИХ ЗОНДОВ | 2015 |
|
RU2681822C2 |
| СПОСОБ ФОРМИРОВАНИЯ МНОГОУРОВНЕВОЙ МЕТАЛЛИЗАЦИИ ИНТЕГРАЛЬНЫХ СХЕМ | 2000 |
|
RU2165114C1 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОБНАРУЖЕНИЯ БИОЛОГИЧЕСКИХ ТОКСИНОВ | 2004 |
|
RU2320994C1 |
| Биологический микрочип для обнаружения опухолевых экзосом в сыворотке крови человека для диагностики колоректального рака | 2016 |
|
RU2682721C2 |

Изобретение относится к молекулярной биологии и биотехнологии и предназначено для анализа состава сложных биологических веществ и их смесей. Технический результат изобретения заключается в повышении чувствительности определения детектируемых молекул. Сущность: сенсор выполнен в виде матрицы детектирующих ячеек, каждая из которых выполнена в виде двух электродов, размещенных на диэлектрической подложке, и по крайней мере одного электрода, размещенного над ними с зазором, заполненным диэлектриком. Все электроды размещены на расстоянии друг от друга от 1 до 10 характеристических размеров детектируемых частиц и подключены к источнику напряжения и блоку регистрации и обработки данных. Источник напряжения выполнен с возможностью изменения знака и величины напряжения, подаваемого на каждый из электродов. 3 з.п. ф-лы, 5 ил.

| US 5891630 А, 06.04.1999 | |||
| US 5846708 А, 08.12.1998 | |||
| УСТРОЙСТВО ДЛЯ ОПРЕДЕЛЕНИЯ БИОЛОГИЧЕСКИ АКТИВНЫХ СОЕДИНЕНИЙ В БИОЛОГИЧЕСКИХ ЖИДКОСТЯХ И СПОСОБ ИЗГОТОВЛЕНИЯ ЧУВСТВИТЕЛЬНОГО ЭЛЕМЕНТА | 1991 |
|
RU2032908C1 |
| ЭЛЕКТРОХИМИЧЕСКИЙ ДАТЧИК ДЛЯ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ГЛЮКОЗЫ | 1994 |
|
RU2076316C1 |
| US 5156810 А, 20.10.1992. | |||
Авторы
Даты
2004-05-20—Публикация
2002-11-10—Подача