Область техники.
Настоящее изобретение относится к микробиологической промышленности, в частности к способу получения L-аминокислот. Конкретно, настоящее изобретение касается использования нового фермента, вовлеченного в биосинтез глутамина и пути ассимиляции азота в штаммах E.coli - продуцентах аминокислот, таких как глутамин и аргинин. Более конкретно, настоящее изобретение представляет новую мутантную глутаминсинтетазу и способ получения аминокислот, таких как глутамин, аргинин, триптофан, гистидин и глутамат, с использованием штаммов E.coli, содержащих указанный фермент.
Предшествующий уровень техники
У глутаминсинтетазы (GS) из E.coli две функции: образование глутамина и ассимиляция аммиака в условиях недостатка аммиака. Глутамин является донором азота в синтезе пуринов и пиримидинов, а также некоторых аминокислот, таких как аргинин, триптофан, аспарагин, гистидин и глутамат. В биосинтезе аргинина глутамин играет значительную роль, поскольку является единственным физиологическим донором аминогруппы в синтезе карбамоилфосфата - общего предшественника для аргинина и пиримидинов. При образовании триптофана глутамин используется в первой реакции биосинтеза триптофана, заключающейся в конверсии хоризмата и глутамина в антранилат, глутамин и пируват. Глутамин-зависимая аспарагинсинтетаза использует глутамин вместе с аспартатом и АТФ в главном пути биосинтеза аспарагина. В имидазольном кольце гистидина азот 3 получается из глутамина. И наконец, глутамин используется глутаматоксоглутарат аминотрансферазой (глутамат синтазой) (GOGAT) в синтезе глутамата.
Ввиду множества функций и важности GS в клеточном метаболизме обе ее каталитические активности и ее синтез тщательно регулируются.
Общая структура активной GS состоит из 12 субъединиц, скомпонованных в два гексамера друг напротив друга. Аденилирование тирозина-397 каждой субъединицы GS снижает ферментативную активность in vivo. Как аденилирование, так и де-аденилирование GS катализируется аденилтрансферазой, кодируемой геном glnE. Направление катализа определяется регуляторным белком PII (glnB), активность которого также определяется обратимой модификацией: немодифицированная форма белка PII активирует аденилирование, в то время как уридилированная форма белка PII активирует де-аденилирование GS. Специфическая уридилилтрансфераза катализирует перенос уридилильной группы с УТФ на белок PII, в то время как активность по удалению уридилильной группы вызывает процесс, противоположный уридилированию белка PII. Обе активности определяются геном glnD. Глутамин стимулирует активность по удалению уридилильной группы, 2-оксоглутарат стимулирует уридилирование белка PII. Таким образом, в конечном счете глутамин вызывает аденилированние GS, в то время как 2-оксоглутарат способствует образованию де-аденилированной (активной) формы GS (Escherichia coli and Salmonella, Second Edition, Editor in Chief: F.C.Neidhardt, ASM Press, Washington D.C., 1996).
Ранее были описаны мутантные глутаминсинтетазы из различных видов, не способные к аденилированию. Такими мутантами являются мутантная GS из Rhizobium meliloli (Arcondeguy et al, FEMS Microbiol. Lett., 1996, 145:1, 33-40), Y398F мутантная GS из Rhodospirillum rubrum (Zhang et al, J. Bacteriol., 2000, 182:4, 938-92) и Y407F мутантная GS из Azobacter vinelandii (Colnaghi et al, Microbiology, 2001, 147:5, 1267-76). Приведенные мутантные GS обладают уровнем активности природного фермента. Но в настоящее время нет сообщений об использовании мутантной GS, не способной к аденилированию, для продукции аминокислот.
Описание изобретения
В настоящем изобретении описывается конструирование мутантного и высокоактивного фермента, играющего ключевую роль в биосинтезе глутамина и аргинина в E.coli.
В настоящем изобретении описывается замена кодона ТАТ, кодирующего тирозин в положении 397 белка GS, на кодон ТТТ, кодирующий аминокислотный остаток фенилаланина, в гене glnA. Замена указанного аминокислотного остатка в аминокислотной последовательности приводит к экспрессии мутантного белка, не способного к аденилированию, причем уровень его активности соответствует уровню активности природного белка. Было установлено, что GS, мутированная, как описано выше, становится нечувствительной к непрямому (опосредованному) ингибированию глутамином. Затем авторы настоящего изобретения обнаружили, что бактерия, принадлежащая к роду Escherichia, - продуцент глутаминовой кислоты, трансформированная с помощью ДНК, содержащей такой мутантный ген, становится способной к продукции глутамина. Таким образом было совершено настоящее изобретение.
Настоящее изобретение включает в себя следующее:
(1). Глутаминсинтетаза, состоящая из последовательности аминокислот, приведенной в Списке последовательностей под номером 1, в которой остаток тирозина, соответствующий положению 397 в последовательности под номером 1, заменен на остаток любой другой аминокислоты;
(2). Глутаминсинтетаза в соответствии с (1), которая состоит из последовательности аминокислот, включающей делеции, замены, вставки и добавления одной или нескольких аминокислот в одном или нескольких положениях, отличных от положения 397, в последовательности аминокислот, приведенной в Списке последовательностей под номером 1;
(3). Глутаминсинтетаза в соответствии с (1) или (2), в которой остаток, соответствующий положению 397 в последовательности аминокислот, приведенной в Списке последовательностей под номером 1, заменен на фенилаланин;
(4). Глутаминсинтетаза в соответствии с (1)-(3), которая является глутаминсинтетазой из Escherichia coli;
(5). ДНК, кодирующая глутаминсинтетазу в соответствии с любым из (1)-(4);
(6). Бактерия, трансформированная с помощью ДНК в соответствии с (5);
(7). Бактерия в соответствии с (6), принадлежащая к роду Escherichia;
(8). Бактерия в соответствии с (7), обладающая способностью к продукции L-аминокислот.
(9). Способ получения L-аминокислоты, включающий стадии:
- выращивания бактерии в соответствии с (6)-(8) в питательной среде с целью продукции и накопления L-аминокислоты в питательной среде, и
- выделения L-аминокислоты из культуральной жидкости.
(10). Способ в соответствии с (9), в котором L-аминокислота выбрана из группы, состоящей из L-глутамина, L-аргинина, L-триптофана, L-гистидина, L-глутамата.
(11). Способ в соответствии с (10), в котором L-аминокислотой является L-глутамин.
Описанная выше GS, содержащая замену остатка тирозина, соответствующего положению 397 в последовательности под номером 1 в Списке последовательностей, упоминается как "мутантная GS". ДНК, кодирующая мутантную GS, упоминается как "мутантный ген glnА", а GS, не содержащая замен, упоминается как "природная GS". Далее настоящее изобретение более детально будет описано ниже.
<1> Мутантная GS и мутантный ген glnA.
Известно, что тирозин в положении 397 является местом аденилирования GS (нумерация остатков аминокислот указанного фермента приводится в соответствии с G.Colombo и J.J.Villafranca. J.Biol. Chem., Vol.261. Issue 23, 10587-10591, 1986). Аденилирование GS приводит к инактивации фермента. Замена аминокислотного остатка, соответствующего тирозину в положении 397, любой другой аминокислотой, предпочтительно фенилаланином, в последовательности аминокислот природной GS приводит к образованию мутантного белка с уровнем активности природного белка и не способного к аденилированию. Мутантная GS становится нечувствительной к непрямому (опосредованному) ингибированию глутамином.
Мутантная GS может быть получена на основе последовательности природного гена glnA путем введения мутаций с использованием обычных методов. В качестве природного гена glnA может быть упомянут ген glnА из E.coli (нуклеотиды с 6558 по 7967 в последовательности АЕ000462 U00096 в базе данных GenBank, SEQ ID NO:2).
Мутантная GS может содержать делеции, замены, вставки и добавления одной или нескольких аминокислот в одном или нескольких положениях, кроме положения 397, при условии, что активность GS не нарушается. Термин “активность GS” означает активность по катализу реакции образования глутамина из глутамата и аммиака с использованием АТР.
Число “нескольких” аминокислот различно в зависимости от положения или типа остатка аминокислоты в трехмерной структуре белка. Это объясняется следующими причинами. Например, некоторые аминокислоты являются в достаточной степени взаимозаменяемыми и отличия в этих аминокислотах не влияют в значительной степени на трехмерную структуру белка. Следовательно, мутантной GS согласно настоящему изобретению может быть мутантная GS, у которой степень гомологии не ниже чем 30-50%, предпочтительно 50-70%, по отношению ко всем остаткам аминокислот, составляющим GS согласно настоящему изобретению, и которая обладает активностью GS.
В настоящем изобретении “последовательность аминокислот, соответствующая положению 397” означает последовательность аминокислот, соответствующую последовательности аминокислот в положении 397 в последовательности аминокислот под номером 1 (SEQ ID NО:1). Положение остатка аминокислоты может быть изменено. Например, если какой-либо остаток аминокислоты добавлен в N-концевой участок, то остаток аминокислоты, находившийся ранее в положении 397, оказывается в положении 398. В таком случае остаток аминокислоты, соответствующий первоначальному положению 397, рассматривается как остаток аминокислоты в положении 397 согласно настоящему изобретению.
ДНК, кодирующая практически такой же белок, как мутантная GS, описанная выше, может быть получена, например, путем модификации последовательности нуклеотидов методом сайт-специфического мутагенеза таким образом, что белок, кодируемый подобной ДНК, будет в определенном положении содержать делеции, замены, вставки или добавления одного или нескольких остатков аминокислот. ДНК, модифицированная описанным выше способом, может быть получена традиционными способами мутагенеза.
К делециям, заменам, вставкам или добавлениям нуклеотидов, описанным выше, относятся мутации, которые встречаются в природных условиях (мутанты или варианты), например, в случае индивидуальных или родовых и видовых различий бактерий, содержащих GS.
<2> Бактерия согласно настоящему изобретению, принадлежащая к роду Escherichia.
Бактерией, принадлежащей к роду Escherichia, согласно настоящему изобретению является бактерия, принадлежащая к роду Escherichia, в которую введен мутантный ген glnA, описанный выше. Примером бактерии, принадлежащей к роду Escherichia, является Е.coli. Мутантный ген glnA может быть введен, например, путем трансформации бактерии, принадлежащей к роду Escherichia, рекомбинантной плазмидой, содержащей вектор, функционирующий в бактерии, принадлежащей к роду Escherichia, и мутантный ген glnA. Мутантный ген glnA также может быть введен заменой гена glnA в хромосоме на мутантный ген glnA.
Примерами векторов, которые можно использовать для введения мутантного гена glnA, являются плазмидные векторы, такие как pMW118, pBR322, pUC19 или подобные им, фаговые векторы, такие как 11059, 1BF101, M13mp9 или подобные им, и транспозоны, такие как Мu, Тn10, Тn5 или подобные им.
Введение ДНК в бактерию, принадлежащую к роду Escherichia, может быть осуществлено, например, по методу D.A.Morrison (Methods in Enzymology, 68, 326 (1979)) или методом, в котором бактериальная клетка - реципиент обрабатывается хлоридом кальция для увеличения проницаемости для ДНК (Mandel, M. and Higa, A., J.Mol.Biol. 53, 159 (1970)) или подобным им методом.
Бактерий, принадлежащих к роду Escherichia, которые обладают способностью к продукции значительных количеств L-глутамина, к настоящему времени описано не было. Отмечалось, что выращивание штамма E.coli К-12 в питательной среде, содержащей более 10 весовых частей азота на 100 весовых частей углерода, приводит к накоплению 0,36 мг/мл L-глутамина (патент Великобритании № 1113117). Таким образом, продуцируемое количество L-глутамина может быть увеличено путем введения мутантного гена glnA в бактерию дикого типа, принадлежащую к роду Escherichia, и экскретирующую глутамин.
Примерами бактерий, принадлежащих к другим родам, обладающих способностью к продукции L-глутамина, являются Brevibacterium flavum FERM-P 4272, Corynebacterium acetoacidophilum ATCC 13870, Microbacterium flavum FERM-BP 664 (AJ 3684), Brevibacterium flavum FERM-BP 662 (AJ 3409), Corynebacterium acetoglulamicum ATCC 13870, Corynebacterium glutamicum FERM-BP 663 (AJ 3682) (патент США 5164307).
Количество продуцируемого L-глутамина может быть увеличено путем введения мутантного гена glnA в бактерию, принадлежащую к роду Escherichia, - продуцент глутаминовой кислоты.
Примерами бактерий, принадлежащих к роду Escherichia, обладающих способностью к продукции L-глутаминовой кислоты, являются следующие штаммы E.coli: штаммы, обладающие устойчивостью к антиметаболитам аспарагиновой кислоты, и дефицитные по активности альфа-кетоглутаратдегидрогеназы, такие как AF13199 (FERM ВР-5807) (патент США 5908768), или штамм FERM Р-12379 дополнительно имеющий низкую активность по разложению L-глутаминовой кислоты (патент США 5393671); штамм E.coli AJ13138 (FERM BP-5565) (патент США 6110714) и подобные им.
Примерами бактерий, принадлежащих к роду Escherichia, обладающих способностью к продукции L-аргинина, являются штамм E.coli 237 (ВКПМ В-7925) (Российская патентная заявка 2000116481), штаммы продуценты аргинина, в которые введен ген argA, кодирующий N-ацетилглутаматсинтетазу (выложенная заявка Японии № 57-5693) и подобные им.
Примерами бактерий, принадлежащих к роду Escherichia, обладающих способностью к продукции L-триптофана, являются штаммы E.coli – производные штамма Genencor JB102/pBE7, содержащие триптофановый оперон, ген aroG и ген serA из E.coli (патент США 5939295), штаммы E.coli DSM10118, DSM 10121, DSM10122, DSM10123 (патент США 5756345), штамм Е.coli SV164 (pGH5) (EP1149911А2), штаммы Е.сoli NRRL В-12257-NRRL В-12264 (патент США 4371614) и подобные им.
Примерами бактерий, принадлежащих к роду Escherichia, обладающих способностью к продукции L-гистидина, являются штаммы E.coli NRRL В-12116, NRRL B-12118, NRRL B-12119, NRRL B-12120, NRRL B-12121 (патент США 4388405) и подобные им.
<3> Способ получения L-аминокислот.
К способам согласно настоящему изобретению относится способ продукции L-аминокислоты, включающий стадии выращивания бактерии согласно настоящему изобретению в питательной среде с целью продукции и накопления L-аминокислоты в указанной питательной среде, и выделения L-аминокислоты из культуральной жидкости.
Как детально объяснено в нижеследующих примерах, к способу согласно настоящему изобретению относится способ продукции L-глутамина, включающий стадии выращивания бактерии согласно настоящему изобретению в питательной среде с целью продукции и накопления L-глутамина в указанной питательной среде, и выделения L-глутамина из культуральной жидкости.
Глутамин является донором азота в синтезе пуринов и пиримидинов, а также некоторых аминокислот, таких как L-аргинин, L-триптофан, L-гистидин и L-глутамат. В биосинтезе аргинина глутамин играет значительную роль, поскольку является единственным физиологическим донором аминогруппы в синтезе карбамоилфосфата - общего предшественника для аргинина и пиримидинов. При образовании триптофана глутамин используется в первой реакции биосинтеза триптофана, заключающейся в конверсии хоризмата и глутамина в антранилат, глутамин и пируват. Глутамин-зависимая аспарагинсинтетаза использует глутамнн вместе с аспартатом и АТФ в главном пути биосинтеза аспарагина. В имидазольном кольце гистидина азот 3 получается из глутамина. И наконец, глутамин используется глутаматоксоглутарат аминотрансферазой (глутамат синтазой) (GOGAT) в синтезе глутамата. В случае, когда пути биосинтеза вышеперечисленных аминокислот оптимизированы для их продукции, доступность глутамина становится одним из лимитирующих факторов. Исходя из вышесказанного, увеличение способности микроорганизма к продукции L-глутамина также приводит к увеличению способности микроорганизма к продукции L-аргинина, L-триптофана, L-гистидина и L-глутамата. Поэтому к способам согласно настоящему изобретению относится способ продукции L-аргинина, включающий стадии выращивания бактерии согласно настоящему изобретению в питательной среде с целью продукции и накопления L-аргинина в указанной питательной среде, и выделения L-аргинина из культуральной жидкости. Также к способам согласно настоящему изобретению относится способ продукции L-триптофана, включающий стадии выращивания бактерии согласно настоящему изобретению в питательной среде с целью продукции и накопления L-триптофана в указанной питательной среде, и выделения L-триптофана из культуральной жидкости. Также к способам согласно настоящему изобретению относится способ продукции L-гистидина, включающий стадии выращивания бактерии согласно настоящему изобретению в питательной среде с целью продукции и накопления L-гистидина в указанной питательной среде, и выделения L-гистидина из культуральной жидкости. И к способам согласно настоящему изобретению относится способ продукции L-глутамата, включающий стадии выращивания бактерии согласно настоящему изобретению в питательной среде с целью продукции и накопления L-глутамата в указанной питательной среде, и выделения L-глутамата из культуралыюй жидкости.
В способе согласно настоящему изобретению выращивание бактерии, принадлежащей к роду Escherichia, сбор и очистка L-глутамина из культуральной жидкости может быть осуществлена способом, подобным традиционным способам ферментации, в которых L-глутамин продуцируется с использованием бактерии. Также в способе согласно настоящему изобретению выращивание бактерии, принадлежащей к роду Escherichia, сбор и очистка L-аргинина из культуральной жидкости может быть осуществлена способом, подобным традиционным способам ферментации, в которых L-аргинин продуцируется с использованием бактерии. Также в способе согласно настоящему изобретению выращивание бактерии, принадлежащей к роду Escherichia, сбор и очистка L-триптофанана из культуральной жидкости может быть осуществлена способом, подобным традиционным способам ферментации, в которых L-триптофан продуцируется с использованием бактерии. Также в способе согласно настоящему изобретению выращивание бактерии, принадлежащей к роду Escherichia, сбор и очистка L-гистидина из культуральной жидкости может быть осуществлена способом, подобным традиционным способам ферментации, в которых L-гистидин продуцируется с использованием бактерии. Также в способе согласно настоящему изобретению выращивание бактерии, принадлежащей к роду Escherichia, сбор и очистка L-глутамата из культуральной жидкости может быть осуществлена способом, подобным традиционным способам ферментации, в которых L-глутумат продуцируется с использованием бактерии.
Питательная среда, используемая для выращивания, может быть как синтетической, так и натуральной, при условии, что указанная среда содержит источники углерода, азота, минеральные добавки и, если необходимо, соответствующее количество питательных добавок, которые требуются микроорганизму для роста. К источникам углерода относятся различные углеводы, такие как глюкоза и сахароза, и различные органические кислоты. В зависимости от степени ассимиляции используемого микроорганизма могут использоваться спирты, такие как этанол и глицерин. В качестве источника азота могут использоваться аммиак, различные соли аммония, такие как сульфат аммония, другие соединения азота, такие как амины, природные источники азота, такие как пептон, гидролизат соевых бобов и ферментолизат микроорганизмов. В качестве минеральных добавок используются монофосфат калия, сульфат магния, хлорид натрия, сульфат железа, сульфат марганца, хлорид кальция. Некоторые питательные добавки могут быть добавлены в питательную среду, если необходимо. Например, если микроорганизму для роста необходим изолейцин (ауксотрофия по изолейцину), подходящее количество изолейцина может быть добавлено в питательную среду для ферментации.
Выращивание осуществляется предпочтительно в аэробных условиях, таких как перемешивание, ферментация с аэрацией, при температуре от 20 до 40°С, предпочтительно от 30 до 38°С. Обычно выращивание осуществляют при рН питательной среды в пределах от 5 до 9, предпочтительно от 6,5 до 7,2. рН среды может регулироваться аммиаком, карбонатом кальция, различными кислотами, основаниями и буферами. Обычно выращивание в течение от 1 до 3 дней приводит к накоплению целевой L-аминокислоты в культуральной жидкости.
Выделение L-глутамина после выращивания может быть осуществлено путем удаления из культуральной жидкости твердых остатков, такие как клетки, методом центрифугирования или фильтрацией, а затем L-глутамин может быть собран и очищен методами ионообменной хроматографии, концентрирования и кристаллизации или подобными им.
Краткое описание чертежа.
На чертеже показано относительное положение затравок SEQ ID NО:3, 4 и 5, использованных в ПУР при получении матунтного гена glnA.
Наилучший способ осуществления изобретения
Настоящее изобретение более детально описано со ссылкой на следующие примеры.
Пример 1. Клонирование мутантного реагента glnA.
Природный ген glnA был получен методом амплификации с помощью ПЦР и клонирован в вектор pMW118. Полученная плазмида была названа pMWglnA12. Хромосомная ДНК штамма E.coli К-12 была использована в качестве матрицы, олигонуклеотиды, приведенные в Списке последовательностей под номерами 3 и 4, использовались в качестве затравок. ПЦР проводили следующим образом: предварительная обработка при 94°С в течение 5 мин, затем 40 циклов при 55°С в течение 30 сек, 72°С в течение 2 мин и 93°С в течение 30 сек. Полученный таким образом продукт ПЦР был обработан рестриктазами ХbаI и HindIII и лигирован в вектор pMW118, предварительно обработанный теми же рестриктазами. Полученная плазмида была названа pMWglnA12. Для замены кодона ТАТ, кодирующего тирозин-397 в белке GS, кодоном ТТТ, кодирующим фенилаланин, была использована процедура сайт-направленного мутагенеза. Плазмида pMWglnA12, содержащая природный ген glnA, использовалась в качестве матрицы, олигонуклеотиды, приведенные в Списке последовательностей под номерами 4 и 5, использовались в качестве затравок. ПЦР проводили следующим образом: 55°С в течение 30 сек, 72°С в течение 1 мин и 94°С в течение 30 сек, 25 циклов. Полученный таким образом продукт ПЦР был обработан рестриктазами NcoI и НindIII и лигирован в плазмиду pMWglnA12, предварительно обработанную теми же рестриктазами. Полученная плазмида была названа pMWglnAphe-4.
Пример 2. Конструирование штамма, дефицитного по ilvA, - производного штамма E.coli К-12, содержащего мутацию в гене ilvA.
Штамм VL334 (ВКПМ В-1641) является штаммом, ауксотрофным по изолейцину и треонину, содержащим мутации в генах thrC и ilvA (патент США 4278765). Аллель дикого типа гена thrC был перенесен методом общей трансдукции с использованием бактериофага Р1, выращенного на природном штамме E.coli К-12 (ВКПМ В-7). В результате был получен штамм VL334thrC+.
Затем плазмида pMWglnAphe-4 была введена в клетки штамма VL334thrC+. Полученный штамм был назван VL334thrC+/pMWglnAphe-4. В качестве контроля плазмида pMWglnA12 также была введена в клетки штамма VL334thrC+. Полученный штамм был назван VL334thrC+/pMWglnA12.
Пример 3. Продукция глутамина и глутаминовой кислоты штаммом, содержащим мутантный ген glnA, при ферментации в пробирках.
Условия выращивания при ферментации в пробирках были следующие. Питательная среда для ферментации содержала 60 г/л глюкозы, 35 г/л сульфата аммония, 2 г/л К2НРO4, 1 г/л MgSO4, 0,1 мг/л тиамина, 50 мг/л L-изолейцина, 5 г/л дрожжевого экстракта Difco, 25 г/л мела (рН 7,2). Глюкоза и мел стерилизовались раздельно. 2 мл питательной среды помещались в пробирку, засевались одной петлей тестируемых микроорганизмов, и выращивание продолжалось при 37°С в течение 2 дней с перемешиванием. Накопленное в культуральной жидкости количество глутамина и глутаминовой кислоты было определено с помощью тонкослойной хроматографии (ТСХ). Состав подвижной фазы для ТСХ: изопропанол: этилацетат: NH4ОH: H2O=16:8:5:10 (v/v). Результаты приведены в таблице.
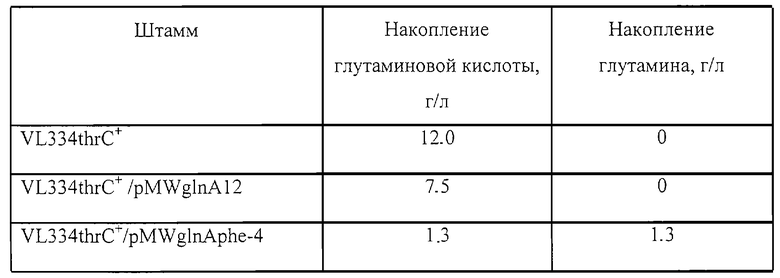
Как видно из таблицы, штамм VL334thrC+/pMWglnAphe-4, содержащий мутантный ген glnA, приобрел способность к продукции L-глутамина.



Аминокислоты, такие как L-глутамин, L-аргинин, L-триптофан,L-гистидин и L-глутамат получают культивированием бактерии, принадлежащей к роду Escherichia, трансформированной фрагментом ДНК, кодирующим мутантную глутаминсинтетазу, в которой аминокислотный остаток тирозина, соответствующий положению 397 в природной глутаминсинтетазе, заменен остатком другой аминокислоты, предпочтительно фенилаланином. В качестве штамма-продуцента может быть использован штамм Escherichia coli VL334thrC+/pMWglnAphe-4. 4 с. и 5 з.п. ф-лы, 1 ил., 1 табл.

| ФРАГМЕНТ ДНК ИЗ ESCHERICHIA COLI, ОПРЕДЕЛЯЮЩИЙ ПОВЫШЕННУЮ ПРОДУКЦИЮ L-АМИНОКИСЛОТ (ВАРИАНТЫ), И СПОСОБ ПОЛУЧЕНИЯ L-АМИНОКИСЛОТ | 1999 |
|
RU2175351C2 |
| US 4430430, 07.02.1984 | |||
| US 4278765, 14.07.1981. | |||
Авторы
Даты
2004-06-10—Публикация
2001-11-30—Подача