Изобретение относится к биотехнологии и, в частности, касается способа получения L-аминокислот, а именно L-глутаминовой кислоты, L-лизина, L-треонина, L-аланина, L-гистидина, L-пролина, L-аргинина, L-валина, или L-изолейцина с помощью бактерий, принадлежащих к роду Escherichia.
Для получения аминокислот с помощью ферментации используются штаммы, выделенные из природных источников, или с целью увеличения продуктивности применяют специально полученные мутанты этих штаммов. В случае L-лизина, например, известно много искусственных мутантов, продуцирующих эту аминокислоту. Большинство из них - это мутанты бактерий, устойчивые к S-2-аминоэтилцистеину, (АЭЦ) принадлежащие к родам Brevibacterium, Corynebucterium, Bacillus или Escherichia. Предложено много различных приемов для повышения продукции аминокислот, например, таких как трансформация рекомбинантными ДНК (Патент США N 4278765). Эти приемы в большинстве случаев основаны на повышении активности ферментов, участвующих в биосинтезе аминокислоты, и/или в придании ключевому ферменту нечувствительности к ингибирующему действию конечного продукта и т. п. (См. Выложенную заявку на патент в Японии N 56- 18596 (1981) и международную заявку WO N 95/16042).
C другой стороны, как пример повышения продуктивности штамма-продуцента аминокислоты путем увеличения экскреции этой аминокислоты известен штамм, принадлежащий к роду Corynebacterium, у которого повышена активность гена экскреции лизина, lysE (Vrljic et al., Mol. Microbiol., 22, 815-826, 1996). Однако в отношении бактерий, принадлежащих к роду Escherichia, наличие белков, обеспечивающих экскрецию этой или какой-либо другой аминокислоты, остается неизвестным. Поэтому неизвестно также, может ли повышение активности белка экскреции повысить продукцию аминокислоты в случае бактерий, принадлежащих к роду Escherichia.
Хотя на сегодня известна нуклеотидная последовательность всей хромосомы штамма Escherichia coli К-12, принадлежащего к роду Escherichia (Science, 227, 1453-1474, 1997), имеется большое число генов, кодирующих трансмембранные белки, функция которых остается неизвестной. Среди них могут быть и белки, участвующие в процессе транспорта аминокислот из клеток бактерий.
Задачей настоящего изобретения является повышение продуктивности штаммов-продуцентов L-аминокислот и разработка на этой основе нового способа получения L-аминокислот биотехнологическим методом.
Поставленную задачу решают путем выявления генов, контролирующих синтез белков, участвующих в экскреции L-аминокислот у Е. coli, и конструирования на их основе штаммов-продуцентов, позволяющих разработать способ получения L- аминокислот, а именно L-глутаминовой кислоты, L-лизина, L- треонина, L-аланина, L-гистидина, L-пролина, L-аргинина, L-валина, или L-изолейцина с повышенным выходом целевой аминокислоты.
Предметом настоящего изобретения являются бактерии (в дальнейшем рассматриваемые как "бактерии по настоящему изобретению"), принадлежащие к роду Escherichia, обладающие способностью к продукции аминокислот, у которых эта способность повышена в результате увеличения экспрессируемого количества, по крайней мере, одного из белков, принадлежащих к группе, состоящей из следующих белков, поименованных в пунктах от А по H:
А - белок, который состоит из аминокислотной последовательности N 5 (Фиг. 1);
В - белок, который состоит из аминокислотной последовательности, включающей также делеции, замены, вставки или добавки из одной или нескольких аминокислот к последовательности N 5, и который имеет активность, обеспечивающую бактериям, содержащим этот белок, повышенную продукцию L-аминокислот;
С - белок, который состоит из аминокислотной последовательности N 6 (Фиг. 2);
D - белок, который состоит из аминокислотной последовательности, включающей также делеции, замены, вставки или добавки из одной или нескольких аминокислот к последовательности N 6, и который имеет активность, обеспечивающую бактериям, содержащим этот белок, повышенную продукцию L-аминокислот;
E - белок, который состоит из аминокислотной последовательности N 7 (Фиг. 3);
F - белок, который состоит из аминокислотной последовательности, включающей также делеции, замены, вставки или добавки из одной или нескольких аминокислот к последовательности N 7, и который имеет активность, обеспечивающую бактериям, содержащим этот белок, повышенную продукцию L-аминокислот;
G - белок, который состоит из аминокислотной последовательности N 8 (Фиг. 4);
H - белок, который состоит из аминокислотной последовательности, включающей также делеции, замены, вставки или добавки из одной или нескольких аминокислот к последовательности N 8, и который имеет активность, обеспечивающую бактериям, содержащим этот белок, повышенную продукцию L-аминокислот.
Бактериями по настоящему изобретению являются: продуценты L-аминокислот, относящиеся к роду Escherichia, а именно: продуценты L-лизина, у которых экспрессируемое количество по крайней мере одного из белков, выбранных из группы, состоящей из белков, поименованных в п.п. с А по D, G и H, увеличено; продуценты L-глутаминовой кислоты, у которых экспрессируемое количество по крайней мере одного из белков, выбранных из группы, состоящей из белков, поименованных в п. п. с А по H, увеличено; продуценты L-аланина, у которых экспрессируемое количество по крайней мере одного из белков, выбранных из группы, состоящей из белков, поименованных в п.п. C и D, увеличено; продуценты L-валина, у которых экспрессируемое количество по крайней мере одного из белков, выбранных из группы, состоящей из белков, поименованных в п.п. C и D, увеличено; продуценты L-пролина, у которых экспрессируемое количество по крайней мере одного из белков, выбранных из группы, состоящей из белков, поименованных в п.п. с А по F, увеличено; продуценты L-треонина, у которых экспрессируемое количество по крайней мере одного из белков, выбранных из группы, состоящей из белков, поименованных в п.п. E и F, увеличено; продуценты L-гистидина, у которых экспрессируемое количество по крайней мере одного из белков, выбранных из группы, состоящей из белков, поименованных в п.п. с C по F, увеличено; продуценты L-аргинина, у которых экспрессируемое количество по крайней мере одного из белков, выбранных из группы, состоящей из белков, поименованных в п.п. G и H, увеличено; продуценты L-изолейцина, у которых экспрессируемое количество по крайней мере одного из белков, выбранных из группы, состоящей из белков, поименованных в п.п. C и D, увеличено.
В клетках бактерий по настоящему изобретению число копий ДНК, кодирующих указанные белки, может быть увеличено. Указанная ДНК в клетках этих бактерий преимущественно находится на многокопийном векторе или на транспозоне.
Настоящее изобретение также защищает способ получения аминокислот, который включает этапы:
культивирования бактерий, полученных в соответствии с настоящим изобретением и обладающих способностью к повышенной продукции аминокислот, в культуральной среде, обеспечивающей продукцию и накопление соответствующей аминокислоты в этой среде, и
выделения накопившейся аминокислоты из этой среды.
Этот способ получения аминокислот включает получение L-лизина с помощью бактерий, продуцирующих L-лизин, у которых экспрессируемое количество по крайней мере одного из белков, выбранных из группы, состоящей из белков, поименованных в п. п. с А по D, G и H, увеличено; получение L-глутаминовой кислоты с помощью бактерий, продуцирующих L-глутаминовую кислоту, у которых экспрессируемое количество по крайней мере одного из белков, выбранных из группы, состоящей из белков, поименованных в п.п. с А по H, увеличено; получение L- треонина с помощью бактерий, продуцирующих L-треонин, у которых экспрессируемое количество по крайней мере одного из белков, выбранных из группы, состоящей из белков, поименованных в п.п. E и F, увеличено; получение L-аланина с помощью бактерий, продуцирующих L-аланин, у которых экспрессируемое количество по крайней мере одного из белков, выбранных из группы, состоящей из белков, поименованных в п.п. C и D, увеличено; получения L-пролина с помощью бактерий, продуцирующих L-пролин, у которых экспрессируемое количество по крайней мере одного из белков, выбранных из группы, состоящей из белков, поименованных в п.п. с А по F, увеличено; получение L-валина с помощью бактерий, продуцирующих L-валин, у которых экспрессируемое количество по крайней мере одного из белков, выбранных из группы, состоящей из белков, поименованных в п.п. C и D, увеличено; получение L-изолейцина с помощью бактерий, продуцирующих L-изолейцин, у которых экспрессируемое количество по крайней мере одного из белков, выбранных из группы, состоящей из белков, поименованных в п.п. C и D, увеличено; получения L-гистидина с помощью бактерий, продуцирующих L-гистидин, у которых экспрессируемое количество по крайней мере одного из белков, выбранных из группы, состоящей из белков, поименованных в п.п. с C по F, увеличено; получения L-аргинина с помощью бактерий, продуцирующих L- аргинин, у которых экспрессируемое количество по крайней мере одного из белков, выбранных из группы, состоящей из белков, поименованных в п.п. G и H, увеличено.
Примеры, представленные в настоящем изобретении, касаются тех случаев, когда экспрессируемое количество белков увеличено за счет увеличения числа копий ДНК, кодирующих в клетках указанные белки.
В соответствии с настоящим изобретением способность продуцировать L-аминокислоты бактериями, принадлежащими к роду Escherichia, может быть усилена, а способ получения аминокислот может быть усовершенствован в том, что касается повышения продукции аминокислот.
Ниже следует детальное объяснение настоящего изобретения. В дальнейшем изложении, если не оговорено, имеются в виду L-стереоизомеры аминокислот.
1. Бактерии по настоящему изобретению.
Бактерии по настоящему изобретению представлены бактериями, принадлежащими к роду Escherichia и способными к продукции аминокислот, у которых эта способность повышена за счет повышения экспрессируемого количества белков, обладающих активностью, которая обеспечивает увеличенную продукцию аминокислот. В дальнейшем эти белки будут обозначены как "белки экскретирующие аминокислоты", однако этот термин не означает, что функция указанных белков ограничивается только экскрецией аминокислот. Примером белков, экскретирующих аминокислоты, являются белки, имеющие аминокислотные последовательности, представленные на Фиг. 1 (последовательность N 5), Фиг. 2 (Последовательность N 6), Фиг. 3 (Последовательность N 7) и Фиг. 4 (Последовательность N 8). Белки, экскретирующие аминокислоты, могут иметь специфичность по отношению к определенным аминокислотам. Эта специфичность может быть определена путем экспрессии соответствующих белков в клетках бактерий, принадлежащих к роду Escherichia, и установления факта повышения минимально ингибирующих концентраций определенных аминокислот или аналогов аминокислот. Кроме того, специфичность может быть определена путем экспрессии соответствующих белков в клетках указанных бактерий, обладающих способностью к продукции аминокислот, и установления факта повышения продукции этих аминокислот.
Например, в случае лизина белок, имеющий последовательность, показанную в списке последовательностей под номером 5, 6 или 8, обнаружил такого рода активность. В случае глутаминовой кислоты белок, имеющий последовательность, показанную в списке последовательностей под номером 5, 6, 7 или 8, обнаруживает такого рода активность. В случае треонина белок, имеющий последовательность, показанную в списке последовательностей под номером 7, обнаруживает такого рода активность. В случае аланина белок, имеющий последовательность, показанную в списке последовательностей под номером 6, обнаруживает такого рода активность. В случае валина белок, имеющий последовательность, показанную в списке последовательностей под номером 6, обнаруживает такого рода активность. В случае изолейцина белок, имеющий последовательность, показанную в списке последовательностей под номером 6, обнаруживает такого рода активность. В случае гистидина белок, имеющий последовательность, показанную в списке последовательностей под номером 6 и 7, обнаруживает такого рода активность. В случае пролина белок, имеющий последовательность, показанную в списке последовательностей под номером 5, 6 или 7, обнаруживает такого рода активность. В случае аргинина белок, имеющий последовательность, показанную в списке последовательностей под номером 8, обнаруживает такого рода активность.
Термин "экспрессируемое количество увеличено" используется в настоящем изобретении для обозначения того факта, что экспрессируемое количество белка больше, чем в исходных штаммах (штаммах "дикого типа"), например в штамме Е. coli MG1655 или Е. coli W3110. Этот термин означает также, что если штамм получен путем генетической модификации, например, с помощью методов генной инженерии и т.п., то экспрессируемое количество белка повышается в результате этой модификации. Экспрессируемое количество белка, экскретирующего аминокислоту, может быть прямо определено путем измерения количества белка, экскретирующего аминокислоту, или косвенно по эффекту этого белка на устойчивость бактерий рода Escherichia к аминокислотам и к аналогам аминокислот.
Способ повышения экспрессируемого количества белка, экскретирующего аминокислоту, включает методы, предполагающие увеличение числа копий ДНК, кодирующих этот белок. Для увеличения числа копий ДНК фрагмент ДНК, кодирующий указанный белок, лигируют с вектором, который может функционировать в бактериях, принадлежащих к роду Escherichia, с образованием рекомбинантной ДНК, которой затем трансформируют клетки бактерии-хозяина. При этом число копий гена, кодирующего белок, экскретирующий аминокислоту (гена белка, экскретирующего аминокислоту), в клетках трансформированных бактерий увеличивается, и таким образом повышается экспрессируемое количество белка, экскретирующего аминокислоту. Для этой цели можно использовать многокопийный вектор.
Кроме того, повышение экспрессируемого количества белка, экскретирующего аминокислоту, может быть достигнуто введением множества копий гена белка экскретирующего аминокислоту в хромосому бактерии-хозяина. Это введение в хромосому бактерий, принадлежащих к роду Escherichia, может быть осуществлено посредством гомологической рекомбинации с использованием в качестве мишеней последовательностей ДНК, множество копий которых существует в хромосоме. В качестве таковых могут быть использованы повторяющиеся последовательности в хромосомной ДНК и обращенные повторы транспозируемых элементов. Альтернативный метод предполагает введение в хромосомную ДНК множества копий гена белка, экскретирующего аминокислоту, с помощью интеграции его в транспозон и последующей индукции множественных актов транспозиции, как это описано в Выложенной заявке на патент в Японии N 2-109985 (1990). В результате осуществления любого из описанных выше подходов число копий гена белка, экскретирующего аминокислоту, увеличится и тем самым увеличится экспрессируемое количество белка, экскретирующего аминокислоту.
Мультикопийные векторы могут быть представлены плазмидными векторами, такими как pBR322, pMW118, pUC19 или подобными, или фаговыми векторами, такими как λ 1059, λ BF101, M13mp9 или подобными. Транспозоны могут быть представлены фагом Mu, транспозонами Tn10, Tn5 или подобными. Введение ДНК в клетки бактерий, принадлежащих к роду Escherichia, может быть осуществлено, например, с помощью метода Моррисона (Methods in Enzymology 68, 326, 1979), или с помощью метода, в котором реципиентные клетки бактерий подвергают воздействию хлористого кальция для увеличения их проницаемости по отношению к ДНК (Mandel and Higa, J. Mol. Biol., 53, 159, 1970), или с помощью другого подобного метода.
Кроме упомянутой выше амплификации генов, экспрессируемое количество белка, экскретирующего аминокислоту, может быть увеличено также путем замены экспрессирующей регуляторной последовательности, такой как промотор гена белка, экскретирующего аминокислоту на более сильный промотор (Выложенная заявка на патент в Японии N 1-215280 (1989)). В качестве сильных промоторов известны lac-промотор, trp- промотор, tac-промотор, PR-промотор и PL-промотор фага ламбда и другие. Замена промотора усиливает экспрессию гена белка, экскретирующего аминокислоту, и тем самым увеличивает экспрессируемое количество указанного белка. Усиление экспрессирующей регуляторной последовательности можно совмещать с увеличением числа копий гена белка, экскретирующего аминокислоту.
В бактериях по настоящему изобретению может быть повышено экспрессируемое количество нескольких белков, экскретирующих аминокислоты.
Белки, экскретирующие аминокислоты, кодируются известными генами (открытыми рамками считывания, ORF) yahN, yeaS, yfiK, yggA, функция которых неизвестна. Поэтому ДНК, кодирующие белки, экскретирующие аминокислоты, могут быть получены путем синтеза праймеров на основе известных последовательностей (например, полной нуклеотидной последовательности хромосомы Escherichia coli К-12, (Science, 277, 1453-1474, 1997)) и амплификации с помощью полимеразной цепной реакции (ПЦР) с использованием хромосомной ДНК бактерий, принадлежащих к роду Escherichia, в качестве матрицы. Кроме того, нужный фрагмент ДНК может быть отобран с помощью гибридизации из библиотеки генов хромосомной ДНК указанных бактерий путем применения зонда, изготовленного на основе известной последовательности. Альтернативный подход предполагает синтез ДНК гена, кодирующего белок, экскретирующий аминокислоту, на основе известной последовательности. Нуклеотидные последовательности фрагментов ДНК, кодирующих белки YahN, YeaS, YfiK и YggA, экскретирующие аминокислоты, представлены в приложении (Последовательности N 1-4).
Методы выделения хромосомной ДНК, получения библиотеки генов, ДНК-ДНК гибридизации, ПЦР, выделения и трансформации плазмидной ДНК, рестрицирования и лигирования ДНК, выбора нуклеотидов для праймеров и т.п. методы хорошо известны и детально описаны во многих руководствах, например, Sambrook, J., Fritsch Е. F. and Maniatis T. (1989) Molecular cloning: a laboratory manual, 2nd ed. Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N. Y.
Белки, экскретирующие аминокислоты, могут содержать делеции, замены, инсерции или добавки в одну или несколько аминокислот в одной или нескольких позициях, не нарушающих при этом активность белка, обеспечивающую повышенную устойчивость к аминокислотам и/или аналогам и повышенную продукцию аминокислот. Термин "несколько" может варьировать в зависимости от положения в пространственной структуре белка или характера аминокислотного остатка. Это связано с тем, что некоторые аминокислоты, такие, например, как изолейцин и валин, имеют высокое сходство друг с другом, и различие между этими аминокислотами заметно не влияет на пространственную структуру белка. Поэтому может существовать белок, который имеет гомологию не менее 70%, а предпочтительнее не менее 90% по отношению ко всей аминокислотной последовательности белка, экскретирующего аминокислоту, и который обладает активностью, повышающей способность к продукции аминокислот бактериями, принадлежащими к роду Escherichia и содержащими этот белок. В частности, "несколько" может соответствовать числам от 20 до 60, но преимущественно от 2 до 20.
Фрагменты ДНК, кодирующие по существу те же белки, что и белки, экскретирующие аминокислоты, описанные выше, могут быть получены, например, путем модификации нуклеотидной последовательности, в частности при помощи сайтнаправленного мутагенеза, так что один или более аминокислотный остаток будет делетирован, заменен, вставлен или добавлен. ДНК, модифицированная описанным выше способом, может быть получена известными методами с помощью мутационных воздействий. Мутационная обработка включает методы обработки ДНК, кодирующей белок, экскретирующий аминокислоту in vitro, например, при помощи гидроксиламина, или методы обработки микроорганизма, в частности бактерий, принадлежащих к роду Escherichia и несущих ДНК, кодирующую белок, экскретирующий аминокислоту, УФ облучением, или мутагенными агентами, такими как N-метил-N'-нитро-N-нитрозогуанидин (НГ) или азотистая кислота, которые обычно используется для индукции мутаций.
Фрагменты ДНК, кодирующие указанные варианты белков, экскретирующих аминокислоты, отбирают путем экспрессии в клетках бактерий рода Escherichia плазмидной ДНК, несущей ген, кодирующий указанный белок, и подвергнутой in vitro мутагенному воздействию, как описано выше, с последующим определением их устойчивости к высокой концентрации аминокислоты и/или аналога аминокислоты и/или способности повышать продукцию аминокислоты.
Изобретение относится также к вариантам белков, экскретирующих аминокислоты, которые встречаются в разных видах, штаммах и вариантах бактерий рода Escherichia и обусловлены природным разнообразием. ДНК, кодирующих эти варианты, и которые гибридизуются в жестких условиях с ДНК, имеющими нуклеотидные последовательности с 1 по 4, показанные в формуле изобретения.
Термин "жесткие условия" означает здесь условия, при которых так называемая специфическая гибридизация происходит, а неспецифическая не происходит. Трудно четко выразить эти условия с помощью каких-то цифровых значений. Однако например, жесткие условия включают условия, при которых ДНК, имеющие высокую гомологию, например не менее 70% гомологии по отношению друг к другу гибридизуются, а ДНК, имеющие гомологию ниже указанной величины, не гибридизуются (условия отмывки при гибридизации по Саузерну: 60oC, растворами 1 х SSC, 0.1% SDS, или предпочтительнее растворами 0.1 х SSC, 0.1% SDS, которые являются обычными условиями при гибридизации по Саузерну).
Среди отобранных таким образом генов могут встречаться гены с появившимся в их средней части стоп-кодоном или гены, кодирующие белок, который утратил активность в результате мутации в активном центре. Такие дефектные гены легко элиминируются после лигирования их с коммерчески доступными экспрессионными векторами и определения способности повышать устойчивость к аминокислотам или аналогам или повышать продукцию аминокислот бактериями, принадлежащими к роду Escherichia, как это описано выше.
Термин "ДНК кодирующая белок", обозначает двунитевую ДНК, одна из нитей которой кодирует белок.
Увеличив экспрессируемое количество белка, экскретирующего аминокислоту в клетках штамма-продуцента, как это описано выше, можно повысить продукцию соответствующей аминокислоты. При этом возможны два варианта:
1. Признак повышенного экспрессируемого количества белка, экскретирующего аминокислоту, вводят в штамм, уже способный продуцировать желаемую аминокислоту.
2. Способность к продукции аминокислот придается штаммам, у которых экспрессируемое количество белка, экскретирующего аминокислоту, уже повышено.
Примеры бактерий, продуцирующих аминокислоты и принадлежащих к роду Escherichia, приведены ниже.
Продуцент глутаминовой кислоты.
В качестве продуцента глутаминовой кислоты может быть представлен штамм Е.coli AJ13199 (Патент Франции N 2747689).
Лизин-продуцирующие бактерии
Продуцент лизина, принадлежащий к роду Escherichia, представлен штаммом Е.coli W3110 (tyrA) (Европейский патент N 488424), в который введена плазмида pCABD2 (Международная заявка WO 95/16042). Штамм W3110 (tyrA) был сконструирован следующим образом. Штамм Е.coli W3110, который хранится в Национальном Институте Генетики (Япония), высевали на чашку с LB-агаром, содержащим стрептомицин, и отбирали стрептомицин-устойчивый мутант. Клетки этого мутанта смешивали с клетками штамма Е. coli К-12 МЕ8424 и подращивали в L-бульоне (состав: 1% бактотриптона, 0.5% дрожжевого экстракта, 0.5% NaCI) при 37oC в течение 15 минут для индукции конъюгации. Штамм Е. coli К-12 МЕ8424 хранится в Национальном Институте Генетики (Япония) и имеет следующие генетические характеристики: (HfrPO45, thi, relA1, tyr::Tn10, ung-1, nadB). Затем, высевая эту суспензию бактерий на полноценную питательную среду (агаризованный L-бульон, содержащий стрептомицин, тетрациклин и тирозин), получили штамм Е. coli W3110 (tyrA). Плазмида pCABD2 может быть получена интеграцией фрагмента, содержащего ген ddh, и фрагмента, содержащего ген dapB, которые амплифицировали из хромосомы Е.coli W3110 на основе известной последовательности, в плазмиду RSED80. Штамм Е. coli, несущий плазмиду RSFD80, депонирован в Национальном Институте Биологических Наук и Гуманитарных Технологий Агентства Промышленной Науки и Технологии (Япония) 28 октября 1993 года под номером FERM Р-13936, откуда он передан в международный депозитарий по Будапештскому договору от 1 ноября 1994 года и получил номер хранения FERM ВР-4859.
Кроме того, в качестве продуцента лизина, принадлежащего к роду Escherichia, используют штамм Е. coli VL614. Этот штамм является производным известного штамма VL613 (Авторское свидетельство СССР N 1354458). Штамм VL613 в свою очередь получен на основе известного штамма Gif 102 (Theze, J. and Saint Girons. J. Bacteriol., 118, 990-998, 1974) в три этапа. На первом этапе был получен мутант этого штамма, устойчивый к 2 мг/мл S(2-аминоэтил)-L-цистеина. На втором этапе мутация rhtA23, сообщающая клеткам устойчивость к высоким концентрациям треонина и гомосерина (ABSTRACTS of 17th International Congress of Biochemistry and Molecular Biology in conjugation with 1997 Annual Meeting of the American Society for Biochemistry and Molecular Biology, San Francicco, California August 24-29, 1997, N 457), была введена в клетки штамм VL611 из штамма ВКПМ В-3996 (Патент США N 5175107) с помощью трансдукции фагом P1. Трансдуктант, отобранный по устойчивости к 10 мг/мл гомосерина обозначен, как штамм VL612. На третьем этапе с помощью трансдукции фагом P1 в этот штамм была введена плазмида pVG478, содержащая гены, связанные с усвоением сахарозы, локализующиеся на транспозоне Tn2555 (Дорошенко и др., Молекулярная генетика, микробиология и вирусология, N 6, 23-28, 1987). Так был получен штамм VL613. Штамм VL614 получают трансдукцией с помощью фага P1 в этот штамм дикого аллеля гена rhtA, сцепленного с транспозоном Tn10, из штамма VKPM В-6204 (zbi- 3058::Tn10). Трасдуктанты отбирают на среде LB с тетрациклином (10 мг/л) и среди них находят клоны, чувствительные на минимальной среде к гомосерину (10 г/л), (т.е.получившие rhtA+ аллель).
Треонин-продуцирующие бактерии
Продуцент треонина, принадлежащий к роду Eschsrichia, представлен штаммом VL2054. Этот штамм является производным известного штамма Е. coli ВКПМ В-3996 (Патент США N 5 175 107) и получен на его основе в два этапа. Сначала из штамма Е. coli ВКПМ В-3996 элиминируют плазмиду pVIC40. В полученном бесплазмидном реципиенте известным методом получают мутацию, повреждающую ген kan транспозона Tn5, интегрированного в ген tdh. В результате штамм становится чувствительным к канамицину, но ген tdh остается инактивированным. Затем с помощью фага P1 трансдуцируют сцепленный с транспозоном Tn10 дикий аллель гена rhtA, связанный с устойчивостью к гомосерину и треонину из штамма VKPM В-6204 (zbi-3058::Tn10). Трансдуктанты отбирают на среде LB с тетрациклином (10 мг/л) и среди них находят клоны, чувствительные на минимальной среде к 10 г/л гомосерина, (т.е.получившие rhtA+ аллель).
На втором этапе в интегративный вектор мини-Mu(Mud) клонируют гены треонинового оперона из плазмиды pVIC40 под PR-промотором фага ламбда и ген cat устойчивости к хлорамфениколу. Полученную конструкцию известным методом (Патент США N 5595889) интегрируют в штамм E.coli C600, откуда ее с помощью трансдукции фагом P1 переносят в полученный на первом этапе штамм. Таким образом получают штамм Е.coli VL2054, который является бесплазмидным продуцентом треонина. Кроме треонина в процессе ферментации штамм Е. coli VL2054 способен накапливать также небольшие количества аланина, валина и изолейцина.
Гистидин-продуцирующие бактерии
В качестве продуцента гистидина, принадлежащего к роду Escherichia, представлен штаммом Е. coli VL2160. Этот штамм получают на основе известного штамма NK5526 hiG::Tn10 (ВКПМ В-3384) путем переноса в него мутации hisGR, нарушающей ингибирование гистидином АТФ- фосфорибозилтрансферазы, с помощью трансдукции фагом P1 из штамма CC46 (Аствацатурянц и др., Генетика, т. 24, с. 1928-1934, 1988).
Пролин-продуцирующие бактерии
В качестве продуцента пролина, принадлежащего к роду Escherichia, представлен штамм Е. coli VL2151 (W3350 proB* ΔputAP,Tn10), сконструированный на основе известного штамма W3350 (Campbell A. Viroligy 14, 22-32, 1961) путем введения в него с помощью трансдукции фагом P1 сцепленной с транспозоном Tn10 (zcc-282: :Tn10 из штамма ВКПМ В-6194)) мутации ΔputAP и последующей селекции мутанта, устойчивого к 3,4-дегидро-DL-пролину, способного накапливать пролин.
Аргинин-продуцирующие бактерии
В качестве продуцента аргинина, принадлежащего к роду Escherichia coli, используют штамм Е. coli W3350 argE::Tn10/рКА10. Этот штамм является производным известного штамма W3350 (Campbell A. Viroligy 14, 22-32, 1961). Он имеет исерционную мутацию argE::Tn10 и содержит плазмиду рКА10, несущую фрагмент ДНК из Corynebaclerium (Brevibacterium)flavum, комплементирующий по крайней мере мутации argA и argE в реципиентном штамме Е. coli (Харитонов А. А. , Тарасов А. П. Молекулярная генетика, микробиология, вирусология, N 9, 29-33, 1986).
Гены белков, экскретирующих аминокислоты по настоящему изобретению, были идентифицированы впервые, как это описано ниже.
Ранее авторы настоящего изобретения идентифицировали гены rhtB и rhtC как гены белков экскреции гомосерина и треонина у Escherichia coli. Далее, основываясь на предположении о том, что белки экскреции аминокислот должны иметь какое-то сходство в своей структуре, был осуществлен поиск белков, гомологичных RhtB.
Поиск гомологов осуществляли: с помощью программы BLAST и PSI-BLAST (Altschul, et al., Nucleic Acids Res. 25:3389-3402, 1997) в базах данных GenBank CDS translations, PDB, SwissProt, Spupdate и PIR; с помощью программы BLITZ (Sturrock, S. S., and J. F. Collins. MPsch version 1.3. Biocomputing research unit. University of Edinburgh, UK (1993)) в базе данных SWALL, и с помощью программы SMART (Ogiwara, I. et al., Protein Sci. 5, 1991-1999 (1996) в базе транслированных генов SWISS PROT. Из более 60 обнаруженных гомологичных последовательностей гены из Е. coli yeaS (кодирует f212 в последовательности N AE 000274 в базе данных GenBank), yahN (кодирует f223 в последовательности N AE 000140 в базе данных GenBank), yfiK (кодирует 0195 в последовательности N AE 000344 в базе данных GenBank) nyggA (кодирует f211 в последовательности N AE 000375 в базе данных GenBank) могут иметь функцию, сходную с функцией RhtB. Эти гены были выделены и клонированы на плазмидных векторах в клетках Е. coli. Затем определяли влияние повышенного экспрессируемого количества продуктов этих генов на чувствительность клеток бактерий Е. coli к высоким концентрациям аминокислот и аналогов аминокислот, а также на продукцию аминокислот. В результате была установлена повышенная устойчивость бактерий, содержащих плазмиды с генами yeaS, yahN, yfiK и yggA, к определенным аминокислотам и их аналогам. Кроме того, была обнаружена повышенная продуктивность штаммов-продуцентов аминокислот, содержащих указанные плазмиды. Установлено также, что в этом отношении гены yahN, yeaS, yfiK и yggA могут обладать как определенной избирательностью, так и проявлять множественный эффект.
2. Получение аминокислот по настоящему изобретению.
Получение аминокислот с помощью штаммов-продуцентов бактерий, полученных в соответствии с настоящим изобретением, включает этапы культивирования штаммов в питательной среде, обеспечивающей продукцию и накопление соответствующей аминокислоты в этой среде, и последующего выделения накопившейся аминокислоты из этой среды.
К числу аминокислот, которые получают по настоящему изобретению, относятся лизин, треонин, глутаминовая кислота, гистидин, аланин, пролин, аргинин, валин и изолейцин.
В соответствии с настоящим изобретением культивирование бактерий, принадлежащих к роду Escherichia, выделение и очистку аминокислоты из культуральной жидкости осуществляют известными методами. Для культивирования используют синтетическую или натуральную среду. Такая среда включает источник углерода, азота, минеральные соли и необходимые добавки в количествах, оптимальных для роста и биосинтеза. В качестве источника углерода используют различные углеводы, такие как глюкоза, сахароза, различные органические кислоты. В зависимости от ассимилирующих способностей можно применять спирты, включая этанол или глицерол. В качестве источника азота используют аммиак, различные соли аммония, такие как сульфат аммония, или другие азотсодержащие соединения, такие как амины, а также природные источники азота, такие как пептон, гидролизат соевых бобов, или гидролизат микробных клеток. В качестве минеральных компонентов используются фосфат калия однозамещенный, сульфат магния, хлористый натрий, сульфат железа, сульфат марганца, карбонат кальция. Культивирование преимущественно осуществляют в аэробных условиях, таких как культивирование на мешалке, или с аэрацией и перемешиванием культуры. Температура культивирования от 30 до 40oC, преимущественно 30-38oC. pH среды 5-9, преимущественно 6,5-7,2. pH среды доводят до желаемых значений с помощью аммония, карбоната кальция, различных кислот, оснований или буферов. Культивирование осуществляют в течение 1-3 дней. После завершения культивирования выделение аминокислоты осуществляют путем удаления твердых частиц, таких как клетки, из среды с помощью центрифугирования или фильтрации через мембранные фильтры с последующим выделением и очисткой целевой аминокислоты с помощью ионообменника, фракционирования с помощью концентрации и кристаллизации.
Перечень фигур.
Фиг. 1. Последовательность белка YahN.
Фиг. 2. Последовательность белка YeaS.
Фиг. 3. Последовательность белка YfiK.
Фиг. 4. Последовательность белка YggA.
Настоящее изобретение более конкретно поясняют нижеследующие примеры.
Пример 1. Получение фрагментов ДНК yahN, yeaS, yfiK и ayggA, кодирующих синтез белков, экскретирующих аминокислоты.
Полная нуклеотидная последовательность хромосомы Escherichia coli К-12 известна (Science, 277, 1453-1474, 1997). На ее основе синтезируют праймеры, которые используют для амплификации фрагментов ДНК (генов) yahN, yeaS, yfiK и ayggA, кодирующих синтез белков, экскретирующих аминокислоты с помощью полимеразной цепной реакции (ПЦР).
(1). В качестве матрицы используют хромосомную ДНК штамма Echerichia coli MG1655, которую выделяют по стандартной методике (Sambrook, J., Fritsch Е. F. and Maniatis T. (1989) Molecular cloning: a laboratory manual, 2nd ed. Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N. Y.). Амплификацию проводили в термоциклере Techne PHC2, используя Tag-полимеразу (Fermentas); условия реакции подбирают в зависимости от температуры плавления праймеров и размеров амплифицируемого фрагмента, как это описано в руководствах (PCR protocols. Current methods and applications. White, B.A., ed. Humana Press, Totowa, New Jersey, 1993). Полученные продукты PCR очищают стандартным способом и рестрицируют, как описано ниже.
Для амплификации гена yahN используют праймеры N 1 и N 2.
Праймер N 1: gtgtggaaccgacgccggat (последовательность, комплементарная последовательности нуклеотидов с 1885 по 1704 в последовательности АЕ000140, хранящейся в базе данных GenBank).
Праймер N 2: tgttgtatggtacggggttcgag (последовательность с 223 по 245 нуклеотид там же).
Полученный продукт ПЦР рестрицируют ферментами PstI, StuI и, используя набор для лигирования, объединяют с вектором pUC21 (Vieira, Messing, Gene, 100, 189-194, 1991), обработанным ферментами PstI и EcoRV. Продуктом лигирования трансформируют компетентные клетки штамма E.col1 TGI (Sambrook, J., Fritsch Е. F. and Maniatis T. (1989) Molecular cloning: a laboratory manual, 2nd ed. Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N. Y.). Клетки высевают на L-arap (бактотриптон -10 г/л, дрожжевой экстракт - 5 г/л, NaCl - 5 г/л NaCl, агар - 15 г/л, pH 7.0), содержащий 10 мкг/мл IPTG (изопропил-β-В-тиогалактопиранозид) и 40 мкг/мл X-gal (5-бромо-4- хлоро-3-индолил-β-D-галактозид) and 100 мкг/мл ампицилина и выращивают в течение ночи. Появляющиеся белые колонии отбирают и рассевают до отдельных колоний на L-агаре с ампициллином. Из нескольких независимых очищенных таким образом трансформантов выделяют щелочным методом плазмидную ДНК и анализируют ее с помощью подходящих рестрицирующих ферментов. В результате получают плазмиду pYAHN.
Для амплификации reнa yeaS используют праймеры N 3 и N 4.
Праймер N 3: ctttgccaatcccgtctccc (последовательность, комплиментарная нуклеотидам с 7683 по 7702 в последовательности АЕ000274 в GenBank).
Праймер N 4: gccccatgcataacggaaag (последовательность с 5542 по 5561 нуклеотид там же).
Полученный продукт ПЦР рестрицируют ферментом Aval, и лигируют с вектором pUC19, и проводят описанные выше манипуляции. В результате получают плазмиду pYEAS.
Для амплификации гена yfiK используют праймеры N 5 и N 6.
Праймер N 5: gaagatcttgtaggccggataaggcg (последовательность с 4155 по 4177 нуклеотид в последовательности АЕ000344 в GenBank, с добавленными на 5' конце нуклеотидами, образующими сайт для BglII).
Праймер N 6: tggttttaccaattggccgc (последовательность, комплиментарная нуклеотидам с 6307 по 6326 в той же последовательности).
Полученный продукт ПЦР рестрицируют ферментами BglII, MunI, и лигируют с вектором pUC21 рестрицированным ферментами BglII и EcoRl, и проводят описанные выше манипуляции. В результате получают плазмиду pYFIK.
Для амплификации reнa yggA используют праймеры N 7 и N 8.
Праймер N 7: acttctcccgcgagccagttc (последовательность, комплиментарная последовательности нуклеотидов с 9606 по 9626 в последовательности АЕ000375 в GenBank).
Праймер N 8: ggcaagcttagcgcctctgtt (последовательность с 8478 по 8498 нуклеотид, там же).
Продукт ПЦР рестрицируют ферментами HindIII и ClaI, и лигируют с вектором рОК12 (Vieira, Messing, Gene, 100, 189-194, 1991), и проводят описанные выше манипуляции. В результате получают плазмиду pYGGA.
Полученными плазмидами трансформируют известный штамм Е. coli TG1 и штаммы Е. coli - продуценты аминокислот.
(2). В качестве матрицы используют хромосомную ДНК штамма Echerichia coli W3110, которую выделяют по стандартной методике, как описано выше.
Для амплификации гена yahN используют праймеры N 9 и N 10:
Праймер N 9: ggcgagctcccagtaaccggaaataag (последовательность, комплементарная последовательности нуклеотидов с 1230 по 1247 в АЕ000140, GenBank с добавленным на 5' конце нуклеотидами, образующими сайт для рестрицирующего фермента SacI,).
Праймер N 10: cgctctagaaaggaccacgcattacgg (последовательность с 429 по 446 нуклеотид с добавленными на 5' в конце нуклеотидами, образующими сайт для рестриктазы XbaI).
Для амплификации гена yeaS используют праймеры N 11 и N 12.
Праймер N 11: ggcgagctcagattggttagcatattc (последовательность, комплиментарная последовательности нуклеотидов с 6542 по 6560 в АЕ000274 в GenBank с добавленными на 5' конце нуклеотидами, образующими сайтом для распознавания рестриктазой Sacl).
Праймер N 12: cggtctagaatcagcgaagaatcaggg- (последовательность с 5799 по 5816 нуклеотид с сайтом распознавания для рестриктазы XbaI, добавленным на 5'-конце).
Для амплификации гена yfiK используют праймеры N 13 и N 14.
Праймер N 13: ggcgagctcatgttccgtgtcgggtac (последовательность с 5192 по 5209 нуклеотид в последовательности АЕ000344 в GenBank с добавленными на 5' конце нуклеотидами, образующими сайт для распознавания ферментом Sacl).
Праймер N 14: ggctctagatagcaagttactaagcgg (последовательность, комплиментарная последовательности нуклеотидов с 5871 по 5854 нуклеотид с добавленными на 5' конце нуклеотидами, образующими сайт для распознавания ферментом XbaI).
Для амплификации гена yggA используют праймеры N 15 и N 16.
Праймер N 15: ctctgaattctctcttattagtttttctgattgcc (последовательность, комплиментарная последовательности нуклеотидов с 9236 по 9270 в последовательности АЕ000375 в GenBank, с добавленными на 5' конце нуклеотидами, образующими сайт для распознавания ферментом EcoRI).
Праймер N 16: cgtgacctgcagcgttctcacagcgcggtagcctttaa (последовательность с 8075 по 8112 нуклеотид с добавленными на 5' конце нуклеотидами, образующими сайт для распознавания PstI).
Полученные продукты ПЦР очищают, как описано выше, рестрицируют ферментами SacI и XbaI (EcoRI и PstI для yggA) и лигируют с вектором pMW118, рестрицированным аналогичными ферментами. Нуклеотидную последовательность полученных вставок определяют с помощью ABI PRISM BigDye Terminator Cycle Sequence Ready Reaction Kit (PE Applied Biosystems) и автоматическим секвенатором ДНК (РЕ Applied Biosystems). Плазмиды, у которых нуклеотидная последовательность вставок соответствовала приведенной в GenBank, были отобраны и названы, соответственно:
несущая ген yahN: pMW 118::yahN
несущая ген yeaS: pMW 118::yeaS
несущая ген yfiK: pMW 118::yfiK
несущая ген yggA: pMW 118::yggA
Полученными плазмидами трансформируют известный штамм JM109 и штамм-продуцент лизина.
Пример 2. Влияние фрагментов ДНК yahN, yeaS, yfiK и yggA на устойчивость бактерий Е. coli к некоторым аминокислотам и аналогам аминокислот.
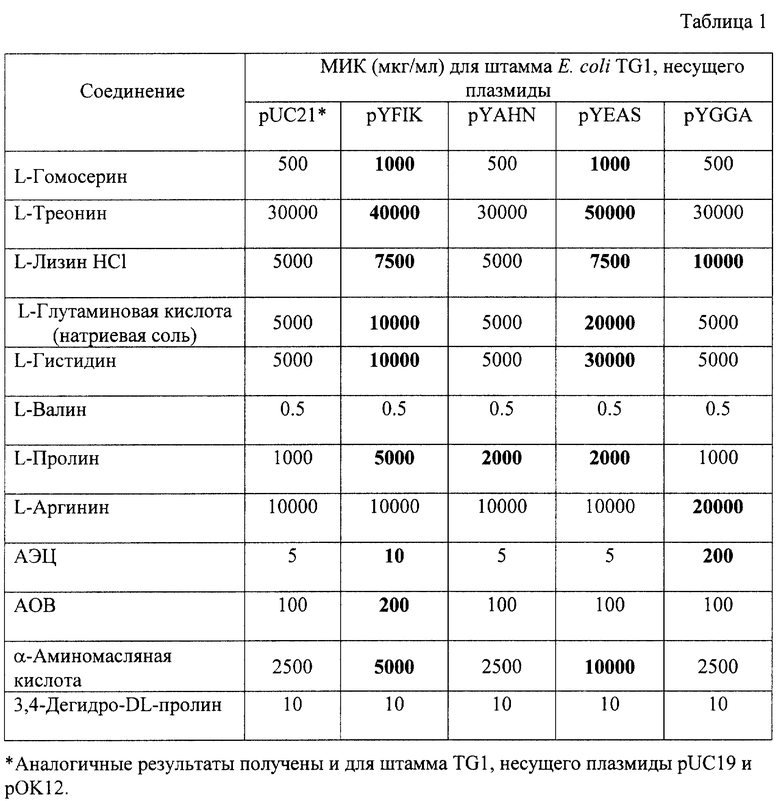
Гомология продуктов генов yahN, yeaS, yfiK и yggA с белком RhtB и с лизиновым транспортером LysE, осуществляющим экспорт L-лизина из клеток Corynebacterium glutamicum (Vrijic et al., Mol. Microbiol., 22, 815-826, 1996), указывает на аналогичную функцию белков - продуктов указанных генов. Известно, что повышение активности генов, контролирующих транспорт из клеток различных ингибиторов роста, увеличивает их устойчивость к соответствующим соединениям. В связи с этим определяют влияние плазмид, несущих фрагменты ДНК yahN, yeaS, yfiK и yggA, на устойчивость бактерий Е. coli TG1 к некоторым аминокислотам и аналогам аминокислот. С этой целью штамм TG1 трансформируют плазмидами pYEAS, pYAHN, pYFIK, pYGGA и векторами pUC21, pUC19 и рОК12. Ночные культуры полученных штаммов, выращенные в минимальной среде М9 на качалке (около 109 клеток/мл), разводят 1:100 и подращивают в течение 5 часов в той же среде. Затем полученные культуры в логарифмической фазе роста разводят и приблизительно по 104 жизнеспособных клеток наносят на высушенные чашки с агаризованной (2% агара) средой М9, содержащей различные концентрации аминокислот, или аналогов аминокислот. Рост или отсутствие роста определяют через 46-48 часов. Таким образом устанавливают минимальные ингибирующие концентрации (МИК) этих соединений (табл. 1).
Как видно из табл. 1, амплификация фрагмента ДНК yfiK существенно повышает устойчивость бактерий к пролину, в меньшей степени возрастает устойчивость к треонину, гомосерину, глутамату, α-аминомасляной кислоте, к аналогу треонина, α-амино-β-оксивалериановой кислоте (АОВ) и к аналогу L-лизина, (8)-2-аминоэтил-L-цистеину (АЭЦ). Амплификация фрагмента ДНК yahN повышает устойчивость бактерий к пролину. Амплификация фрагмента ДНК yeaS существенно повышает устойчивость бактерий к глутамату, гистидину и α-аминомасляной кислоте, в меньшей степени возрастает устойчивость к треонину, гомосерину, лизину. Амплификация фрагмента ДНК yggA существенно повышает устойчивость бактерий к лизину и его аналогу (8)-2-аминоэтил-L-цистеину (АЭЦ), также возрастает устойчивость к аргинину.
Эти результаты свидетельствуют о том, что почти каждый из предполагаемых экскретирующих аминокислоты белков, кодируемых указанными фрагментами ДНК, обладает специфичностью по отношению к нескольким субстратам (аминокислотам) или может обнаруживать неспецифический эффект в результате амплификации.
Пример 3. Влияние аплификации фрагментов ДНК yeaS, yahN и yfiK на продукцию глутаминовой кислоты.
В качестве продуцента глутаминовой кислоты используют штамм Е. coli АJ 13199 (Патент Франции N 2747689).
Штамм АJ 13199 трансформируют отдельно каждой из плазмид pYAHN, pYEAS, pYFIK, несущей фрагменты ДНК кодирующие белки, экскретирующие аминокислоты, а в качестве контроля - вектором pUC21. В результате получают штаммы: AJ13199/pYAHN (ВКПМ В-7729); AJ13199/pYEAS (ВКПМ В-7731); AJ13199/pYFIK (ВКПМ В-7730) и AJ13199/pUC21 (ВКПМ В-7728).
Каждый из полученных таким образом штаммов культивируют при 37oC 18 часов в LB бульоне, содержащем 100 мг/л ампициллина. Затем по 0.3 мл полученной культуральной жидкости вносят в пробирки 20 х 200 мм с 3 мл ферментационной среды (состав приведен ниже), содержащей также 0.2 г/л L-метионина, 0.2 г/л лизина и 100 мг/л ампициллина, и культивируют при 37oC 46 часов на роторной качалке (120 об/мин).
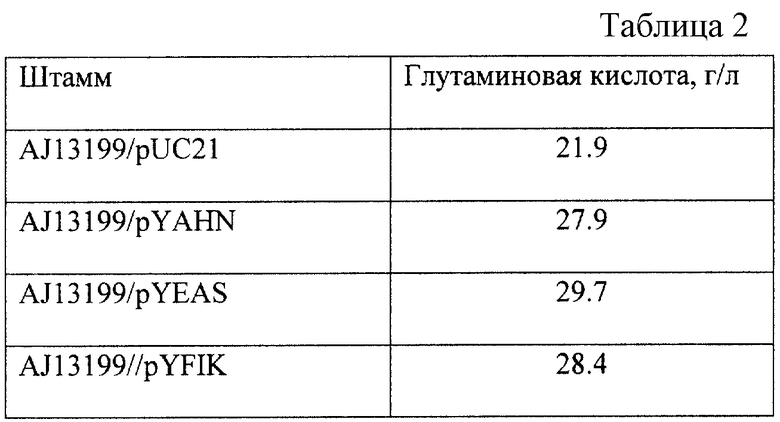
После культивирования количество глутаминовой кислоты в культуральной жидкости определяют известным методом. Результаты представлены в табл. 2.
Состав ферментационной среды (г/л):
Глюкоза - 80.0
(NH4)2SO4 - 22.0
K2HPO4 - 2.0
NaCl - 0.8
MgSO4 • 7H2O - 0.8
FeSO4 • 7H2O - 0.02
MnSO4 • 5H2O - 0.02
Тиамин HCl - 0.0002
Дрожжевой экстракт - 1.0
CACO3 - 30.0
Глюкоза и сернокислый магний стерилизуются отдельно. СаСО3 стерилизуется сухим жаром при 180oC в течение 2 часов. pH доводится до 7.0. Антибиотики вносят в среду после стерилизации.
Как следует из табл. 2, увеличение экспрессируемого количества каждого из белков YahN, YeaS и YfiK, кодируемых соответствующими генами, локализованными на многокопийных плазмидах, повышает продукцию глутаминовой кислоты штаммом- продуцентом. Наибольший эффект дает reн yeaS, амплификация которого повышает продукцию аминокислоты на 35%.
Пример 4. Влияние амплификации фрагментов ДНК yahN, yeaS, yfiK и yggA на продукцию лизина.
(1). В качестве исходного лизин-продуцирующего штамма используют штамм E.coli W3110 (tyrA) (Европейский патент N 488424), в который вводят плазмиду pCABD2 (Международной заявке WO 95/16042) и каждую из плазмид pMW118::yahN, pMW118: : : yeaS, pMW118::yfiK, несущих гены экскреции аминокислот, а также вектор pMW118. Так были получены следующие штаммы Е. coli:
W3110 (tyrA)/pCABD2+pMW 118: :yahN, W3110 (tyrA)/pCABD2+pMW 118::yeaS, W3110 (tyrA)/pCABD2+pMW 118::yfiK, W3110 (tyrA)/pCABD2+pMW 118.
Способность к продукции лизина этими штаммами определяют, культивируя их в ферментационной среде следующего состава (г/л):
Глюкоза - 40.0
MgSO4 • 7H2O - 1.0
(NH4)2SO4 - 16.0
К2HPO4 - 1.0
FeSO4 • 7H2O - 0.01
MnSO4 • 7H2O - 0.01
Дрожжевой экстракт - 2.0
Тирозин - 0.1
CaCO3 - 25.0
Глюкоза и сернокислый магний стерилизуется отдельно. CaCO3 стерилизуется сухим жаром при 180oC в течение 2 часов. pH доводится до 7.0. Антибиотики, ампицилин - 50 мг/л и стрептомицин - 20 мг/л, вносят в среду после стерилизации.
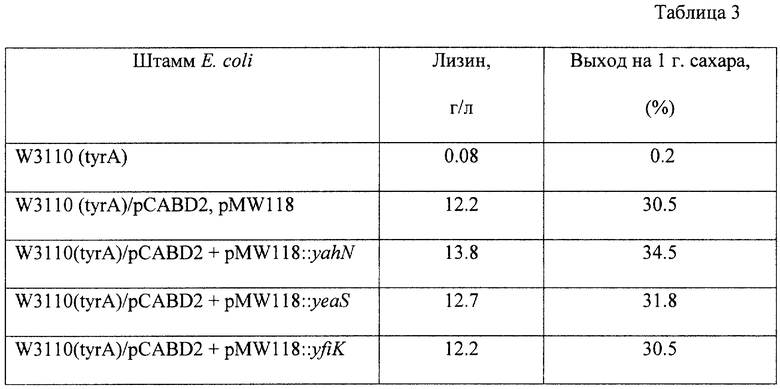
Культивирование осуществляют при 37oC в течение 30 часов с аэрацией (роторная качалка, 115 об/мин). Результаты представлены в табл. 3
Как следует из табл. 3, из исследованных в этом примере генов наибольший эффект на продукцию лизина оказывают гены yahN и yeaS.
(2). В качестве исходного лизин-продуцирующего штамма используют штамм Е. coli VL614. Этот штамм является производным известного штамма Е. coli VL613 (Авторское свидетельство СССР N 1354458). Штамм VL614 получают трансдукцией с помощью фага P1 в исходный штамм VL613 дикого аллеля rhtA+, сцепленного с транспозоном Tn10. Трансдуктанты отбирают на среде LB с тетрациклином (10 мг/л) и среди них находят клоны, чувствительные на минимальной среде к гомосерину (10 г/л). Полученный таким путем штамм VL614 трансформируют плазмидой pYGGA и в качестве контроля - вектором рОК12. В результате получают штаммы VL614/pYGGA (ВКПМ В-7719) и VL614/pOK12 (ВКПМ В-7722).
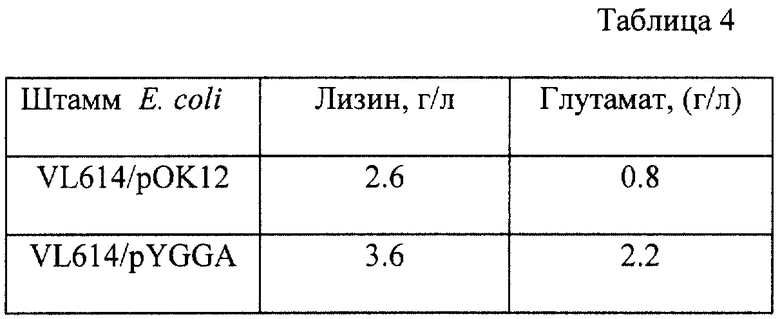
Каждый из полученных штаммов культивируют при 37oC 18 часов в LB бульоне с 50 мг/л канамицина. Затем по 0.3 мл полученной культуральной жидкости вносят в пробирки 20 х 200 мм с 3 мл ферментационной среды, описанной в примере 3, содержащей также 0.2 г/л L-треонина, 0.2 г/л L-метионина и 50 мг/л канамицина, и культивируют при 34oC 68 часов на роторной качалке. После культивирования количество накопленного в среде лизина, а также глутаминовой кислоты измеряют известными методами. Результаты представлены в табл. 4.
Как видно из табл. 4, амплификация фрагмента ДНК yggA на плазмиде рОК12 заметно повышает продукцию лизина. Одновременно с этим повышается накопление в культуральной жидкости и глутаминовой кислоты.
Пример 5. Влияние амплификации фрагментов ДНК yfiK и yeaS на продукцию треонина, аланина, валина и изолейцина.
В качестве продуцента треонина используют штамм Е. coli VL2054. Этот штамм является бесплазмидным продуцентом треонина, полученным на основе известного штамма Е. coli ВКПМВ-3996 (Патент США N 5 175 107), после элиминации плазмиды pVIC40, индукции мутации, повреждающей ген kan транспозона Tn5, интегрированный в ген tdh, и введения с помощью трансдукции фагом P1 сцепленного с транспозоном Tn10 дикого аллеля гена rhtA. Он содержит интегрированный в хромосому вектор мини-Мu (Mud), в который под PR-промотором фага ламбда
клонированы гены треонинового оперона из плазмиды pVIC40 и ген cat устойчивости к хлорамфениколу. Кроме треонина в процессе ферментации штамм Е. coli VL2054 способен накапливать также небольшие количества аланина, валина и изолейцина.
Штамм Е. coli VL2054 трансформируют отдельно каждой из плазмид pYEAS, pYFIK, а также вектором pUC21. В результате получают штаммы Е. coli VL2054/pYEAS (ВКПМ В-7707), Е. coli VL2054/pFIK (ВКПМ В-7712) и Е. coli VL2054/pUC21 (ВКПМ В-7708).
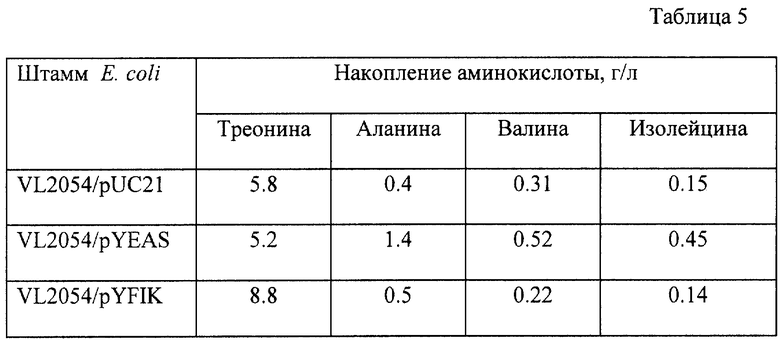
Каждый из полученных таким образом штаммов культивируют при 37oC 18 часов в LB бульоне со 100 мг/л ампициллина. Затем по 0.3 мл полученной культуральной жидкости вносят в пробирки 20 х 200 мм с 3 мл ферментационной среды, описанной в примере 3, содержащей 100 мг/л ампициллина, и культивируют при 37oC 46 часов на роторной качалке. После культивирования количество накопленного в культуральной жидкости треонина, аланина, валина и изолейцина измеряют известными методами. Результаты представлены в табл. 5.
Как показано в табл. 5, штамм Е. coli VL2054/pYFIK накапливает в культуральной жидкости значительно больше треонина, чем штамм Е. coli VL2054/pUC21, в котором экспрессируемое количество продукта гена yflK не увеличено. Штамм Е. coli VL2054/pYEAS накапливает больше аланина, валина и изолейцина, чем контрольный штамм Е. coli VL2054/pUC21.
Пример 6. Влияние амплификации фрагментов ДНК yeaS и yfiK на продукцию гистидина.
В качестве продуцента гистидина, принадлежащего к роду Escherichia, используют штамм Е. coli VL2160. Этот штамм получают на основе известного штамма NK5526 hisG: : Tn10 (ВКПМ В-3384) путем переноса в него с помощью трансдукции фагом P1 мутации hisGR, нарушающей ингибирование АТФ-фосфорибозилтрансферазы гистидином, из штамма СС46 (Аствацатурянц и др., Генетика, т. 24, с. 1928-1934, 1988). Штамм VL2160 трансформируют отдельно каждой из плазмид pYEAS, pYFIK, а также вектором pUC21. В результате получают штаммы: E. coli VL2160/pYEAS (ВКПМ В-7753), Е. coli VL2160/pYFIK (ВКПМ В-7754), Е. coli VL2160/pUC21 (ВКПМ В-7752).
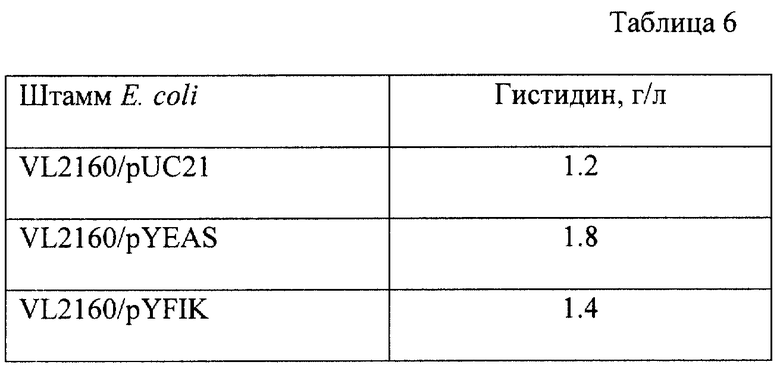
Каждый из полученных таким образом штаммов культивируют при 37oC 18 часов в LB бульоне со 100 мг/л ампициллина. Затем по 0.3 мл полученной культуральной жидкости вносят в пробирки 20 х 200 мм с 3 мл ферментационной среды, описанной в примере 3, содержащей повышенную концентрацию дрожжевого экстракта (3 г/л) и 100 мг/л ампициллина, и культивируют при 37oC 70 часов на роторной качалке. После культивирования количество накопленного в среде гистидина определяют известным методом. Результаты представлены в табл. 6.
Как следует из табл. 6, штаммы Е. coli VL2160/pYEAS и Е. coli VL2160/pYFIK продуцируют больше гистидина, чем штаммы Е. coli VL2160/pUC21, у которого экспрессируемое количество белков, продуктов генов yeaS и yflK, не увеличено. При этом видно, что набольший положительный эффект на продукцию гистидина дает амплификация на плазмиде гена yeaS.
Пример 7. Влияние амплификации фрагментов ДНК yahN, yfiK и yeaS на продукцию пролина
В качестве продуцента пролина, принадлежащего к роду Escherichia, используют штамм VL2151 (Е. coli W3350 proB*, Δ putAP, Tn10), сконструированный на основе известного штамма W3350 путем введения с помощью трансдукции фагом P1 мутации Δ putAP, сцепленной с транспозоном Tn10, и последующей селекции мутантов, устойчивых к 20 мг/л 3,4-дегидро-DL-пролина
Штамм Е. coli VL2151 трансформируют отдельно каждой из плазмид pYAHN, pYEAS, pYFIK, а также вектором pUC21. В результате получают штаммы Е. coli VL2151/pYEAS (ВКПМ В-7714), VL2151/pYAHN (ВКПМ В-7748), Е. coli VL2151/pFIK (ВКПМ В-7713) и Е.coli VL2151/pUC21 (ВКПМ В-7715).
Каждый из полученных таким образом штаммов культивируют при 37oC 18 часов в LB бульоне со 100 мг/л ампициллина. Затем по 0.3 мл полученной культуральной жидкости вносят в пробирки 20 х 200 мм с 3 мл ферментационной среды, описанной в примере 3, содержащей 100 мг/л ампициллина, и культивируют при 37oC 46 часов на роторной качалке.
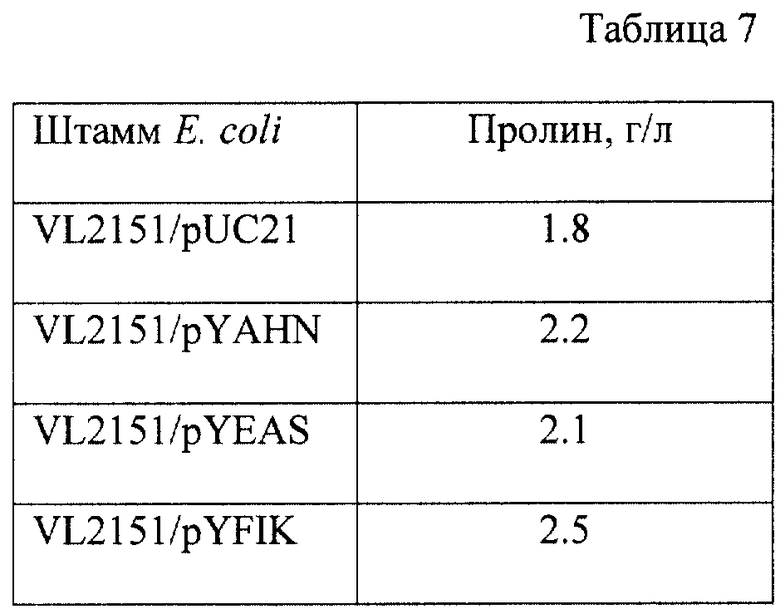
После культивирования количество накопленного в среде пролина определяют известным методом. Результаты представлены в табл. 7.
Как видно из табл. 7, штаммы Е. coli VL2151/pYFIK, Е. coli VL2151/pYAHN и Е. coli VL2151/pYEAS накапливают больше пролина, чем штамм Е. coli VL2151/pUC21, у которого экспрессируемое количество белков, продуктов генов yfiK, yahN и yeaS, не увеличено. При этом видно, что наибольший положительный эффект на продукцию пролина оказывает ген yfiK.
Пример 8. Влияние амплификации фрагмента ДНК yggA на продукцию аргинина
В качестве продуцента аргинина, принадлежащего к роду Escherichia coli, используют штамм Е. coli W3350 argE::Tn10/pKA10, который содержит плазмиду рКА10, несущую гены биосинтеза аргинина из Corynebacterium glutamicum (Харитонов А.А., Тарасов А.П. Молекулярная генетика, микробиология, вирусология, N 9, 29-33, 1986).
Штамм Е. coli W3350 argE::Tn10/pKA10 трансформируют плазмидой pYGGA, а в качестве контроля - вектором рОК12. В результате получают штаммы Е. coli W3350 argE::Tn10/pKA10, pYGGA (ВКПМ В-7716) и Е. coli W3350 аrgE:: Tn10/рКА10, рОК12 ВКПМВ-7718).
Каждый из полученных таким образом штаммов культивируют при 37oC 18 часов в LB бульоне с 100 мг/л ампициллина и 50 мг/л канамицина. Затем по 0.3 мл полученной культуральной жидкости вносят в пробирки 20 х 200 мм с 3 мл ферментационной среды, описанной в примере 3, содержащей 100 мг/л ампициллина и 50 мг/л канамицина, и культивируют при 37oC 46 часов на роторной качалке. После культивирования количество накопленного в среде аргинина измеряют известным методом. Результаты представлены в табл. 8.
Как видно из табл. 8, штамм Е. coli штаммы Е. coli W3350 argE:: Tn10/рКА10, pYGGA накапливают больше аргинина, чем штамм Е. coli W3350 argE: : Tn10/pKA10, рОК12, у которого экспрессируемое количество белка, продукта гена yggA, не увеличено.









Изобретение относится к биотехнологии и генетической инженерии. Предложены фрагменты ДНК yahN, yeaS, yfiK, yggA, кодирующие синтез белков, придающих бактериям Esherichia coli повышенную устойчивость к L-аминокислотам. На основе этих фрагментов сконструированы штаммы бактерий Е. coli, обладающие повышенной способностью к продукции L-лизина, L-треонина, L-глутаминовой кислоты, L-гистидина, L-пролина, L-аланина, L-аргинина, L-валина и L-изолейцина. Описан способ получения L - аминокислот с использованием новых штаммов-продуцентов. 5 с. и 1 з.п.ф-лы, 8 табл., 4 ил.
| US 4278765, 14.07.1981 | |||
| W0 95/16042, 15.06.1995. |
Авторы
Даты
2001-10-27—Публикация
1999-03-09—Подача