Камптотецин представляет собой природное соединение, которое впервые было выделено из листьев и коры китайского растения, называемого camptotheca acuminata (см. Wall и др., J. Amer. Chem. Soc., 88, 3888 (1966)). Камптотецин является пентациклическим соединением, состоящим из фрагмента индолизино[1,2-b]хинолина, сконденсированного с шестичленным α-гидроксилактоном. Углерод в положении 20, который несет α-гидроксильную группу, является асимметрическим и придает молекуле вращательную способность. Природная форма камптотецина имеет абсолютную конфигурацию S у углерода в положении 20 и отвечает следующей формуле:
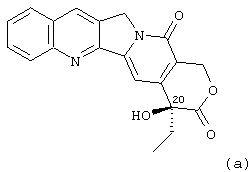
Камптотецин обладает антипролиферативной активностью в отношении некоторых раковых клеточных линий, включающих линии клеток человеческих опухолей ободочной кишки, легкого и молочной железы (М. Suffness и др.: The Alcaloids Chemistry and Pharmacology, ред. A. Bross, том 25, с. 73 (Academic Press, 1985)). Отмечают, что антипролиферативная активность камптотецина связана с его ингибирующей активностью в отношении топоизомеразы I ДНК.
Показано, что α-гидроксилактон абсолютно необходим одновременно для активности in vivo и in vitro камптотецина (Camptothecines: New Anticancer Agents, изд. М. Putmesil и др., с. 27 (CRC Press, 1995); M. Wall и др., Cancer Res., 55, 753 (1995); Hertzberg и др., J. Med. Chem., 32, 715 (1982) и Crow и др., J. Med. Chem., 35, 4160 (1992)). Заявитель впоследствии разработал новый класс аналогов камптотецина, в которых β-гидроксилактон заменяет природный α-гидроксилактон камптотецина (см. Международные заявки на патент WO-97/00876, WO-98/28304 и WO-98/28305).
Настоящая заявка относится к новым β-гидроксилактоновым аналогам камптотецина, биологическая активность которых, выраженная, например, в виде концентраций, ингибирующих пролиферацию опухолевых клеточных колоний, неожиданно превышает активность уже известных соединений. Объектом изобретения также являются лекарственные средства, представляющие собой вышеуказанные соединения, а также содержащие их фармацевтические композиции. Изобретение относится также к способу получения соединений согласно изобретению.
Следовательно, объектом изобретения являются соединения общей формулы (I), которая отвечает формуле (IA):
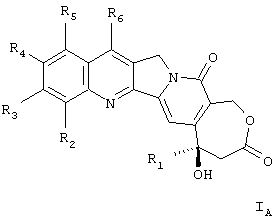
в которой:
R1 означает низший алкильный радикал;
R2, R3, R4 и R5, независимо, означают атом водорода, галоидный радикал или радикал -OSO2R10;
R6 означает атом водорода; линейный или разветвленный алкильный радикал с 1-12 атомами углерода, возможно замещенный одним или несколькими одинаковыми или разными галоидными радикалами; низший гидроксиалкил, (низший алкокси)(низший алкил), циклоалкил, циклоалкил(низший алкил), нитрогруппу, атом галогена, группу -(СН2)mSiR7R8R9, замещенный или незамещенный арил или замещенный или незамещенный арил(низший алкил), причем один или несколько заместителей, одинаковых или разных, арильных групп выбирают из радикалов: низший алкил, гидроксил, атом галогена, аминогруппа, (низший алкил)аминогруппа, ди(низший алкил)аминогруппа, CF3 или OCF3;
R7, R8 и R9, независимо, означают низший алкильный радикал;
R10 означает низший алкильный радикал, возможно замещенный одним или несколькими одинаковыми или разными галоидными радикалами, или арильный радикал, возможно замещенный одним или несколькими одинаковыми или разными низшими алкильными радикалами;
m означает целое число от 0 до 6;
при условии, что, когда R2 означает Н, тогда
R6 означает линейный или разветвленный алкильный радикал с 7-12 атомами углерода, -(CH2)mSiR7R8R9 или арил, замещенный одним или несколькими одинаковыми или разными заместителями, выбираемыми среди ди(низший алкил)аминогруппы или ОСF3,
и/или по меньшей мере один из радикалов R3, R4 или R5 означает -OSO2R10; либо представляют собой:
(5R)-5-этил-11-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-бензил-5-этил-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-бутил-5-этил-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5,12-диэтил-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-5-гидрокси-12-фенил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-циклогексил-5-этил-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-5-гидрокси-12-(4-метилфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-10-хлор-5-этил-12-(2-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-фенил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-фенил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-бутил-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-бензил-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5,12-диэтил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино [3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-бутил-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5,12-диэтил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1Н,3Н-оксепино [3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-бутил-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5,12-диэтил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-5-гидрокси-12-изопентил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-12-(4-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(2,6-дифторфенил)-5-этил-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(3,5-дифторфенил)-5-этил-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-5-гидрокси-12-(3,4,5-трифторфенил)-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-5-гидрокси-12-(2,4,6-трифторфенил)-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-5-гидрокси-12-(2,3,5,6-тетрафторфенил)-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-5-гидрокси-12-(2,3,4,5,6-пентафторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-12-(4-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(2,6-дифторфенил)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7 ]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(3,5-дифторфенил)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-(3,4,5-трифторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-(2,4,6-трифторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-(2,3,5,6-тетрафторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-(2,3,4,5,6-пентафторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-12-(4-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(2,6-дифторфенил)-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(3,5-дифторфенил)-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-(3,4,5-трифторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-(2,4,6-трифторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-(2,3,5,6-тетрафторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]-индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-(2,3,4,5,6-пентафторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]-индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-12-(4-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(2,6-дифторфенил)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(3,5-дифторфенил)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-(3,4,5-трифторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-(2,4,6-трифторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-(2,3,5,6-тетрафтор-фенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]-индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-(2,3,4,5,6-пентафтор-фенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]-индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1Н,3Н-оксепино-[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-(3,3,3-трифторпропил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-изопентил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-пентил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-фенетил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(2-циклогексилэтил)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(3,3-диметилбутил)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-(3,3,3-трифторпропил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-изопентил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-пентил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-фенетил-4,5,13,15-тетрагидро-1H,3Н-оксепино-[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(2-циклогексилэтил)-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(3,3-диметилбутил)-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6, 7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-(3,3,3-трифторпропил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-изопентил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-пентил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-фенетил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(2-циклогексилэтил)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(3,3-диметилбутил)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-хлор-5-этил-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино [3’,4’:6,7]-индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-5-гидрокси-12-гидроксиметил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-иэобутил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-неопентил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-12-(3-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-(4-трифторметилфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-[4-(трет-бутил)фенил]-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(2-этоксиэтил)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10,11-трифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион или их аддитивные соли.
В вышеуказанных определениях выражение "галоидный радикал" означает фтор-, хлор-, бром- или иод-радикал и предпочтительно хлор-, фтор- или бром-радикал. Под низшим алкильным радикалом согласно настоящей заявке понимают линейный или разветвленный алкильный радикал с 1-6 атомами углерода, такие как метильный, этильный, пропильный, изопропильный, бутильный, изобутильный, втор-бутильный и трет-бутильный, пентильный, изопентильный, неопентильный, гексильный или изогексильный радикалы. Из алкильных радикалов с 1-12 атомами углерода можно назвать низшие алкилы, такие, как указанные выше, а также гептильный, октильный, нонильный или децильный радикалы. Низшие алкоксильные радикалы могут соответствовать вышеуказанным алкильным радикалам, как, например, метоксигруппа, этоксигруппа, пропилоксигруппа или изопропилоксигруппа, а также линейная, вторичная или третичная бутоксигруппа.
Термин "циклоалкил" означает цикл с 3-7 атомами углерода, как, например, циклопропил, циклобутил, циклопентил или циклогексил. Термин "циклоалкил(низший алкил)" означает радикалы, в которых, соответственно, циклоалкильный и низший алкильный радикалы представляют собой такие, как указанные выше, как, например, метилциклогексил, этилциклогексил. Термин "арил" означает моно-, ди- или трициклическое углеводородное соединение по меньшей мере с одним ароматическим циклом, причем каждый цикл является максимально семичленным, как, например, фенил, нафтил, антрацил, бифенил или инденил. (Низший алкил)арильные радикалы означают радикалы, в которых, соответственно, арильный и низший алкильный радикалы являются такими, как определенные выше, как, например, бензил, фенетил или метилнафтил.
Термин "низший гидроксиалкил" относится к радикалам, в которых алкильная цепь может быть линейной или разветвленной и может включать 1-6 атомов углерода. Термины "(низший алкил)аминогруппа и ди(низший алкил)аминогруппа" предпочтительно означают радикалы, в которых алкильные радикалы являются такими, как определенные выше, как, например, метиламино-, этиламино-, диметиламино-, диэтиламино- или метилэтиламиногруппа.
Более конкретно, объектом изобретения являются соединения общей формулы (IIA):
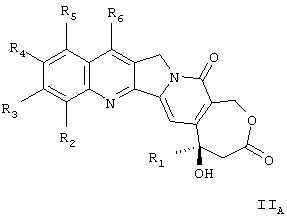
в которой:
R1 означает низший алкильный радикал;
R2, R3, R4 и R5, независимо, означают атом водорода, галоидный радикал или радикал -OSO2R10;
R6 означает атом водорода; линейный или разветвленный алкильный радикал с 1-12 атомами углерода, возможно замещенный одним или несколькими одинаковыми или разными галоидными радикалами; низший гидроксиалкил, (низший алкокси)(низший алкил), циклоалкил, циклоалкил(низший алкил), нитрогруппу, атом галогена, группу -(CH2)mSiR7R8R9, замещенный или незамещенный арил или замещенный или незамещенный арил(низший алкил), причем один или несколько заместителей, одинаковых или разных, арильных групп выбирают из радикалов: низший алкил, гидроксил, атом галогена, аминогруппа, (низший алкил)аминогруппа, ди(низший алкил)аминогруппа, СF3 или ОСF3;
R7, R8 и R9, независимо, означают низший алкильный радикал;
R10 означает низший алкильный радикал, возможно замещенный одним или несколькими одинаковыми или разными галоидными радикалами, или арильный радикал, возможно замещенный одним или несколькими одинаковыми или разными низшими алкильными радикалами;
m означает целое число от 0 до 6;
или соль этих последних;
отличающиеся тем, что:
по меньшей мере один из радикалов R2, R3, R4 или R5 означает радикал -OSO2R10
и/или
R6 означает линейный или разветвленный алкильный радикал с 7-12 атомами углерода, радикал -(CH2)mSiR7R8R9 или арильный радикал, замещенный одним или несколькими одинаковыми или разными радикалами, выбираемыми
среди ди(низший алкил)аминогруппы или ОСF3;
и/или
R2 означает галоидный радикал;
или аддитивные соли этих соединений.
Особенно предпочтительными соединениями согласно изобретению являются такие, в которых R1 означает этильный радикал, а также такие, в которых R3 означает галоидный радикал, в особенности фтор-радикал.
Соединения формулы (IIA) предпочтительно представляют одно из следующих соединений:
(5R)-5-этил-8-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-(2-триметилсилилэтил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-5-гидрокси-12-(2-триметилсилилэтил)-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-децил-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-децил-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-децил-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-(трифторметоксифенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(4-диметиламинофенил)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-3,15-диоксо-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-10-илтрифторметансульфонат;
и особенно предпочтительны следующие соединения:
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-(2-триметилсилилэтил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b] хинолин-3,15-дион;
(5R)-5-этил-5-гидрокси-12-(2-триметилсилилэтил)-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион.
Более предпочтительно объектом изобретения являются также соединения формулы (I), указанные выше и представляющие собой одно из следующих соединений:
(5R)-5-этил-11-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино [3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино [3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-бензил-5-этил-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино [3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-бутил-5-этил-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино [3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5,12-диэтил-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино-[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-5-гидрокси-12-фенил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-циклогексил-5-этил-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-5-гидрокси-12-(4-метилфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-10-хлор-5-этил-12-(2-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-фенил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-фенил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-бутил-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-бензил-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5,12-диэтил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-бутил-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5,12-диэтил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-бутил-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5,12-диэтил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-5-гидрокси-12-изопентил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-12-(4-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1Н, 3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(3,5-дифторфенил)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-фенетил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-хлор-5-этил-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино [3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-5-гидрокси-12-гидроксиметил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-изобутил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-неопентил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-12-(3-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-(4-трифторметилфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-[4-(трет-бутил)фенил]-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(2-этоксиэтил)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10,11-трифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион или аддитивные соли этих соединений.
Соединения формулы (I) предпочтительно отвечают одной из следующих формул:
(5R)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино [3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5,12-диэтил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино [3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5,12-диэтил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-12-(4-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(3,5-дифторфенил)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-фенетил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-хлор-5-этил-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино [3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-12-(3-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-(4-трифторметилфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(2-этоксиэтил)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион или аддитивные соли этих соединений.
Объектом изобретения также являются соединения формулы (I), указанные выше и отвечающие одной из следующих формул:
(5R)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино [3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-фенил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-фенил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-бутил-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-бензил-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5,12-диэтил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-(2-триметилсилилэтил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино [3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-бутил-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5,12-диэтил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-бутил-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино-[1,2-b]хинолин-3,15-дион;
(5R)-5,12-диэтил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино [3’,4’: 6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-12-(4-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(2,6-дифторфенил)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(3,5-дифторфенил)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-(3,4,5-трифторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-(2,4,6-трифторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-(2,3,5,6-тетрафторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-(2,3,4,5,6-пентафторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-12-(4-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(2,6-дифторфенил)-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(3,5-дифторфенил)-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-(3,4,5-трифторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-(2,4,6-трифторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-(2,3,5,6-тетрафторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]-индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-(2,3,4,5,6-пентафторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]-индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-12-(4-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(2,6-дифторфенил)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(3,5-дифторфенил)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-(3,4,5-трифторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино-[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-(2,4,6-трифторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-(2,3,5,6-тетрафторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-(2,3,4,5,6-пентафторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]-индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-(3,3,3-трифторпропил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-изопентил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-пентил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-фенетил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-децил-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(2-циклогексилэтил)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(3,3-диметилбутил)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-(3,3,3-трифторпропил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-изопентил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-пентил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-фенетил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-децил-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(2-циклогексилэтил)-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(3,3-диметилбутил)-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-3-этил-9,11-дифтор-5-гидрокси-12-(3,3,3-трифторпропил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-изопентил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-пентил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-фенетил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-децил-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(2-циклогексилэтил)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(3,3-диметилбутил)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-хлор-5-этил-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-5-гидрокси-12-гидроксиметил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-изобутил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-неопентил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-12-(3-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-(4-трифторметилфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-(4-трифторметоксифенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(4-диметиламинофенил)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-[4-(трет-бутил)фенил]-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,11-дифтор-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(2-этоксиэтил)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10,11-трифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-3,15-диоксо-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-10-илтрифторметансульфонат.
Соединения общей формулы (I) могут быть получены следующим образом:
- продукт общей формулы (М):
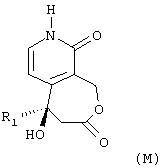
в которой R1 имеет вышеуказанное значение, вводят во взаимодействие с соединением формулы (N):
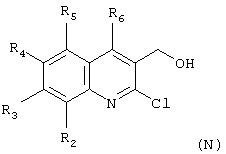
в которой R2, R3, R4, R5 и R6 имеют вышеуказанное значение, для получения соединения формулы (О):
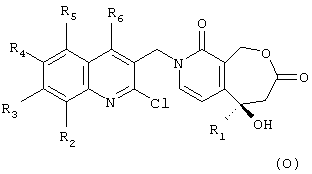
в которой R2, R3, R4, R5 и R6 имеют вышеуказанное значение;
- соединение формулы (О) затем циклизуют для получения соединения формулы (I).
Соединения формулы (О) получают из соединений общих формул (М) и (N) путем обработки, известной специалисту под названием реакции Mitsunobu (см. О. Mitsunobu и др., Synthesis, с. 1 (1981)). Речь идет о замещении гидроксильной группы соединения (N) нуклеофилом, таким как соединение (М), или де-протонированным производным этого последнего путем обработки с помощью фосфина, например трифенилфосфина, и азодикарбосилатного производного, например диэтил- или диизопропилазодикарбоксилата, в апротонном растворителе, таком как, например, тетрагидрофуран или N,N-диметилформамид. Циклизацию соединений (О) для получения соединений формулы (I) предпочтительно осуществляют в присутствии палладийсодержащего катализатора (как, например, диацетат палладия) в щелочных условиях (достигаемых, например, с помощью ацетата щелочного металла, возможно в сочетании с агентом переноса фаз, таким как тетрабутиламмонийбромид), в апротонном растворителе, таком как ацетонитрил или N,N-диметилформамид, при температуре 50-120°С (R. Grigg и др., Tetrahedron, 46, 4003 (1990)).
Объектом изобретения также является соединение общей формулы (М), указанное выше, в качестве нового промышленного продукта. Этот продукт (М) может быть использован для приготовления лекарственных средств. Предпочтительно R1 означает этильный радикал.
Соединение формулы (М) получают согласно новому способу, состоящему из следующих последовательных стадий:
- рацемический сложный эфир формулы
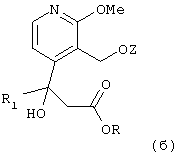
в которой R1 имеет вышеуказанное значение, R означает низший алкил и Z означает защитную группу спиртовой функциональной группы (в отношении его получения см., в частности, Международную заявку на патент WO-97/00876), превращают в соответствующую карбоновую кислоту;
- затем это соединение подвергают операции разделения энантиомеров, известной специалисту под названием расщепление (см. Jacques и др. "Enantiomers, Racemates and Resolution", второе издание, Wiley, Нью-Йорк, 1991) и позволяющей получать обогащенное энантиомером соединение общей формулы (А):
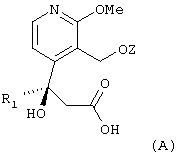
в которой R1 и Z имеют вышеуказанное значение;
- удаляют защитную группу спиртовой функциональной группы соединения общей формулы (А) для получения продукта общей формулы (В):
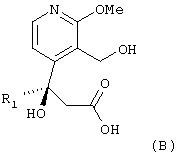
в которой R1 имеет вышеуказанное значение;
- соединение общей формулы (В) затем циклизуют для получения соединения общей формулы (С):
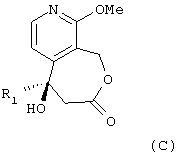
в которой R1 имеет вышеуказанное значение;
- наконец, метоксигруппу соединения общей формулы (С) превращают в карбонильную группу для получения соединения общей формулы (М):
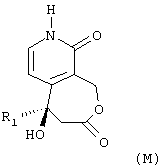
в которой R1 имеет вышеуказанное значение.
В частном случае, когда R1 означает этил, R означает трет-бутил и Z означает бензил, соединение формулы (М) синтезируют согласно способу, состоящему из следующих последовательных стадий:
- рацемический сложный трет-бутиловый эфир (способ его получения см., в частности, в Международной заявке на патент WO-97/00876) общей формулы
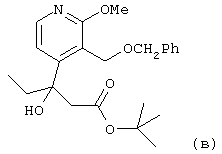
обрабатывают трифторуксусной кислотой в течение 18 часов при комнатной температуре для получения соответствующей карбоновой кислоты;
- нагревают в изопропиловом спирте гуанидиновую соль 3-(3-бензилоксиметил-2-метокси-4-пиридил)-3-гидроксипентановой кислоты до температуры выше 30°С и предпочтительно примерно до 50°С, а затем охлаждают реакционную среду до комнатной температуры таким образом, чтобы кристаллизовалась соль (+)-энантиомера 3-(3-бензилоксиметил-2-метокси-4-пиридил)-3-гидроксипентановой кислоты, а соль (-)-изомера, анион которой представлен ниже, остался в растворе:
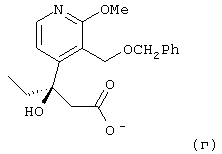
- раствор в изопропиловом спирте соли (-)-энантиомера 3-(3-бензилоксиметил-2-метокси-4-пиридил)-3-гидроксипентановой кислоты концентрируют и обрабатывают соляной кислотой для получения соединения формулы (А’):
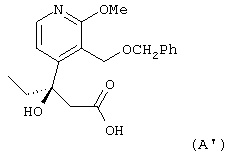
- соединение (А’) затем вводят в контакт с палладием в присутствии источника водорода для получения дебензилированного продукта формулы (В’):
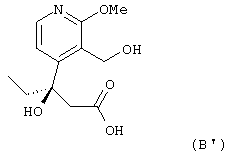
- затем соединение формулы (В’) циклизуют для получения соединения формулы (С’):
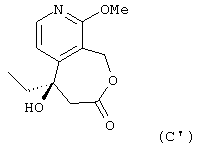
- наконец, метоксигруппу соединения формулы (С’) превращают в карбонильную группу для получения (+)-5-этил-5-гидрокси-1,3,4,5,8,9-гексагидрооксепино[3,4-с]пиридин-3,9-диона (или (+)-EHHOPD), представленного ниже:
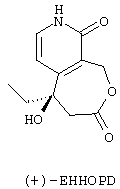
В вышеописанном способе реакцию, приводящую к образованию соединения формулы (В’) из соединения формулы (А’), предпочтительно осуществляют в метаноле и предпочтительно путем нагревания реакционной среды до температуры 40°С после добавления формиата аммония. Циклизацию соединения формулы (В’) для получения соединения формулы (С’) можно осуществлять в тетрагидрофуране предпочтительно при температуре около 50°С. В случае реакции, приводящей к образованию (+)-EHHOPD из соединения формулы (С’), предпочтительно работают при комнатной температуре при использовании ацетонитрила в качестве растворителя.
Соединения формулы (I), в которой по меньшей мере один из радикалов R2, R3, R4 и R5 означает сульфонатную группу (как, например, мезилат, трифлат или тозилат), могут быть получены по способу, отличающемуся тем, что соответствующее гидроксилированное соединение в безводном апротонном растворителе обрабатывают сульфонилирующим агентом в присутствии основания. Апротонным растворителем может быть дихлорметан или N,N-диметилформамид, сульфонилирующим агентом может быть метансульфонилхлорид, ангидрид трифторметансульфокислоты, N-фенилимид трифторметансульфокислоты или п-толуолсульфонилхлорид и основанием может быть триэтиламин, пиридин или гидрид натрия. Сульфонатная группа также может быть введена на уровне промежуточных продуктов.
Соединения формулы (N), в которой R6 означает атом водорода и R2, R3, R4 и R5 имеют вышеуказанное значение, могут быть получены из анилинов формулы (Р):
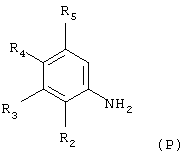
в которой R2, R3, R4 и R5 имеют вышеуказанное значение, по следующему способу: анилин формулы (Р) подвергают N-ацетилированию путем обработки ацетилирующим агентом, таким как, например, уксусный ангидрид. Таким образом полученный ацетанилид при температуре 50-100°С, предпочтительно примерно при 75°С, обрабатывают реагентом, известным специалисту под названием реактив Вильсмайера (получаемый путем воздействия фосфорилоксихлорида на N,N-диметилформамид при температуре 0-10°С), для получения соответствующего 2-хлор-3-хинолинкарбальдегида (см., например, Meth-Cohn и др., J. Chem. Soc., Perkin Trans., I, 1520 (1981); Meth-Cohn и др., J. Chem. Soc., Perkin Trans., I, 2509 (1981) и Nakasimhan и др., J. Am. Chem. Soc., 112, 4431 (1990)). Это промежуточное соединение легко восстанавливают до соответствующего хинолилметанола формулы (N) в известных специалисту классических условиях, таких как обработка в спиртовом растворителе (например, в метаноле) боргидридом натрия при температуре 0-40°С.
Соединения формулы (N), в которой R2, R3, R4, R5 и R6 имеют вышеуказанное значение, также могут быть получены из карбоксилированных хинолонов формулы (Q):
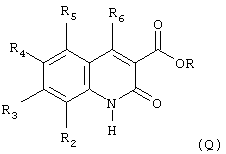
в которой R2, R3, R4, R5 и R6 имеют вышеуказанное значение, согласно следующему способу: хинолон формулы (Q) хлорируют для получения соответствующего хлорхинолина, карбоксильную группу которого восстанавливают для получения соединения общей формулы (N). Хлорирование может быть осуществлено с помощью хлорфосфиноксида, такого как оксихлорид фосфора или хлордифенилфосфиноксид, при использовании в чистом состоянии или в присутствии инертного апротонного сорастворителя, такого как толуол или хлороформ, при температуре 50-120°С. Хлорирование осуществляют предпочтительно с помощью избытка оксихлорида фосфора при температуре 80°С. Восстановление может быть осуществлено с помощью гидрида алюминия в апротонном растворителе, таком как диэтиловый эфир, трет-бутилметиловый эфир, тетрагидрофуран, дихлорметан, хлороформ, трихлорэтан или толуол, при температуре 0-50°С. Восстановление предпочтительно осуществляют с помощью диизобутилалюминийгидрида в дихлорметане при комнатной температуре.
Соединения формулы (Q), в которой R6 означает атом водорода и R2, R3, R4 и R5 имеют вышеуказанное значение, могут быть получены из антраниловых кислот формулы (R):
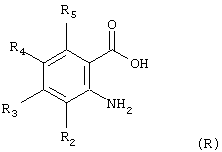
в которой R2, R3, R4 и R5 имеют вышеуказанное значение, согласно следующему способу: кислоту формулы (R) восстанавливают для получения соответствующего бензилового спирта. Спиртовую группу в полученном промежуточном соединении селективно защищают, чтобы сохранить аминогруппу. Полученный в результате анилин ацилируют с помощью производного малоновой кислоты. От ранее защищенной спиртовой группы удаляют защитную группу, затем окисляют для получения соответствующей карбонильной группы и таким образом полученное промежуточное соединение подвергают внутримолекулярной реакции, известной специалисту под названием конденсация Кневенагеля, для получения карбоксилированных хинолонов формулы (Q), в которой R6 означает атом водорода и R2, R3, R4 и R5 имеют вышеуказанное значение. Восстановление кислоты в спирт может быть осуществлено с помощью гидрида металла в инертном апротонном растворителе при температуре 0-50°С и предпочтительно с помощью смешанного литийалюминийгидрида в тетрагидрофуране при комнатной температуре. Защита промежуточного бензилового спирта может быть осуществлена согласно обычным, известным специалисту методам (Т. Greene и др. "Protective groups in Organic Synthesis", второе издание, Wiley, Нью-Йорк, 1991) или же с помощью силилхлорида в присутствии основания в апротонном растворителе при температуре 0-50°С и предпочтительно с помощью трет-бутилдифенилсилилхлорида в присутствии имидазола в диметилформамиде при комнатной температуре.
Ацилирование может быть осуществлено с помощью производного малоновой кислоты, такого как этилмалонилхлорид или метилмалонат, в присутствии основания, такого как триэтиламин или 4-диметиламинопиридин, в апротонном растворителе, таком как ацетонитрил, тетрагидрофуран или толуол, при температуре 0-110°С и предпочтительно с помощью этилмалонилхлорида в ацетонитриле при комнатной температуре и в присутствии триэтиламина. Удаление защитной группы может быть осуществлено в зависимости от предварительно выбранной защитной группы для бензилового спирта (Т. Greene) и в случае простых силилированных эфиров с помощью источника фтор-иона, такого как фторид цезия или калия, в присутствии агента переноса фаз, или же тетрабутиламмонийфторида, в апротонном растворителе, таком как тетрагидрофуран, при температуре 0-50°С и предпочтительно при комнатной температуре. Окисление может быть осуществлено в присутствии солей хрома-(VI), несущих пиридильные лиганды, с помощью реактива Сверне или же с помощью пиридинтриоксидного комплекса серы в диметилсульфоксиде в присутствии триэтиламина и предпочтительно с помощью пиридинийдихромата в дихлорметане при комнатной температуре. Внутримолекулярная конденсация Кневенагеля может происходить спонтанно или ее можно осуществлять в растворе в присутствии основания и предпочтительно в дихлорметане в присутствии триэтиламина при комнатной температуре.
Соединения формулы (Q), в которой R2, R3, R4, R5 и R6 имеют вышеуказанное значение, могут быть получены из аминокетонов формулы (S):
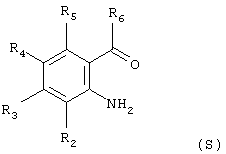
в которой R2, R3, R4, R5 и R6 имеют вышеуказанное значение, согласно следующему способу: аминокетон формулы (S) ацилируют с помощью производного малоновой кислоты и таким образом полученное промежуточное соединение подвергают внутримолекулярной реакции, известной специалисту под названием конденсация Кневенагеля, для получения карбоксилированных хинолонов формулы (Q). Ацилирование может быть осуществлено с помощью производного малоновой кислоты, такого как этилмалонилхлорид или метилмалонат, в присутствии основания, такого как триэтиламин или 4-диметиламинопиридин, в апротонном растворителе, таком как ацетонитрил, тетрагидрофуран или толуол, при температуре 0-110°С и предпочтительно с помощью этилмалонилхлорида в ацетонитриле при комнатной температуре и в присутствии триэтиламина. Внутримолекулярная конденсация Кневенагеля может происходить спонтанно или ее можно осуществлять в растворе в присутствии основания и предпочтительно в ацетонитриле в присутствии этилата натрия при комнатной температуре.
Аминокетоны формулы (S), в которой R2, R3, R4, R5 и R6 имеют вышеуказанное значение, могут быть получены из о-аминобензонитрилов формулы
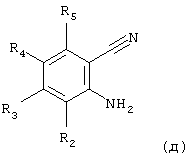
в которой R2, R3, R4 и R5 имеют вышеуказанное значение, путем обработки с помощью реактива Гриньяра формулы R6-MgX, где Х означает атом галогена и R6 имеет вышеуказанное значение, согласно известным специалисту методам.
Аминокетоны формулы (S), в которой R6 означает арильный радикал и R2, R3, R4 и R5 имеют вышеуказанное значение, могут быть получены из антраниловых кислот вышеприведенной формулы (R) путем обработки с помощью бензоилхлорида при температуре кипения с обратным холодильником для получения бензоксазона, который в присутствии реактива Гриньяра формулы R6-MgX, где Х означает атом галогена и R6 означает арильный радикал, может быть превращен в соответствующий о-аминобензофенон, который может быть дебензоилирован с помощью реагентов, таких как, например, бромоводород в виде раствора в воде или в ледяной уксусной кислоте.
Аминокетоны формулы (S), в которой R2, R3, R4, R5 и R6 имеют вышеуказанное значение, могут быть получены из анилинов формулы (Р), в которой R2, R3, R4 и R5 имеют вышеуказанное значение, согласно следующему способу: атом азота анилина формулы (Р) подвергают ацилированию с помощью реагента, придающего орто-ориентирующий характер в реакции металлирования арилов, и таким образом полученное соединение металлируют, затем обрабатывают альдегидом формулы R6-СНО, в которой R6 имеет вышеуказанное значение. В способе тогда дополнительно проводят реакцию окисления полученного спиртового промежуточного соединения, а затем высвобождают азотсодержащую группу для получения аминокетона формулы (S). В случае этого способа переход к орто-ориентирующей группе может быть осуществлен путем обработки анилина формулы (Р) с помощью BOC-реагента и предпочтительно с помощью ди-трет-бутилдикарбоната в апротонном растворителе, таком как тетрагидрофуран, диоксан или диметиловый эфир этиленгликоля, при температуре кипения с обратным холодильником. Металлирование может быть достигнуто путем обработки с помощью литийсодержащего реагента, такого как трет-бутиллитий, втор-бутиллитий, мезитиллитий или н-бутиллитий в присутствии тетраметилэтилендиамина, предпочтительно обработкой н-бутиллития в присутствии тетраметилэтилендиамина, в апротонном растворителе, таком как тетрагидрофуран, диоксан или диметиловый эфир этиленгликоля, при температуре от -80°С до 0°С. Окисление может быть осуществлено в присутствии солей хрома-(VI), несущих пиридильные лиганды, с помощью реактива Сверна или же с помощью комплекса пиридин-триоксид серы в диметилсульфоксиде в присутствии триэтиламина и предпочтительно с помощью пиридинийдихромата в дихлорметане при температуре кипения с обратным холодильником. Азотсодержащая группа может быть получена путем обработки в кислой среде и предпочтительно с помощью трифторуксусной кислоты в дихлорметане при комнатной температуре.
Аналоги промежуточных соединений типа (N) описаны ранее и в особенности в Международной заявке на патент WO-95/05427.
Соединения формулы (III):
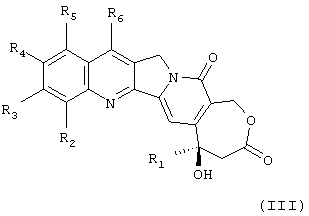
в которой:
R1 означает низший алкильный радикал;
R2, R3, R4 и R5, независимо, означают атом водорода, галоидный радикал или радикал -OSO2R10;
R6 означает линейный или разветвленный алкильный радикал с 1-12 атомами углерода, возможно замещенный одним или несколькими одинаковыми или разными галоидными радикалами; низший гидроксиалкил, (низший алкокси)-(низший алкил), циклоaлкил(низший алкил), группу -(CH2)mSiR7R8R9 или арил(низший алкил), незамещенный или замещенный одним или несколькими одинаковыми или разными заместителями, выбираемыми из радикалов: низший алкил, гидроксил, атом галогена, аминогруппа, (низший алкил)аминогруппа, ди(низший алкил)аминогруппа, СF3 или ОСF3;
R7, R8 и R9, независимо, означают низший алкильный радикал;
R10 означает низший алкильный радикал, возможно замещенный одним или несколькими одинаковыми или разными галоидными радикалами, или арильный радикал, возможно замещенный одним или несколькими одинаковыми или разными низшими алкильными радикалами;
m означает целое число от 0 до 6;
могут быть получены новым способом, отличающимся тем, что соединение формулы (IV):
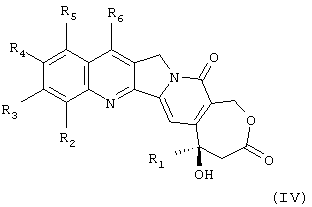
в которой R1, R2, R3, R4 и R5 имеют вышеуказанное значение, в сильно кислой среде в присутствии соли железа-(III) и предшественника свободного радикала R6 обрабатывают раствором, содержащим гидроксильный или алкоксильный радикал.
Хотя в уровне техники упоминается применение подобной реакции к аналогам камптотецина, содержащим α-гидроксилактон (S. Sawada и др., Chem. Pharm. Bull., 39, 2574 (1991); заявка РСТ WO-98/35940), ее использование для аналогов камптотецина, таких как соединения формулы (IV), содержащие β-гидроксилактон, не было предусмотрено и является неожиданным, так как в сильно кислой среде гидроксильную группу у третичного атома углерода и бензильную группу в β-положении по отношению к карбоксильной группе обычно удаляют для получения соответствующего олефина (Nagasawa и др., Heterocycles, 28, 703 (1989); Н. Kimura и др., Chem. Pharm. Bull., 30, 553 (1982); Т. Fujita и др., J. Appl. Chem. Biotechnol., 32, 421 (1982); R.E. Miller и др., J. Org. Chem., 15, 89 (1950); L.F. Fieser и др., J. Am. Chem. Soc., 70, 3209 (1948)).
В случае вышеуказанного способа сильно кислая среда может быть образована водными или неводными кислотами, такими как трифторуксусная кислота или серная кислота и предпочтительно водной серной кислотой; солью железа-(III) предпочтительно является гептагидрат сульфата железа-(III), а предшественником свободного радикала - альдегид формулы R6-CHO, в которой R6 означает линейный или разветвленный алкильный радикал с 1-12 атомами углерода, возможно замещенный одним или несколькими одинаковыми или разными галоидными радикалами; низший гидроксиалкил, (низший алкокси)(низший алкил), циклоалкил-(низший алкил), группу -(СН2)mSiR7R8R9 или арил (низший алкил), незамещенный или замещенный одним или несколькими одинаковыми или разными заместителями, выбираемыми из радикалов: низший алкил, гидроксил, атом галогена, аминогруппа, (низший алкил)аминогруппа, ди(низший алкил)аминогруппа, СF3 или ОСF3. Раствор, содержащий гидроксильные или алкоксильные радикалы, может быть образован пероксидом водорода или трет-бутилгидропероксидом и предпочтительно пероксидом водорода в концентрации 30 объемов.
Соединения согласно настоящему изобретению обладают ценными фармакологическими свойствами. Так, соединения согласно настоящему изобретению обладают ингибирующей топоизомеразу I и/или II активностью или противоопухолевой активностью. Уровень техники позволяет полагать, что соединения согласно изобретению обладают противопаразитарной и/или противовирусной активностью. Соединения согласно настоящему изобретению также могут быть использованы при различных терапевтических применениях.
Ниже, в экспериментальной части, приводится пояснение фармакологических свойств соединений согласно изобретению.
Соединения могут ингибировать топоизомеразу, например, типа I и/или типа II у пациента, например у млекопитающего, такого как человек, путем введения этому пациенту терапевтически эффективного количества одного из соединений согласно изобретению.
Соединения согласно изобретению обладают противоопухолевой активностью. Они могут быть использованы для лечения опухолей, например опухолей, экспрессирующих топоизомеразу, путем введения вышеуказанному пациенту терапевтически эффективного количества одного из соединений согласно изобретению. Примеры опухолей или злокачественных опухолей включают рак пищевода, рак желудка, рак кишечника, рак прямой кишки, рак полости рта, рак глотки, рак гортани, рак легкого, рак ободочной кишки, рак молочной железы, рак шейки матки, рак тела эндометрия, рак яичников, рак простаты, рак яичек, рак мочевого пузыря, рак почек, рак печени, рак поджелудочной железы, рак костей, рак соединительных тканей, рак кожи, например меланомы, рак глаз, рак головного мозга и рак центральной нервной системы, а также рак щитовидной железы, лейкоз, болезнь Ходжкина, лимфомы, другие, чем таковые Ходжкина, множественные миеломы и другие.
Они также могут быть использованы для лечения паразитарных инфекций путем ингибирования паразитирующих в крови жгутиконосцев (например, в случае трипаносомоза или лейшманиозных инфекций) или путем ингибирования плазмодия (как, например, при малярии), а также для лечения вирусных инфекций или вирусных заболеваний.
Эти свойства делают соединения согласно изобретению пригодными для фармацевтического использования. Объектом настоящей заявки являются также лекарственные средства, представляющие собой соединения согласно изобретению и, в частности, продукты общих формул (I), (IIA) или (III), указанные выше. Изобретение относится также к фармацевтическим композициям, содержащим по меньшей мере одно из лекарственных средств, указанных выше, в качестве действующего начала.
Изобретение относится также к фармацевтическим композициям, содержащим соединение согласно изобретению или его фармацевтически приемлемую аддитивную соль с кислотой в сочетании с фармацевтически приемлемым носителем в зависимости от выбранного способа введения (например, перорально, внутривенно, интраперитонеально, внутримышечно, чрескожно или подкожно). Фармацевтическая (например, терапевтическая) композиция может быть в твердой, жидкой форме, в форме липосом или липидных мицелл.
Фармацевтическая композиция может быть в твердой форме, как, например, в форме порошков, пилюль, гранул, таблеток, липосом, желатиновых капсул или свечей. Пилюля, таблетка или желатиновая капсула могут быть покрыты веществом, способным защищать композицию от действия кислоты желудочного сока или ферментов в желудке субъекта в течение периода времени, достаточного для прохождения этой композиции без расщепления в тонкую кишку этого субъекта. Соединение может быть также введено локально, например в само местоположение опухоли. Соединение также может быть введено по способу пролонгированного высвобождения (например, в виде композиции с пролонгированным высвобождением или с помощью насоса для вливания). Соответствующими твердыми носителями могут быть, например, фосфат кальция, стеарат магния, карбонат магния, тальк, сахара, лактоза, декстрин, крахмал, желатина, целлюлоза, метилцеллюлоза, натрийкарбоксиметилцеллюлоза, поливинилпирролидин и воск. Фармацевтические композиции, содержащие соединение согласно изобретению, следовательно, также могут находиться в жидкой форме, как, например, растворы, эмульсии, суспензии или лекарственная форма с пролонгированным высвобождением. Соответствующими жидкими носителями могут быть, например, вода, органические растворители, такие как глицерин, или гликоли, такие как полиэтиленгликоль, также, как их смеси, в изменяемых соотношениях, в воде.
Объектом изобретения является также применение соединений согласно изобретению для приготовления лекарственных средств, предназначенных для ингибирования топоизомераз и преимущественно топоизомераз типа I или типа II; лекарственных средств, предназначенных для лечения опухолей; лекарственных средств, предназначенных для лечения паразитарных инфекций, а также лекарственных средств, предназначенных для лечения вирусных инфекций или вирусных заболеваний.
Доза соединения согласно настоящему изобретению, предусматриваемая для лечения вышеуказанных заболеваний или нарушений, изменяется в зависимости от способа введения, возраста и массы тела излечиваемого субъекта, а также от состояния этого последнего, и ее определяет в конечном счете лечащий врач или ветеринар. Такое, определенное лечащим врачом или ветеринаром, количество называют здесь "терапевтически эффективное количество".
Если только не указано ничего другого, все технические и научные термины, используемые в настоящем описании, имеют то же самое значение, что и таковое, обычно понятное для рядового специалиста в области, к которой относится настоящее изобретение. Точно также, все публикации, заявки на патенты, все патенты и все другие ссылки, приведенные в настоящем описании, включены в виде ссылки.
Следующие примеры представлены для пояснения вышеуказанных методик осуществления и ни в коем случае не должны рассматриваться как ограничение объема охраны изобретения.
Экспериментальная часть:
Пример 1
(5R)-5-Этил-11-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Стадия 1а: Хинидиний-(3R)-3-(3-бензилоксиметил-2-метокси-4-пиридил)-3-гидроксипентаноат
Трет-бутил-3-(3-бензилоксиметил-2-метокси-4-пиридил)-3-гидроксипентаноат (получаемый по способу, описанному в заявке на патент РСТ WO-97/00876) в количестве 40 г (100 ммоль) обрабатывают с помощью 150 мл трифторуксусной кислоты и реакционную среду перемешивают в течение 18 часов при температуре 20°С, затем концентрируют при пониженном давлении. Остаток, обработанный с помощью 200 мл водного насыщенного раствора гидрокарбоната натрия, промывают 2 раза по 100 мл дихлорметаном и полученный в результате раствор подкисляют до рН 1 с помощью 6 н. соляной кислоты, после чего экстрагируют 2 раза по 200 мл дихлорметаном. Объединенные экстракты сушат над сульфатом магния и концентрируют. Таким образом полученную рацемическую кислоту в количестве 31,1 г (90 ммоль), растворенную в 30 мл изопропилового спирта, обрабатывают с помощью раствора 29,2 г (90 ммоль) хинидина в 30 мл изопропилового спирта и полученную в результате смесь перемешивают при температуре 50°С до полного растворения. Тогда температуру оставляют понижаться до 40°С, перемешивание прекращают и оставляют охлаждаться до комнатной температуры. Реакционную среду доводят до температуры 0°С без перемешивания, после чего выдерживают при этой температуре в течение 16 часов. Затем температуру оставляют повышаться до 20°С и перемешивают до кристаллизации. Среду разбавляют изопропиловым спиртом, после чего фильтруют. Осадок промывают изопропиловым спиртом. Правовращающая соль осаждается, тогда как левовращающая соль остается растворенной в изопропиловом спирте. Получают фильтрат, который концентрируют для получения целевого продукта. Анализ с помощью ВЭЖХ (высокоэффективная жидкостная хроматография) (колонка CHIRAL-AGP, 5 микрон (10 см×4 мм); элюируют смесью изопропиловый спирт/вода/фосфатный буфер с рН 6,5 в соотношении 30/920/50, с расходом 1,2 мл/мин; УФ-детектирование при 280 нм) показывает время удерживания 6,4 минуты для левовращающей соли и 2,8 минуты для правовращающей соли и соотношение диастереоизомеров составляет 83/17.
Стадия 1b: (5R)-5-Этил-5-гидрокси-1,3,4,5,8,9-гексагидрооксепино[3,4-с]пиридин-3,9-дион, или (+)-EHHOPD
Полученный в стадии 1а остаток перемешивают в течение 16 часов при температуре 20°С в смеси из 270 мл дихлорметана и 270 мл 1 н. соляной кислоты. После декантации органическую фазу концентрируют и остаток обрабатывают с помощью 87 мл метанола для введения в следующую стадию. Этот раствор выливают, в атмосфере азота, на 27,7 г (13 ммоль) 10%-ного палладия-на-угле с 50%-ной влажностью. Реакционную смесь перемешивают в течение 5 минут, затем приливают раствор 11,5 г (183 ммоль) формиата аммония в 135 мл метанола. Реакционную среду перемешивают в течение 30 минут при изменении температуры, затем нагревают при температуре 40°С в течение 30 минут. Среду тогда фильтруют через слой Clarcel и концентрируют. Приливают 40 мл толуола, который выпаривают, и эту операцию повторяют для удаления следов метанола. Остаток, растворенный в 45 мл тетрагидрофурана, обрабатывают раствором 7,18 г (34,5 ммоль) дициклогексилкарбодиимида в 20 мл тетрагидрофурана. Реакционную среду нагревают при температуре 50°С в течение 1 часа, затем доводят до температуры 20°С и отфильтровывают дициклогексилмочевину. Фильтрат концентрируют досуха и остаток, растворенный в 46 мл ацетонитрила, обрабатывают с помощью 6,0 г (40,5 ммоль) иодида натрия и 5,13 мл (40,5 ммоль) триметилсилилхлорида. Реакционную среду выдерживают при перемешивании при комнатной температуре в течение 5 часов, затем добавляют 28 мл ацетонитрила и 5,6 мл воды. Полученный осадок отфильтровывают, после чего обрабатывают с помощью 10 мл воды и полученную смесь нейтрализуют с помощью раствора гидроксида аммония. Осадок отфильтровывают, затем обрабатывают 40 мл ацетона, к которому добавлено 150 мл воды. Образовавшиеся кристаллы отфильтровывают и высушивают, получая 3 г (+)-EHHOPD с соотношением энантиомеров 99,4/0, 6.
1H-ЯМР (ДМСО-d6, м.д.): 0,8 (т, 3Н); 1,65 (м, 2Н); 3,00-3,35 (к, 2Н); 5,3 (к, 2Н); 5,7 (с, 1Н); 6,35 (д, 1Н); 7,3(д, 1Н), 11,7 (с, 1Н).
Стадия 1с: 2-Aминo-6-фтpopфeнилмeтaнoл
В атмосфере аргона раствор 5 г (32 ммоль) 2-амино-6-фторбензойной кислоты в 100 мл безводного тетрагидрофурана обрабатывают при комнатной температуре с помощью литийалюминийгидрида (1 М раствор в тетрагидрофуране; 64 мл; 64 ммоль). Реакционную среду перемешивают в течение трех часов, затем гидролизуют при температуре 0°С с помощью 100 мл водного насыщенного раствора хлорида аммония. Полученную в результате смесь экстрагируют 2 раза по 70 мл этилацетатом. Объединенные экстракты промывают водой и водным насыщенным раствором хлорида натрия, затем сушат над сульфатом магния и концентрируют, получая 3,8 г целевого продукта в виде твердого вещества белого цвета (т.пл.: 93°С).
ИК-спектр (КВr): 784, 1001, 1471, 1591, 1621 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 4,44 (дд, 2Н); 4,93 (т, 1Н); 5,27 (с, 2Н); 6,27 (т, 1Н); 6,45 (д, 1Н); 6,96 (к, 1Н).
Стадия 1d: Этил-2-(3-фтор-2-гидроксиметилфенилкарбамоил)-ацетат
Раствор 3,8 г (27 ммоль) аминобензилового спирта (полученного в стадии 1с) и 4,3 г (64 ммоль) имидазола в 52 мл N,N-диметилформамида обрабатывают с помощью 8,37 мл (32 ммоль) трет-бутилдифенилсилилхлорида. Полученную в результате смесь перемешивают в течение двух часов при комнатной температуре, затем добавляют 100 мл воды и экстрагируют 2 раза по 60 мл этилацетатом. Объединенные экстракты промывают водой и водным насыщенным раствором хлорида натрия, после чего сушат над сульфатом магния и концентрируют. Таким образом полученное промежуточное силилированное соединение в количестве 10 г обрабатывают 52 мл ацетонитрила, затем к раствору добавляют 4,5 мл (32,4 ммоль) триэтиламина и полученную смесь обрабатывают путем прикапывания 4,15 мл (32,4 ммоль) этилмалонилхлорида. Полученную в результате смесь перемешивают в течение двух часов при комнатной температуре, затем добавляют 100 мл воды и экстрагируют 2 раза по 60 мл этилацетатом. Объединенные экстракты промывают водой и водным насыщенным раствором хлорида натрия, после чего сушат над сульфатом магния и концентрируют. Остаток в количестве 16 г растворяют в 50 мл тетрагидрофурана и обрабатывают путем прикапывания тетрабутиламмонийфторидом (1 М раствор в тетрагидрофуране; 27 мл; 27 ммоль). Полученную в результате смесь перемешивают в течение 1 часа при комнатной температуре, затем добавляют 100 мл воды и экстрагируют 2 раза по 60 мл этилацетатом. Объединенные экстракты промывают водой и водным насыщенным раствором хлорида натрия, после чего сушат над сульфатом магния и концентрируют. Очистка остатка путем хроматографии среднего давления (SiO2, CH2Cl2/CH3OH в соотношении 95/5) дает 4,8 г твердого вещества белого цвета (т.пл.: 91°С).
ИК-спектр (КВr): 1472, 1542, 1589, 1657, 1719, 3286, 3482 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 1,19 (т, 3Н); 3,54 (с, 2Н); 4,14 (к, 2Н); 4,55 (дд, 2Н); 5,21 (т, 1Н); 6,97 (т, 1Н); 7,31 (дд, 1Н); 7,53 (д, 1Н).
Стадия 1е: Этил-5-фтор-2-оксо-1,2-дигидро-3-хинолинкарбоксилат
Раствор 4,8 г (19 ммоль) производного малоновой кислоты (полученного в стадии 1d) в 280 мл дихлорметана обрабатывают с помощью 8,3 г (22 ммоль) пиридинийдихромата. Полученную в результате суспензию перемешивают в течение 4 часов при комнатной температуре, затем обрабатывают с помощью 30 мл (220 ммоль) триэтиламина. Реакционную среду перемешивают при комнатной температуре в течение 16 часов, после чего концентрируют при пониженном давлении. Очистка остатка путем хроматографии среднего давления (SiО2, СН2Сl2/СН3ОН в соотношении 95/5) дает 2,1 г твердого вещества желтого цвета (т.пл.: 180°С).
ИК-спектр (КВr): 1441, 1498, 1655, 1747 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 1,31 (т, 3Н); 4,28 (к, 2Н); 7,06 (т, 1Н); 7,16 (д, 1Н); 7,61 (дд, 1Н); 8,43 (с, 1Н); 12,27 (с, 1Н).
Стадия 1f: Этил-2-хлор-5-фтор-3-хинолинкарбоксилат
2,1 г Хинолона (полученного в стадии 1е) нагревают при температуре 80°С в 14 мл оксихлорида фосфора до полного протекания реакции (контролируют с помощью тонкослойной хроматографии (ТСХ): SiO2, СН2Сl2/СН3ОН в соотношении 95/5). Полученный в результате раствор концентрируют при пониженном давлении и остаток обрабатывают водой. Таким образом полученный осадок отфильтровывают, промывают водой до нейтрального значения рН и высушивают при пониженном давлении в присутствии пенткосида фосфора, получая 1,8 г твердого вещества белого цвета (т.пл.: 97°С).
ИК-спектр (КВr): 1268, 1631, 1723 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 1,38 (т, 3Н); 4,42 (к, 2Н); 7,60 (т, 1Н); 7,89 (д, 1Н); 7,97 (дд, 1Н); 8,92 (с, 1Н).
Стадия 1g: 2-Хлор-5-фтор-3-хинолилметанол
Раствор 1,8 г (6,7 ммоль) хинолинкарбоксилата (полученного в стадии 1f) в 40 мл дихлорметана в атмосфере аргона обрабатывают путем прикапывания раствором диизобутилалюминийгидрида (1 М раствор в дихлорметане; 20 мл; 20 ммоль) при температуре, поддерживаемой при 10°С с помощью бани с водой и льдом. Реакционную смесь перемешивают в течение 1 часа при комнатной температуре, затем выливают в 200 мл 20%-ного раствора тартрата натрия и калия. Полученную в результате смесь интенсивно перемешивают в течение 1 часа, затем фильтруют через целит. Фильтрат экстрагируют 2 раза по 100 мл дихлорметаном. Объединенные экстракты промывают водой и водным насыщенным раствором хлорида натрия, затем сушат над сульфатом магния и концентрируют. Очистка остатка путем хроматографии среднего давления (SiO2, СН2Сl2/СН3ОН в соотношении 98/2) дает 450 мг твердого вещества белого цвета (т.пл.: 176°С).
1H-ЯМР (ДМСО-d6, м.д.): 4,71 (д, 2Н); 5,78 (т, 3Н); 7,51 (т, 1Н); 7,75-7,83 (м, 2Н), 8,50 (с, 1Н).
Стадия 1h: (5R)-5-Этил-11-фтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Раствор 422 мг (2 ммоль) хинолилметанола (полученного в стадии 1g), 446 мг (2 ммоль) (+)-EHHOPD (полученного в стадии 1b) и 592 мг (2,2 ммоль) трифенилфосфина в 8 мл N,N-диметилформамида обрабатывают путем прикапывания 0,43 мл (2,2 ммоль) изопропилазодикарбоксилата. Реакционную смесь перемешивают в течение 16 часов при комнатной температуре, затем добавляют 100 мл воды и экстрагируют 2 раза по 100 мл этилацетатом. Объединенные экстракты промывают водой и водным насыщенным раствором хлорида натрия, затем сушат над сульфатом магния и концентрируют при пониженном давлении. Остаток очищают путем хроматографии среднего давления (SiO2; этилацетат/гептан в соотношении 30/70). Смесь 325 мг (0,78 ммоль) полученного промежуточного соединения, 42 мг (0,156 ммоль) трифенилфосфина, 114 мг (1,17 ммоль) ацетата калия, 276 мг (0,86 ммоль) тетрабутиламмонийбромида и ацетата палладия (0,078 ммоль) в безводном ацетонитриле кипятят с обратным холодильником в течение 16 часов в атмосфере аргона, затем охлаждают до комнатной температуры и концентрируют при пониженном давлении. Остаток очищают путем хроматографии среднего давления (SiO2; СН3ОН/СН2Сl2 в соотношении 5/95), получая 80 мг ожидаемого твердого вещества (т.пл. >250°С).
ИК-спектр (КВr): 1659, 1734, 3386 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,85 (к, 2Н); 3,07 (д, 1Н); 3,46 (д, 1Н), 5,28 (с, 2Н); 5,39 (д, 1Н); 5,52 (д, 1Н); 6,02 (с, 1Н); 7,43 (с, 1Н); 7,55 (т, 1Н); 7,85 (к, 1Н); 8,01 (д, 1Н); 8,82 (с, 1Н).
Пример 2
(5R)-5-Этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Это соединение получают при использовании 2-амино-4-фторбензойной кислоты в стадиях 1с-1h согласно методике вышеприведенного примера 1. Получают твердое вещество (т.пл. >250°С).
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,84 (к, 2Н); 3,04 (д, 1Н); 3,47 (д, 1Н); 5,24 (с, 2Н); 5,39 (д, 1Н); 5,52 (д, 1Н); 6,06 (с, 1Н); 7,39 (с, 1Н); 7,65 (т, 1Н); 7,88 (д, 1Н); 8,22 (дд, 1Н); 8,71 (с, 1Н).
Пример 3
(5R)-5-Этил-8-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Это соединение получают при использовании 2-амино-3-фторбензойной кислоты (получаемой согласно Muchowski и др., J. Org. Chem., 45, 4798) в стадиях 1с-1h согласно методике вышеприведенного примера 1. Получают твердое вещество (т.пл. >250°С).
ИК-спектр (КВr): 1659, 1731, 3344 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 0,88 (т, 3Н); 1,85 (к, 2Н); 3,07 (д, 1Н); 3,47 (д, 1Н); 5,29 (с, 2Н); 5,40 (д, 1Н); 5,53 (д, 1Н); 6,06 (с, 1Н); 7,44 (с, 1Н); 7,69 (м, 2Н); 7,96 (м, 1Н); 8,75 (с, 1Н).
Пример 4
(5R)-12-Бензил-5-этил-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Стадия 4а: 1-(2-Аминофенил)-2-фенил-1-этанон
Раствор 4,25 г (36 ммоль) 2-аминобензонитрила в 40 мл безводного диэтилового эфира при температуре 0°С и в атмосфере аргона обрабатывают бензилмагнийхлоридом (2 М раствор в тетрагидрофуране; 50 мл; 100 ммоль). Реакционную среду выдерживают при перемешивании в течение 1 часа при комнатной температуре, затем при температуре 0°С гидролизуют путем добавления 10%-ной соляной кислоты, перемешивают в течение 1 часа и нейтрализуют гидроксидом натрия. Полученную в результате смесь экстрагируют этилацетатом. Объединенные экстракты промывают водой и водным насыщенным раствором хлорида натрия, затем сушат над сульфатом магния и концентрируют, получая 3,5 г желательного продукта в виде твердого вещества белого цвета (т.пл.: 100-101°С).
ИК-спектр (КВr): 1469, 1612, 1725 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 4,25 (с, 2Н); 6,53 (т, 1Н); 6,74 (д, 1Н); 7,2-7,35 (м, 8Н); 7,90 (д, 1Н).
Стадия 4b: Этил-4-бензил-2-оксо-1,2-дигидро-3-хинолинкарбоксилат
Раствор 13,5 г (16 ммоль) аминокетона (полученного в стадии 4а) и 3,9 мл (28 ммоль) триэтиламина в 66 мл ацетонитрила при температуре 10°С обрабатывают путем прикапывания 3,64 мл (28 ммоль) этилмалонилхлорида. Реакционную среду перемешивают в течение 16 часов при комнатной температуре, затем обрабатывают с помощью этилата натрия, получаемого путем растворения 0,4 г (17 ммоль) натрия в 25 мл этанола. Полученную в результате смесь перемешивают в течение 16 часов при комнатной температуре, затем добавляют 200 мл воды и экстрагируют 2 раза по 100 мл дихлорметаном. Объединенные экстракты промывают водой и водным насыщенным раствором хлорида натрия, после чего сушат над сульфатом магния и концентрируют. Остаток обрабатывают диэтиловым эфиром, получая осадок, который отфильтровывают, высушивают при пониженном давлении при температуре 50°С, получая ожидаемое твердое вещество (т.пл.: 230°С).
1H-ЯМР (ДМСО-d6, м.д.): 1,19 (т, 3Н); 4,17 (с, 2Н); 4,27 (к, 2Н); 7,13 (т, 1Н); 7,15-7,20 (м, 1Н); 7,20-7,40 (м, 5Н); 7,49 (т, 1Н); 7,69 (д, 1Н); 12,15 (с, 1Н).
Стадия 4с: (5R)-12-Бензил-5-этил-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино-[1,2-b]хинолин-3,15-дион
Полученный согласно стадии 4b хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1. Получают твердое вещество (т.пл. >250°С).
ИК-спектр (КВr): 1578, 1655, 1751 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,87 (к, 2Н); 3,05 (д, 1Н); 3,49 (д, 1Н); 4,65 (д, 1Н); 4,70 (д, 1Н); 5,20 (д, 1Н); 5,25 (д, 1Н); 5,39 (д, 1Н); 5,52 (д, 1Н); 6,06 (с, 1Н); 7,15-7,30 (м, 5Н); 7,41 (с, 1Н); 7,67 (т, 1Н); 7,83 (т, 1Н); 8,16 (д, 1Н); 8,28 (д, 1Н).
Пример 5
(5R)-12-Бутил-5-этил-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]-индолизино[1,2-b]хинолин-3,15-дион
2-Аминобензонитрил обрабатывают н-бутилмагнийбромидом согласно методике, подобной таковой стадии 4а, и полученный в результате аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1. Получают твердое вещество (т.пл.: 220-221°С).
ИК-спектр (КВr): 1611, 1655, 1725 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 0,96 (т, 3Н); 1,49 (к, 2Н); 1,67 (к, 2Н); 1,86 (к, 2Н); 3,05 (д, 1Н); 3,19 (т, 2Н); 3,49 (д, 1Н); 5,28 (с, 2Н); 5,40 (д, 1Н); 5,54 (д, 1Н); 6,05 (с, 1Н); 7,39 (с, 1Н); 7,72 (т, 1Н); 7,85 (т, 1Н); 8,14 (д, 1Н); 8,26 (д, 1Н).
Пример 6
(5R)-5,12-Диэтил-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Аминобензонитрил обрабатывают этилмагнийбромидом согласно методике, подобной таковой стадии 4а, и полученный в результате аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1. Получают твердое вещество (т.пл.: >280°С).
ИК-спектр (КВr): 1652, 1758, 3329 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 0,85 (т, 3Н); 1,31 (т, 3Н); 1,87 (к, 2Н); 3,04 (д, 1Н); 3,24 (к, 2Н); 3,54 (д, 1Н); 5,25 (с, 2Н); 5,36 (д, 1Н); 5,53 (д, 1Н); 6,06 (с, 1Н); 7,39 (с, 1Н); 7,72 (т, 1Н); 7,85 (т, 1Н); 8,15 (д, 1Н); 8,28 (д, 1Н).
Пример 7
(5R)-5-Этил-5-гидрокси-12-фенил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Аминофенилфенилметанон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1. Получают твердое вещество (т.пл.: >250°С).
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,85 (к, 2Н); 3,05 (д, 1Н); 3,49 (д, 1Н); 5,09 (с, 2Н); 5,38 (д, 1Н); 5,50 (д, 1Н); 6,07 (с, 1Н); 7,45 (с, 1Н); 7,60-7,75 (м, 6Н); 7,82 (д, 1Н); 7,90 (т, 1Н); 8,25 (д, 1Н).
Пример 8
(5R)-12-Циклогексил-5-этил-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Аминобензонитрил обрабатывают циклогексилмагнийхлоридом согласно методике, подобной таковой стадии 4а, и полученный в результате аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1. Получают твердое вещество (т.пл.: >250°С).
ИК-спектр (КВr): 1655, 1728, 3500 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,42 (т, 1Н); 1,59 (т, 2Н); 1,84 (м, 9Н); 3,04 (д, 1Н); 3,48 (д, 1Н); 3,69 (м, 1Н); 5,39 (д, 1Н); 5,40 (с, 2Н); 5,53 (д, 1Н); 6,06 (с, 1Н); 7,38 (с, 1Н); 7,70 (т, 1Н); 7,83 (т, 1Н); 8,13 (д, 1Н); 8,37 (с, 1Н).
Пример 9
(5R)-5-Этил-5-гидрокси-12-(4-метилфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Аминофенил-4-метилфенилметанон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1. Получают твердое вещество (т.пл.:>280°С).
ИК-спектр (КВr): 1655, 1754, 3407 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 0,87 (т, 3Н); 1,87 (к, 2Н); 2,47 (с, 3Н); 3,07 (д, 1Н); 3,48 (д, 1Н); 5,07 (д, 2Н); 5,39 (д, 1Н); 5,49 (д, 1Н); 6,04 (с, 1Н); 7,45 (с, 1Н); 7,48 (м, 2Н); 7,54 (м, 2Н); 7,65 (м, 1Н); 7,85 (м, 2Н); 8,22 (д, 1Н).
Пример 10
(5R)-10-Хлор-5-этил-12-(2-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-5-хлорфенил-2-фторфенилметанон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1. Получают твердое вещество (т.пл.: >250°С).
ИК-спектр (КВr): 1656, 1744, 3397 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,85 (к, 2Н); 3,06 (д, 1Н); 3,47 (д, 1Н); 4,93 (д, 1Н); 5,17 (д, 1Н); 5,37 (д, 1Н); 5,49 (д, 1Н); 6,05 (с, 1Н); 7,46 (с, 1Н); 7,50-7,65 (м, 3Н); 7,65-7,80 (м, 2Н); 7,91 (д, 1Н); 8,27 (д, 1Н).
Пример 11
(5R)-5-Этил-9,10-дифтор-5-гидрокси-12-фенил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Стадия 11а: 6,7-Дифтор-2-фенил-4Н-бензо[d][3,1]оксазин-4-он
Смесь 3,46 г (20 ммоль) 2-амино-4,5-дифторбензойной кислоты и 56 мл (480 ммоль) бензоилхлорида кипятят с обратным холодильником в течение 16 часов, затем выливают в 200 мл водного насыщенного раствора гидрокарбоната натрия и перемешивают в течение двух часов при температуре 80°С. Полученную в результате смесь экстрагируют 2 раза по 100 мл дихлорметаном. Объединенные экстракты промывают водой и водным насыщенным раствором хлорида натрия, затем сушат над сульфатом магния и концентрируют при пониженном давлении. Остаток обрабатывают диэтиловым эфиром и таким образом полученный осадок отфильтровывают, промывают диэтиловым эфиром и высушивают при пониженном давлении, получая 3,2 г твердого вещества белого цвета (т.пл.: 154°С).
ИК-спектр (КВr): 1613, 1657, 3341, 3467 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 7,5-7,8 (м, 3Н); 7,8-7,9 (м, 1Н); 8,1-8,3 (м, 1Н).
Стадия 11b: 2-Бензоил-4,5-дифтор-1-фенилкарбоксамидобензол
Суспензию 6,78 г (26 ммоль) бензоксазина (полученного согласно стадии 11а) в 260 мл дихлорметана обрабатывают путем прикапывания в атмосфере аргона и при температуре -78°С фенилмагнийбромидом (3 М раствор в диэтиловом эфире; 22 мл; 66 ммоль). Полученную смесь перемешивают при температуре -78°С в течение 1 часа, затем гидролизуют путем добавления 200 мл водного насыщенного раствора хлорида аммония и экстрагируют 2 раза по 100 мл дихлорметаном. Объединенные экстракты промывают водой и водным насыщенным раствором хлорида натрия, после чего сушат над сульфатом магния и концентрируют при пониженном давлении. Остаток, обработанный диизопропиловым эфиром, дает белые кристаллы, которые отделяют путем фильтрации и высушивают. Получают 7,3 г продукта (т.пл.: 58-59°С).
ИК-спектр (КВr): 1423, 1537, 1599, 1682 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 7,4-7,6 (м, 9Н); 7,69 (д, 2Н); 7,88 (дд, 1Н).
Стадия 11с: 2-Амино-4,5-дифторфенилфенилметанон
Раствор 7,3 г (21,7 ммоль) N-бензоилированного аминокетона (полученного согласно стадии 11b) в 300 мл ледяной уксусной кислоты обрабатывают с помощью 150 мл 48%-ной бромоводородной кислоты и реакционную среду кипятят с обратным холодильником в течение 10 часов. После охлаждения до комнатной температуры полученную смесь концентрируют при пониженном давлении, затем обрабатывают с помощью 200 мл водного насыщенного раствора гидрокарбоната натрия и экстрагируют 2 раза по 100 мл этилацетатом. Объединенные экстракты промывают водой и водным насыщенным раствором хлорида натрия, затем сушат над сульфатом магния и концентрируют при пониженном давлении. Остаток обрабатывают пентаном и таким образом образовавшийся осадок отфильтровывают, получая 4 г твердого вещества светло-желтого цвета (т.пл.: 100-101°С).
ИК-спектр (КВr): 1514, 1563, 1645, 3372, 3482 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 6,83 (дд, 1Н), 7,1-7,4 (м, 3Н), 7,5-7,7 (м, 5Н).
Стадия 11d: (5R)-5-Этил-9,10-дифтор-5-гидрокси-12-фенил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]-индолизино[1,2-b]хинолин-3,15-дион
Полученный в стадии 11с аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1. Получают твердое вещество (т.пл. >250°С).
ИК-спектр (КВr): 1659, 1734, 3386 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 0,85 (т, 3Н); 1,80 (к, 2Н); 3,06 (д, 1Н); 3,45 (д, 1Н); 5,00 (д, 1Н); 5,35 (д, 1Н); 5,48 (д, 1Н); 6,03 (с, 1Н); 7,39 (с, 1Н); 7,55-7,75 (м, 6Н); 8,24 (дд, 1Н)).
Пример 12
(5R)-5-Этил-9-фтор-5-гидрокси-12-фенил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4-фторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11a-11с, и полученный в результате аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1. Получают твердое вещество (т.пл.: >250°С).
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,84 (к, 2Н); 3,06 (д, 1Н); 3,46 (д, 1Н); 5,00 (д, 1Н); 5,08 (д, 1Н); 5,37 (д, 1Н); 5,49 (д, 1Н); 6,03 (с, 1Н); 7,43 (с, 1Н); 7,50-7,80 (м, 6Н); 7,85 (т, 1Н); 7,96 (д, 1Н).
Пример 13
(5R)-12-Бутил-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Стадия 13а: N-(3,4-Дифторфенил)ацетамид
Смесь 50 мл (500 ммоль) 3, 4-дифторанилина и 70 мл (500 ммоль) триэтиламина в 1,5 л дихлорметана охлаждают с помощью бани со льдом. Добавляют по каплям 71,5 мл (750 ммоль) уксусного ангидрида и реакционную смесь перемешивают в течение 1 часа при комнатной температуре. Полученную смесь затем промывают последовательно водой, 10%-ным раствором гидрокарбоната натрия и водным насыщенным раствором хлорида натрия. Высушенную над сульфатом натрия органическую часть концентрируют при пониженном давлении. Остаток суспендируют в пентане, отфильтровывают и высушивают при пониженном давлении, получая ожидаемый анилид в виде твердого вещества белого цвета (т.пл.: 126-127,5°С).
1H-ЯМР (ДМСО-d6, м.д.): 2,15 (с, 3Н); 7,10-7,65 (м, 2Н); 7,65-8,10 (м, 1Н); 10,30 (уш.пик 1Н).
Стадия 13b: 2-Хлор-6,7-дифтор-3-хинолинкарбальдегид
К реактиву Vilsmeyer, полученному в атмосфере аргона с 34 мл (440 ммоль) безводного N,N-диметилформамида, охлажденному на бане со льдом, обработанному путем прикапывания 103 мл (1,1 моль) оксихлорида фосфора, затем перемешиваемому в течение 0,5 часа перед тем, как оставить температуру повышаться до комнатной, добавляют 32 г (220 ммоль) полученного в стадии 13а ацетанилида. Таким образом полученную смесь перемешивают в течение 16 часов при температуре 70°С, затем охлаждают до комнатной температуры. Реакционную смесь тогда приливают по каплям к 400 мл смеси воды со льдом и полученную смесь перемешивают в течение двух часов. Полученный осадок отфильтровывают и промывают вплоть до нейтрального значения рН, затем высушивают при пониженном давлении в присутствии пентоксида фосфора, получая твердое вещество желтого цвета (т.пл: 226-229°С).
ИК-спектр (КВr): 888, 1061, 1262, 1507, 1691 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 8,17 (дд, 1Н); 8,39 (дд, 1Н); 8,97 (д, 1Н); 10,34 (д, 1Н).
Стадия 13с: 2-Хлор-6,7-дифтор-3-хинолилметанол
Суспензию 9 г (39 ммоль) полученного в стадии 13b хинолинкарбальдегида в 400 мл метанола обрабатывают с помощью 2 г (53 ммоль) боргидрида натрия при комнатной температуре в течение 0,5 часа. Избыток боргидрида разрушают с помощью 2 мл уксусной кислоты и реакционную среду концентрируют при пониженном давлении. Остаток, растворенный в 500 мл этилацетата, промывают последовательно водным 10%-ным раствором гидрокарбоната натрия, водой и водным насыщенным раствором хлорида натрия. Органическую фазу, осушенную над сульфатом магния, концентрируют при пониженном давлении. Остаток перекристаллизуют из 1,2-дихлорэтана, получая ожидаемый хинолилметанол в виде твердого вещества бежевого цвета (т.пл.: 166,5-167°С).
ИК-спектр (КВr): 871, 1038, 1253, 1513 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 4,67 (д, 2Н); 5,80 (т, 1Н); 8,01 (дд, 1Н); 8,22 (дд, 1Н); 8,48 (с, 1Н).
Стадия 13d: (5R)-5-Этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино-[1,2-b]хинолин-3,15-дион
Полученный в стадии 13с хинолилметанол обрабатывают с помощью (+)-EHHOPD согласно методике стадии 1h. Получают твердое вещество белого цвета.
ИК-спектр (КВr): 871, 1261, 1512, 1579, 1654, 1746 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 0,87 (т, 3Н); 1,85 (м, 2Н); 3,08 (д, 1Н); 3,44 (д, 1Н); 5,26 (с, 2Н); 5,39 (д, 2Н); 5,52 (д, 1Н); 5,99 (с, 1Н); 7,39 (с, 1Н); 8,15 (дд, 1Н); 8,23 (дд, 1Н); 8,68 (с, 1Н).
Стадия 13е: (5R)-12-Бутил-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]-индолизино[1,2-b]хинолин-3,15-дион
100 мг (0,25 ммоль) Продукта, полученного в стадии 13d, растворяют в смеси из 1,33 мл воды и 1 мл 95%-ной серной кислоты. К этому раствору добавляют 28 мг (0,10 ммоль) гептагидрата сульфата железа-(II), 0,17 мл (1,60 ммоль) валеральдегида и полученный в результате раствор охлаждают на бане со льдом.
Реакционную смесь затем обрабатывают путем прикапывания 0,38 мл (1 ммоль) 30%-ного пероксида водорода, перемешивают в течение 5 часов при комнатной температуре, после чего разбавляют с помощью 50 мл воды и экстрагируют 4 раза по 50 мл дихлорметаном. Объединенные экстракты промывают водой и водным насыщенным раствором хлорида натрия, затем сушат над сульфатом магния и концентрируют при пониженном давлении. Остаток очищают путем хроматографии среднего давления (SiO2; СН3ОН/СН2Сl2 в соотношении 5/95), получая ожидаемое твердое вещество (т.пл. >275°С).
ИК-спектр (КВr): 1656, 1748, 3385 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 0,85 (т, 3Н); 0,94 (т, 3Н); 1,47 (к, 2Н); 1,64 (м, 2Н); 1,83 (к, 2Н); 3,05 (д, 1Н); 3,16 (м, 2Н); 3,47 (д, 1Н); 5,27 (с, 2Н); 5,39 (д, 1Н); 5,52 (д, 1Н); 6,05 (с, 1Н); 7,35 (с, 1Н); 8,13 (с, 1Н); 8,32 (м, 1Н).
Пример 14
(5R)-12-Бензил-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в стадии 13d продукт обрабатывают фенилацетальдегидом согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество (т.пл.: 275°С (разложение)).
ИК-спектр (КВr): 1656, 1707, 1749 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,84 (к, 2Н); 3,05 (д, 1Н); 3,48 (д, 1Н); 4,64 (с, 2Н); 5,19 (д, 2Н); 5,38 (д, 1Н); 5,51 (д, 1Н); 6,06 (с, 1Н); 7,20 (м, 1Н); 7,26 (м, 4Н); 7,37 (с, 1Н); 8,15 (т, 1Н); 8,31 (т, 1Н).
Пример 15
(5R)-5-Этил-9,10-дифтор-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1H, 3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в стадии 13d продукт обрабатывают бутиральдегидом согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество (т.пл.: 250°С).
ИК-спектр (КВr): 1656, 3425 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,04 (т, 3Н); 1,70 (к, 2Н); 1,84 (к, 2Н); 3,07 (д, 1Н); 3,15 (т, 2Н); 3,46 (д, 1Н); 5,25 (с, 1Н); 5,39 (д, 1Н); 5,52 (д, 1Н); 6,02 (с, 1Н); 7,36 (с, 1Н); 8,12 (м, 1Н); 8,34 (м, 1Н).
Пример 16
(5R)-5,12-Диэтил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в стадии 13d продукт обрабатывают пропионовым альдегидом согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество (т.пл. >275°С).
ИК-спектр (КВr): 1656, 1725, 3308 см-1.
1H-ЯМР (ДMCO-d6, м.д.): 0,85 (т, 3Н); 1,28 (т, 3Н); 1,83 (к, 2Н); 3,05 (д, 1Н); 3,19 (к, 2Н); 3,47 (д, 1Н); 5,29 (с, 2Н); 5,39 (д, 1Н); 5,52 (д, 1Н); 6,06 (с, 1Н); 7,36 (с, 1Н); 8,15 (м, 1Н); 8,35 (м, 1Н).
Пример 17
(5R)-5-Этил-9,10-дифтор-5-гидрокси-12-(2-триметилсилилэтил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в стадии 13d продукт обрабатывают с помощью 3-триметилсилилпропаналя (получаемого согласно Т.К. Sarkar и др., Tetrahedron, 46, 1885 (1990)) согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество (т.пл.: 276°С).
1H-ЯМР (ДМСО-d6, м.д.): 0,14 (с, 9Н); 0,86 (м, 5Н); 1,83 (к, 2Н); 3,07 (м, 3Н); 3,46 (д, 1Н); 5,26 (с, 2Н); 5,40 (д, 1Н); 5,51 (д, 1Н); 6,06 (с, 1Н); 7,34 (с, 1Н); 8,14 (м, 2Н).
Пример 18
(5R)-5-Этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
При использовании 3,5-дифторанилина осуществляют стадии 13а-13с и таким образом полученный хинолилметанол обрабатывают с помощью (+)-EHHOPD согласно методике стадии 1h. Получают твердое вещество белого цвета (т.пл.: 227°С (разложение)).
ИК-спектр (КВr): 1638, 1748, 3310 см-1.
1H-ЯМP (ДМСО-d6, м.д.): 0,87 (т, 3Н); 1,85 (к, 2Н); 3,07 (д, 1Н); 3,46 (д, 1Н); 5,26 (с, 2Н); 5,40 (д, 1Н); 5,52 (д, 1Н); 6,03 (с, 1Н); 7,42 (с, 1Н); 7,70 (т, 1Н); 7,80 (д, 1Н); 8,82 (с, 1Н).
Пример 19
(5R)-12-Бутил-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 18 продукт обрабатывают валеральдегидом согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество (т.пл.: 190°С).
ИК-спектр (КВr): 1657, 1751, 3385 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 0,96 (т, 3Н); 1,49 (к, 2Н); 1,66 (к, 2Н); 1,84 (к, 2Н); 3,07 (д, 1Н); 3,46 (д, 1Н); 5,30 (с, 2Н); 5,40 (д, 1Н); 5,53 (д, 1Н); 6,03 (с, 1Н); 7,39 (с, 1Н); 7,67 (т, 1Н); 7,78 (д, 1Н).
Пример 20
(5R)-5,12-Диэтил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 18 продукт обрабатывают пропионовым альдегидом согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество (т.пл.: 255°С).
1H-ЯМР (ДМСО-d6, м.д.):. 0,86 (т, 3Н); 1,33 (т, 3Н); 1,84 (к, 2Н); 3,06 (д, 1Н); 3,29 (м, 2Н); 3,57 (д, 1Н); 5,28 (с, 2Н); 5,35 (д, 1Н); 5,53 (д, 1Н); 6,04 (с, 1Н); 7,38 (с, 1Н); 7,69 (м, 1Н); 7,80 (м, 1Н).
Пример 21
(5R)-5-Этил-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
(5R)-5-Этил-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион (полученный по методике, описанной в заявке на патент РСТ WO-97/00876) обрабатывают бутиральдегидом согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество (т.пл.: 265°С (разложение)).
ИК-спектр (КВr): 1590, 1653, 3287 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 0,87 (т, 3Н); 1,06 (т, 3Н); 1,73 (к, 2Н); 1,82 (к, 2Н); 3,06 (д, 1Н); 3,19 (т, 2Н); 3,48 (д, 1Н); 5,24 (с, 2Н); 5,31 (д, 1Н); 5,54 (д, 1Н); 6,02 (с, 1Н); 7,38 (с, 1Н); 7,72 (т, 1Н); 7,85 (т, 1H), 8,15 (д, 1Н); 8,28 (с, 1H).
Пример 22
(5R)-5-Этил-5-гидрокси-12-(2-триметилсилилэтил)-4,5,13,15-тетрагидро-1H, 3Н-оксепино [3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
(5R)-5-Этил-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’, 4’:6,7]индолизино[1,2-b]хинолин-3,15-дион (полученный по методике, описанной в заявке на патент РСТ WO-97/00876) обрабатывают с помощью 3-триметилсилилпропаналя (полученного согласно Т.К. Sarkar и др.. Tetrahedron, 46, 1885 (1990)) согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество (т.пл. >250°С).
ИК-спектр (КВr): 1655, 1753, 3420 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 0,11 (с, 9Н); 0,88 (т, 3Н); 0,91 (м, 2Н); 1,89 (к, 2Н); 3,07 (д, 1H); 3,12 (м, 2Н); 3,47 (д, 1H); 5,25 (с, 2Н); 5,33 (д, 1H); 5,41 (д, 1H); 5,54 (д, 1H); 6,02 (с, 1H); 7,39 (с, 1H); 7,73 (т, 1H), 7,82 (т, 1H); 8,15 (с, 1H).
Пример 23
(5R)-12-Бутил-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 2 продукт обрабатывают валеральдегидом согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество (т.пл.: 235-236°С).
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 0,95 (т, 3Н); 1,48 (м, 2Н); 1,67 (м, 2Н); 1,85 (к, 2Н); 3,06 (д, 1H); 3,20 (т, 2Н); 3,46 (д, 1Н); 5,27 (с, 2Н); 5,40 (д, 1Н); 5,53 (д, 1Н); 6,02 (с, 1Н); 7,38 (с, 1Н); 7,64 (т, 1Н), 7,87 (д, 1Н); 8,36 (дд, 1Н).
Пример 24
(5R)-5,12-Диэтил-9-фтор-5-гидрокси-4,5,13,15-гетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 2 продукт обрабатывают пропионовым альдегидом согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,31 (т, 3Н); 1,85 (к, 2Н); 3,06 (д, 1Н); 3,22 (к, 2Н); 3,47 (д, 1Н); 5,24 (с, 2Н); 5,39 (д, 1Н); 5,53 (д, 1Н); 6,03 (с, 1Н); 7,38 (с, 1Н); 7,64 (т, 1Н); 7,87 (д, 1Н); 8,37 (дд, 1Н).
Пример 25
(5R)-5-Этил-5-гидрокси-12-изопентил-4,5,13,15-тетрагидро-1Н, 3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Аминобензонитрил обрабатывают изопентилмагнийбромидом согласно методике, подобной таковой стадии 4а, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1. Получают твердое вещество (т.пл.: 263°С).
ИК-спектр (КВr): 1655, 1743, 3343 см-1.
1H-ЯМР (ДМСО-d6, м.д.): 0,85 (т, 3Н); 1,00 (д, 6Н); 1,54 (м, 2Н); 1,79 (м, 1Н); 1,82 (м, 2Н); 3,06 (4, 1Н); 3,14 (м, 2Н); 3,45 (д, 1Н); 5,20 (с, 2Н); 5,38 (д, 1Н); 5,52 (д, 1Н); 5,99 (с, 1Н); 7,37 (с, 1H); 7,70 (т, 1Н), 7,82 (т, 1Н), 8,12 (д, 1Н), 8,19 (д, 1Н).
Пример 26
(5R)-5-Этил-12-(4-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Аминобензонитрил обрабатывают 4-фторфенилмагнийбромидом согласно методике, подобной таковой стадии 4а, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 27
(5R)-12-(2,6-Дифторфенил)-5-этил-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Аминобензонитрил обрабатывают 2,6-дифторфенилмагнийбромидом согласно методике, подобной таковой стадии 4а, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 28
(5R)-12-(3,5-Дифторфенил)-5-этил-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Аминобензонитрил обрабатывают 3,5-дифторфенилмагнийбромидом согласно методике, подобной таковой стадии 4а, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 29
(5R)-5-Этил-5-гидрокси-12-(3,4,5-трифторфенил)-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Аминобензонитрил обрабатывают 3,4,5-трифторфенилмагнийбромидом согласно методике, подобной таковой стадии 4а, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 30
(5R)-5-Этил-5-гидрокси-12-(2,4,6-трифторфенил)-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Аминобензонитрил обрабатывают 2,4,6-трифторфенилмагнийбромидом согласно методике, подобной таковой стадии 4а, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 31
(5R)-5-Этил-5-гидрокси-12-(2,3,5,6-тетрафторфенил)-4,5,13,15-тетрагидро-1H, 3Н-оксепино [3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Аминобензонитрил обрабатывают 2,3,5,6-тетрафторфенилмагнийбромидом согласно методике, подобной таковой стадии 4а, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 32
(5R)-5-Этил-5-гидрокси-12-(2,3,4,5,6-пентафторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Аминобензонитрил обрабатывают 2,3,4,5,6-пентафторфенилмагнийбромидом согласно методике, подобной таковой стадии 4а, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 33
(5R)-5-Этил-9-фтор-12-(4-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4-фторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 4-фторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,83 (к, 2Н); 3,06 (д, 1Н); 3,46 (д, 1Н); 5,06 (дд, 2Н); 5,37 (д, 1Н); 5,49 (д, 1Н); 6,04 (с, 1Н); 7,43 (с, 1H); 7,52 (т, 2Н); 7,60 (т, 1Н); 7,73 (м, 2Н); 7,83 (т, 1H); 7,97 (д, 1H).
Пример 34
(5R)-12-(2,6-Дифторфенил)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4-фторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 2,6-дифторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 35
(5R)-12-(3,5-Дифторфенил)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1H, 3Н-оксепино [3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4-фторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 3,5-дифторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,84 (к, 2Н); 3,06 (д, 1H); 3,47 (д, 1H); 5,15 (дд, 2Н); 5,37 (д, 1H); 5,50 (д, 1H); 6,04 (с, 1H); 7,43 (с, 3Н); 7,55 (т, 1H); 7,63 (т, 1H); 7,87 (т, 1H); 7,98 (д, 1H).
Пример 36
(5R)-5-этил-9-фтор-5-гидрокси-12-(3,4,5-трифторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4-фторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 3,4,5-трифторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 37
(5R)-5-этил-9-фтор-5-гидрокси-12-(2,4,6-трифторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]-индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4-фторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 2,4,6-трифторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 38
(5R)-5-Этил-9-фтор-5-гидрокси-12-(2,3,5,6-тетрафторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4-фторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 2,3,5,6-тетрафторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 39
(5R)-5-Этил-9-фтор-5-гидрокси-12-(2,3,4,5,6-пентафторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4-фторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 2,3,4,5,6-пентафторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 40
(5R)-5-этил-9,10-дифтор-12-(4-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4,5-дифторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 4-фторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 41
(5R)-12-(2,6-Дифторфенил)-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4,5-дифторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 2,6-дифторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 42
(5R)-12-(3,5-Дифторфенил)-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4,5-дифторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 3,5-дифторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 43
(5R)-5-Этил-9,10-дифтор-5-гидрокси-12-(3,4,5-трифторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4,5-дифторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 3,4,5-трифторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 44
(5R)-5-Этил-9,10-дифтор-5-гидрокси-12-(2,4,6-трифторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]-индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4,5-дифторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 2,4,6-трифторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 45
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-(2,3,5,6-тетрафторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино-[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4,5-дифторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 2,3,5,6-тетрафторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 46
(5R)-5-Этил-9,10-дифтор-5-гидрокси-12-(2,3,4,5,6-пентафторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино-[3’,4’:6,7]-индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4,5-дифторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 2,3,4,5,6-пентафторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 47
(5R)-5-Этил-9,11-дифтор-12-(4-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1H, 3Н-оксепино [3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4,6-дифторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 4-фторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 48
(5R)-12-(2,6-Дифторфенил)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4,6-дифторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 2,6-дифторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 49
(5R)-12-(3,5-Дифторфенил)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4,6-дифторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 3,5-дифторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 50
(5R)-5-Этил-9,11-дифтор-5-гидрокси-12-(3,4,5-трифторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4,6-дифторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 3,4,5-трифторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 51
(5R)-5-Этил-9,11-дифтор-5-гидрокси-12-(2,4,6-трифторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]-индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4,6-дифторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 2,4,6-трифторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 52
(5R)-5-Этил-9,11-дифтор-5-гидрокси-12-(2,3,5,6-тетрафторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино-[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4,6-дифторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 2,3,5,6-тетрафторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 53
(5R)-5-Этил-9,11-дифтор-5-гидрокси-12-(2,3,4,5,6-пентафторфенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино-[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4,6-дифторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 2,3,4,5,6-пентафторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
Пример 54
(5R)-5-Этил-9-фтор-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 2 продукт обрабатывают бутиральдегидом согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 55
(5R)-5-Этил-9-фтор-5-гидрокси-12-(3,3,3-трифторпропил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 2 продукт обрабатывают 4,4,4-трифторбутиральдегидом согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 56
(5R)-5-Этил-9-фтор-5-гидрокси-12-изопентил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 2 продукт обрабатывают с помощью 4-метилпентаналя согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 57
(5R)-5-Этил-9-фтор-5-гидрокси-12-пентил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 2 продукт обрабатывают с помощью гексаналя согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 58
(5R)-5-Этил-9-фтор-5-гидрокси-12-фенетил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 2 продукт обрабатывают с помощью 3-фенилпропаналя согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,84 (к, 2Н); 3,02 (м, 2Н); 3,07 (д, 1Н); 3,44 (д, 1Н); 3,51 (м, 2Н); 5,01 (дд, 2Н); 5,38 (д, 1Н); 5,51 (д, 1Н); 6,02 (с, 1Н); 7,22 (м, 5Н); 7,37 (с, 1Н); 7,62 (м, 1Н); 7,89 (дд, 1Н); 8,40 (м, 1Н).
Пример 59
(5R)-12-Децил-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:67]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 2 продукт обрабатывают с помощью ундеканаля согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 60
(5R)-12-(2-Циклогексилэтил)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 2 продукт обрабатывают с помощью 3-циклогексилпропаналя согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 61
(5R)-12-(3,3-Диметилбутил)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 2 продукт обрабатывают с помощью 4,4-диметилпентаналя согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 62
(5R)-5-Этил-9,10-дифтор-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в стадии 13d продукт обрабатывают бутиральдегидом согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 63
(5R)-5-Этил-9,10-дифтор-5-гидрокси-12-(3,3,3-трифторпропил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в стадии 13d продукт обрабатывают 4,4,4-трифторбутиральдегидом согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 64
(5R)-5-Этил-9,10-дифтор-5-гидрокси-12-изопентил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в стадии 13d продукт обрабатывают с помощью 4-метилпентаналя согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 65
(5R)-5-Этил-9,10-дифтор-5-гидрокси-12-пентил-4,5,13,15-тетрагидро-1H, 3Н-оксепино[3’,4’: 6, 7]индолизино [1, 2-b] хинолин-3,15-дион
Полученный в стадии 13d продукт обрабатывают с помощью гексаналя согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 66
(5R)-5-Этил-9,10-дифтор-5-гидрокси-12-фенетил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в стадии 13d продукт обрабатывают с помощью 3-фенилпропаналя согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 67
(5R)-12-Децил-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в стадии 13d продукт обрабатывают с помощью ундеканаля согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 68
(5R)-12-(2-Циклогексилэтил)-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в стадии 13d продукт обрабатывают с помощью 3-циклогексилпропаналя согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 69
(5R)-12-(3,3-Диметилбутил)-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в стадии 13d продукт обрабатывают с помощью 4,4-диметилпентаналя согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 70
(5R)-5-Этил-9,11-дифтор-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 18 продукт обрабатывают бутиральдегидом согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 71
(5R)-5-Этил-9,11-дифтор-5-гидрокси-12-(3,3,3-трифторпропил)-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 18 продукт обрабатывают 4,4,4-трифторбутиральдегидом согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 72
(5R)-5-Этил-9,11-дифтор-5-гидрокси-12-изопентил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 18 продукт обрабатывают с помощью 4-метилпентаналя согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 73
(5R)-5-Этил-9,11-дифтор-5-гидрокси-12-пентил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 18 продукт обрабатывают с помощью гексаналя согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 74
(5R)-5-Этил-9,11-дифтор-5-гидрокси-12-фенетил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 18 продукт обрабатывают с помощью 3-фенилпропаналя согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 75
(5R)-12-Децил-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 18 продукт обрабатывают с помощью ундеканаля согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 76
(5R)-12-(2-Циклогексилэтил)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 18 продукт обрабатывают с помощью 3-циклогексилпропаналя согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 77
(5R)-12-(3,3-Диметилбутил)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 18 продукт обрабатывают с помощью 4,4-диметилпентаналя согласно методике, подобной таковой стадии 13е, получая ожидаемое твердое вещество.
Пример 78
(5R)-12-Хлор-5-этил-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино [3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Используют этил-2,4-дихлор-3-хинолинкарбоксилат (получаемый согласно J. Heterocyclic Chem., 35, 627 (1998)) для осуществления стадий 1g-1h согласно методике вышеприведенного примера 1.
1H-ЯМР (ДМСО-d6, м.д.): 0,87 (т, 3Н); 1,85 (к, 2Н); 3,07 (д, 1Н); 3,46 (д, 1Н); 5,27 (с, 2Н); 5,40 (д, 1Н); 5,52 (д, 1Н); 6,03 (с, 1Н); 7,41 (с, 1Н); 7,86 (т, 1Н); 7,97 (т, 1Н); 8,82 (д, 1Н); 8,30 (д, 1Н).
Пример 79
(5R)-5-Этил-5-гидрокси-12-гидроксиметил-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
(5R)-5-Этил-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино [3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион (получаемый согласно методике, описанной в заявке на патент РСТ WO-97/00876) обрабатывают с помощью метанола согласно методике, подобной таковой стадии 13е, получая ожидаемый продукт.
1H-ЯМР (ДМСО-d6, м.д.): 0,87 (т, 3Н); 1,85 (к, 2Н); 3,08 (д, 1Н); 3,44 (д, 1Н); 5,19 (д, 2Н); 5,38 (м, 3Н); 5,52 (д, 1Н); 5,80 (м, 1Н); 5,98 (с, 3Н); 7,38 (с, 1Н); 8,15 (м, 1Н); 8,23 (м, 1Н).
Пример 80
(5R)-5-Этил-9-фтор-5-гидрокси-12-изо6утил-4,5,13,15-тетрагидро-1H, 3Н-оксепино [3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 2 продукт обрабатывают с помощью 3-метилбутаналя согласно методике, подобной таковой стадии 13е, получая ожидаемый продукт.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 0,98 (д, 6Н); 1,84 (к, 2Н); 2,11 (м, 1Н); 3,05 (д, 1Н); 3,12 (м, 2Н); 3,46 (д, 1Н); 5,25 (дд, 2Н); 5,39 (д, 1Н); 5,52 (д, 1Н); 6,02 (с, 1Н); 7,39 (с, 1Н); 7,65 (м, 1Н); 7,87 (дд, 1Н); 8,37 (м, 1Н).
Пример 81
(5R)-5-Этил-9-фтор-5-гидрокси-12-неопентил-4,5,13,15-тетрагидро-1H, 3Н-оксепино [3’,4’:6,7]индолизино [1,2-b] хинолин-3,15-дион
Полученный в примере 2 продукт обрабатывают с помощью 3,3-диметилбутаналя согласно методике, подобной таковой стадии 13е, получая ожидаемый продукт.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,01 (с, 9Н); 1,84 (к, 2Н); 3,05 (д, 1Н); 3,22 (м, 2Н); 3,46 (д, 1Н); 5,26 (дд, 2Н); 5,38 (д, 1Н); 5,52 (д, 1Н); 6,01 (с, 1Н); 7,39 (с, 1Н); 7,60 (м, 1Н); 7,85 (дд, 1Н); 8,46 (м, 1Н).
Пример 82
(5R)-5-Этил-9-фтор-12-(3-фторфенил)-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4-фторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 3-фторфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,84 (к, 2Н); 3,06 (д, 1Н); 3,46 (д, 1Н); 5,08 (м, 2Н); 5,37 (д, 1Н); 5,49 (д, 1Н); 6,04 (с, 1Н); 7,43 (с, 1H); 7,48 (м, 2Н); 7,61 (м, 2Н); 7,73 (м, 1H); 7,83 (м, 1H); 7,97 (м, 1H).
Пример 83
(5R)-5-Этил-9-фтор-5-гидрокси-12-(4-трифторметилфенил)-4,5,13,15-тетрагидро-1Н, 3Н-оксепино [3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4-фторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 4-трифторметилфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,83 (к, 2Н); 3,06 (д, 1H); 3,46 (д, 1H); 5,06 (дд, 2Н); 5,37 (д, 1H); 5,49 (д, 1H); 6,04 (с, 1H); 7,43 (с, 1H); 7,52 (т, 2Н); 7,60 (т, 1H); 7,73 (м, 2Н); 7,83 (т, 1H); 7,97 (д, 1H).
Пример 84
(5R)-5-Этил-9-фтор-5-гидрокси-12-(4-трифторметоксифенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4-фторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 4-трифторметоксифенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,83 (к, 2Н); 3,06 (д, 1Н); 3,46 (д, 1H); 5,06 (дд, 2Н); 5,37 (д, 1Н); 5,49 (д, 1H); 6,03 (с, 1H); 7,43 (с, 1H); 7,59 (м, 1H); 7,68 (м, 2Н); 7,81 (м, 1H); 7,97 (дд, 1H).
Пример 85
(5R)-12-(4-Диметиламинофенил)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4-фторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 4-диметиламинофенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,84 (к, 2Н); 3,04 (с, 6Н); 3,06 (д, 1H); 3,46 (д, 1H); 5,10 (дд, 2Н); 5,36 (д, 1H); 5,49 (д, 1H); 6,02 (с, 1H); 6,95 (д, 2Н); 7,40 (с, 1H); 7,49 (д, 2Н); 7,57 (т, 1H); 7,90 (д, 1H); 8,01 (т, 1H).
Пример 86
(5R)-12-[4-(трет-Бутил)фенил]-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
2-Амино-4-фторбензойную кислоту обрабатывают согласно методике, подобной таковым стадий 11а-11с, используя 4-трет-бутилфенилмагнийбромид в стадии 11b, и полученный аминокетон обрабатывают согласно методике, подобной таковой стадии 4b. Полученный хинолон используют для осуществления стадий 1f-1h согласно методике вышеприведенного примера 1.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,40 (с, 9Н); 1,85 (к, 2Н); 3,05 (д, 1Н); 3,47 (д, 1Н); 5,08 (дд, 2Н); 5,37 (д, 1Н); 5,49 (д, 1Н); 6,04 (с, 1Н); 7,44 (с, 1Н); 7,60 (м, 3Н); 7,69 (д, 2Н); 7,89 (м, 1Н); 7,96 (м, 1Н).
Пример 87
(5R)-5-Этил-9,11-дифтор-5-гидрокси-12-пропил-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 18 продукт обрабатывают бутиральдегидом согласно методике, подобной таковой стадии 13е, получая ожидаемый продукт.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,04 (т, 3Н); 1,70 (к, 2Н); 1,84 (к, 2Н); 3,05 (д, 1Н); 3,14 (м, 2Н); 3,47 (д, 1Н); 5,25 (дд, 2Н); 5,35 (д, 1Н); 5,52 (д, 1Н); 6,07 (с, 1Н); 7,38 (с, 1Н); 7,67 (м, 1Н); 7,78 (м, 1Н).
Пример 88
(5R)-12-(2-Этоксиэтил)-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
Полученный в примере 18 продукт обрабатывают с помощью 3-этоксипропаналя согласно методике, подобной таковой стадии 13е, получая ожидаемый продукт.
1H-ЯМР (ДМСО-d6, м.д.): 0,86 (т, 3Н); 1,05 (т, 3Н); 1,84 (к, 2Н); 3,07 (д, 1Н); 3,43 (м, 5Н); 3,77 (т, 2Н); 5,26 (дд, 2Н); 5,39 (д, 1Н); 5,52 (д, 1Н); 6,03 (с, 1Н); 7,39 (с, 1Н); 7,67 (м, 1Н); 7,79 (дд, 1Н).
Пример 89
(5R)-5-Этил-9,10,11-трифтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-дион
В стадиях 13а-13с используют 3,4,5-трифторанилин и таким образом полученный хинолилметанол обрабатывают с помощью (+)-EHHOPD согласно методике стадии 1h, получая ожидаемый продукт.
1H-ЯМР (ДМСО-d6, м.д.): 0,87 (т, 3Н); 1,83 (к, 2Н); 3,07 (д, 1Н); 3,45 (д, 1Н); 5,26 (с, 2Н); 5,39 (д, 1Н); 5,51 (д, 1Н); 6,03 (с, 1Н); 7,40 (с, 1Н); 8,09 (м, 1Н); 8,86 (с, 1Н).
Пример 90
(5R)-5-Этил-9-фтор-5-гидрокси-3,15-диоксо-4,5,13,15-тетрагидро-1H,3Н-оксепино[3’,4’:6,7]-индолизино[1,2-b]хинолин-10-илтрифторметансульфонат
Раствор 28 мг (5R)-5-этил-9-фтор-5,10-дигидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3’,4’:6,7]индолизино[1,2-b]хинолин-3,15-диона (получаемого согласно Примеру получения 20, описанному в заявке на патент РСТ WO-98/28304) в 5 мл безводного диметилформамида при температуре 0°С обрабатывают с помощью 1,1 эквивалента гидрида натрия, затем с помощью 1,1 эквивалента N-фенилтрифторсульфонимида. Реакционную среду выдерживают при перемешивании в течение двух часов при комнатной температуре, после чего выливают в воду со льдом и экстрагируют этилацетатом. Органическую фазу сушат и выпаривают, затем остаток обрабатывают диэтиловым эфиром и отфильтровывают, получая ожидаемый продукт.
1H-ЯМР (ДМСО-d6, м.д.): 0,87 (т, 3Н); 1,86 (к, 2Н); 3,07 (д, 1Н); 3,46 (д, 1Н); 5,29 (с, 1Н); 5,40 (д, 1Н); 5,52 (д, 1Н); 6,04 (с, 1Н); 7,43 (с, 1H); 8,31 (д, 1Н); 8,66 (д, 1Н); 8,82 (с, 1H).
Фармакологическое исследование продуктов согласно изобретению
Методика
Клетки НТ29 аденокарциномы человеческой ободочной кишки культивировали в монослое при температуре 37°С в увлажненной атмосфере, содержащей 95% воздуха и 5% СO2, в модифицированной эссенциальной среде Эрла с концентрацией 4,5 г/л (Gibco, Paisley, Royaume-Uni), дополненной с помощью 10% инактивированной плодной телячьей сыворотки, 2 мМ глутамина и 50 мкг/мл гентамицина (Gibco, Paisley, Royaume-Uni).
Осуществляли посев примерно 2000 клеток вместе с вышеуказанной культуральной средой в лунки микропланшета (96 лунок, плоское дно) и инкубировали в течение 24 часов. К культурам на планшете добавляли растворы в N,N-диметилацетамиде (ДМА) каждого из соединений, полученных в примерах согласно изобретению, разведенных в культуральной среде таким образом, чтобы конечная концентрация ДМА составляла 0,1% (объем/объем), для получения серий конечных концентраций от 1×10-13 до 1×10-5 М, и клетки инкубировали в течение 72 часов.
В каждую лунку затем добавляли маркировочный реагент WST1 (Boehringer, Mannheim, Германия) до конечной концентрации 9% и клетки инкубировали в течение двух часов при температуре 37°С. Эта стадия в присутствии митохондриальной дегидрогеназы живых клеток позволяет превратить соль тетразолия WST1 оранжевого цвета в формазан пурпурного цвета. Полученные в результате окрашенные растворы количественно оценивали путем двухлучевого детектирования (450 и 690 нм) с помощью многокюветного сканирующего спектрофотометра.
Результаты
Приведенные в таблице результаты выражены в виде ингибирующей на 50% концентрации (ИК50 в нмоль) с доверительным интервалом. Оценивают ингибирующие активности в отношении пролиферации клеток НТ29 аденокарциномы человеческой ободочной кишки, получаемые с помощью соединений, полученных в примерах согласно изобретению, причем эти активности неожиданно превосходят активность ссылочного соединения, описанного в заявке на патент РСТ WO-97/000876 (и соответствующего соединению IA, в котором R1 - этил; R2=R3=R4=R5 - Н; R6 - Н).
Токсичность: соединения согласно изобретению относятся к соединениям средней токсичности в отличие от камптотецинов и его аналогов, относящихся к соединениям с более высокой токсичностью.
Примеры композиций в жидкой и твердой форме.
Жидкая композиция:
Соединение примера 84 100 мг
ДМА (диметилацетат) 5 г
Полисорбат 80 3,5 г
Физическая сыворотка до 200 г
Твердая композиция:
Соединение примера 17 10 мг
Лактоза (порошок) 80 мг
Микрокристаллическая целлюлоза 20 мг
Безводный коллоидный кремнезем 3 мг
Стеарат магния 1 мг
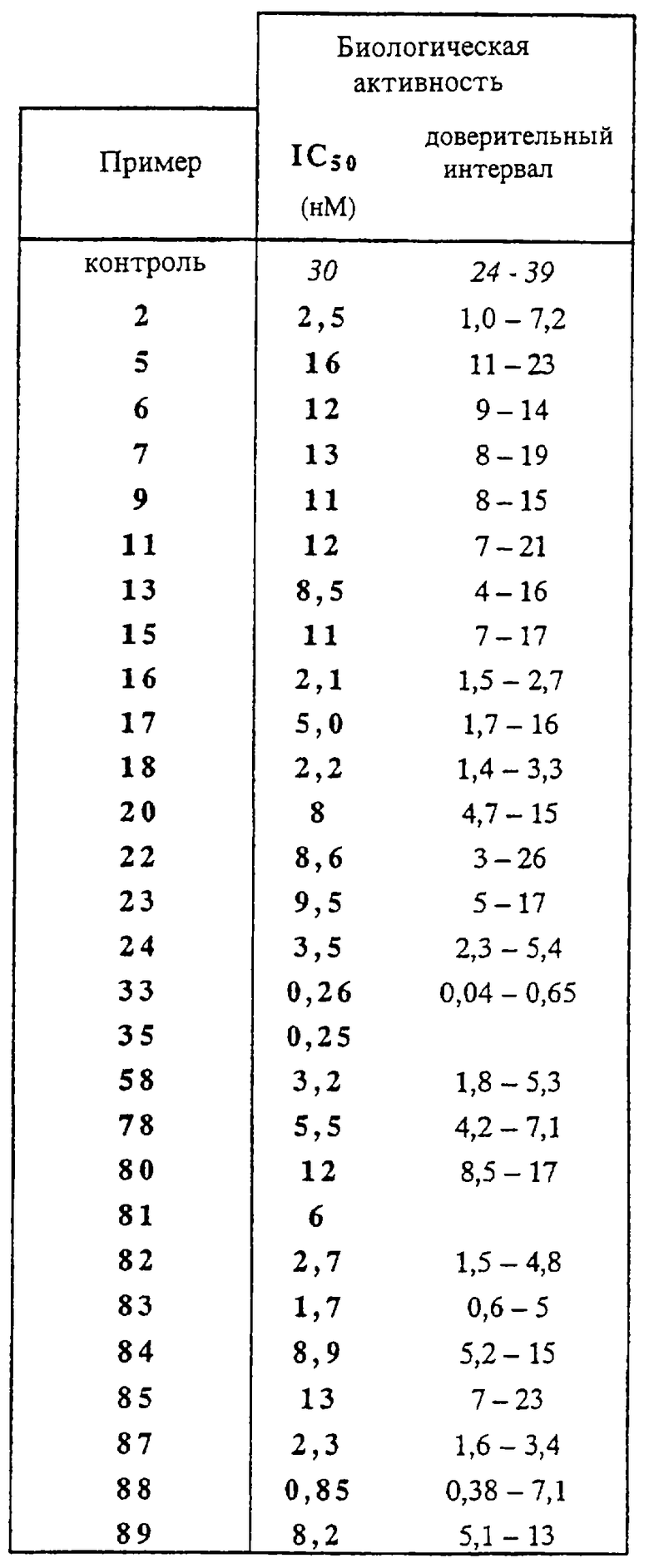
| название | год | авторы | номер документа |
|---|---|---|---|
| СОЕДИНЕНИЯ КАМПТОТЕЦИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ И ТЕРАПЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 1996 |
|
RU2164515C2 |
| НОВЫЕ АНАЛОГИ КАМПТОТЕЦИНА, ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ СРЕДСТВ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 1997 |
|
RU2194051C2 |
| АНАЛОГИ КАМПТОТЕЦИНА, СПОСОБЫ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1997 |
|
RU2190613C2 |
| ОПТИЧЕСКИ ЧИСТЫЕ АНАЛОГИ КАМПТОТЕЦИНА, ОПТИЧЕСКИ ЧИСТЫЙ ПРОМЕЖУТОЧНЫЙ ПРОДУКТ СИНТЕЗА И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1998 |
|
RU2233283C2 |
| СПОСОБ ИДЕНТИФИКАЦИИ ПРОТИВООПУХОЛЕВЫХ ЦЕЛЕВЫХ ФЕРМЕНТОВ | 2002 |
|
RU2319482C2 |
| ЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ИЗОТИАЗОЛ-ПИРИДОН АЦЕТИДИНИЛА И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ | 1991 |
|
RU2041226C1 |
| ГЕКСАЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ | 1992 |
|
RU2071476C1 |
| ПЕПТИДНЫЕ ВЕКТОРЫ | 2004 |
|
RU2361876C2 |
| ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ ДЛЯ ПОЛУЧЕНИЯ ТРАНС-5-ХЛОР-2-МЕТИЛ-2,3,3f,12b-ТЕТРАГИДРО-1Н-ДИБЕНЗ[2,3:6,7]-ОКСЕПИНО[4,5-c]ПИРРОЛА | 2006 |
|
RU2397164C2 |
| ТИЕНОПИРИМИДИНДИОНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ) И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2002 |
|
RU2294937C9 |
Изобретение относится к органической химии, в частности к новым соединениям общей формулы IA:
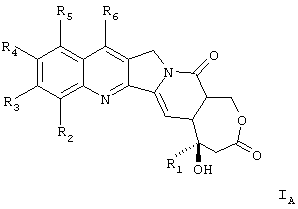
в которой R1 означает низший алкильный радикал; R2, R3, R4 и R5 означают, независимо, водород, галоидный радикал или -OSO2R10; R6 означает атом водорода, линейный или разветвленный алкильный радикал с 1-12 атомами углерода, возможно замещенный одним или несколькими одинаковыми или разными галоидными радикалами, низший гидроксиалкил, (низший алкокси)-(низший алкил), циклоалкил, циклоалкил(низший алкил), атом галогена, группу -(СН2)mSiR7R8R9, замещенный или незамещенный арил или замещенный или незамещенный арил(низший алкил), причем один или несколько заместителей, одинаковых или разных, арильных групп выбирают из радикалов: низший алкил, атом галогена, аминогруппа, (низший алкил)аминогруппа, ди(низший алкил)аминогруппа, CF3 или OCF3; R7, R8 и R9, независимо, означают низший алкильный радикал; R10 означает низший алкильный радикал, возможно замещенный одним или несколькими одинаковыми или разными галоидными радикалами; m означает целое число от 0 до 6. Эти соединения являются ингибиторами топоизомераз и особенно представляют интерес в качестве лекарственных средств, обладающих противоопухолевой активностью. 1 табл.
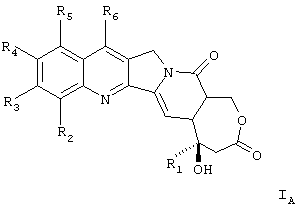
в которой R1 означает низший алкильный радикал;
R2, R3, R4 и R5, независимо, означают атом водорода, галоидный радикал или радикал -OSO2R10;
R6 означает атом водорода; линейный или разветвленный алкильный радикал с 1-12 атомами углерода, возможно замещенный одним или несколькими, одинаковыми или разными галоидными радикалами; низший гидроксиалкил, (низший алкокси)-(низший алкил), циклоалкил, циклоалкил(низший алкил), атом галогена, группу -(СН2)mSiR7R8R9, замещенный или незамещенный арил, или замещенный или незамещенный арил(низший алкил), причем один или несколько заместителей, одинаковых или разных, арильных групп выбирают из радикалов: низший алкил, атом галогена, аминогруппа, (низший алкил)аминогруппа, ди(низший алкил)аминогруппа, СF3 или ОСF3;
R7, R8 и R9, независимо, означают низший алкильный радикал;
R10 означает низший алкильный радикал, возможно замещенный одним или несколькими, одинаковыми или разными галоидными радикалами,
m означает целое число от 0 до 6;
при условии, что, когда термин "низший алкил" относится к алкильному радикалу, то он включает самое большее 6 атомов углерода, и когда R2 означает Н, тогда
R6 означает линейный или разветвленный алкильный радикал с 7-12 атомами углерода, -(CH2)mSiR7R8R9 или арил, замещенный одним или несколькими, одинаковыми или разными заместителями, выбираемыми из ди(низший алкил)аминогруппы или ОСF3, и/или по меньшей мере один из радикалов R3, R4 или R5 означает - OSO2R10;
или аддитивные соли этих соединений.
(5R)-5-этил-8-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3',4':6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-(2-триметилсилилэтил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3',4':6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-5-гидрокси-12-(2-триметилсилилэтил)-4,5,13,15-тетрагидро-1H,3Н-оксепино[3',4':6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-децил-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3',4':6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-децил-5-этил-9,10-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3',4':6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-децил-5-этил-9,11-дифтор-5-гидрокси-4,5,13,15-тетрагидро-1H,3Н-оксепино[3',4':6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-12-(4-трифторметоксифенил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3',4':6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-12-(4-диметиламинофенил)-5-этил-9-фтор-5-гидрокси-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3',4':6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-9-фтор-5-гидрокси-3,15-диоксо-4,5,13,15-тетрагидро-1H,3Н-оксепино[3',4':6,7]индолизино[1,2-b]хинолин-10-илтрифторметансульфонат.
(5R)-5-этил-9,10-дифтор-5-гидрокси-12-(2-триметилсилилэтил)-4,5,13,15-тетрагидро-1Н,3Н-оксепино[3',4':6,7]индолизино[1,2-b]хинолин-3,15-дион;
(5R)-5-этил-5-гидрокси-12-(2-триметилсилилэтил)-4,5,13,15-тетрагидро-1H,3Н-оксепино[3',4':6,7]индолизино[1,2-b]хинолин-3,15-дион.
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| Дорожная спиртовая кухня | 1918 |
|
SU98A1 |
| ГЕКСАЦИКЛИЧЕСКОЕ СОЕДИНЕНИЕ | 1992 |
|
RU2071476C1 |
Авторы
Даты
2004-06-20—Публикация
2000-02-24—Подача