Изобретение относится к медицине, а именно к пульмонологии, и может быть использовано для ускоренной диагностики степени тяжести хронического обструктивного бронхита.
В настоящее время хронические заболевания органов дыхания, к которым относится и хронический бронхит (ХБ), занимают 3-4 место среди причин смерти населения, уступая только сердечно-сосудистым и онкологическим заболеваниям. По данным ВОЗ ежедневно в мире от них умирает около 2,2 млн человек [1, 6]. Во всех промышленно развитых странах ХБ представляет важнейшую медицинскую и социальную проблему [4]. По данным ГНЦ пульмонологии МЗ РФ распространенность ХБ среди взрослого населения России составляет 16%, а общее число таких больных достигает 3,5 миллиона, что превышает суммарное число больных туберкулезом и злокачественными опухолями всех локализаций. Экономический ущерб, наносимый обструктивной формой ХБ, определяется тем, что трудопотери, связанные с его обострениями, составляют около 2/3 всех трудопотерь от хронических неспецифических заболеваний легких. В перечне наиболее частых диагнозов в терапевтических стационарах ХОБ занимает шестое место и сравнительно рано приводит к стойкой утрате трудоспособности. Инвалидизация наступает в среднем через 10 лет после установки диагноза, что обуславливает необходимость своевременной диагностики степени тяжести данного заболевания для адекватного лечения [1, 5]. Продолжительность жизни инвалидов с хроническими обструктивными болезнями легких (ХОБЛ) по данным А.Н.Кокосова не превышает в среднем 6 лет, что в 3,5 раза меньше, чем при бронхиальной астме (БА).
Таким образом, распространенность, значительный экономический ущерб, обусловленный временной утратой трудоспособности, ранней инвалидизацией и преждевременной смертностью больных ХОБЛ, обуславливают актуальность проблемы и необходимость разработки своевременной диагностики этого заболевания с целью адекватного лечения в зависимости от степени тяжести, профилактики его прогрессирования и полноценной реабилитации заболевших.
В настоящее время рекомендовано для постановки диагноза руководствоваться клиническими критериями, предложенными в документе (NHLBI Global Initiative for chronic Obstructive Lung Disease (GOLD) Work shop Summary, Am. j. Respir. Crit. Care Med., 2001, v.163, pp.1256-1276) на конгрессе Европейского респираторного общества в 2000 г. с обязательным проведением диагностического комплекса, включающего спирографию, рентгенографию органов грудной клетки и лабораторные исследования. Однако данный диагностический комплекс имеет ряд недостатков: во-первых, на функцию внешнего дыхания могут влиять и внелегочные нарушения, такие как поражение костно-мышечного каркаса грудной клетки (кифосколиоз, деформация позвоночника и др.), нарушение регуляции дыхания (опухоли, травмы центральной нервной системы), увеличение объема брюшной полости, болевой синдром, что приводит к ограничению подвижности диафрагмы. Эти причины изменяют легочные объемы и показатели вентиляции и затрудняют диагностику степени тяжести заболевания. Кроме того, индивидуальные личностно-психологические особенности порой не позволяют вообще провести спирографию. Во-вторых, лабораторно-инструментальные исследования, включающие клинический минимум, анализ мокроты, рентгенографию органов грудной полости, занимают длительное время обследования, полученные результаты зависят от сопутствующих заболеваний у обследуемого и грамотности медперсонала. Проводя дифференциальную диагностику ХОБ и БА, к этим методам необходимо добавить суточное мониторирование пиковой скорости выдоха в течение не менее 7 дней, что еще больше удлиняет время обследования и отодвигает своевременное назначение необходимого медикаментозного лечения в зависимости от степени тяжести ХОБ.
Задача изобретения - разработка достоверного ускоренного метода диагностики тяжести заболевания ХОБ.
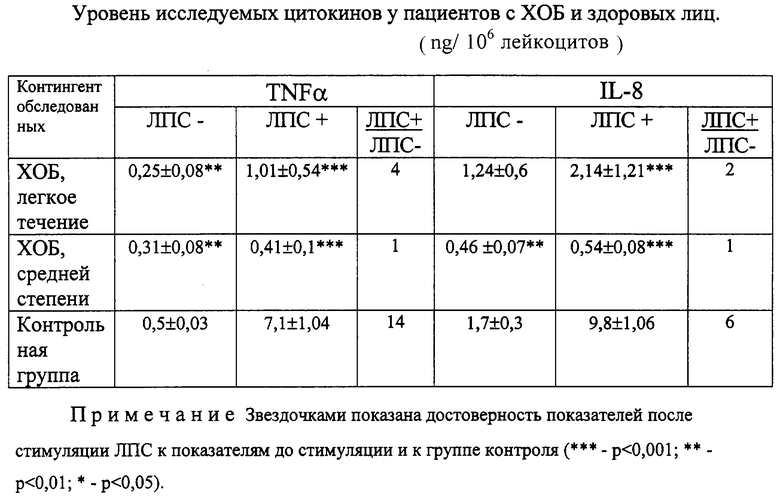
Поставленная задача достигается определением реактивной способности иммунокомпетентных клеток (ИКК) вырабатывать туморнекротизирующий фактор (TNF-α) и интерлейкин-8 (IL-8), и при спонтанном уровне интерлейкина 8 (IL-8) 1,24±0,6 нг/106 лейкоцитов, фактора некроза опухолей α (TNFα) 0,25±0,08 нг/106 лейкоцитов и индуцированном липополисахаридом уровне IL-8=2,14±1,21 нг/106 лейкоцитов и TNFα=1,0±0,54 нг/106 лейкоцитов диагностируют легкую степень течения хронического обструктивного бронхита, а при спонтанном уровне IL-8=0,46±0,07 нг/106 лейкоцитов, TNFα=0,31±0,086 нг/106 лейкоцитов и индуцированном липиполисахаридом уровне IL-8=0,54±0,08 нг/106 лейкоцитов, TNFα=0,41±0,1 нг/106 лейкоцитов диагностируют среднюю степень хронического обструктивного бронхита. Под наблюдением находилось 18 больных ХОБ, которые проходили обследование в клинике института медицинской климатологии и восстановительного лечения (ИМКВЛ). Все обследованные ХОБ имели среднюю длительность заболевания 11,2±5,2 года, средний возраст 58±4,2 года. Пациентов с легкой и средней степенью заболевания было поровну. Среди сопутствующей патологии 35% больных ХОБ имели заболевания сердечно-сосудистой системы, 24% - заболевания гепатобиллиарной системы и ЖКТ и 13% (2 человека) - мочеполовой системы. Аллергических заболеваний выявлено не было. Группу контроля составили пациенты (15 человек), не имеющие хронической бронхолегочной патологии и аллергических заболеваний, некурящие, с нормальной функцией внешнего дыхания, подверженные аналогичным клиническим и лабораторным методам обследования.
Им проведено обследование по предлагаемой методике. Оценивали реактивную способность иммунокомпетентных клеток по уровню цитокинов TNFα и IL-8, определяемому с помощью специфических реактивов фирмы “Genzyme diagnostics” методом иммуноферментного анализа согласно прилагаемой инструкции. Результаты оценивали с помощью иммуноферментного анализатора EL-800 при длине волны 450 нм.
В результате анализа лабораторных показателей у обследованных с ХОБ выявлен сниженный спонтанный и индуцированный ЛПС синтез TNF-α и IL-8 по сравнению с контрольной группой (таблица). Исследования по уровню цитокинов у практически здоровых лиц проводились ранее в ИМКВЛ, получено положительное решение на выдачу патента (по заявлению №2000115968/14(016607)). Продукция TNF-α и IL-8 отличалась при спонтанном и индуцированном синтезе у больных с разной степенью тяжести ХОБ. У пациентов с легким течением заболевания базальный уровень IL-8 составил 1,24±0,6 ng/106 лейкоцитов, при стимуляции Е.соli его уровень возрастал в 2 раза. Спонтанная секреция TNF-α составляла 0,25±0,08 ng/106 лейкоцитов, после индукции ЛПС его синтез повысился в 4 раза. У пациентов со средним течением хронического воспалительного процесса обращает на себя внимание резкое истощение показателей по сравнению с аналогичными уровнями у пациентов с легким течением ХОБ: базальный синтез TNF-α и IL-8 составил 0,31±0,086 и 0,46±0,07 ng/106 лейкоцитов соответственно. При стимуляции ЛПС уровни TNF-α и IL-8 не менялись. Имеется достоверное количественное различие показателей по сравнению с контрольной группой, где спонтанный синтез и стимулированный увеличивается в 6 и 14 раз соответственно (р<0,001).
Полученные результаты играют важную роль при дифференциальной диагностике ХОБ и бронхиальной астмы (БА). По литературным данным синтез цитокинов клетками крови больных с БА без дополнительной стимуляции оказывался на уровне ЛПС-индуцированного синтеза клетками крови здоровых доноров [3].
Диагностика степени тяжести ХОБ была проведена в течение 13 часов. Это в 12 раз ускорило дифференциальную диагностику и определение тяжести течения основного заболевания, что способствовало быстрому своевременному назначению необходимых лекарственных препаратов.
Полученные результаты были дополнительно проверены общепринятыми критериями постановки диагноза хронического обструктивного бронхита. Диагноз подтверждали на основании функциональных и лабораторных методов обследования индивидуально для каждого больного. Сопоставление результатов полностью подтвердило достоверность предложенного метода диагностики степени тяжести ХОБ.
Пример. Больная Ш, 67 лет, поступила в клинику института медицинской климатологии и восстановительного лечения СО РАМН с жалобами на продуктивный кашель с небольшим количеством слизистой мокроты, одышку смешанного характера при незначительной физической нагрузке, дистанционные хрипы в ночное время. Из анамнеза: выше указанные жалобы беспокоят в течение 15 лет, необходимого лечения не получает, периодически принимает сосательные таблетки, смягчающие кашель. Последние 3 года вышеуказанные жалобы беспокоят 3-4 раза в год с длительностью обострения более месяца, отмечает подверженность острым респираторным вирусным заболеваниям. При объективном осмотре: состояние удовлетворительное, кожные покровы бледно-розовые. Перкуторно над легкими коробочный звук, аускультативно ослабление дыхания и сухие низкотональные хрипы при форсированном выдохе. ЧД 19 в 1 мин, ЧСС 72 в 1 мин. АД 130/70 мм рт.ст. По остальным органам и системам без патологических особенностей. Пациентке проведено обследование по предлагаемой методике. Получены следующие результаты: спонтанный уровень IL-8 0,483 ng/106 лейкоцитов, TNFα 0,2196 ng/106 лейкоцитов и индуцированный липополисахаридом уровень IL-8 0,515 ng/106 лейкоцитов, TNFα 0,309 ng/106 лейкоцитов. Согласно результатам обследования, которое заняло 13 часов, пациентке был выставлен диагноз: Хронический катаральный обструктивный бронхит, средней тяжести. Назначены М-холинилитики и пролонгированные метилксантины. Через 3 недели приема препаратов состояние пациентки значительно улучшилось, увеличилась толерантность к физической нагрузке, купированы дистанционные хрипы, уменьшилась гиперреактивность верхних дыхательных путей.
Таким образом, оценка реактивной способности иммунокомпетентных клеток с целью дифференциальной диагностики хронического обструктивного бронхита и бронхиальной астмы и определения степени тяжести хронического обструктивного бронхита является актуальным, достоверным, информативным и ускоренным диагностическим методом, показанным всем больным, не имеющим противопоказаний. Помогает диагностировать заболевание, оценивать не только тяжесть но и резервные возможности клеток, что необходимо для более дифференцированного, своевременного и качественного лечения.
Литература
1. Гусейнов Х.Ю. Распространенность хронического бронхита (по материалам эпидемиологических исследований) // Проблемы туберкулеза. - 2000. - №5. - С.54-56.
2. 3емсков А.М., Земсков В.М., Золоедов В.И. Иммунокоррекция при заболеваниях легких // Иммунология. - 1998. - №4. - С.40-45.
3. Исаченко Е.Г., Виткина Т.И., Геронина С.А., Бердышев Е.В.Спонтанный и липополисахаридиндуцированный синтез цитокинов клетками крови человека в норме и при аллергопатологиях // Иммунология. – 1999. - №5. - С.37-39.
4. Кокосов А.Н. Болезни органов дыхания. Клиника и лечение. Избранные лекции. - СПб.: Издательство "Лань", 1999. - 256 с.
5. Кокосов А.Н. Хронический бронхит и обструктивная болезнь легких: аналитический очерк // Терапевт. арх. - 2000. - №3. - С.75-77.
6. Чучалин А.Г. Хронический обструктивные болезни легких. - М.:БИНОМ, 1999. - 512 с.
Изобретение относится к медицине, а именно к пульмонологии, и может быть использовано для ускоренной диагностики степени тяжести хронического обструктивного бронхита. Предложенный метод включает иммунологические исследования с определением показателей реактивной способности иммунокомпетентных клеток, спонтанного и индуцированного липополисахаридом интерлейкина-8 и фактора некроза опухолей-α для диагностики легкой или средней степени тяжести хронического обструктивного бронхита. Преимущество изобретения заключается в ускорении способа и повышении его информативности. 1 табл.
Способ диагностики степени тяжести хронического обструктивного бронхита, включающий лабораторные исследования, отличающийся тем, что проводят иммунологические исследования с определением реактивной способности иммунокомпетентных клеток и, при спонтанном уровне интерлейкина 8 (IL-8), значения которого находятся в интервале 0,64-1,84 нг/106 лейкоцитов, фактора некроза опухолей α (TNFα) - в интервале 0,17-0,33 нг/106 лейкоцитов и индуцированном липополисахаридом уровне IL-8 в интервале 0,93-3,35 нг/106 лейкоцитов и TNFα в интервале 0,47-1,55 нг/106 лейкоцитов, диагностируют легкую степень, а при спонтанном уровне IL-8, значения которого находятся в диапазоне 0,39-0,53 нг/106 лейкоцитов, TNFα - в интервале 0,23-0,39 нг/106 лейкоцитов и индуцированном липиполисахаридом уровне IL-8 в интервале 0,46-0,62 нг/106 лейкоцитов, TNFα в интервале 0,31-0,51 нг/106 лейкоцитов, диагностируют среднюю степень течения хронического обструктивного бронхита.
| PAUWELS R.А | |||
| et al | |||
| Global strategy for tne diagnosis, anagement and prevention of chronic obstructive pulmonary disease: NHLBI Global Initiative for chronic obstructive Lung disease (GOLD) Workshop Summary, Am | |||
| J | |||
| Respir | |||
| Crit | |||
| Care Med., 2001, v.63, р.1256-1276 | |||
| СПОСОБ ДИФФЕРЕНЦИАЛЬНОЙ ДИАГНОСТИКИ ХРОНИЧЕСКОЙ ОБСТРУКТИВНОЙ БОЛЕЗНИ ЛЕГКИХ | 1998 |
|
RU2143695C1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ НАРУШЕНИЙ ИММУНИТЕТА ПРИ ХРОНИЧЕСКОМ БРОНХИТЕ | 1988 |
|
RU2050002C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ТЕЧЕНИЯ ЭМПИЕМЫ ПЛЕВРЫ И ПИОПНЕВМОТОРАКСА | 1992 |
|
RU2043636C1 |
Авторы
Даты
2004-06-27—Публикация
2002-08-08—Подача