Лечение злокачественных опухолей, воспалительных процессов или аутоиммунных заболеваний наряду с недостаточной эффективностью терапевтических средств связано с тяжелыми побочными явлениями. Этот недостаток можно объяснить, главным образом, слишком незначительной переносимостью in vivo используемых активных веществ.
Предметом изобретения является улучшение переносимости активнодействующих веществ, применяемых при лечении, и, в случае необходимости, повышение эффективности путем модификации препарата.
Поэтому изобретение относится к препарату, содержащему
1) соединение формулы (I),
гликозил-Y[-С(=Y)-X-]p-W(R)n-X-C(=Y) - активнодействующее вещество (I),
где гликозил является энзиматически отщепляемым поли-, олиго- или моносахаридом,
W является ароматическим или гетероароматическим углеводородом или алифатом с сопряженными двойными связями или производным аминокислоты, циклизирующимся после отщепления остатка гликозила,
при этом заместитель R является атомом водорода, метилом, метокси, карбокси, CN, метилкарбонилом, гидрокси, нитро, фтором, хлором, бромом, сульфонилом, сульфонамидом или сульфон-(C1-C4)-алкиламидом,
р равно 0 или 1,
n является целым числом,
Х является атомом кислорода, NH, метиленокси, метиленамино или метилен-(C1-C4)-алкиламино и
Y является атомом кислорода или NH и
активнодействующее вещество обозначает связанное через группу гидрокси,- амино- или имино-соединение с биологической активностью,
и/или физиологически переносимую соль соединения формулы (I),
2) сахар и/или сахарный спирт и
3) фармацевтически приемлемый носитель. Под активнодействующим веществом понимаются соединения, как, например, антрациклин, предпочтительно доксорубицин, 4'-эпидоксорубицин, 4-или 4'-дезоксидоксорубицин или соединение, предпочтительно, из группы, включающей этопозиды, N-бис(2-хлорэтил)-4-гидроксианилин, 4-гидроксициклофосфамид, виндезин, винбластин, винкристин, терфенадин, тербуталин, фенотерол, салбутамол, мускарин, оксифенбутазон, салициловую кислоту, р-аминосалициловую кислоту, 5-фтороурацил, метотрексат, диклофенак, флуфенаминокислоту, 4-метиламинофеназон, теофиллин, нифедипин, митомицин С, митоксантрон, камптотецин и производные камптотецина, m-AMSA, таксол, другие таксаны, нокодаксол, колхицин, фексофенадин, циклофосфамид, рахелмицин, цисплатин, мелфалан, блеомицин, азот-горчичный газ, фосфорамид-горчичный газ, веррукарин А, неокарциностатин, калихеамицин, динемицин, эсперамицин А, кверцетин, генистеин, эрбстатин, тирфостин, производное рогитукина, ретиноловую кислоту, масляную кислоту, сложный форболэфир, диметилсульфоксид, аклациномицин, прогестерон, бузерелин, тамоксифен, мифепристон, онапристон, N-(4-аминобутил)-5-хлоро-2-нафталенсульфонамид, пиридинилоксазол-2-он, квинолил-, изоквинолилоксазол-2-он, стауроспорин, этаноламин, ферапамил, форсколин, 1,9-дидеоксифорсколин, квинин, квинидин, резерпин, 18-O-(3,5-диметокси-4-гидроксибензоил)-резерпат, лонидамин, бутионинсульфоксимин, диэтилдитиокарбамат, циклоспорин А, рапамицин, азатиоприн, хлорамбуцил, производное-2 амида гидроксикротоновой кислоты, лефлуномид, 15-деоксисперквалин, FK 506, ибупрофен, аспирин, сульфасалазин, пеницилламин, хлороквин, дексаметазон, преднизолон, мефонамидную кислоту, парацетамол, 4-аминофеназон, мускозин, орципреналин, изопренанилин, амилорид, р-нитрофенилгуанидинбензоат или их производные, дополнительно замещенные одной или несколькими группами гидрокси, амино или имино.
n является целым числом от 1 до 8, предпочтительно, от 1 до 6.
Под понятием "сахар" понимаются альдозы с 3-7 атомами углерода, которые могут принадлежать ряду D или R; сюда относятся также аминосахар или уроновые кислоты. В качестве примеров можно назвать глюкозу, маннозу, фруктозу, галактозу, рибозу, эритрозу, глицеринальдегид, седогептулозу, глюкозамин, галактозамин, глюкуроновую кислоту, галактуроновую кислоту, глюконовую кислоту, галактоновую кислоту или манноновую кислоту.
Сахарные спирты возникают, например, путем восстановления вышеуказанных сахаров; сюда относится глюцитол, маннитол (маннит), сорбитол, глицерол или инозитол.
Пригодными фармацевтически переносимыми солями соединений формулы (I) являются, например, щелочные, щелочноземельные и аммиачные соли, включая соли органических аммиачных оснований и соли протонированных остатков аминокислоты. Предпочтительными являются щелочные соли, как, например, соли калия или натрия.
Препараты согласно изобретению содержат, в частности, дополнительно двухвалентные ионы. Под понятием "двухвалентные ионы" понимаются, например, двухвалентные ионы металлов, например, Са, Мg, Fe, Сu или Ni.
Предпочтительным является использование соединений формулы (I), где
W является остатком фенила или многократно замещенным остатком фенила, и при этом заместитель
R является атомом водорода, метилом, метокси, карбокси, метилоксикарбонилом, CN, гидрокси, нитро, фтором, хлором, бромом, сульфонилом, сульфонамидом или сульфон-(C1-C4)-алкиламидом и
р равно 0 или 1,
n равно 1-4,
Х является атомом кислорода, NH, метиленокси, метиленамино или метилен-(C1-C4)-алкиламино и
Y является атомом кислорода или NH и
активное вещество обозначает указанное выше соединение.
Особенно предпочтительным является использование соединений формулы (I), где
гликозил является поли-, олиго- или моносахаридом, в частности, α - или β -O-гликозидно связанным остатком D-глюкуронила, D-глюкопиранозила, D-галактопиранозила, N-ацетил-D-глюкозаминила, остатком N-ацетил-D-галактозаминила, D-маннопиранозила или L-фукопиранозила,
W является остатком фенила или монозамещенным остатком фенила, при этом заместитель
R является метокси, метилоксикарбонилом, CN, гидрокси, нитро, фтором, хлором, бромом, сульфонилом или сульфонамидом и остальные являются атомом водорода,
Х является О, NH, метиленокси, метиленамино или метиленметиламино и
Y является О или NH и
активнодействующее вещество обозначает указанное соединение, описанное выше.
Используются, предпочтительно, соединения, которые характеризуются тем, что остаток гликозила может быть отщеплен путем энзиматического гидролиза, что разделитель может быть самопроизвольно отщеплен химическим гидролизом, что активнодействующее вещество является фармацевтическим средством или его производным, полученным путем введения дополнительных групп гидрокси, амино или имино, что они являются более гидрофильными, чем активнодействующее вещество, что они in vivo ведут к меньшим токсичным реакциям, чем активнодействующее вещество как таковое, что активное вещество является фармакологически активным веществом, что активнодействующее вещество дополнительно замещено одной или несколькими группами гидрокси, амино или имино и замедляет рост опухолей, что активное вещество является стандартным цитостатическим средством, что активнодействующее вещество является антиметаболитом, что активнодействующее вещество является 5-фтороцитидином, 5-фтороуридином, цитозинарабинозидом или метотрексатом, что активнодействующее вещество является вводящимся в ДНК веществом, что активнодействующее вещество является доксорубицином, дауномицином, идарубицином, или митоксантроном, что активнодействующее вещество тормозит топоизомеразу I+II, что активнодействующее вещество является камптотецином и производными камптотецина, этопозидом или M-AMSA, что активнодействующее вещество является ингибитором тубулина, что активнодействующее вещество является винкристином, винбластином, таксолом и таксанами, нокодаксолом, колхицином или эторозидом, что активнодействующее вещество является алкилантом, что активнодействующее вещество является циклофосфамидом, митомицином С, рахелмицином, цисплатином, фосфорамид-горчичным газом, мелфаланом, блеомицином, азот-горчичным газом или N-бис(2-хлорэтил-4-гидроксианилином), что активнодействующее вещество является неокарциностатином, калихеамицином, эпотилоном А-С, динемицином или эсперамицином А, что активнодействующее вещество является соединением, инактивирующим рибосомы, что активнодействующее вещество является веррукарином А, что активнодействующее вещество является ингибитором тирозинфосфокиназы, что активнодействующее вещество является кверцетином, генистеином, эрбстатином, тирфостином или производным рогитукина, что активнодействующее вещество является дифференцирующим индуктором, что активнодействующее вещество является ретиноловой кислотой, масляной кислотой, сложным форболэфиром, DMSO или аклациномицином, что активнодействующее вещество является гормоном, гормонным агонистом или гормонным антагонистом, что активнодействующее вещество является прогестероном, бузерелином, тамоксифеном или онапристоном, что активнодействующее вещество является веществом, которое изменяет плейотропную сопротивляемость по отношению к цитостатическим средствам, что активнодействующее вещество является ингибитором кальмодулина, что активнодействующее вещество является ингибитором протеинкиназы С, что активнодействующее вещество является ингибитором Р-гликопротеина, что активное вещество является модулятором митохондриально связанной гексокиназы, что активнодействующее вещество является ингибитором γ -глютамилцистеин-синтетазы или глютатион-S-трансферазы, что активнодействующее вещество является ингибитором супероксидисмутазы, что активное вещество представляет собой ингибитор определенного Mak Ki67 пролиферационно ассоциированного определенного протеина в клеточном ядре делящихся клеток, что активнодействующее вещество является веществом, которое обладает иммуносупрессивным эффектом, что активнодействующее вещество является стандартным иммунносупрессивным средством, что активнодействующее вещество является макролидом, что активнодействующее вещество является циклоспорином А, рапамицином, FK 506, что активнодействующее вещество является азатиоприном, метотрексатом, циклофосфамидом или хлорамбуцилом, что активнодействующее вещество является веществом, которое имеет антивоспалительное действие, что активнодействующее вещество является нестероидальным антивоспалительным средством, что активнодействующее вещество является медленно действующим антиревматическим лечебным средством, что активнодействующее вещество представляет собой стероид, что активнодействующее вещество является веществом, которое имеет противовоспалительное, анальгетическое или жаропонижающее действие, что активнодействующее вещество является производным органической кислоты, что активнодействующее вещество представляет собой не кислое анальгетическое средство, противовоспалительное средство, что активнодействующее вещество является оксифенбутазоном, что активно-действующее вещество является местно-анестизирующим средством, что активнодействующее вещество является антиаритмическим средством, что активнодействующее вещество является антагонистом Са2+, что активнодействующее вещество является противогистаминным средством, что активнодействующее вещество является ингибитором фосфодиестеразы, что активнодействующее вещество является парасимпатомимитическим средством, что активнодействующее вещество является симпатомимитическим средством или что активнодействующее вещество является веществом с ингибирующим действием на человеческую урокиназу; и кроме того, соединение, отличающееся тем, что остаток гликозила является α - или β -O-гликозидно связанным остатком D-глюкуронила, D-глюкопиранозила, D-галактопиранозила, N-ацетил-О-глюкозаминилом, остатком N-ацетил-O-галактозаминила, D-маннопиранозила или L-фукопиранозила, что оно представляет собой 4'-О-[4-(α -D-глюкопиранозилокси)-фениламинокарбонил]-этопозид,
натриевую соль N-[4-O-(β -D-глюкопиранозилуроновая кислота)-3-нитробензилоксикарбонил]-доксорубицина (соединение II),
натриевую соль N-[4-O-(β -D-глюкопиранозилуроновая кислота)-3-хлоро-бензилоксикарбонил]-доксорубицина,
натриевую соль N-[4-O-(β -D-глюкопиранозилуроновая кислота)-3-фторо-бензилокси-карбонил]-доксорубицина,
натриевую соль N-[4-O-(β -D-глюкопиранозилуроновая кислота)-3-нитро-бензилоксикарбонил]-даунорубицина,
натриевую соль N-[4-O-(β -D-глюкопиранозилуроновая кислота)-3-хлоро-бензилоксикарбонил]-даунорубицина,
N-[4-O-(α -D-галактопиранозил)-3-нитро-бензилоксикарбонил] даунорубицин,
N-[4-O-(альфа-О-галактопиранозил)-3-хлоро-бензилоксикарбонил] -даунорубицин,
N-[4-O-(α -D-галактопиранозил)-3-фторо-бензилокси-карбонил]-даунорубицин,
натриевую соль N-[4-O-(β -D-глюкопиранозилуроновая кислота)-3-нитро-бензилоксикарбонил]-доксорубицина,
натриевую соль N-[2-O-(β -D-глюкопиранозилуроновая кислота)-5-хлоро-бензилоксикарбонил]-доксорубицина,
натриевую соль N-[2-O-(β -D-глюкопиранозилуроновая кислота)-5-фторо-бензилоксикарбонил]-доксорубицина,
натриевую соль N-[2-O-(β -D-глюкопиранозилуроновая кислота)-5-нитро-бензилоксикарбонил]-даунорубицина,
натриевую соль N-[2-O-(бета-D-глюкопиранозилуроновая кислота)-5-хлоро-бензилоксикарбонил]-даунорубицина,
N-[2-O-(альфа-D-галактопиранозил)-5-нитро-бензилоксикарбонил]-даунорубицин,
N-[2-O-(α -D-галактопиранозил)-5-хлоро-бензилоксикарбонил]-даунорубицин,
N-[2-O-(альфа-D-галактопиранозил)-5-фторо-бензилоксикарбонил]-даунорубицин,
4'-О-[4-(β -D-глюкопиранозилокси)-фениламинокарбонил]-этопозид,
4'-О-[4-(α -D-галактапиранозилокси)-фениламинокарбонил]-этопозид,
4'-О-[4-(β -D-глюкуронилокси)-фениламинокарбонил]-этопозид,
4'-О-[4-(β -D-глюкуронилокси)-3-нитро-бензиламинокарбонил]-этопозид,
4'-О-[4-(β -D-глюкуронилокси)-3-хлор-бензиламинокарбонил]-этопозид,
1-N-[4-(β -D-глюкоронилокси)-бензилоксикарбонил]-митомицин С,
14-O-[4-(β -D-глюкуронилокси)-3-нитробензиламинокарбонил]-доксорубицин,
4-O-[4-(β -D-глюкуронилокси)-бензиламино-карбонил]-4-гидрокси-1-N-(бис-2-хлорэтил)-анилин,
4-O-[4-(β -D-глюкуронилокси)-бензиламинокарбонил]-терфенадин,
3'-О-[4-(β -D-глюкуронилокси)-бензиламинокарбонил]-тербуталин,
3'-О-[4-(β -D-глюкуронилокси)-бензиламинокарбонил]-фенотерол,
1''-O-[4-(β -D-глюкуронилокси)-бензиламинокарбонил]-салбутамол,
3-O-[4-(β -D-глюкуронилокси)-бензиламинокарбонил]-мускарин,
4'-О-[4-(β -D-глюкуронилокси)-бензиламинокарбонил]-оксфенбутазон,
2-O-[4-(β -D-глюкуронилокси)-бензиламинокарбонил]-салициловую кислоту,
N-[4-(β -D-глюкуронилокси)-бензиламинокарбонил]-диклофенак,
N-[4-(β -D-глюкуронилокси)-бензиламинокарбонил]-флуфенаминовую кислоту,
4-N-[4-(β -D-глюкуронилокси)-бензиламинокарбонил]-4-метиламинофеназон,
7-N-[4-(β -D-глюкуронилокси)-бензиламинокарбонил]-теофиллин,
1-N-[4-(β -D-глюкуронилокси)-бензиламинокарбонил]-нифедипин,
[4-(β -D-глюкуронилокси)-3-нитробензил]-2-[1-циано-1-(N-4-трифторметилфенил)-карбамоил]пропен-1-ил-карбонат,
3'-N-[4-N-(α -D-галактозилоксикарбонил)-4-аминобензил-оксикарбонил]-доксорубицин,
9-O-[4-(β -D-глюкуронилокси)-3-хлоробензилоксикарбонил]-квинин или
18-O-[3,5-диметокси-4-[4-(β -D-глюкуронилокси)-3-хлоробензилоксикарбонил]бензоил]-резерпат.
В частности, предпочтительным является использование в качестве активнодействующего вещества соединения II
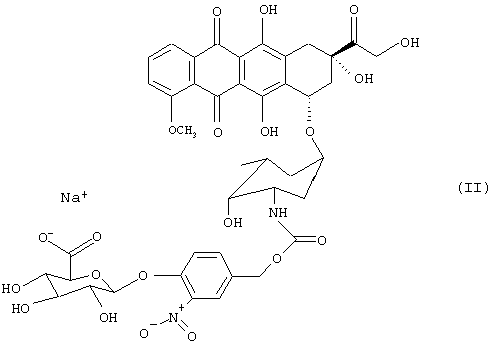
а также маннитола в качестве сахарного спирта и Са2+ в качестве двухвалентного иона.
Получение соединения формулы I осуществляют, например, как это описано в Европейском патенте ЕР 0751144.
Соединение II применяют в количестве от 1 до 1000 мг/кг живого веса, предпочтительно от 5 до 500 мг/кг.
Если препарат является растворимым, то используют маннитол в количестве от 1 мг/мл до 150 мг/мл, предпочтительно, от 10 до 100 мг/мл. В растворимом препарате используют ионы Са2+, например, в виде CaCl2 в количестве от 0,01 мг/мл до 10 мг/мл, предпочтительно, от 0,05 до 2 мг/мл, в частности, 0,4 мг/мл CaCl2×2H2O.
Твердый препарат согласно изобретению пригоден, например, для лечения:
- острых иммунологических проявлений, как, например, сепсис, аллергия, реакции "трансплантат против хозяина" и "хозяин против трансплантата",
- аутоиммунных заболеваний, в частности ревматоидного артрита, системной красной волчанки, рассеянного склероза,
- псориаза, атопического дерматита, астмы, крапивницы, ринита,
- фиброза печени, кистозного фиброза, колита,
- раковых заболеваний, как, например, рака легких, лейкемии, рака яичников, саркомы, саркомы Калоши, менингиомы, рака кишки, рака лимфатического узла, опухоли головного мозга, рака груди, рака поджелудочной железы, рака простаты или рака кожи.
Твердый препарат согласно изобретению может охватывать также комбинированные упаковки или композиции, в которых составляющие части поставлены рядом друг с другом и поэтому могут быть использованы одновременно, по отдельности или поэтапно во времени на одном и том же человеческом или животном организме.
В соответствии с изобретением компоненты 1, 2 и, при необходимости, двухвалентные ионы могут присутствовать в параллельных, разделенных лекарственных формах, в частности, тогда, когда лекарственные формы из-за пространственных размеров затрудняют применение. Это особенно относится к оральным формам, т.к. часто пожилые пациенты имеют антипатию к большим таблеткам или капсулам. Неотложным является то, что разделенные, стоящие рядом друг с другом формы должны быть приготовлены для общего во времени приема. При этом могут использоваться также различные формы, например, таблетки и капсулы, стоящие друг с другом.
Кроме того, изобретение относится к способу получения препарата согласно изобретению, который отличается тем, что компоненты 1), 2), при необходимости, двухвалентные ионы и фармацевтические носители перерабатывают в одну фармацевтическую форму применения.
Твердый препарат согласно изобретению может присутствовать в качестве дозировочной единицы в виде лекарственных форм, таких, например, как капсулы (включая микрокапсулы), таблетки (включая драже и пилюли) или свечки, при этом при применении капсул материал капсул может выполнять функцию носителя, а содержимое может находиться в виде порошка, геля, эмульсии, дисперсии или раствора. Однако наиболее предпочтительным и простым является изготовление оральных (пероральных) форм с тремя компонентами 1), 2) и, при необходимости, двухвалентными ионами, которые содержат расчетные количества активных веществ вместе с каждым желаемым фармацевтическим носителем. Может применяться также соответствующая форма (свечи) для ректальной терапии. Возможно также трансдермальное применение в виде мазей, кремов или оральное применение растворов, содержащих препарат согласно изобретению. Кроме того, соединения формулы I могут находиться также в виде лиофилизата, который перед применением реконструируют раствором, содержащим 5% маннитола и 0,4 мг CaCl2×2H2O/мл (рН, примерно, 7).
Мази, пасты, кремы и пудра наряду с активнодействующими веществами могут содержать обычные носители, например, животные и растительные жиры, воск, парафин, крахмал, трагакант, производные целлюлозы, полиэтиленгликоли, силиконы, бентониты, тальк, окись цинка, молочный сахар, кремневую кислоту, гидроксид алюминия, силикат кальция и полиамидный порошок или смеси этих веществ.
Таблетки, пилюли или гранулы можно получать обычными способами, как, например, способами прессования, погружения или псевдоожижения или котлового дражирования, и они могут содержать носитель и другие обычные вспомогательные вещества, как, например, желатину, агарозу, крахмал (например, картофельный, кукурузный или пшеничный крахмал), целлюлозу, например, этилцеллюлозу, двуокись кремния, различные сахара, например, молочный сахар, карбонат магния и/или фосфаты кальция. Раствор для дражирования состоит, обычно, из сахара и/или крахмального сиропа и содержит, чаще всего, также желатин, гумми арабику, поливинилпирролидон, синтетические сложные эфиры целлюлозы, поверхностно-активные вещества, смягчители, пигменты и аналогичные добавки согласно уровню техники. Для получения препаратов можно применять каждое обычное средство регулирования текучести, смазывающее или скользящее средство, например, стеарат магния и разделительное средство.
Применяемая дозировка зависит, естественно, от различных факторов, например, от подлежащего лечению живого существа (например, человека или животного), веса, возраста, общего состояния здоровья, степени тяжести симптомов подлежащего лечению заболевания, возможных сопутствующих заболеваний (если таковые есть), вида сопутствующего лечения другими лечебными средствами или от частоты лечения. Дозы даются, например, от одного до трех раз в неделю (интравенозно).
Количество активнодействующих компонентов зависит, естественно, от числа отдельных дозировок, а также от подлежащей лечению болезни. Отдельная дозировка может состоять из нескольких одновременно даваемых дозировочных единиц.
Примеры
Фармакологическое испытание
В качестве подопытных животных служат голые мыши племенного штамма NMRI с весом тела от 17 до 25 г, носящие опухоли. В каждой опытной группе используют 6-8 животных. Животные получают интравенозно соединение II в растворенном виде с физиологическим раствором поваренной соли (доза соединения II как указано в таблице 1 в 0,9% NaCl), маннитолом (доза соединения II как указано в таблице 1 в 5%-ном растворе маннитола в воде с рН 7), и препаратом согласно изобретению, содержащим соединение II, CaCl2 и маннитол (доза соединения II, как указано в таблице 1 в 5%-ном растворе маннитола с 0,4 мг СаСl2×2Н

(Т-С) 200% обозначает: время удвоения опухоли (объема опухоли) при лечении соединением II в соответствующем препарате в днях минус время удвоения опухоли при лечении соответствующим препаратом без соединения II в днях.
(Т-С) 400% обозначает: время учетверения опухоли (объема опухоли) при лечении соединением II в соответствующем препарате в днях минус время учетверения опухоли при лечении соответствующим препаратом без соединения II в днях.
Минимальное соотношение Т/С (%) обозначает: наиболее низкое значение роста опухоли терапевтической группы по сравнению с контрольной группой.
Минимальное соотношение Т/С (день) обозначает: день, в котором рост опухоли терапевтической группы имеет наиболее низкое значение по сравнению с контрольной группой.
С помощью интравенозного применения соединения II в физиологическом растворе поваренной соли с дозой 3× 25 мг/кг достигается лишь слабый противоопухолевый эффект. (Т-С) 200% составляет 3,9 дня. Однако снижение веса (мера побочных воздействий соединения II) уже достаточно высокое (24% снижения веса и 33% умерших животных).
Интравенозное применение 3× 350 мг/кг соединения II в физиологическом растворе приводит к быстрой смерти всех подопытных животных.
Введение соединения II в маннитоле приводит к явным противоопухолевым эффектам (Т-С) 200% составляет 17,3 дня) и умеренной переносимости (28% снижения веса и 17% умерших животных).
Введение 3× 400 мг/кг соединения II в Са/маннитоле приводит к сильным противоопухолевым эффектам (Т-С) 200% составляет 19,6 дня) и хорошо переносится подопытными животными (18% снижения веса и нет умерших животных).
Аналогичные положительные результаты наблюдались в опытах над обезьянами Масаса fascicularis после введения 3× 120 мг/кг соединения II в растворе Са/маннитол. Животные пережили эту экстремально высокую дозу без явных признаков побочных явлений. При растворении соединения II в 0,1 М фосфатного буфера, рН 7,35, переносится максимально 1× 40 мг/кг. Эти исследования доказывают, что соединение II в растворе Са/маннитол согласно изобретению не только лучше переносится, но и является явно более эффективным.
| название | год | авторы | номер документа |
|---|---|---|---|
| НИЗКОМОЛЕКУЛЯРНЫЕ КОНЪЮГАТЫ ПРОТИВООПУХОЛЕВЫХ АГЕНТОВ И ВЫСОКОСЕЛЕКТИВНЫХ ЛИГАНДОВ АСИАЛОГЛИКОПРОТЕИНОВОГО РЕЦЕПТОРА ДЛЯ ТЕРАПИИ ОНКОЛОГИЧЕСКИХ ПАТОЛОГИЙ ПЕЧЕНИ | 2017 |
|
RU2696096C2 |
| НОВЫЕ ПЕНТАСАХАРИДЫ И СОДЕРЖАЩИЕ ИХ ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ | 1999 |
|
RU2193040C2 |
| ПРОЛЕКАРСТВО ДЛЯ ТЕРАПИИ ОПУХОЛЕЙ И ВОСПАЛИТЕЛЬНЫХ ЗАБОЛЕВАНИЙ | 1997 |
|
RU2191021C2 |
| ПОЛИМЕРОСОДЕРЖАЩЕЕ ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ОСНОВЕ ПРОТИВООПУХОЛЕВОГО ПРЕПАРАТА ЭТОПОЗИДА | 2015 |
|
RU2595859C1 |
| КОНЪЮГАТЫ ЭТОПОЗИДА И ДОКСОРУБИЦИНА ДЛЯ ДОСТАВКИ ЛЕКАРСТВЕННЫХ СРЕДСТВ | 2009 |
|
RU2531591C2 |
| СПОСОБЫ ЛЕЧЕНИЯ РАКА ПОДЖЕЛУДОЧНОЙ ЖЕЛЕЗЫ | 2017 |
|
RU2768479C2 |
| ГЛИКОЛИПИДНЫЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В ЛЕЧЕНИИ ОПУХОЛЕЙ | 2015 |
|
RU2719486C2 |
| КОНЪЮГАТЫ ДИСОРАЗОЛОВ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ, НАЗВАННЫЕ КОНЪЮГАТЫ ДЛЯ ИЗГОТОВЛЕНИЯ ЛЕКАРСТВЕННОГО СРЕДСТВА, НАБОР И СПОСОБ ИХ ПОЛУЧЕНИЯ | 2007 |
|
RU2473562C2 |
| СПОСОБ ЛЕЧЕНИЯ ПУТЕМ ПРИМЕНЕНИЯ КОМБИНИРОВАННОЙ ТЕРАПИИ | 2010 |
|
RU2543348C2 |
| КОМБИНИРОВАННАЯ ТЕРАПИЯ ПРОТИВООПУХОЛЕВЫМ АЛКАЛОИДОМ | 2018 |
|
RU2767664C2 |
Препарат содержит соединение формулы (I) гликозил - Y[-C(=Y)-X-]p-W(R)n-X-C(=Y)- активное вещество (I), где значения радикалов, р и n приведены в формуле изобретения, сахар и/или сахарный спирт, фармацевтически приемлемый носитель и, необязательно, двухвалентные ионы металлов Са, Mg, Fe, Cu или Ni. Предпочтительным соединением формулы (I) является доксорубицин. Препарат используется при лечении злокачественных опухолей, воспалительных процессов и аутоиммунных заболеваний. Модификация препарата обеспечивает улучшенную переносимость in vivo и повышение эффективности действия. 2 с. и 5 з.п. ф-лы, 1 табл.
гликозил - Y[-C(=Y)-X-]p-W(R)n-X-C(=Y)- активное вещество (I),
где гликозил является ферментативно отщепляемым поли-, олиго- или моносахаридом;
W является остатком фенила или многократно замещенным остатком фенила;
и при этом заместитель R является атомом водорода, метилом, метокси, карбокси, метилоксикарбонилом, CN, гидрокси, нитро, фтором, хлором, бромом, сульфонилом, сульфонамидом или сульфон-(С1-С4)-алкиламидом;
р равно 0 или 1;
n равно 1-4;
Х является атомом кислорода, NH, метиленокси, метиленамино или метилен-(С1-С4)-алкиламино;
Y является атомом кислорода или NH,
активное вещество обозначает связанное через гидрокси, - амино- или иминогруппу соединение с биологической активностью, причем в качестве активного вещества содержатся антрациклин, предпочтительно, доксорубицин, а также активные вещества из группы, включающей этопозиды, эпотилон А-С, N-бис(2-хлорэтил)-4-гидроксианилин, 4-гидроксициклофосфамид, виндезин, винбластин, винкристин, 5-фторурацил, метотрексат, митомицин С, митоксантрон, камптотецин и производные камптотецина, m-АМSA, таксол, другие таксаны, циклофосфамид, рахелмицин, мелфалан, блеомицин, неокарциностатин, калихеамицин, динемицин, эсперамицин А, производное рогитукина, лефлуномид, или их дополнительно замещенные одной или несколькими гидрокси-, амино- или иминогруппами производные,
и/или физиологически переносимую соль соединения формулы I, 2) сахар и/или сахарный спирт и 3) фармацевтически приемлемый носитель.

| Способ определения устойчивости растений хлопчатника к вилту | 1974 |
|
SU511917A1 |
| МАШКОВСКИЙ М.Д | |||
| Лекарственные средства | |||
| - М.: Медицина, 1986, ч.2, с.457-464 | |||
| ЕР 0751144 А1, 02.01.1997. | |||
Авторы
Даты
2004-08-20—Публикация
1998-05-14—Подача