ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Данное изобретение относится к макропористым хитозановым гранулам и способу получения макропористых хитозановых гранул. Более конкретно, данное изобретение относится к макропористым хитозановым гранулам, которые превосходны по прикреплению к ним клеток, биосовместимости с клетками и биодеградации и, таким образом, пригодны для роста клеток, ангиогенеза и для диффузии питательных веществ, и к способу получения макропористых хитозановых гранул. Данное изобретение относится также к способу культивирования клеток животных и растений с использованием макропористых хитозановых гранул.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
В последнее время активные исследования были обращены к клеточным культурам для получения замены метаболическим тканям, таким как ткани печени и поджелудочной железы, а также хряща и кости. Для эффективного культивирования клеток необходимы матрицы для культур, чтобы была возможность прикрепления клеток, чтобы облегчить рост клеток и помочь клеткам сохранять их функции, кроме того, что они должны обладать биосовместимостью, способностью к биодеградации, пластичностью и должны быть пористыми. В частности, матрикс для клеток должен быть пористым, чтобы разместить как можно больше клеток в ограниченном пространстве. В этом отношении размер и трехмерное строение пор должны определяться при тщательном рассмотрении клеточного роста, ангиогенеза и диффузии питательных веществ.
К настоящему времени в качестве матрикса для культур клеток использовалось много природных и синтетических полимеров. Например, для создания трехмерных пористых заменителей кости использовали сетку из ПГК (PGA; полигликолевая кислота), которая дает возможность множеству клеток прикрепиться к ней, кроме того, что она способствует быстрой регенерации ткани и является превосходной по биодеградации (Vunjak-Nonakovi G. et al., Journal of Biotechnology Progress, vol. 14, 193-202, 1998). Du С. et al. синтезировали пНАС (нано-НАр/коллаген) (Journal of Biomedical Materials Research, vol. 44, 407-415, 1999). PLLA (поли-L-молочная кислота) была успешно использована для культивирования остеобластов (Lo et al., Journal of Biomedical Materials Research, vol. 30, 475-484, 1996; Evans G.R. et al., Journal of Biomaterials, vol. 20, 1109-1115, 1999). Из PGA и PLLA были изготовлены сетка или трехмерный пористый остов с использованием метода литья в растворителе или выщелачивания частиц, на которых выращиваются хондроциты (Freed et al., Journal of Biomedical Materials Research, vol. 27, 11-23, 1993). Была предпринята попытка культивировать фибробластные клетки на пористом матриксе, изготовленном из ПЭГ (полиэтиленгликоля), сопряженного с фибриногеном (Pandit A. S. et al., Journal of Biomaterials Application, vol. 12, 222-236). Другой успех в культивировании фибробластов был достигнут путем использования трубчатой ПГК, формируемой с помощью метода литья напылением раствора PLLA или PLGA (поли-D,L-молочной-согликолевой кислоты) в хлороформе, у которой была выявлена повышенная прочность на сжатие.
Для эффективного культивирования клеток необходим в основном пористый матрикс, чтобы дать возможность легко и равномерно прикрепиться к ним как можно большему числу клеток в ограниченном пространстве, а также для облегчения роста клеток. Однако вышеуказанные матриксы недостаточно удовлетворяют данным требованиям.
Было сделано предположение, что бусиноподобные матрицы скомпенсируют недостатки вышеназванных матриц. Исследование различных биосовместимых материалов со свойствами фактора роста, эффективным и для гомеостаза в случае травмы, привело к открытию того, что положительно заряженные гранулы более эффективны в остановке кровотечения (Wu L. et al., Journal of Surgical Research, vol. 85, 43-50, 1999). Альгинатные гранулы использовали для культуры хондроцитов и через 1-2 дня культивирования добавляли ИЛ-1β (интерлейкин-lβ) для облегчения формирования внеклеточного матрикса (Beekman В. et al., Osteoarthritis Cartilage, vol. 5, 330-340, 1998).
Кроме того, были разработаны другие пористые матрицы для клеточных культур из желатина, коллагена, гиалуроновой кислоты, целлюлозы и стекла. Пористые желатиновые гранулы полимеризуют путем добавления ГЭМА (2-гидроксиэтилметакрилат) и ЭДМ (этиленгликольдиметакрилат) и придают им пористость с помощью повторных циклов замораживания и оттаивания.
Такие желатиновые гранулы делают возможным прикрепление к ним различных видов клеток. Затем клетки имплантируют в ткани чтобы изучить замещение ткани. Данные гранулы могут варьировать по размеру, в зависимости от материалов, но они непригодны для использования в клеточной культуре по причине малых размеров их пор, заключенных в интервале от 0,7 до 2,6 мкм. Матрицы в виде круглых гранул обладают преимуществами размещения большого числа клеток в ограниченном пространстве, что дает возможность хорошего роста клеток и эффективного выделения продуктов. Однако у матриц в виде гранул, изготовленных из альгината или желатина, есть сложности в формировании пор желаемых размеров и в возможности равномерного распределения на них и в них. Когда они изготовлены из коллагена или стекла, гранулы страдают тем недостатком, что имеют плохую биосовместимость. Поэтому эти гранулы непригодны в качестве матриц для адсорбции клеток с точки зрения неустойчивости клеток и силы адсорбции.
Что касается эффективного применения при исследовании по замещению ткани посредством имплантации клеток, необходимы полимеры, которые обладают способностью к прикреплению клеток и обладают биосовместимостью, способностью к биодеградации, пластичностью и пористостью. Превосходя по пластичности в отношении размера и формы природные полимеры, синтетические полимеры хуже их по биосовместимости и в отношении биодеградации. Поэтому синтетические полимеры обладают свойством оказывать различные побочные эффекты на прямую имплантацию ткани. По этим причинам природные полимеры, которые являются безопасными и имеют разнообразное применение, активно изучаются.
Хитин, предшественник хитозана, обнаруживается на поддающемся количественному определению уровне в панцирях ракообразных, таких как крабы и креветки, и насекомых, и в клеточных стенках низших грибов, грибов и бактерий. Он является полимером, состоящим из повторяющихся N-ацетил-D-глюкозаминовых звеньев, которые связаны друг с другом через (1→4)-β-гликозидную связь. Хитозан, щелочной полисахарид, полученный путем N-дезацетилирования хитина с помощью высокой концентрации щелочи, как известно, превосходит по способности к прикреплению клеток, биосовместимости, биодеградируемости и пластичности вышеназванные синтетические полимеры.
Эти преимущества послужили причиной того, что было предпринято множество попыток использовать хитозан в качестве матрикса для клеточной культуры. Например, структурированный глютаральдегидом хитозан и модифицированный фруктозой хитозан использовали в качестве матриц для культивирования гепатоцитов (Yagi, et al., Biological Pharmaceutical Bulletin, vol. 20, No. 6, 708-710 & vol. 20, No. 12, 1290-1294, 1997). Эти хитозановые матрицы могут быть получены путем смешивания глютаральдегида или фруктозы с чистым хитозаном для улучшения прикрепления клеток и изготовлены в желаемой форме. Однако культивирование клеток с использованием этих модифицированных хитозановых матриц может происходить только в двухмерной системе культивирования, так как клетки адсорбируются только на поверхности матриц.
Хитозановые пленки с желаемыми размерами пор были получены с помощью различных методик лиофилизации и использовались при тканевой инженерии (Madihally S. V. et al., Journal of Biomaterials, vol. 20, 1133-1142, 1999). Эти хитозановые пленки оказались очень эффективными для получения пор желаемого размера, но все еще оставались ограниченными методиками двухмерного культивирования клеток.
Кроме того, сообщалось о хитозановых гранулах, которые были получены посредством лиофилизации (Tsu-Yang et al., Journal of Industrial Engineering Chemical Research, vol. 36, 3631-3638, 1997). Эти хитозановые гранулы были модифицированы путем сшивания глутаральдегида с аминокислотными остатками хитозановых гранул, и производилось измерение для демонстрации высокой степени адсорбции ионов кадмия.
Новые хитозановые гранулы были также описаны и в публикации, принадлежащей Wolfgang G. et al. из USPTO, 1999. Эти авторы использовали немагнитный янтарный ангидрид для получения хитозановых гранул с карбоксильными группами. Их подвергали взаимодействию с хлоридом железа (FeCl2) и промывали избыточным количеством воды с получением магнитных хитозановых гранул, которые, как сообщается, могут использоваться для очистки белков или для абсорбции магнитных материалов. Вследствие малого размера пор пористые хитозановые гранулы используются для адсорбции и/или очистки ионов магнитных материалов. Однако нигде не было обнаружено использование пористых хитозановых гранул в качестве матриц для культуры клеток.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В виду превосходства хитозана по способности к прикреплению клеток, биосовместимости, биодеградации и пластичности его изучали с целью получения макропористых гранул с равномерно распределенными большими порами, в которых можно благополучно культивировать клетки. На пути к данному изобретению глубокие и интенсивные исследования, проведенные авторами настоящего изобретения, привели к обнаружению того, что раствор хитозана претерпевает фазовое разделение в органическом растворителе, так что могут быть получены макропористые хитозановые гранулы с равномерными порами на и внутри них.
Поэтому объектом данного изобретения является преодоление проблем, встречающихся в предшествующих решениях, и в получении макропористых хитозановых гранул, которые имеют одинаковые поры внутри и снаружи.
Другим объектом данного изобретения является получение макропористых хитозановых гранул, которые имеют такую большую площадь поверхности, чтобы абсорбироввать на ней клетки.
Дополнительным объектом данного изобретения является получение макропористых хитозановых гранул, которые являются наилучшими по способности к прикреплению клеток, биосовместимости и деградируемости и, таким образом, пригодны для клеточного роста, ангиогенеза и диффузии питательных веществ.
Еще одним объектом данного изобретения является создание способа получения макропористых хитозановых гранул.
И еще одним объектом данного изобретения является создание способа культивирования животных и растительных клеток с использованием макропористых хитозановых гранул.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
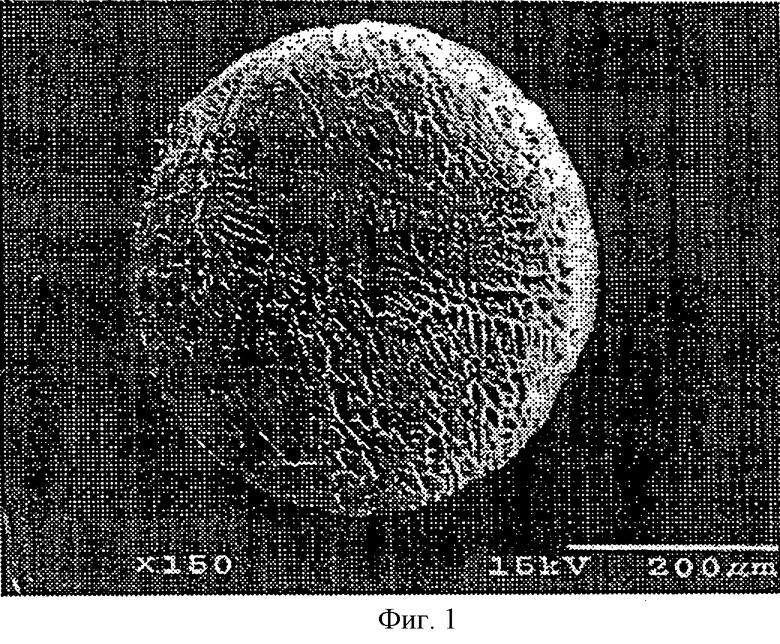
Фиг.1 является РЭМ фотографией, на которой представлена поверхность пористых хитозановых гранул данного изобретения перед тем, как клетки культивируются внутри гранул и на гранулах.
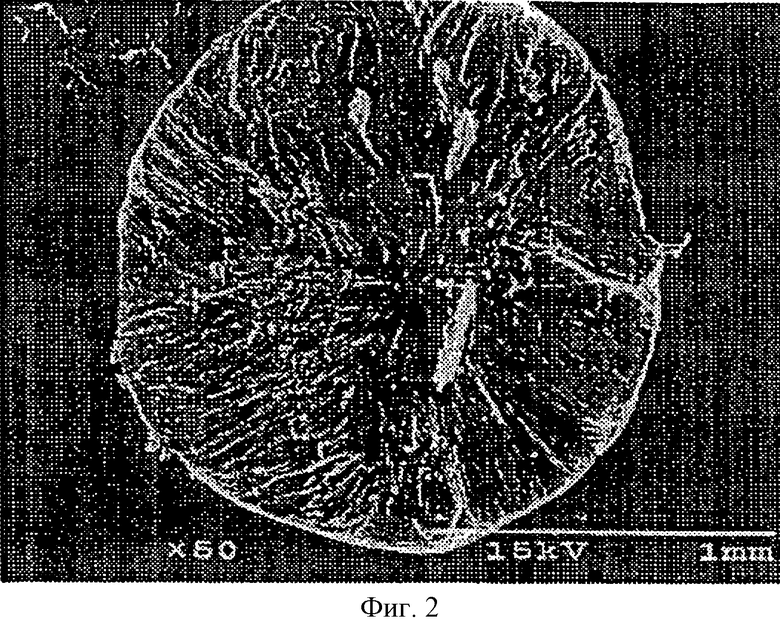
Фиг.2 является РЭМ фотографией, представляющей поперечное сечение пористых хитозановых гранул данного изобретения перед тем, как клетки культивируются внутри гранул и на гранулах.
Фиг.3 является РЭМ фотографией, на которой представлены пористые хитозановые гранулы данного изобретения после того, как гепатоциты культивированы внутри пористых хитозановых гранул и на гранулах в течение 10 дней.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Прежде чем будут раскрыты или описаны указанные макропористые хитозановые гранулы и их получение, следует уточнить, что терминология, использованная здесь, предназначена только для целей описания конкретных воплощений и не предназначена для ограничения ими изобретения.
Термин “раствор хитозана”, который здесь использован, означает водный раствор уксусной кислоты, содержащий хитозан. Термин “водный раствор хитозана”, который здесь использован, означает раствор водорастворимого хитозана в деионизированной воде.
И также термин “хитозановые гранулы” или “пористые хитозановые гранулы”, который здесь использован, означает пористые хитозановые частицы 1-4 мм с относительно одинаковыми порами, изготовленные из раствора хитозана, водного раствора хитозана и их смесей.
В то же время термин "матрикс" ("матрица") или “матрикс для культуры клеток”, который использован здесь, означает твердую основу или твердый носитель, к которым клетки прикрепляются при культивировании в среде, для того чтобы размножаться.
В одном аспекте данное изобретение относится к пористым хитозановым гранулам для клеточной культуры, которые являются превосходными по их биосовместимости, биодеградируемости, способности к прикреплению клеток и пластичности, с одинаковыми и большими по размеру порами. С этими преимуществами пористые хитозановые гранулы являются очень полезными матрицами, на которых можно культивировать различные виды животных и растительных клеток. Пористые хитозановые гранулы данного изобретения могут использоваться в качестве матриц для культивирования животных и растительных клеток всех видов, и, в частности, пригодны для культивирования гепатоцитов, фибробластов, остеобластов, эпителиальных клеток и упаковочных клеток для вирусов.
Что касается пор пористых хитозановых гранул данного изобретения, их размер предпочтительно заключается в пределах 1-500 мкм и более предпочтительно в пределах 5-200 мкм. Гранулы предпочтительно колеблются по размеру от 0,1 до 10 мм и более предпочтительно от 1 до 4 мм.
В другом аспекте данное изобретение относится к способу получения пористых хитозановых гранул. Изготовление хитозановых гранул начинается с раствора хитозана, водного хитозана или их смеси. Как упомянуто выше, раствор хитозана получают путем растворения хитозана в водном растворе уксусной кислоты, тогда как водный раствор хитозана получают путем растворения водорастворимого хитозана в деионизированной воде. Затем раствор по каплям добавляют в органический растворитель при низкой температуре или жидкий азот с получением гранул. В заключение хитозановые гранулы лиофилизируют.
Хотя хитозан растворим в кислоте, водорастворимый хитозан проявляет значительную растворимость в воде. Применимым в данном изобретении является хитозан со средней молекулярной массой, составляющей 5000-1000000.
Предпочтительная средняя молекулярная масса водорастворимого хитозана заключена в интервал 5000-1000000. Для растворения хитозана раствор уксусной кислоты предпочтительно имеет концентрацию 0,1-10% по массе. После завершения растворения хитозан предпочтительно присутствует в количестве 0,1-20% по массе в растворе уксусной кислоты. При растворении в деионизированной воде содержание водорастворимого хитозана предпочтительно колеблется по концентрации от 0,5 до 1,5% по массе. Более высокие концентрации дают в результате меньший размер пор. Таким образом, когда концентрации хитозана выше 4%, образуются очень маленькие поры, ограничивающие внедрение и рост клеток.
Когда хитозан используется вместе с водорастворимым хитозаном, хитозан предпочтительно смешивают при весовом отношении 1:9-9:1 с водорастворимым хитозаном. Чем выше пропорция водорастворимого хитозана, тем больше поры по размеру.
Примеры органического растворителя, пригодного в данном изобретении, включают в себя хлорциклогексан, хлорпентан, н-гексан, дихлорметан, хлороформ и этилацетат. Эти органические растворители, обладающие низкими температурами плавления, хотя и не растворяют хитозан, однако очень полезны для отвердения хитозана посредством разделения фаз, благодаря различию в растворимости и температуре плавления. Как показано в результате исследования зависимости изменения размера пор от органических растворителей, хлорпентан образует поры большего размера, чем дихлорпентан.
Предпочтительно, чтобы температура органического растворителя сохранялась постоянно низкой. Если температура, поддерживаемая постоянной, колеблется, отверждаемые пористые гранулы неожиданно плавятся на их поверхности, так что теряют свою пористость до такой степени, что трехмерная структура, необходимая для прикрепления клеток и помощи клеткам в выполнении их функций, разрушается. Органические растворители предпочтительно поддерживают при температуре -5 - -65°С, а жидкий азот - примерно при -198°С. Например, более низкие температуры приводят к образованию пор меньших размеров. С другой стороны, если органические растворители выдерживают при слишком высоких температурах, разделения фаз вследствие различия температуры не происходит. Наиболее предпочтительные условия для данного изобретения включают в себя добавление 1% раствора хитозана в хлорпентановый растворитель, выдерживаемый при -5 - -25°С, и добавление 1% водного раствора хитозана в хлороформный растворитель, поддерживаемый при -5 - -25°С.
Для поддержания низких температур органических растворителей можно использовать сухой лед или этанол, охлажденный в морозильнике. Альтернативно можно использовать жидкий азот примерно при -198°С.
Полученные таким образом пористые хитозановые гранулы являются гомогенными по размеру с распределением в пределах от 1 до 4 мм. Чтобы быть пригодными в качестве матриц для клеточной культуры, пористые хитозановые гранулы должны допускать их различную предварительную обработку, например лиофилизацию, нейтрализацию для удаления остающихся кислот и органических растворителей, стерилизацию этанолом, заполнение культуральной средой и затем снова лиофилизацию.
В следующем аспекте данное изобретение представляет собой способ культивирования клеток животных и растений с использованием пористых хитозановых гранул. Сначала, после того как приготовленные пористые хитозановые гранулы погружают в культуральную среду, проводят предварительное культивирование для прикрепления клеток к пористым хитозановым гранулам. После удаления несвязанных клеток прикрепленные клетки пролиферируют, и в это время старую среду заменяют свежей средой. Предварительное культивирование для прикрепления клеток предпочтительно проводится в течение 4-6 часов. Предпочтительно, чтобы культуральная среда заменялась каждые два или три дня.
Пористые хитозановые гранулы были получены в различных условиях концентрации хитозана и уксусной кислоты и видов и температур органических растворителей, и использовались в качестве матрикса для культивирования различных видов клеток, включая гепатоциты, фибробласты, остеобласты, эндотелиальные клетки, упаковывающие клетки для вирусов.
В результате были сформированы поры различных размеров, соответствующих условиям получения. Подробнее, размер образуемых пор пористых хитозановых гранул, как было обнаружено, мал, когда органические растворители поддерживают при низких температурах или же раствор хитозана или водный раствор хитозана имеет повышенную концентрацию. То есть размер пор определяется температурой, при которой происходит разделение раствора хитозана или водного раствора хитозана, и концентрацией раствора хитозана или водного раствора хитозана. К тому же вид органического растворителя влияет на предопределение размера пор хитозановых гранул. При использовании хлорпентана размер пор согласно измерениям был наибольшим. С другой стороны, дихлорпентан давал в результате и наименьшие поры. В случае смесей хитозана и водорастворимого хитозана наибольший размер пор получили, когда использовали смесь хитозана и водорастворимого хитозана в соотношении 4:6. Сравнение хитозана с водорастворимым хитозаном при одной и той же концентрации дает возможность придти к заключению, что хитозан имеет преимущества перед водорастворимым хитозаном и в формировании увеличенного размера пор.
Следовательно, 1% водный хитозан и хлороформ при -5 - -25°С или 1% хитозан и хлорпентан при -5 - -25°С могут привести к образованию пор хитозановых гранул наибольшего размера.
В сравнении с обычными матрицами пористые хитозановые гранулы, полученные способом данного изобретения, демонстрируют превосходство по адсорбции разных видов клеток животных и растений. Через 2-3 дня после того, как они адсорбировались на пористых хитозановых гранулах, клетки росли внутри и снаружи гранул, а также на их поверхности. Кроме того, было обнаружено, что гепатоциты, культивированные с использованием матрикса согласно изобретению, сохраняют свои клеточные функции, что подтверждено в результате различных биохимических экспериментов.
ПРИМЕРЫ
Лучшее понимание данного изобретения может быть получено в свете следующих примеров, которые представлены для иллюстрации, но не должны интерпретироваться как ограничение данного изобретения.
Пример 1. Получение пористых гранул с использованием 1% раствора хитозана и хлорпентана
В 1% водном растворе уксусной кислоты растворяли хитозан (Fluka, USA) в количестве, равном 1% по массе, после чего раствор хитозана медленно добавляли к хлорпентану (Sigma, USA), выдерживаемому при -5 - -25°С, при -25 - -45°С и при -45 - 65°С с помощью этанола, содержащего сухой лед (Sigma, USA), при помощи 10 мл шприца. Гранулы, которые формировались через 5-10 сек после добавления, отделяли, используя ложку, и замораживали при -70°С в течение 1 дня с последующей лиофилизацией в течение 2-3 дней в аппарате для лиофильной сушки (Cole-Parmer Instrument Company, USA). Их изучали на морфологию поверхности под сканирующим электронным микроскопом и определяли размер пор. Результаты представлены в таблице 1 и показаны на фиг. 1 и 2.
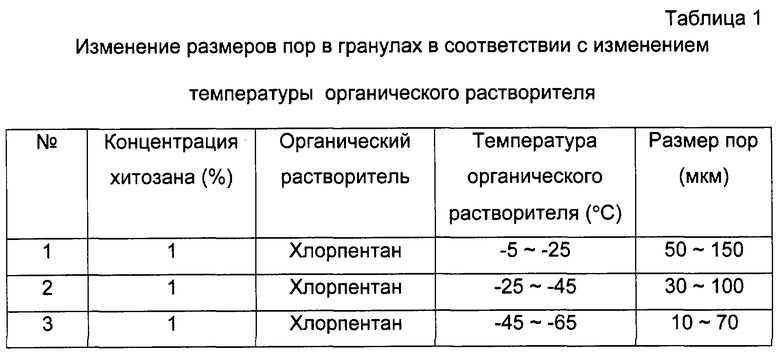
Когда пористые хитозановые гранулы получали с использованием 1% хитозана при тех же самых показателях всех параметров, за исключением температуры органического растворителя, что видно из таблицы 1, были получены поры меньшего размера при более низких температурах.
Пример 2. Получение пористых гранул с использованием 1% хитозана и различных органических растворителей
Хитозановые гранулы были получены методом, подобным таковому из примера 1, за исключением того, что использовали 1% водный раствор уксусной кислоты, содержащий хитозан в количестве 1% по массе, и различные органические растворители, такие как хлорпентан, н-гексан, дихлорпентан, хлороформ и этилацетат, выдерживаемые при -5 - -25°С.
Хитозановые гранулы исследовали с помощью сканирующего электронного микроскопа и определяли размер пор. Результаты представлены в таблице 2.
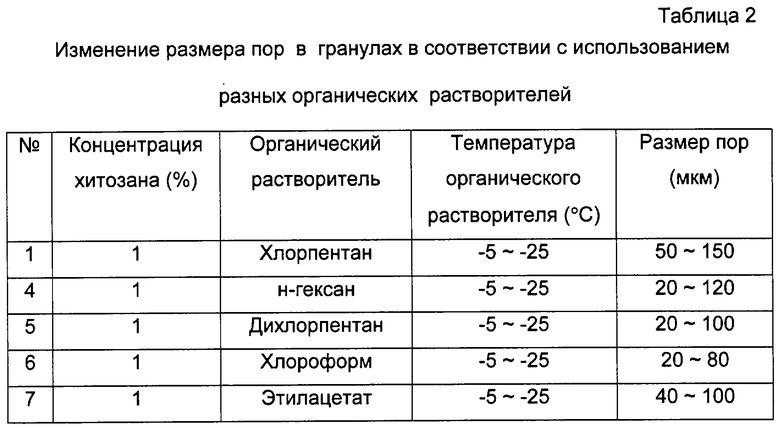
В таких же условиях при тех же самых параметрах, за исключением органических растворителей, средний размер пор хитозановых гранул согласно измерениям был наименьшим при использовании хлороформа и наибольшим при использовании хлорпентана.
Пример 3. Получение пористых гранул с использованием 2% хитозана и хлорпентана
Хитозановые гранулы получали методом, подобным таковому из примера 1, за исключением того, что использовали 1% раствор уксусной кислоты, содержащий хитозан в количестве 2% по массе, и хлорпентан, выдерживаемые при -5 - -15°С и -15 - -25°С.
Хитозановые гранулы исследовали с помощью сканирующего электронного микроскопа и определяли размер пор. Изменения размера пор в зависимости от концентрации хитозана представлены в таблице 3.
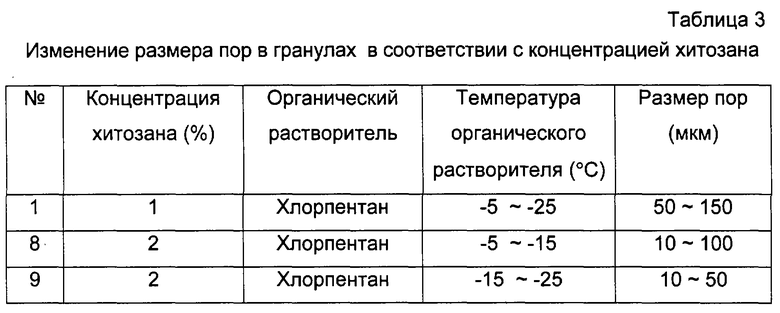
Как видно из таблицы 3, хитозановые гранулы имеют меньшие размеры пор, когда концентрация хитозана в растворе повышается.
Пример 4. Получение пористых гранул с использованием растворов 2% хитозана в 1-4% водных растворах уксусной кислоты и хлорпентана
Хитозановые гранулы получали методом, подобным таковому из примера 1, за исключением того, что использовали 2% (мас.) раствор хитозана, 1, 2, 3 и 4% водный раствор уксусной кислоты и хлорпентан, выдерживаемые при -15 - -25°С.
Исследование под сканирующим электронным микроскопом показало, что размер пор пористых хитозановых гранул заключен в пределах от 10 до 80 мкм. Результаты наблюдений представлены вместе с результатами из примера 3 в таблице 4. Как видно из таблицы 4, более высокие концентрации раствора уксусной кислоты давали в результате большие размеры пор.

Пример 5. Получение пористых гранул с использованием 2% хитозана и жидкого азота
Хитозановые гранулы получали методом, подобным таковому из примера 1, за исключением того, что использовали раствор 2% (мас.) хитозана в 1% водном растворе уксусной кислоты и жидкий азот.
Исследование в сканирующем электронном микроскопе показало, что размер пор пористых хитозановых гранул заключен в пределах от 5 до 50 мкм. Это наблюдение согласуется с данными, полученными в примере 1, что дает возможность заключить, что более низкие температуры соответствуют образованию пор меньших размеров, так как температура жидкого азота ниже, чем температура органических растворителей.
Пример 6. Получение пористых гранул с использованием 2% хитозана и хлорциклогексана
Хитозановые гранулы получали методом, подобным таковому из примера 1, за исключением того, что использовали 2% (мас.) раствор хитозана в 1% водном растворе уксусной кислоты и хлорциклогексане, выдерживаемых при -5 - -15°С, -15 - -25°С и -25-50°С. Исследование в сканирующем электронном микроскопе показало, что размер пор пористых хитозановых гранул заключен в пределах от 10 до 150 мкм. Результаты наблюдений представлены в таблице 5.

При тех же условиях по всем параметрам, за исключением температуры органического растворителя, как видно из таблицы 5, средний размер пор хитозановых гранул согласно измерениям был сходным с размером пор, полученным с использованием хлорпентана, и становился меньше при снижении температуры.
Пример 7. Получение пористых гранул с использованием смесей хитозана и водорастворимого хитозана в хлорпентане
Хитозановые гранулы получали методом, подобным таковому из примера 1, за исключением того, что использовали растворы 1% (мас.) смесей хитозана и водорастворимого хитозана (Jakwang Co. Ltd., Korea) в соотношениях 8:2, 6:4, 4:6 и 2:8, и хлорпентан, выдерживаемый при -5-25°С и -25-45°С.
Исследование в сканирующем электронном микроскопе показало, что размер пор составлял от 10 до 120 мкм. Изменения в размере пор в соответствии с пропорциями в смеси и температурой органического растворителя представлены в таблице 6.
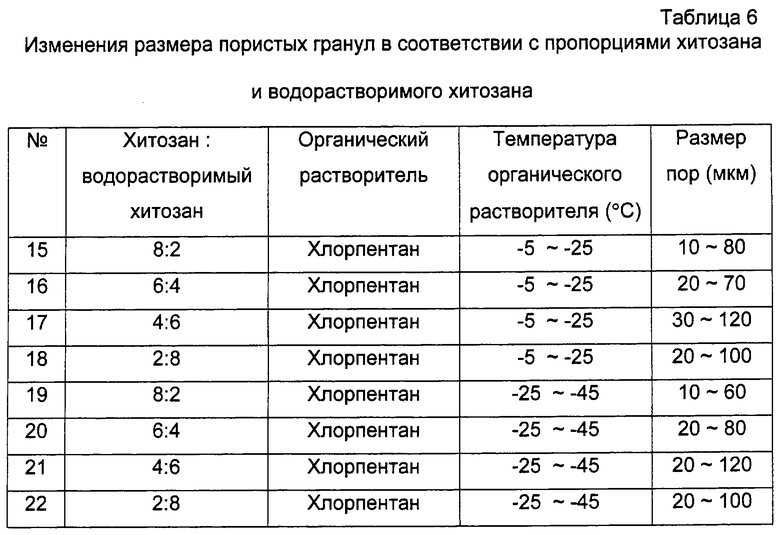
Как видно из таблицы 6, более высокое содержание водорастворимого хитозана способствует образованию пор большего размера, тогда как температура хлорпентана почти не оказывает влияния на размер пор. В частности, при использовании смеси хитозана и водорастворимого хитозана 4:6 показан больший средний размер пор хитозановых гранул, который согласно измерениям составляет от 30 до 120 мкм.
Пример 8. Получение пористых гранул с использованием водорастворимого хитозана в хлорпентане
Хитозановые гранулы получали методом, подобным таковому из примера 1, за исключением того, что использовали 1% (мас.) раствор водорастворимого хитозана в деионизированной воде и хлорпентан, выдерживаемый при -5 - -25°С, -25 - -45°С и –45 -65°С. Исследование в сканирующем электронном микроскопе показало, что размер пор пористых хитозановых гранул составляет от 10 до 70 мкм. Производили измерение размеров пор гранул, и результаты представлены в таблице 7.
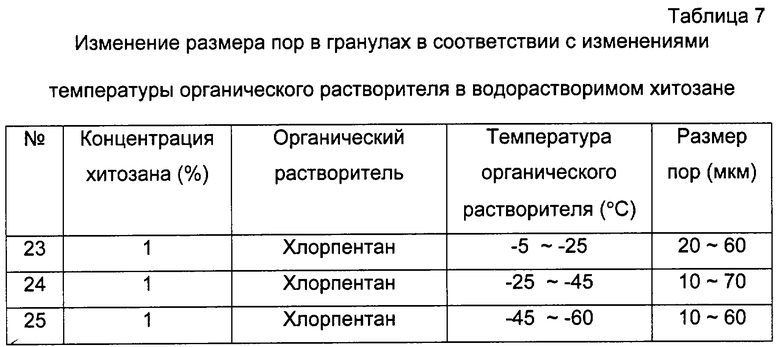
Как видно из таблицы 7, хитозановые гранулы, полученные из раствора водорастворимого хитозана, имеют размеры пор менее размеров пор хитозановых гранул, полученных из раствора хитозана. Кроме того, размер пор этих хитозановых гранул не подвергается большому изменению в зависимости от температуры, в отличие от хитозановых гранул, полученных из раствора хитозана.
Пример 9. Получение пористых гранул с использованием водорастворимого хитозана и различных органических растворителей
Хитозановые гранулы получали методом, подобным таковому из примера 1, за исключением того, что использовали 1% (мас.) раствор водорастворимого хитозана в деионизированной воде и различные органические растворители, такие как хлорпентан, н-гексан, дихлорпентан, хлороформ и этилацетат, выдерживаемые при -5 - -25°С. Исследование в сканирующем электронном микроскопе показало, что размер пор пористых хитозановых гранул составляет от 20 до 200 мкм. При изготовлении из водорастворимого хитозана проводили измерения размеров пор хитозановых гранул в соответствии с видами органических растворителей. Результаты представлены в таблице 8.
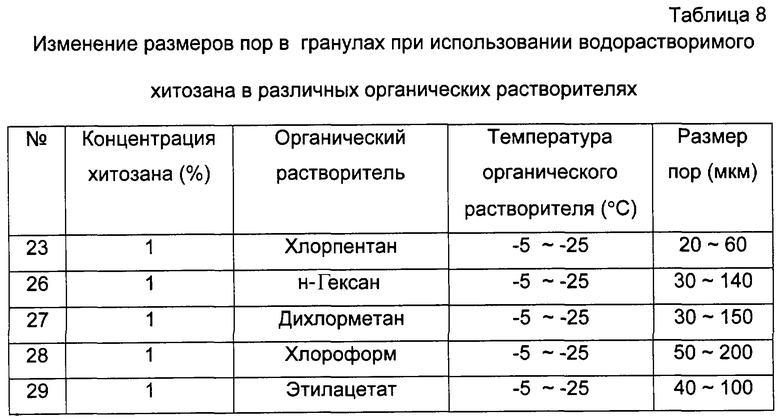
В хитозановых гранулах, полученных из раствора гранулы большего размера образуются, когда в качестве органического растворителя используется хлороформ, чем при использовании других органических растворителей. С другой стороны, хитозановые гранулы, изготовленные из хитозанового раствора, имели наибольшие размеры пор при использовании хлорпентана (таблица 2). Из этих результатов видно, что на размеры пор хитозановых гранул, полученных из раствора хитозана или раствора водорастворимого хитозана, влияет вид органического растворителя.
Экспериментальный пример 1. Культура гепатоцитов
Пористые хитозановые гранулы размером 1-4 мм с порами 50-150 мкм, полученные в примере 1, нейтрализовали 5 N раствором гидроксида натрия в этаноле для удаления оставшихся кислот и органических растворителей с последующей стерилизацией 70% этанолом. После внесения в культуральную среду (DMEM, рН 7,4, Gibco BRL, USA) хитозановые гранулы лиофилизировали. В культуральную среду погружали лиофилизированные хитозановые гранулы, к которым затем прикреплялись гепатоциты крыс. Для этого прикрепления проводили предварительное культивирование в течение 4-6 часов. Чтобы удалить клетки, оставшиеся несвязанными, среду заменяли свежей. С этого времени среду заменяли каждые два или три дня за 1-10 дней, в течение которых гепатоциты, прикрепленные к хитозановым гранулам, культивировали при 37°С. Когда клетки агломерировали, в сканирующем электронном микроскопе наблюдали клетки, которые росли в порах хитозановых гранул, а также на поверхности хитозановых гранул, что показано на фиг.3.
Экспериментальный пример 2. Культура клеток NIH3T3
Используя клетки NIH3T3, которые являются фибробластными клетками (АТСС НВ-11601, США), производили ту же процедуру в отношении культуры клеток, что и в экспериментальном примере 1.
Исследование в сканирующем электронном микроскопе показало, что клетки прочно прикреплялись к хитозановым гранулам, а также росли в порах. Кроме того, фибробластные клетки, как оказалось, росли быстро и прочно контактировали друг с другом.
Экспериментальный пример 3. Культура клеток МСЗТЗ-Е1
Используя клетки МСЗТЗ-Е1, которые являются клетками остеобластов (Korean Cell Line Bank in Seoul National University College of Medicine, Seoul, Korea), проводили ту же самую процедуру, что и в экспериментальном примере 1 в отношении культуры клеток.
В сканирующем электронном микроскопе наблюдали, что эти клетки прочно связаны с хитозановыми гранулами и хорошо растут.
Экспериментальный пример 4. Культура клеток СНО-К1
Используя клетки СНО-К1, которые являются эпителиальными клетками (АТСС CCL-61, США), проводили ту же самую процедуру, что и в экспериментальном примере 1 в отношении культуры клеток.
В сканирующем электронном микроскопе наблюдали, что эти клетки прочно связаны с хитозановыми гранулами, а также растут в порах.
Экспериментальный пример 5. Культура клеток РТ67
Используя клетки РТ67, которые являются упаковочными клетками (Korean Cell Line Bank in Seoul National University College of Medicine, Seoul, Korea), проводили ту же самую процедуру, что и в экспериментальном примере 1 в отношении культуры клеток.
В сканирующем электронном микроскопе наблюдали, что эти клетки не только прочно связаны с хитозановыми гранулами, секретируя в то же время внеклеточный матрикс в большом количестве, но также и быстро растут.
ПРОМЫШЛЕННАЯ ПРИМЕНИМОСТЬ
Как описано выше, пористые хитозановые гранулы согласно изобретению имеют одинаковые поры снаружи и внутри, так что они могут быть пригодными в качестве матрикса, который обеспечивает трехмерные структуры, используемые для помощи клеткам в осуществлении их функций. Кроме того, в отличие от общеизвестных матриц для клеточной культуры, в пористых хитозановых гранулах согласно изобретению достигнуто превосходство в прикреплении клеток, биосовместимости и биодеградируемости, а также в отношении роста клеток, ангиогенеза и диффузии питательных веществ. С такими преимуществами пористые хитозановые гранулы согласно изобретению пригодны в качестве матрикса для культивирования животных и растительных клеток. В дополнение к этому пористые хитозановые гранулы могут быть эффективно использованы для исследований по замещению метаболических тканей, таких как печень и поджелудочная железа, или хряща или кости, а также по продукции биологически полезных веществ, включая белки, антибиотики, противораковые средства, полисахариды, биологически активные материалы и гормоны растений и животных.
Данное изобретение было описано иллюстративным способом, и должно быть ясно, что использованная терминология предназначена для его описания, а не ограничения. Возможны многие модификации и варианты данного изобретения в свете вышеприведенных указаний. Поэтому должно быть понятно, что в рамках прилагаемой формулы данное изобретение может быть осуществлено на практике и иначе, чем конкретно описано.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ МИКРОТРУБОК ИЗ ХИТОЗАНА (ВАРИАНТЫ) | 2014 |
|
RU2564921C1 |
| СПОСОБ ПОЛУЧЕНИЯ МАКРОПОРИСТОГО ПОЛИМЕРНОГО МАТЕРИАЛА | 1994 |
|
RU2078099C1 |
| Регенеративный материал соединительных тканей, способ получения регенеративного материала, применение регенеративного материала, имплантат | 2018 |
|
RU2788658C2 |
| БИОСОВМЕСТИМЫЙ БИОДЕГРАДИРУЕМЫЙ ПОРИСТЫЙ КОМПОЗИЦИОННЫЙ МАТЕРИАЛ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2011 |
|
RU2471824C1 |
| Способ обработки трансплантатов для сердечно-сосудистой хирургии с использованием суб- и сверхкритического диоксида углерода | 2022 |
|
RU2796364C1 |
| БИОПОЛИМЕРНЫЙ МАТЕРИАЛ ДЛЯ КЛЕТОЧНО-ИНЖЕНЕРНЫХ И/ИЛИ ТКАНЕИНЖЕНЕРНЫХ КОНСТРУКЦИЙ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2021 |
|
RU2774947C1 |
| БИОАКТИВНЫЙ РЕЗОРБИРУЕМЫЙ ПОРИСТЫХ 3D-МАТРИКС ДЛЯ РЕГЕНЕРАТИВНОЙ МЕДИЦИНЫ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2013 |
|
RU2533457C1 |
| МАКРОПОРИСТЫЕ МАТРИЦЫ ДЛЯ КЛЕТОЧНОГО КУЛЬТИВИРОВАНИЯ | 2022 |
|
RU2798558C1 |
| СПОСОБ ПОЛУЧЕНИЯ ДВУХСЛОЙНОЙ БАРЬЕРНОЙ МЕМБРАНЫ ДЛЯ НАПРАВЛЕННОЙ КОСТНОЙ РЕГЕНЕРАЦИИ | 2018 |
|
RU2689782C1 |
| ОСНОВАННЫЙ НА ИОННОМ ПОЛИСАХАРИДЕ ПОРИСТЫЙ ПОЛИМЕРНЫЙ МАТЕРИАЛ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2020 |
|
RU2762729C1 |

Изобретение относится к макропористым хитозановым гранулам, имеющим относительно большие и одинаковые поры размером 30-150 мкм снаружи и внутри, которые распределены от поверхности до области ядра, и способу их получения, включающему в себя следующие стадии: добавление по каплям хитозанового раствора, водного хитозанового раствора или их смеси в низкотемпературный органический растворитель или жидкий азот; регуляцию размера пор с помощью метода разделения фаз за счет разницы температур. Макропористые хитозановые гранулы согласно изобретению делают культивирование клеток более эффективным, чем предшествующие субстраты, так как клетки могут эффективно прикрепляться к ним благодаря большой площади их поверхности, клеткам легко войти в них и клетки, прикрепленные к таким субстратам, могут существовать дольше благодаря их трехмерной структуре, поэтому макропористые хитозановые гранулы могут быть использованы для изучения продукции белка, антибиотиков, противораковых средств, полисахаридов, физиологически активных веществ, гормонов животных или гормонов растений, а также изучения замещения метаболических органов, хряща или кости. 4 с. и 10 з.п. ф-лы, 8 табл., 3 ил.
| CHANG GUNG CHEN | |||
| Bioprocess Eng | |||
| Металлический водоудерживающий щит висячей системы | 1922 |
|
SU1999A1 |
| US 4833237 A, 23.05.1983 | |||
| Бесколесный шариковый ход для железнодорожных вагонов | 1917 |
|
SU97A1 |
| RU 95106078 A1, 10.01.1997. | |||
Авторы
Даты
2004-08-20—Публикация
2000-11-30—Подача