Изобретение относится к области медицины, ветеринарии, а именно к фармакологии, и может использоваться для профилактики и лечения опухолевых болезни у инокурабельных больных.
Для профилактики и лечения заболевания большое значение имеет индукция эндогенного α-, β-, γ-интерферона. Эндогенный интерферон обладает большой биологической активностью, что проявляется в противовирусном, противоопухолевом, антипролиферативном и иммуностимулирующем действии.
Однако в настоящее время в качестве индуктора эндогенного α-, β-, γ-интерферона используются ослабленные живые вирусы и вакцины, которые сами неблагоприятно воздействуют на организм.
Особенно остро встает этот вопрос при лечении хронических больных или аллергиков, которым требуется длительное лечение.
Поэтому в настоящее время возрастает интерес к природным препаратам, не обладающим токсичностью и вызывающим коррекцию иммунной системы.
Наиболее близким по технической сущности к заявляемому является средство, включающее мед, прополис, маточное молочко, экстракт солодки и левзеи (Патент СССР 1836094, А 64 R 35/64, 1993).
Известное средство повышает сопротивляемость организма к действию неспецифических повреждающих факторов - токсинов и радиации.
Недостатком известного средства является активирование процесса клеточной пролиферации, которая способствует опухолевой трансформации клеток.
Задачей изобретения является создание иммунотропного препарата, обладающего способностью коррекции гуморального и клеточного иммунитета, комплемента, фагоцитарной и лизосомальной активности, а также активации эндогенного α-, β-, γ-интерферона с целью увеличения срока жизни у инокурабельных опухолевых больных.
Поставленная задача достигается иммунотропным препаратом, включающим 98-25 мас.ч. монофлерного пчелиного меда, содержащего 3-окси-флавон-силибин, 98-25 мас.ч. экстракта солодки голой, экстракт листьев мать-и-мачехи 98-25 мас.ч., экстракт цветущего просвирника лесного 98-25 мас.ч., экстракт цветущего горца птичьего 98-25 мас.ч., экстракт прополиса, в частности березового, 1-20 мас.ч., с последующим фракционированием путем замораживания водного раствора полученного меда до температуры -60°С с последующим размораживанием до 15-30°С.
Используемый монофлерный пчелиный мед семейства сложноцветных, содержащий 10-20 мас.% 3-окси-флавон-силибина, не обладающего токсическим действием и тормозящего лектинининдуцированный митогенез. Кроме этого известно, что 3-окси-флавон-силибин содержится в экстракте чертополоха колючего и не обладает токсическими свойствами (Драник Т.Н., Гриневич Ю.А., Дизик Г.М. Иммунотропные препараты. - Киев: Здоровья, 1994, с.212).
Указанный экологически чистый монофлерный мед преимущественно очищают путем медленного замораживания водного раствора или раствора, дополнительно содержащего экстракт меда, с концентрацией не более 80 мас.%. Постепенное изменение температуры позволяет удалить белки, вызывающие побочные негативные реакции, вызванные компонентами неразрушенных пыльцевых зерен. Такая очистка позволяет получать фракции монофлерного меда с полным отсутствием токсичности и аллергических реакций, проверенным в лабораторных условиях на белых мышах, морских свинках, кроликах и птицах, а также на крупных домашних животных при парентеральном введении.
Наличие 3-окси-флавон-силибина в монофлерном меде подтверждают на цыплятах, чувствительных к заражению вирусом саркомы Рауса. Цыплятам с растущими опухолями вводят монофлерный мед, содержащий 3-окси-флавон-силибин. Только при наличии 3-окси-флавон-силибина наблюдается рассасывание опухолей, уменьшение некроза. В подопытной группе цыплят наблюдается сухой некроз и постепенное рассасывание опухоли.
Вторым компонентом заявляемого иммунотропного препарата является экстракт солодки голой, содержащей гликопептиды глицирризиновой кислоты. Экстракт может содержать гликопептиды глицирризиновой кислоты до 30 мас.ч.
Третьим компонентом является экстракт листьев мать-и-мачехи, содержащей гликозиды и эфирные масла, стимулирующие выработку эндогенного альфа-, бета-, гамма-интерферона и обладающие противовоспалительным действием. Экстракт может содержать гликозиды и эфирные масла до 20 мас.ч.
Четвертым компонентом заявляемого иммунотропного препарата является экстракт просвирника лесного, содержащего пальмитиновую, стеариновую, олеиновую кислоты и углеводы. Данные вещества обладают способностью восстанавливать белково-синтетическую функцию печени и нормализовать литическую активность комплемента. Экстракт может содержать олеиновую, пальмитиновую и стеариновую кислоты до 30 мас.ч. Экстракцию биологически активных веществ осуществляют обработкой 70%-ным водным раствором этилового спирта цветущих растений, что позволяет полностью отделить экстракт от пектинов, с последующим загущением в вакуумном устройстве до содержания влаги не более 25%.
Пятым компонентом заявляемого иммунотропного препарата является экстракт травы горца птичьего. Экстракт травы горца птичьего содержит в своем составе кремниевые кислоты и флавоноиды, повышающие активность фагоцитоза. Вероятно, кремниевые кислоты находятся в коллоидном состоянии в сочетании с цинком, флавоноидами, дубильными веществами, витаминами С и К и улучшают биохимический аппарат биоцидности фагоцитирующей клетки и переваривание объекта фагоцитоза, а также обладают повышенной способностью фиксироваться на объекте фагоцитоза. Стандартизацию фагоцитирующей активности иммунотропного препарата проводят по данным иммунобиохимических исследований сыворотки крови. Экстракт может содержать кремниевые кислоты и флавоноиды до 20 мас.ч.
Шестым компонентом заявляемого иммунотропного препарата являются флавоноидные фракции прополиса березового, предпочтительно разведенные раствором хлорофилла вида “а” и “в”. Известно, что водорастворимый хлорофилл содержит порфириновые производные преимущественно в виде их комплексов с магнием (Шлык А.А. Проблемы биосинтеза хлорофиллов. - Минск, 1971).
Прополис в своем составе содержит большое количество фенольных структурно-родственных хелатообразующих соединений. Вероятно, фенольные соединения прополиса взаимодействуют с порфириновыми комплексами, включающими магний или металлы переменной валентности, с образованием хелатных соединений, обуславливающих противоопухолевую активность.
Стандартизацию прополиса проводят экспресс-методами, позволяющими при использовании небольшого количества вещества дать характеристику каждой приготовленной партии. Основу разработанных экспресс-методов составляют цветные реакции 0,1%-ного спиртового раствора прополиса с рядом комплексообразующих реагентов, в частности водными растворами хлорного железа, ацетата, меди и ацетата свинца, определяющими наличие и содержание флавоноидов, и 20%-ной щелочью, изомеризующей флавононы, постоянно присутствующие в прополисе. Для характеристики каждой партии прополиса используется различная адсорбируемость его компонентов на окиси алюминия второй степени активности, а также его способность максимально растворяться в смеси хлороформ:ацетон при их массовом соотношении 2:1 соответственно, что в итоге позволяет количественно определить содержание балластной и биологически активной фракции прополиса. Стандартизировать прополис можно и по подавлению роста растений.
Предлагаемый по изобретению препарат получают смешиванием всех указанных компонентов с последующим скармливанием полученного состава отобранным пчелиным семьям на изолированной пасеке в период окончания продуктивного взятка в ульях Дадана-Блатта. В отобранных пчелиных семьях предварительно удаляли все рамки с ранее заготовленным медом, а вместо них ставили рамки с сушью. После скармливания отбирали рамки с запечатанным медом. Откачку меда проводили на специальных медогонках, исключающих контакт экспрессного меда с металлом и воздухом.
Полученный экспрессный мед освобождают от белковых фракций описанным выше способом замораживания и размораживания, после чего его вновь скармливают пчелам. Предпочтительно этот процесс повторяют трижды с целью концентрирования компонентов и обеспечения максимальной биологической очистки заявляемого препарата.
Экспрессный мед обеспечивает полную совместимость смеси и защитное действие по отношению к 3-окси-флавон-силибину, флавоноидным фракциям прополиса, хлорофиллу высших растений, гликопептидам глицирризиновой кислоты, гликозидам, олеиновой, пальмитиновой, стеариновой и кремниевой кислотам.
Препарат может дополнительно содержать комплекс витаминов, содержащий, по крайней мере витамины А, Е, PP, F и микроэлементы, включающие, как правило, Mg, Se, Ca, Zn, Ni, Fe, I.
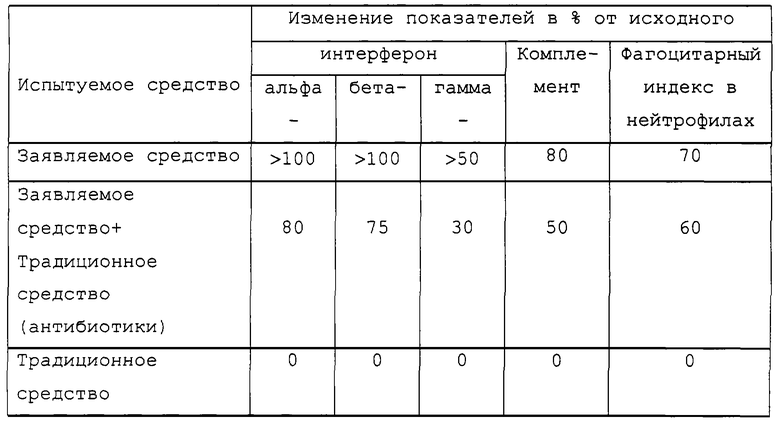
Необходимо отметить, что смесь компонентов препарата по изобретению обладает более выраженным бактериостатическим, противовирусным, противоопухолевым действием, чем отдельно взятые компоненты. Препарат корректирует гуморальный и клеточный иммунитет, активирует комплемент, фагоцитарную и лизосомальную активность в 1,5-2 раза, а также эндогенный альфа-, бета-, гамма-интерферон в 2 раза. Кроме этого, отдельные компоненты препарата разрушаются при длительном хранении, теряя при этом свою биологическую активность. Однако смесь этих же компонентов сохраняется в течение нескольких лет в активном состоянии.
Изобретение иллюстрируется нижеприведенными примерами.
Пример 1.
В монофлерный зрелый мед семейства сложноцветных, соответствующий ГОСТ 19792-74, содержащий в своем составе 3-окси-флавон-силибин, добавляют до 10 мас.ч. экстракта солодки голой, экстракт листьев мать-и-мачехи до 10 мас.ч., экстракт цветущего просвирника лесного до 10 мас.ч., экстракт цветущего горца птичьего до 10 мас.ч., экстракт флавоноидных фракций прополиса до 10 мас.ч.
Пример 2.
Для приготовления препарата по изобретению использовали 50 мас.ч. монофлерного меда, полученного из нектара растений семейства сложноцветных, содержащих 3-окси-флавон-силибин, 10 мас.ч. экстракта солодки голой, 10 мас.ч. экстракта листьев мать-и-мачехи, 10 мас.ч. экстракта просвирника лесного, 10 мас.ч. экстракта цветущего горца птичьего, 10 мас.ч. экстракта флавоноидных фракций прополиса березового. Дополнительно вводили в состав до 30 мас.ч. хлорофилла в расчете на 100 мас.ч. смеси.
Полученную смесь дважды скармливают пчелам, последующее фракционирование осуществляют путем замораживания со скоростью 1°С/ч до температуры -60°С и размораживания также со скоростью 1°С/ч до температуры 30°С. Первые фракции, содержащие белок, не использовали.
Пример 3.
К препарату, полученному согласно примеру 1, добавляют комплекс витаминов, включающий витамины А, Е, PP, F и микроэлементы Mg, Са, Se, Zn, Ni, Fe, I в количестве, обычно используемом в таких препаратах. Добавленные витамины и микроэлементы совместно с имеющимися в прополисе и экспрессном меде витаминами и микроэлементами обогащают предлагаемый препарат.
Пример 4.
Для препаратов, полученных согласно примерам 1-3, проводили определение цитотоксических и ингибирующих опухолевые вирусы доз in vitro в субкультуре клеток куриных эмбриональных фибробластов, зараженных типовыми штаммами вируса саркомы Рауса. Культивирование клеток куриных эмбриональных фибробластов первой генерации с установленным фенотипом с/о (чувствительные к заражению онкогенными вирусами) проводили с использованием среды роста субкультур клеток на основе среды Игла и триптозофосфатного бульона “Дифко” при рН=6-8.
Для стандартизации препарата по данным 5-7 опытов устанавливали методом разведения препарата следующие дозы:
1. Цитотоксическая доза должна быть не ниже 125 мкг/мл (ЦТД50/мл).
2. Ингибирующая опухолевую трансформацию клеток доза (индекс ингибиции) должна быть не ниже 1,5±0,2 lg ОД 50/мл (онкогенных доз).
3. Концентрация экстракта цветущих растений семейства сложноцветных в пределах 250 мкг/мл.
Пример 5.
Больной А. - 65 лет, диагноз при поступлении - рак пищевода. Метастазы в лимфатические узлы и печень. Больной не операбельный. Применен курс химиотерапии и одновременно назначена активная неспецифическая иммунотерапия иммунотропным препаратом согласно примеру 2 в дозе 0,03 мл/кг внутримышечно с интервалом в двое суток в течение 40 суток. У больного исчезла интоксикация, боли, улучшились показатели клеточного и гуморального иммунитета. Наступило улучшение.
Больной К. - 70 лет, диагноз при поступлении - рак толстого отдела кишечника. Метастазы в лимфатические узлы, позвоночник, печень. Отмечали резко выраженные признаки интоксикации и болевой синдром. Больному была назначена активная иммунотерапия иммунотропным препаратом до химиотерапии, в период химиотерапии и после химиотерапии в течение 3 месяцев. Использовали иммунотропный прапарат согласно примеру 1 в дозе 0,03 мл/кг с интервалом в двое суток. Для разведения препарата готовили разбавитель, включающий апирогенную ионообменную воду, микроэлементы Mn, Сu, Zn, Co, Cr, Аl, Аu, Аg, I, макроэлементы К, Са, Mg, Fe, флавоноидные фракции прополиса, экстрат череды трехраздельной, экстракта горца птичьего до 10 мас.ч. на 100 мас.ч. воды. У больного исчезли болевые синдромы, улучшилось самочуствие и показатели клеточного и гуморального иммунитета. Наступило длительное улучшение.
Пример 6.
Больная С. - 13 лет, диагноз при поступлении - саркома в области мышц бедра, с метастазами в лимфатические узлы, признаки интоксикации и резко выражен болевой синдром. Назначена химиотерапия и иммунотропный препарат в дозе 0,03 мл/кг с интервалом в двое суток в течение 30 дней. Больная подготовлена к операции. Болевые синдромы исчезли, улучшились показатели иммунитета.
Пример 7.
Проверка эффективности заявляемого препарата проводилась при лечении инокурабельных опухолевых больных в дозе 0,03 мл/кг с интервалом в двое суток в течение 45 дней.
Клинические испытания иммунотропного препарата проводили на двух группах больных с клиническим признаками интоксикации и болевыми синдромами. В опытной группе больных наблюдали улучшение основных показателей. В контрольной группе больных при лечении традиционными методами не наблюдали улучшения показателей иммунной системы. В опытной группе не отмечали случаев непереносимости и токсичности препарата. Заявленный иммунотропный препарат может быть с успехом использован для увеличения срока и комфортабельности жизни больных.
Препарат может быть использован на разных стадиях опухолевого роста и особенно у инокурабельных больных в связи с повышением иммунологической реактивности организма. На I и II стадии опухоль исчезает бесследно, а на III (конец) и IV стадии снижается болевой синдром и увеличивается продолжительность жизни. Кроме того, препарат может быть использован больными СПИДом, у которых не происходит повышение иммунологической реактивности.
Препарат может использоваться как для парентерального, так и для орального, наружного и местного применения (интраназального, конъюнктивального, вагинального).
| название | год | авторы | номер документа |
|---|---|---|---|
| ИММУНОТРОПНЫЙ ПРЕПАРАТ "ВИТУЛИН А" | 2001 |
|
RU2236247C2 |
| ИММУНОТРОПНЫЙ ПРЕПАРАТ "ВИТУЛИН Е" | 2001 |
|
RU2236245C2 |
| ИММУНОТРОПНЫЙ ПРЕПАРАТ "ВИТУЛИН В" | 2001 |
|
RU2236244C2 |
| ИММУНОТРОПНЫЙ ПРЕПАРАТ "ВИТУЛИН Д" | 2001 |
|
RU2241476C2 |
| ИММУНОТРОПНЫЙ ПРЕПАРАТ "ТУЛИМКАР" | 2001 |
|
RU2236243C2 |
| ИММУНОТРОПНЫЙ ПРЕПАРАТ "ВИТУЛИН" | 2001 |
|
RU2236248C2 |
| ИММУНОТРОПНЫЙ ПРЕПАРАТ | 1997 |
|
RU2132689C1 |
| ИММУНОТРОПНОЕ СРЕДСТВО | 1997 |
|
RU2133616C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО, ОБЛАДАЮЩЕЕ ИММУНОМОДУЛИРУЮЩИМ И АНТИОКСИДАНТНЫМ ДЕЙСТВИЕМ | 2008 |
|
RU2390347C2 |
| СБОР ЛЕКАРСТВЕННЫХ РАСТЕНИЙ, ОБЛАДАЮЩИЙ ПРОТИВОВИРУСНЫМ, ПРОТИВОМИКРОБНЫМ И ИММУНОМОДУЛИРУЮЩИМ ДЕЙСТВИЯМИ | 2000 |
|
RU2160596C1 |
Изобретение относится к фармакологии, а именно к средствам для профилактики и лечения опухолевых болезней инокурабельных больных. Предложен иммунотропный препарат, представляющий собой мед, полученный путем скармливания пчелам состава, включающего монофлерный мед семейства сложноцветных, содержащий 3-окси-флавон-силибин, экстракт флавоноидных фракций прополиса, экстракт солодки голой, экстракт листьев мать-и-мачехи, экстракт цветущего просвирника лесного, экстракт цветущего горца птичьего в определенном соотношении. Препарат индуцирует эндогенный α-, β- и γ-интерферон, улучшает показатели клеточного иммунитета, способствует увеличению срока жизни у инокурабельных опухолевых больных. 3 з.п. ф-лы, 1 табл.
Монофлерный мед семейства
сложноцветных, содержащий
3-окси-флавон-силибин 25-98
Экстракт солодки голой 25-98
Экстракт листьев мать-и-мачехи 25-98
Экстракт цветущеого
просвирника лесного 25-98
Экстракт цветущего горца птичьего 25-98
Экстракт флавоноидных
фракций прополиса 1-20
с последующим фракционированием путем замораживания водного раствора полученного меда до температуры -60°С и размораживанием до 15-30°С.
| ИММУНОТРОПНЫЙ ПРЕПАРАТ | 1997 |
|
RU2132689C1 |
| ИММУНОТРОПНОЕ СРЕДСТВО | 1997 |
|
RU2133616C1 |
| СРЕДСТВО, ОБЛАДАЮЩЕЕ АНТИОКСИОКСИДАНТНЫМ И ГЕПАТОЗАЩИТНЫМ СВОЙСТВАМИ | 1990 |
|
RU2020946C1 |
| ЛЕКАРСТВЕННОЕ СРЕДСТВО ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ВИЧ-ИНФЕКЦИИ | 1991 |
|
RU2020942C1 |
| Долото | 1982 |
|
SU1162415A1 |
| Сорбент для тонкослойной хроматографии | 1985 |
|
SU1310017A1 |
| DE 4111782, 15.10.1992. | |||
Авторы
Даты
2004-09-20—Публикация
2001-12-27—Подача