Настоящее изобретение относится к новому применению саредутанта. Саредутант (saredutant) представляет собой международное непатентованное название (INN) для (S)-(-)-N-метил-N-[4-(4-ацетиламино-4-фенилпиперид-1-ил)-2-(3,4-дихлорфенил)бутил]бензамида формулы
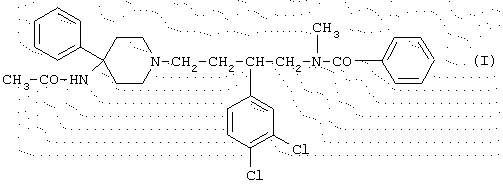
Это соединение и его фармацевтически приемлемые соли описаны в патенте ЕР 0474561 В1 и в патенте US 5236921.
Эти соединения описаны как антагонисты рецепторов нейрокинина А и могут быть полезны при любой нейрокинин А - зависимой патологии и более конкретно при нейрогенных воспалениях дыхательных путей. Эти соединения также были описаны как сильнодействующие и селективные непептидные антагонисты NK2-рецепторов нейрокинина A (Life Sciences, 1992, 50 (15), PL101-PL106).
Обнаружено, что саредутант и его фармацевтически приемлемые соли полезны при лечении или предупреждении больших депрессивных расстройств.
Задача настоящего изобретения заключается в применении саредутанта и его фармацевтически приемлемых солей для приготовления лекарственных продуктов, которые полезны при лечении или предупреждении больших депрессивных расстройств.
Саредутант и его фармацевтически приемлемые соли получают в соответствии со способом, описанным в патенте ЕР 0474561 В1, или способом, описанным в патенте ЕР 0698601 В1.
Соли соединения формулы (I) представляют собой соли с общепринятыми фармацевтически приемлемыми неорганическими или органическими кислотами, такие как гидрохлорид, гидробромид, сульфат, кислый сульфат, однозамещенный кислый фосфат, метансульфонат, метилсульфат, ацетат, оксалат, малеат, фумарат, сукцинат, 2-нафталинсульфонат, гликонат, глюконат, цитрат, изотионат, бензолсульфонат или пара-толуолсульфонат.
Для их применения в качестве лекарственных продуктов соединение формулы (I) и его фармацевтически приемлемые соли обычно вводят в виде единиц дозировки. Указанные единицы дозировки предпочтительно приготавливают в виде фармацевтических композиций, в которых активное начало смешано с фармацевтическим эксципиентом.
В фармацевтических композициях по настоящему изобретению для перорального, сублигвального, ингаляционного, подкожного, внутримышечного, внутривенного, трансдермального, местного или ректального введения активное начало в отдельности или в комбинации с другим активным началом можно вводить в стандартной форме животным или людям в смеси с традиционными фармацевтическими основами. Соответствующие стандартные формы для введения включают в себя пероральные формы, такие как таблетки, желатиновые капсулы, порошки, гранулы и пероральные растворы или суспензии, сублингвальные или трансбуккальные формы для введения, аэрозоли, формы для местного введения, имплантаты, формы для подкожного, трансдермального, внутримышечного, внутривенного или интраназального введения и формы для ректального введения.
Суточная доза соединения формулы (I) составляет от 0,05 до 5 мг/кг, преимущественно от 1 до 2,5 мг/кг, предпочтительно от 2 до 2,5 мг/кг, для введения в один или более чем один прием дозы. Соединение формулы (I) и его соли обычно приготавливают в единице дозировки, содержащей от 2,5 до 500 мг, преимущественно от 50 до 250 мг и предпочтительно от 100 до 250 мг активного начала на единицу дозировки для введения в один, два или более приемов дозы в одно и то же время по необходимости. Хотя эти дозы являются примерами обычных ситуаций, могут быть особые случаи, при которых подходят более высокие или более низкие дозы, и такие дозы также составляют часть данного изобретения. В соответствии с обычной практикой доза, которая подходит для конкретного пациента, определяется врачом в соответствии со способом введения, возрастом, массой и реакцией указанного пациента.
Когда приготавливают твердую композицию в форме таблетки, фармацевтический носитель добавляют к тонкоизмельченному или неизмельченному активному началу, причем этот носитель может состоять из разбавителей, таких как, например, лактоза, микрокристаллическая целлюлоза, крахмал, и добавок для препарата, таких как связующие вещества (поливинилпирролидон, гидроксипропилметилцеллюлоза и так далее), агенты, улучшающие текучесть, такие как диоксид кремния, смазывающие вещества, такие как стеарат магния, стеариновая кислота, глицерилтрибегенат или стеарилфумарат натрия.
Увлажняющие агенты или поверхностно-активные вещества, такие как лаурилсульфат натрия, могут быть добавлены к препарату.
Таблетки могут быть приготовлены с помощью различных методик: прямое таблетирование, сухая грануляция, влажная грануляция, горячее плавление.
Таблетки могут быть простые или покрытые сахарной оболочкой (например, покрытые сахарозой) либо покрытые различными полимерами или другими подходящими материалами.
Таблетки с немедленным, отсроченным или пролонгированным высвобождением могут быть получены путем приготовления полимерных матриц или путем применения специфических полимеров при операции покрытия пленкой.
Препарат в виде желатиновой капсулы получают путем простого смешивания активного начала с сухими фармацевтическими носителями (простое смешивание или сухая грануляция, влажная грануляция или горячее плавление), жидкими или полутвердыми фармацевтическими носителями.
Желатиновые капсулы могут быть мягкими или твердыми и покрытыми пленкой либо каким-либо другим образом, так чтобы обладать немедленным, отсроченным или пролонгированным действием (например, посредством энтеросолюбильной формы).
Препарат в форме сиропа или эликсира может содержать активное начало вместе с подсластителем, предпочтительно некалорийным подсластителем, метилпарабеном и пропилпарабеном в качестве антисептика, а также усилителем вкусоароматических свойств и подходящим красителем.
Диспергируемые в воде порошки или гранулы могут содержать активное начало в виде смеси с диспергирующими агентами, увлажняющими агентами или суспендирующими агентами, такими как поливинилпирролидон, а также с подсластителями или усилителями вкусоароматических свойств.
Для ректального введения осуществляют применение суппозиториев, которые приготавливают со связующими веществами, которые плавятся при температуре прямой кишки, например маслом кокоса или полиэтиленгликолями.
Для парентерального или интраназального введения применяют водные суспензии, изотонические солевые растворы или стерильные инъецируемые растворы, которые содержат фармакологически совместимые диспергирующие агенты и/или солюбилизирующие агенты, например пропиленгликоль или бутиленгликоль.
Таким образом, для приготовления водного раствора для внутривенной инъекции возможно применение сорастворителя, такого как, например, спирт, такой как этанол, или гликоля, такого как, например, полиэтиленгликоль или пропиленгликоль, и гидрофильного поверхностно-активного вещества, такого как Tween® 80. Для приготовления масляного раствора для внутримышечной инъекции активное начало может быть растворено с триглицеридом или эфиром глицерина.
Для местного введения можно применять кремы, мази, гели или глазные капли.
Для трансдермального введения можно применять пластыри в многослойной или резервуарной форме, в которых активное начало может быть в спиртовом растворе.
Для введения путем ингаляции применяют аэрозоль, содержащий, например, сорбитантриолеат или олеиновую кислоту, а также трихлорфторметан, дихлорфторметан, дихлортетрафторэтан или любой другой биологически совместимый газ-пропеллент; также может быть использована система, содержащая активное начало отдельно или объединенное с эксципиентом, в форме порошка.
Активное начало может также быть в форме комплекса с циклодекстрином, например α-, β- или γ-циклодекстрином, 2-гидроксипропил-β-циклодекстрином или метил-β-циклодекстрином.
Активное начало может также быть приготовлено в форме микрокапсул или микросфер, возможно, с одной или более чем одной основой или добавкой.
Среди форм с пролонгированным высвобождением, которые полезны в случае длительного лечения, могут быть использованы имплантаты. Они могут быть приготовлены в форме масляной суспензии или в форме суспензии микросфер в изотонической среде.
В соответствии с настоящим изобретением предпочтительны формы для перорального введения.
Действие саредутанта на большие депрессивные расстройства изучалось на пациентах в возрасте от 18 до 65 лет. Пациенты получали саредутант перорально (300 мг/сутки) в течение примерно шести недель.
Улучшение при депрессивных синдромах оценивали по значительному уменьшению в показателях по шкале оценок депрессии Гамильтона (Hamilton) (HAM-D), а также по впечатлениям, полученных лечащим врачом, и общих впечатлениям пациента. Шкала оценок депрессии Гамильтона охарактеризована М. Hamilton в J.Neurol. Neurosurg. Psychiat, 1960, 23, 56-62.
В следующих примерах саредутант применяют в форме моносукцината.
Пример 1. Желатиновая капсула, содержащая 25 мг саредутанта:
Саредутант (определено для основания) 25,0 мг.
Моногидрат лактозы (200 меш) - сколько требуется на 170 мг.
Кросскармеллоза натрия 3,4 мг.
Стеарат магния 1,7 мг.
Очищенная вода (выпаренная при высушивании после влажной грануляции) - сколько требуется для непрозрачной белой желатиновой капсулы размера 3, заполненной до 170 мг.
Пример 2. Желатиновая капсула, содержащая 100 мг саредутанта:
Саредутант (определено для основания) 100 мг.
Моногидрат лактозы (200 меш) - сколько требуется на 170 мг.
Кросскармеллоза натрия 3,4 мг.
Стеарат магния 1,7 мг.
Очищенная вода (выпаренная при высушивании после влажной грануляции) - сколько требуется для непрозрачной белой желатиновой капсулы размера 3, заполненной до 170 мг.
| название | год | авторы | номер документа |
|---|---|---|---|
| ПРИМЕНЕНИЕ АНТАГОНИСТА ЦЕНТРАЛЬНЫХ КАННАБИНОИДНЫХ РЕЦЕПТОРОВ ДЛЯ ПРИГОТОВЛЕНИЯ ЛЕКАРСТВ, ПРЕДНАЗНАЧЕННЫХ ДЛЯ ОБЛЕГЧЕНИЯ ПРЕКРАЩЕНИЯ КУРЕНИЯ | 2001 |
|
RU2257207C2 |
| ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ | 2015 |
|
RU2785871C2 |
| АНТАГОНИСТЫ НЕЙРОКИНИНОВОГО РЕЦЕПТОРА NK-1 ДЛЯ ВЫХОДА ИЗ НАРКОЗА | 2005 |
|
RU2337685C2 |
| ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, ВКЛЮЧАЮЩИЕ ВАЛСАРТАН И ИНГИБИТОРЫ НЕЙТРАЛЬНОЙ ЭНДОПЕПТИДАЗЫ (NEP) | 2003 |
|
RU2334513C2 |
| ЛЕКАРСТВЕННЫЕ ФОРМЫ ИНГИБИТОРА ГИСТОНДИАЦЕТИЛАЗЫ В КОМБИНАЦИИ С БЕНДАМУТИНОМ И ИХ ПРИМЕНЕНИЕ | 2011 |
|
RU2609833C2 |
| ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ | 2015 |
|
RU2728787C2 |
| МЕТАБОЛИТЫ АНТАГОНИСТОВ NK-1 ПРОТИВ РВОТЫ | 2006 |
|
RU2404969C2 |
| НОВАЯ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2001 |
|
RU2241462C2 |
| НОВЫЕ СПОСОБЫ | 2014 |
|
RU2682658C1 |
| СПОСОБ ЛЕЧЕНИЯ ГЛУБОКОЙ ДЕПРЕССИИ У ЧЕЛОВЕКА | 2007 |
|
RU2445973C2 |
Изобретение относится к области медицины, а именно к фармакологии. Применяют саредутант и его фармацевтически приемлемые соли для приготовления лекарственных продуктов, которые полезны для лечения или предупреждения больших депрессивных расстройств. Указанное применение расширяет арсенал лекарственных средств для лечения больших депрессий.
Применение саредутанта и его фармацевтически приемлемых солей для приготовления лекарственных продуктов, которые полезны при лечении или предупреждении больших депрессивных расстройств.
| ЧЕТВЕРТИЧНЫЕ АМИДЫ ОСНОВНОГО ХАРАКТЕРА, СПОСОБ ИХ ПОЛУЧЕНИЯ И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2120436C1 |
| WO 9416697 А, 14.02.1994 | |||
| WO 9732865 А, 03.07.1997. | |||
Авторы
Даты
2004-10-27—Публикация
2000-04-25—Подача