Настоящее изобретение относится к циннамоиламиноалкилзамещенным производным бензолсульфонамида формулы I
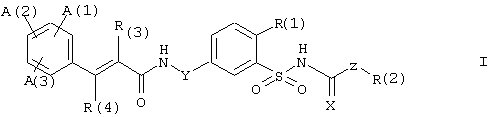
в которой А(1), А(2), А(3), R(1), R(2), R(3), R(4), X, Y и Z имеют значения, указанные ниже. Соединения формулы (I) являются ценными фармацевтически активными соединениями, которые проявляют, например, ингибирующее действие на АТФ-чувствительные калиевые каналы в сердечной мышце и/или сердечном нерве и пригодны, например, для лечения расстройств сердечно-сосудистой системы, таких как ишемическая болезнь сердца, аритмия, сердечная недостаточность или кардиомиопатии, или для предотвращения внезапной остановки сердца или для улучшения пониженной сократимости сердечной мышцы. Кроме того, изобретение относится к способам получения соединений формулы I, к их применению и к включающим их фармацевтическим композициям. Гипогликемическое действие описано для некоторых бензолсульфонилмочевин. Глибенкламид, который используют терапевтически как агент для лечения сахарного диабета, считается прототипом гипогликемических сульфонилмочевин такого типа. Глибенкламид блокирует АТФ-чувствительные калиевые каналы, и его используют в исследованиях как инструмент для исследования калиевых каналов такого типа. В дополнение к своему гипогликемическому действию, глибенкламид проявляет еще другие воздействия, которые связывают с блокадой в точности тех же АТФ-чувстительных калиевых каналов, но которые, однако, пока еще не могут быть использованы терапевтически. Эти воздействия включают, в частности, антифибрилляторное воздействие на сердце. Однако при лечении желудочковой фибрилляции или ее ранних стадий глибенкламидом значительная гипогликемия, одновременно вызываемая этим веществом, может быть нежелательной или даже опасной, так как она может дополнительно ухудшить состояние пациента.
В различных заявках на патенты, например, US-A-5698596, US-A-5476850 или US-A-5652268 и WO-A-00/03978 (патентная заявка Германии 19832009.4), описываются антифибрилляторные бензолсульфонилмочевины и тиомочевины, имеющие пониженную гипогликемическую активность. WO-A-00/15204 (патентная заявка Германии 19841534.6) описывает действие некоторых из этих соединений на автономную нервную систему. Свойства этих соединений, однако, неудовлетворительны во многих отношениях, и поэтому, кроме того, существует потребность в соединениях, имеющих более благоприятный профиль фармакодинамических и фармакокинетических свойств, который лучше подходит, в частности, для лечения нарушенного сердечного ритма и его последствий. Различные бензолсульфонилмочевины, имеющие ациламиноалкильный заместитель, в котором ацильная группа может также быть получена, среди прочего, из коричной кислоты, описаны в германских выложенных заявках DE-A-1443878, DE-A-1518816, DE-A-1518877 и DE-A-1545810. Эти соединения имеют гипогликемическое действие, но их действие на сердце пока неизвестно. Неожиданно было обнаружено, что некоторые циннамоиламиноалкилзамещенных производных бензолсульфонамида характеризуются значительным воздействием на АФТ-чувствительные каналы в сердце и дополнительными благоприятными фармакологическими воздействиями.
Одним предметом настоящего изобретения являются соединения формулы I
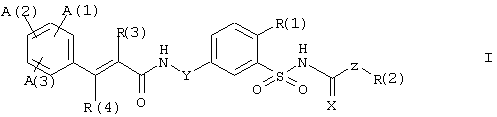
в которых
Х представляет кислород, серу или цианоимино;
Y представляет -(CR(5)2)n-;
Z представляет NH или кислород;
остатки А(1), А(2) и А(3), которые не зависят друг от друга и могут быть идентичными или различными, представляют водород, галоген, (С1-С4)-алкил, (С1-С4)-алкокси, метилендиокси, формил или трифторметил;
R(1) представляет
1) (С1-С4)-алкил; или
2) - О(C1-C4)-алкил; или
3) -О-(С1-С4)-алкил-Е(1)-(С1-С4)-алкил-D(1), в котором D(1) представляет водород или -Е (2) (C1-C4)-алкил-D (2), в котором D(2) представляет водород или -Е(3)-(С1-С4)-алкил, где Е(1), Е (2) и Е (3), которые не зависят друг от друга и могут быть идентичными или различными, представляют О, S или NH; или
4) -O-(С1-С4)-алкил, который замещен остатком насыщенного гетероцикла с числом членов от 4 до 1, который содержит один или два атома кислорода в качестве гетероатомов кольца; или
5) -O-(С2-С4)-алкенил; или
6) -O-(С1-С4)-алкил-фенил, в котором фенильная группа является незамещенной или замещена одним или двумя одинаковыми или разными заместителями из группы, состоящей из галогена, (С1-С4)-алкила, (С1-С4)-алкокси и трифторметила; или
7) -O-фенил, который является незамещенным или замещенным одним или двумя одинаковыми или разными заместителями из группы, состоящей из галогена, (С1-С4)-алкила, (С1-С4)-алкокси и трифторметила; или
8) галоген; или
9) фенил, который является незамещенным или замещенным одним или двумя одинаковыми или разными заместителями из группы, состоящей из галогена, (С1-С4)-алкила, (С1-С4)-алкокси, -S(O)m-(С1-С4)-алкила, фенила, амино, гидрокси, нитро, трифторметила, циано, гидроксикарбонила, карбамоила, (C1-C4)-алкоксикарбонила и формила; или
10) (С2-С5)-алкенил, который является незамещенным или замещенным заместителем из группы, состоящей из фенила, циано, гидроксикарбонила и (С1-С4)-алкоксикарбонила; или
11) (С2-С5)-алкинил, который является незамещенным или замещенным заместителем из группы, состоящей из фенила и (C1-С4)-алкокси; или
12) моноциклический или бициклический гетероарил, имеющий в кольце один или два одинаковых или различных гетероатома из группы, состоящей из кислорода, серы и азота; или
13) -S(Оm)-фенил, который является незамещенным или замещенным одним или двумя одинаковыми или разными заместителями из группы, состоящей из галогена, (C1-C4)-алкила, (C1-C4)-алкокси, и трифторметила; или
14) -S(Оm)(C1-C4)-алкил;
R(2) представляет водород, (C1-C6)-алкил или (С3-С7)-циклоалкил, но не является водородом, если Z представляет кислород;
остатки R(3) и R(4), которые не зависят друг от друга и могут быть идентичными или различными, представляют фенил, который является незамещенным или замещенным одним или двумя заместителями, выбранными из группы, состоящей из галогена, (C1-C4)-алкила, (C1-C4)-алкокси, и трифторметила или водорода или (C1-C4)-алкила;
остатки R(5), которые не зависят друг от друга и могут быть идентичными или различными, представляют водород или (C1-С3)-алкил;
m равно 0, 1 или 2;
n равно 1, 2, 3 или 4;
во всех своих стереоизомерных формах и их смесях во всех соотношениях, и их физиологически переносимые соли;
где исключены соединения формулы I, в которых одновременно Х представляет кислород, Z представляет NH, R(1) представляет галоген, (C1-C4)-алкил или -О-(C1-C4)-алкил и R(2) представляет (C2-C4)-алкил или (C5-C7)-циклоалкил.
Если остатки, заместители или переменные могут несколько раз встретиться в соединениях формулы I, все они имеют указанные значения независимо друг от друга и в каждом случае могут быть одинаковыми или различными.
Термин "алкил" означает насыщенный углеводородный остаток с прямой или разветвленной цепью. То же применимо к полученным из них остаткам, таким как, например, алкокси, алкилкарбонил или остаток -S (О)m-алкил. Примерами алкильных остатков являются метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изо-бутил, трет-бутил, н-пентил, 1-метилбутил, изопентил, нео-пентил, трет-пентил, н-гексил или изогексил. Примерами алкокси являются метокси, этокси, н-пропокси, изопропокси, трет-бутокси, и т.д. То же применимо к замещенным алкильным остаткам, например, фенилалкильным остаткам, или к двухвалентным алкильным остаткам (алкандиильным остаткам), в которых заместители или связи, через которые остатки связаны с соседними группами, могут быть расположены в любых желаемых положениях. Примерами алкильных остатков такого типа, которые связаны с двумя соседними группами и которые, среди прочего, могут представлять группу Y, являются –СН2-, -СН(СН3)2, -С(СН3)2, -СН2-СН2-, -СН(СН3)-СН2-, -СН2-СН(СН3)-, -СН2-СН2-СН2 или -СН2-СН2-СН2-СН2.
Алкенил и алкинил означают моно- или полиненасыщенные углеводородные остатки с прямой или разветвленной цепью, в которых двойные связи и/или тройные связи могут быть размещены в любых желаемых положениях. Предпочтительно остатки алкенил и алкинил содержат одну двойную связь и одну тройную связь. Примерами алкенила и алкинила являются винил, проп-2-енил (аллил), проп-1-енил, бут-2-енил, бут-3-енил, 3-метилбут-2-енил, пент-2,4-диенил, этинил, проп-2-инил (пропаргил), проп-1-инил, бут-2-инил и бут-3-инил. В замещенных алкенильных остатках и алкинильных остатках заместители могут быть расположены в любых желаемых положениях.
Примерами циклоалкильных остатков являются циклопропил, циклобутил, циклопентил, циклогексил или циклопентил.
Галоген представляет фтор, хлор, бром или иод, предпочтительно хлор или фтор.
В замещенных фенильных остатках заместители могут находиться в любых возможных положениях. В монозамещенных фенильных остатках заместитель может быть расположен в положении-2, положении-3 или положении-4. В двузамещенных фенильных остатках заместители могут быть расположены в положении 2, 3, положении 2, 4, положении 2, 5, положении 2, 6, положении 3, 4 или положении 3, 5. Если фенильный радикал несет три заместителя, они могут быть расположены в положении 2, 3, 4, положении 2, 3, 5, положении 2, 3, 6, положении 2, 4, 5, положении 2, 4, 6 или положении 3, 4, 5. Если фенильный радикал несет другой фенильный остаток в качестве заместителя, этот второй фенильный остаток может также быть незамещенным или может быть замещен заместителями, которые приведены для первого фенильного остатка (помимо фенильного остатка).
Термин "гетероарил" понимается как означающий остатки моноциклических или бициклических ароматических кольцевых систем, которые в случае моноциклических систем имеют 5-членное кольцо или 6-членное кольцо, а в случае бициклических систем имеют два конденсированных 5-членных кольца, 6-членное кольцо, конденсированное с 5-членным кольцом или два конденсированных 6-членных кольца. Гетероарильные остатки могут быть представлены как остатки, производимые из циклопентадиенила, фенила, пенталенила, инденила или нафтила путем замены одной или двух групп СН и/или групп CH2 на S, О, N, NH (или на атом N, несущий заместитель, такой, например, как N-СН3), где сохранена ароматическая кольцевая система или образована кольцевая ароматическая система. В дополнение к одному или двум гетероатомам кольца они могут содержать от трех до девяти кольцевых углеродных атомов. Примерами гетероарилов являются, в частности, фурил, тиенил, пирролил, имидазолил, пиразолил, 1,3-оксазолил, 1,2-оксазолил, 1,3-тиазолил, 1,2-тиазолил, пиридил, пиразинил, пиримидил, пиридазинил, индолил, бензофуранил, хинолил, изохинолил или бензопиранил. Гетероарильный остаток может быть присоединен через любой подходящий атом углерода. Например, тиенильный остаток может быть представлен как 2-тиенильный остаток или 3-тиенильный остаток, фурильный остаток - как 2-фурильный остаток или 3-фурильный остаток, пиридильный остаток - как 2-пиридильный остаток, 3-пиридильный остаток или 4-пиридильный остаток. Остаток, который происходит от 1,3-тиазола или от имидазола, может быть присоединен по 2-положению, 4-положению или 5-положению. Подходящие азотные гетероциклы могут быть также представлены как N-оксиды или четвертичные соли, имеющие анион, происходящий от физиологически переносимой кислоты, в качестве противоиона. Пиридильные остатки могут быть представлены, в частности, в виде N-оксидов пиридина.
Если в насыщенном 4-7-членном гетероцикле, содержащем один или два атома кислорода в качестве гетероатомов кольца, присутствуют два кольцевых атома кислорода, то они не связаны непосредственно друг с другом, а между ними размещен по меньшей мере один атом углерода. Примерами насыщенных 4-7-членных гетероциклов, содержащих один или два атома кислорода в качестве гетероатомов кольца, являются оксетан, тетрагидрофуран, тетрагидропиран, оксепан, 1,3-диоксалан или 1,4-диоксан. Предпочтительными гетероциклами являются те, которые содержат один кольцевой атом кислорода. Особо предпочтительными гетероциклами являются тетрагидрофуран и тетрагидропиран. Насыщенные кислородные гетероциклы могут быть присоединены по любому углеродному атому кольца, например, оксетан по положению-2 или положению-3, тетрагидрофуран по положению-2 или положению-3, тетрагидропиран по положению-2, положению-3 или положению-4, 1,3-диоксалан по положению-2 или положению-4. Тетрагидрофуран и тетрагидропиран предпочтительно присоединены по положению-2.
Настоящее изобретение включает все стереоизомерные формы соединений формулы I. Все асимметричные центры, присутствующие в соединениях формулы I, могут независимо друг от друга иметь S конфигурацию или R-конфигурацию, или соединения могут быть представлены как смесь R/S по отношению к любому из асимметричных центров. Изобретение включает все возможные энантиомеры и диастереомеры, а также все смеси двух или нескольких стереоизомерных форм, например, смеси энантиомеров и/или диастереомеров во всех соотношениях. Таким образом, энантиомеры, например, являются предметом изобретения в энантиомерно чистой форме в виде как левовращающих, так и правовращающих антиподов, в форме рацематов и в форме смесей двух энантиомеров во всех соотношениях. При наличии цис/транс изомерии (или E/Z изомерии) предметом изобретения являются и цис-форма, и транс-форма, и смеси этих форм во всех соотношениях. Получение индивидуальных стереоизомеров может быть осуществлено, если требуется, разделением смеси общепринятыми способами, например, хроматографией или кристаллизацией, или с использованием в синтезе стереохимически однородных исходных веществ, или путем стереоселективных реакций. Если целесообразно, дериватизация или образование соли могут быть осуществлены перед разделением стереоизомеров. Разделение смеси стереоизомеров может быть осуществлено на стадии соединений формулы I, или на стадии промежуточных соединений в ходе синтеза. Изобретение включает также все таутомерные формы соединений формулы I.
Физиологически переносимые соли соединений формулы I представляют собой, в частности, нетоксичные соли или фармацевтически применяемые соли. Они могут содержать неорганические или органические солевые компоненты. Такие соли могут быть получены, например, из соединений формулы I, которые содержат одну или несколько кислотных групп, и нетоксичных неорганических или органических оснований.
Возможными основаниями являются, например, подходящие соединения щелочных металлов или щелочноземельных металлов, такие как гидроксид натрия или гидроксид калия, или аммиак, или органические аминосоединения, или гидроксиды четвертичного аммония. Реакции соединений формулы I с основаниями для получения солей обычно проводят в растворителе или разбавителе по общепринятым методикам. С точки зрения физиологической и химической стабильности предпочтительными солями при наличии кислотных групп во многих случаях являются соли натрия, калия, магния или кальция, или соли аммония, которые могут нести один или несколько органических остатков на атоме азота. Образование солей по атому азота бензолсульфонамидной группы ведет к соединениям формулы II:
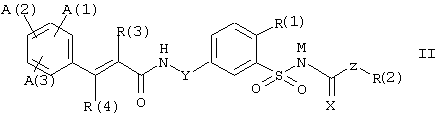
в которой А(1), А(2), А{3), R(1), R(2), R(3), R(4), X, Y и Z имеют значения, указанные выше, а катион М, например, является ионом щелочного металла или, эквивалентно, ионом щелочноземельного металла, например, ионом натрия, калия, магния или кальция, или незамещенным ионом аммония, или ионом аммония, имеющим один или несколько органических остатков. Ион аммония, который представляет М, может также быть, например, катионом, который получен из аминокислоты путем протонирования, в частности, из основной аминокислоты, такой как, например, лизин или аргинин.
Соединения формулы I, которые содержат одну или несколько протоноспособных групп, могут быть представлены и использоваться по изобретению в форме своих солей присоединения кислот с физиологически переносимыми неорганическими или органическими кислотами, например, в виде солей с хлористым водородом, фосфорной кислотой, серной кислотой, или с органическими карбоновыми кислотами или сульфокислотами, такими как, например, п-толуилсульфокислота, уксусная кислота, винная кислота, бензойная кислота, фумаровая кислота, малеиновая кислота, лимонная кислота, и т.д. Соли присоединения кислот могут быть также получены из соединений формулы I общепринятыми способами, известными специалистам, например, сочетанием с органической или неорганической кислотой в растворителе или разбавителе. Если соединение формулы I содержит в молекуле одновременно кислотные и основные группы, настоящее изобретение включает, в дополнение к описанным формам солей, также внутренние соли или бетаины (цвиттер-ионы). Настоящее изобретение включает также все соли соединений формулы I, которые из-за их низкой физиологической переносимости непригодны для непосредственного применения в фармацевтических препаратах, но пригодны, например, для использования в качестве промежуточных соединений для химических реакций или для получения физиологически переносимых солей путем, например, анионного обмена или катионного обмена.
Настоящее изобретение включает, кроме того, все сольваты соединений формулы I, например, гидраты или аддукты со спиртами, а также производные соединений формулы 1, такие как, например, сложные эфиры и амиды кислотных групп, и пролекарства и активные метаболиты соединений формулы I.
В соединениях формулы I X предпочтительно представляет кислород или серу. Особо предпочтительная группа соединений образована теми соединениями, в которых Х представляет серу и Z представляет NH. В соединениях формулы I, в которых Z представляет кислород, Х наиболее предпочтительно представляет кислород. Особо предпочтительная группа соединений формулы I образована также теми соединениями, в которых Х представляет кислород и одновременно R(4) представляет водород или (C1-C4)алкил, где в особо предпочтительной подгруппе этих соединений R(2) представляет метил.
Y предпочтительно представляет остаток -(CR(5)2)n-, в котором остатки R(5) представляют водород или метил, особо предпочтительно, водород. Величина n предпочтительно составляет 2 или 3, особо предпочтительно 2. Особо предпочтительной группой Y является группа –CH2-CH2-.
Z предпочтительно представляет NH, т.е. предпочтительными соединениями формулы I являются производные бензолсульфонамида формулы Iа:
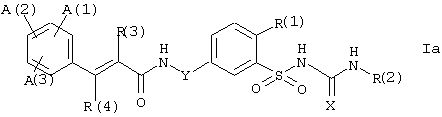
в которой А(1), А(2), А(3), R(1), R(2), R(3), R(4), X, Y и Z имеют значения, указанные выше, во всех своих стереоизомерных формах и их смесей во всех соотношениях, и их физиологически приемлемые соли. Особо предпочтительными соединениями формулы I являются те соединения, в которых Х представляет кислород или серу, т.е. соединения, которые являются производными бензолсульфонмочевины или производными бензолсульфонтиомочевины.
Остатки А(1), А(2) и А(3) могут быть расположены в любом желаемом положении в фенильном кольце, к которому они прикреплены, как было объяснено выше по отношению к заместителям в фенильных остатках. Если одним из остатков А(1), А(2) и А(3) является водород, а два других имеют значения, отличные от водорода, два отличных от водорода остатка находятся предпочтительно в положении 2,4. Положения в фенильном кольце, к которым не прикреплен ни один из остатков А(1), А(2) и А(3), занимают атомы водорода. Предпочтительно, одним из остатков А(1), А(2) и А(3) является водород, а два других являются одинаковыми или разными остатками из группы, состоящей из водорода, галогена, (С1-С4)-алкила, (C1-C4)-алкокси, метилендиокси, формила и трифторметила, т.е. фенильный остаток, несущий остатки А(1), А(2) и А(3), является предпочтительно незамещенным или замещенным одним или двумя одинаковыми или различными заместителями. Особо предпочтительно, одним из остатков А(1), А(2) и А(3) является водород, одним из остатков А(1), А(2) и А(3) является водород, галоген, (С1-С4)-алкил, (С1-С4)-алкокси, метилендиокси, формил или трифторметил, и еще одним из остатков А(1), А(2) и А(3) является водород, галоген, (С1-С4)-алкил, (С1-С4)-алкокси, метилендиокси, формил или трифторметил, т.е. фенильный остаток, несущий остатки А(1), А(2) и А(3), особо предпочтительно представляет собой замещенный фенильный остаток, который несет один или два одинаковых или разных заместителя. Если остатки А(1), А(2) и А(3) имеют значения, отличные от водорода, они предпочтительно представляют собой одинаковые или разные остатки из группы, состоящей из галогена, (С1-С4)-алкила, (С1-С4)-алкокси, метилендиокси, и трифторметила, в частности, одинаковые или различные остатки из группы, состоящей из галогена, (С1-С4)-алкила, (C1-C4)-алкокси и трифторметила. Наиболее предпочтительно остатки А(1), А(2) и А(3) являются одинаковыми или разными остатками из группы, состоящей из водорода, метила, метокси, этокси, фтора, хлора и трифторметила. В особенно предпочтительном осуществлении фенильный остаток, несущий остатки А(1), А (2) и А(3), представляет собой замещенный фенильный остаток, который несет один или два одинаковых или разных заместителя из группы, состоящей из метила, метокси, этокси, фтора, хлора и трифторметила. Еще более предпочтительно, когда фенильный остаток, несущий остатки А(1), А(2) и А(3), представляет собой 2,4-диметоксифенильный остаток.
Остаток (С1-С4)-алкил, представляющий R(1), предпочтительно является одним из остатков метил, этил и иэопропил. Остаток (С1-С4)-алкокси, представляющий R(1), предпочтительно является одним из остатков метокси или этокси, предпочтительно, метокси.
В остатке -O-(С1-С4)-алкил-Е(1)-(С1-С4)-алкил-D(1), представляющем остаток R(1), группы Е (1), Е(2) и Е(3), которые могут присутствовать в нем, предпочтительно представляют кислород. D(1) предпочтительно представляет водород. Если D(1) имеет значения, отличные от водорода, D(2) предпочтительно представляет водород. Предпочтительными значениями остатка -O-(С1-С4)-алкил-Е(1)(С1-С4)-алкил-D(1) являются -O-(С1-С4)-алкил-O-(С1-С4)-алкил и -O-(С1-С4)-алкил-O-(С1-С4)-алкил-O-(С1-С4)-алкил, особо предпочтительным значением является -O-(C1-C4)-алкил-O-(С1-С4)-алкил. Наиболее предпочтительными значениями остатка -O-(С1-С4)-алкил-Е(1)-(С1-С4)-алкил-D(1) являются 2-метоксиэтокси 2-(2-метоксиэтокси)этокси-, в особенности 2-метоксиэтокси.
Остаток -О(С1-С4)-алкил, представляющий R(1), который замещен остатком кислородного гетероцикла, представляет предпочтительно один из остатков тетрагидрофуран-2-илметокси и тетрагидропиран-2-илметокси. Остатком -О(С2-С4)-алкенил, представляющим R(1), предпочтительно является аллилокси. Остатком -О(C1-C4)-алкилфенил, представляющим R(1), предпочтительно является бензилокси. Остатком -O-фенил, представляющим R(1), предпочтительно является незамещенный или монозамещенный фенокси, особенно предпочтительно незамещенный фенокси или фенокси, замещенный в положение-4, в частности незамещенный фенокси, 4-метилфенокси, 4-метоксифенокси, 4-фторфенокси или 4-трифторметилфенокси. Присутствующим в R(1) галогеном предпочтительно является бром или иод.
Фенильным остатком, представляющим R(1), предпочтительно является незамещенный или монозамещенный фенил, особо предпочтительно, незамещенный фенил или фенил, замещенный в положение-4, в частности незамещенный фенил, 4-метилфенил, 4-метоксифенил, 4-фторфенил или 4-трифторметилфенил, в особенности незамещенный фенил. Остатком (С2-С5)-алкенил, представляющим R(1), предпочтительно является аллил. Остатком (С2-С5)-алкинил, представляющим R(1), предпочтительно является этинил. Гетероарильный остаток, представляющий R(1), предпочтительно содержит один гетероатом и предпочтительно представляет моноциклический остаток, особенно предпочтительно, пиридильный остаток, тиенильный остаток или фурильный остаток, в частности, один из остатков 2-пиридил, 3-пиридил, 2-тиенил и 2-фурил, в особенности 2-фурил.
Остаток -S(Оm)-фенил, представляющий R(1), предпочтительно представляет незамещенный или монозамещенный -S(Оm)-фенил, особенно предпочтительно, незамещенный -S(Оm)-фенил, и в особенности незамещенный остаток -S-фенил. Остатком -S(O)m-(С1-С4)-алкил, который представляет R(1), предпочтительно является -S(Оm)-метил, в частности, -S-метил.
Значение m предпочтительно равно 0 или 2, особо предпочтительно равно 0.
R(1) предпочтительно представляет:
1) метил, этил или изопропил; или
2) метокси или этокси; или
3) 2-метоксиэтокси; или
4) тетрагидрофуран-2-илметокси или тетрагидропиран-2-ил-метокси; или
5) аллилокси; или
6) бензилокси; или
7) фенокси, 4-метилфенокси, 4-метоксифенокси, 4-фторфенокси или 4-трифторметилфенокси; или
8) бром или иод; или
9) фенил, 4-метилфенил, 4-метоксифенил, 4-фторфенил или 4-трифторметилфенил; или
10) аллил; или
11) этинил; или
12) пиридил, фурил или тиенил; или
13) -S-фенил; или
14) -S-метил.
Особенно предпочтительно, R(1) представляет один из остатков, упомянутых в общем или в предпочтительном определении R(1), которые присоединены к бензольному кольцу, несущему группу R(1) через атом кислорода, или необязательно замещенный фенильный остаток или гетероарильный остаток. Весьма предпочтительно, R(1) представляет один из остатков метокси, 2-метоксиэтокси-, тетрагидрофуран-2-илметокси-, тетрагидро-пиран-2-илметокси-, аллилокси, бензилокси и фенокси, наиболее предпочтительно, один из остатков метокси, 2-метоксиэтокси.
Если Z представляет NH, R(2) предпочтительно представляет водород, (С1-С4)-алкил или (С3-С6)-циклоалкил, особенно предпочтительно водород, метил, этил, изопропил или циклогексил. Группа наиболее предпочтительных соединений формулы I, в которых Z представляет NH, образована соединениями, в которых R(2) представляет водород или метил, другая группа образована соединениями, в которых R(2) представляет метил, этил, изопропил или циклогексил. Если Z представляет кислород, R(2) предпочтительно представляет (C1-С4)-алкил. Наиболее предпочтительным значением R(2) является метил.
R(3) предпочтительно представляет водород, метил или незамещенный фенил, особо предпочтительно водород. R(4) предпочтительно представляет водород.
Предпочтительными соединениями формулы I являются те, в которых один или несколько из содержащихся остатков имеют предпочтительные значения, где все сочетания предпочтительных значений заместителей являются предметом настоящего изобретения. Кроме того, в том, что касается всех предпочтительных соединений формулы I, то настоящее изобретение включает все их стереоизомерные формы и их смеси во всех соотношениях и их физиологически переносимые соли. Кроме того, из предпочтительных соединений, которые являются предметом настоящего изобретения как таковые, исключены те соединения, которые исключены выше заявителем из общего определения соединений формулы I.
Так например, группа предпочтительных соединений образована теми соединениями формулы I, в которых Z представляет NH, Х представляет серу и R(2) представляет метил, а другие остатки имеют указанные выше общие или предпочтительные значения, во всех их стереоизомерных формах и их смесях во всех соотношениях, и их физиологически переносимыми солями.
Группа предпочтительных соединений формулы I образована также теми соединениями формулы I, в которых
Y представляет -СН2-СН2-;
один из остатков А(1), А(2) и А(3) представляет водород, а два других являются одинаковыми или разными остатками из группы, состоящей из водорода, метила, метокси, этокси, фтора, хлора и трифторметила;
R(2) представляет метил, этил, изопропил или циклогексил;
R(3) и R(4) представляют водород;
и R(1), X и Z имеют общие или предпочтительные значения, указанные выше, во всех своих стереоизомерных формах и их смесях во всех соотношениях, и их физиологически переносимыми солями. Особо предпочтительные подгруппы этих соединений образованы соединениями формулы I, в которых Z представляет NH и/или Х представляет серу. Наиболее предпочтительная подгруппа образована соединениями формулы I, в которых R(2) представляет метил.
Группа наиболее предпочтительных соединений образована, например, соединениями формулы Ib:
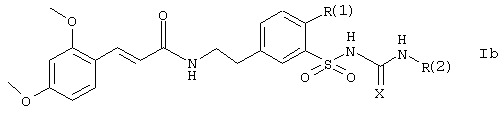
в которой:
Х представляет кислород или серу;
R(1) представляет метокси, 2-метоксиэтокси-, тетрагидрофуран-2-илметокси, тетрагидропиран-2-илметокси-, аллилокси, бензилокси или фенокси;
R(2) представляет метил, этил, изопропил или циклогексил;
во всех своих стереоизомерных формах и их смесях во всех соотношениях, и их физиологически переносимыми солями. Предпочтительным значением R(2) в соединениях формулы Ib является метил. Предпочтительно, остатком Х в соединениях формулы Ib является сера. Таким образом, группа наиболее предпочтительных соединений образована соединениями формулы Ib, в которых Х представляет серу;
R(1) представляет метокси, 2-метоксиэтокси-, тетрагидрофуран-2-илметокси, тетрагидропиран-2-илметокси-, аллилокси, бензилокси или фенокси;
R(2) представляет метил, этил, изопропил или циклогексил;
во всех своих стереоизомерных формах и их смесях во всех соотношениях, и их физиологически переносимыми солями, где кроме того, во всех таких соединениях R(2) предпочтительно представляет метил.
Настоящее изобретение относится также к способам получения соединений формулы I, которые изложены ниже и по которым можно получить соединения по изобретению.
Соединения формулы I, в которых Х представляет серу и Z представляет NH, т.е. бензолсульфонилтиомочевины формулы Iс:
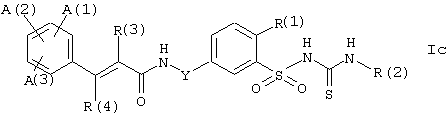
где А(1), А(2), А(3), R(1), R(2), R(3), R(4) и Y имеют вышеупомянутые значения, могут быть получены, например, реакцией бензолсульфонамида формулы III
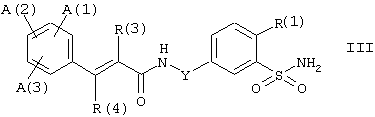
где А(1), А(2), А(3), R(1), R(2), R(3), R(4) и Y имеют вышеупомянутые значения, в инертном растворителе или разбавителе с основанием и с R(2)-замещенным изотиоцианатом формулы IV
R(2)-N=C=S, IV
где R(2) имеет значение, указанное выше. Подходящими основаниями являются, например, гидроксиды щелочных металлов или щелочноземельных металлов, гидриды, амиды или алкоголяты, такие как гидроксид натрия, гидроксид калия, гидроксид кальция, гидрид натрия, гидрид калия, гидрид кальция, амид натрия, амид калия, метилат натрия, этилат натрия, трет-бутилат калия, или гидроксиды четвертичного аммония. Реакцию соединения формулы III с основанием можно вначале провести в отдельную стадию, и первоначально образующуюся соль формулы V
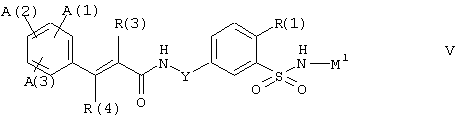
где А(1), А(2), А(3), R(1), R(2), R(3), R(4) и Y имеют вышеупомянутые значения, а М' является ионом щелочного металла, например, натрия или калия, или эквивалентом иона щелочноземельного металла, например, магния или кальция, или ионом аммония, который является инертным в условиях реакции, например, ионом четвертичного аммония, можно, если это требуется, также выделить в виде промежуточного соединения. Однако может быть также особенно выгодно, чтобы соль формулы V была получена in situ из соединения формулы III и напрямую реагировала с изотиоцианатом формулы IV. Подходящими инертными растворителями для реакции являются, например, простые эфиры, такие как тетрагидрофуран (ТГФ), диоксан, диметиловый эфир этиленгликоля (ДМЭ) или диглим, кетоны, такие как ацетон или бутанон, нитрилы, такие как ацетонитрил, нитросоединения, такие как нитрометан, сложные эфиры, такие как этилацетат, амиды, такие как диметилформамид (ДМФА) или N-метилпирролидон (N-МП), гексаметилфосфортриамид (ГМФТ), сульфоксиды, такие как диметилсульфоксид (ДМСО) или углеводороды, такие как бензол, толуол или ксилолы. Кроме того, пригодными являются смеси этих растворителей друг с другом. Реакцию соединений формулы III и/или V с соединением формулы IV обычно проводят при температурах от комнатной температуры до 150°С.
Соединения формулы I, в которых Х представляет кислород и Z представляет NH, т.е. бензолсульфонилмочевины формулы Id:
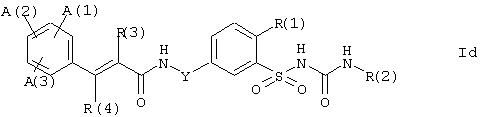
где А(1), А(2), А(3), R(1), R(2), R(3), R(4) и Y имеют вышеупомянутые значения, могут быть получены, например, аналогично описанному выше синтезу производных тиомочевины формулы Iс, реакцией бензолсульфонамидов формулы III и/или их солей формулы V в инертном растворителе или разбавителе с основанием и R(2)-замещенным изоцианатами формулы VI
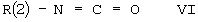
где R(2) имеет значения, указанные выше. Приведенные выше объяснения для реакции с изотиоцианатами соответствующим образом применимы для реакции с изоцианатами.
Бензолсульфонилмочевины формулы Id могут быть также получены из бензолсульфонамидов формулы III и/или их солей формулы V реакцией с R (2)-замещенными 2,2,2-трихлорацетамидами формулы VII:
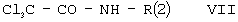
где R(2) имеет значения, указанные выше, в присутствии основания в инертном высококипящем растворителе, таком как, например, ДМСО.
Бензолсульфонилмочевины формулы Id могут быть также получены из соответствующих бензолсульфонилтиомочевин формулы Iс реакцией превращения (десульфуризации). Замену атома серы в тиомочевинной группе соединений формулы Iс на атом кислорода можно осуществить, например, с помощью оксидов или солей тяжелых металлов или с использованием окислителей, таких как перекись водорода, перекись натрия или азотистая кислота.
Бензолсульфонилмочевины и -тиомочевины формул Id и Iс могут быть также получены реакцией аминов формулы R(2)-NH2 с бензолсульфонилизоцианатами и иэотиоцианатами формулы VIII:
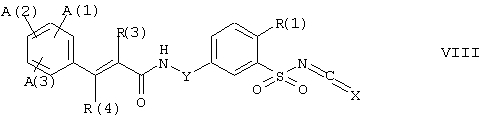
где А(1), А(2), А(3), R(1), R(2), R(3), R(4) и Y имеют вышеупомянутые значения и Х представляет кислород или серу. Сульфонилизоцианаты формулы VIII (Х=кислород) могут быть получены из бензолсульфонамидов формулы III по общепринятым способам, например, с использованием фосгена. Сульфонилизо-тиоцианаты формулы VIII (Х=сера) могут быть получены реакцией сульфонамида формулы III с гидроксидами щелочных металлов и дисульфидом углерода в органическом растворителе, таком как ДМФА, ДМСО или N-МП. Полученная в этом случае двухатомная соль сульфонилдитиокарбаминовой кислоты со щелочным металлом может быть введена в реакцию в инертном растворителе с небольшим избытком фосгена или заместителя фосгена, такого как трифосген, или с эфиром хлормуравьиной кислоты (2 эквивалента), или с тионилхлоридом. Полученный раствор сульфонилизо(тио)цианата формулы VIII может быть напрямую введен в реакцию с подходящим замещенным амином формулы R(2)-NH2 или, если должны быть получены соединения формулы I, в которых R(2) представляет водород, с аммиаком.
Соответственно, исходя из бензолсульфонилизо(тио)цианатов формулы VIII, посредством присоединения спиртов формулы R(2)-ОН могут быть получены соединения формулы I, в которых Z представляет кислород, т.е. производные бензолсульфонилуретана формулы Iе:
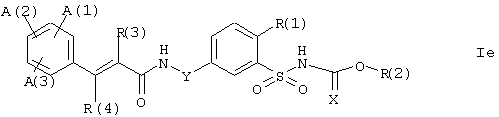
где А(1), А(2), А(3), R(1), R(2), R(3), R(4) и Y имеют вышеупомянутые значения, но, как указывалось, R(2) не является водородом и Х представляет кислород или серу. Соединения формулы Iе могут быть также получены, например, аналогично описанному выше синтезу, реакцией бензолсульфонамидов формулы III и/или их солей формулы V в инертном растворителе, например, высококипящем простом эфире, с реакционноспособными производными угольной кислоты, например, с эфирами хлормуравьиной кислоты формулы Cl-CO-OR(2) или диэфирами пироугольной кислоты формулы (R(2)O-C(=O))2O. Исходя из соединений формулы Iе, в которых Х представляет кислород, могут быть получены соединения формулы Id путем реакции с подходящим амином формулы R(2)-NH2 в инертном высококипящем растворителе, например, толуоле, при температурах до температуры кипения соответствующего растворителя.
Соединения формулы I, в которых Х представляет цианоиминную группу =N-CN, могут быть получены, например, путем реакции дифенил-N-цианоиминокарбонатов формулы NC-N=C(O-C6H5)2 с бензолсульфонамидом формулы III и/или его солью формулы V в присутствии основания и последующей реакции полученной в качестве промежуточного соединения N-циано-О-фенилбензолсульфонилизомочевины с амином формулы R(2)-NH2.
Бензолсульфонамиды формулы III в качестве исходных соединений для вышеупомянутых способов синтеза бензол-сульфонил(тио)мочевин могут быть получены в соответствии или по аналогии с известными методами, описанными в литературе, например, в стандартных справочниках, таких как Houben-Weyl, Methoden der Organischen Chemie [Методы органической химии], Georg Thieme Verlag, Stuttgart и Organic Reactions, John Wiley Sons, Inc., New York, а также в указанной выше патентной литературе, если требуется, с необходимой корректировкой условий реакции, которая хорошо известна специалистам. Могут быть использованы также варианты синтеза, которые сами по себе известны, но не упомянуты здесь более подробно. В ходе синтезов может потребоваться временно блокировать функциональные группы, которые могли бы реагировать нежелательным образом или дать начало побочным реакциям, защитными группами или применить их в форме предшествующих групп, которые позже превращаются в нужные группы. Стратегии такого типа известны специалистам. Исходные вещества, если требуется, могут также быть образованы in situ таким образом, чтобы они не выделялись из реакционной смеси, а немедленно реагировали дальше.
Так, например, п-замещенные производные бензола формулы IX
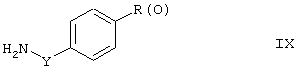
где Y имеет вышеуказанные значения, a R(O) представляет, например, (С1-С4)-алкил, (С1-С4)-алкокси, бром или нитро, могут быть введены в реакцию с трифторуксусным ангидридом в присутствии пиридина в инертном растворителе, таком как ТГФ, с получением соединений формулы X:
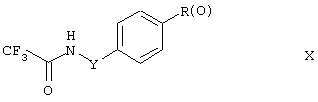
где Y и R(O) имеют значения, указанные выше.
Исходя из соединений формулы X, в которых R(O) представляет нитро, можно посредством восстановления нитро-группы с использованием восстановителя, такого как, например, SnCl2×2H2O, в инертном растворителе, таком как этилацетат, диазотирования образующейся амино-группы и последующей реакции промежуточного диазосоединения известными способами, такими как, например, описанные в Larock, Comprehensive Organic Transformations, VCH, 1989, например, путем реакции с иодидом калия для получения иодсодержащих соединений, получить соответствующие п-галогензамещенные соединения формулы XI:
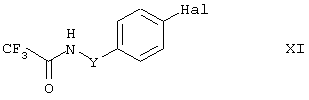
где Y имеет значение, указанное выше, a Hal представляет галоген.
Соединения формулы XI и соединения формулы X, в которых R(O) представляет (С1-С4)-алкил, (С1-С4)-алкокси или бром, которые обобщенно обозначены как соединения формулы XII:
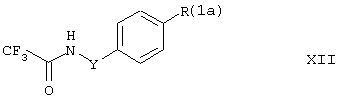
где Y имеет значение, указанное выше, a R(1a) представляет (С1-С4)-алкил, (C1-C4)-алкокси или галоген, могут быть превращены известным самим по себе способом в бензолсульфонамиды формулы XIII:
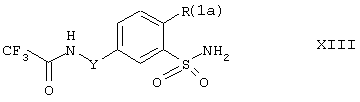
где Y и R(1a) имеют значения, указанные выше. Сульфонамиды формулы XIII могут быть получены из соединений формулы XII в одну, две или более стадий. В частности, предпочтительны способы, в которых ациламины формулы XII вначале превращают в 2,5-замещенные бензолсульфоновые кислоты или их производные, такие как, например, сульфонилгалогениды, электрофильными реагентами в присутствии или в отсутствие инертных растворителей при температурах от -20° С до 120°С, предпочтительно от 0° С до 100° С. Для этого можно, например, провести сульфонирование с серной кислотой или олеумом, галосульфонирование с галогеносульфоновыми кислотами, такими как хлоросульфоновая кислота, реакции с сульфурилгалогенидами в присутствии безводных галогенидов металлов с последующим окислением, проводимым известным способом для получения сульфонилхлоридов. Если первичными реакционными продуктами являются сульфоновые кислоты, они могут быть либо непосредственно превращены в галогенангидриды сульфоновых кислот известным способом посредством галогенидов кислот, таких как, например, тригалогениды фосфора, пентагалогениды фосфора, тионилгалогениды или оксалилгалогениды, или после обработки аминами, такими как, например, триэтиламин или пиридин, или гидроксидами щелочных металлов или щелочноземельных металлов, или реагентами, которые образуют такие основные соединения in situ. Производные сульфоновых кислот превращают в сульфонамиды формулы XIII известными из литературы способами. Предпочтительно, хлориды сульфоновых кислот вводят в реакцию с водным аммиаком в присутствии инертного растворителя, такого как, например, ацетон, при температурах от 0° С до 100° С.
Для получения соединений формулы I, в которых R(1) представляет (С1-С4)-алкил, (С1-С4)-алкокси или галоген, соединения формулы XIII могут быть превращены путем обработки кислотой, такой как, например, хлористоводородная кислота или серная кислота, если требуется, с добавлением полярного органического растворителя, такого как метанол или этанол, при температурах от 0° С до температуры кипения растворителя, в соединения формулы XIV:
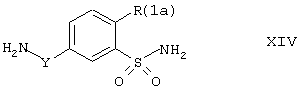
где R(1a) представляет (С1-С4)-алкил, (С2-С4)-алкокси или галоген, a Y имеет значение, указанное выше. Для получения соединений формулы I, в которых R(1) обозначает вышеупомянутые остатки, сульфонамидная группа подходящих соединений формулы XIII может быть сперва временно защищена превращением в N-(N,N-диметиламинометилен)сульфонамидную группу. Например, исходя из соединений формулы XIII, могут быть получены диметиламинометиленовые соединения формулы XV:
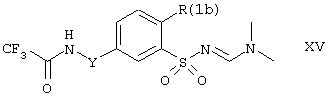
где Y имеет значения, указанные выше, a R(1b) представляет (C1-C4)-алкокси, бром или иод, посредством реакции соединений формулы XIII, например, с диметилацеталем N,N-диметилформамида или реакции с N,N-диметилформамидом в присутствии дегидратирующих агентов, таких как тионилхлорид, оксихлорид фосфора или пентахлорид фосфора.
Соединения формулы XV, в которых R(1b) представляет (C1-С4)-алкокси, могут быть затем превращены путем разложения простых эфиров до фенолов формулы XVI:
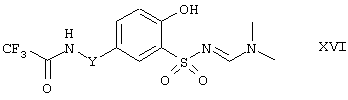
где Y имеет значения, определенные выше. Такое разложение простого эфира осуществляют, например, путем взаимодействия метоксисоединений формулы XV с кислотами или с кислотами Льюиса, такими как трифторид бора, трихлорид бора, трибромид бора или трихлорид алюминия, или с их эфиратами, предпочтительно с трибромидом бора, в инертном растворителе, таком как, например, метиленхлорид.
Полученные фенолы формулы XVI могут быть превращены в соединения формулы XVII:
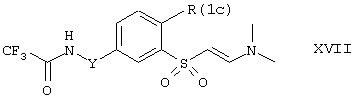
где Y имеет вышеуказанные значения, a R(1c) представляет один из остатков -О-(C1-C4)-алкил-Е(1)-(С1-С4)-алкил-D(1), -O-(C1-С4)-алкил, который замещен кислородным гетероциклом, -O-(C1-С4)-алкенил, -О(C1-C4)-алкилфенил или -O-фенил. Такое превращение осуществляют путем O-алкилирования фенолов формулы XVI, используя соответствующим образом замещенные галогенсодержащие соединения, например, иодиды или бромиды, или соответствующим образом замещенные эфиры сульфоновых кислот, такие как мезилаты, тозилаты или трифторметилсульфонаты. Так, например, при использовании 2-бромэтилметилового эфира или бензилбромида получают соединения формулы I, в которых R(1) представляет 2-метоксиэтокси- или бензилокси. O-алкилирование обычно проводят известными, как таковые, способами в присутствии основания в инертном растворителе при температурах от 0° С до температуры кипения растворителя. Получение соединений формулы XVII, в которых R(1c) представляет O-фенил, осуществляют путем O-арилирования фенолов формулы XVI, используя фенилбороновые кислоты, например, фенилбороновую кислоту, или замещенные фенилбороновые кислоты, такие как 4-метоксифенилбороновая кислота, в присутствии медных катализаторов, например, ацетата меди(II), аналогично, например, реакции, описанной в Tetrahedron Lett. 39 (1998), 2973.
Исходя из соединений формулы XV, в которых R(1b) представляет бром или иод, можно получить соединения формулы XVIII:
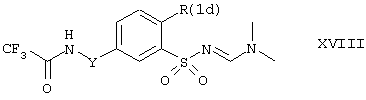
где Y имеет вышеуказанные значения, a R(1d) представляет один из остатков (C1-C4) -алкил, фенил, (С2-С5)-алкенил, (C2-C5)-алкинил, гетероарил, -S(О)m-фенил или -S(О)m-(С1-С4)-алкил. Такое превращение в соединения формулы XVIII осуществляют путем катализируемого палладием сочетания по Сузуки (Suzuki) с арилбороновыми кислотами, например, фенилбороновой кислотой, 4-метоксифенилбороновой кислотой или 4-метилтиофенилбороновой кислотой, или сочетания по Штилле (Stille) с триалкилстаннанами, например, трибутилстаннилфураном, триметилстаннилпиридином или этинилтрибутилстаннаном. Сочетание по Сузуки проводят в присутствии ацетата палладия(II) и трифенилфосфина или тетракис-(трифенилфосфин)палладия и основания, такого как, например, карбонат цезия или карбонат калия; соответствующие реакции описаны в литературе. Сочетание по Штилле проводят аналогично описанной в литературе методике, используя в качестве катализатора хлорид бис(трифенилфосфин)палладия (II). Получение подходящих станнанов описано, например, в Tetrahedron 49 (1993), 3325. Получение соединений формулы XVIII, в которых R(1d) представляет алкил, ведут путем Pd(0)-катализируемого сочетания Никиши-Кумада (Nikishi-Kumada) соединений формулы XV, в которых R(1b) представляет иод, с соответствующими цинкорганическими производными в присутствии 1,1'-бис-(дифенилфосфино)ферроцена, ацетата палладия (II) и иодида меди (I) в качестве катализаторов в инертном растворителе; соответствующие сочетания описаны, например, в Synlett 1996, 473.
Соединения формулы XVIII, в которых R(1d) представляет -S-фенил или -S-(С1-С4)-алкил, могут быть синтезированы аналогично литературным методикам посредством катализируемой иодидом меди (I) реакции нуклеофильного замещения из соединений формулы XV, в которых R(1b) представляет иод, при использовании натриевой соли соответствующего меркаптана. Введенная таким образом тиоэфирная группа, а также тиоэфирная группа в другом положении молекулы формулы I, могут быть окислены до сульфоксидной группы или до сульфоновой группы обычными способами, например, с использованием перкислоты, такой как м-хлорпербензойная кислота.
Последующее удаление диметиламинометиленовой группы и/или трифторацетильной группы, действующей как группа, защищающая сульфонамид, или как группа, защищающая амино, из соединений формул XVII или XVIII, соответственно, приводит затем к соответствующим соединениям, имеющим группу H2N-Y и группу H2N-SO2, которые, вместе с соединениями формулы XIV, представлены формулой XIX:
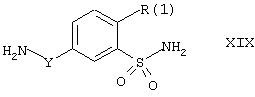
где Y и R(1) имеют значения, указанные выше для формулы I. Такое удаление защитных групп может быть осуществлено либо в основных, либо в кислых условиях. Предпочтительно его осуществляют путем взаимодействия соединений формул XVII и XVIII с кислотами, такими как, например, хлористоводородная кислота, в подходящем растворителе, например, спирте.
Затем бензолсульфонамиды формулы XIX вводят в реакцию с производными коричной кислоты для получения замещенных циннамоиламиноалкилом бензолсульфонамидов формулы III. Обычно такое ацилирование осуществляют, превращая вначале нужную коричную кислоту в реакционноспособное производное, например, реакцией коричной кислоты с карбонилбисимидазолом в инертном растворителе, таком как, например, ТГФ, диоксан или ДМФА, с последующей реакцией с амином формулы XIX, если нужно, в присутствии основания, такого как триметиламин или пиридин. Реакционноспособными производными коричной кислоты, которые могут быть использованы, являются также, например, галогенангидриды коричной кислоты или ангидриды коричной кислоты. В таком случае реакции предпочтительно ведут при температурах от 0° С до температуры кипения выбранного растворителя, особо предпочтительно, при комнатной температуре. Ацилирование аминов формулы XIX коричными кислотами можно вести также, например, в присутствии конденсирующих агентов, таких как, например, N,N’-дициклогексилкарбодиимид, тетрафторборат O-((циано(этокси-карбонил)метилен)амино)-1,1,3,3-тетраметилурония (TOTU) или гексафторфосфат 1-бензотриазолилоксипирролидинофосфония (PyВОР).
Описанные здесь стадии синтеза соединений формулы I могут быть осуществлены в другой последовательности. В зависимости от вводимых на отдельных стадиях заместителей, может быть более благоприятен тот или иной вариант. Так например, синтез соединений формулы III, в которых R(1) представляет один из остатков (C1-C4)-алкил, фенил, (C2-C5)-алкенил, (C2-C5)-алкинил, гетероарил, -S(O)m-фенил или -S(О)m(C1-C4)-алкил, может быть также осуществлен таким образом, что соединение формулы XIV, в котором R(la) представляет иод или бром, вначале путем описанного выше сочетания с производным коричной кислоты и временной защиты сульфонамидной группы превращают в соединение формулы XX:
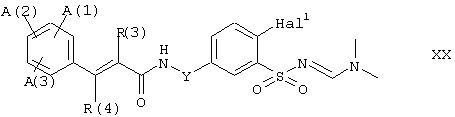
где А(1), А(2), А(3), R(1), R(2), R(3), R(4) и Y определены как для формулы I, a Hal1 представляет иод или бром. Исходя из соединения формулы XX, можно затем посредством описанных выше сочетаний Сузуки, Штилле или Никиши-Кумада с соответствующими компонентами сочетания, перечисленными выше, получить соединения формулы XXI:
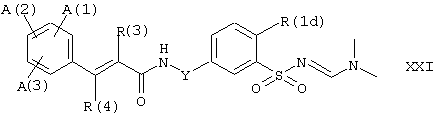
где А(1), А(2), А(3), R(1), R(2), R(3), R(4) и Y имеют значения, указанные выше. Соединения формулы XXI могут быть затем превращены в соединения формулы III путем удаления защитной группы для сульфонамида по описанной выше методике.
Соединения формулы I ингибируют АТФ-чувствительные калиевые каналы и изменяют потенциал действия клеток, в особенности, клеток сердечной мышцы. В частности, они оказывают нормализующее действие на нарушенный потенциал действия, что имеет место, например, при ишемиях, и пригодны, например, для лечения и профилактики расстройств сердечно-сосудистой системы, в частности при аритмиях и их последствиях, например, при желудочковой фибрилляции. Активность соединений формулы I может быть показана, например, на описанной ниже модели, в которой продолжительность потенциала действия определяли на папиллярной мышце морских свинок.
В дополнение к своему воздействию на АТФ-чувствительные калиевые каналы в клетках сердечной мышцы соединения формулы I оказывают также воздействие на периферическую и/или центральную автономную нервную систему. В частности, они влияют на АТФ-чувствительные калиевые каналы вагусной нервной системы и обладают стимулирующим действием на вагусную нервную систему, в особенности, стимулирующим действием на вагусную нервную систему сердца путем ингибирования АТФ-чувствительных калиевых каналов в сердечном нерве.
В идеальном случае существует оптимальное взаимодействие, приспособленное к конкретной ситуации, между вагусной (парасимпатической) нервной системой (= угнетающей нервной системой) и симпатической нервной системой (= возбуждающей нервной системой). В случае заболевания, однако, такое взаимодействие может быть нарушено, и может появиться дисфункция автономной нервной системы; т.е. может существовать дисбаланс между активностью вагусной нервной системы и активностью симпатической нервной системы. Симпатовагусный дисбаланс понимается обычно как означающий сверхактивность или гиперфункцию симпатической (= возбуждающей) нервной системы и/или ослабленную функцию или гипофункцию вагусной (= угнетающей) нервной системы, где две части нервной системы могут взаимно влиять друг на друга. В частности, известно, что гипофункция вагусной системы может вызвать гиперфункцию симпатической системы. Поэтому в таких случаях, для того, чтобы избежать повреждения клеток или органов тела из-за овершута биологических или биохимических процессов, который стимулируется слишком высокой активностью симпатической нервной системы, пытались сбалансировать симпатовагусный дисбаланс, например, восстановить нормальную вагусную активность лечением вагусной дисфункции или гипофункции.
Примерами заболеваний, при которых возможно устранение вредного симпатовагусного дисбаланса путем лечения вагусной дисфункции, являются органические сердечные заболевания, например, ишемическая болезнь сердца, сердечная недостаточность и кардиомиопатии. Опасностями для здоровья, которые возникают при дисбалансе автономной нервной системы, когда дисфункция затрагивает сердце, являются, например, ослабление сократительной способности миокарда и летальные сердечные аритмии. Роль автономной нервной системы во внезапной остановке сердца при сердечных болезнях описана, например, P.J.Schwartz (The ATRAMI prospective study: implications for risk stratification after myocardial infarction; Cardiac Electrophysiology Review 1998, 2, 38-40) или T.Kinugawa et al. (Altered vagal and sympathetic control of heart rate in left ventricular dysfunction and heart failure; Am.J.Physiol. 1995, 37, R310-316). Экспериментальные исследования с электростимуляцией сердечного вагусного нерва или стимулирующими аналогами вагусного медиатора ацетилхолина, например карбахолом, подтверждают защитное действие вагусной активации против летальных сердечных аритмий (см., например, Vanoli et al., Vagal stimulation and prevention of sudden death in conscious dogs with a healed myocardial infarction; Circ.Res. 1991, 68(5), 1471-81).
Симпатовагусный дисбаланс может также, однако, возникнуть, например, в результате метаболического расстройства, например, сахарного диабета (см., например, A.J.Burger et al., Short- and long-term reproducibility of heart rate variability in patients with long-standing type I diabetes mellitus; J.Am.Cardiol. 1997, 80, 1198-1202). Гипофункция вагусной системы может также временно возникнуть, например, в случае кислородной недостаточности, например, кислородной сердечной недостаточности, которая приводит к пониженному выделению вагусных нейромедиаторов, например, ацетилхолина.
За счет неожиданной способности соединений формулы I устранять гипофункцию вагусной нервной системы или восстанавливать нормальную вагусную активность эти соединения предоставляют действенную возможность снижать, устранять или предотвращать дисфункции автономной нервной системы, в особенности в сердце, и их последствия, такие как, например, упомянутые болезненные состояния. Эффективность соединений формулы I при устранении дисфункций автономной нервной системы, в особенности вагусной дисфункции сердца, может быть продемонстрирована, например, на описанной ниже модели вызванной хлороформом желудочной фибрилляции у мышей.
Вышеприведенные и нижеследующие утверждения, касающиеся биологического действия на АТФ-чувствительные калиевые каналы в сердце и на автономную нервную систему и применения соединений формулы I, применимы не только к соединениям, определенным выше, которые сами по себе являются предметом настоящего изобретения, но также и к соединениям формулы I, в которых одновременно Х представляет кислород, Z представляет NH, R(1) представляет галоген, (C1-C4)-алкил или -O-(C1-C4)-алкил, и R(2) представляет (С2-С6)-алкил или (С5-С7)-циклоалкил, и к их физиологически переносимым солям и пролекарствам, т.е. также к соединениям, которые исключены заявителем из вышеприведенного определения соединений, но которые также, неожиданно, обладают воздействием на автономную нервную систему, в частности на сердце, и могут устранять вагусную дисфункцию. Если не указано иное, во всех вышеприведенных и нижеследующих утверждениях, касающихся биологического действия и применения соединения формулы I, следует определенно понимать как включающие также соединения, исключенные выше заявителем. Вышеприведенные объяснения, касающиеся соединений как таковых, например, касающиеся предпочтительных значений остатков, применимы, соответственно, ко всем соединениям формулы I, как они понимаются здесь. Как особенно предпочтительные группы соединений по отношению к их биологическому действию и применению, кроме соединений формулы I, включая те, в которых одновременно Х представляет кислород, Z представляет NH, R(1) представляет галоген, (C1-C4)-алкил или -О-(C1-C4)-алкил и R(2) представляет (C2-C6)-алкил или (C5-С7)-циклоалкил, и их физиологически переносимых солей, могут быть упомянуты здесь те, в которых R(2) представляет (C1-С3)-алкил, в особенности метил, и/или Х представляет серу.
Соединения формулы I и их физиологически переносимые соли могут быть применены как лекарства в чистом виде, в смесях друг с другом или в форме фармацевтических препаратов для животных, предпочтительно млекопитающих, и в особенности, для человека. Млекопитающими, для которых могут применяться или испытываться соединения формулы I, являются, например, обезьяны, собаки, мыши, крысы, кролики, морские свинки, кошки и более крупные сельскохозяйственные животные, такие как, например, рогатый скот и свиньи. Поэтому изобретение относится также к соединениям формулы I без соединений, в которых одновременно Х представляет кислород, Z представляет NH, R(1) представляет галоген, (C1-C4)-алкил или -O-(C1-C4)-алкил и R(2) представляет (C2-C6)-алкил или (С5-С7)-циклоалкил и их физиологически переносимым солям и их пролекарствам для применения в качестве лекарств. Изобретения относится также к фармацевтическим препаратам (или фармацевтическим композициям), которые содержат эффективную дозу по меньшей мере одного соединения формулы I без соединений, в которых одновременно Х представляет кислород, Z представляет NH, R(1) представляет галоген, (С1-С4)-алкил или -О-(С1-С4)-алкил и R(2) представляет (С2-С6)-алкил или (С5-С7)-циклоалкил и/или его физиологически переносимой соли и/или его пролекарства в качестве активного составляющего и фармацевтически переносимый носитель, т.е. один или несколько фармацевтически безвредных наполнителей и/или добавок.
Фармацевтические препараты могут быть предназначены для энтерального или парентерального применения и обычно содержат от примерно 0,5 до 90 мас.% соединения формулы I и/или его физиологически переносимых солей. Количество активного соединения формулы I и/или его физиологически переносимых солей в фармацевтических препаратах обычно составляет от примерно 0,2 до примерно 1000 мг, предпочтительно от примерно 1 до примерно 500 мг. Фармацевтические препараты могут быть получены способами, которые, как таковые, известны специалистам. Для этого соединения формулы I и/или их физиологически переносимые соли смешивают с одним или несколькими твердыми или жидкими носителями и/или вспомогательными веществами и, если требуется, в сочетании с другими лекарствами, например, лекарствами, имеющими сердечно-сосудистую активность, такими как, например, антагонисты кальция, АСЕ-ингибиторами или β -блокаторами, и вводят в нужную дозированную форму и форму введения, которую затем используют в качестве лекарства в медицине или в ветеринарной медицине.
Подходящими носителями являются органические и неорганические вещества, которые пригодны, например, для энтерального (например, перорального или ректального) введения или для парентерального введения (например, внутривенных, внутримышечных или подкожных инъекций или инфузий) или для местного или чрескожного нанесения и не взаимодействуют нежелательным образом с соединениями формулы I. Примерами, которые могут быть упомянуты, являются вода, растительные масла, воски, спирты, такие как этанол, пропандиол или бензиловые спирты, глицерин, полиспирты, полиэтиленгликоли, полипропиленгликоли, триацетат глицерина, желатин, углеводы, такие как лактоза или крахмал, стеариновая кислота и ее соли, такие как стеарат магния, тальк, ланолин, петролатум или смеси носителей, например, смеси воды с одним или несколькими органическими растворителями, такие как смеси воды со спиртами. Для перорального и ректального введения используются, в частности, такие фармацевтические формы как таблетки, таблетки с пленочным покрытием, таблетки с сахарным покрытием, гранулы, твердые и мягкие желатиновые капсулы, свечи, растворы, предпочтительно масляные, спиртовые или водные растворы, сиропы, соки или капли, кроме того суспензии или эмульсии. Для местного применения используют, в частности, мази, кремы, пасты, лосьоны, гели, спреи, пены, аэрозоли, растворы или порошки. Растворителями, которые могут быть использованы для растворов, являются, например, вода или спирты, такие как этанол, изо-пропанол или 1,2-пропандиол, или их смеси друг с другом или с водой. Дополнительно возможными фармацевтическим формами являются, например, импланты. Соединения формулы I и их физиологически переносимые формы могут быть также лиофилизированы и полученные лиофилизаты могут использоваться, например, для получения препаратов для инъекций. Возможны также липосомальные препараты, в особенности для местного применения. Примерами вспомогательных веществ (или добавок), которые могут присутствовать в фармацевтических препаратах и которые могут быть упомянуты, являются лубриканты, консерванты, загустители, стабилизирующие агенты, разрыхлители, смачивающие агенты, агенты для достижения эффекта депо, эмульгаторы, соли (например, для изменения осмотического давления), буферные вещества, красители, вкусовые добавки и ароматизаторы. Фармацевтические препараты, если требуется, могут также содержать одно или несколько дополнительных активных соединений и/или, например, один или несколько витаминов.
Ввиду своей способности ингибировать АТФ-чувствительные калиевые каналы, в особенности в сердце, и/или уменьшать или устранять неправильную функцию вагусной нервной системы и, тем самым, вагусную дисфункцию или дисфункцию автономной нервной системы, в особенности, в сердце соединения формулы I и их физиологически переносимые соли и пролекарства являются ценными агентами для лечения и профилактики, которые пригодны не только в качестве антиаритмических средств и для контроля и профилактики последствий аритмий, но также для лечения и профилактики других сердечных заболеваний или расстройств сердечно-сосудистой системы. Примерами заболеваний такого типа, которые могут быть упомянуты, являются сердечная недостаточность, кардиомиопатии, гипертрофия сердца, ишемическая болезнь сердца, стенокардия, ишемии, вагусная дисфункция сердца, или, например, вагусная дисфункция сердца при сахарном диабете. Соединения формулы I могут быть в общем случае применены при лечении или профилактике заболеваний, которые связаны с дисфункцией автономной нервной системы, или с гипофункцией или дисфункцией вагусной нервной системы, в особенности, в сердце, или вызваны дисфункцией такого типа, или заболеваний для лечения или профилактики которых показаны увеличение или нормализация активности вагусной нервной системы. Соединения формулы I могут также применяться при дисфункциях автономной нервной системы, в частности, вагусной дисфункции сердца, которая появляется в результате метаболических расстройств, например, сахарного диабета.
Прежде всего, соединения формулы I используют как антиаритмические средства для лечения сердечных аритмий самого разного происхождения и, в особенности, для предотвращения внезапной остановки сердца из-за аритмии. Примерами аритмических расстройств сердца являются верхнежелудочковые аритмии, такие как, например, предсердная тахикардия, трепетание предсердий или пароксизмальные верхнежелудочковые аритмии, или желудочковые аритмии, такие как желудочковые экстрасистолы, но, в особенности, угрожающая жизни желудочковая тахикардия или особо опасная желудочковая фибрилляция. Они особенно подходят для тех случаев, когда аритмии являются результатом сужения коронарных сосудов, такого, которое происходит, например, при стенокардии или во время острого кардиального инфаркта или как хронический результат кардиального инфаркта. Они поэтому особо подходят для предотвращения внезапной остановки сердца у постинфарктных пациентов. Другими синдромами, в которых играют роль аритмии такого типа и/или внезапная остановка сердца из-за аритмии, являются, например, сердечная недостаточность или кардиальная гипертрофия как результат повышенного кровяного давления.
Кроме того, соединения формулы I способны положительно влиять на пониженную сократимость сердца и ослабленную сократительную способность миокарда. Это может быть снижением кардиальной сократимости, связанным с заболеванием как например, при сердечной недостаточности, но может быть также острыми случаями, такими как сердечная недостаточность как эффект шока.
В общем, соединения формулы I и их физиологически переносимые соли пригодны для улучшения сердечной функции. В особенности при трансплантации сердца, под влиянием соединений формулы I сердце может быстрее и более надежно восстановить свою работоспособность после того, как произошла операция. То же приложимо к операциям на сердце, которые требовали временной остановки сердечной активности посредством кардиоплегических решений.
Благодаря тому факту, что соединения формулы I в дополнение к их прямому воздействию на сердце, т.е. к влиянию на потенциал действия клеток сердечной мышцы, обладают также непрямым воздействием на нервную систему сердца или на части нервной системы, действующие на сердце, они могут уменьшать или предотвращать нежелательные последствия для сердца, исходящие от нервной системы или медиируемые нервной системой при наличии соответствующего болезненного состояния. Тем самым можно снизить или предотвратить последующие опасности для здоровья, такие как ослабление сократительной способности миокарда или, в некоторых случаях, летальные сердечные аритмии, такие как желудочковая фибрилляция. Благодаря устранению или снижению дисфункции автономной нервной системы соединения формулы I вызывают такой эффект, что ослабленная сократимость сердечной мышцы вновь нормализуется и больше не возникают сердечные аритмии, которые могут привести к внезапной остановке сердца. Путем выбора соединений формулы I, имеющих нужный профиль действия в отношении прямого воздействия на сердце (= прямого влияния на потенциал действия клеток сердечной мышцы и, за счет этого, прямого влияния на сократительную способность и прямого антиаритмического действия), с одной стороны, и воздействия на сердечные нервы, с другой стороны, с помощью соединений формулы I можно особо эффективным образом благоприятно влиять на сердечные заболевания. В зависимости от наличествующего синдрома может также быть выгодно применять в конкретном случае такие соединения формулы I, которые оказывают лишь относительно слабое прямое воздействие на сердце и, вследствие этого, оказывают, например, лишь относительно слабое влияние на сократительную способность сердца или на возникновение аритмий, но могут улучшить или нормализовать сократительную способность миокарда или сердечный ритм путем воздействия на автономную нервную систему.
Настоящее изобретение относится поэтому также к применению соединений формулы I, включая соединения, в которых одновременно Х представляет кислород, Z представляет NH, R(1) представляет галоген, (C1-C4)-алкил или -О(C1-C4)-алкил и R(2) представляет (С2-С6)-алкил или (С5-С7)-циклоалкил, и/или их физиологически переносимых солей и/или их пролекарств для лечения или профилактики упомянутых синдромов, и к их применению для получения фармацевтических препаратов для лечения или профилактики упомянутых синдромов, и к их применению для получения фармацевтических препаратов для лечения или профилактики упомянутых синдромов. Из соединений формулы I, в которых одновременно Х представляет кислород, Z представляет NH, R(1) представляет галоген, (C1-C4)-алкил или -O-(С1-С4)-алкил и R(2) представляет (С2-С6)-алкил или (C5-C7)-циклоалкил, предпочтительными соединениями для лечения или профилактики упомянутых синдромов и для приготовления фармацевтических препаратов для лечения или профилактики упомянутых синдромов являются те соединения, которые оказывают только слабое влияние на уровень сахара в крови.
Дозировка соединений формулы I или их физиологически переносимых солей зависит, как это принято, от обстоятельств рассматриваемого индивидуального случая иустанавливается специалистом в соответствии с общепринятыми правилами и процедурами. Она зависит, например, от вводимого соединения формулы I, его силы и продолжительности действия, от природы и тяжести индивидуального синдрома, от пола, возраста, веса и индивидуальной восприимчивости человека или животного, которых надо лечить, от того, является ли лечение острым или профилактическим, и от того, вводятся ли в добавление к соединениям формулы I другие активные соединения. Обычно в случае введения взрослому весом около 75 кг требуется доза, которая составляет от примерно 0,1 мг до примерно 100 мг на 1 кг в сутки, предпочтительно от примерно 1 мг до примерно 10 мг на 1 кг в сутки (в каждом случае в мг на кг веса тела). Ежедневная доза может вводиться в форме пероральной или парентеральной отдельной дозы или может быть разделена на несколько, например, две, три или четыре отдельные дозы. Введение можно также проводить непрерывно. В частности, если лечат острые случаи сердечных аритмий, например, в отделении интенсивной терапии, может быть предпочтительным парентеральное введение, например, инъекцией или непрерывной инфузией. Предпочтительный интервал доз в критических ситуациях составляет тогда от примерно 1 до примерно 100 мг на кг веса тела в день. Если требуется, в зависимости от индивидуальной характеристики, может оказаться необходимым изменять дозу в сторону увеличения или уменьшения от указанных доз.
Кроме использования в качестве фармацевтически активного соединения в медицине и ветеринарной медицине, соединения формулы I могут применяться также, например, в качестве вспомогательных средств при биохимических исследованиях или как инструмент научного исследования, если предполагается сравнительное воздействие на ионные каналы, или для выделения или характеристики калиевых каналов. Кроме того они могут использоваться в диагностических целях, например, в диагностике in vitro образцов клеток или образцов тканей. Соединения формулы I и их соли могут, далее, использоваться как химические промежуточные соединения для получения других фармацевтически активных соединений.
Предметом настоящего изобретения являются также некоторые циннамоиламиноалкил-замещенные бензолсульфонилмочевины как таковые, которые были исключены заявителем из определенных выше соединений формулы I, являющихся самими по себе предметом настоящего изобретения, но которые не заявлены конкретно в предшествующих патентах и которые представляют выборку из соединений, описанных в общей форме в предшествующих патентах. Таковыми являются соединения формулы If
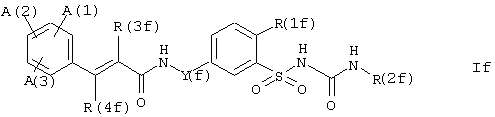
где
Y(f) представляет -(CR(5f)2)n(f)-;
остатки A(1f), A(2f) и A(3f), которые не зависят друг от друга и могут быть идентичными или различными, представляют водород, галоген, (С1-С4)-алкил, (С1-С4)-алкокси, метилендиокси, формил или трифторметил;
R(1f) представляет -О(C1-C4) -алкил;
R(2f) представляет (С2-С6)-алкил или (С5-С7)-циклоалкил;
остатки R(3f) и R(4f), которые не зависят друг от друга и могут быть идентичными или различными, представляют водород или (C1-C4)-алкил;
остатки R(5f), которые все не зависят друг от друга и могут быть идентичными или различными, представляют водород или (C1-С3)-алкил;
n(f) равно 1, 2, 3 или 4;
во всех своих стереоизомерных формах и их смесях во всех соотношениях, и их физиологически переносимые соли.
Подобно соединениям формулы I, соединения формулы If ингибируют, как уже объяснялось выше, АТФ-чувствительные калиевые каналы, в особенности в сердце, и способны уменьшать или восстанавливать дисфункцию автономной нервной системы или гипофункцию или дисфункцию вагусной нервной системы, в частности, в сердце. Все приведенные выше подробности о соединениях формулы I приложимы также к соединениям формулы If. В соединениях формулы If Y(f) предпочтительно представляет остаток –CH2-CH2-. Остатки A(1f), A(2f) и A(3f), которые не зависят друг от друга и могут быть одинаковыми или различными, предпочтительно представляют водород, галоген, (C1-C4)-алкил, (С1-С4)-алкокси или трифторметил, в частности водород, метил, хлор, фтор, метокси, этокси или трифторметил. Дополнительные указания в отношении предпочтительных значений остатков А(1), А(2) и А(3), приведенные выше, применимы, соответственно, к A(1f), A(2f) и A(3f). R(1f) предпочтительно представляет метокси или этокси, в особенности метокси. R(2f) предпочтительно представляет (С2-С3)-алкил или циклогексил, в особенности этил, изопропил или циклогексил. R(3f) и R(4f) предпочтительно представляют водород. Настоящее изобретение относится также к соединениям формулы If и их физиологически переносимым солям и пролекарствам для применения в лекарственных препаратах, а также к фармацевтическим препаратам, которые содержат эффективное количество по меньшей мере одного соединения формулы If и/или его физиологически переносимой соли и/или пролекарства и фармацевтически переносимый носитель. Все сделанные выше утверждения применимы соответствующим образом к таким фармацевтическим препаратам.
Изобретение иллюстрируется ниже примерами, не будучи ограниченным ими.
Сокращения
DCI десорбционная химическая ионизация
ДХМ дихлорметан
ЭА этилацетат
ESI ионизация электрораспылением
FAB ионизация при бомбардировке ускоренными атомами
т.пл. температура плавления
ч час(ы)
мин минута (минуты)
МС масс-спектр
КТ комнатная температура
Пример 1
1-(5-(2-(2,4-диметоксициннамоиламино)этил)-2-метоксифенилсульфонил)-3-метилтиомочевина
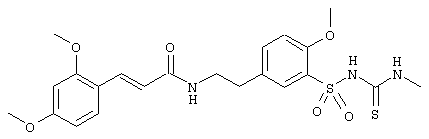
2,2,2-трифтор-N-(2-(4-метоксифенил)этил)ацетамид
32,2 мл (0,23 моль) трифторуксусного ангидрида добавляли по каплям к раствору 22,3 мл (0,15 моль) 2-(4-метоксифенил)-этиламина и 24,7 мл (0,23 моль) пиридина в 125 мл абсолютного ТГФ, охлажденному до 5° С, и полученный раствор перемешивали при КТ в течение 3 ч. Затем реакционный раствор выливали на 750 мл льда, и выпавший осадок отфильтровывали с отсосом и сушили при 40° С в глубоком вакууме. Получали 36,3 г указанного в заголовке соединения в виде твердого вещества бежевого цвета. Т.пл.: 74-77° С. Rf (SiO2, ЭА/толуол 1:4)=0,62.
MC (ESI): m/e=248 [M+H]+
b) 2-метокси-5-(2-(2,2,2-трифторацетамидо)этил)бензолсульфонамид
36,3 г (0,15 моль) соединения из примера 1а) добавляли частями к 200 мл хлорсульфоновой кислоты, и полученную смесь перемешивали при КТ в течение 2 ч. Затем реакционный раствор по каплям добавляли к примерно 1,5 л льда, и выпавший осадок отфильтровывали с отсосом. Полученный осадок растворяли в 100 мл ацетона, раствор обрабатывали 250 мл концентрированного раствора аммиака при охлаждении льдом и перемешивали в течение 45 мин. Затем реакционный раствор выливали на примерно 800 мл льда. Выпавший осадок отфильтровывали с отсосом и сушили в глубоком вакууме. Выход: 30,4 г указанного в заголовке соединения в форме бледно-желтого твердого вещества. Т.пл.: 160-161° С. Rf (SiO2, ЭА/гептан 4:1)=0,51.
MC (DCI): m/e=327 [M+H]+
с) 5-(2-аминоэтил)-2-метоксибензолсульфонамид
Раствор 30,3 г (93,0 ммоль) соединения из примера 1b) в 130 мл 2н. хлористоводородной кислоты нагревали при кипении с обратным холодильником в течение 12 ч. Выпавший осадок отфильтровывали с отсосом, растворяли в 70 мл воды и доводили рН полученного раствора примерно до 10 добавлением 2н. раствора гидроксида натрия. Эту смесь быстро нагревали до 100° С. Затем раствор охлаждали на ледяной бане и выпавший осадок отфильтровывали с отсосом и сушили в глубоком вакууме. Выход: 13,7 г указанного в заголовке соединения в форме твердого вещества бежевого цвета. Т.пл.: 180-181° С. Rf (SiO2, ЭА/гептан 4:1)=0,02.
MC (ESI): m/e=231 [M+H]+
d) 5-(2-(2,4-диметоксициннамоиламино)этил)-2-метоксибензолсульфонамид
Раствор 500 мг (2,17 ммоль) соединения из примера 1с, 452 мг (2,17 ммоль) транс-2,4-диметоксикоричной кислоты, 752 мг (2,17 ммоль) TOTU и 382 мкл (2,17 ммоль) N-этилдиизопропиламина в 50 мл абсолютного ДМФА перемешивали при КТ в течение 2 ч. Реакционный раствор концентрировали и остаток переносили в ДХМ/воду. Органическую фазу отделяли, водную фазу дважды экстрагировали ДХМ и объединенные органические фазы сушили над Na2SO4. Маслянистый остаток, оставшийся после отгонки растворителя, очищали хроматографией на SiO2, используя смесь ДХМ/ЭА в качестве элюента. Содержащие продукт фракции соединяли, растворитель отгоняли и оставшийся кристаллический остаток растирали в небольшом количестве ЭА. Осадок отфильтровывали с отсосом и сушили в глубоком вакууме. Выход: 606 мг указанного в заголовке соединения в форме белого твердого вещества. Т.пл.: 183° С. Rf (SiO2, ЭА/гептан 4:1)=0,13.
MC (DCI): m/e=421 [M+H]+
е) 1-(5-(2-(2,4-диметоксициннамоиламино)этил)-2-метокси-фенилульфонил)-3-метилтиомочевина
Раствор 600 мг (1,43 ммоль) соединения из примера Id) и 192 мг (1,71 ммоль) трет-бутилата натрия в 12 мл абсолютного ДМФ перемешивали при КТ в течение 15 мин. Добавляли 1,57 мл (1,57 ммоль) 1-молярного раствора метилизотиоцианата в абсолютном ДМФА и полученный раствор перемешивали при 80° С в течение 1 ч. Затем реакционный раствор выливали на 80 мл 1н. хлористоводородной кислоты, выпавший осадок отфильтровывали с отсосом и несколько раз промывали водой. Сушка осадка в глубоком вакууме дает 626 мг указанного в заголовке соединения в виде бледно-желтого аморфного твердого вещества. Rf (SiO2, ЭА/гептан 10:1)=0,52.
MC (DCI): m/e=494 [М+Н]+
Пример 2
1-(5-(2-(2,4-диметоксициннамоиламино)этил)-2-метоксифенилсульфонил)-3-метилмочевина
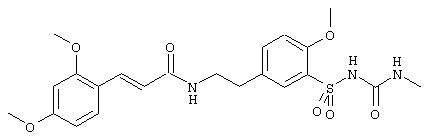
80 мг (0,16 ммоль) соединения из примера 1) растворяли в 1 мл 1н. раствора гидроксида натрия. Добавляли 150 мкл 35%-ного водного раствора Н2О2 и полученный раствор нагревали на водяной бане в течение 30 мин. Затем рН раствора доводили до 2 добавлением 2н. хлористоводородной кислоты, выпавший осадок промывали небольшим количеством воды и в конце сушили в глубоком вакууме. Получали 63 мг указанного в заголовке соединения в виде белого твердого вещества. Т.пл.: 210° С. Rf (SiO2, ЭА/гептан 4:1)=0,06.
MC (DCI): m/e=478 [M+H]+
Пример 3
1-(5-(2-(2,4-диметоксициннамоиламино)этил)-2-метоксифенилсульфонил)-3-этилтиомочевина
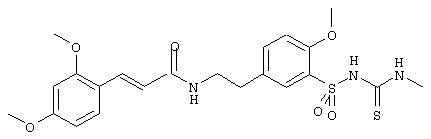
Синтез проводили согласно методике, описанной в примере 1е), причем вместо метилизотиоцианата использовали этилизотиоцианат. В данном случае из 150 мг (0,36 ммоль) соединения примера Id) и 36,1 мкл (0,39 ммоль} этилизотиоцианата получали 161 мг указанного в заголовке соединения в виде бледно-желтого твердого вещества. Т.пл.: 90° С (размягчение). Rf (SiO2, ЭА/гептан 10:1)=0,42.
MC (ESI): m/e=508 [M+Н]+
Пример 4
1-(5-(2-(2,4-диметоксициннамоиламино)этил)-2-метоксифенилсульфонил)-3-этилмочевина
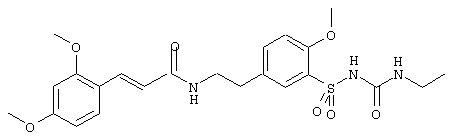
Синтез проводили согласно способу, описанному в примере 2. Из 80 мг (0,16 ммоль) соединения из примера 3 в этом случае получено 69 мг указанного в заголовке соединения в виде белого твердого вещества. Т.пл.: 96° С (размягчение). Rf (SiO2, ЭА/гептан 10:1)=0,14.
MC (FAB): m/e=492 [M+H]+
Пример 5
1-(5-(2-(2,4-диметилциннамоиламино)этил)-2-метоксифенилсульфонил)-3-метилтиомочевина
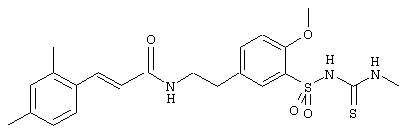
a) (5-(2-(2,4-диметилциннамоиламино)этил)-2-метоксибензол-сульфонамид
341 мг (1,94 ммоль) 2,4-диметилкоричной кислоты и 339 мг (2,1 ммоль) карбонил-бис-имидазола растворяли в 15 мл абсолютного ТГФ. После перемешивания при КТ в течение 2 ч к этому раствору добавляли 500 мг (2,17 ммоль) соединения из примера 1с) и 870 мкл триэтиламина. Смесь перемешивали при КТ в течение 12 ч, и затем реакционную смесь выливали на 40 мл 1н. раствора НСl. Выпавший осадок отфильтровывали с отсосом, промывали водой и затем сушили в вакууме. Получали 610 мг указанного в заголовке соединения в виде белого твердого вещества. Т.пл.: 202° С. Rf (SiO2, ЭА/гептан 4:1)=0,25.
MC (ESI): m/e=389 [М+Н]+
b) 1-(5-(2-(2,4-диметилциннамоиламино)этил)-2-метоксифенилсульфонил)-3-метилтиомочевина
Синтез проводили согласно способу, описанному в примере 1e). В этом случае из 604 мг (1,56 ммоль) соединения из примера 5а) и 1,1 мл (1,71 ммоль) метилизотиоцианата получено 580 мг указанного в заголовке соединения в виде белого твердого вещества. Т.пл.: 190-192° С. Rf (SiO2, ЭА/гептан 4:1)=0,47.
MC (ESI): m/e=462 [M+Н]+
Пример 6
1-(5-(2-(2,4-диметилциннамоиламино)этил)-2-метоксифенилсульфонил)-3-метилмочевина
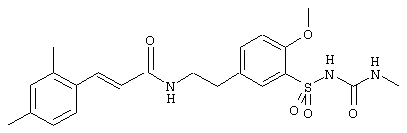
Синтез проводили согласно способу, описанному в примере 2. В этом случае из 100 мг (0,22 ммоль) соединения из примера 5 получено 79 мг указанного в заголовке соединения в виде белого твердого вещества. Т.пл.: 227-229° С. Rf (SiO2, ЭА/гептан 6:1)=0,10.
MC (FAB): m/e=446 [M+H]+
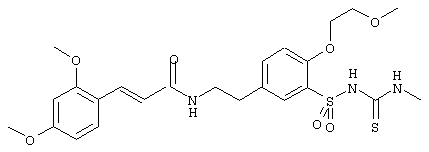
Пример 7
1-(5-(2-(2,4-диметоксициннамоиламино)этил)-2-(2-метокси-этокси)фенилсульфонил)-3-метилтиомочевина
а) N-диметиламинометилен-2-метокси-5-[2-(2,2,2-трифтор-ацетамидо)этилбензолсульфонамид
30,2 г (92,6 ммоль) соединения из примера 1b) растворяли в 70 мл абсолютного ДМФА, добавляли 14,0 мл (105,4 ммоль) диметилацеталя диметилформамида и полученный раствор перемешивали при КТ в течение 3 ч. Раствор концентрировали досуха, и полученный остаток смешивали со 100 мл воды и 100 мл 5%-ного раствора NaHSO4. Кристаллический осадок отфильтровывали с отсосом, несколько раз промывали водой и затем сушили в глубоком вакууме. Получали 29,6 г указанного в заголовке соединения в виде белого твердого вещества. Т.пл.: 143-144° С. Rf (SiO2, ЭА)=0,25.
MC (DCI): m/e=382 [M+H]+
b) N-диметиламинометилен-2-гидрокси-5-(2-(2,2,2-трифтор-ацетамидо)этилбензолсульфонамид
100 мл 1-молярного раствора ВВr3 в ДХМ добавляли по каплям при КТ за период 40 мин к раствору 29,5 г (77,2 ммоль) соединения из примера 7а) в 450 мл ДХМ. После перемешивания при КТ в течение 5 ч реакционную смесь обрабатывали 150 мл метанола и затем примерно 2 л диизопропилового эфира. Выпавший осадок отфильтровывали с отсосом и сушили в глубоком вакууме. Получали 32,7 г указанного в заголовке соединения как бромистоводородную соль в форме белого твердого вещества. Т.пл.: 160-161° С. Rf (SiO2, ЭА)=0,52.
МС (DCI): m/e=368 [M+H]+
c) N-диметиламинометилен-2-(2-метоксиэтокси)-5-(2-(2,2,2-трифторацетамидо)этил)бензолсульфонамид
Раствор 9,1 г (20,3 ммоль) соединения из примера 7b) и 7,1 г (50,8 ммоль) карбоната калия в 50 мл абсолютного ДМФА вводили во взаимодействие с 6,7 мл (71,7 ммоль) 2-бромэтилметилового эфира, и смесь перемешивали при 70° С в течение 3 ч. После добавления еще 6,7 мл 2-бромэтилметилового эфира и перемешивания при 70° С в течение 2 ч реакционную смесь обрабатывали примерно 300 мл ЭА. Смесь промывали водой и насыщенным раствором NaCl, органическую фазу сушили над Na2SO4 и концентрировали досуха. Оставшееся слабо окрашенное в желтый цвет масло очищали хроматографией на SiO2, используя в качестве элюента ЭА. После концентрирования содержащих продукт фракций и сушки в глубоком вакууме получали 7,25 г указанного в заголовке соединения в форме бледно-желтого твердого вещества. Т.пл.: 134-136° С. Rf (SiO2, ЭA)=0,35.
МС (DCI): m/e=426 [М+Н]+
d) 5-(2-аминоэтил)-2-(2-метоксиэтокси)бензолсульфонамид
Раствор 7,24 г (17,0 ммоль) соединения из примера 7с) в 100 мл метанола и 100 мл полуконцентрированной хлористоводородной кислоты нагревали при кипении с обратным холодильником в течение 8 ч. Затем к реакционному раствору добавляли примерно 40 мл этанола и выпавший осадок отфильтровывали с отсосом. Осадок промывали холодным этанолом и сушили в глубоком вакууме. Выход: 4,0 г указанного в заголовке соединения как хлористоводородной соли в форме белого твердого вещества. Т.пл.: 230-233° С.
МС (DCI): m/e=275 [М+Н]+
е) 5-(2-(2,4-диметоксициннамоиламино)этил)-2-(2-метоксиэтокси) бензолсульфонамид
Синтез проводили путем реакции 2,00 г (6,34 ммоль) соединения из примера 7d) с 1,32 г (6,34 ммоль) транс-2,4-диметоксикоричной кислоты по способу, описанному в примере 1d). После хроматографической очистки на SiO2 с использованием смеси ДХМ/ЭА в качестве элюента получали 2,40 г указанного в заголовке соединения в форме белого твердого вещества. Т.пл.: 175-178° С. Rf (SiO2, ЭA)=0,13.
МС (DCI): m/e=465 [М+Н]+
f) 1-(5-(2-(2,4-диметоксициннамоиламино)этил)-2-(2-ме-токсиэтокси)фенилсульфонил)-3-метилтиомочевина
Синтез проводили по способу, описанному в примере 1e). В этом случае из 1,30 г (2,80 ммоль) соединения из примера 7е) и 1,1 мл (1,10 ммоль) 1-молярного раствора метилизотиоцианата в абсолютном ДМФА получали после хроматографии на SiO2 с использованием смеси ЭА/гептан (6:1) в качестве элюента 857 мг указанного в заголовке соединения в виде белой аморфной пены. (SiO2, ЭА/гептан)=0,51.
МС (DCI): m/e=538 [M+H]+
Пример 8
1-(5-(2-(2,4-диметоксициннамоиламино)этил)-2-(2-метокси-этокси)фенилсульфонил)-3-метилмочевина
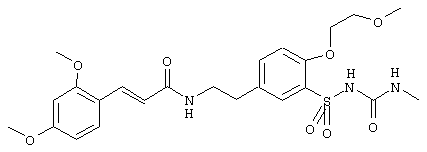
Синтез проводили согласно способу, описанному в примере 2. В этом случае из 652 мг (1,21 ммоль) соединения из примера 7f) получено 538 мг указанного в заголовке соединения в виде аморфного твердого вещества. Rf (SiO2, ЭА/гептан 10:1)=0,07.
MC (DCI): m/e=522 [M+H]+
Пример 9
1-(5-(2-(2,4-диметоксициннамоиламино)этил)-2-(2-метокси-этокси)фенилсульфонил)-3-этилтиомочевина
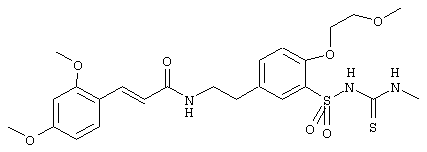
Синтез проводили согласно способу, описанному в примере 1е), причем вместо метилизотиоцианата использовали этилизотиоцианат. Из 150 мг (0,32 ммоль) соединения из примера 7е) и 32,6 мкл (0,36 ммоль) этилизотиоцианата получено после хроматографии на SiO2 с использованием смеси ЭА/гептан (7:1) в качестве элюента 139 мг указанного в заголовке соединения в виде белой аморфной пены. Т.пл.: 146-148° С. Rf (SiO2, ЭА/гептан 10:1)=0,48.
MC (ESI): m/e=522 [M+H]+
Пример 10
1-(5-(2-(2,4-диметоксициннамоиламино)этил)-2-(2-метокси-этокси)фенилсульфонил)-3-этилмочевина
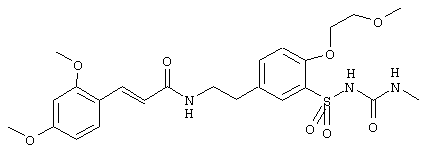
Синтез проводили из 80 мг (0,15 ммоль) соединения из примера 9 согласно способу, описанному в примере 2. В этом случае получено 68 мг указанного в заголовке соединения в виде бледно-желтого аморфного твердого вещества. Rf (SiO2, ЭА/гептан 10:1)=0,09.
MC (ESI): m/e=536 [М+Н]+
Пример 11
Метил-N-(5-(2-(2,4-диметоксициннамоиламино)этил))-2-(2-метоксиэтокси)фенилсульфонил)карбамат
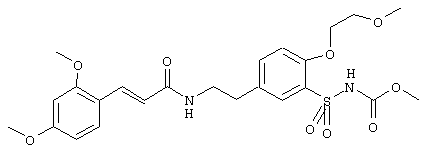
Раствор 150 мг (0,32 ммоль) соединения из примера 7е), 34,6 мкл (0,32 ммоль) диметилпирокарбоната и 89 мг карбоната калия в 8 мл диметилового эфира диэтиленгликоля нагревали при кипении с обратным холодильником в течение 8 ч. Затем реакционную смесь концентрировали досуха в вакууме и полученный остаток переносили в смесь ДХМ и 10%-ного раствора KH2PO4 (1:1). Органическую фазу отбирали, промывали раствором КН2РO4, сушили, используя Na2SO4, и концентрировали. Хроматографическая очистка остатка на SiO2 с использованием смеси ЭА/гептан (10:1) дала 55 мг указанного в заголовке соединения в виде окрашенного в слабо-желтый цвет аморфного твердого вещества. Rf (SiO2, ЭА/гептан 10:1)=0,17.
МС (DCI): m/e=523 [M+H]+
Пример 12
1-(5-(2-(циннамоиламино)этил)-2-метоксифенилсульфонил)-3-метилтиомочевина
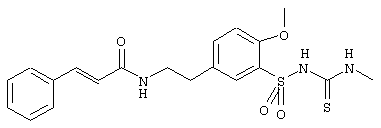
a) 5-(2-(циннамоиламино)этил)-2-метоксибензолсульфонамид
Раствор 463 мг (3,13 ммоль) транс-коричной кислоты, 984 мкл (5,73 ммоль) N-этилдиизопропиламина и 1,35 г (2,60 ммоль) РуВОР в 14 мл хлороформа перемешивали при 50° С в течение 1 ч. К этому раствору добавляли по каплям раствор 600 мг (2,60 ммоль) соединения из примера 1с) и затем смесь перемешивали при 50°С в течение 2,5 ч. Реакционную смесь упаривали досуха и остаток переносили в ДХМ. Раствор промывали 5%-ным раствором KHSO4 и 5%-ным раствором NaHCO3, сушили и концентрировали. Остаток очищали хроматографией на SiO2 с использованием смеси ЭА/гептан (5:1). Выход: 299 мг указанного в заголовке соединения в виде аморфного твердого вещества. Rf (SiO2, ЭА/гептан 5:1)=0,33.
МС (ESI): m/e=361 [M+H]+
b) 1-(5-(2-(циннамоиламино)этил)-2-метоксифенилсульфонил)-3-метилтиомочевина
Синтез проводили путем реакции 94 мг (0,26 ммоль) соединения из примера 12а) с метилизотиоцианатом по способу, описанному в примере 1e). Выход: 46 мг указанного в заголовке соединения в форме белого аморфного твердого вещества. Rf (SiO2, ЭА/гептан 5:1)=0,46.
MC (FAB): m/e=434 [M+H]+
Пример 13
1-(5-(2(α -метилциннамоиламино)этил)-2-метоксифенилсульфонил]-3-метилтиомочевина
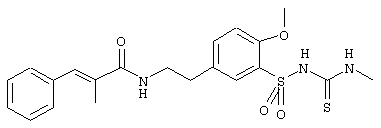
a) 1-(5-(2-(α -метилциннамоиламино)этил)-2-метоксибензолсульфонамид
Синтез проводили путем реакции соединения из примера 1с) с α -метилкоричной кислотой по способу, описанному в примере 12а).
Rf (SiO2, ЭА/гептан 4:1)=0,35.
MC (DCI): m/е=375 [M+H]+
b) 1-(5-(2-(α -метилциннамоиламино)этил)-2-метоксифенилсульфонил)-3-метилтиомочевина
Синтез проводили путем реакции соединения из примера 13а) с метилизотиоцианатом по способу, описанному в примере 1e).
Rf (SiO2, ЭА/гептан 4:1)=0,46.
MC (DCI): m/e=448 [М+Н]+
Пример 14
1-(5-(2-(α -фенилциннамоиламино)этил)-2-метоксифенилсульфонил)-3-метилтиомочевина
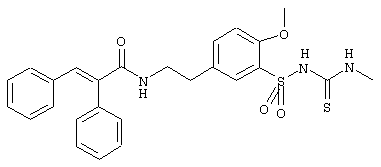
а) 5-(2-(α -фенилциннамоиламино)этил)-2-метоксибензолсульфонамид
Синтез проводили путем реакции соединения из примера 1с) с α -фенилкоричной кислотой по способу, описанному в примере 12а).
Rf (SiO2, ЭА/гептан 5:1)=0,32.
МС (DCI): m/е=437 [М+Н]+
b) 1-(5-(2-(α -фенилциннамоиламино)этил)-2-метоксифенилсульфонил)-3-метилтиомочевина
Синтез проводили путем реакции соединения из примера 14а) с метилизотиоцианатом по способу, описанному в примере 1e).
Rf (SiO2, ЭА/гептан 5:1)=0,42.
МС (DCI): m/e=510 [M+H]+
Пример 15
1-(5-(2-(2,4-диметилциннамоиламино)этил)-2-фенилфенилсульфонил)-3-метилтиомочевина
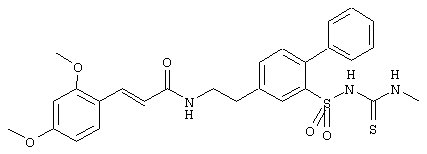
а) 2,2, 2-трифтор-N-(2-(4-нитрофенил)этил)ацетамид
Синтез проводили путем реакции 4-нитрофенилэтиламина и трифторуксусного ангидрида по способу, описанному в примере 1а). Из 29,8 г (0,15 моль) 4-нитрофенилэтиламина гидрохлорида получено 34,7 г указанного в заголовке соединения в виде твердого вещества бежевого цвета. Т.пл.: 96-97° С. Rf (SiO2, ЭА/гептан 1:1)=0,52.
МС (ESI): m/e=263 [M+H]+
b) 2,2,2-трифтор-N-(2-(4-аминофенил)этил)ацетамид
Раствор 34,6 г (0,13 моль) соединения из примера 15а) и 197 г (0,87 моль) SnСl2×2Н2О в 1 л ЭА перемешивали при 80° С в течение 3,5 ч. Затем реакционный раствор обрабатывали 2 л 10%-ного раствора NaHCO3 и осадок отфильтровывали. Органическую фазу отделяли, сушили над Na2SO4 и концентрировали досуха в вакууме. Получали 26,9 г указанного в заголовке соединения в виде светло-коричневого твердого вещества. Т.пл.: 81-85° С. Rf (SiO2, ЭА/гептан 1:1)=0,35.
МС (ESI): m/e=233 [M+H]+
c) 2,2,2-трифтор-N-(2-(4-иодфенил)этил)ацетамид
Раствор 8,3 г (0,12 ммоль) нитрита натрия в 28 мл воды добавляли по каплям к суспензии 26,8 г (0,11 моль) соединения из примера 15b) в 125 мл разбавленной хлористоводородной кислоты, охлажденной до 0° С. После перемешивания при этой температуре в течение 15 мин по каплям добавляли раствор 19,9 г (0,12 моль) иодида калия, и полученный реакционный раствор перемешивали при КТ в течение 3 ч.
Реакционную смесь экстрагировали ДХМ, органическую фазу отделяли, промывали 10%-ным раствором NаНSО3 и водой и сушили над Na2SO4. После концентрирования и хроматографической очистки остатка на SiO2 с использованием смеси ДХМ/ЭА (80:1) в качестве элюента получали 17,1 г указанного в заголовке соединения в виде бледно-желтого твердого вещества. Т.пл.: 136-138° С. Rf (SiO2, ЭА/гептан 1:1)=0,67.
МС (DCI): m/e=344 [M+H]+
d) 2-иод-5-(2-(2,2,2-трифторацетамидо) этил) бензолсульфонамид
10 г (29,1 ммоль) соединения из примера 15с) добавляли частями к 95 мл хлорсульфоновой кислоты, охлажденной до 0° С. После перемешивания при КТ в течение 3,5 ч реакционный раствор добавляли по каплям к 400 мл льда, и образовавшийся осадок отфильтровывали с отсосом. Этот осадок растворяли в 200 мл ацетона и к раствору добавляли по каплям 56 мл концентрированного раствора аммиака при охлаждении льдом. После перемешивания при КТ в течение 45 мин образовавшийся осадок отфильтровывали с отсосом, и ацетон отгоняли на роторном испарителе. Оставшийся раствор экстрагировали ЭА, ЭА-фазу отделяли, промывали насыщенным раствором NaCl и сушили над Na2SO4. После концентрирования и хроматографической очистки остатка на SiO2 с использованием смеси ЭА/гептан (1:2) в качестве элюента получали 4,5 г указанного в заголовке соединения. Т.пл.: размягчение со 100° С. Rf (SiO2, ЭА/гептан 1:1)=0,32.
МС (ESI): m/е=423 [М+Н]+
е) 5-(2-аминоэтил)-2-иодбензолсульфонамид
Раствор 4,0 г (9,47 ммоль) соединения из примера 15d) в 25 мл 2н. хлористоводородной кислоты перемешивали при кипении с обратным холодильником в течение 4,5 ч. Затем рН раствора доводили до 10 добавлением 2н. раствора гидроксида натрия, и раствор несколько раз экстрагировали ЭА. Органическую фазу сушили над Na2SO4 и концентрировали. Оставшийся остаток объединяли с осадком, выпавшим из водной фазы, и отфильтровывали с отсосом. После сушки в глубоком вакууме получали 2,65 г указанного в заголовке соединения. Т.пл.: 215° С. Rf (SiO2, ЭА/гептан 1:1)=0,10.
MC (ESI): m/e=327[M+H]+
f) 5-(2-(2,4-диметоксициннамоиламино)этил)-2-иодбензолсульфонамид
Раствор 693 мг (3,33 ммоль) транс-2,4-диметоксикоричной кислоты и 583 мг (3,60 ммоль) карбонилбисимидазола в 25 мл ТГФ перемешивали при КТ в течение 2 ч. Затем к этому раствору добавляли 1,2 г (3,73 ммоль) соединения из примера 15е) и раствор перемешивали при КТ в течение 24 ч. Реакционный раствор выливали на 70 мл 1н. хлористоводородной кислоты, экстрагировали ЭА, и органические экстракты сушили над Na2SO4 и концентрировали. Остаток перемешивали с ЭА, и оставшийся осадок отфильтровывали с отсосом и очищали хроматографией на SiO2 с использованием смеси ЭА/гептан (2:1) в качестве элюента. Получали 1,2 г указанного в заголовке соединения в виде бледно-желтого твердого вещества. Т.пл.: 180° С. Rf (SiO2, ЭА/гептан 2:1)=0,26.
MC (FAB): m/e=517 [M+H]+
g) 5-(2-(2,4-диметоксициннамоиламино)этил)-N-диметиламинометилен-2-иодбензолсульфонамид
Раствор 1,1 г (2,15 ммоль) соединения из примера 16f) и 346 мкл (2,58 ммоль) диметилацеталя N,N-диметилформамида в 8 мл абсолютного ДМФА перемешивали при КТ в течение 1 ч. Смесь упаривали досуха под вакуумом, остаток переносили в ДХМ, и раствор промывали водой и раствором NaCl и концентрировали. Хроматографическая очистка на SiO2 с использованием смеси ДХМ/метанол (20:1) в качестве элюента давала 998 мг указанного в заголовке соединения в виде аморфной желтой пены. Rf (SiO2, ЭА/гептан 7:3)=0,10.
МС (ESI): m/e=572 [M+H]+
h) 5-(2-(2,4-диметоксициннамоиламино)этил)-N-диметиламинометилен-2-фенилбензолсульфонамид
Раствор 53 мг (0,44 ммоль) фенилбороновой кислоты в 2,5 мл этанола добавляли по каплям в атмосфере аргона к раствору 250 мг (0,44 ммоль) соединения из примера 15g) и 16 мг (0,01 ммоль) тетракис(трифенилфосфин)палладия в 2,5 мл толуола. После перемешивания при КТ в течение 15 мин добавляли 510 мкл 2-молярного раствора карбоната цезия, и полученную реакционную смесь перемешивали при 80° С в течение 6 ч. Смесь концентрировали в вакууме, остаток переносили в ДХМ и раствор несколько раз промывали водой, сушили над Na2SO4 и концентрировали. Хроматографическая очистка на SiO2 с использованием ЭА в качестве элюента давала 207 мг указанного в заголовке соединения в виде аморфного бежевого твердого вещества. Rf (SiO2, ЭА)=0,25.
МС (FAB): m/е=522 [М+Н]+
i) 5-(2-(2,4-диметоксициннамоиламино)этил)-2-фенилбензолсульфонамид
Раствор 202 мг (0,39 ммоль) соединения из примера 15h) и 1 мл концентрированной хлористоводородной кислоты в 5 мл метанола нагревали при кипячении с обратным холодильником в течение 4 ч. Затем рН реакционного раствора доводили до 5 добавлением 2н. раствора гидроксида натрия и затем раствор несколько раз экстрагировали ЭА. Объединенные ЭА-экстракты сушили над Na2SO4 и концентрировали. Хроматографическая очистка на SiO2 с использованием смеси ЭА/толуол (5:1) в качестве элюента давала 78 мг указанного в заголовке соединения в виде бежевого твердого вещества. Т.пл.: 85° С (размягчение).
Rf (SiO2, ЭА/толуол 5:1)=0,48.
МС (ESI): m/е=467 [М+Н]+
j) 1-(5-(2-(2,4-диметоксициннамоиламино)этил)-2-фенилфенилсульфонил)-3-метилтиомочевина
Синтез проводили путем реакции 64 мг (0,14 ммоль) соединения из примера 15i) с метилизотиоцианатом по способу, описанному в примере 1e). В этом случае получали 68 мг указанного в заголовке соединения в виде бледно-желтого аморфного твердого вещества. Rf (SiO2, ЭА/гептан 2:1)=0,29.
МС (ESI): m/e=540 [M+H]+
Пример 16
1-(5-(2-(2,4-диметоксициннамоиламино)этил)-2-(2-фурил)фенил-сульфонил)-3-метилтиомочевина
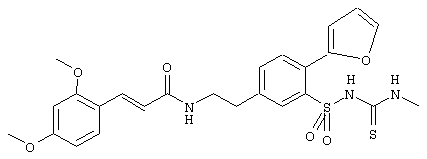
а) 5-(2-(2,4-диметоксициннамоиламино)этил)-N-диметиламинометилен-2-(2-фурил)бензолсульфонамид
К раствору 400 мг (0,70 ммоль) соединения из примера 15g) в 5 мл ТГФ в атмосфере аргона добавляли 2,7 мг (0,004 ммоль) хлорида бис(трифенилфосфин) палладия(II) и 305 мкл (0,97 ммоль) 2-(трибутилстаннил)фурана. Полученный реакционный раствор нагревали при кипении с обратным холодильником в течение 18 ч. Затем его разбавляли ЭА, и раствор промывали водой, сушили над Na2SO4 и концентрировали. Хроматографическая очистка на SiO2 с использованием ЭА в качестве элюента давала 287 мг указанного в заголовке соединения в виде аморфной белой пены. Rf (SiO2, ЭА)=0,35.
МС (ESI): m/e=512 [М+Н]+
b) 5-(2-(2,4-диметоксициннамоиламино)этил)-2-(2-фурил)-бензолсульфонамид
Синтез осуществляли путем взаимодействия 281 мг (0,55 ммоль) соединения из примера 16а) с хлористоводородной кислотой по способу, описанному в примере 15i). После хроматографической очистки на SiO2 с использованием ЭА в качестве элюента получали 82 мг указанного в заголовке соединения в виде окрашенного в желтый цвет аморфного твердого вещества. Rf (SiO2, ЭА)=0,72.
МС (ESI): m/e=457 [М+Н]+
c) 1-(5-(2-(2,4-диметоксициннамоиламино)этил)-2-(2-фурил)фенилсульфонил)-3-метилтиомочевина
Синтез проводили путем реакции 52 мг (0,14 ммоль) соединения из примера 16b) с метилизотиоцианатом по способу, описанному в примере 1e). Выход: 28 мг указанного в заголовке соединения в форме аморфного твердого вещества. Rf (SiO2, ЭА/гептан 2:1)=0,18.
МС (ESI): m/e=434 [M+H]+
Пример 17
1-(5-(2-(циннамоиламино)этил)-2-(2-метоксиэтокси)фенилсульфонил)-3-метилтиомочевина
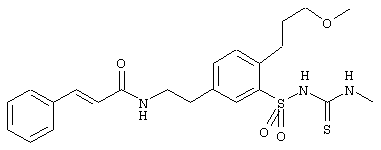
a) 5-(2-(циннамоиламино)этил)-2-(2-метоксиэтокси)бензолсульфонамид
Указанное в заголовке соединение получали реакцией соединения из примера 7d) с транс-коричной кислотой по способу, упомянутому в примере 5а). Из 1,75 г (5,62 ммоль) соединения из примера 7d) и 1,0 г (6,75 ммоль) транс-коричной кислоты получали после кристаллизации растиранием с небольшим количеством ЭА 910 мг указанного в заголовке соединения в виде белого твердого вещества. Т.пл.: 133° С. Rf (SiO2, ЭА/гептан 4:1)=0,24
МС (ESI): m/e=405 [М+Н]+
b) 1-(5-(2-(циннамоиламино)этил)-2-(2-метоксиэтокси)фенилсульфонил)-3-метилтиомочевина
Указанное в заголовке соединение получали реакцией соединения из примера 17а) с метилизотиоцианатом по способу, описанному в примере 1e). Из 600 мг (1,48 ммоль) соединения из примера 17а) после хроматографии на SiO2 с использованием ЭА в качестве элюента получали 401 мг указанного в заголовке соединения в форме белого твердого вещества. Т.пл.: 150° С (размягчение). Rf (SiO2, ЭA)=0,75.
МС (ESI): m/e=478 [M+H]+
Пример 18
Натриевая соль 1-(5-(2-(циннамоиламино)этил)-2-(2-метоксиэтокси)фенил-сульфонил)-3-метилтиомочевины
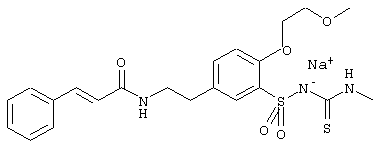
24,1 мг (1,05 ммоль) натрия растворяли в 13,5 мл абсолютного метанола. Затем добавляли 500 мг (1,05 ммоль) соединения из примера 17b) и полученный раствор перемешивали при КТ в течение 1 ч. После добавления 90 мл изопропанола и выдержки в холодильнике в течение 2 суток выкристаллизовавшийся осадок отфильтровывали с отсосом и промывали небольшим количеством изопропанола. После сушки в глубоком вакууме получали 441 мг указанного в заголовке соединения в виде белого твердого вещества. Т.пл.: 245° С.
МС (ESI): m/e=478 [M+H]+
Пример 19
1-(5-(2-(циннамоиламино)этил)-2-(2-метоксиэтокси)фенилсульфонил)-3-метилмочевина
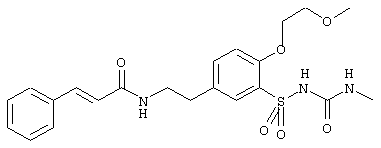
Указанное в заголовке соединение получали реакцией соединения из примера 17b) с перекисью водорода по способу, упомянутому в примере 2. Из 48 мг (0,1 ммоль) соединения из примера 17b) в этом случае получали 25 мг указанного в заголовке соединения в виде белого твердого вещества. Т.пл.: 65° С (размягчение). Rf (SiO2, ЭA)=0,10.
MC (ESI): m/e=462 [M+H]+
Пример 20
1-(2-бензилокси-5-(2-(2,4-диметоксициннамоиламино)этил)фенилсульфонил)-3-метилтиомочевина
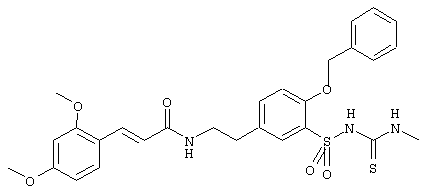
а) 2-бензилокси-1-диметиламинометилен-5-(2-(2,2,2-трифторацетамидо)этил)-бензолсульфонамид
Смесь 2,76 г (7,51 ммоль) соединения из примера 7b), 3,13 мл (26,3 ммоль) бензилбромида и 2,62 г (18,8 ммоль) карбоната калия в 20 мл абсолютного ДМФА перемешивали при 70° С в течение 6 ч, затем разбавляли ДХМ и обрабатывали водой. Органическую фазу отделяли, промывали насыщенным раствором NaCl и сушили над Na2SO4. После концентрирования и хроматографической очиcтки на SiO2 с использованием смеси ДХМ/ЭА (4:1) в качестве элюента получали 1,9 г указанного в заголовке соединения в виде белого твердого вещества. Т.пл.: 103° С (размягчение). Rf (SiO2, ДХМ/ЭА 4:1)=0,26.
MC (ESI): m/e=458 [M+H]+
b) 5-(2-аминоэтил)-2-бензилоксибензолсульфонамид
Указанное в заголовке соединение получали взаимодействием соединения из примера 20а) с 2н. НСl по способу, упомянутому в примере 7d). Из 1,88 г (4,13 ммоль) соединения из примера 20а) получали 1,2 г указанного в заголовке соединения в виде белого твердого вещества. Т.пл.: 210° С. Rf (SiO2, ЭА)=0,02.
MC (ESI): m/e=307 [М+Н]+
c) 2-бензилокси-5-(2-(2,4-диметоксициннамоиламино)этил)-бензолсульфонамид
Указанное в заголовке соединение получали реакцией соединения из примера 20b) с транс-2,4-диметоксикоричной кислотой по способу, упомянутому в примере 5а). В этом случае из 1,2 г (4,1 ммоль) соединения из примера 20b) получали 503 мг указанного в заголовке соединения в виде белого твердого вещества. Т.пл.: 133° С.
Rf (SiO2, ЭА/гептан 2:1)=0,43.
MC (ESI): m/e=497 [M+H]+
d) 1-(2-бензилокси-5-(2-(2,4-диметоксициннамоиламино)этил) фенилсульфонил)-3-метилтиомочевина
Указанное в заголовке соединение получали реакцией соединения из примера 20с) с метилизотиоцианатом по способу, описанному в примере 1e). Из 181 мг (0,36 ммоль) соединения из примера 20с) в этом случае получали 204 мг указанного в заголовке соединения в форме бежевого аморфного твердого вещества. Rf (SiO2, ЭА/гептан 2:1)=0,23.
MC (ESI): m/e=570 [M+H]+
Пример 21
1-(5-(2-(5-хлор-2-метоксициннамоиламино)этил)-2-метоксифенил-сульфонил)-3-метилтиомочевина
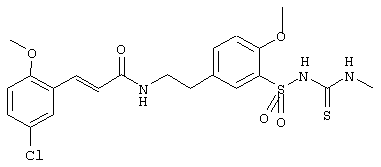
a) этил-5-хлор-2-метоксициннамат
Раствор 10,6 г (48,2 ммоль) 2-бром-4-хлоранизола в 30 мл триэтиламина в атмосфере аргона вводили во взаимодействие с 10,1 мл (81,2 ммоль) этилакрилата, 1,23 г три-о-толилфосфина и 0,45 г ацетата палладия(II). Реакционную смесь перемешивали при 100° С в течение 2 суток, затем разбавляли ЭА и фильтровали через целит. Фильтрат промывали 1н. НСl и насыщенным раствором NaCl, сушили над Na2SO4 и концентрировали. После хроматографической очистки через SiO2 с использованием смеси ЭА/гептан (1:8) в качестве элюента получали 0,85 г указанного в заголовке соединения в виде бледно-желтого масла. Rf (SiO2, ЭА/гептан 1:4)=0,34.
МС (ESI): m/e=512 [М+H]+
b) 5-хлор-2-метоксикоричная кислота
Раствор 0,84 г (3,46 ммоль) соединения из примера 21а) в 2 мл этанола и 1 мл воды обрабатывали 0,67 г (12 ммоль) гидроксида натрия и перемешивали при КТ в течение 45 мин. Затем этанол отгоняли под вакуумом в роторном испарителе, остаток разбавляли 10 мл воды и рН раствора доводили до 1 добавлением 2н. НСl. Выпавший осадок отфильтровывали с отсосом, промывали водой и сушили при 40°С в глубоком вакууме. Получали 545 мг указанного в заголовке соединения в виде белого твердого вещества. Т.пл.: 188-190° С. Rf (SiO2, ЭА/гептан 1:2)=0,14.
МС (ESI): m/e=213 [М+Н]+
c) 5-(2-(5-хлор-2-метоксициннамоиламино)этил)-2-метокси-бензолсульфонамид
Указанное в заголовке соединение получали реакцией соединения из примера 21b) с соединением из примера 1с) по способу, упомянутому в примере 5а). Из 350 мг (1,64 ммоль) соединения из примера 21b) и 315 мг (1,37 ммоль) соединения из примера 1с) получали 470 мг указанного в заголовке соединения в виде белого твердого вещества. Т.пл.: 196-198° С. Rf (SiO2, ЭА/гептан 4:1)=0,13.
МС (ESI): m/e=425 [M+H]+
d) 1-(5-(2(5-хлор-2-метоксициннамоиламино)этил)-2-метоксифенилсульфонил)-3-метилтиомочевина
Указанное в заголовке соединение получали реакцией соединения из примера 21с) с метилизотиоцианатом по способу, описанному в примере 1e). Из 100 мг (0,24 ммоль) соединения из примера 21с) в этом случае получали 93 мг указанного в заголовке соединения в виде белого твердого вещества. Т.пл.: 188-190° С. Rf (SiO2, ЭА/гептан 4:1)=0,33.
МС (ESI): m/e=499 [M+H]+
Пример 22
1-(5-(2-(2,4-диметоксициннамоиламино)этил)-2-феноксифенил-сульфонил)-3-метилтиомочевина
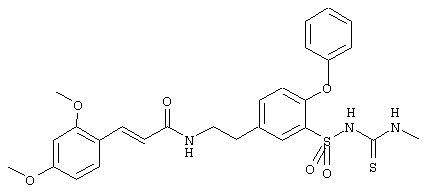
а) N-диметиламинометилен-2-фенокси-5-(2-(2,2,2-трифтор-ацетамидо)этил)бензолсульфонамид
Смесь 500 мг (1,36 ммоль) соединения из примера 7b), 247 мг (1,36 ммоль) ацетата меди(II), 498 мг (4,08 ммоль) фенилбороновой кислоты и 943 мкл (6,80 ммоль) триэтиламина в 15 мл ДХМ перемешивали при КТ в течение 24 ч в атмосфере аргона в присутствии размолотого и высушенного молекулярного сита. Реакционную смесь фильтровали и фильтрат промывали 10%-ным раствором KHSO4 и 10%-ным раствором NaHCO3, сушили над Na2SO4 и затем концентрировали. После хроматографической очистки на SiO2 с использованием смеси ЭА/гептан (3:1) в качестве элюента получали 197 мг указанного в заголовке соединения в виде белой аморфной пены. Rf (SiO2, ЭА)=0,72.
МС (ESI): m/e=444 [М+Н]+
b) 5-(2-аминоэтил)-2-феноксибензолсульфонамид
Указанное в заголовке соединение получали реакцией соединения из примера 22а) с 2н. НСl по способу, упомянутому в примере 7d). Из 149 мг (0,34 ммоль) соединения из примера 22а) получали 98 мг указанного в заголовке соединения в виде белого аморфного твердого вещества. Rf (SiO2, ЭА)=0,02.
МС (ESI): m/e=293 [М+Н]+
с) 1-(5-(2-(2,4-диметоксициннамоиламино)этил)-2-фенокси-бензолсульфонамид
Указанное в заголовке соединение получали реакцией соединения из примера 22b) с транс-2,4-диметоксикоричной кислотой по способу, упомянутому в примере 5а). В этом случае из 96 мг (0,33 ммоль) соединения из примера 22b) получали 90 мг указанного в заголовке соединения в виде бледно-желтого аморфного твердого вещества. Rf (SiO2, ЭА/гептан 2:1)=0,27.
МС (ESI): m/e=483 [M+H]+
d) 1-(5-(2-(2,4-диметоксициннамоиламино)этил)-2-фенокси-фенилсульфонил)-3-метилтиомочевина
Указанное в заголовке соединение получали реакцией соединения из примера 22с) с метилизотиоцианатом по способу, описанному в примере 1e). Из 85 мг (0,18 ммоль) соединения из примера 22с) в этом случае получали 77 мг указанного в заголовке соединения в виде бежевого аморфного твердого вещества.
Rf (SiO2, ЭА/гептан 2:1)=0,23.
МС (ESI): m/e=556 [M+H]+
Пример 23
1-(2-аллилокси-5-(2-(2,4-диметоксициннамоиламино)этил)фенил-сульфонил)-3-метилтиомочевина
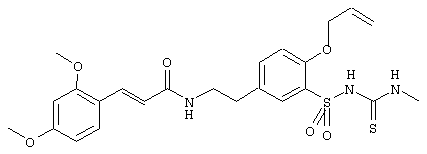
а) 2-аллилокси-N-диметиламинометилен-5-(2-(2,2,2-трифторацетамидо)этил)бензолсульфонамид
Раствор 2,0 г (0,54 ммоль) соединения из примера 7b) и 1,65 мл (19 ммоль) аллилбромида в 15 мл абсолютного ДМФА вводили во взаимодействие с 1,9 г (13,6 ммоль) карбоната калия и перемешивали при 70° С в течение 6 ч. Реакционную смесь разбавляли ДХМ и добавляли воду. Отделенную органическую фазу промывали насыщенным раствором NaCl, сушили над Na2SO4 и концентрировали. Хроматографическая очистка на SiO2 с использованием смеси ДХМ/ЭА (4:1) в качестве элюента дает 1,2 г указанного в заголовке соединения в виде белого твердого вещества. Т.пл.: 92-93° С. Rf (SiO2, ЭА)=0,52.
МС (ESI): m/e=408 [М+Н]+
b) 2-аллилокси-5-(2-аминоэтил)бензолсульфонамид
Указанное в заголовке соединение получали реакцией соединения из примера 23а) с 2н. НСl по способу, упомянутому в примере 7d). Из 1,2 г (2,95 ммоль) соединения из примера 23а) получали 550 мг указанного в заголовке соединения в виде белого твердого вещества. Т.пл.: 195° С. Rf (SiO2, ЭА)=0,02.
МС (ESI): m/e=257 [М+Н]+
с) 1-(2-аллилокси-5-(2-(2,4-диметоксициннамоиламино)этил)-бензолсульфонамид
Указанное в заголовке соединение получали реакцией соединения из примера 23b) с 2,4-диметоксикоричной кислотой по способу, упомянутому в примере 5а). Из 1,55 г (6,05 ммоль) соединения из примера 23b) и 1,26 г (6,05 ммоль) 2,4-диметоксикоричной кислоты получали 430 мг указанного в заголовке соединения в виде бледно-желтого твердого вещества. Т.пл.: 166-168° С. Rf (SiO2, ЭА/гептан 2:1)=0,26.
MC (ESI): m/e=447 [M+H]+
d) 1-(2-аллилокси-5-(2-(2,4-диметоксициннамоиламино)-этил)фенилсульфонил)-3-метилтиомочевина
Указанное в заголовке соединение получали реакцией соединения из примера 23с) с метилизотиоцианатом по способу, описанному в примере 1е). Из 180 мг (0,40 ммоль) соединения из примера 23с) в этом случае получали 110 мг указанного в заголовке соединения в виде бледно-желтого твердого вещества. Т.пл.: 171-175° С. Rf (SiO2, ЭА/гептан 4:1)=0,18.
MC (ESI): m/e=520 [M+H]+
Пример 24
1-(5-(2-(2,4-дихлорциннамоиламино)этил)-2-(2-метоксиэтокси)-фенилсульфонил)-3-метилтиомочевина
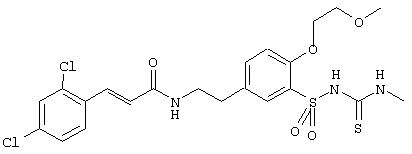
а) 1-(5-(2-(2,4-дихлорциннамоиламино)этил)-2-(2-метоксиэтокси)бензолсульфонамид
Указанное в заголовке соединение получали реакцией соединения из примера 7d) с 2,4-диметоксикоричной кислотой по способу, упомянутому в примере 5а). Из 1,6 г (5,15 ммоль) соединения из примера 7d) и 1,08 г (6,18 ммоль) 2,4-дихлоркоричной кислоты получали 1,56 г указанного в заголовке соединения в виде белого твердого вещества. Rf (SiO2, ЭА/гептан 4:1)=0,14.
MC (ESI): m/e=474 [M+H]+
b) 1-(5-(2-(2,4-дихлорциннамоиламино)этил)-2-(2-метокси-этокси)фенилсульфонил)-3-метилтиомочевина
Указанное в заголовке соединение получали реакцией соединения из примера 24а) с метилизотиоцианатом по способу, описанному в примере 1e). Из 150 мг (0,32 ммоль) соединения из примера 24а) в этом случае получали 143 мг указанного в заголовке соединения в виде белого твердого вещества. Т.пл.: 76-78° С. Rf (SiO2, ЭА/гептан 4:1)=0,18.
МС (ESI): m/e=547 [M+H]+
Пример 25
1-(5-(2-(5-трет-бутил-2-метоксициннамоиламино)этил)-2-(2-метоксиэтокси)фенилсульфонил)-3-метилтиомочевина
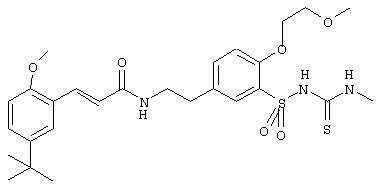
а) 4-трет-бутил-2-иоданизол
Раствор 8,0 г (0,11 ммоль) нитрита натрия в 25 мл воды добавляли по каплям к раствору 20 г (0,11 ммоль) 5-трет-бутил-2-метоксианилина в 120 мл смеси вода/концентрированная НСl (1:1), охлажденному до 5° С. После перемешивания при 5° С в течение 15 мин по каплям добавляли раствор 19,1 г (0,11 ммоль) иодида калия в 25 мл воды, и полученный раствор перемешивали при КТ в течение 4 ч. Раствор несколько раз экстрагировали ДХМ и отделенную органическую фазу промывали 10%-ным раствором NaHSO3 и водой, сушили над Na2SO4 и концентрировали. Хроматографическая очистка остатка на SiO2 с использованием смеси ЭА/гептан (1:40) в качестве элюента давала 27 г указанного в заголовке соединения в виде бледно-красного масла. Rf (SiO2, ЭА/гептан 1:1)=0,86.
МС (ESI): m/e=291 [М+Н]+
b) этил-5-трет-бутил-2-метоксициннамат
Раствор 25 г (86,4 ммоль) соединения из примера 25а), 18,1 мл (145,6 ммоль) этилакрилата, 2,2 г три-о-толилфосфина и 814 мг (3,62 ммоль) хлорида палладия(II) перемешивали при 60° С в течение 2 ч под атмосферой аргона. Затем реакционную смесь разбавляли 150 мл ЭА, осадок отфильтровывали и фильтрат промывали 1н. НСl и насыщенным раствором NaCl. После сушки над Na2SO4, концентрирования и хроматографической очистки оставшегося остатка на SiO2 с использованием смеси ЭА/гептан (1:20) в качестве элюента получали 19,7 г указанного в заголовке соединения в виде бледно-желтого масла. Rf (SiO2, ЭА/гептан 1:10)=0,30.
МС (ESI): m/e=263 [M+H]+
с) 5-трет-бутил-2-метоксикоричная кислота
Указанное в заголовке соединение получали путем взаимодействия соединения из примера 25b) с КОН по способу, описанному в примере 21b). В этом случае из 19,7 г (75,1 ммоль) соединения из примера 25b) получали 17,5 г указанного в заголовке соединения в виде бледно-серого твердого вещества. Т.пл.: 165-167° С. Rf (SiO2, ЭА/гептан 1:10)=0,04.
МС (ESI): m/e=235 [M+H]+
d) 1-(5-(2-(5-трет-бутил-2-метоксициннамоиламино)этил)-2-(2-метоксиэтокси)бензолсульфонамид
Указанное в заголовке соединение получали реакцией соединения из примера 7d) с соединением из примера 25с) по способу, упомянутому в примере 5а). Из 1,1 г (3,56 ммоль) соединения из примера 7d) и 1,0 г (4,27 ммоль) соединения из примера 25с) получали 866 мг указанного в заголовке соединения в виде белого твердого вещества. Т.пл.: 154° С. Rf (SiO2, ЭА/гептан 2:1)=0,13.
МС (ESI): m/e=491 [M+H]+
е) 1-(5-(2-(5-трет-бутил-2-метоксициннамоиламино)этил)-2-(2-метоксиэтокси)фенилсульфонил)-3-метилтиомочевина
Указанное в заголовке соединение получали реакцией соединения из примера 25d) с метилизотиоцианатом по способу, описанному в примере 1e). Из 286 мг (0,58 ммоль) соединения из примера 25d) в этом случае получали 327 мг указанного в заголовке соединения в виде белого твердого вещества. Т.пл.: 73° С (размягчение). Rf (SiO2, ЭА)=0,64.
МС (ESI): m/e=564 [M+H]+
Пример 26
1-(5-(2-(2,4-диметилциннамоиламино)этил)-2-(2-метоксиэтокси)фенилсульфонил)-3-метилтиомочевина
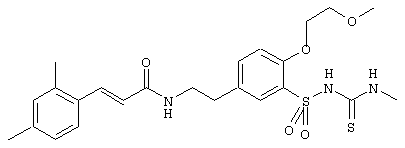
а) 1-(5-(2-(2,4-диметилциннамоиламино)этил)-2-(2-метокси-этокси)бензолсульфонамид
Указанное в заголовке соединение получали реакцией соединения из примера 7d) с транс-2,4-коричной кислотой по способу, упомянутому в примере 5а). Из 1,6 г (5,15 ммоль) соединения из примера 7d) и 1,0 г (6,15 ммоль) транс-2,4-коричной кислоты после хроматографии на SiO2 с использованием смеси ЭА/гептан (4:1) в качестве элюента получали 1,05 г указанного в заголовке соединения в виде белого твердого вещества. Rf (SiO2, ЭА/гептан 4:1)=0,09.
МС (ESI): m/e=432 [M+H]+
b) 1-(5-(2-(2,4-диметилициннамоиламино)этил)-2-(2-метокси-этокси)фенилсульфонил)-3-метилтиомочевина
Указанное в заголовке соединение получали реакцией соединения из примера 26а) с метилизотиоцианатом по способу, описанному в примере 1e). Из 150 мг (0,35 ммоль) соединения из примера 26а) в этом случае получали 134 мг указанного в заголовке соединения в виде бежевого аморфного твердого вещества. Т.пл.: 116° С. Rf (SiO2, ЭА/гептан 2:1)=0,16.
МС (ESI): m/e=506 [M+H]+
Фармакологические исследования
Продолжительность потенциала действия на папиллярную мышцу морской свинки
Состояния АТФ-недостаточности, такие как наблюдаются при ишемии в клетках сердечной мышцы, приводят к сокращению продолжительности потенциала действия. Их рассматривают как одну из причин так называемых аритмий циркуляции возбуждения, которые могут вызывать внезапную остановку сердца. Считается, что это вызывается открытием АТФ-чувствительных калиевых каналов из-за понижения концентрации АТФ (АТФ=адезинотрифосфат). Для измерений потенциала действия в папиллярной мышце морских свинок применяли стандартную микроэлектродную методику.
Морских свинок обоего пола убивали ударом по голове, сердца извлекали, папиллярные мышцы выделяли и суспендировали в ванне для органов. Ванну для органов орошали раствором Рингера (136 ммоль/л NaCl, 3,3 ммоль/л КСl, 2,5 ммоль/л CaCl2, 1,2 ммоль/л КН2РO4, 1,1 ммоль/л MgSO4, 5,0 ммоль/л глюкозы, 10,0 ммоль/л N-(2-гидроксиэтил)пиперазин-N’-(2-этансульфоновой кислоты) (HEPES), рН доведено до 7,4 с помощью NaOH) и аэрировали 100%-ным кислородом при температуре 37° С. Мышцу стимулировали посредством электрода, используя квадратно-волновые импульсы в 1 В, продолжительностью 1 мс и частотой 1 Гц. Потенциал действия вызывали и регистрировали с помощью введенного внутриклеточно стеклянного микроэлектрода, который заполняли 3 моль/л раствором КСl. Испытуемое вещество добавляли к раствору Рингера в концентрации 2 мкмоль/л. Потенциал действия усиливали, используя усилитель от Hugo Sachs (March-Hugstetten, Germany), сохраняли и анализировали с помощью компьютера. Продолжительность потенциала действия определяли при степени реполяризации 90% (АРD90). Сокращение потенциала действия вызывали добавлением раствора открывающего калиевые каналы вещества рилмакалима (НОЕ 234) (W.Linz et al., Arzneimittelforschung/Drug Research, 42 (II) (1992) 1180-1185) (концентрация рилмакалима 1 мкг/мл). Спустя 30 минут после ввода рилмакалима регистрировали продолжительность потенциала действия. Затем добавляли испытуемое вещество, и продолжительность потенциала действия, который вновь пролонгировали, регистрировали спустя еще 60 минут. Испытуемые вещества добавляли в раствор в ванне в виде основного раствора в пропандиоле.
Были зарегистрированы следующие величины APD90 (в миллисекундах):
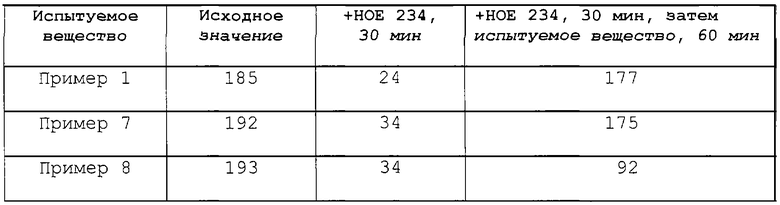
Найденные значения подтверждают нормализующее действие соединений по изобретению на сокращенную продолжительность потенциала действия.
Индуцированная хлороформом желудочковая фибрилляция у мышей (действие в случае вагусной дисфункции)
Гипофункция вагусной нервной системы приводит к гиперфункции симпатической нервной системы. Вред для здоровья, который является результатом неустойчивости автономной нервной системы, когда дисфункция связана с сердцем, включает ослабление сократительной способности миокарда и летальные сердечные аритмии, такие как желудочковая фибрилляция. Действие испытуемых соединений изучали на модели индуцированной хлороформом желудочковой фибрилляции у мышей (см. J.W.Lawson, Antiarrythmic activity of some isoquinoline derivativies determined by a rapid screening procedure in the mouse; J. Pharmacol. Exp. Ther. (1968) 160, 22).
Испытуемые вещества растворяли в смеси диметилсульфоксида (ДМСО) и 10%-ного раствора гидрокарбоната натрия и вводили внутрибрюшинно (i.p.). Спустя 30 минут мышь анестезировали хлороформом в лабораторном стакане. Как только под глубокой анестезией происходило угнетение дыхания (токсическая стадия анестезии), грудную клетку животного вскрывали парой ножниц и визуально контролировали сердечное сокращение. Можно было установить взглядом, бьется ли сердце, или фибриллирует, или остановилось. Угнетение дыхания, индуцированное хлороформом, приводит через абсолютную аноксию (кислородную недостаточность) в сочетании с прямым стимулирующим действием хлороформа на симпатическую нервную систему к сильному стимулированию симпатической нервной системы, что, в свою очередь, в сочетании с энергетической недостаточностью, вызванной в сердце недостатком кислорода, приводит к летальной аритмии - желудочковой фибрилляции. Такая токсическая хлороформовая анестезия приводит к желудочковой фибрилляции у 100% необработанных мышей (контроль). Процентная доля мышей, у которых наблюдалась желудочковая фибрилляция, в отдельных тестовых группах (с числом животных n) обозначена как коэффициент фибрилляции.
Были определены следующие коэффициенты фибрилляции:
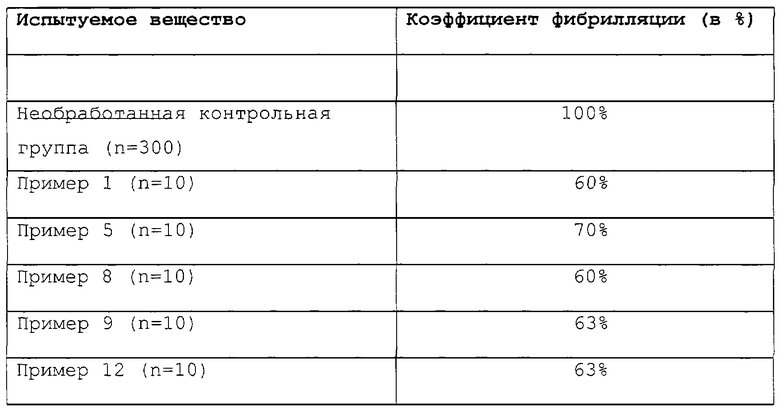
Снижение процентной доли мышей с желудочковой фибрилляцией по сравнению с контрольной группой (со 100% коэффициентом фибрилляции) подтверждает, что соединения формулы I существенно предотвращают наступление желудочковой фибрилляции.
Наблюдаемый эффект атропина, классического блокатора мускаринергических (вагусных) рецепторов автономной нервной системы, который блокирует действие вагусного медиатора ацетилхолина на уровне рецептора, позволяет сделать заключение о механизме действия. Эксперимент здесь проводили так, как описано выше. Соединение примера 8 вводили i.p. животным первой экспериментальной группы (n = число животных = 20) в количестве 10 мг/кг. Спустя 30 минут после введения животных анестезировали хлороформом и определяли коэффициент фибрилляции. Животным второй экспериментальной группы (n=10) вводили i.v. атропин в количестве 1 мг/кг. Спустя 15 минут после введения животных анестезировали хлороформом и определяли коэффициент фибрилляции. Животным третьей группы (n=10) сперва вводили i.p. соединение примера 8 в количестве 10 мг/кг и затем спустя 15 минут вводили i.v. атропин в количестве 1 мг/кг. Спустя 15 минут после введения животных анестезировали хлороформом и определяли коэффициент фибрилляции.
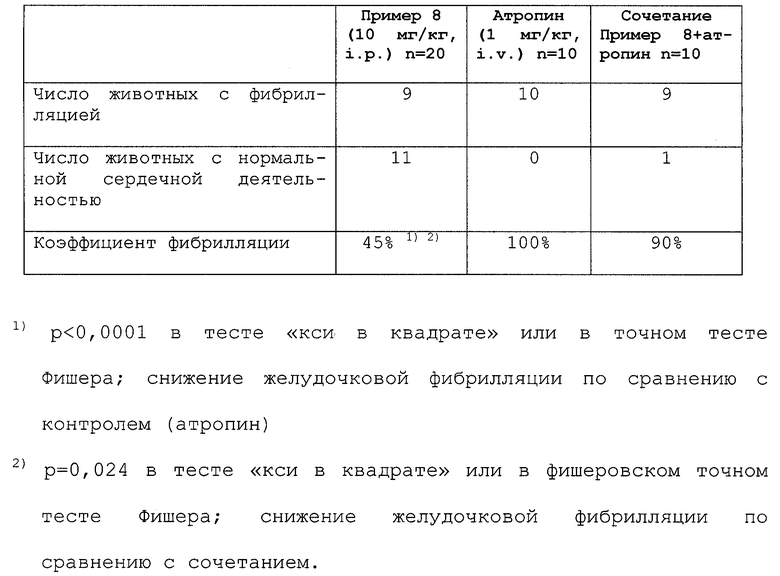
Результаты показывают, что атропин снижает или предотвращает защитное действие соединений формулы I. Такая отмена защитного действия соединений формулы I атропином ясно указывает на вагусный механизм действия.
Отсутствующее или лишь очень слабое гипогликемическое действие соединений формулы I может быть установлено, например, определением мембранного потенциала на изолированных β -клетках поджелудочной железы, например, по методу, описанному в US-A-5698596 или ЕР-А-612724, релевантное содержание которых является частью настоящего описания и включено здесь в качестве ссылки, или может быть показано на подходящих клетках млекопитающих, например, клетках СНО, которые трансфектированы протеинами человека SUR1/Kir6.2 в качестве молекулярных составляющих панкреатических АТФ-чувствительных калиевых каналов.
| название | год | авторы | номер документа |
|---|---|---|---|
| 1-(П-ТИЕНИЛБЕНЗИЛ)-ИМИДАЗОЛЫ В КАЧЕСТВЕ АГОНИСТОВ РЕЦЕПТОРОВ АНГИОТЕНЗИНА-(1-7) И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2000 |
|
RU2247121C2 |
| СОЕДИНЕНИЯ С МЕДИЦИНСКИМИ ЭФФЕКТАМИ, ОБУСЛОВЛЕННЫМИ ВЗАИМОДЕЙСТВИЕМ С РЕЦЕПТОРОМ ГЛЮКОКОРТИКОИДОВ | 2006 |
|
RU2430086C2 |
| ИМИДАЗО-АННЕЛИРОВАННЫЕ ИЗО- И ГЕТЕРОЦИКЛЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2076105C1 |
| 1,3,4-ОКСАДИАЗОЛТИОКАРБОНИЛЬНЫЕ СОЕДИНЕНИЯ В КАЧЕСТВЕ ИНГИБИТОРА ГИСТОНДЕАЦЕТИЛАЗЫ 6 И СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 2022 |
|
RU2831346C2 |
| ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ИНГИБИТОРОВ КИНАЗЫ-3 ГЛИКОГЕНСИНТАЗЫ | 2011 |
|
RU2623427C2 |
| НОВЫЕ АКТИВАТОРЫ РАСТВОРИМОЙ ГУАНИЛАТЦИКЛАЗЫ И ИНГИБИТОРЫ ФОСФОДИЭСТЕРАЗЫ С ДВОЙНЫМ МЕХАНИЗМОМ ДЕЙСТВИЯ И ИХ ПРИМЕНЕНИЕ | 2018 |
|
RU2758373C2 |
| ЦИКЛИЧЕСКИЕ АЗАИНДОЛ-3-КАРБОКСАМИДЫ, ИХ ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ | 2009 |
|
RU2487874C2 |
| НОВЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ ФТОРГЛИКОЗИДНЫЕ ПРОИЗВОДНЫЕ, СОДЕРЖАЩИЕ ЭТИ СОЕДИНЕНИЯ ЛЕКАРСТВЕННЫЕ СРЕДСТВА И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2339641C2 |
| СОЕДИНЕНИЯ ХИНОЛИНА, ПРИГОДНЫЕ ДЛЯ ЛЕЧЕНИЯ НАРУШЕНИЙ, ЯВЛЯЮЩИХСЯ ОТВЕТОМ НА МОДУЛЯЦИЮ РЕЦЕПТОРА 5-HT СЕРОТОНИНА | 2008 |
|
RU2483068C2 |
| НОВЫЕ АРОМАТИЧЕСКИЕ ФТОРГЛИКОЗИДНЫЕ ПРОИЗВОДНЫЕ, СОДЕРЖАЩИЕ ЭТИ СОЕДИНЕНИЯ ЛЕКАРСТВЕННЫЕ СРЕДСТВА, И ИХ ПРИМЕНЕНИЕ | 2003 |
|
RU2340622C2 |
Настоящее изобретение относится к циннамоиламиноалкилзамещенным производным бензолсульфонамида формулы (I),
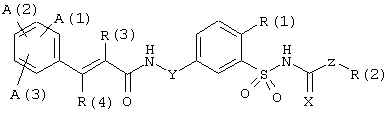
где Х представляет кислород, серу; Y представляет -(CR(5)2)n-; Z представляет NH или кислород. Соединения формулы (I) являются ценными фармацевтически активными соединениями, которые проявляют ингибирующее воздействие на АТФ-чувстительные калиевые каналы в сердечной мышце и пригодны для лечения расстройств сердечно-сосудистой системы. Изобретение, кроме того, относится к способу получения соединений формулы (I), возможному их применению и фармацевтической композиции на основе этих соединений. 5 н. и 9 з.п. ф-лы.
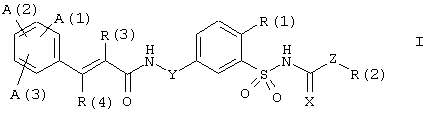
где Х представляет кислород или серу;
Y представляет -(CR(5)2)n-;
Z представляет NH или кислород;
остатки А(1), А(2) и А(3), которые не зависят друг от друга и могут быть идентичными или различными, представляют водород, галоген, (C1-C4)-алкил или (C1-C4)-алкокси;
R(1) представляет
1) -(C1-C4)-алкил; или
2) -О-(C1-C4)-алкил; или
3) -О-(C1-C4)-алкил-Е(1)-(C1-C4)-алкил-D(1), где D(1) представляет водород, Е(1) представляет О; или
5) -О-(С2-С4)-алкенил; или
6) -О-(C1-C4)-алкилфенил, в котором фенильная группа является незамещенной; или
7) -O-фенил, который является незамещенным; или
9) фенил, который является незамещенным; или
12) моноциклический гетероарил, содержащий в кольце один гетероатом кислорода;
R(2) представляет (C1-C6)-алкил;
остатки R(3) и R(4), которые не зависят друг от друга и могут быть идентичными или различными, представляют фенил, который является незамещенным, или водород или (C1-C4)-алкил;
остатки R(5), которые все не зависят друг от друга и могут быть идентичными или различными, представляют водород или (C1-С3)-алкил;
n равно 1, 2, 3 или 4;
во всех своих стереоизомерных формах и их смесях во всех соотношениях, и их физиологически переносимые соли; где исключены соединения формулы I, в которых одновременно Х представляет кислород, Z представляет NH, R(1) представляет (C1-C4)-алкил или -О-(C1-C4)-алкил и R(2) представляет (С2-С6)-алкил.
1) -О-(C1-C4)-алкил; или
2) -О-(C1-C4)-алкил-Е(1)-(C1-C4)-алкил-D(1), где D(1) представляет водород; или
4) -О-(C2-C4)-алкенил; или
5) -О-(C1-C4)-алкилфенил, в котором фенильная группа является незамещенной; или
6) -O-фенил, который является незамещенным; или
7) фенил, который является незамещенным; или
8) моноциклический гетероарил, содержащий в кольце один гетероатом кислорода;
во всех своих стереоизомерных формах и их смесях во всех соотношениях, и его физиологически переносимые соли.
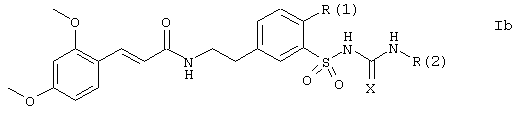
в котором Х представляет кислород или серу;
R(1) представляет метокси-, 2-метоксиэтокси-, аллилокси, бензилокси или фенокси;
R(2) представляет метил, этил или изопропил,
во всех своих стереоизомерных формах и их смесях во всех соотношениях, и его физиологически переносимые соли.
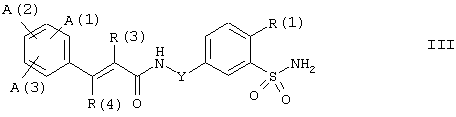
или его соли с изо(тио)цианатом формулы R(2)-N=C=X, причем А(1), А(2), А(3), R(1), R(2), R(3), R(4), X и Y являются такими, как определено в пп.1-7.
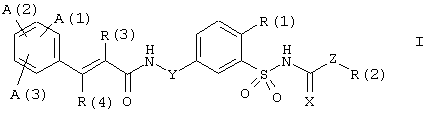
где Х представляет кислород или серу;
Y представляет -(CR(5)2)n-;
Z представляет NH или кислород;
остатки А(1), А(2) и А(3), которые не зависят друг от друга и могут быть идентичными или различными, представляют водород, галоген, (C1-C4)-алкил или (C1-C4)-алкокси;
R(1) представляет
1) (C1-C4)-алкил; или
2) -О-(C1-C4)-алкил; или
3) -О-(C1-C4)-алкил-Е(1)-(C1-C4)-алкил-D(1), где D(1) представляет водород, Е(1) представляет О; или
5) -О-(С2-С4)-алкенил; или
6) -О-(C1-C4)-алкилфенил, в котором фенильная группа является незамещенной; или
7) -O-фенил, который является незамещенным; или
9) фенил, который является незамещенным; или
12) моноциклический гетероарил, содержащий в кольце один гетероатом из группы, состоящей из кислорода;
R(2) представляет (C1-С6)-алкил;
остатки R(3) и R(4), которые не зависят друг от друга и могут быть идентичными или различными, представляют фенил, который является незамещенным, или водород или (C1-C4)-алкил;
остатки R(5), которые все не зависят друг от друга и могут быть идентичными или различными, представляют водород или (C1-С3)-алкил;
n равно 1, 2, 3 или 4;
во всех своих стереоизомерных формах и их смесях во всех соотношениях, и их физиологически переносимые соли, пригодные для ингибирования АТФ-чувствительных калиевых каналов или для стимуляции вагусной нервной системы.
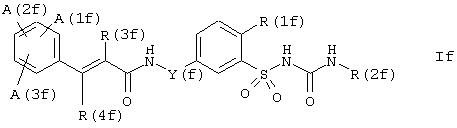
где Y(f) представляет -(CR(5f)2)n-;
остатки A(1f), A(2f) и A(3f), которые не зависят друг от друга и могут быть идентичными или различными, представляют водород, галоген, (C1-C4)-алкил или (C1-C4)-алкокси;
R(1f) представляет -О-(C1-C4)-алкил;
R(2f) представляет (С2-С6)-алкил или (С5-С7)-циклоалкил;
остатки R(3f) и R(4f), которые не зависят друг от друга и могут быть идентичными или различными, представляют водород или (C1-C4)-алкил;
остатки R(5f), которые все не зависят друг от друга и могут быть идентичными или различными, представляют водород или (C1-С3)-алкил;
n(f) равно 1, 2, 3 или 4;
во всех своих стереоизомерных формах и их смесях во всех соотношениях, и его физиологически переносимые соли.
| RU 96102869 A1, 10.05.1998.DE 1443878 A, 12.12.1968.EP 612724 A, 31.08.1994. |
Авторы
Даты
2004-12-20—Публикация
2000-05-06—Подача