Изобретение относится к медицине, точнее иммунодиагностике и может найти применение для обнаружения рецидива и метастазов до их клинического проявления у больных раком легкого и определения сроков противоопухолевой терапии после проведения оперативного удаления очага поражения.
Показания к проведению послеоперационной химио- и лучевого лечения определены в достаточной мере. Они показаны при мелкоклеточном и низкодифференцированных формах рака легкого, III стадии заболевания, метастатическом поражении лимфатических узлов корня легкого, средостения. Однако у 20-30% больных с I стадией заболевания и при отсутствии метастазов в лимфатических узлах в дальнейшем также могут выявляться метастазы и рецидивы. В настоящее время нет метода, определяющего показания в этой группе больных, для проведения послеоперационного противоопухолевого лечения. В то же время остается открытым вопрос о продолжительности и количестве курсов при проведении химиотерапии. Предлагается проводить от одного до 3-4 и даже 7 курсов лечения в первые 2 года после операции, когда наиболее вероятно повторное прогрессирование болезни (Трахтенберг А.Х. с соавт. Комбинированное лечение рака легкого. Вопросы онкологии, 1987 г. №10, Т.25, стр.25-31). Объективных же критериев и методов контроля за проведением послеоперационной химиотерапии не предложено. Таким образом, очевидна актуальность поиска и разработки информативных методов для раннего выявления рецидива и метастазов после операций при раке легкого, а также критериев для определения режима проведения послеоперационного профилактического лечения.
Известен способ диагностики скрытых метастазов и рецидивов рака легкого с помощью диагностических сывороток к 3-оксиантраниловой кислоте (ОАК), уровень которой повышается при опухолевом процессе. Диагностические сыворотки получают после иммунизации кроликов 3-ОАК антигеном (Вестник хирургии им. Грекова, 1984 г. №4).
Применяемый авторами способ обнаружения рецидивов и метастазов не только длителен по времени его выполнения, но и не обладает достаточной диагностической чувствительностью и специфичностью. Упомянутый способ является весьма трудоемким в выполнении.
В качестве прототипа нами избран “Способ выявления скрытого метастазирования при увеальной меланоме”, патент №2147373, G 01 N 33/53, Российской Федерации. Авторы избрали в качестве определяющего теста исследование иммунокомпетентных клеток периферической крови, при этом оценку проводят по количественному подсчету субпопуляций Т-лимфоцитов CD3, CD4, CD8 и индекса их соотношения и при отклонении всех указанных показателей от нормы ≤1,0 или ≥2,0 констатируют наличие скрытого метастазирования.
Для определения субпопуляций Т-лимфоцитов используют проточную цитофлуорометрию. Лимфоциты выделяют из гепаринизированной крови центрифугированием на градиенте Фиколл-Верографина (плотность 1,077 г/мл). 1-0,1 млн лимфоцитов в объеме 50 мкл вносят в центрифужные пробирки или лунки 96-луночного круглодонного планшета. К клеткам добавляют 5 мкл тестируемого моноклонального антитела (к CD3, CD4, CD8 дифференцировочным антигенам Т-лимфоцитов) и инкубируют 30-45 минут. Добавляют 150 мкл раствора Хенкса и центрифугируют 5 минут при 200 g. К осадку отмытых клеток добавляют 150 мкл F(ab’)2 - фрагментов овечьих антител к Ig G мыши, меченных ФИТЦ и разведенных 1/100. Для разведения используют физраствор, забуференный фосфатами (PBS), содержащий 0,5% желатины и 0,1% азида натрия. Клетки суспендируют и инкубируют 30 мин при +4°С. Клетки 2 раза отмывают: добавляют 150 мкл раствора Хенкса и центрифугируют 5 минут при 200 g. Удаляют супернатант. Затем вносят 50 мкл раствора Хенкса, клетки суспендируют, добавляют 150 мкл раствора Хенкса и центрифугируют 5 минут при 200 g. Окрашенные клетки анализируются на проточном цитометре или просматриваются с помощью флюоресцентного микроскопа. Количество антигенпозитивных клеток определяют как % флюоресцирующих клеток при просматривании 200 лимфоцитов за вычетом % флюоресцирующих клеток в препарате контроля. В качестве отрицательного контроля используют препараты, подготовленные аналогичным образом, за исключением того, что вместо моноклональных антител клетки обрабатывают раствором Хенкса или нормальным Ig G мыши. После подсчета нужных клеток производят расчет отношения клеток друг к другу и прогнозируют развитие метастазов или рецидивов.
Указанный способ также имеет недостатки, к которым относятся длительность его выполнения, до 3-х месяцев, неспецифичность способа и высокая трудоемкость.
Целью настоящего изобретения является возможность выявления рецидивов и метастазов на их доклиническом этапе и осуществление противоопухолевой терапии в более ранние сроки.
Поставленная цель достигается тем, что в сыворотке крови больных раком легкого через 2 недели и в течение последующих 2 лет после оперативного удаления опухоли в реакции пассивной гемагглютинации исследуют уровень антител к антигенам опухоли легкого и при показателе 1/8 и выше констатируют наличие рецидива или метастаза и проводят противоопухолевую химиотерапию, а при уровне антител в титре 1/4 противоопухолевую химиотерапию отменяют.
Анализ существующих известных способов выявления рецидивов и метастазов рака легкого после оперативного удаления очага поражения и предлагаемого “Способа прогнозирования рецидивов и метастазов рака легкого” позволяет говорить о новизне последнего. Новизна заявляемого способа заключается в определении в сыворотке крови больного в различные сроки после операции, с помощью реакции пассивной гемагглютинации (РПГА), уровня антител к антигенам опухоли легкого и по их динамике в проведении соответствующего противоопухолевого лечения.
Предлагаемый “Способ прогнозирования рецидивов и метастазов рака легкого” является промышленно применимым, так как может быть воспроизведен и многократно повторен в лечебных учреждениях специализированного профиля при наличии возможности проведения реакции пассивной гемагглютинации с целью выявления антител к антигенам опухолевой ткани легкого.
Способ осуществляется следующим образом.
Для постановки реакции исследуемую сыворотку адсорбируют формалинизированными эритроцитами барана в течение 1 часа при температуре 37°С, затем центрифугируют при 3 тыс. оборотов в минуту в течение 15 минут, надосадочную жидкость инактивируют на водяной бане в течение 30 минут при 56°С. Затем сыворотку дополнительно адсорбируют эритроцитарным диагностикумом, содержащим антиген из нормальной ткани легкого, при температуре 37°С в течение 1 часа, соотношение сыворотки и диагностикума 1:2. Из обработанной таким образом сыворотки готовят двукратные разведения в объеме 0,05 мкл в микропластинах Такачи. В каждую из лунок с разведенной сывороткой прибавляют по 0,025 мл опухолевого эритроцитарного диагностикума, пластины встряхивают и оставляют при комнатной температуре. Учет реакции производят через 3 часа. Титром сыворотки считают ее наибольшее разведение, которое дает положительную реакцию с диагностикумом. При титре реакции более или равным 1/8 реакцию считают положительной. Контролем специфичности РПГА служит реакция торможения пассивной гемагглютинации (РТПГА). В лунках микропластин Такачи готовят двукратные разведения сыворотки в объеме 0,025 мл, добавляют 0,025 мл антигена в количестве 10-20 минимальных нейтрализующих доз и оставляют при 37°С на 1 час, по истечении указаного срока в каждую лунку добавляют эритроциты, сенсибилизированные аналогичным антигенным препаратом. После добавления эритроцитов пластины встряхивают и оставляют при комнатной температуре. Если активность антител подавлялась антигеном в 4-8 раз (2-3 лунки), то РТПГА считают положительной.
Для приготовления эритроцитарных диагностикумов с антигенами нормальной ткани легкого и антигенами опухолевой ткани легкого используют формалинизированные эритроциты барана, полученные по методу Чизмеса в модификации Леви М.И. (1962 г.), обработанные раствором танина в разведении 1:20000 в течение 30 минут при температуре 37°С. Отмытые от танина эритроциты сенсибилизируют антигенными препаратами, полученными из нормальной и опухолевой ткани легкого методом β-нафтоловой экстракции, изложенным в описании к патенту РФ №1623429 от 10.12.1992, БИ №3, 1995 г. К танизированным эритроцитам добавляют тканевый антиген из расчета 20 мкг антигена по белку на 1 мл эритроцитов; ставят на сенсибилизацию в термостат.
Исследование сыворотки больных проводят на разных сроках послеоперационного периода. Нарастание титра антител в динамике, в отдаленные сроки послеоперационного периода от 2 недель до 2 лет до титра 1/8 и более или отсутствие значительного снижения титра антител до полного отсутствия (титр <1/4) в течение 0,5 лет после операции свидетельствует о прогрессировании опухолевого процесса. В соответствии с этим проводят назначение курса химиотерапии, направленного на подавление последнего. Последующее снижение титра антител менее 1/8 позволяет прекращать химиотерапию.
Примером конкретного выполнения заявленного способа могут служить выписки из историй болезни.
Пример 1: Больной А. 1946 г.р. поступил в торакальное отделение РНИОИ 27.12.1999 г. с клиническим диагнозом: периферический рак верхней доли правого легкого, III В стадия Т3 N0 M0. 05.01.2000 г. произведена операция верхняя лобэктомия. После операции произведен курс химиотерапии и лучевой терапии. Титр антител через 2 недели -1/64, через 5 месяцев антител в крови не обнаружено (титр <1/4). Через 9 месяцев после операции титр антител 1/8. Вскоре после повышения титра антител у больного появились боли в грудном отделе позвоночника и рентгенологически выявлен метастаз в 10 грудной позвонок. Титр повысился до 1/128. Больной умер через месяц после клинически и рентгенологически выявленного метастаза.
Пример 2: Больная В. 1952 г.р. поступила в торакальное отделение РНИОИ 17.01.2000 г. с клиническим диагнозом: периферический рак верхней доли правого легкого, I В стадия Т2 N0 M0. 31.01.2000 г. произведена операция: верхняя лобэктомия справа. После операции титр антител долгое время оставался высоким. Через 2 недели после операции - 1/128, через 6 месяцев - 1/16. Больная была вызвана на курс химиотерапии. Однако через 3 недели появилась клиника метастаза в мозг. Больная умерла через 2 месяца.
Пример 3: Больной С. 1943 г.р. поступил в торакальное отделение РНИОИ с диагнозом: центральный рак левого легкого, II В стадия T3N0 М0. 24.04.01 выполнена операция: левосторонняя пневмонэктомия. Через 3 месяца после операции титр антител составил 1/32. Через полгода после операции антитела в крови не выявлялись (титр антител <1/4). Через 10 месяцев титр антител также составил <1/4. Клинических данных за рецидив или метастаз нет. Продолжается наблюдение.
Пример 4: Больной Д. 1934 г.р. поступил в торакальное отделение РНИОИ с диагнозом: центральный рак левого легкого, III В стадия Т2 N1 М0. 27.12.2000 г. выполнена операция: левосторонняя пневмонэктомия. Через 3 месяца после операции титр антител составил 1/64. После операции в связи с тяжелым состоянием больного химиотерапия не проводилась. Но, учитывая, что спустя полгода после операции титр антител был 1/16, проведен курс химиотерапии. После курса химиотерапии антитела в сыворотке крови не обнаружились (титр <1/4). После курса химиотерапии прошло 5 месяцев, антитела в реакции пассивной гемагглютинации не выявляются (титр <1/4). Клинических данных за рецидив и метастазы нет.
Пример 5: Больной С. 1937 г.р. поступил в торакальное отделение РНИОИ с диагнозом: периферический рак правого легкого, I стадия. 05.07.2000 г. произведена клиновидная резекция верхней доли правого легкого. После операции проведен курс лучевой терапии. Через 3 месяца после операции титр антител составил 1/16. На сроке 6 месяцев после операции в РПГА антитела не выявлялись (титр <1/4). Еще через 3 месяца титр антител повысился до 1/32. Назначен курс химиотерапии. После курса химиотерапии титр антител снизился до <1/4. Клинических данных за рецидив и метастазы нет. Продолжается наблюдение.
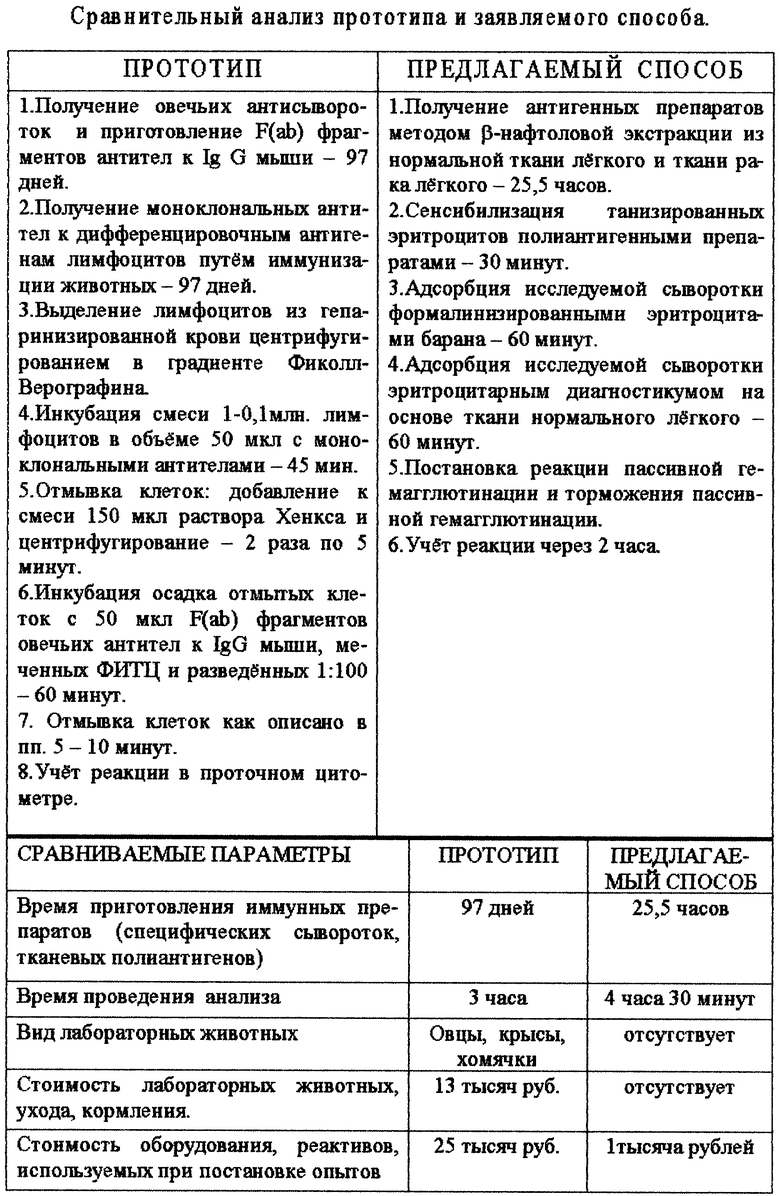
Заявленным способом было обследовано в различные сроки после операции более 150 больных раком легкого. При разработке и на стадии его клинической апробации были выявлены существенные преимущества разработанного технического решения, доказательством может служить таблица.
Технико-экономическая эффективность “Способа прогнозирования рецидивов и метастазов рака легкого" заключается в возможности выявить рецидив заболевания или метастатическое проявление последнего в более ранние сроки; провести своевременное лучевое и/или химиотерапевтическое лечение или исключить проведение высокотоксичных видов противоопухолевой терапии.
| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ДИАГНОСТИКИ ДОБРОКАЧЕСТВЕННЫХ И ЗЛОКАЧЕСТВЕННЫХ ГЛИАЛЬНЫХ ОПУХОЛЕЙ | 1999 |
|
RU2154830C1 |
| Способ диагностики тугоухости | 1985 |
|
SU1332230A1 |
| Способ прогнозирования течения аденокарциномы легкого | 2018 |
|
RU2706116C1 |
| СПОСОБ ПРОГНОЗИРОВАНИЯ ЭФФЕКТИВНОСТИ ПРОТИВООПУХОЛЕВОГО ЛЕЧЕНИЯ | 2009 |
|
RU2411913C1 |
| СПОСОБ КОМПЛЕКСНОГО ЛЕЧЕНИЯ РАКА ЛЕГКОГО | 2003 |
|
RU2257218C1 |
| Способ определения эффективности химиотерапии препаратами платины при раке яичников III-IV стадии | 2020 |
|
RU2738167C1 |
| СПОСОБ ЛЕЧЕНИЯ МЕСТНО-РАСПРОСТРАНЕННОГО РАКА ЛЕГКОГО | 2007 |
|
RU2348420C2 |
| Способ диагностики новообразований голов-НОгО МОзгА | 1977 |
|
SU664505A1 |
| Способ лечения онкологической боли | 2019 |
|
RU2707954C1 |
| СПОСОБ ЛЕЧЕНИЯ РАКА ЛЕГКОГО | 2009 |
|
RU2406452C1 |
Изобретение относится к иммунодиагностике и может быть использовано для обнаружении рецидивов и метастазов до их клинического проявления у больных раком легкого и определения сроков и вида противоопухолевой терапии после проведения оперативного удаления очага поражения. Сущность способа заключается в том, что с помощью реакции пассивной гемагглютинации исследуют уровень антител к антигенам опухоли легкого и при показателе 1/8 и выше констатируют наличие рецидива или метастаза и проводят противоопухолевую химиотерапию, а при уровне антител 1/4 противоопухолевую химиотерапию отменяют. Техническим результатом является раннее выявление рецидивов или метастазирования и проведение своевременного лечения. 1 табл.
Способ прогнозирования рецидивов и метастазов рака легкого путем исследования сыворотки крови больного в различные после операции сроки, отличающийся тем, что с помощью реакции пассивной гемагглютинации исследуют уровень антител к антигенам опухоли легкого и при показателе 1/8 и выше констатируют наличие рецидива или метастаза и проводят противоопухолевую химиотерапию, а при уровне антител 1/4 противоопухолевую химиотерапию отменяют.
| ЧИССОВ В.И | |||
| и др | |||
| Видоизменение пишущей машины для тюркско-арабского шрифта | 1923 |
|
SU25A1 |
| Российский онкологический журнал | |||
| Электрическое сопротивление для нагревательных приборов и нагревательный элемент для этих приборов | 1922 |
|
SU1997A1 |
| US 5965360 А, 12.10.1999 | |||
| RAY P | |||
| et al | |||
| Productive factors of tumor response and prognostic factors of survival during lung cancer chemotherapy | |||
| Cancer Detect Prev | |||
| Способ и аппарат для получения гидразобензола или его гомологов | 1922 |
|
SU1998A1 |
Авторы
Даты
2004-12-27—Публикация
2003-04-21—Подача