В течение последних нескольких лет в патентной и технической литературе сообщалось о соединениях, обладающих как активностью, ингибирующей фермент, конвертирующий ангиотензин (АСЕ), так и активностью, ингибирующей нейтральную эндопептидазу (ЕС24 11, NEP). Эти соединения представляют интерес как сердечно-сосудистые агенты, особенно при лечении гипертонии, застойной сердечной недостаточности и почечного заболевания. Эти соединения известны также как ингибиторы вазопептидазы, двойственной металлопротеазы, NEP/ACE или ACE/NEP. Омапатрилат является таким ингибитором вазопептидазы, который в настоящее время подвергается клиническим исследованиям. Омапатрилат имеет химическое наименование [4S-[4α(R*), 7α, 10αβ]]октагидро-4-[(2-меркапто-1-оксо-3-фенил-пропил)амино]-5-оксо-7Н-пиридо[2,1-b][1,3]тиазепин-7-карбоновая кислота и структурную формулу:
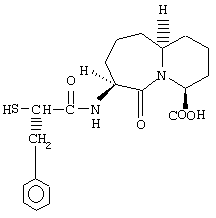
Омапатрилат, его получение и его применение для лечения сердечно-сосудистых заболеваний описаны в патенте США 5508272.
BMS 189921 является другим ингибитором вазопептидазы, который в настоящее время подвергается клиническим исследованиям. BMS 189921 представляет собой [S-(R*, R*)]гексагидро-6-[(2-меркапто-1-оксо-3-фенилпропил)амино]-2,2-диметил-7-оксо-1Н-азепин-1-уксусную кислоту структурной формулы:
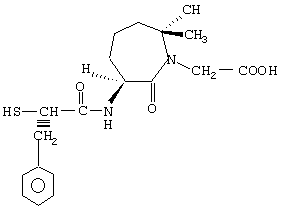
BMS 189921, его получение и его применение при лечении сердечно-сосудистых заболеваний описаны в патенте США 5552394.
Сущность изобретения
Данное изобретение направлено на применение ингибитора вазопептидазы для лечения и/или облегчения симптомов стенокардии. Предпочтительными для этой цели ингибиторами вазопептидазы являются омапатрилат или его фармацевтически приемлемая соль, BMS 189921 или его фармацевтически приемлемая соль или их смеси. Наиболее предпочтительно применение омапатрилата.
Согласно настоящему изобретению для лечения стенокардии можно применять один или несколько ингибиторов вазопептидазы в отдельности или в сочетании друг с другом. Ингибитор или ингибиторы вазопептидазы могут также применяться в сочетании с одним или более фармацевтически активными агентами, известными для лечения стенокардии. Такие агенты включают длительно действующие нитраты, β-адренергические блокирующие агенты, блокаторы проникновения кальция, антитромбины и т.д. Комбинационная терапия может использовать препарат в виде единичных доз, содержащий ингибитор или ингибиторы вазопептидазы или их фармацевтически приемлемые соли, и другой агент или агенты, применяемые для лечения стенокардии, совместное введение отдельных доз каждого активного агента или введение отдельных доз каждого активного агента в соответствии с установленной схемой.
Краткое описание фигур
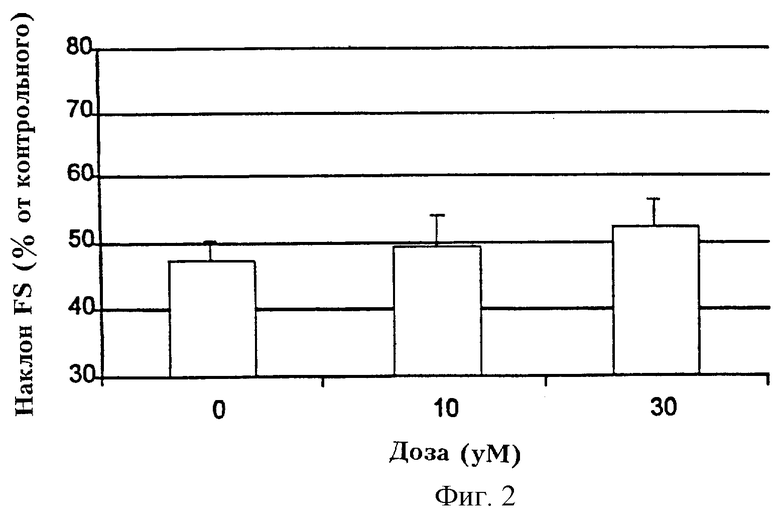
На Фиг.1 представлен график, показывающий действие ингибитора вазопептидазы омапатрилата, что отражает наклонная линия Франка-Старлинга, через 30 минут после развития ишемии на модели изолированного перфузного сердца крысы.
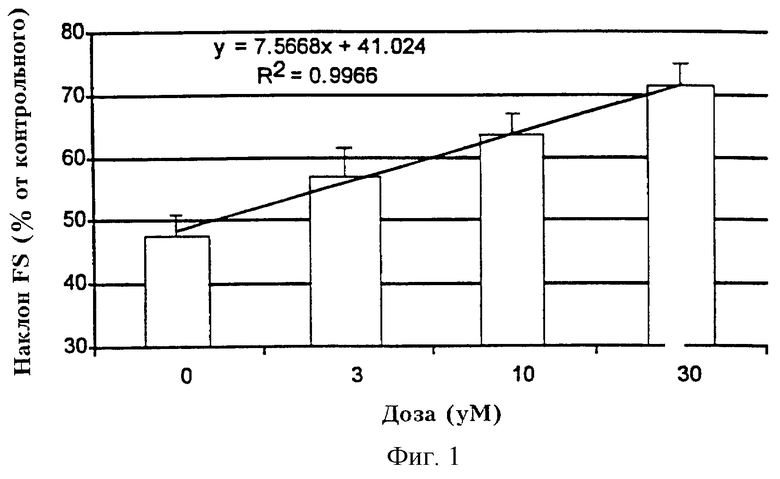
На Фиг.2 представлен график, отражающий действие ингибитора фермента, конвертирующего селективный ангиотензин, фосиноприлата, отраженное на наклонной линии Франка-Старлинга на той же модели изолированного перфузного сердца крысы.
Подробное описание изобретения
Стенокардия обычно описывается как недомогание в загрудной области, проявляющееся в виде сжатия, или давления, или ощущения воспаления. Характерно, что она не характеризуется каким-либо определенным местом, то есть больной не может показать точное место, где болит. Дискомфорт может ощущаться в левом плече или руках или в шее и челюсти. Некоторые больные описывают стенокардию нетипичными терминами как "резкую боль при метеоризме", дискомфорт только в области челюстей, зубов, предплечья или спины или дискомфорт, начинающийся в эпигастральной области и распространяющийся на грудную область. Некоторые пациенты описывают ее как затруднение дыхания без ощущения дискомфорта, этот симптом называется одышкой эквивалентной стенокардии.
Стенокардия возникает, когда потребность в миокардиальном кислороде возрастает до уровней, которым не удовлетворяет возросший ток коронарной крови, обычно вследствие стенозных атеросклеротических поражений в одном или нескольких эпикардиальных коронарных сосудах. Соответственно, стенокардия обычно возникает при физическом истощении или эмоциональном стрессе. Большинство пациентов с устойчивой стенокардией могут назвать особые виды активности или ситуации, которые предсказуемо избавят от дискомфорта; типичными примерами являются прогулка по пологой поверхности или ускоренная ходьба. Не является необычным разный порог усилий. Деятельность в холодную погоду, после еды или ранним утром скорее всего может вызвать приступ стенокардии. Некоторые пациенты сообщают, что усилия с поднятыми над головой руками вызывают ощущение дискомфорта. Различные пороговые усилия, приводящие к развитию стенокардии у некоторых пациентов, наводят на мысль, что динамические изменения тока коронарной крови (например, вследствие скачкообразного увеличения коронарного вазомоторного тона) приводят к фиксированному атеросклеротическому стенозу в ограничении тока крови. Приступы устойчивой стенокардии обычно возникают постепенно и длятся 2-10 минут. Дискомфорт обычно быстро исчезает при отдыхе или подъязычном введении нитроглицерина.
Вызванная стрессом стенокардия возникает также у некоторых пациентов с вальвулярным стенозом аорты, с гипертрофией левого желудочка или легочной коронарной гипертензией в отсутствие значительного стеноза коронарных артерий. В этих ситуациях даже нормальный коронарный ток крови может быть недостаточным для удовлетворения потребности в повышенном количестве миокардиального кислорода. Стенокардия может также развиться у лиц с очень дилатированными левыми желудочками, особенно в случаях, когда это сопровождается пониженным диастолическим коронарным давлением перфузии, как при аортальной регургитации.
Стенокардия, которая развилась недавно или внезапно прогрессировала по степени серьезности, частоты или длительности приступов - особенно если она сопровождается остаточной болью, считается неустойчивой. Пациенты с недавними приступами стенокардии, особенно если они происходят при низкой активности или во время отдыха, также относятся к этой категории. Большинство пациентов с неустойчивой стенокардией страдают обструктивным коронарным заболеванием; непредсказуемый приступ болезни или переход от устойчивой к неустойчивой форме обычно возникает при образовании щели в атеросклеротической бляшке с наложением тромбоцита или обогащенного фибрином тромба.
Неустойчивая форма может осложняться также экстракоронарными факторами (вторичная неустойчивая стенокардия). Сильная анемия или воздействие окиси углерода, например, ограничивает способность крови переносить или выделять кислород и может привести к возникновению стенокардии в условиях, которые пациент с коронарным заболеванием обычно хорошо переносит. Неконтролируемая системная артериальная гипертония, сильная аритмия или гипоксемия вследствие легочного заболевания могут также спровоцировать развитие стенокардии, как и гипертиреоз. Стенокардия Принцметала похожа по характеру и месту возникновения болей на устойчивую стенокардию и часто реагирует на нитроглицерин. Характерно, что ее приступы возникают в состоянии покоя, однако без очевидной провокации или предшествующего увеличения пульса или кровяного давления. Эти признаки объясняются механизмом возникновения приступа: скоротечным спазмом коронарной артерии. Часто это происходит ранним утром. Некоторые пациенты, страдающие стенокардией Принцметала, сообщают о других вазомоторных симптомах, таких как мигрень или феномен Рейно, см. Textbook of lnternel Medicine, Third Edition, pages 316-317 (1997).
Данное изобретение направлено на применение одного или нескольких ингибиторов вазопептидазы для лечения и/или облегчения симптомов стенокардии. Предпочтительными для этой цели ингибиторами вазопептидазы являются омапатрилат или его фармацевтически приемлемая соль и BMS 189921 или его фармацевтически приемлемая соль, особенно омапатрилат. Ингибитор вазопептидазы можно вводить пациенту, страдающему стенокардией, в количестве от примерно 0,1 мг/кг до примерно 2,0 мг/кг в течение 24 часов, предпочтительно от примерно 0,3 мг/кг до примерно 1,0 мг/кг за 24 часа. Ингибитор вазопептидазы можно вводить в течение 24 часов одной или несколькими дозами, чтобы обеспечить общее количество активного вещества в вышеуказанных пределах. Если в течение 24 часов вводится более одной дозы, эти дозы могут быть равными или же они могут меняться. Конечно, количество применяемого активного вещества регулируется врачом в зависимости от типа и серьезности стенокардии. Если же применяют комбинацию ингибиторов вазопептидазы, то один или оба ингибитора можно вводить в меньшем количестве, при условии, что общее их количество находится в вышеуказанных пределах.
Ингибитор вазопептидазы предпочтительно вводить перорально в виде таблетки или капсулы. Однако можно использовать и другие методы введения, включая подъязычный, буккальный, парентеральный, например, подкожный, внутривенную или внутримышечную инъекцию или метод инфузии, через нос, например, при ингаляции, локальный, например, в виде крема или мази, черескожный, например, в виде пластыря, накладываемого на кожу, или ректальный, например, в виде суппозиториев. Различные дозированные препараты кроме ингибитора вазопептидазы содержат обычные фармацевтически приемлемые носители, стабилизаторы, консерваторы, смазывающие агенты, разбавители и другие обычные добавки. Препарат может использоваться для немедленного высвобождения или замедленного высвобождения.
Другим аспектом настоящего изобретения является способ лечения стенокардии одним или несколькими ингибиторами вазопептидазы, как указано выше, в сочетании с другим классом фармацевтически активных веществ, применяемых при лечении стенокардии. Такие вещества включают длительно действующие нитраты, например, нитроглицерин, мононитрат изосорбида, динитрат изосорбида, β-адренергические блокаторы, например, гидрохлорид пропанолола, малеат тимолола, карведилол, тартрат и атенолол и блокаторы поступления кальция, такие как бесилат амлодипина, дилтиаземгидрохлорид и верапамилгидрохлорид. Настоящее изобретение также относится к комбинации одного или нескольких ингибиторов вазопептидазы и фармацевтически активных веществ, используемых при лечении стенокардии, таких как антитромбины. Такие антитромбины включают клопидогрел, тиклопидин, аспирин и дипиридамол. При такой комбинированной терапии обычно применяют такое количество длительно действующего нитрата, β-адренергического блокатора, блокатора поступления кальция и/или антитромбина, которое уже рекомендовано для лечения стенокардии или же врачом назначается меньшее количество. Точно также при комбинированной терапии количество ингибитора вазопептидазы может быть меньше, чем указанное выше при монотерапии. Ингибитор вазопептидазы и другой фармацевтически активный агент или агенты могут применяться в виде одной дозированной формы, или же вводиться совместно в виде отдельных дозированных форм, или применяться раздельно в соответствии с назначенной схемой.
Термин "фармацевтически приемлемая соль" включает соли щелочных металлов, например, натрия и калия, соли щелочноземельных металлов, например, кальция и магния, соли аминокислот, таких как аргинин, лизин и т.д. и соли аминов, таких как алкиламины, например, трет.бутиламин, трет.амиламин и т.д., замещенных алкиламинов, например, бензиламина, диалкиламинов, замещенных диалкиламинов, например, N-метилглюкамина, триалкиламинов, замещенных триалкиламинов, и четвертичные аммониевые соли. Нижеследующие примеры иллюстрируют активность ингибитора вазопептидазы омапатрилата против стенокардии.
Пример 1.
Модель изолированного перфузного сердца крысы, пораженного ишемией.
Методика.
Самцам крыс Sprague-Dawley (350-450 г) накануне не давали еды и затем анестезировали их пентобарбиталом натрия (30-40 мг/кг, внутрибрюшинно). Осуществляли интубацию путем рассечения трахеи, после чего искусственная вентиляция животных осуществлялась при помощи респиратора (Model 683, Harvard Instruments, South Natick, MA) с приливно-отливным объемом 4-5 мл, доставляемьм со скоростью 65-75 дыхании/мин и проводилась антикоагуляция гепарином натрия (1000 м. ед/кг) через наружную яремную вену. Осуществляли торакотомию и ретракцию ребер и обнажали сердце. Перикард удаляли и очищали восходящую часть аорты от соединительных тканей. Вокруг основания аорты для закрепления канюли для перфузии помещали шелковую нить 2-0. Затем зажимали нижнюю полую вену и делали разрез в основании аорты. В разрез быстро вставляли стальную канюлю, соединенную с запорным краном и закрепляли ее нитью. Проводили ретроградную экстракорпоральную перфузию оксигенированным (95% кислорода, 5% двуокиси углерода, рН 7,4) раствором Krebs-Henseleit, содержащим (в мМ) 1,25 хлорида кальция, 112 хлорида натрия, 25 бикарбоната натрия, 5 хлорида калия, 1 дифосфата калия, 1,2 сульфата магния и 5,5 декстрозы. Затем сердце помещали в стандартный аппарат Langendorff для перфузии (Doring et aL, The isolated perfused warmblooded heard according to Langendorff, 1st ed. March: Biomesstechnik-Verlag; 1988), где осуществляли перфузию оксигенированным буфером Krebs-Henseleit, нагретьм до 37°С, при постоянном давлении перфузии, равным 86 мм рт. ст. Наполненный водой баллончик, изготовленный из латекса, извлекали из держателя (#55613-413, VWR Scientific, S. Plainfield, NJ) и прикрепляли к канюле из нержавеющей стали (модель LL2, Hugo Sachs, March-Hugstetten, Germany), которую затем помещали в левый желудочек. Канюлю прикрепляли к датчику давления (модель Р23, Gould Instruments, Valley View, ОН) для измерения возникшего в желудочке усилия. Затем сердце помещали в баню с водяной рубашкой (37°С). Ток перфузата контролировали при помощи экстракорпорального электромагнитного пробника (модель MDL 1401, Skalar Instruments, Litchfield, CT). Сердца бились с нормальной частотой. Все данные постоянно представлялись в цифровом виде при частоте 250 Гц для последующего анализа (Po-Neh-Mah Acquisition System, Gould Instruments, Valley View, ОН). Исходя из полученных цифровых данных получали устойчивые величины частоты сердечных сокращений, тока перфузата и развившегося в левом желудочке давления (LV систолическое - LV конечное диастолическое давление) во время исследования, предварительного введения лекарства, пониженной скорости потока. Сердца препарировали и исследовали в квадрипликате.
Работа желудочка.
Периодические независимые индексы работы миокарда получали в виде средней величины наклона линейной части триплетных кривых Frank-Starling (FS) [Schlant, Normal physiology of the cardiovascular system. In: Hurst JW, ed. The Heart, 4th ed. New York: McGraw-Hill; 1978: 71-100]. Записывали также и усредняли среднее пиковое значение давления, развившегося в левом желудочке (LVDPmax, полученного во время каждой дискретной серии кривых FS. Кривые FS получали путем надутия баллона, находящегося в желудочке с постоянной скоростью 50 мкл/мин при помощи насоса с программируемым циклом вздутие/спуск (модель 44, Harvard Apparatus, South Natick, MA). Надутие баллона прерывали в момент наклона сегмента кривой FS, определенного в точке, где давление, развившееся в левом желудочке (LVDP), снижалось с дальнейшим увеличением объема баллона (предварительная загрузка). Затем объем баллона уменьшали со скоростью 300 мкл/мин до тех пор, пока LVDP не перестает измеряться (<2 мм рт.ст.). Этот процесс повторяли до получения трех воспроизводимых кривых.
Приготовление лекарственного препарата и введение его.
Испытуемые соединения растворяли в диметилсульфоксиде (DMSO) в количестве 2500х концентрацию, доставляемую в организм, и затем вливали раствор в дистальный перфузионный поток каждого сердца при помощи программируемого насоса (модель 22, Harvard Apparatus, South Natick, MA). Каждый насос управлялся компьютерной программой, которая непрерывно регистрировала перфузионный поток в каждом сердце и динамически регулировала скорость вливания испытуемого соединения для поддержания концентрации в ДМСО, равной 0,04%. Контрольные сердца обрабатывали так же, но без лекарства.
Протокол опытов.
С использованием вышеописанной модели ингибитор вазопептидазы омапатрилат сравнивали с носителем и селективньм ингибитором фермента, конвертирующего ангиотензин, фосиноприлатом (фосиноприл в виде свободной кислоты). Омапатрилат вводили в 20 сердец, носитель - в 21 и фисиноприлат - в 19.
Максимальная доза каждого соединения ограничивалась максимальной гемодинамической дозой, не дающей эффекта, достигаемой для нормальных сердец, для того, чтобы избежать нежелательных эффектов кардиодепрессии, вызванной лекарствами, влияющее на работу желудочков.
После 5-минутного равновесного периода контрольные кривые FS получали для каждого сердца и записывали также для каждого сердца LVDPmax. Затем регулировали экспериментальную предварительную нагрузку (объем баллона) до величины единственного объема баллона, обеспечивающей 70% LVDPmax в каждом сердце. Этот объем поддерживали, как детально описано ниже. Затем, как только заданная предварительная нагрузка достигалась во всех сердцах, следовал 5- минутный контрольный период. В этот момент начинали вливание или лекарства, или носителя и продолжали это до конца опыта.
Для того, чтобы избежать нежелательного инотропного действия лекарств, дозирование лекарства в процессе ишемии с низким током должно было заканчиваться при наибольшей величине концентрации, которая не влияет на устойчивое состояние гемодинамики при нормальном давлении перфузии.
После 5- минутного контрольного периода вводили лекарство при постоянном вливании в течение 10 минут при нормальной перфузии (86 мм рт.ст.) и в течение 45 минут ишемии с низким потоком (50 мм рт.ст.). Отношение наклона кривых Frank-Starling (FS) использовали как независимый индекс функции сокращения желудочка во время контрольного периода и ишемии с низким потоком. Все данные FS нормализовали и выражали как процент от контрольных значений FS для каждого сердца. Группировали данные для всех подобных групп и выражали их как среднее значение ±sem (стандартное отклонение от средней величины). Все группы данных сравнивали методом вариантного анализа. Величина р<0,05 рассматривалась как значительная (табл.1).
Таблица 1
Графическое представление этих данных приведено на Фиг.1 (омапатрилат) и Фиг.2 (фосиноприлат).
Эти данные показывают, что ингибитор вазопептидазы омапатрилат изменял наклон FS в зависимости от дозы (R2=0,99), в то время как селективный ингибитор, конвертирующий ангиотензин, фосиноприлат, незначительно отличался от носителя при эквимолярных дозах.
Пример 2.
Модель собаки с дисфункцией усилий.
Омапатрилат (0,3 мг/кг, внутривенно, n=7) оценивали на модели собаки с миокардной дисфункцией усилия (Matsuzaki et al., "Effects of a calcium entry blocker (diltiazem) on regional myocardial flow and function during exercise in conscious dogs", Circulation, 1984, 69, 801-814). Собаки, снабженные техническим приспособлением, приводимым в движение мышечной силой с перфузией коллатерально зависимой задней стенки, были приучены бегать по топчаку, снабженному мотором. По окончании контрольного периода (Стадия-2) и введения лекарства (Стадия-1) начинали упражнения (Стадия-1) и увеличивали его каждые две минуты, до тех пор, пока скорость сердцебиения не перестанет возрастать с увеличением нагрузки или прекращением ее. Максимальная нагрузка задавалась на Стадии 7. Стадии восстановления (8, 9) после упражнения также длились по две минуты. Наблюдались следующие результаты (табл.2).
Таблица 2
Непрерывно измерялись системная гемодинамика, местное утолщение стенки миокарда и снимались локальные электрограммы желудочков, эти данные переводили в цифровую форму для последующего анализа. Все упражнения проводили на парах собак, введение носителя сопровождалось через 4 часа введением омапатрилата. Все данные нормализовали и выражали как процент от соответствующей контрольной величины. Все группы сравнивали, анализируя вариантность или при помощи t-теста. Полученные данные, как и известные опубликованные в виде таких же протоколов, показывают, что полное восстановление после единичного упражнения с большой нагрузкой наступает через 3 часа. В вышеописанном исследовании полное восстановление после контрольного упражнения подтверждается тем фактом, что все гемодинамические величины перед вторым (омапатрилат) упражнением восстанавливались на 100% от контрольного значения (носитель).
В этом опыте (омапатрилат) (0,3 мг/кг, внутривенно) не влиял значительно на систолическое давление в левом желудочке или на произведение: скорость сердцебиения × систолическое давление в левом желудочке во время контрольного опыта или упражнения. Поскольку для каждой собаки наблюдалась своя точка окончания упражнения, все данные выражали как % от контрольного значения (с носителем).
Были получены следующие данные (табл.3-5).
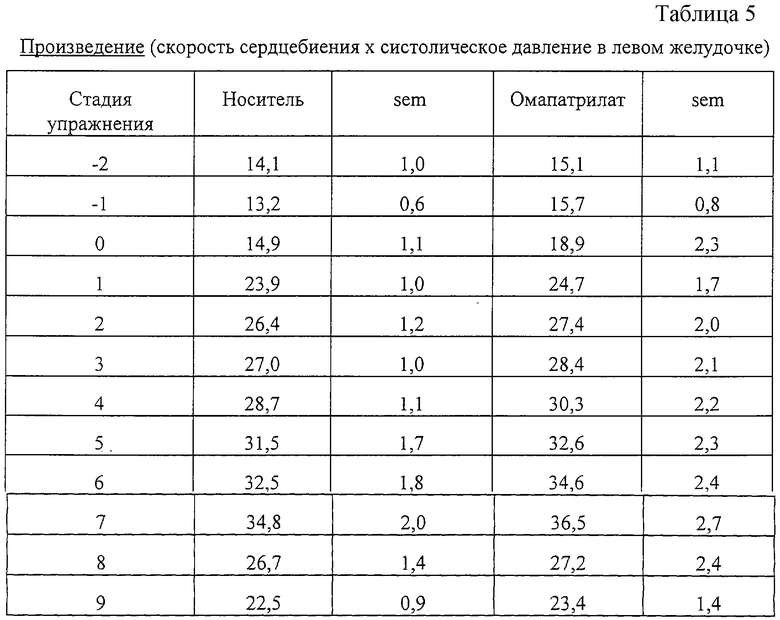
Исходя из вышеприведенных данных можно сделать вывод, что улучшения в способности выполнять упражнения нельзя приписать изменениям в нагрузке на желудочек или в скорости сердцебиения.
Хотя омапатрилат не влиял на системную гемодинамику, пиковое значение способности к упражнениям увеличилось у шести собак из семи, что показывают следующие данные.
Это увеличение сопровождалось значительным утолщением ишемической области стенки (р<0,001) и тенденцией к уменьшению повышения ST на соответствующей электрограмме (р=0,06). Были получены следующие данные (табл.6, 7).
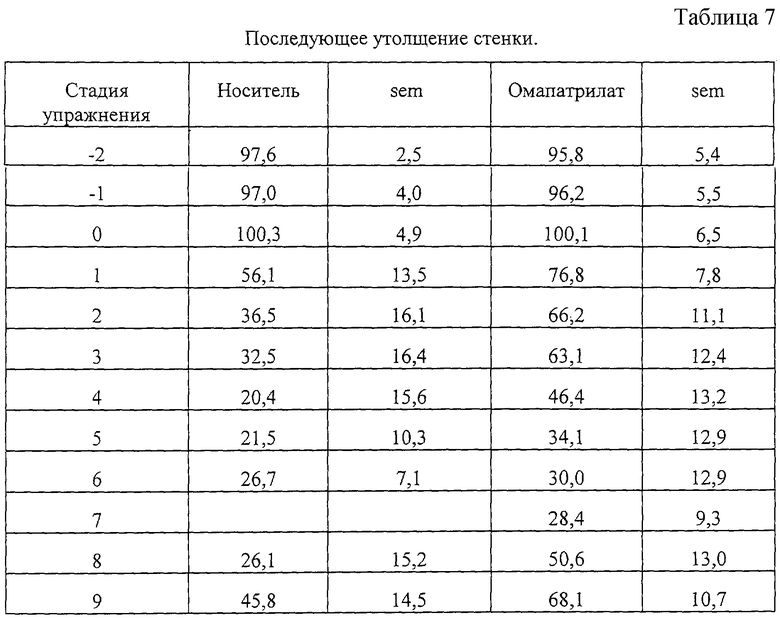
Последующее утолщение стенки значительно уменьшилось при введении омапатрилата. Соответствующее увеличение сегмента ST отражает эту функцию ишемической зоны. Это улучшение функции соответствует улучшенной способности к упражнениям, показанной выше.
Изобретение относится к медицине, кардиологии. Пациенту со стенокардией вводят эффективное количество омапатрилата или его фармацевтически приемлемой соли отдельно или в сочетании с другим фармацевтически активным агентом. Другим фармацевтически активным веществом может быть органический нитрат, β-адренергический блокатор, блокатор поступления кальция или антитромбоцитарное средство. Предложено применение омапатрилата или его фармацевтически приемлемой соли для приготовления лекарства для лечения и/или облегчения симптомов стенокардии. Способ позволяет расширить арсенал лекарственных средств для лечения или облегчения симптомов стенокардии. 3 с. и 13 з.п. ф-лы, 8 табл., 2 ил.
| BUNETT J.C., Vasopeptidase inhibition: A new aconcept in blood pressure management, J / Hypertention, suppL, 1999, Feb., 17(1), 5, p.37-43 | |||
| МЕТЕЛИЦА В.И., Справочник по клинической фармакологии сердечно-сосудистых лекарственных средств, М., Мед | |||
| практика, 1996, с.277-278 | |||
| US 5552397 A (KAPANEWSKY et al), 03.09.1996 | |||
| US 5508272 A (ROBL) 16.04.1996. |
Авторы
Даты
2005-01-27—Публикация
2000-03-09—Подача