Изобретение относится к области молекулярной биологии, вирусологии и медицины, а именно к применению новых производных нуклеозидов, а именно амидов d4T для подавления репродукции вируса иммунодефицита человека.
Новые соединения являются высокоэффективными ингибиторами репродукции вируса иммунодефицита человека 1-го типа в культуре перевиваемых лимфоцитов МТ-4, а также обеспечивают защиту клеток от цитопатогенного действия вируса.
В настоящее время известен целый ряд соединений, обладающих противовирусной активностью в отношении ВИЧ, в том числе и используемых в медицинской практике. К ним относятся производные нуклеозидов, ингибиторы протеаз и так называемые ненуклеозидные ингибиторы. Среди нуклеозидных производных наиболее известны и используются 3'-азидо-3'-дезокситимидин (AZT), 2'3'-дидезоксицитидин, 2'3'-дидезоксиинозин, 2'3'-дидезокси-2'3'-дидегидротимидин и 2'3'-дидезокси-3'-тиотимидин [1-2].
Наиболее близким аналогом заявляемого соединения (прототипом) является соединение, относящееся к группе нуклеозидных ингибиторов 2'3'-дидезокси-2'3'-дидегидротимидин (d4T) [2]. При умеренной токсичности для неинфицированных перевиваемых клеток лимфоидной линии МТ-4 это соединение обладает высокой анти-ВИЧ активностью. Механизм действия указанных соединений-аналогов состоит в том, что после проникновения в инфицированные клетки они подвергаются трифосфорилированию и специфично блокируют синтез ДНК, катализируемый обратной транскриптазой ВИЧ.
Однако, к сожалению, по сравнению с природными нуклеозидами процесс фосфорилирования модифицированных нуклеозидов клеточными ферментами значительно менее эффективен и протекает медленно, что дает время проникшему в клетки вирусу интегрироваться в геном в форме провирусной ДНК. Кроме того, высокая изменчивость ВИЧ приводит к быстрому возникновению резистентных штаммов вируса [3, 4] и, следовательно, к необходимости смены препарата на основе вышеприведенных соединений-аналогов, в том числе и на основе соединения-прототипа. К тому же в условиях длительного применения используемые препараты оказывают выраженное токсическое действие на организм.
В основу изобретения положена задача создания новых высокоэффективных в отношении ВИЧ модифицированных нуклеозидных производных, способных проникать внутрь клетки, устойчивых к действию ферментов дефосфорилирования и обладающих избирательной активностью в подавлении синтеза ДНК, катализируемого обратной транскриптазой ВИЧ.
Относящийся к группе нуклеозидных ингибиторов 2'3'-дидезокси-2'3'-дидегидротимидин (d4T) при умеренной токсичности для неинфицированных перевиваемых клеток лимфоидной линии МТ-4 обладает высокой анти-ВИЧ активностью, что позволило провести на его основе направленный синтез новых эффективных производных.
Указанная задача решена тем, что согласно изобретению заявляются новые соединения 5'аминокарбонилфосфонаты - производные 2'3'-дидезокси-2'3'-дидегидротимидина (d4T- прототип) [2] общей формулы:
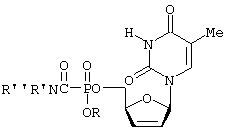
где: R'=H, alkyl, aryl; R''=H, alkyl, aryl; R', R’’=cyclic alkyl R=alkyl
На фиг.1 приведены дозозависимые кривые для расчета количественных характеристик ингибирования ВИЧ-1 исследуемыми соединениями (на примере соединения 3 b) при одновременном внесении с вирусом. Аналогичные графики получены и для соединений 3 а; 3 с.
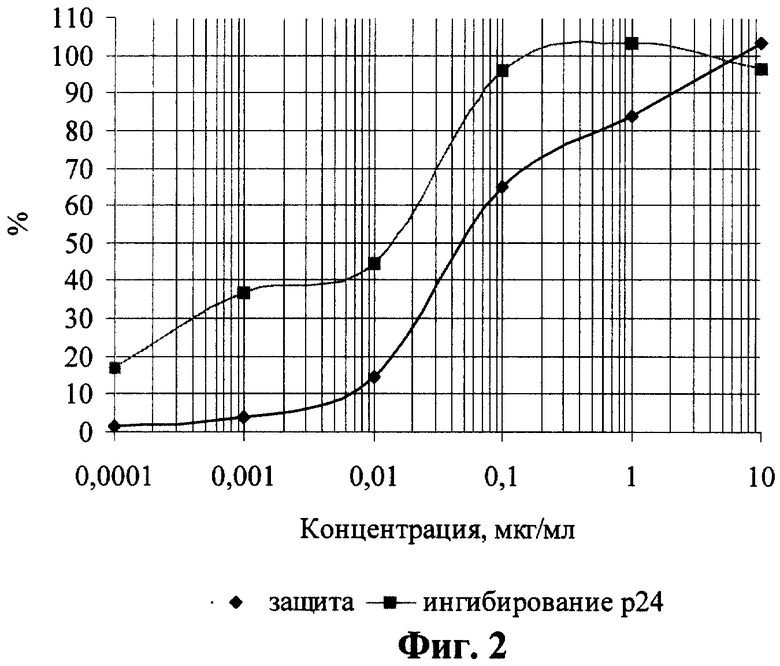
На фиг.2 приведены дозозависимые кривые для расчета количественных характеристик ингибирования ВИЧ-1 исследуемыми соединениями (на примере соединения 3 b) при внесении после адсорбции вируса. Аналогичные графики получены и для соединений 3 а; 3 с.
Схема получения заявляемых целевых 5'аминокарбонилфосфонатов
Целевые 5'аминокарбонилфосфонаты получали по следующей схеме:
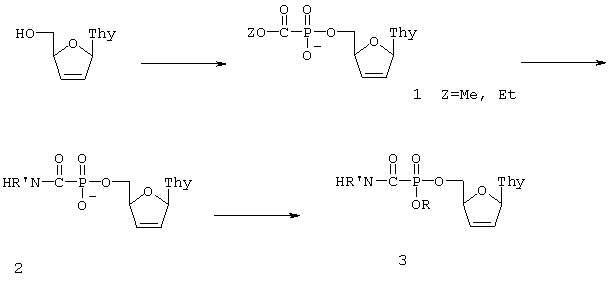
Исходным соединением послужил 2',3'-дидезокси-2',3'-дидегидротимидин-5'-этоксикарбонилфосфонат (1) (или соответствующий 5'-метоксикарбонилфосфонат), синтезированный ранее. Аминирование этоксикарбонилфосфоната (1) соответствующими аминами приводит к амидофосфонатам (2), которые алкилируют спиртами в присутствии триизопропилсульфонилхлорида (TPSC1) или в условиях реакции Мицунобу.
Ниже приведены конкретные примеры, раскрывающие сущность изобретения.
Пример 1
2',3'-Дидезокси-2',3'-дидегидротимидин-5'-аминокарбонилфосфонат (соединение 2а) (R'=H)
2',3'-Дидезокси-2',3'-дидегидротимидин-5'-этоксикарбонилфосфонат (73 мг, 0,2 ммоль) (или -5'-метоксикарбонилфосфонат, 70 мг, 0.2 ммоль) растворили в 25% водном растворе аммиака (3 мл), полученный раствор перемешивали 2 часа при комнатной температуре, а затем сконцентрировали в вакууме. Остаток растворили в воде и хроматографировали на DEAE-Toyopearl, элюировали линейным градиентом NH4HCO3 (0-0.2 М), целевой продукт элюировали 0.12 М NН4НСО3. Получили 62 мг (94%) соединения (1). УФ УФ (МеОН, λмакс): 266 нм. 1Н ЯМР (D2O, δ, м.д.): 7.51 (1Н, с, Н6), 6.87 (1Н, м, Н1'), 6.41 (1Н, м, Н2'), 5.90 (1Н, м, Н3'), 5.03 (1Н, м, Н4'), 4.09 (2Н, м, Н5'), 1.81 (3Н, с, СН3). 31РЯМР (D2O, δ, м.д.): -1.62 с.
2',3'-Дидезокси-2',3'-дидегидротимидин-5'-(этил)(аминокарбонил)фосфонат (соединение 3а) (R=Et, R'=H)
Метод А. Соединение (2а) (70 мг, 0.21 ммоль) растворили в пиридине (2 мл) и раствор сконцентрировали в вакууме. Эту процедуру повторили три раза, а затем остаток растворили в пиридине (3 мл) и добавили EtOH (0.5 мл) и TPSCl (90 мг, 0.3 ммоль). Реакционную массу перемешивали 16 часов при комнатной температуре. Растворитель удалили в вакууме. Остаток хроматографировали на колонке с силикагелем (2×25 см), элюируя системой хлороформ-метанол 96:4. Получили 54 мг (72%) соединения 3а. УФ (МеОН, λмакс): 266 нм. 1Н ЯМР (CD3OD, δ, м.д.): 7.35 (1Н, с, Н6), 6.96 (1Н, м, H1'), 6.37 (1Н, м, Н2'), 5.94 (1Н, м, Н3'), 5.02 (1Н, м, Н4'), 4.37 (2Н, м, Н5'), 4.19 (2Н, м, 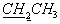 ), 1.88 (3Н, с, СН3), 1.35 (3Н, м,
), 1.88 (3Н, с, СН3), 1.35 (3Н, м, 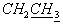 ). 31Р ЯМР (СО3ОD, δ, м.д.): 0.15 с, - 0.12 с.
). 31Р ЯМР (СО3ОD, δ, м.д.): 0.15 с, - 0.12 с.
Метод Б. К раствору соединения 1 (120 мг, 0.5 ммоль) в ДМФА (2 мл) прибавили трифенилфосфин (130 мг, 0.5 ммоль) и этанол (100 мкл), раствор охладили до 4°С и прибавили к нему раствор диэтилазодикарбоксилата (0.5 ммоль, 77 мкл) в ТГФ (1 мл). Реакционную смесь выдерживали при комнатной температуре 5 ч, упаривали, остаток хроматографировали на колонке с силикагелем (2.5×30 см), элюируя градиентом метанола в хлороформе (0→10%). Получили 45 мг (60%) соединения 3а.
Пример 2
2',3'-Дидезокси-2',3'-дидегидротимидин-5'-(N-метиламинокарбонил)фосфонат (соединение 2b) (R'=Me)
Соединение 2b синтезировали из соединения 1 по методу, описанному для аминокарбонилфосфоната 2а кипячением в водном растворе метиламина. Выход соединения 2b составил 92%. УФ (МеОН): λмакс 267 нм. 1Н ЯМР (D2O, δ, м.д.): 7.43 (1Н, с, Н6), 6.85 (1Н, м, H1'), 6.35 (1Н, м, Н2'), 5.86 (1Н, м, Н3'), 4.97 (1Н, м, Н4'), 4.03 (2Н, м, Н5'), 2.61 (3Н, с, 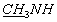 ), 1.76 (3Н, с, СН3). 31Р ЯМР (D2O, δ, м.д.): - 1.53 с.
), 1.76 (3Н, с, СН3). 31Р ЯМР (D2O, δ, м.д.): - 1.53 с.
2',3'-Дидезокси-2',3'-дидегидротимидин-5'-(этил)(N-метиламинокарбонил)фосфонат (соединение 3b) (R'=Me, R=Et)
Соединение 3b синтезировали аналогично аминокарбонилфосфонату 3а с выходом 48% по методу А и 80% по методу В. УФ (МеОН): λмакс 267 нм. 1Н ЯМР (СDСl3, δ, м.д.): 8.92 (1Н, с, NH), 7.39 (1Н, с, NH), 7.34 и 7.32 (1Н, 2с, Н6), 7.00 (1Н, м, H1'), 6.28 (1Н, м, Н2'), 5.88 (1Н, м, Н3'), 4.98 (1Н, м, Н4'), 4.40 (2Н, м, Н5'), 4.19 (2Н, м, 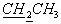 ), 2.87 и 2.86 (3Н, 2с,
), 2.87 и 2.86 (3Н, 2с, 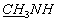 ), 1.93 (3Н, с, СН3), 1.34 (3Н, м,
), 1.93 (3Н, с, СН3), 1.34 (3Н, м, 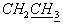 ). 31Р ЯМР (CD3CN, δ, м.д.): -0.27 с, -0.76 с.
). 31Р ЯМР (CD3CN, δ, м.д.): -0.27 с, -0.76 с.
Пример 3
2',3'-Дидезокси-2',3'-дидегидротимидин-5'-(N-фенилэтиламинокарбонил)фосфонат (соединение 2с) (R'=PhCH2CH2-)
Соединение 2с синтезировали из соединения 1 по методу, описанному для аминокарбонилфосфоната 2а перемешиванием в фенилэтиламине. Выход соединения 2с составил 94%. УФ (МеОН): λмакс 267 нм. 1Н ЯМР (D2O, δ, м.д.): 7.43 (1Н, с, Н6), 7.45-7.17 (5Н, м, Ph), 6.89 (1Н, м, H1'), 6.25 (1Н, м, Н2'), 5.86 (1H, м, Н3'), 4.95 (1H, м, Н4'), 4.10 (2Н, м, Н5'), 3.60 (2Н, M, 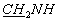 ), 2.61 (2Н, с,
), 2.61 (2Н, с, 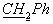 ), 1.86 (3Н, с, СН3). 31P ЯМР (D2O, δ, м.д.): -1.47 с.
), 1.86 (3Н, с, СН3). 31P ЯМР (D2O, δ, м.д.): -1.47 с.
2',3'-Дидезокси-2',3'-дидегидротимидин-5'-(этил)(N-фенилэтиламинокарбонил)фосфонат (соединение 3с) (R'=PhCH2CH2-, R=Et)
Соединение 3с синтезировали аналогично аминокарбонилфосфонату 3а с выходом 51% по методу А и 72% по методу В. УФ (МеОН): λмакс 267 нм. 1Н ЯМР (СDСl3, δ, м.д.): 9.17 (1H, с, NH), 7.45 (1H, с, NH), 7.33 и 7.31 (1H, 2с, Н6), 7.45-7.17 (5Н, м, Ph), 6.99 (1H, уш. с, Н1'), 6.27 и 6.17 (1H, 2м, Н2'), 5.84 (1H, м, Н3'), 4.91 (1H, м, Н4'), 4.29 (2Н, м, Н5'), 4.09 (2Н, м, 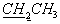 ), 3.62 (2Н, м,
), 3.62 (2Н, м, 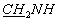 ), 2.85 (2Н, с,
), 2.85 (2Н, с, 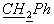 ), 1.91 (3Н, 2с, СН3), 1.29 (3Н, м,
), 1.91 (3Н, 2с, СН3), 1.29 (3Н, м, 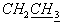 ). 31P ЯМР (СDСl3, δ, м.д.): -0.14 с, -0.75 с.
). 31P ЯМР (СDСl3, δ, м.д.): -0.14 с, -0.75 с.
Исследование ингибирования репродукции ВИЧ включает культивирование первично инфицированных лимфоидных клеток линии МТ-4 в присутствии исследуемых соединений, конечные концентрации которых в культуральной среде составляют 0,0001-100 мкг/мл, на протяжении одного пассажа - в течение 4 суток.
Об ингибировании репродукции ВИЧ в культуре чувствительных клеток судят по снижению накопления вирусспецифического белка р24 (по данным иммуноферментного анализа), а также по увеличению жизнеспособности клеток в присутствии препарата по сравнению с контролем, определяемому на 4-е сутки культивирования [5-6] при окрашивании 3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide (MTT).
Пример 4
Оценка цитотоксичности соединений
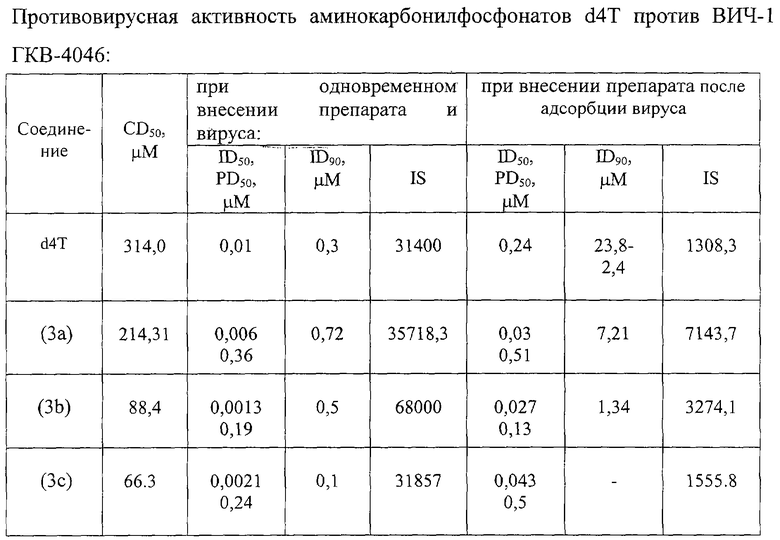
Цитотоксичность препарата оценивают путем добавления его разведений в бессывороточной среде RPMI-1640 к клеточной суспензии МТ-4, помещенной в лунки 96-луночного планшета ("Cel-Cult", England), до конечных концентраций 0,001-100 мкг/мл (по три лунки на каждую дозу) с последующим культивированием при 37°С в течение 4 суток [7]. Посевная концентрация составляет 0,5×106 клеточных частиц в миллилитре. Контролем служат клетки без добавления препарата, вместо которого вносят такое же количество бессывороточной среды. Жизнеспособность клеток подсчитывают на 4 сутки культивирования, пользуясь формазановым методом (прижизненным окрашиванием клеток 3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide (MTT). Токсичность различных доз препарата определяют по жизнеспособности клеток относительно контроля (фиг.1, 2), по полученным результатам строят дозозависимую кривую и определяют концентрацию, на 50% снижающую жизнеспособность клеток (СD50). Следует отметить, что исследуемые соединения не оказывают токсического действия на клетки МТ-4 в эффективных концентрациях: 50% токсичные дозы на 5-6 порядков превышают эффективные в отношении ВИЧ-1 дозы (таблица).
Пример 5
Изучение влияния исследуемых соединений на репродукцию ВИЧ-1 в культуре клеток МТ-4
Исследование противовирусной активности соединений в отношении ВИЧ-1 проводят на перевиваемой линии чувствительных клеток МТ-4. Для заражения используют супернатант инфицированных клеток, хранящийся в жидком азоте, множественность заражения составляет 0,2-0,5 инфекционных единиц на клетку. Суспензию клеток МТ-4 с концентрацией 2,0×106 клеточных частиц в миллилитре и жизнеспособностью не менее 90% помещают в лунки 96-луночного планшета ("Orange") непосредственно после внесения вируссодержащего материала и сразу же добавляют исследуемые соединения, разведенные в среде RPMI-1640 без сыворотки, до конечных концентраций 0,0001-100 мкг/мл (по три лунки на каждую дозу). Контролями служат инфицированные ВИЧ-1 клетки МТ-4 без добавления препарата (вместо препарата вносят такое же количество среды RPMI-1640 без добавок) и неинфицированные клетки.
Планшет инкубируют в течение часа при 37°С для адсорбции вируса, затем клетки разводят до посевной концентрации (0,5×106 в миллилитре) питательной средой RPMI-1640 с добавлением 10% фетальной сыворотки КРС, предварительно инактивированной прогреванием при 56°С в течение 30 минут, 300 мг/мл L-глютамина и 100 мкг/мл гентамицина. Затем планшет помещают в термостат на 37°С в атмосфере 5% СО2. На 4 сутки культивирования подсчитывают концентрацию и жизнеспособность клеток формазановым методом. По полученным данным строят графики зависимости прироста жизнеспособности клеток относительно контроля под действием возрастающих доз препаратов, т.е. определяют способность препаратов защищать инфицированные клетки от цитопатогенного действия вируса. Оценку анти-ВИЧ активности соединений проводят с использованием количественного определения вирусспецифического белка р24 методом прямого иммуноферментного анализа, как описано в [8], и строят дозозависимые кривые (фиг.1, 2), по которым рассчитывают концентрации, на 50 и 90% подавляющие прирост вирусного антигена (ID50 и ID90). Терапевтический индекс, или индекс селективности (IS), считают как отношение 50%-ной токсической концентрации соединения к его 50%-ной эффективной дозе (результаты представлены в таблице). На основании этих количественных показателей ингибирования можно судить об эффективности противовирусного действия соединений, заключающейся в высокой степени подавления репликации ВИЧ-1 в культуре клеток МТ-4, сравнимой с эффективностью d4T при одновременном внесении препарата и вируса и в 2-5 раз превышающей ее при проведении исследования в постадсорбционных условиях.
Из полученных экспериментальных данных видно, что исследуемые соединения, не оказывая токсического действия на клетки в эффективных концентрациях (50%-ные токсические дозы на 5-6 порядков превышают 50%-ные ингибирующие дозы), помимо способности защищать клетки от гибели в результате цитопатогенного действия вируса (>50% в дозах 0,1-0,5 мкг/мл), в высокой степени подавляют репродукцию вируса иммунодефицита 1 типа в культуре клеток МТ-4. Терапевтические индексы исследуемых соединений (IS) сравнимы с IS d4T при одновременном внесении препарата и вируса и в 2-5 раз превышают IS d4T в постадсорбционных условиях.
Это говорит о перспективности новых производных d4T для дальнейших исследований с целью создания на их основе лекарственных форм для лечения ВИЧ/СПИД.
* Относительную степень защиты инфицированных клеток от гибели различными дозами препарата рассчитывают по формуле:
Защита (%)=(X-V)/(K-V)*100,
где Х - % жизнеспособности инфицированных клеток в присутствии препарата на 4 сутки культивирования, К - % жизнеспособности в контроле клеток, V - % жизнеспособности инфицированных клеток в контроле вируса (без добавления препарата).
Относительную степень ингибирования репродукции вирусного белка считают по формуле:
%ингибир.=(Рх-Ро)/(Р-Ро)*100,
где Рх - концентрация белка р24 на 4 сутки культивирования в присутствии препарата, Ро - концентрация р24 после 1 часа инкубирования ВИЧ-1 с клетками без добавления препарата ("O" точка), Р - концентрация р24 на 4 сутки культивирования ВИЧ-1 в клетках без добавления препарата (контроль вируса).
Терапевтический индекс, или индекс селективности (IS), определяют как отношение концентрации препарата, токсичной для 50% клеток (CD50), к концентрации, на 50% подавляющей прирост вирусного антигена (ID50):
IS=CD50/ID50
Промышленная применимость
Заявляемые соединения обладают выраженной ингибирующей активностью в отношении вируса иммунодефицита человека и могут являться потенциальными кандидатами для получения противовирусных средств, используемых в медицине и фармацевтической промышленности.
Источники информации
1. Veal G.J., Agrawal S., Byrn R.A. Synergistic inhibition of HIV-1 by an antisense oligonucleotide and nucleoside analog reverse transcriptase inhibitors. Antiviral Research 1998, 38, 63-73.
2. Cardona V.M., Ayi A.I., Aubertin A.M., Guedj R. Synthesis and anti-HIV activity of some novel arylphosphate and H-phosphonate derivatives of 3'-azido-2',3'-dideoxythymidine and 2',3'-didehydro-2',3'-dideoxythymidine. Antiviral Res 1999, 42(3), 189-196.
3. Schinazi R.F., Lloyd R.M., Ramanathan C.S. and Taylor E.W. Antiviral Drug Resistance Mutation in Human Immunodeficiency Virus Ttype 1 Reverse Transcriptase Occur in Specific RNA Structural Regions. Antimicrobial Agents and Chemotherapy 1994, 38(2), 268-274.
4. Avramis V.I., Kwock R., Solorzano M.M. and Gomperts E. Evidense of In Vitro Development of Drug Resistanse to Azidothymidine in T-Lymphocytic Leukemia Cell Lines (Jurkat E6-1/AZT-100) and in Pediatric Patients with HIV-1 Infection. Journal of Acquired Immune Deficiency Syndromes 1993, 6, 1287-1296.
5. Svinarchuk P.P., Konevetz D.A., Pliasunova O.A., Pokrovsky A.G., Vlasov V.V. Inhibition of HIV proliferation in MT-4 cells by antisense oligonucleotide conjugated to lipophilic groups. Biochimie 1993, 75, 49-54.
6. Pokrovskii A.G., Pliasunova O.A., Blinov V.M., Vlasov V.V., Svinarchuk P.P., Abramova T.V., Gorn V.V. and Konevetz D.A. Inhibition of Human Immunodeficiency Virus by Sense and Antisense Oligodeoxynucleotides. Molecular Biology 1993, 27(5), № 1, 641-644.
7. Патент РФ 2144956, кл. С 12 N 7/04, опубл. 27.01.2000 г. БИ № 3.
8. Иммуноферментный анализ. // Под ред. Т-Т.Нго, Г.Ленхоффа. - М: Мир. - 1988.
| название | год | авторы | номер документа |
|---|---|---|---|
| 2',3'-ДИДЕГИДРО-2',3'-ДИДЕЗОКСИТИМИДИН-5'[(ЭТОКСИКАРБОНИЛ)(ЭТИЛ)ФОСФОНАТ]- ИНГИБИТОР РЕПРОДУКЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА | 2000 |
|
RU2188203C2 |
| ФОСФОРАМИДАТЫ НУКЛЕОЗИДНЫХ АНАЛОГОВ - ИНГИБИТОРЫ РЕПРОДУКЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА | 2003 |
|
RU2243972C1 |
| ПРОИЗВОДНЫЕ 5'-H-ФОСФОНАТА 3'-АЗИДО-3'-ДЕЗОКСИТИМИДИНА И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ НА ИХ ОСНОВЕ | 2001 |
|
RU2187509C1 |
| 5'-ФОСФОРСОДЕРЖАЩИЕ ПРОИЗВОДНЫЕ 2',3'-ДИДЕЗОКСИ-3'-ТИАЦИТИДИНА НОВЫЕ ПРОТИВОВИРУСНЫЕ АГЕНТЫ | 2007 |
|
RU2373218C2 |
| МОДИФИЦИРОВАННЫЕ 5'-ФОСФОНАТЫ АЗТ В КАЧЕСТВЕ АКТИВНЫХ КОМПОНЕНТОВ ДЛЯ ПОТЕНЦИАЛЬНЫХ ПРОТИВОВИРУСНЫХ ПРЕПАРАТОВ | 2004 |
|
RU2322450C2 |
| СОЛИ 5'-АМИНОКАРБОНИЛФОСФОНАТА 3'-АЗИДО-3'-ДЕЗОКСИТИМИДИНА, ЯВЛЯЮЩИЕСЯ СЕЛЕКТИВНЫМИ ИНГИБИТОРАМИ ПРОДУКЦИИ ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА ВИЧ-1 | 2010 |
|
RU2441016C1 |
| НОВЫЕ ДЕПО-ФОРМЫ ЗИДОВУДИНА И ЛАМИВУДИНА НА ОСНОВЕ ПРОИЗВОДНЫХ ФОСФОНОВЫХ КИСЛОТ | 2009 |
|
RU2430104C1 |
| МОДИФИЦИРОВАННЫЕ НУКЛЕОЗИД-5'-ТРИФОСФАТЫ КАК АНТИВИРУСНЫЕ АГЕНТЫ | 1996 |
|
RU2183213C2 |
| УРЕТАНОВЫЕ ПРОИЗВОДНЫЕ АЗТ - ПОТЕНЦИАЛЬНЫЕ ПРОТИВОВИРУСНЫЕ ПРЕПАРАТЫ | 2009 |
|
RU2430103C1 |
| 5`-ХОЛИНФОСФАТ 3`-АЗИДО-3`-ДЕЗОКСИТИМИДИНА КАК АНТИВИРУСНЫЙ АГЕНТ | 2002 |
|
RU2293739C2 |
Изобретение относится к области технологии органических соединений, а именно к 5'-аминокарбонилфосфонатам d4T - ингибиторам репродукции вируса иммунодефицита человека. Описываются 5'-аминокарбонилфосфонаты d4T, имеющие общую формулу

где: R'=H, алкил, арил; R''=H, алкил, арил; R', R''=циклический алкил, R=алкил - ингибиторы репродукции вируса иммунодефицита человека. Технический результат - получены новые соединения, обладающие полезными биологическими свойствами. 2 ил., 1 табл.

5'-Аминокарбонилфосфонаты d4T, имеющие общую формулу
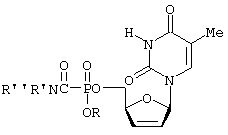
где R'=H, алкил, арил; R''=Н, алкил, арил; R', R''=циклический алкил,
R=алкил
- ингибиторы репродукции вируса иммунодефицита человека.
| Cardova V.M | |||
| et al., Synthesis and anti-HIV activity of some novel arylphosphonate and H-phosphonate derivatives of 3'-azido-2',3'-dideoxythymidine and 2',3'-didehydro-2',3'-dideoxythymidine | |||
| Antiviral Research, 1999, 42(3), р.186-196 | |||
| Shirokova E.A., et al., New Lipophinic Derivatives of AZT and d4T 5'-Phosphonates | |||
| Nucleosides, Nucleotides & Nucleic Asids, may 2003, 22, р.981-985. |
Авторы
Даты
2005-02-27—Публикация
2003-06-16—Подача