ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
А. Отсылочные заявки
В соответствии с § 119 раздела 35 Кодекса законов США в настоящей заявке испрашивается приоритет по двум предварительным заявкам США с регистрационным номером 60/137733, поданной 07 июня 1999 и с регистрационным номером 60/138006, поданной также 07 июня 1999. Содержание каждой из названных выше заявок полностью включено в данный документ.
В. Область техники, к которой относится изобретение
Настоящее изобретение относится к способу нанесения покрытий на частицы, и к частицам, полученным этим способом. В частности, настоящее изобретение относится к частицам лекарственных препаратов или частицам доставки лекарственных препаратов, покрытых материалом, подверженным биологическому разложению или обладающим биологической совместимостью, например полимером. Покрытие передает частице целый ряд характеристик, включая изменение ее поверхностных свойств, скорости растворения или скорости диффузии и/или выделения активного компонента. Кроме того, в настоящем изобретении предлагается способ приготовления составов твердых частиц, покрытых ультратонкими слоями покрывающих материалов, предпочтительно органическими полимерами, наносимыми с помощью неводных технологий, не связанных с применением растворителей. В частности, одним из предпочтительных способов является способ осаждения из паровой фазы, например, абляция импульсным лазером. Среди других преимуществ описываемых способов можно назвать контроль толщины и однородности покрытия на поверхностях отдельных твердых частиц лекарственных препаратов.
С. Описание современного уровня развития техники в смежных областях
Технологии приготовления средств доставки лекарственных препаратов, обеспечивающие доставку препаратов в течение продолжительного периода времени, в корне изменили фармацевтическую промышленность. Независимо от характера доставки, будь то длительная доставка, изменяемая, контролируемая, продленного действия или доставка с задержкой, концепция, в основном, остается прежней - обеспечить с помощью одной дозы то, что прежде требовало применения многих доз. (Термин "длительное выделение" будет использоваться здесь для описания родового класса механизмов выделения). Желательно, чтобы лекарственный препарат в эффективной концентрации действовал в течение достаточно продолжительного периода времени.
Такие технологии обладают целым рядом преимуществ. Например, обеспечивают более низкие концентрации лекарственного препарата в теле пациента на протяжении боле длительного времени, что понижает частоту возникновения токсичности для лекарственных препаратов с узким спектром действия, и часто улучшают общий эффект. Кроме того, пациенты легче соглашаются на сокращение дозировок и охотнее идут на прием одной дозы в день, чем на прием двух, трех или даже четырех доз в день. Это справедливо для лекарственных препаратов, принимаемых внутрь через рот, а также для препаратов, вводимых с помощью инъекции, ингаляции или доставляемых через кожу или слизистую.
Обычно длительное выделение препарата достигалось путем нанесения на частицы или гранулы лекарственного препарата покрывающего материала. Таким образом получали таблетки, капсулы, пилюли и другие лекарственные препараты в виде гранул с покрытием. В зависимости от требуемого характера выделения лекарственного препарата центральная часть лекарственного препарата либо покрывается одним слоем покрытия, либо предусмотрены чередующиеся слои, либо лекарственный препарат в виде дисперсии распределяется внутри материала покрытия. Существует множество разных вариантов, и частные случаи технологий приготовления лекарственных средств выбираются исходя из требуемого характера выделения лекарственного препарата. Краткое описание этих технологий приготовления лекарственных средств дано во втором издании книги "Современная фармацевтика" (Modem Pharmaceutics), второе издание, под редакцией Банкера Г.С. и Родеса С.Е. (Gilbert S. Banker & Christopher T. Rhodes), ссылка на которую приводится в списке противопоставленных документов.
Системы длительной доставки лекарственного препарата, включая прием препарата внутрь через рот, основывались в основном на матричных системах или системах с использованием частиц с применением растворителя. В этих системах для контроля за скоростью выделением активного материала лекарственного препарата используют покрытие, наносимое методом распыления или механическое перемешивание центральной части частиц лекарственного препарата и/или гранулированный наполнитель с полимером, например, целлюлозой, полиакрилатом, разлагаемым сложным полиэфиром и т.п., кроме того, традиционные матричные системы могут содержать гельобразующий наполнитель, например, поливиниловый спирт, оксид полиэтилена (или полиэтиленгликоль), целлюлозы, например, те, которые после доставки образуют слой геля, с помощью которого лекарственный препарат выделяется из матрицы путем диффузии в течение определенного времени. К числу недостатков этих систем можно отнести длительное и тяжелое многоэтапное освоение системы от лабораторного до коммерческого производства, для которого часто требуется специальное оборудование и дорогостоящие растворители. Кроме того, известные системы производят лекарственные средства с относительно высокими концентрациями полимеров, с толстыми покрытиями и не обеспечивают при производстве строго идентичные характеристики выделения лекарственного препарата.
Поэтому для приготовления частиц лекарственного препарата с покрытием необходимы усовершенствованные способы, которые не имеют перечисленных недостатков и которые могут применяться при изготовлении лекарственных препаратов с наилучшими свойствами доставки и действенности.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
А. Особенности и преимущества данного изобретения
В настоящем изобретении приведенные выше и другие недостатки существующих способов преодолеваются путем применения новых способов нанесения покрытий, которые применяются для приготовления частиц с покрытием и, в частности, частиц лекарственных препаратов с покрытием, которые улучшают их фармацевтические свойства. В общем, в описываемых здесь способах рассматриваются средства для нанесения на материал частиц одно- или многослойных покрытий из зернистого материала или материала для обеспечения однородного сцепления материала или материала покрытия с поверхностью материала частицы с образованием сплошных или дискретных покрытий в зависимости от конкретного применения твердых частиц с покрытием.
В настоящем изобретении с целью значительного улучшения фармакокинетических характеристик лекарственных препаратов с покрытием предусмотрены также изменения (1) характеристик агрегирования; (2) свойств текучести; (3) скорости выделения лекарственного препарата путем нанесения покрытий способами по настоящему изобретению.
Кроме того, к числу преимуществ относятся улучшенные свойства текучести на этапе производства и стабильность свойств лекарственного препарата, например, при хранении.
Описанные здесь способы нанесения покрытия обеспечивают высокую эффективность процесса инкапсуляции лекарственных препаратов (более 99%) при минимально необходимой обработке. Кроме того, способ обработки обладает несколькими преимуществами по сравнению с существующими в настоящее время методами, включая:
1. Высокую скорость обработки (т.е. длительность нанесения покрытия на частицу от начала до конца) порядка нескольких минут.
2. Возможность применения разнообразных материалов для покрытия твердых частиц, что позволяет выполнять пленки из материалов с гарантированной биологической совместимостью.
3. Возможность применения сухой технологии без использования растворителей в стерильном помещении.
4. Минимизацию агрегирования/сцепления частиц путем нанесения покрытия, оказывающего влияние на характеристики связывания материалов и электростатический заряд на поверхности твердых частиц.
5. Обеспечение контроля за кинетикой выделения лекарственного препарата, помещаемого в микрокапсулу, образованную с помощью осаждения покрытий на поверхность частицы, путем: (а) диффузии лекарственного препарата через полимер; (б) разложения полимерного покрытия, подверженного биологическому разложению, на частицах лекарственного препарата, обеспечивая, таким образом, выделение центральной части лекарственного препарата.
6. Возможность применения лазерной абляции, выполняемой в нормальных условиях атмосферного давления в противоположность вакууму, исключая, таким образом, необходимость использования в данной технологии вакуумных устройств, включая камеры и насосы, и обеспечивая тем самым возможность применения непрерывного технологического процесса. Это преимущество существенно сокращает время изготовления продукции и, таким образом, снижает производственные издержки и уменьшает трудности, связанные с освоением технологии.
В. Краткое изложение сущности изобретения
В настоящем изобретении раскрыты способы нанесения покрытий на материал центральной части (сердцевины) частиц, включающие подачу материалов мишени и материалов сердцевины частиц; абляцию материалов мишени с образованием уносимых материалов твердой мишени; нанесение покрытия на материалы сердцевины частиц из уносимых материалов твердой мишени, при этом данный способ осуществляется при давлении приблизительно 10 Торр или выше. Абляция может также выполняться при давлении приблизительно 20 Торр или выше, включая 760 Торр.
Средний диаметр центральной части частиц может примерно составлять от 0,5 мкм до 1 мм. На материал сердцевины частиц может наноситься покрытие толщиной менее приблизительно 1000 нм из материала уносимых частиц мишени. Толщина покрытия материала центральной части частиц составляет менее приблизительно 100 нм или менее приблизительно 10 нм.
Средний диаметр покрытия из уносимого материала частиц мишени, наносимого на материал центральной части частиц, составляет менее приблизительно 1 мм, менее приблизительно 100 мкм или менее приблизительно 10 мкм. Предпочтительно, чтобы в состав материала мишени входил, по крайней мере, один полимер, подверженный биологическому разложению, полимер, обладающий биологической совместимостью, полисахарид и/или протеин.
Абляция достигается использованием высокоэнергетического источника, которым может быть лазер. В качестве лазера может использоваться, но не ограничиваться этим, ионный лазер, полупроводниковый лазер, импульсный эксимерный лазер. В предпочтительных вариантах изобретения покрытие материала центральной части частиц материалом уносимых частиц мишени выполняется путем смешивания материалов центральной части частиц с материалами уносимых частиц мишени с применением псевдоожиженного слоя. Псевдоожиженный слой можно получить с помощью пневматической флюидизации (псевдоожижения).
В состав материалов сердцевины частиц могут входить лекарственные препараты для людей или животных, пестициды, гербициды, фунгициды, косметика, краски или пигменты и/или инертные частицы. Желательно, чтобы материалы центральной части частиц включали, по крайней мере, один лекарственный препарат для людей или животных. При нанесении материалов мишени на материалы центральной части частиц может получиться сплошное покрытие или дискретное покрытие.
В других вариантах настоящего изобретения описаны способы нанесения на частицы покрытий, толщиной менее приблизительно 100 нм, при этом данный способ включает подачу материалов мишени и материалов сердцевины частиц; абляцию материалов мишени с образованием материалов уносимых частиц мишени; нанесение покрытия на материалы центральной части частиц из материалов уносимых частиц мишени, при этом материалы центральной части частиц с использованием пневматической флюидизации образуют псевдоожиженный слой.
В других вариантах настоящего изобретения раскрываются способы нанесения покрытий на материалы центральной части частиц, включающие подачу материалов мишени и материалов сердцевины; абляцию материалов мишени с образованием материалов уносимых частиц мишени; нанесение покрытия на материалы центральной части частиц из материалов уносимых частиц мишени, при этом способ осуществляется при давлении приблизительно 760 Торр и материал сердцевины подвергается псевдоожижению с использованием пневматического псевдоожижения.
Настоящее изобретение также относится к частицам с покрытием, полученным в соответствии с этими способами.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Графические материалы являются частью настоящего описания и включены в него, чтобы продемонстрировать определенные аспекты настоящего изобретения. Изобретение может быть лучше понято, если вместе с подробным описанием представленных вариантов настоящего изобретения даются ссылки на одно или большее число фигур.
На Фиг.1 представлено схематическое изображение одного из вариантов настоящего изобретения.
На Фиг.2 представлено схематическое изображение другого варианта настоящего изобретения.
На Фиг.3 представлено изображение пленки из частиц нанометрового диапазона, осажденных при атмосферном давлении (увеличение 100000 X), полученное с помощью просвечивающего электронного микроскопа.
На Фиг.4 представлено другое изображение пленки из частиц нанометрового диапазона, осажденных при атмосферном давлении (увеличение 100000 X), полученное с помощью просвечивающего электронного микроскопа.
На Фиг.5 показан протонный ЯМР-спектр А) исходного PLGA (сополимер молочно-гликолевой кислоты), В) осажденного PLGA при плотности энергии 500 мДж/см2 при атмосферном давлении, С) при давлении около атмосферного (10 Торр).
На Фиг.6 представлена скорость осаждения PLGA при различных давлениях.
На Фиг.7 представлена гельпроникающая хроматограмма А) исходного PLGA молекулярной массой 56 кДа, В) PLGA молекулярной массой 7 кДа, осажденного при плотности энергии 500 мДж/см2, и при атмосферном давлении.
На Фиг.8 представлено изображение порошка ТА (триамцинолонацетонид) без покрытия, полученное с помощью растровой электронной микроскопии, при увеличении А) 1000 X, В) 5000 X, С) 10000 Х и D) 20000 X.
На Фиг.9 представлено изображение порошка ТА с покрытием из PLGA, полученное с помощью растровой электронной микроскопии, при увеличении А) 1000 X, В) 5000 X, С) 10000 Х и D) 20000 X.
На Фиг.10 показано растворение порошка ТА без покрытия и порошка ТА с покрытием из PLGA в забуференном фосфатном соляном растворе с уровнем рН 7,4 (50 мМ, 1% додецилсульфата натрия - SDS) при 37°С (n=3). Кривые представлены для порошка ТА без покрытия (ТА)  и порошка с покрытием спустя 30 минут при плотности энергии 500 мДж/см2 (PLGA30)
и порошка с покрытием спустя 30 минут при плотности энергии 500 мДж/см2 (PLGA30)  , при атмосферном давлении.
, при атмосферном давлении.
На Фиг.11 показана кривая выделения препарата для альбумина бычьей сыворотки, покрытого PLGA  и альбумина бычьей сыворотки без покрытия
и альбумина бычьей сыворотки без покрытия  .
.
На Фиг.12 показан протонный ЯМР-спектр А) исходного НРМС, В) осажденного НРМС при плотности энергии 500 мДж/см2 и при давлении около атмосферного (10 Торр).
На Фиг, 13 показано растворение порошка ТА без покрытия и порошка ТА с покрытием из НРМС в забуференном фосфатном соляном растворе с уровнем рН 7,4 (50 мМ, 1% додецилсульфата натрия) при 37°С (n=3). Кривые представлены для порошка ТА без покрытия (ТА)  и порошка с покрытием спустя 10 минут при плотности энергии 500 мДж/см2 (НРМС200)
и порошка с покрытием спустя 10 минут при плотности энергии 500 мДж/см2 (НРМС200)  и, и при плотности энергии 625 мДж/см2 (НРМС250)
и, и при плотности энергии 625 мДж/см2 (НРМС250)  .
.
На Фиг.14 показан протонный ЯМР-спектр А) исходного препарата Eudragit 4135, В) осажденного препарата Eudragit 4135 при плотности энергии 500 мДж/см2 и при давлении около атмосферного (10 Торр).
На Фиг.15 показан протонный ЯМР-спектр А) исходного додецилсульфата натрия, В) осажденного додецилсульфата натрия при плотности энергии 500 мДж/см2 и давлении около атмосферного (10 Торр).
На Фиг.16 показана диаграмма соударений каскада Андерсена для порошка ТА без покрытия и с покрытием из додецилсульфата натрия.
На Фиг.17 показана кривая выделения препарата Griseofulin (GRIS), покрытого PLGA  и GRIS без покрытия
и GRIS без покрытия  .
.
На Фиг.18 показана кривая выделения препарата Bupivacaine-HCl (ВUP), покрытого PLGA  и BUP без покрытия
и BUP без покрытия  .
.
На Фиг.19 показан протонный ЯМР-спектр А) исходного PC, В) исходного PEG20K и С) твердой мишени PC+PEG20K, осаждаемой при атмосферном давлении.
На Фиг.20 показан протонный ЯМР-спектр А) исходного PC, В) исходного PEG400 и С) жидкой мишени PC+PEG400, осаждаемой при атмосферном давлении.
На Фиг.21 показан протонный ЯМР-спектр А) исходного PC, В) исходного PEG20K и С) гель-образной мишени PC+PEG20K (термическое смешивание), осаждаемой при атмосферном давлении.
На Фиг.22 показан протонный ЯМР-спектр А) исходного PC, В) исходного PEG400 и С) замороженной жидкой мишени PC+PEG400, осаждаемой при атмосферном давлении.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способам нанесения покрытий на материалы частиц и к материалам частиц с покрытием, полученным этими способами. К частицам, на которые наносится покрытие по настоящему изобретению, относятся такие частицы, на которые требуется нанести тонкое покрытие. Такие частицы (центральные части или сердцевины частиц) могут включать, но не ограничиваются ими, лекарственные препараты для людей или животных, косметику, пестициды, гербициды, фунгициды, краски или пигменты, а также инертные частицы, для которых требуется тонкое покрытие. Конечно, это изобретение также применимо к нанесению на инертные частицы тонких слоев активных материалов. Примерами могут служить нанометровые частицы с биологически активными покрытиями, например, антигенами, нуклеиновыми кислотами, протеинами или даже лекарственными препаратами. Существует множество разных возможностей и их сочетаний.
В частности, настоящее изобретение относится к материалам твердых частиц в виде лекарственного препарата или материалов доставки лекарственного препарата, покрытых материалом, который может подвергаться биологическому разложению или обладает биологической совместимостью, включая полимеры, подверженные биологическому разложению или обладающие биологической совместимостью. Покрытие может передавать материалу частиц целый ряд характеристик, включая изменение их поверхностных свойств, скорости растворения, или скорости диффузии и/или выделения активного компонента. Кроме того, в настоящем изобретении предлагается способ приготовления составов материалов частиц, покрываемых ультратонкими слоями покрывающих материалов, предпочтительно органическими полимерами, наносимыми с помощью неводных технологий, не связанных с применением растворителей. В частности, одним из предпочтительных способов является способ осаждения из паровой фазы, например, абляция импульсным лазером. Среди других преимуществ описываемых способов можно назвать контроль толщины и однородности покрытия на поверхностях отдельных твердых частиц лекарственных препаратов.
А. СПОСОБЫ ПОЛУЧЕНИЯ ЧАСТИЦ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ С ПОКРЫТИЕМ
Способ по настоящему изобретению включает физическое осаждение из паровой фазы полимерного покрытия на поверхность материала мишени. Специалистам хорошо известны методы физического осаждения из паровой фазы, которые включают такие способы, как термовакуумное испарение, напыление и лазерная абляция материала мишени для получения потока материалов покрытия, которые затем вступают в контакт с материалом центральной части частиц, и позволяют образовывать на них покрытие. Наиболее предпочтительным способом является лазерная абляция. Для достижения конкретных целей данного процесса нанесения покрытий в зависимости от количества пара или продолжительности фазы осаждения можно менять количество частиц покрытия и толщину получаемого слоя покрытия на материале центральной части частицы. Лазерная абляция для частиц покрытия при очень низком давлении описана в документе WO 00/28969, описание которого дается в списке противопоставленных документов.
На протяжении всего описания термины "материал центральной части частиц", "сердцевина частиц" и "центральная часть частиц" будут использоваться как взаимозаменяемые, так же как и термины "материал покрытия", "частицы покрытия" и "материалы покрытия частиц". Эти взаимозаменяемые термины в данном тексте имеют одинаковое значение.
Для получения ультратонких, тонких и гранулированных частиц материалов, частиц лекарственных препаратов с толщиной покрытия, передающего улучшенные фармацевтические качества приготавливаемым лекарственным препаратам, сопоставимой с размерами от размера атомов до нанометрового диапазона, используется абляция импульсным лазером. Желательно применять способы нанесения покрытия по настоящему изобретению, что обеспечит защиту центральной части частиц лекарственного препарата от влияния условий, способных разложить, разрушить или изменить активность самого лекарственного препарата.
Применение абляции импульсным лазером также минимизирует термическое разложение или денатурирование самого материала покрытия и обеспечивает нанесение материала покрытия на центральную часть частиц лекарственных препаратов, которое в течение процесса осаждения может выполняться при температуре окружающей среды и атмосферном давлении.
Путем регулирования физических параметров процесса осаждения (включая фоновый газ, и давление, и время нанесения покрытия) квалифицированный специалист может впервые приготовить различные лекарственные препараты, включая ультратонкие покрытия частиц. В частности, данный способ обеспечивает контроль как за протяженностью молекулярного покрытия, так и толщиной получаемого слоя покрытия на поверхности частиц лекарственных препаратов. Как относительно толстые, так и относительно тонкие слои покрытия могут выполняться при контроле за продолжительностью процесса лазерной абляции и за воздействием частиц покрытия на материал покрытия, уносимый лазером.
Путем правильного выбора плотности энергии материал мишени для покрытия уносится в виде кластеров, что обеспечивает неизменность большей части характеристик материала мишени. В общем, чем больше плотность энергии (флюенс), тем больше абляция воспринимает от природы атома, и в состав уносимого потока попадают атомы, которые не обладают признаками исходного материала.
Для обеспечения оптимального осаждения покрытия на поверхность центральной части частицы могут применяться псевдоожиженные слои или механизмы перемешивания для перемешивания центральных частей частиц во время процесса нанесения покрытия как для того, чтобы предотвратить агломерацию получаемых центральных частей частиц с покрытием, так и для контроля за толщиной покрытия на сердцевине частиц. К числу таких механизмов можно отнести организацию потока воздуха или газа или какой-либо другой текучей среды на пути движения частиц мишени для обеспечения их перемешивания во время процесса осаждения, или организацию альтернативного физического перемешивания. Для достижения планируемых результатов в некоторых случаях требуется использовать как механическое перемешивание, так и псевдоожиженное состояние частиц, получаемое с помощью пневматики. В способе по настоящему изобретению предлагается некоторое усовершенствование процесса получения отдельных частиц с покрытием, которые после нанесения покрытия по существу не образуют агломерации.
Осуществление процесса нанесения покрытия почти при атмосферном давлении предполагает наличие непрерывной технологии. Вместо необходимости применять вакуумную технологию для каждой партии при нанесении покрытий способ по настоящему изобретению, осуществляемый почти при атмосферном давлении, предусматривает непрерывную обработку. Например, частицы без покрытия переносятся в напылительную камеру с псевдоожиженным слоем и на них наносится покрытие при атмосферном давлении с применением способа по настоящему изобретению. Механизм непрерывного псевдоожижения, например газовый поток, способен поднять в напылительную камеру только непокрытые частицы. После нанесения покрытия частицы становятся тяжелее и выпадают из газового потока для обеспечения их транспортировки из камеры. В другом случае для одновременного разделения частиц и нанесения на них покрытия в непрерывном режиме может использоваться несущий газовый поток (циклон). На протяжении этого процесса частицы без покрытия транспортируются внутрь, а покрытые частицы наружу. Кроме того, для улучшения характеристик псевдоожиженного слоя при пониженных расходах газового потока можно в нижней части устроить механическое перемешивание. Сравнительно инертная атмосфера обеспечивается путем непрерывной подачи газа типа гелия в камеру. Газ после фильтрации и очистки может циркулировать многократно. Желательно, чтобы применяемый газ был сравнительно легок и инертен. Предпочтительно использовать такие газы, как гелий, аргон, азот и т.п. В другом случае, при необходимости, можно дополнительно использовать газ, обладающей более высокой химической активностью, или использовать только этот газ.
В соответствии с настоящим изобретением в напылительной камере поддерживается давление, близкое к атмосферному, и его значение может составлять в нижнем пределе приблизительно 10 Торр до высшего предела приблизительно 2500 Торр.
Предпочтительно, чтобы давление в напылительной камере было больше 20 или 30 или 40 или 50 Торр, но лучше, если оно будет приблизительно 100 или 500 Торр, но лучше всего, если оно будет больше 700 Торр. Желательно, чтобы давление в напылительной камере было меньше приблизительно 1000 Торр, еще лучше, если оно будет меньше приблизительно 900 Торр, но лучше всего, если оно будет меньше приблизительно 820 Торр. В самом лучшем варианте давление в напылительной камере должно составлять приблизительно 760 Торр или быть атмосферным.
Желательно, чтобы в процессе нанесения покрытия использовались такие материалы, которые при абляции с помощью энергетического источника образовывали бы пар из дискретных частиц очень малого размера - желательно, чтобы средний диаметр частиц покрытия был в диапазоне от приблизительно 1 нанометра до приблизительно 1000 нанометров. Следует понимать, что эти частицы не обязательно должны иметь сферическую форму - они могут быть неправильной формы. Таким образом, когда упоминается диаметр, то это значит, что говорится об "эквивалентном диаметре" или о "геометрическом эквивалентном диаметре", предполагая при этом, что частицы могут быть неправильной формы. Измерения проводятся с помощью рассеянного света с применением, например, счетчика Коултера (Beckman Coulter, Inc., г.Фуллертон, штат Калифорния, США). Методики измерения частиц неправильной формы обсуждаются в Статистике малых частиц, ссылка на которую дается в списке противопоставленных документов.
В состав материалов для осаждения, которые используются при изготовлении частиц лекарственных препаратов с покрытием, могут входить неорганические или органические материалы, включая, но не ограничиваясь ими, полимеры, протеины, сахара, липиды, а также биологически активные керамики, анионные, катионные или амфотерные полимеры или липиды, а также антитела или антигены. В предпочтительном варианте изобретения для лазерной абляции и осаждения на поверхность соединений лекарственных препаратов используется органический полимер. В частности, желательно, чтобы в качестве материалов покрытий использовались органические соединения типа молочной кислоты, гликолевой кислоты, PLGA и родственные им полимеры, подверженные биологическому разложению, и их производные.
Материалы, наносимые в качестве покрытия, могут использоваться для изменения скорости выделения активного соединения центральной части частиц или скорости их включения клетками. Такие покрытия, обеспечивающие длительное выделение лекарственного препарата могут действовать с помощью механизмов диффузии или растворения.
Покрытия могут также улучшать физическую стабильность частиц лекарственных препаратов, например, их устойчивость к образованию сколов или трещин. Покрытие может также служить препятствием на пути проникновения влаги, увеличивающим сроки хранения лекарственных препаратов, подверженных быстрому разложению. Обеспечивая сухое нанесение покрытий на частицы лекарственных препаратов, настоящее изобретение является особенно перспективным, позволяющим продлить сроки хранения этих препаратов. Таким образом, настоящее изобретение наилучшим образом подходит для фармацевтических композиций, чувствительных к влаге или растворителям (типа протеинов), что затрудняет нанесение на них покрытий. Настоящее изобретение решает эту проблему. Кроме того, качество покрытия по настоящему изобретению, т.е. его возможность избежать пористости, уникально и дает еще одно преимущество при нанесении покрытий на чувствительные составы.
Уникальным аспектом настоящего изобретения является способность получать непористые покрытия. При использовании методик нанесения покрытий, основанных на применении растворителей, получаются пористые покрытия, так как во время сушки растворитель испаряется, оставляя после себя в покрытии мельчайшие поры. Так как во время нанесения покрытия образуются поры, то для обеспечения необходимой целостности покрытия требуется увеличить его толщину. Таким образом, при использовании методики, основанной на применении растворителей, требуется наносить более толстое покрытие. В противоположность этому в настоящем изобретении предлагается способ нанесения чрезвычайно тонких покрытий, относительная толщина которых составляет от 10 до 50 нм, при нанесении которых используются частицы нанометрового диапазона, что, по крайней мере, частично объясняется почти полным отсутствием пор, что в свою очередь обеспечивает целостность такого покрытия.
Покрытие может также играть непосредственную роль в фармакологии или фармакокинетике частиц лекарственных препаратов. Например, покрытие может изменять взаимодействие частиц с тканями или клетками, направляя их в специфические типы клеток или тканей, или улучшая их включение клетками, или даже провоцируя иммунный ответ. Способ по настоящему изобретению может даже использоваться для нанесения нуклеиновых кислот на инертные частицы с целью трансфекции растений или животных с помощью бомбардировки частицами (для применения в "генной пушке"). Существует очень много возможностей и поэтому все из них здесь перечислить нельзя. Короче говоря, в данном изобретении предлагается способ нанесения покрытий на частицы для любой известной области применения частиц с покрытием и для областей применения, раскрываемых здесь впервые.
При использованием раскрываемых здесь устройства и способа лазерной абляции эти материалы можно без труда осаждать на поверхности частиц лекарственных препаратов при любом размере этих частиц и обеспечивая при этом любую толщину слоя. Этот способ можно использовать для осаждения покрытий, с нанесением одного или большего числа слоев, состоящих из частиц нанометрового диапазона (толщина каждого слоя составляет от приблизительно 1 нм до приблизительно 1000 нм), на центральные части частиц, диаметр которых находится в диапазоне от приблизительно 0,1 мкм до приблизительно 1 мм. Средний диаметр получаемых в результате частиц лекарственных препаратов с покрытием составляет от приблизительно 0,1 мкм до нескольких миллиметров. Очевидно, что размер частицы с покрытием зависит от потребностей пользователя и колеблется от частиц с покрытием меньшего размера, которые могут найти применение, например, в молекулярной биологии до частиц с покрытием большего размера, которые могут найти применение, например, в приготовлении лекарственных препаратов.
Для получения более однородного покрытия во время осаждения материал центральной части (сердцевины) покрываемой частицы должен быть в псевдоожиженном состоянии, создаваемом с помощью потока газа и/или механическим способом. Толщина покрытия, размер частиц и адгезия могут меняться, что обеспечивается контролем за условиями процесса во время осаждения.
Этот способ нанесения покрытия обеспечивает быстрое испарение с использованием импульсного эксимерного лазера в качестве источника тепла для нанесения твердых материалов на частицы. При использовании этого способа масса материала покрытия составляет не более 1-5% от массы частицы, а время нанесения покрытия меньше одного часа, и при этом нет необходимости сушить растворители. Этот способ имеет широкий диапазон применения в фармацевтике и обеспечивает улучшение свойств агломерации и текучести, повышает стабильность, улучшает включение клетками и межклеточные взаимодействия, а также контроль скорости выделения лекарственного препарата.
С помощью описанных здесь аппарата и способов можно получать частицы лекарственных препаратов и частицы доставки лекарственных препаратов с полимерными покрытиями, подверженными биологическому разложению или обладающими биологической совместимостью, контролируемой толщины и однородности. Толщина покрытия частицы лекарственного препарата может контролироваться до нанометровых значений, а инкапсуляция может быть частичной или полной.
На материал сердцевины частиц, размер которой может меняться, например, от нескольких нанометров до нескольких миллиметров в диаметре, наносится сравнительно однородное дисперсное дискретное или сплошное покрытие из отдельных частиц, размеры которых находятся в диапазоне от размеров, сопоставимых с размерами атомов, и до нескольких нанометров. Частицы покрытия создаются осаждением из паровой фазы и, предпочтительно, лазерной абляцией, в процессе которой пучок импульсного лазера направляется на мишень, состоящую из материала покрытия при условиях, достаточных для испускания мишенью отдельных частиц в направленный под прямым углом к мишени абляционный поток, при этом для мишени может применяться, например, твердый материал, замороженная жидкая матрица и т.п. Абляция импульсным лазером особенно подходит для многоэлементных осаждений, в которых поддерживается стехиометрия уносимых веществ. Это может быть важно, когда в качестве материалов покрытия используются органические соединения типа полимеров или другие мезоскопические вещества типа антибиотиков (Agarwal, 1998 г.). Во время лазерной абляции материал центральной части частиц может перемешиваться или быть в псевдоожиженном состоянии, поэтому сохраняется непрерывное движение всех центральных частей частиц. Относительная площадь покрытия, наносимого на поверхность частицы, регулируется изменением параметров лазера, включая плотность энергии, число импульсов, а также временем обработки.
На частицы лекарственных препаратов и фармацевтических соединений может наносится однородное покрытие. Такое покрытие может задерживать диффузию и растворение лекарственного препарата до тех пор, пока не произойдет диффузия лекарственного препарата через покрытие в случае с покрытием, не подверженным биологическому разложению. Однородное покрытие может также использоваться для защиты частицы лекарственного препарата от неблагоприятных условий окружающей среды. Скорость выделения лекарственного препарата может регулироваться с помощью покрытия, которое оказывает влияние на поверхностные свойства частиц. Покрытие способно также предотвращать измельчение частиц лекарственного препарата в случае дробления прессованных таблеток, которое обеспечивается более слабым взаимодействием частиц и их разделением по границе раздела прежде, чем произойдет разрушение самой частицы лекарственного препарата под действием напряжения. Покрытие может также улучшить характеристики текучести, что очень важно для процесса изготовления или повышения эффективности механизмов доставки лекарственных препаратов.
В. УСТРОЙСТВА ДЛЯ НАНЕСЕНИЯ ПОКРЫТИЯ НА ЧАСТИЦЫ
Устройства по настоящему изобретению, в общем, состоят из напылительной камеры, в которой размещаются материал мишени и вещество частицы. Внешний источник напыления, типа импульсного эксимерного лазера, попадает в камеру через окно, предпочтительно кварцевое, и взаимодействует с матричной мишенью. В другом варианте устройства источник напыления выполнен встроенным, т.е. в такой же камере, с такой же матрицей и частицами.
Слой материала мишени нанометровой толщины абсорбирует энергию лазерного импульса, поверхность быстро нагревается, и от мишени отходит шлейф уносимых частиц размеров, соизмеримых с размерами атомов, до частиц микрометрового диапазона. Затем шлейф частиц осаждается на псевдоожиженные центральные части (сердцевины) частиц.
В области мишени абсорбируется энергия падающего потока, например, энергия эксимерного лазера (ультрафиолетовый эксимерный лазер с излучением в диапазоне длин волн 193-308 нм, твердотельные лазеры на иттрий-алюминиевом гранате с неодимом с излучением в диапазоне длин волн 255-1064 нм). Глубина абсорбции падающего потока лазерного излучения зависит от структуры биологически совместимой мишени и обычно находится в пределах от 10 до 100 нм. Быстрая (в течение нескольких наносекунд) абсорбция и последующий нагрев поверхности мишени лазерным импульсом обеспечивает выход энергии, необходимый для осаждения полимера из биологически совместимой мишени. В результате фазовых превращений в мишени, нагреваемой в наносекундном диапазоне, поверхность матричной мишени испускает плотный шлейф кластеров нанометрового размера, молекулы, цепи молекул, полимеры и/или фрагменты липидов. (Лазерная абляция полимеров рассматривается в работе Ogale, 1994 г., которая включена в прилагаемый список противопоставленных документов). Затем шлейф нанометровых кластеров, молекул, цепей молекул, полимеров и фрагментов липидов осаждается на центральных частях частиц, находящихся в псевдоожиженном состоянии. (Псевдоожижение рассматривается в работе Kodas и Hampden-Smith, которая включена в прилагаемый список противопоставленных документов).
В состав матричной мишени должна входить матрица из биологически совместимых материалов покрытия или материалов мишени, подверженных биологическому разложению и/или мезоскопических молекул, которые изменяют поверхностные взаимодействия. Биологически совместимые материалы покрытия, применяемые для изготовления матричной мишени, могут включать полимеры, протеины, сахара, липиды и/или биологически активные или неактивные материалы. Нанофункциональные молекулы, которые изменяют поверхностные взаимодействия, могут включать биологически активные керамики, анионные или катионные полимеры и липиды, антитела или антигены. Матричные материалы в твердом, жидком виде или в виде геля могут поочередно вводиться в виде дисперсии в растворитель, который испаряется сравнительно быстро из центральных частей частиц. В качестве центральных частей частиц могут использоваться фармацевтически релевантные частицы, например, активные лекарственные препараты, фармацевтически инертные частицы наполнителей или другие предварительно изготовленные смеси частиц.
Желательно, чтобы для получения более однородного покрытия центральные части частиц или материалы частиц предварительно переводились в псевдоожиженное состояние в напылительной камере. Предпочтительно, чтобы псевдоожижение выполнялось с применением воздушного или газового потока. Это значит, что центральные части частиц или материалы центральной части частиц размещаются на пути потока воздуха или газа, который переводит эти частицы в псевдоожиженное состояние, что улучшает их перемешивание и воздействие на них атмосферы напылительной камеры. Псевдоожиженное состояние можно также получить и механическим перемешиванием, но использование для этих целей воздуха или газа является более предпочтительным. К предпочтительным можно также отнести и комбинированное псевдоожижение, получаемое с использованием как струи воздуха или газа, так и механического перемешивания.
Использование внешнего источника напыления (например, лазера) и отдельно стоящей камеры напыления позволяет изменять структуру покрытия и его толщину в широком диапазоне. Кроме того, при использовании соответствующего внешнего источника напыления можно наносить на частицы покрытия из различных материалов. Состав покрытия строго зависит от технологических параметров лазера, например, от потока энергии падающего излучения (Дж/см2), частоты повторения лазерных импульсов, давления газа, создающего псевдоожиженный слой, молекулярной массы газа, создающего псевдоожиженный слой, расстояния между мишенью и субстратом, коэффициента оптического поглощения матричной мишени и других узлов.
На Фиг.1 показан пример воплощения настоящего изобретения. Устройство, изображенное на Фиг.1, является устройством 1 с напылением сверху. В состав устройства 1 с напылением сверху входит камера напыления 2, которая состоит из цилиндрической части 5, соединенной с конической частью 3. Хотя на Фиг.1 показана цилиндрическая камера напыления, тем не менее, она может иметь и другое сечение в зависимости от требований пользователя или изготовителя, включая, например, квадратное, прямоугольное или многогранное.
Коническая часть 3 соединена своим коническим концом с газопроницаемой пористой пластиной 7 и газораспределителем 9, примыкающим к пластине 7. С другого конца цилиндрической части 5 установлен фильтр 11 с цилиндрическим кожухом. По вытяжному каналу 13 циркулирует газ, который через сборку фильтра 15, газодувку (не показана), регулятор температуры 17 возвращается обратно на вход газораспределителя 9 и затем попадает в камеру напыления. Циркуляция, фильтрация и контроль температуры технологического газа являются предпочтительными аспектами настоящего изобретения.
В состав устройства 1 с напылением сверху входит внешний источник напыления 21, который направлен вверх в центральную камеру 2 через окно 23 на матричную мишень 25 приблизительно под углом 45°. Окно 23 выполняется из оптически прозрачного материала, предпочтительно из кварца. Шлейф 27 отходит от матричной мишени 25 вниз по направлению к псевдоожиженному слою частиц 41, расположенному под матричной мишенью 25. Шлейф 27 наносит покрытие на частицы 41, которые контактируют друг с другом.
Для подачи питания на матричную мишень 25 или ее поворота используется внешнее устройство управления 31 и контейнер 33 с трубкой управления двигателем поворота и/или подачи питания. Контейнер 33 может также включать охладитель для заморозки материала матричной мишени 25.
Частицы 41 находятся в псевдоожиженном слое при регулируемой температуре, и растворитель 43 из матричной мишени 25 высушивается во время процесса напыления. Вместе с псевдоожижением, основанном на подаче потока газа, можно использовать и механический вибратор 45, что предотвращает агломерацию частиц и позволяет подавать газ на псевдоожижение при меньшем расходе.
На Фиг.2 показано другое воплощение настоящего изобретения - устройство 101 с напылением снизу. В состав устройства 101 с напылением снизу входит камера напыления 102, которая состоит из цилиндрической части 105, соединенной с конической частью 103. Коническая часть 103 соединена своим коническим концом с газопроницаемой пористой пластиной 107 и газораспределителем 109, примыкающим к пластине 107. С другого конца цилиндрической части 105 установлен фильтр 111 с цилиндрическим кожухом. По вытяжному каналу 113 циркулирует газ, который через сборку фильтра 115, газодувку (не показана), регулятор температуры 117, возвращается обратно на вход газораспределителя 109 и затем попадает в камеру напыления.
Внешний источник напыления 121, расположенный вне камеры 102, направлен вниз в камеру напыления 102 через окно 123 на матричную мишень 125 приблизительно под углом 45°. Аэрозольный шлейф 127 отходит от матричной мишени 125 вверх по направлению к псевдоожиженному слою частиц 141, расположенному над матричной мишенью 125, и наносится на поверхности частиц 41 в качестве частичного покрытия.
Для подачи питания на матричную мишень 125 или ее поворота используется внешнее устройство управления 131 и контейнер 133 с трубкой управления двигателем поворота и/или подачи питания. Контейнер 133 может также включать охладитель для заморозки материала матричной мишени 125.
Частицы 141 находятся в псевдоожиженном слое при регулируемой температуре, и растворитель 143 из матричной мишени 125 высушивается во время процесса напыления. Вместе с псевдоожижением, основанном на подаче потока газа, можно использовать и механический вибратор 145, что предотвращает агломерацию частиц и позволяет подавать газ на псевдоожижение при меньшем расходе.
В предпочтительном варианте устройства по настоящему изобретению и как показано на Фиг.1 и 2 для изготовления частиц с покрытием в качестве метода физического осаждения из паровой фазы используется лазерная абляция. При желании для получения потока уносимых веществ, осаждаемых на материале субстрата, могут использоваться другие методы физического осаждения из паровой фазы, например термовакуумное испарение или напыление. Обычно в качестве лазера, применяемого для осуществления способа по настоящему изобретению, используется импульсный эксимерный газовый лазер модели 1248 Lambda Physik с длиной волны в ультрафиолетовом диапазоне 248 нм. Могут также применяться и многие другие подходящие лазеры, например, лазеры на иттрий-алюминиевом гранате с неодимом с излучением в диапазоне длин волн 255-1064 нм. С помощью лазерного пучка получают поток частиц, который располагается под прямым углом к поверхности мишени.
Длина волны лазерного излучения выбирается на основе природы материала, подвергаемого абляции. Высокий коэффициент поглощения и низкая отражательная способность являются фактором, обеспечивающим эффективный перенос материала с помощью процесса абляции. Коэффициент поглощения зависит от типа материала и длины волны лазерного излучения и в некоторых случаях от интенсивности лазерного излучения. Обычно при повышении температуры поверхности повышается и коэффициент поглощения материала. Таким образом, выбор длины волны лазерного излучения зависит от типа и характеристик уносимого материала.
Кроме того, для длин волн в синей и ультрафиолетовой областях спектра коэффициент поглощения повышается, а отражательная способность падает. Таким образом, хотя и можно использовать излучение любой длины волны, излучение с длиной волны менее 350 нм может обеспечить более эффективный перенос материала.
Ввиду того, что в соответствии с предпочтительным вариантом изобретения система лазера и камера напыления выполняются отдельно друг от друга, возможно изменение экспериментальных параметров в широком диапазоне. При использовании соответствующего лазера эта технология может применяться для нанесения на частицы покрытий из различных материалов. Состав покрытия зависит от технологических параметров лазера, например, от потока энергии падающего излучения (Дж/см2), частоты повторения лазерных импульсов, расстояния между мишенью и субстратом, коэффициента оптического поглощения мишени.
В большинстве случаев камера напыления выполняется отдельно от лазера. Однако при использовании компактных лазеров, типа твердотельного лазера с длиной волны в диапазоне от 248 до 1056 им, лазер можно крепить сбоку камеры напыления. К числу особых условий, которые влияют на осаждение покрытия, можно отнести следующие: (I) контроль за работой лазера; (II) контроль за размером лазерного пятна; (III) контроль за составом и расходом газа; (IV) контроль за скоростью пульсаций; (V) число импульсов и длина волны светового излучения. Контролируя все эти параметры, которые различны для различных материалов, можно менять такие характеристики покрытия частиц лекарственных препаратов, как целостность, микроструктура, топология, архитектура, толщина и адгезия.
С. СОСТАВЫ ЧАСТИЦ С ПОКРЫТИЕМ
Описываемые здесь методики нанесения можно применять к разнообразным составам, включая, но не ограничиваясь ими, составы фармацевтических композиций для людей или животных, составы для биотехнологий, гербициды или пестициды. Фармацевтические композиции включают органические и неорганические активные соединения, включая биологически активные пептиды, протеины и нуклеиновые кислоты. Фармацевтические композиции по настоящему изобретению могут доставляться с помощью ингаляции, через дыхательный тракт, а также через рот, парентерально или через кожу. С помощью имплантанта или другой структуры, обеспечивающей медленное выделение лекарственного препарата, такие составы могут вводиться в тело вручную. Кроме того, поверхность частиц может дополнительно снабжаться сайт-специфическими веществами, обеспечивающими перенос центральной части лекарственного препарата к определенной ткани. Способы доставки таких составов хорошо известны и описаны во втором издании книги "Современная фармацевтика" (Modern Pharmaceutics), второе издание, под редакцией Банкера Г.С. и Родеса С.Е. (Gilbert S. Banker & Christopher T. Rhodes), ссылка на которую приводится в списке противопоставленных документов.
В одном из вариантов настоящего изобретения лекарственный препарат для приема через рот имеет тонкое пленочное покрытие по настоящему изобретению. Образцы фармацевтических композиций, свойства которых улучшаются при нанесении такого покрытия, включают лекарственные препараты, используемые в структурах с контролируемым или направляемым выделением препарата, при маскировании вкуса или изменении поверхности частицы перед таблетированием или наполнением капсулы.
В другом варианте предлагается структура для приема через легкие на основе сухого порошка с тонким пленочным покрытием по настоящему изобретению. Образцы лекарственных препаратов для приема через легкие включают глюкокортикоид и другие лекарственные препараты, локализирующие астму, а также лекарственные препараты и биологически активные пептиды и протеины для систематического приема, типа инсулина, которые плохо усваиваются при приеме через пищеварительный тракт. Способ по настоящему изобретению обеспечивает высокую эффективность инкапсуляции, уменьшение числа частиц лекарственных препаратов, разрушаемых в процессе нанесения покрытия, и предотвращает получение таких покрытий, толщина которых препятствовала бы проникновению лекарственного препарата через дыхательные пути.
Лекарственные препараты локального применения, которые можно было бы использовать, включают антибиотики, антигрибковые препараты и противовоспалительные препараты местного применения. Лекарственные препараты парентерального применения, которые можно было бы использовать, включают многие используемые в настоящее время суспензии и препараты длительного или местного выделения или просто препараты для снижения гидратации и продления срока хранения порошкового протеина.
В иллюстративных воплощениях материалы покрытия могут осаждаться на поверхность частиц лекарственных препаратов с помощью процесса лазерной абляции, в котором диаметр отдельной частицы материала покрытия, осаждаемой на центральные части лекарственных препаратов, находится в пределах от приблизительно 1-2 нм до приблизительно 40-50 нм. Еще лучше, если диаметр этих частиц находится в диапазоне от приблизительно 3-4 нм до приблизительно 20-30 нм. В других примерах диаметр этих частиц находится в пределах от приблизительно 5-6 нм до приблизительно 10-15 нм. Изменяя соответствующие параметры процесса нанесения покрытия можно получать частицы с небольшим отклонением диаметра от среднего размера.
Такие слои не обязательно целиком покрывают поверхность частицы лекарственного препарата и в соответствии с некоторыми вариантами настоящего изобретения в значительной степени обеспечивается дискретное осаждение частиц покрытия на поверхности частиц лекарственных препаратов для получения частиц лекарственных препаратов с покрытием, имеющих конкретные, обусловленные фармацевтическими требованиями свойства. В некоторых случаях возникает необходимость получить такие покрытия, которые почти не покрывают поверхности частиц лекарственных препаратов.
Более того, в некоторых случаях может возникнуть необходимость покрывать частицы лекарственных препаратов смесями из двух или большего числа материалов. Такие покрывающие смеси могут готовиться таким образом, что каждый компонент из множества материалов покрытия может одновременно уноситься и наноситься на поверхности частиц лекарственных препаратов, или, что более традиционно, возможно возникнет необходимость чередовать или последовательно наносить два или большее число материалов на поверхность частиц лекарственного препарата. Возможности способа обеспечить многослойное покрытие могут потребоваться, в частности, для получения композиций с нормированным по времени, регулируемым или длительным выделением лекарственного препарата. Такие сочетания покрывающих материалов могут обеспечить получение вполне определенных свойств частиц лекарственных препаратов с покрытием, обусловленных конкретными фармацевтическими требованиями. Такие сочетания могут включать как сочетания инертных покрывающих материалов или сочетания покрывающих материалов, так и фармацевтически активных составов, или даже множества инертных материалов, и множества лекарственных препаратов или сайт-специфических структур направленного действия. Эти сочетания ограничены только выбором пользователя и совместимостью соединений.
Выбор размера центральной части частиц, выбор покрывающего материала (материалов), размер частиц покрывающих материалов, и общая толщина, и сплошная/дискретнаяая структура слоя (слоев) покрытия, конечно же, отличаются для разных случаев применения. Квалифицированные специалисты в состоянии отрегулировать эти параметры для приготовления частиц лекарственных препаратов с покрытием, имеющих вполне определенные, отвечающие требованиям физические или фармацевтические свойства. Выбор этих параметров часто зависит от конкретного состава, на который наносится покрытие, и/или от конкретного покрытия, которое наносится на основную частицу. Более того, получение основной частицы может меняться в зависимости от конкретной толщины покрытия, наносимого в процессе лазерной абляции. При некоторых обстоятельствах может возникнуть необходимость усушить, размолоть, распылить или другим способом уменьшить размеры материалов центральной части частиц для получения частиц определенного размера или консистенции перед осаждением покрывающих материалов (материала) или после их осаждения на поверхность частиц основного лекарственного препарата. Кроме того, разделение частиц и нанесение на них покрытия могут выполняться в непрерывном режиме с целью уменьшения агломерации и переноса частиц после достижения частицами заданного размера (с помощью циклона). Применяя хорошо известные в фармацевтике способы в другом варианте изобретения можно без труда добиться размалывания частиц лекарственных препаратов с покрытием или без покрытия. Например, для уменьшения размера частиц до конкретного среднего диаметра можно использовать механическую резку или размалывание. Более того, для обеспечения равномерности частиц по размеру в данной пробе могут применяться способы типа просеивания.
При необходимости не требуется ни размалывания, ни сортировки по крупности, а фактически лекарственные препараты, на которые наносится покрытие, проходят лазерную абляцию, описываемую здесь в их естественном или отвечающем техническим условиям состоянии. Кроме того, в тех случаях, когда получаемый материал покрытия сохраняет все или большинство своих характеристик, может даже не потребоваться обеспечивать заданный размер покрывающей частицы или заданную толщину покрытия или даже накладывать последовательно сплошные слои покрывающего материала на поверхность частицы лекарственного препарата.
Как описано выше, средняя толщина покрывающего материала (материалов), осаждаемого на поверхность центральной части частицы может находиться в диапазоне от приблизительно 1 нм до приблизительно 1000 нм. В некоторых вариантах изобретения частицы покрытия образуют один или несколько слоев на поверхности частиц лекарственных препаратов, при этом толщина каждого слоя составляет приблизительно 6, приблизительно 7, приблизительно 8, приблизительно 9, приблизительно 10, приблизительно 11, приблизительно 12, приблизительно 13, приблизительно 14, приблизительно 15, приблизительно 16, приблизительно 17, приблизительно 18, приблизительно 19, приблизительно 20, приблизительно 21, приблизительно 22, приблизительно 23, приблизительно 24, приблизительно 25, приблизительно 26, приблизительно 27, приблизительно 28, приблизительно 29, или приблизительно 30 нм. В других вариантах могут потребоваться чуть более толстые слои покрытий, и в этих примерах для применения в фармацевтике могут быть полезны покрытия частиц лекарственных материалов, средняя толщина слоев которых составляет приблизительно 31, приблизительно 32, приблизительно 33, приблизительно 34, приблизительно 35, приблизительно 36, приблизительно 37, приблизительно 38, приблизительно 40, приблизительно 41, приблизительно 42, приблизительно 43, приблизительно 44, приблизительно 45, приблизительно 46, приблизительно 47, приблизительно 48, приблизительно 49, приблизительно 50, приблизительно 51, приблизительно 52, приблизительно 53, приблизительно 54, приблизительно 55, приблизительно 56, приблизительно 57, приблизительно 58, приблизительно 59, или приблизительно 60 нм. Более того, если возникает необходимость использовать более толстые слои, то для покрытия частиц лекарственных препаратов, с целью получения частиц лекарственных препаратов, обладающих определенными фармацевтическими свойствами, могут потребоваться слои средней толщиной приблизительно 65, приблизительно 70, приблизительно 75, приблизительно 80, приблизительно 85, приблизительно 90, приблизительно 95, приблизительно 100, приблизительно 120, приблизительно 140, приблизительно 160, приблизительно 180, приблизительно 200, приблизительно 225, приблизительно 250, приблизительно 275, приблизительно 300, приблизительно 400, приблизительно 450, приблизительно 500, приблизительно 550, приблизительно 600, приблизительно 650, приблизительно 700, приблизительно 750, приблизительно 800, приблизительно 850, приблизительно 900, приблизительно 950, или даже приблизительно 1000 нм. Конечно, при необходимости путем изменения технологических параметров можно получить более толстые или более тонкие слои.
Как описано, средний диаметр центральной части частиц лекарственного препарата, на который наносится покрытие, может находиться в диапазоне размеров приблизительно от 0,1 мкм до приблизительно 1000 мкм. В некоторых вариантах изобретения средний диаметр частицы основного лекарственного препарата обычно составляет приблизительно 0,2, приблизительно 0,3, приблизительно 0,4, приблизительно 0,5, приблизительно 0,6, приблизительно 0,7, приблизительно 0,8, приблизительно 0,9, приблизительно 1, приблизительно 2, приблизительно 3, приблизительно 4, приблизительно 5, приблизительно 6, приблизительно 7, приблизительно 8, приблизительно 9, приблизительно 10, приблизительно 11, приблизительно 12, приблизительно 13, приблизительно 14, приблизительно 15, приблизительно 16, приблизительно 17, приблизительно 18, приблизительно 19, или приблизительно 20 мкм. Средний диаметр частиц некоторых лекарственных препаратов может быть чуть больше. Кроме того, данный способ может также применяться для нанесения покрытий на эти частицы. В этих примерах средние диаметры частиц лекарственных препаратов могут составлять приблизительно 21, приблизительно 22, приблизительно 23, приблизительно 24, приблизительно 25, приблизительно 26, приблизительно 27, приблизительно 28 приблизительно 29, приблизительно 30, приблизительно 40, приблизительно 50, приблизительно 60, приблизительно 70, приблизительно 80, приблизительно 90, приблизительно 100, приблизительно 120, приблизительно 140, приблизительно 160, приблизительно 180, приблизительно 200, приблизительно 220, приблизительно 240, приблизительно 260, приблизительно 280, приблизительно 300, приблизительно 350, приблизительно 400, приблизительно 450, или даже приблизительно 500 мкм. С помощью описываемого способа могут быть получены и промежуточные размеры по каждому из приведенных диапазонов, и эти промежуточные размеры относятся к объему настоящего изобретения.
Средние диаметры частиц лекарственных препаратов по настоящему изобретению могут меняться от приблизительно 0,1 мкм до приблизительно 2-3 мм включительно. В некоторых вариантах изобретения средний диаметр готовых частиц с покрытием обычно составляет приблизительно 0,2, приблизительно 0,3, приблизительно 0,4, приблизительно 0,5, приблизительно 0,6, приблизительно 0,7, приблизительно 0,8, приблизительно 0,9, приблизительно 1, приблизительно 2, приблизительно 3, приблизительно 4, приблизительно 5, приблизительно 6, приблизительно 7, приблизительно 8, приблизительно 9, приблизительно 10, приблизительно 11, приблизительно 12, приблизительно 13, приблизительно 14, приблизительно 15, приблизительно 16, приблизительно 17, приблизительно 18, приблизительно 19, или приблизительно 20 мкм. Средний диаметр частиц с покрытием некоторых лекарственных препаратов может быть чуть больше и составлять приблизительно 21, приблизительно 22, приблизительно 23, приблизительно 24, приблизительно 25, приблизительно 26, приблизительно 27, приблизительно 28 приблизительно 29, приблизительно 30, приблизительно 40, приблизительно 50, приблизительно 60, приблизительно 70, приблизительно 80, приблизительно 90, приблизительно 100, приблизительно 120, приблизительно 140, приблизительно 160, приблизительно 180, приблизительно 200, приблизительно 220, приблизительно 240, приблизительно 260, приблизительно 280, приблизительно 300, приблизительно 350, приблизительно 400, приблизительно 450, или даже приблизительно 500 мкм и может быть даже больше и составлять приблизительно 0,75, приблизительно 1,0, приблизительно 1,25, приблизительно 1,5, приблизительно 1,75, приблизительно 2,0, или даже приблизительно 2,5 мм. Во всех случаях предполагается, что с помощью описываемого способа могут быть получены и промежуточные размеры по каждому из приведенных диапазонов, и эти промежуточные размеры относятся к объему настоящего изобретения.
Предпочтительные размеры готовых частиц с покрытием зависят от области применения. Ниже описаны предпочтительные размеры частиц для различных областей применения.
D. ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ ЧАСТИЦЫ ЛЕКАРСТВЕННЫХ ПРЕПАРАТОВ
Настоящее изобретение также относится к описываемым здесь композициям из одного или большего числа составов частиц лекарственных препаратов с покрытием в фармацевтически приемлемых растворах для введения в клетку или приема животными, либо только к этой композиции, либо в сочетании этой композиции с одним или большим числом других лекарственных препаратов для терапии определенных болезней или состояний.
Описываемые здесь составы частиц лекарственных препаратов с покрытием могу вводиться в сочетании с другими препаратами типа протеинов или полипептидов или различными фармацевтически активными препаратами. Если состав содержит хотя бы один из описываемых здесь составов частиц лекарственных препаратов с покрытием, то существует возможность включения и других составов, при условии, что эти дополнительные препараты не вызовут серьезного неблагоприятного воздействия при контакте с целевой клеткой или основной тканью. Описываемые составы могут доставляться вместе с другими препаратами в соответствии с требованиями соответствующих инстанций. Такие вторичные составы, включаемые в фармацевтические композиции, могут очищаться от клеток хозяина или других биологических источников, или синтезироваться химическим способом, как описано здесь. В состав такой композиции могут входить замещенные или производные составы РНК, ДНК или полиядерные ароматические соединения, или в качестве такой композиции могут также применяться модифицированные производные, замещающие пептид или нуклеиновую кислоту, или другие лекарственные препараты с покрытием или без покрытия.
Композиции фармацевтически приемлемых наполнителей и растворов-носителей хорошо известны квалифицированным специалистам, как и разработки подходящих дозировок и режимов лечения для применения описываемых здесь соответствующих составов при различных режимах лечения, включая, например, разработку рецептуры и применение внутрь через рот, парентерально, внутривенно, интраназально, внутримышечно.
В общем, фармацевтически приемлемые частицы/материалы частиц по настоящему изобретению включают частицы от 0,1 мкм до 2-3 мм, при этом композиции для применения через рот включают частицы от 10 мкм до 1 мм или более, размеры частиц порошков для инъекции составляют от 80 мкм до 200 мкм, а размеры частиц порошка для ингаляции или назального применения составляют от 1 до 10 мкм (обычно для ингаляции - от 1 до 5 мкм, а для назального применения - от 1 до 10 мкм).
Настоящее изобретение, в частности, подходит для нанесения покрытий на лекарственные препараты нескольких классов, включая, но не ограничиваясь ими, порошки для ингаляции, типа глюкокортикоидов. Покрытия нанометровой толщины, наносимые на композиции из сухих порошков, улучшают свойства текучести и обеспечивают длительное выделение уже разработанных и утвержденных Управлением по контролю за качеством пищевых и фармацевтических продуктов композиций без изменения продукта, выпускаемого массовыми партиями, или его полной переработки.
Глюкокортикоиды оказывают благоприятное влияние при терапии различных легочных заболеваний, включая астму, саркоидоз и другие заболевания, связанные с альвеолитом. Хотя при таких состояниях глюкокортикоидная терапия является эффективной, ее длительное применение влечет за собой риск токсикоза и побочные эффекты (Mutschler и Derendorf, 1995 г.). Для снижения побочных эффектов были предприняты попытки использовать глюкокортикоиды, включая ТА, прошедшие клиническую апробацию, для обеспечения доставки в качестве аэрозолей или сухих порошков.
В последних исследованиях показано, что было достигнуто положительное влияние на легкие при внутритрахеальном введении крысам трех различных порошков и взвесей глюкокортикоида (Talton, 1999 г.). В другом случае при введении различных глюкокортикоидов внутритрахеально не наблюдалось направленного действия на легкие (отношение местного к системному эффектам) главным образом из-за быстрого поглощения липофильных стероидов (Hochhaus и др., 1995 г.). Из этого можно предположить, что направленное действие на легкие зависит от возможности медленного выделения при доставке лекарственного препарата, что обеспечивает длительное пребывание препарата в легких.
Как предполагалось, применение липосом обеспечивает длительное выделение различных лекарственных препаратов в легких, включая такие глюкокортикоиды, как беклометазон и дексаметазон (Tremblay и др., 1993 г., Fielding и Abra, 1992 г., Schreier и др., 1993 г.). Однако, хотя при равновесных условиях липосомы так же как и ТА имеют умеренную несущую способность по липофильным глюкокортикоидам (от 10 до 20%), при неравновесных условиях при растворении или введении ТА быстро выделяется из липосомной матрицы (Schreier и др., 1994 г.).
В соответствии с приведенными примерами настоящее изобретение, в частности, подходит для глюкокортикоидных композиций.
Устройства для доставки лекарственных препаратов, типа сухих порошковых ингаляторов и дозировочных ингаляторов, в последние несколько лет были усовершенствованы таким образом, что осаждение в легких может составить от 10% для традиционных систем доставки до 40% для недавно разработанных устройств третьего поколения (Newman и др., 1997 г.).
Интересно, что один из преобладающих факторов, ответственных за направленное действие в легких, среднее время пребывания препарата в легких, не был оценен всесторонне. Время пребывания в легких определяется скоростью выделения вдыхаемой частицы из вдыхаемой твердой (порошок) или другой системы доставки типа липосом, скоростью поглощения растворенного лекарственного препарата через легочные мембраны и клиренсом реснитчатого эпителия, который обеспечивает перенос частиц лекарственного препарата из верхних частей легких. Поглощение мембранами является быстрым процессом для липофильных глюкокортикоидов (Burton и Schanker, 1974 г.) и, следовательно, скорость растворения порошка глюкокортикоида будет основной детерминантой для регулирования времени пребывания в легких. Моделирование с использованием недавно разработанной PD/PD модели продемонстрировало, что для продуктов ингаляции с очень быстрой кинетикой выделения лекарственных препаратов не наблюдалось никакого направленного действия из-за очень быстрого поглощения из легкого в большой круг кровообращения. При увеличении скорости выделения лекарственных препаратов (скорость растворения) направленное действие в легком повышается, что видно из диссоциации легочной зоны и зоны системного рецептора. Дальнейшее снижение скорости выделения лекарственного препарата приводит к снижению направленного действия в легком, так как существенная часть лекарственного препарата удаляется через клиренс реснитчатого эпителия и после глотания доступна для поглощения через рот. Таким образом, вдыхаемый глюкокортикоид должен обладать определенными характеристиками растворения или выделения для того, чтобы продемонстрировать существенные свойства направленного действия.
Однако это изобретение подходит для приготовления всех форм фармацевтических препаратов, некоторые из которых обсуждаются ниже.
1. Оральный прием
Описываемые здесь фармацевтические препараты могут доставляться путем введения животным через рот и таким образом эти составы могут составляться с использованием инертного разбавителя или усвояемого пищевого носителя, или они могут заключаться в жесткие или мягкие желатиновые капсулы, или они могут запрессовываться в таблетки, или они могут добавляться непосредственно в состав пищи диеты.
Составы, содержащие частицы лекарственного препарата с покрытием, могут даже входить в состав наполнителя и использоваться в виде проглатываемых таблеток, трансбукальных таблеток, пастилок, капсул, эликсиров, взвесей, сиропов, облаток и т.п. (Mathiowitz и др., 1997 г.; патент США №5641515; патент США №5580579; патент США №5792451; каждый из этих источников включен в список противопоставленных документов). Эти таблетки, пастилки, пилюли, капсулы и т.п. также могут содержать следующие элементы: связующее, например, резиновую смесь трагакант, акацию, зерновой крахмал или желатин; наполнитель типа фосфата дикальция; распадающийся препарат типа зернового крахмала, картофельного крахмала, альгиновой кислоты и т.п.; смазку типа стеарата магния; может добавляться подслащивающий препарат типа сахарозы, лактозы или сахарина или ароматизирующее вещество типа перечной мяты, винтергринового масла или аромата вишни. При использовании в качестве дозировочной единицы одной капсулы в ее состав может входить помимо перечисленных выше препаратов еще и жидкий носитель. Другие материалы могут присутствовать в качестве покрытий или другим способом изменять физическую форму дозировочной единицы. Например, таблетки, пилюли или капсулы могут покрываться шеллаком, сахаром или ими обоими. Сироп или эликсир могут содержать сахарозу активных элементов в качестве метила подслащивающего препарата и пропилпарабены в качестве консервантов, пигмент и ароматизатор, например, вишневый или апельсиновый. Конечно, любое вещество, применяемое при изготовлении дозировочной единицы любой формы, должно быть фармацевтически чистым и в значительной степени нетоксичным в применяемых количествах. Кроме того, активные компоненты могут включаться в состав препаратов и композиций длительного выделения.
Обычно эти композиции могут содержать, по крайней мере, приблизительно 0,1% активного состава или больше, хотя относительное массовое или объемное содержание активного ингредиента (ингредиентов) может, безусловно, меняться и в общем случае составлять от приблизительно 1 или 2% до приблизительно 95 или 98% или больше от массы или объема всей композиции. Естественно, что количество активного состава (составов) в каждой терапевтически полезной смеси может готовиться таким образом, чтобы получить подходящую дозу в каждой дозировочной единице состава. Такие факторы как растворимость, биологическая пригодность, биологический период полураспада, маршруты введения, сроки хранения, а также другие фармакологические соображения должны учитываться специалистами во время приготовлению таких фармацевтических композиций, желательно также учитывать и разнообразие дозировок и режимов лечения.
При оральном введении лекарственных препаратов смеси по настоящему изобретению могут попеременно чередоваться с одним или большим числом наполнителей в форме растворов для полоскания рта, зубного порошка, трансбукальных таблеток, распылителей для полости рта или подъязычной композиции. Например, раствор для полоскания можно приготовить включением необходимых количеств активных ингредиентов в соответствующий раствор, например, в раствор борнокислого натрия (раствор Добеля). В другом случае активный ингредиент можно включать в раствор для полоскания рта, в состав которого входит борнокислый натрий, глицерин и бикарбонат калия, или в зубной порошок, включающий гели, пасты, порошки и взвеси, или использовать в качестве добавки в терапевтически эффективных количествах к зубной пасте, которая может включать воду, связующие, абразивные материалы, ароматизаторы, пенообразующие вещества и гигроскопические вещества, или заключать в таблетку или раствор, которые можно положить под язык или по-другому растворить во рту.
2. Введение с помощью инъекции
В другом случае описываемые здесь фармацевтические композиции могут вводиться парентерально, внутривенно, внутримышечно или даже интроперитонеально как описано в патенте США №5543158; патенте США №5641515; патенте США №5399363 (каждый из них включен в список противопоставленных документов). Растворы активных составов в виде фармацевтически приемлемых солей можно готовить в воде, смешанными соответствующим образом с поверхностно активными веществами, типа гидроксипропилцеллюлозы. Дисперсии можно также готовить в глицерине, жидком полиэтиленгликоле, в их смесях и в маслах. При обычных условиях хранения и использования в состав этих препаратов вводятся консерванты, которые предотвращают развитие микроорганизмов.
Фармацевтические формы, подходящие для инъекций, содержат стерильные водные растворы или дисперсии (патент США №5466468, который включен в список противопоставленных документов). Во всех случаях эта форма должна быть стерильной и должна быть жидкой до такой степени, чтобы можно было применять шприц. Эта форма должна обладать устойчивостью в условиях изготовления и хранения и должна быть защищена от проникновения в нее микроорганизмов типа бактерий и грибков. Носителем может быть растворитель или дисперсная среда, содержащая, например, воду, этанол, высокомолекулярный спирт (например, глицерин, пропиленгликоль и жидкий полиэтиленгликоль и т.п.), подходящие смеси из них и/или растительные масла. Необходимая текучесть может обеспечиваться, например, применением покрытия типа лецитина, обеспечением необходимого размера частиц в случае дисперсии и использованием поверхностно-активных веществ. Для защиты от действия микроорганизмов можно использовать различные антибактериальные и антигрибковые препараты, например, парабены, хлорбутанол, фенол, сорбеновая кислота, тимерозал и т.п., во многих случаях желательно включать изотонические препараты, например сахара или хлорид натрия. Обеспечение длительного поглощения инъецируемых составов может осуществляться при использовании препаратов, задерживающих поглощение, например моностеарата алюминия и желатина.
Для парентерального введения в виде, например, водного раствора, этот раствор, при необходимости, должен быть соответствующим образом забуферен, и жидкий разбавитель должен сделать сначала его изотоническим с достаточным содержанием соли или глюкозы. Эти конкретные водные растворы особенно подходят для внутривенного, внутримышечного, подкожного и интроперитонеального введения. Специалистам хорошо известна стерильная водная среда, которая может найти применение в этой связи. Например, одну дозу можно растворить в 1 мл изотонического раствора NaCl и либо добавить к 1000 мл жидкости, вводимой в подкожную клетчатку, либо инъецировать в предложенное место введения (см., например, Фармацевтические науки Ремингтона, 15-е издание, стр. 1035-1038 и 1570-1580, см. также список противопоставленных документов). Некоторые изменения дозировки происходят в зависимости от состояния объекта лечения. Лицо, ответственное за введение препарата, должно в любом случае определять соответствующую дозу индивидуально для каждого объекта лечения. Кроме того, для введения человеку препараты должны соответствовать требованиям стерильности, пирогенности, и общей безопасности, и эталонам чистоты в соответствии с требованиями биологических стандартов Управления по контролю за качеством пищевых и фармацевтических продуктов.
Стерильные инъецируемые растворы готовятся путем введения необходимых количеств активных смесей в соответствующий раствор, содержащий и другие ингредиенты, перечисленные выше, в соответствии с требованиями, соблюдаемыми при стерилизации фильтрацией. В общем случае дисперсии готовятся путем включения различных активных ингредиентов в стерильное средство доставки, которое содержит основную дисперсную среду и другие необходимые ингредиенты, перечисленные выше. В случае стерильных порошков для приготовления стерильных инъецируемых растворов желательно, чтобы в качестве способов их приготовления применялась вакуумная сушка и сублимационная сушка, которые обеспечивают получение порошка активного ингредиента и вдобавок к нему любого требуемого ингредиента из предварительно стерилизованного фильтрацией раствора.
Составы лекарственного препарата, на который наносится покрытие описываемым здесь способом, могут быть составлены либо в их естественной форме, либо в форме соли. Фармацевтически приемлемые соли включают кислые соли (имеющие три аминогруппы протеинов) и получены с использованием неорганических кислот, например соляной или фосфорной кислоты, или таких органических кислот, как уксусная, щавелевая, винная, миндальная и т.п. Соли с тремя карбоксильными группами могут быть также получены из нерганических оснований, например натрия, калия, аммония, кальция или гидроокисей железа, и таких органических оснований, как изопропиламин, триметиламин, гистидин, прокаин и т.п. После получения растворы вводятся способом, обеспечивающим необходимую дозировку, и в терапевтически эффективных количествах. Могут использоваться различные формы дозировок, например инъецируемые растворы, капсулы с лекарственными препаратами и т.п.
"Носитель" включает растворы, дисперсные среды, средства доставки, покрытия, разбавители, антибактериальные и антигрибковые препараты, изотонические препараты и препараты, задерживающие поглощение, буферные растворы, растворы-носители, взвеси, коллоиды и т.п. Применение таких сред и препаратов для фармацевтически активных веществ хорошо известно специалистам. Исключение составляют только те среды или препараты, которые не совместимы с активным ингредиентом. В эти составы могут также включаться дополнительные активные ингредиенты.
Выражение "фармацевтически приемлемый" относится к молекулярным веществам и составам, применение которых не влечет за собой аллергических или подобных нежелательных реакций при их введении человеку. Специалистам хорошо известны способы получения водного состава, который в качестве активного ингредиента содержит протеин. Обычно такие составы готовятся как инъецируемые либо в виде водных растворов, либо суспензий; как твердые формы для получения из них растворов или суспензий в жидкости. Препарат может быть также эмульгирован. Иммуногенетические составы, типа вакцин, которые вызывают иммунную реакцию, должны быть фармацевтически приемлемыми.
3. Назальное введение
Учитывается также введение фармацевтических композиций с помощью интраназального распылителя, ингаляции и/или других средств доставки аэрозолей. Способы доставки генов, нуклеиновых кислот и пептидных составов непосредственно в легкие посредством назальных аэрозольных распылителей описаны, например, в патенте США №5756353; патенте США №5804212 (каждый из этих источников включен в список противопоставленных документов), а способы доставки лекарственных препаратов с использованием интраназальных смол из микрочастиц (Takenaga и др., 1998 г.) и лизофосфатид-глицериновых составов (патент США №5725871, включен в список противопоставленных документов) также хорошо известны. Более того, доставка лекарственных препаратов через слизистую в виде несущей матрицы политетрафторэтилена описана в патенте США №5780045 (включен в список противопоставленных документов).
Введение аэрозольных композиций лекарственных препаратов по настоящему изобретению может выполняться способами, описанными в патенте США №5849265 и в патенте США №5922306 (каждый из этих источников включен в список противопоставленных документов).
В частности, в число предпочтительных лекарственных препаратов для введения с использованием аэрозольных композиций в соответствии с настоящим изобретением входят (но не ограничиваются ими) антиаллергетики, бронхолитические средства и противовоспалительные стероиды, применяемые при лечении респираторных заболеваний типа астмы и т.п.
Лекарственные средства, на которые могут наноситься покрытия и которые могут вводиться в виде аэрозольных композиций в соответствии с настоящим изобретением, включают любой лекарственный препарат, применяемый в терапии с помощью ингаляции, который может иметь форму, нерастворимую в значительно степени в газе-вытеснителе. Таким образом соответствующие лекарственные препараты могут отбираться, например, из анальгетиков (кодеин, дигидроморфин, эрготамин, фентанил, морфин и т.п.); ангинозных препаратов; антиаллергетиков (хромогликат, кетотифен, недохромил и т.п.); противоинфекционных препаратов (цефалоспорины, пенициллины, рифампицин, стрептомицин, сульфонамиды, макролиды, пентамидины, тетрациклины и т.п.); антигистаминные препараты (метапирилен и т.п.); противовоспалительных препаратов (флунизолид, будезонид, типредан, триамцинолонацетонид и т.п.); противокашлевые средства (носкапин и т.п.); бронхолитических средств (эфедрин, адреналин, фенотерол, фомлотерол, изопреналин, метапротеренол, фенилэфрин, фенилпропанолаин, пирбутерол, репротерол, римитерол, тербуталин, изоэтарин, тулобутерол, орхипреналин и т.п.); мочегонных препаратов (амилорид и т.п.); антихолинергических средств (ипратропиум, атропин, окситропиум и т.п.); гомонов (кортизон, гидрокортизон, преднизолон и т.п.); ксантинов (включая аминофиллин, холин теофиллин, лизин теофиллинат и теофиллин); и терапевтических протеинов и пептидов (например, инсулин или глюкагоны).
Специалисты должны понимать значение того, что при определенных обстоятельствах частицы лекарственных препаратов с покрытием по настоящему изобретению могут выполняться в виде солей (например, щелочных металлов, или солей амина, или кислые соли), или сложных эфиров (например, низшие алкилсодержащие сложные эфиры), или в качестве сольватов (например, гидратов) с целью оптимизации активности, и/или обеспечения стабильности лекарственного средства, и/или минимизации растворимости лекарственного средства в средстве доставки или газе-вытеснителе.
Специалисты должны понимать значение того, что аэрозольные композиции в соответствии с настоящим изобретением при необходимости могут включать в свой состав сочетания из двух или большего числа активных ингредиентов. Известны аэрозольные составы, содержащие два активных ингредиента (в обычной системе с газом-вытеснителем), например, для лечения респираторных заболеваний типа астмы. В соответствии с настоящим изобретением предлагаются также аэрозольные композиции, в состав которых входят два или большее число лекарственных средств, состоящих из твердых частиц, покрытых в соответствии со способом по настоящему изобретению. Эти лекарственные средства могут составляться из подходящих комбинаций упоминаемых здесь лекарственных средств типа будезонида (BUD), триамцинолонацетонида (ТА), флутиказон пропината (FP) и т.п. или могут даже включать подходящие комбинации других бронхолитических средств (включая эфедрин и теофиллин, фенотерол, ипратропиум, изоэтарин, фенилэфрин и т.п.).
Предпочтительные аэрозольные композиции по настоящему изобретению включают легочные лекарственные препараты в эффективных количествах, состоящих из частиц с полимерным покрытием, и фторированный углеводородный газ или фторхлорированный углеводородный газ вытеснитель, содержащий водород. Готовая аэрозольная композиция обычно может иметь следующее массовое содержание: от приблизительно 0,005 весовых % до приблизительно 10 весовых % частиц лекарственного препарата с покрытием, лучше от приблизительно 0,05 весовых % до приблизительно 5 весовых % частиц лекарственного препарата с покрытием, еще лучше от приблизительно 0,1 весовых % до приблизительно 3,0 весовых % частиц лекарственного препарата с покрытием от общей массы композиции.
В качестве газа-вытеснителя для применения в настоящем изобретении может использоваться либо фторированный углеводородный газ, фторхлорированный углеводородный газ, содержащий водород или их смеси, как описано в патенте США №5922306.
4. Дополнительные виды введения лекарственных препаратов
Помимо описанных выше способов доставки в качестве альтернативных видов доставки составов частиц лекарственных препаратов с покрытием рассматриваются также следующие методы. Как описано в патенте США №5656016, эхофорез (например, ультразвуковой) применялся для увеличения скорости и эффективности проникновения лекарственных препаратов в систему циркуляции и для переноса по ней. В качестве альтернативы доставки лекарственных средств рассматривалась внутрикостная инъекция (патент США №5779708), устройство с микропроцессором (патент США №5797898), офтальмологические композиции (Bourlais и др., 1998 г.), чрескожные матрицы (патент США №5770219 и патент США №5783208) и доставка с обратной связью (патент США №5697899), все эти источники включены в список противопоставленных документов.
Е. СОСТАВЫ ДЛЯ НАНЕСЕНИЯ ПОКРЫТИЙ
Материалы мишени, используемые для нанесения покрытий, включают большую часть твердых веществ, используемых в настоящее время в фармацевтике и пищевой промышленности, а именно те материалы, которые могут эффективно подвергаться абляции с помощью энергетического источника. Эти материалы включают, но не ограничиваются ими, полимеры, полисахариды и протеины, подверженные биологическому разложению или обладающие биологической совместимостью. В число подходящих полимеров, подверженных биологическому разложению, входят полилактиды, полигликолиды, поликапролактоны, полидиоксаноны, поликарбонаты, полигидроксибутираты, полиаклиленоксалаты, полиангидриды, полиамиды, полиэфирные амиды, полиуретаны, полиацетаты, поликеталы, полиортокарбонаты, полифосфазены, полигидроксивалераты, полиалкиленсукцинат, поли(яблочная кислота), поли(аминокислоты), поливинилпирролидон, полиэтилнгликоль, полигидроксицеллюлоза, полиортоэфиры и их сочетания, а также другие полимеры полимолочной кислоты и сополимеры, полиортоэфиры, и поликапролактоны, и т.п. в число полимеров, обладающих биологической совместимостью, входят полиэтиленгликоли, поливинилпирролидон и поливиниловые спирты и т.п. в число подходящих полисахаридов входят декстраны, целлюлоза, ксантам, хитины, хитозаны и т.п. В число подходящих протеинов входят полилизины и другие полиамиды, коллаген, альбумин и т.п. В патенте США №5702716 описан целый ряд материалов, которые могут использоваться в качестве материалов для нанесения покрытий.
F. СУБСТРАТЫ ДЛЯ НАНЕСЕНИЯ ПОКРЫТИЙ
Сердцевина занимает основную часть частицы с покрытием или материала частицы при использовании способа, применяемого для получения частиц размером от приблизительно 0,1 до приблизительно 1000 мкм. Понятно, что размер центральной части (сердцевины) частицы, может быть меньше - до нескольких нанометров в диаметре, или больше - до нескольких миллиметров в диаметре. Материалы сердцевины удерживаются внутри контейнера для обработки, объем которого достаточен для того, чтобы частицы внутри него могли передвигаться. Верх контейнера открыт или закрыт сеткой для предотвращения выхода из него частиц и во время псевдоожижения контейнер сохраняет вертикальное положение или на части поверхности контейнера для обработки, например, на всей боковой поверхности или поверхности днища или только на части этих поверхностей выполняются отверстия для удержания центральных частей частиц внутри контейнера для обработки, если осаждение покрытия на частицы происходит сбоку или снизу.
Сердцевины частиц должны перемешиваться или приводиться в псевдоожиженное состояние таким образом, чтобы вся поверхность каждой основной частицы подвергалась воздействию частиц покрытия, поступающих в контейнер для обработки с целью обеспечения однородности покрытия и предотвращения агломерации центральных частей отдельных частиц. Такое псевдоожиженное состояние может обеспечиваться различными способами механического перемешивания, включая вибрацию, вращение или перемещение контейнера для обработки, с помощью перемешивающего устройства, устанавливаемого внутри контейнера, желательно при помощи пневматического перемешивания, путем пропускания потока газа через центральные части частиц. Специалистам хорошо известны механизмы для приведения частиц в псевдоожиженное состояние, и примеры таких устройств описаны в книге "Псевдоожижение" (Fluidization, под редакцией Grace и Matsen, Plenum Press, Нью Йорк, 1980 г.), описание которой приводится в списке противопоставленных документов.
Относительная доля площади покрытия частиц регулируется путем контроля за размером частиц покрытия и временем обработки. Чем дольше обработка, тем больше частиц покрытия прилипает к поверхности сердцевины, увеличивая при этом как долю площади покрытия, так и толщину покрывающего слоя. Доля площади покрытия может регулироваться от 1 до 100%. Размер частиц покрытия контролируется составом атмосферы. Желательно использовать инертные газы типа гелия, аргона или азота и т.п., но могут использоваться и химически активные газы. Химически активные газы типа кислорода, аммиака или закиси азота обеспечивают более высокие концентрации молекул, в противоположность атомам, изотопам внутри потока уносимых частиц и применяются тогда, когда требуется осаждение кислорода, азота или подобных частиц.
Давление внутри системы обычно бывает близким к атмосферному, т.е. приблизительно 1 атм или приблизительно 760 Торр. Однако давление может меняться до некоторой степени и может быть как низким приблизительно 10 Торр, так и высоким приблизительно 2500 Торр или принимать любое промежуточное значение. Желательно, чтобы давление в камере напыления было выше приблизительно 20, или 30, или 40, или 50 Торр, лучше, если оно будет больше приблизительно 100 или 500 Торр, но лучше всего, если оно будет больше приблизительно 700 Торр. Желательно, чтобы давление в напылительной камере было меньше приблизительно 1000 Торр, еще лучше, если оно будет меньше приблизительно 900 Торр, но лучше всего, если оно будет меньше приблизительно 820 Торр. В самом лучшем варианте давление в напылительной камере должно составлять приблизительно 760 Торр или быть атмосферным. Давление может меняться и принимать значения как внутри этих диапазонов, так и около этих величин.
К. МИКРОИНКАПСУЛЯЦИЯ
Область микроинкапсуляции является относительно новой, которая прежде ограничивалась методиками выпаривания растворителей (Thies, 1982 г.; Manekar и др., 1992 г.; Conti и др., 1992 г.). в настоящее время в промышленности существует несколько различных способов нанесения покрытий на частицы, главным образом путем напыления покрытий (Gopferich и др., 1994 г.). Пранлукаст - ингибитор лейкотриена, инкапсулированный с помощью нанометровых сфер гидроксипропилметилцеллюлозы, полученной распылительной сушкой, показал повышение эффективности при ингаляции, но не показал существенной разницы в скорости растворения (Kawashima и др., 1998 г.). К недостаткам нанесения покрытий микронной толщины (10-100 мкм) для длительного выделения препаратов можно отнести как то, что необходимо сушить большие количества растворителей в условиях вентилирования, так и то, что при увеличении размера частиц уменьшается эффективность при использовании ингаляции (Zeng и др., 1995 г.; Talton, 1999 г.).
L. ПРИМЕРЫ
С помощью следующих примеров рассматриваются предпочтительные варианты изобретения. Специалисты должны понимать значение того, что методы, описанные в данных примерах авторами изобретения, предназначены для практического применения и могут рассматриваться как продолжение предпочтительных способов этого практического применения. Однако в свете настоящего описания специалисты должны понимать значение того, что в отдельных примерах возможны изменения, которые не меняют по существу объема и сущности настоящего изобретения.
1. Твердая матричная мишень при комнатной температуре
Требуемые биологически совместимые материалы покрытий (биологически активные керамики, анионные или катионные полимеры или липиды, антитела или антигены, биополимеры, лекарственные препараты, протеины, сахара, липиды, электронные полимеры, интеллектуальные полимеры, функциональные органические молекулы, метастабильные соединения и биологически неактивные материалы) могут сочетаться с N числом материалов составляющих частей (биологически активные керамики, анионные или катионные полимеры или липиды, антитела или антигены, биополимеры, лекарственные препараты, протеины, сахара, липиды, электронные полимеры, интеллектуальные полимеры, функциональные органические молекулы, метастабильные соединения и биологически неактивные материалы) с образованием твердой матричной мишени для нанесения покрытий на центральные части частиц. Все материалы составляющих частей вместе должны иметь в общем более высокий коэффициент поглощения излучения внешнего источника напыления, ослабляя тем самым взаимодействие излучения с биологическими материалами покрытий, обеспечивая тем самым перенос частиц покрытия на псевдоожиженные центральные части частиц, не оказывая при этом на них отрицательного влияния. В другом случае для того, чтобы сделать процесс нанесения покрытий на частицы более эффективным, химические свойства упомянутых выше материалов составляющих частей могут изменяться под действием внешнего источника напыления. В зависимости от состава и скорости переноса материалов составляющих частей выполняется или не выполняется их удаление по причине токсичности.
ПРИМЕР 1
С использованием мишени из твердой PLGA в течение различных временных интервалов в условиях псевдоожиженного слоя на триамцитонолонацетонид (ТА) наносилось покрытие. Перед нанесением покрытия на порошок на предметные стекла осаждалась пленка с целью идентификации материалов осажденной пленки.
PLGA осаждалось на медную сетку просвечивающего электронного микроскопа Joel 200 при атмосферном давлении для получения нанометровых частиц. На Фиг. 3 показаны результаты с изображением осажденной при атмосферном давлении пленки (увеличение 100000 X), полученные с помощью электронной просвечивающей микроскопии. На Фиг.4 показано другое изображение осажденной при атмосферном давлении пленки (увеличение 100000 крат), полученное с помощью электронной просвечивающей микроскопии.
Сферические частицы PLGA размером от 20 нм и меньше наблюдались при увеличении 100000 X. Эти частицы осаждались равномерно по субстрату при частоте повторения импульсов, равной только 5 при плотности энергии 750 мДж/см2.
Приведенные характеристики исходных материалов PLGA, HPMC, Eudragit 4135 и додецилсульфата натрия показывают универсальность процесса нанесения покрытий.
Характеристики, полученные с использованием ЯМР, показывает сильную зависимость максимумов характеристик осажденного материала от вида исходного материала (Фиг.5). При оптимальных условиях скорость осаждения PLGA также немного выше при давлении около атмосферного, чем при низком давлении (Фиг.6). На фиг.7 показаны результаты сравнения гельпроникающей хроматографии исходной PLGA и уносимой PLGA. В соответствии с результатами исследования покрытия из PLGA на порошке ТА, выполненного методом сканирующей электронной микроскопии, наблюдалось увеличение размера частиц в сравнении с исходными порошками ТА, подтверждая, что с помощью этого процесса можно получать сравнительно тонкие покрытия нанометрового диапазона (Фиг.8 и 9). Наконец, на Фиг.10 показано сравнение характеристик растворения ТА, покрытого PLGA, с характеристиками растворения исходного ТА; покрытие на порошок наносится в течение 30 минут и при этом обеспечивается выделение ин витро в течение 12-24 часов. Кроме того, успешно выполнялось и осаждение других материалов, включая поливинилпироллидон (PVP), полиэтиленгликоль (PEG), амилопектиновый крахмал, альбуминовый протеин и хитин.
ПРИМЕР 2
Покрытие из PLGA на альбумине бычьей сыворотки обеспечивает продолжительность выделения от 2 до 3 часов. Порошок альбумина бычьей сыворотки просеивался и фракции крупностью от 75 до 250 мкм покрывались сополимерами молочной и глюколевой кислот (poly(lactic-co-glycolic acid)-PLGA) в течение 30 минут. По три партии порошков массой 20 мг с покрытием и без покрытия растворялись в 40 мл изотонического соляного раствора в центрифужной пробирке вращающегося барабана при комнатной температуре. Отфильтрованные пробы отбирались через разные промежутки времени на протяжении 12 часов и анализировались с использованием пробы биоцинхониновой кислоты протеина на 96-луночной пластине и устройства считавания пластин при 568 нм. На Фиг.11 представлены результаты анализа.
ПРИМЕР 3
Другими подходящими материалами, используемыми в виде таблеток для приема внутрь, являются различные целлюлозы, например, гидроксипропилметилцеллюлоза (НРМС). Сначала для получения характеристик покрытия из гидроксипропилметилцеллюлозы осаждались на предметные стекла и затем в течение 30 минут на порошки ТА микронного диапазона крупности. На Фиг.12 показаны протонные ЯМР-спектры исходной гидроксипропилметилцеллюлозы и гидроксипропилметилцеллюлозы, осажденной при плотности энергии 500 мДж/см2, при давлении около атмосферного (10 Торр). Очевидно, что максимум концентрации 3,6 частей на миллион коррелирует с протонами метила и множественные максимумы концентраций 6 частей на миллион - с протонами полициклических соединений.
На Фиг.13 показаны экспериментальные результаты растворения для порошков ТА с покрытием и без покрытия. При использовании покрытий из гидроксипропилметилцеллюлозы 80% состава выделялось в течение периода времени от 2 до 4 часов, а при использовании покрытий из PLGA 80% состава выделялось в течение 24 часов, и как показали исследования с использованием метода соударений каскада Андерсена дополнительно была улучшена текучесть исследуемого материала.
ПРИМЕР 4
Другими подходящими материалами, используемыми в виде таблеток для приема внутрь, являются поли(акриловые кислоты), например, препарат Eudragit (Rohm), выделение которого зависит от уровня рН. Для получения характеристик на плоские предметные стекла наносились покрытия из препарата Eudragit. На Фиг.14 показаны протонные ЯМР-спектры исходного препарата Eudragit и осажденного препарата Eudragit.
ПРИМЕР 5
В качестве поверхностно-активного вещества, применяемого в таблетках для приема внутрь с целью повышения растворимости и текучести, использовался додецилсульфат натрия. Для получения характеристик на плоские предметные стекла наносились покрытия из додецилсульфата натрия. На Фиг.15 показаны протонные ЯМР-спектры исходного додецилсульфата натрия и осажденного додецилсульфата натрия.
Кроме того, с использованием метода соударений каскада Андерсена выполнялись измерения осаждений на порошке ТА с покрытием из додецилсульфата натрия и без него для разных этапов, основанные на аэродинамических размерах частиц. На Фиг.16 показано увеличение почти вдвое выделенной дозы порошка в сравнении с дозой порошка без покрытия, что объясняется более высокой текучестью и осаждением в легких.
ПРИМЕР 6
Покрытия из PLGA на препарате Griseofulvin (GRIS) (фунгистатик полсти рта) обеспечили длительность выделения от 12 до 24 часов. Порошки GRIS покрывались сополимерами молочной и глюколевой кислот (poly(lactic-co-glycol acid) - PLGA) в течение 30 минут при атмосферном давлении в потоке гелия и с механическим перемешиванием. Растворение 50 г порошка с покрытием и без него выполнялось в ванне растворения фармакопеи США (с частотой вращения мешалки 50 оборотов в минуту) в забуфекренном фосфатном соляном растворе с уровнем рН 7,4, содержащем 0,5% додецилсульфата натрия при 37°С. Отфильтрованные пробы отбирались через разные промежутки времени на протяжении 24 часов и анализировались с использованием пробы гидроксипропилметилцеллюлозы. На Фиг.17 представлены результаты анализа.
ПРИМЕР 7
Покрытия из PLGA на бупивакайн-НСl (bupivacaine-HCl-BUP) (инъецируемое болеутоляющее) обеспечили длительность выделения от 2 до 4 часов. Порошки GRIS покрывались сополимерами молочной и глюколевой кислот (poly(lactic-co-glycol acid)-PLGA) в течение 30 минут при атмосферном давлении в потоке гелия и с механическим перемешиванием. По три партии порошков массой 4 мг с покрытием и без покрытия растворялись в 40 мл изотонического соляного раствора в центрифужной пробирке вращающегося барабана при комнатной температуре. Отфильтрованные пробы отбирались через разные промежутки времени на протяжении 12 часов и анализировались в спектрометре ультрафиолетового излучения Бекмана при 568 нм. На Фиг.18 представлены результаты анализа.
ПРИМЕР 8
Для получения характеристик на предметные стекла с использованием твердой матрицы осаждались полиэтиленгликоль - PEG 20000, фосфатидилхолин (PC) (липид, присутствующий в мембране клетки). На Фиг.19 показаны протонные ЯМР-спектры А) исходного фосфатидилхолина (PC), исходного PEG400, и С) осажденного в течение 10 минут PEG400/PC при плотности энергии 500 мДж/см2.
2. Жидкая матричная мишень при комнатной температуре
Требуемые биологически совместимые материалы покрытий (биологически активные керамики, анионные или катионные полимеры или липиды, антитела или антигены, биополимеры, лекарственные препараты, протеины, сахара, липиды, электронные полимеры, интеллектуальные полимеры, функциональные органические молекулы, метастабильные соединения и биологически неактивные материалы) могут сочетаться с N числом материалов составляющих частей (биологически активные керамики, анионные или катионные полимеры или липиды, антитела или антигены, биополимеры, лекарственные препараты, протеины, сахара, липиды, электронные полимеры, интеллектуальные полимеры, функциональные органические молекулы, метастабильные соединения и биологически неактивные материалы) для образования жидкой матричной мишени для нанесения покрытий на центральные части частиц. Все материалы составляющих частей вместе должны иметь в общем более высокий коэффициент поглощения излучения внешнего источника напыления, ослабляя тем самым взаимодействие излучения с биологическими материалами покрытий, обеспечивая тем самым перенос частиц покрытия на псевдоожиженные центральные части частиц, не оказывая при этом на них отрицательного влияния. Хотя материалом мишени является жидкость, взаимодействие с излучением внешнего источника напыления в течение времени порядка нано-микросекунд позволяет произойти следующим событиям:
1) Нагрев зоны взаимодействия лазера.
2) Последующее отверждение и избирательное поглощение биологического покрытия и материалов составляющих частей.
3) Выпаривание биологически активного материала и нанесение его на центральные части частиц.
В другом случае для того, чтобы сделать процесс нанесения покрытий на частицы более эффективным, химические свойства упомянутых выше материалов составляющих частей могут изменяться под действием внешнего источника напыления. В зависимости от состава и скорости переноса материалов составляющих частей выполняется или не выполняется их удаление по причине токсичности.
ПРИМЕР 9
Для получения характеристик на предметные стекла с использованием твердой матрицы осаждлись полиэтиленгликоль - PEG 400, фосфатидилхолин (PC) (липид, присутствующий в мембране клетки). На Фиг.20 показаны протонные ЯМР-спектры А) исходного фосфатидилхолина (PC), исходного PEG400, и С) осажденного в течение 10 минут PEG400/PC при плотности энергии 500 мДж/см2.
3. Твердожидкая матричная мишень при комнатной температуре
Требуемые биологически совместимые материалы покрытий (биологически активные керамики, анионные или катионные полимеры или липиды, антитела или антигены, биополимеры, лекарственные препараты, протеины, сахара, липиды, электронные полимеры, интеллектуальные полимеры, функциональные органические молекулы, метастабильные соединения и биологически неактивные материалы) могут сочетаться с N числом материалов составляющих частей (биологически активные керамики, анионные или катионные полимеры или липиды, антитела или антигены, биополимеры, лекарственные препараты, протеины, сахара, липиды, электронные полимеры, интеллектуальные полимеры, функциональные органические молекулы, метастабильные соединения и биологически неактивные материалы) для образования гель-подобной матричной мишени для нанесения покрытий на сердцевины. Все материалы составляющих частей вместе должны иметь в общем более высокий коэффициент поглощения излучения внешнего источника напыления, ослабляя тем самым взаимодействие излучения с биологическими материалами покрытий, обеспечивая тем самым перенос частиц покрытия на псевдоожиженные центральные части частиц, не оказывая при этом на них отрицательного влияния. Разница между вторым и третьим случаями состоит в следующем:
1) Функционально мишень основана на поглощающей способности твердого материала, которая отличается от поглощающей способности жидкого материала, материала составляющей части или материала биологического покрытия.
2) Упомянутый выше твердый материал может выпадать из жидкого раствора во время реакции каталитического типа.
3) Материал составляющей части обеспечивает контроль за процессами взаимодействия, связанными с внешним источником напыления.
Хотя материалом мишени может быть твердый материал или композитный материал из твердой и жидкой фаз, взаимодействие с излучением внешнего источника напыления в течение времени порядка нано-микросекунд позволяет произойти следующим событиям:
1) Нагрев зоны взаимодействия лазера.
2) Последующее отверждение и избирательное поглощение биологического покрытия и материалов составляющих частей. В случае чистой жидкости твердые материалы составляющих частей могут осаждаться из раствора и играть роль участков избирательного поглощения, хромофор, частиц нанометровой крупности или объекта.
3) Выпаривание биологически активного материала и нанесение его на центральные части частиц.
В другом случае для того, чтобы сделать процесс нанесения покрытий на частицы более эффективным химические свойства упомянутых выше материалов составляющих частей могут изменяться под действием внешнего источника напыления. В зависимости от состава и скорости переноса материалов составляющих частей выполняется или не выполняется их удаление по причине токсичности.
ПРИМЕР 10
Для получения характеристик на предметные стекла с использованием гель-подобной матрицы осаждался полиэтиленгликоль - PEG 20000, после охлаждения осаждался фосфатидилхолин (PC) (смешанный с PEG 20K при 60°С). На Фиг.21 показаны протонные ЯМР-спектры А) исходного фосфатидилхолина (PC), В) исходного PEG20K, и С) осажденного в течение 10 минут геля PEG20K/PC при плотности энергии 500 мДж/см2
4. Твердая матричная мишень при температуре ниже комнатной
Требуемые биологически совместимые материалы покрытий (биологически активные керамики, анионные или катионные полимеры или липиды, антитела или антигены, биополимеры, лекарственные препараты, протеины, сахара, липиды, электронные полимеры, интеллектуальные полимеры, функциональные органические молекулы, метастабильные соединения и биологически неактивные материалы) могут сочетаться с N числом материалов составляющих частей (биологически активные керамики, анионные или катионные полимеры или липиды, антитела или антигены, биополимеры, лекарственные препараты, протеины, сахара, липиды, электронные полимеры, интеллектуальные полимеры, функциональные органические молекулы, метастабильные соединения и биологически неактивные материалы) для образования матричной мишени, замороженной при температуре ниже комнатной (<300 К) для нанесения покрытий на центральные части частиц. Все материалы составляющих частей вместе должны иметь в общем более высокий коэффициент поглощения излучения внешнего источника напыления, ослабляя тем самым взаимодействие излучения с биологическими материалами покрытий, обеспечивая тем самым перенос частиц покрытия на псевдоожиженные центральные части частиц, не оказывая при этом на них отрицательного влияния. Хотя материалом мишени может быть твердый материал или композитный материал из твердой и жидкой фаз, взаимодействие с излучением внешнего источника напыления в течение времени порядка нано-микросекунд позволяет произойти следующим событиям:
1) Нагрев зоны взаимодействия лазера.
2) Избирательное поглощение биологического покрытия и материалов составляющих частей.
3) Выпаривание биологически активного материала и нанесение его на центральные части частиц.
В другом случае для того, чтобы сделать процесс нанесения покрытий на частицы более эффективным, химические свойства упомянутых выше материалов составляющих частей могут изменяться под действием внешнего источника напыления. В зависимости от состава и скорости переноса материалов составляющих частей выполняется или не выполняется их удаление по причине токсичности.
ПРИМЕР 11
Для получения характеристик на предметных стеклах с использованием замороженной матрицы осаждался полиэтиленгликоль - PEG 400, с применением N2 мгновенно замораживался фосфатидилхолин (PC). На Фиг.22 показаны протонные ЯМР-спектры А) исходного фосфатидилхолина (PC), В) исходного PEG20K, и С) осажденного в течение 10 минут геля PEG20K/PC при плотности энергии 500 мДж/см2.
VI ПРОТИВОПОСТАВЛЕННЫЕ ДОКУМЕНТЫ
Сюда включены следующие литературные ссылки, а также ссылки, приведенные ранее по причинам, указанным в приведенном выше тексте:
Агарвал и Фадке, "Лазерное осаждение сверхмолекул структур на поверхности твердых тел", Mat Sci Eng С 6:13-17, 1998 г.
(Agarwal and Phadke, "Laser assisted deposition of supramolecular organizates on solid surfaces", Mat Sci Eng С 6:13-17, 1998).
"Современная фармацевтика", второе издание, под редакцией Байкера Г.С.и Родеса С.Е„ Нью-Йорк, 1990 г.
(Banker and Rhodes, Eds, Modern Pharmaceutics, Marcel Deklcer, Inc., New York, 1990).
Бурла и др., "Последние успехи в системах доставки лекарственных препаратов в области офтальмологии". Prog Retin Eye Res. 17(1): 33-58, 1998 г.
(Bourlais. et al., "Ophthalmic drug delivery systems - recent advances". Prog Retin Eye Res. 17(1); 33-58. 1998).
Буртон и Шанкер, "Поглощение кортикостероидов из легкого крысы". Steroids, 23(5):617-24. 1974 г.
(Burton and Schanker, "Absorption of corticosteroids from the rat lung," Steroids, 23(5):617-24. 1974).
Конти, Паванетто и Гента, "Применение полимолочной кислоты для получения систем доставки лекарственных препаратов в виде микрочастиц", J. Microencapsul., 9(2); 153-66, 1992 г.
(Conti, Pavanetto and Genta, "Use of polylactic acid for the preparation of microparticulate drug delivery systems," J.Microencapsul., 9(2); 153-66, 1992).
Филдинг и Абра, "Факторы, влияющие на скорость выделения тербуталина из липосомных композиций после внутритрахеальной инстилляции морской свинке", Pharm. Res., 9(2):220-23. 1992 г.
(Fielding and Abra, "Factors affecting the release rate of terbutaline from liposome formulations after intratracheal instillation in the guinea pig," Pharm. Res., 9(2):220-23. 1992).
Глатт, "Многоцелевая обработка с помощью псевдоожиженного слоя", Product Literature, 1998 г.
(Glatt, "Multi-purpose Fluid Bed Processing," Product Literature, 1998).
Гопферих А., Алонсо М. и Лангер Р., "Разработки и характеристики микроинкапсулированных микросфер", Pharm Res, 11(11): 1568-74. 1994 г.
(Gopferich, A., Alonso. M., and Langer, R., "Development and characterization of microencapsulated microspheres", Pharm Res, 11(11): 1568-74. 1994).
Хердан Г., Статистика Малых Частиц, Второе издание, Буттервортс, Лондон, 1960 г.
(Herdan. G. Small Particle Statistics, Second Edition. Butterworths, London, 1960).
Хохаус, Дерендорф, Моллманн и Гонзалес-Роти, "Аспекты фармакокинетики и фармакодинамики аэрозольной терапии с использованием глюкоконикоидов в качестве модели", J. din. Pharmacol. 37:881-92, 1997 г.
(Hochhaus, Derendorf, Mollmann and Gonzalez-Rothi, "Pharmacokinetic/pharmacodynamic Aspects of Aerosol Therapy Using Glucoconicoids as a Model." J. din. Pharmacol. 37:881-92, 1997).
Хохаус, Гонзалес-Роти, Лукьянов, Дерендорф, Шрайер и Далла Коста, "Оценка неправленного действия глюкокортикоида в легких с помощью рецептор-связывающих экс-виво исследований", Pharm. Res., 12:134-37, 1995.
(Hochhaus, Gonzalez-Rothi, Lukyanov, Derendorf, Schreier and Dalla Costa, "Assessment of glucocorticoid lung targeting by ex-vivo receptor binding studies," Pharm. Res., 12:134-37, 1995).
Хуанг, Тамада, Хохаус и Бодор, "Модель на основе AMI для оценки относительного связывающего сродства для глюкокортикоидов", 1-я конференция по оптимизации лекарственных препаратов черем ретрометаболизм, остров Амелия, Die Pharmazie. 1997 г.
(Huang, Tamada, Hochhaus and Bodor, "An AMI-based model for the estimation of the relative binding affinity for glucocorticoids," in "1st Drug Optimization via Retrometabolism Conference." Amelia Island: Die Pharmazie. 1997).
Кавашима, Серигано, Хино, Ямамото и Такеучи, “Новый способ проектирования порошка для повышения эффективности ингаляции аэрозолей сухого порошка пранлукастгидрата путем поверхностной модификации с помощью нанометровых сфер гидроксипропилметилцеллулозфталата”. Рharm. Res., 15(11): 1748-52. 1998 г.
(Kawashima, Serigano, Hino, Yamamoto and Takeuchi. "A new powder design method to improve inhalation efficiency of pranlukast hydrate dry powder aerosols by surface modification with hydroxypropylmethylcellulose phthalate nanospheres." Pharm. Res., 15(11); 1748-52. 1998).
Кодас Т. и Хампден-Смит М., Аэрозольная обработка материалов, Wiley-VCH, Нью-Йорк, 1999 г.
(Kodas, Т. and Hampden-Smith, M., Aerosol Processing of Materials. Wiley-VCH, New York, 1999).
Манекар, Пураник и Джоши, "Микроинкапсуляция пропранололгидрохлорида с помощью метода выпаривания растворителя", J. Microencapsul., 9(1):63-66, 1992 г.
(Manekar, Puranik and Joshi, "Microencapsulation of propranolol hydrochloride by the solvent evaporation technique,". J. Microencapsul., 9(1):63-66, 1992).
Матиович и др., "Микросферы, подверженные биологической эрозии в качестве потенциальных систем доставки лекарственных препаратов через рот". Nature, 386(6623): 410-4, 1997 г.
(Mathiowitz, et. AL, "Biologically erodable microspheres as potential oral drug delivery systems". Nature, 386(6623); 410-4, 1997).
Мутшлер и Дорендорф в кн. "Действия лекарственных средств", СКС Press, Boca Raton. FL, стр.286-87, 1995 г.
(Mutschler and Derendorf, in "Drug Actions," CRC Press, Boca Raton. FL, pp.286-87, 1995).
Ньюман, Стид, Ридер, Хупер и Зиренберг, "Эффективная доставка в легкие аэрозоли флунозолида с помощью нового переносного многодозового ручного распылителя", J.Pharm. Sci., 85:960-64, 1997 г.
(Newman, Steed. Reader, Hooper and Zierenberg, "Efficient delivery to the lungs of flunisolide aerosol from a new portable hand-held multidose nebulizer," J. Pharm. Sci., 85:960-64, 1997).
Огале С.Б., "Осаждение тонких полимерных пленок с помощью лазерной абляции", в кн. Осаждение тонких пленок с помощью импульсного лазера, под редакцией Чрисей Д.Б. и Хублера Г.К., Дж. Вилей анд Соне, Нью-Йорк, 1994 г., Гл.25.
(Ogale, S. В., "Deposition of Polymer Thin Films by Laser Ablation," in Pulsed Laser Deposition of Thin Films. Chrisey, D. B. and Hubler, G.K... Eds. John Wiley & Sons, New York. 1994, Chapter 25).
Шрайер, Гонзалес-Роти и Стеценко, J. Control Release. 24:209-23, 1993 г.
(Schreier, Gonzalez-Rothi and Stecenko, J.Control Release. 24:209-23, 1993).
Шрайер, Лукьянов, Хохаус и Гонзалес-Роти, "Аспекта термодинамики и кинетики взаимодействия триамцинолонацетодина с липосомами", Proceed Inter. Symp.Control. Rel. Bioact. Mater., 21:228-29, 1994 г.
(Schreier, Lukyanov. Hochhaus and Gonzalez-Rothi, "Thermodynamic and kinetic aspects of the interaction of triamcinolone acetonide with liposomes." Proceed Inter. Symp.Control. Rel. Bioact. Mater., 21:228-29, 1994).
Такенага М и др., "Микрочастицы резины в качестве потенциальной системы назальной доставки лекарственных препаратов для инсулина", J. Controlled Release, 52(1-2):81-7, 1998 г.
(Takenaga, M., et al., "Microparticle resins as a potential nasal drug delivery system for insulin" J Controlled Release, 52(1-2):81-7, 1998).
Талтон Дж. Д, д-р наук, тезисы, Университет Флориды, 1999 г.
(Talton, James D., Ph.D. Thesis, University of Florida, 1999).
Тиес, "Микрокапсулы в качестве устройств доставки лекарственных препаратов", Crit. Rev.Biomed. Eng., 8(4):335-83, 1982 г.
(Thies, "Microcapsules as drug delivery devices," Crit. Rev.Biomed. Eng., 8(4):335-83, 1982).
Тремблей, Териен, Рочлью и Кормиер, Eur. J. din. Inv., 23:656-61, 1993 г.
(Tremblay, Therien, Rocheleau and Cormier, Eur. J. din. Inv., 23:656-61, 1993).
Видгрен, Уалдреп, Арппе, Блэк, Родарте, Коле и Найт, "Исследование аэрозоли липосом белкометазондипроприонатдилауройлфосфатидилхолина на нормальных добровольцах", Int. J. Pharm., 115:209-16, 1995 г.
(Vidgren, Waldrep, Arppe, Black, Rodarte, Cole and Knight, "A study of99m technetium-labeled beclomethasone diproprionate dilauroylphosphatidylcholine liposome aerosol in normal volunteers," Int. J. Pharm., 115:209-16, 1995).
Зенг, Мартин и Марриот, "Контролируемая доставка лекарственных препаратов в легкие", Int. J. Pharm., 124:149-64, 1995 г.
(Zeng, Martin and Marriott, "The Controlled Delivery of Drugs to the Lungs," Int. J. Pharm., 124:149-64, 1995).
Все описанные и приведенные в формуле изобретения составы и способы могут быть составлены и применены без излишних экспериментов в свете настоящего описания. Так как составы и способы по настоящему изобретению описаны с помощью предпочтительных вариантов изобретения, то специалистам должно быть ясно, что возможны модификации этих составов, способов и этапов или последовательностей этапов описанных способов, что по существу не противоречит идее, не меняет объем и сущность настоящего изобретения. В частности должно быть очевидно, что при условии достижения такого же или сходного результата описанные здесь препараты могут заменяться родственными им по химическим или физиологическим свойствам препаратам. Все такие замены и модификации ясны для специалистов и не изменяют сущности, объема и идеи изобретения, сформулированных в приведенной формуле изобретения.
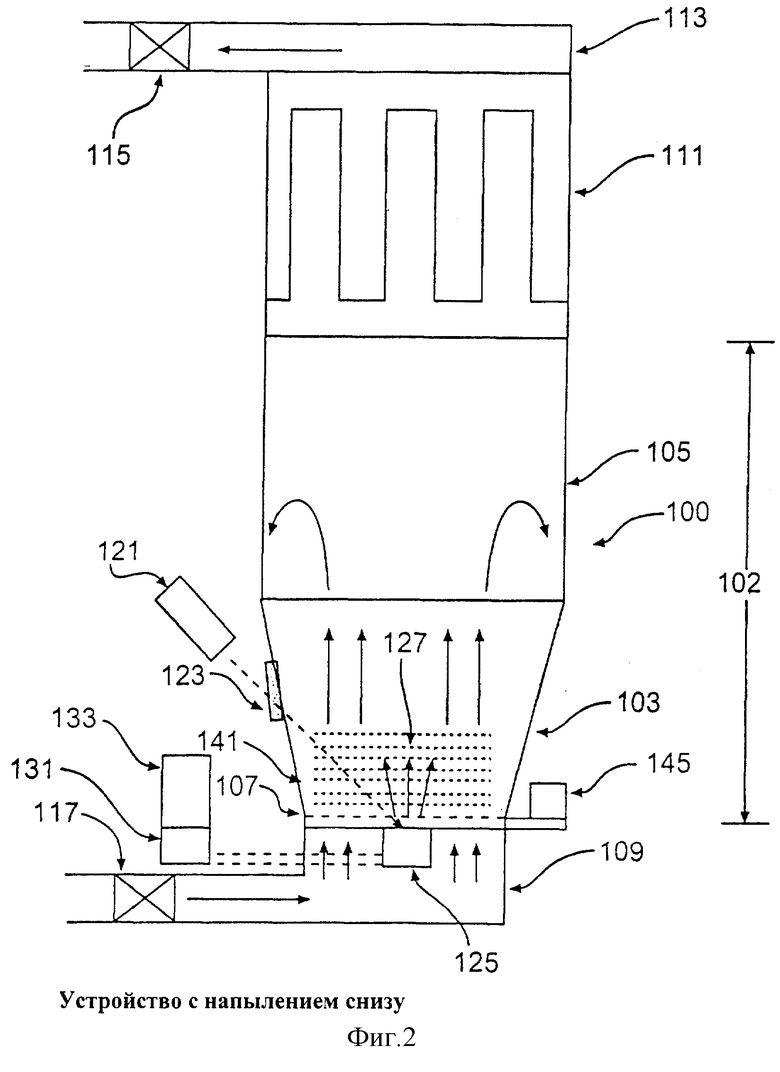
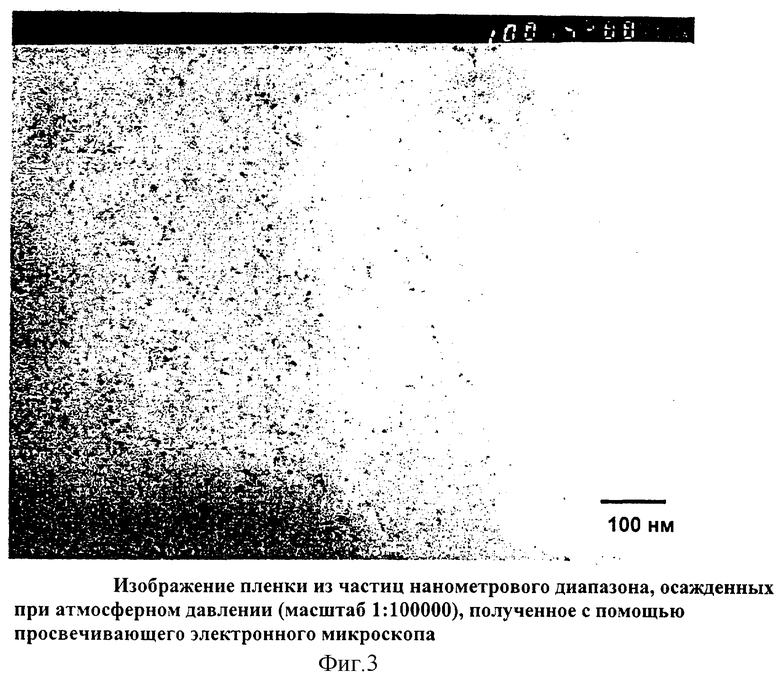
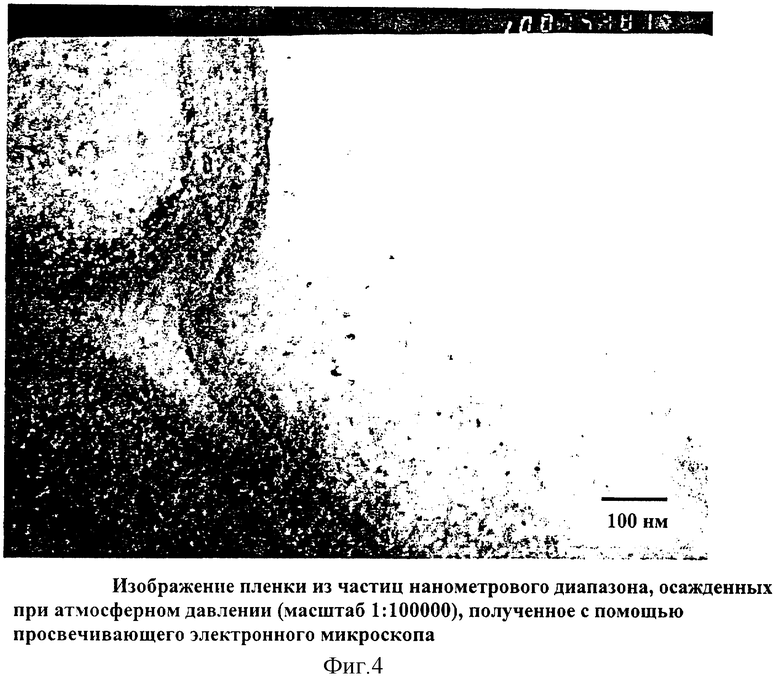
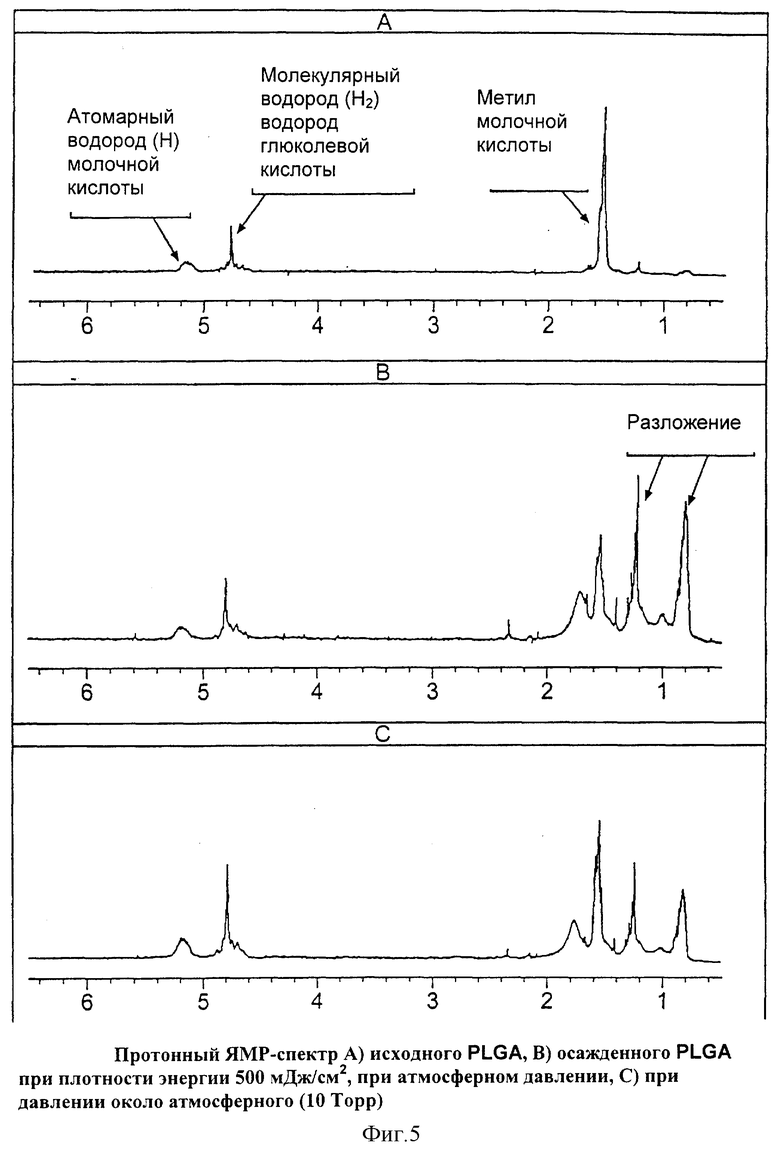
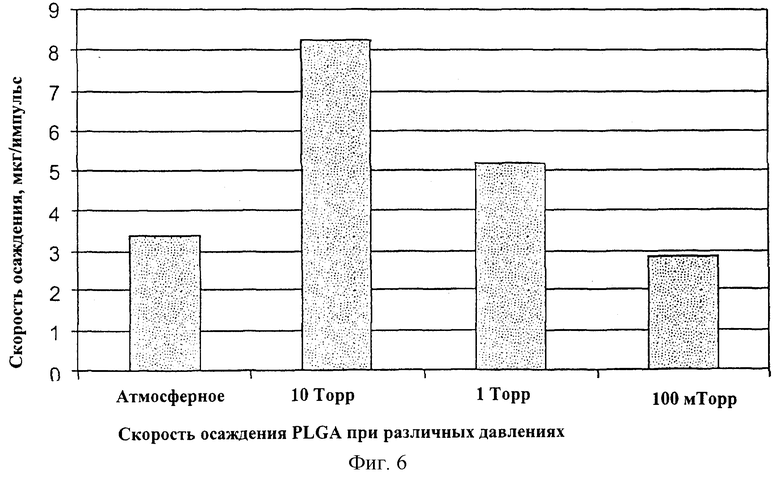
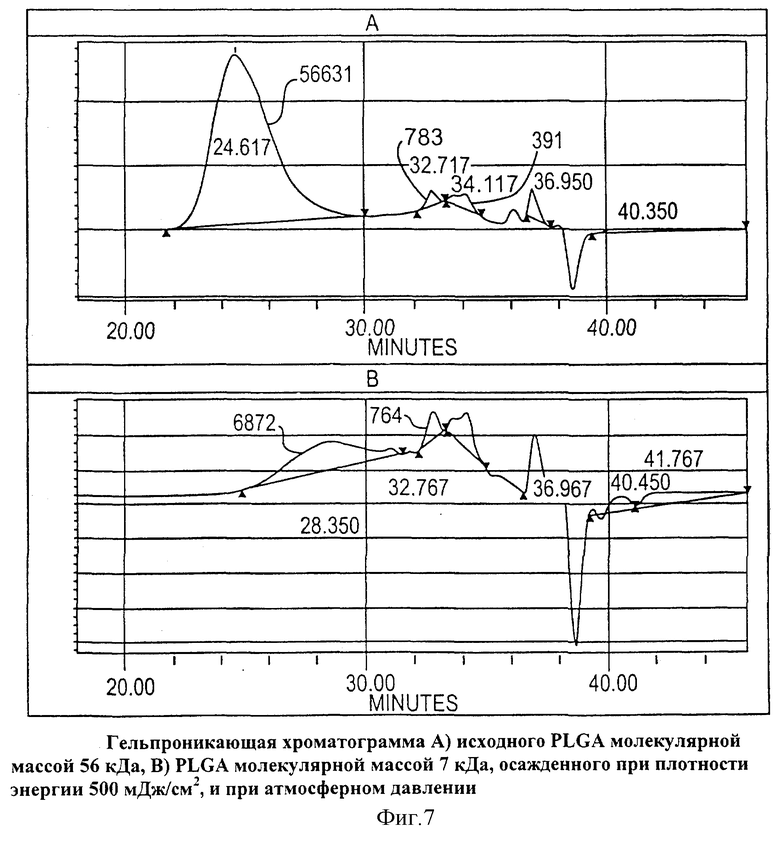
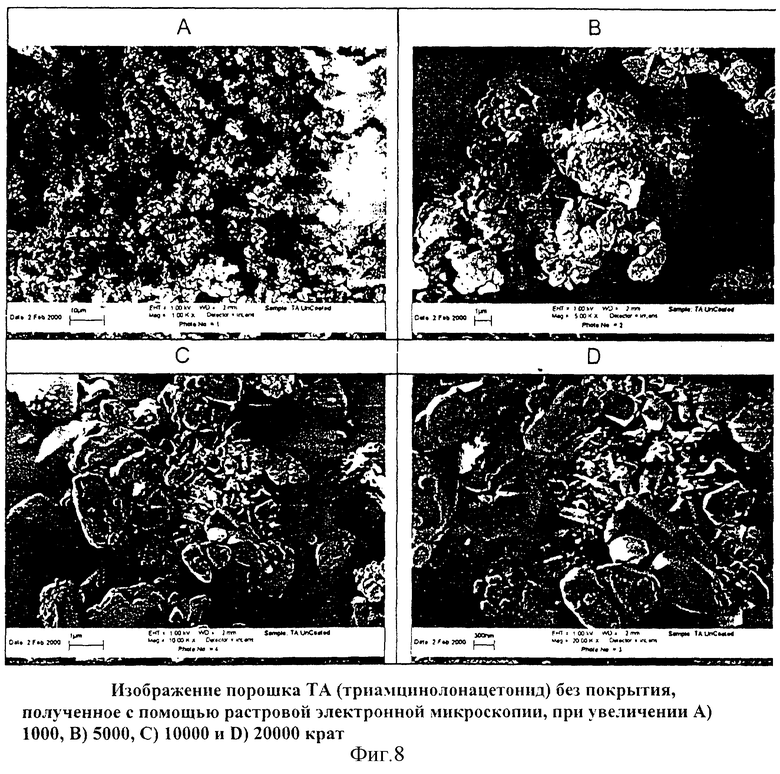
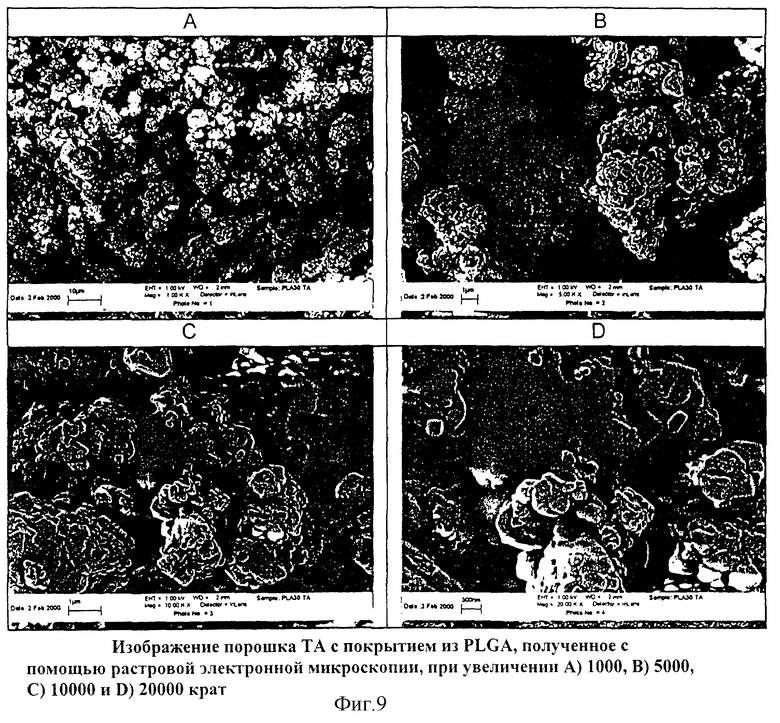
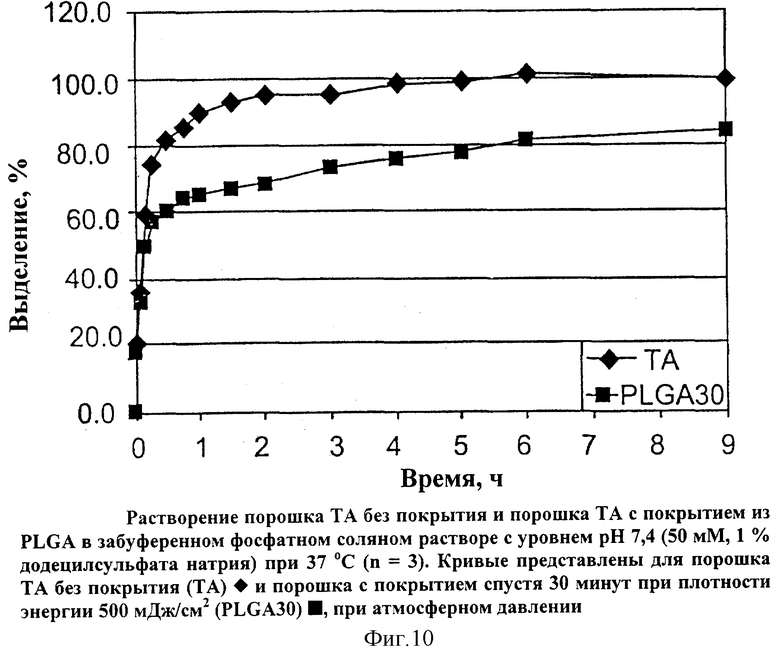
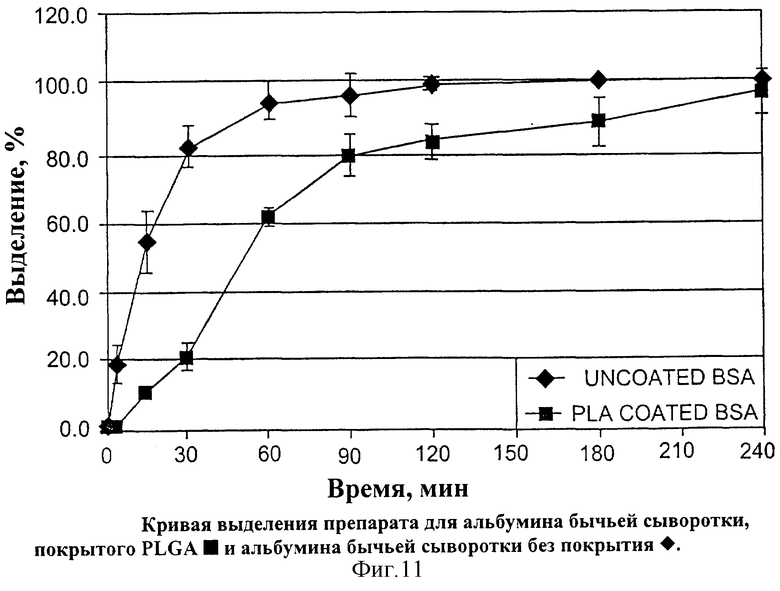
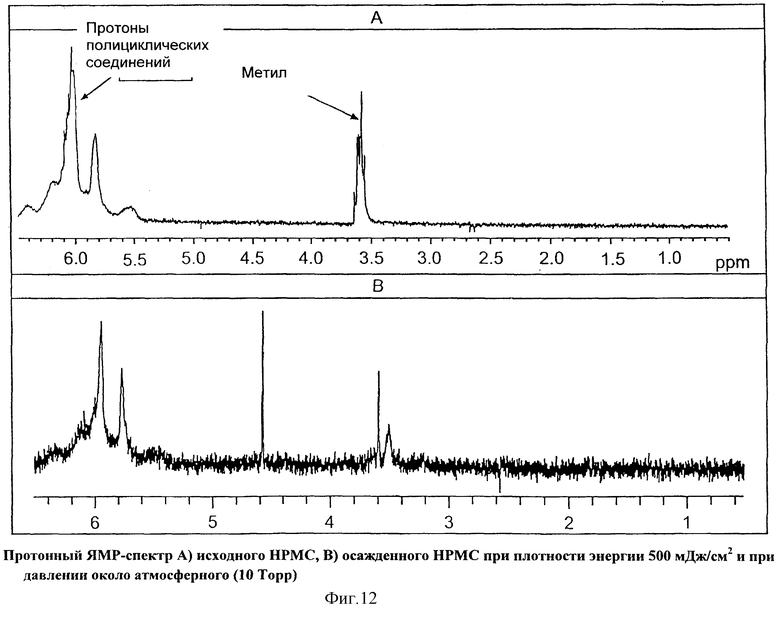
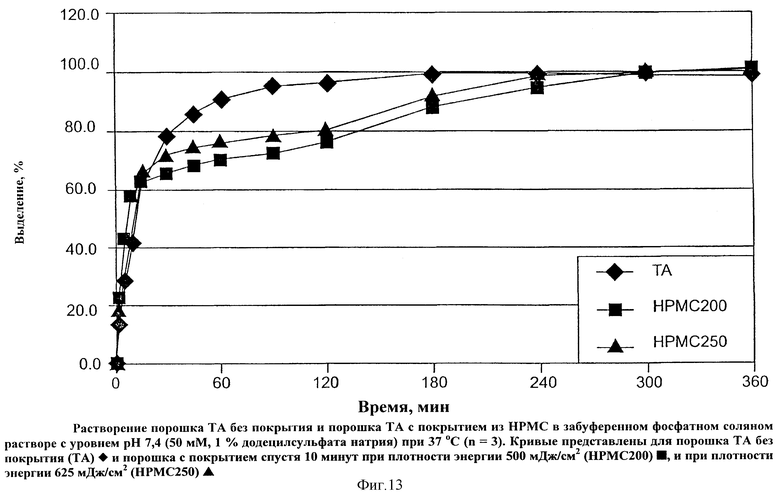
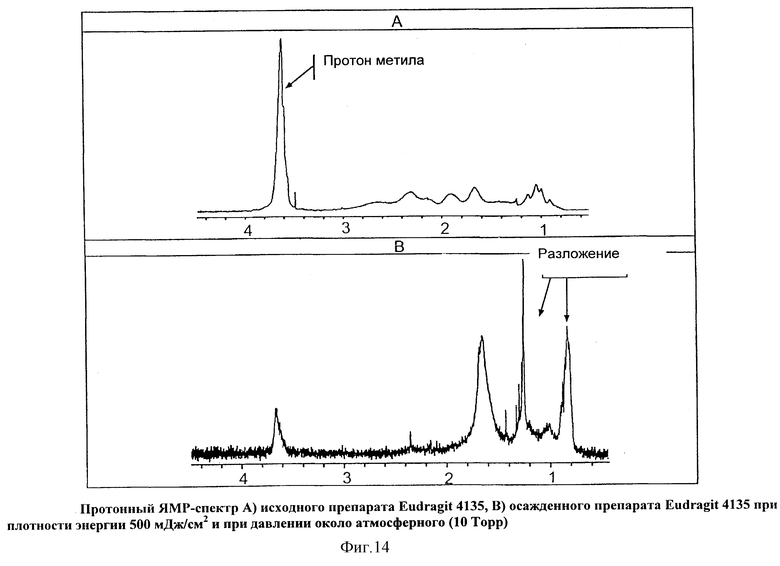
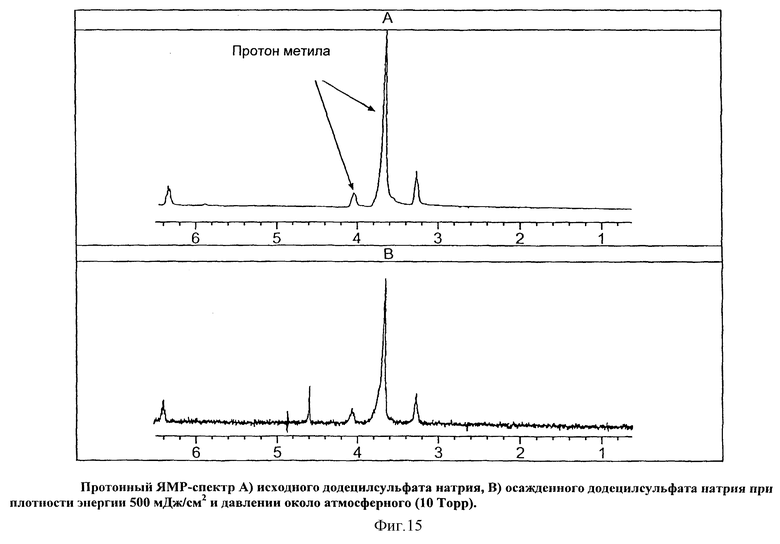
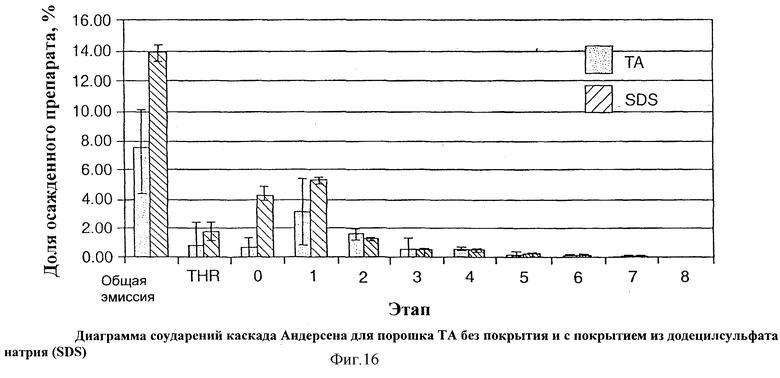
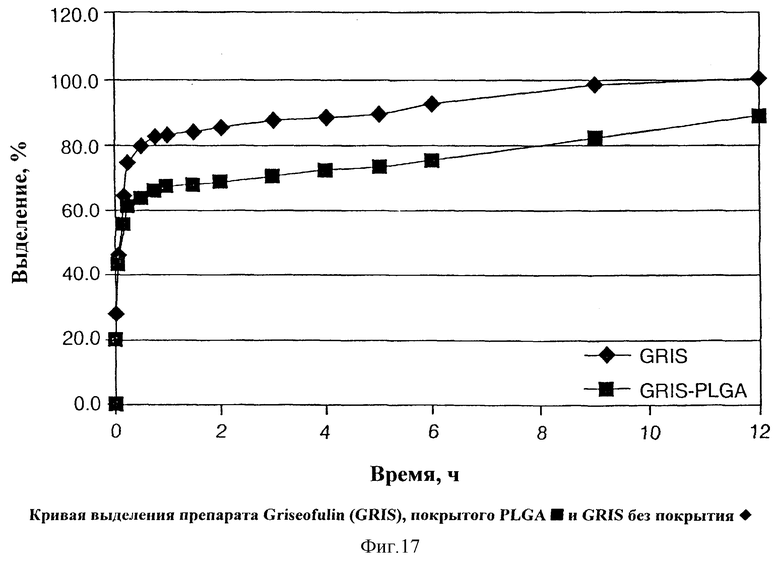
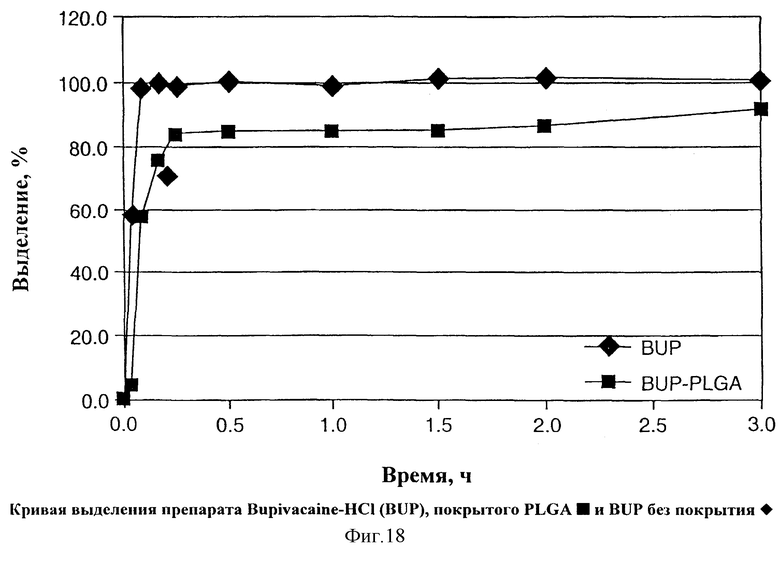
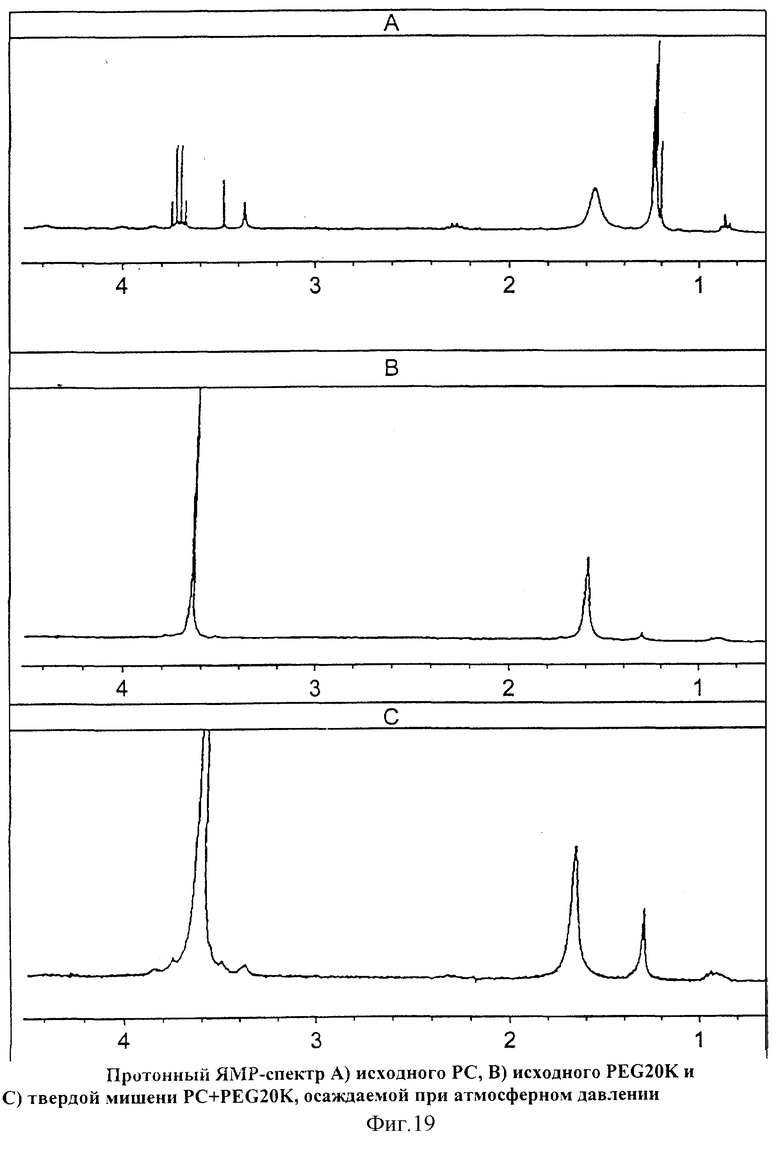
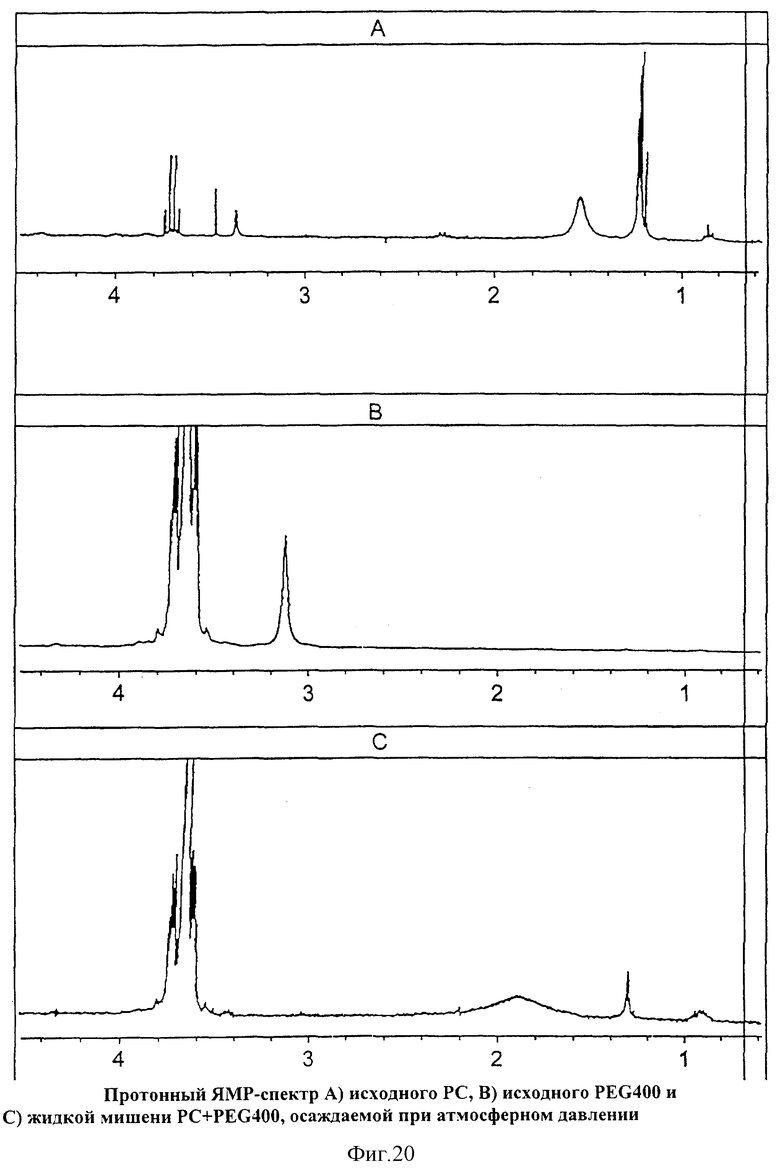
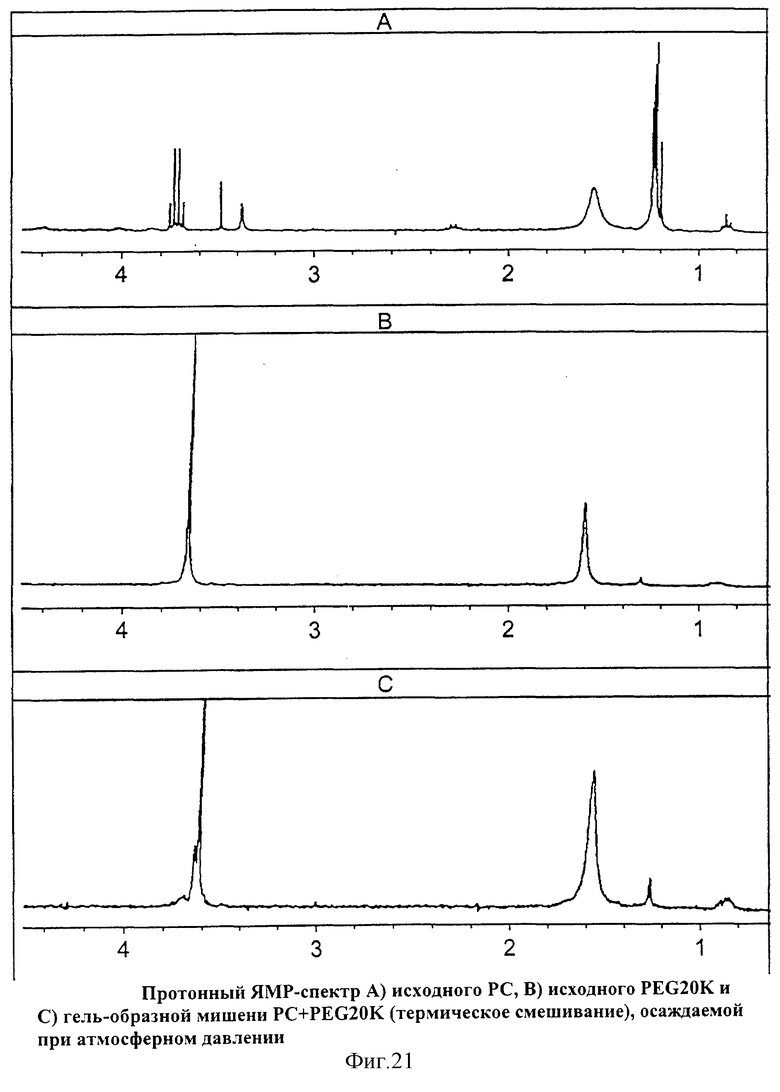
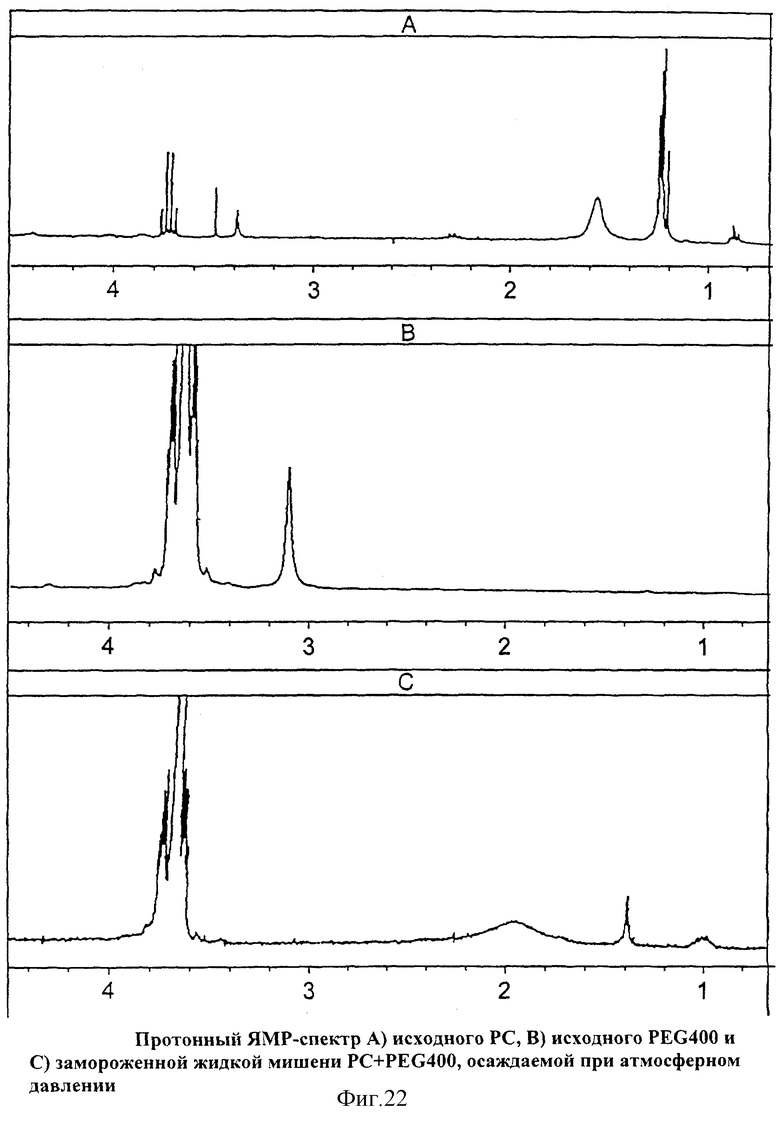
Изобретение относится к химико-фармацевтической промышленности и касается способа нанесения покрытий на материалы сердцевины частиц, включающего подачу материалов мишени и материалов сердцевины, абляцию материалов мишени с образованием материалов уносимых частиц мишени, нанесения покрытий на материалы сердцевины из материалов уносимых частиц мишени, при этом его осуществление происходит при давлении приблизительно 10 Торр или выше. Способ нанесения покрытий толщиной от одного до многих нанометров на частицы при атмосферном давлении и использование при этом псевдоожиженного состояния частиц, созданного с помощью пневматического псевдоожижения. Изобретение улучшает фармакокинетические характеристики лекарственных препаратов, в части свойства текучести на этапе производства и стабильность свойств препарата, например, при хранении. 4 н. и 18 з.п. ф-лы, 22 ил.
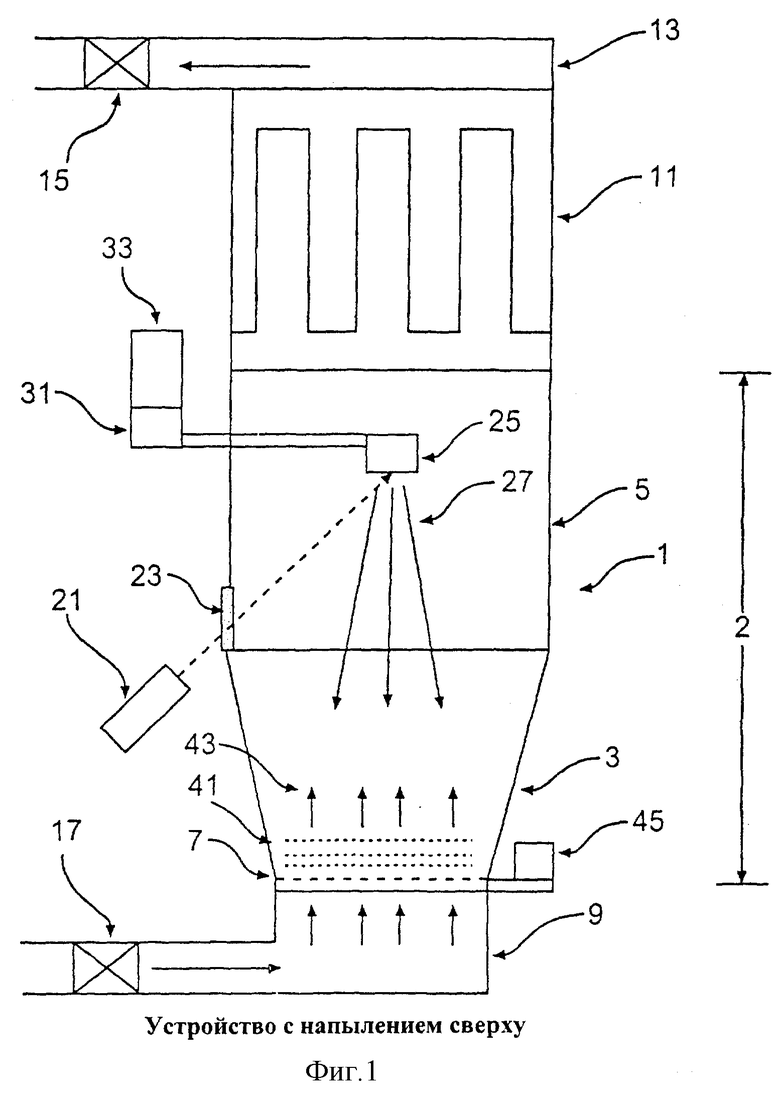
| ТВЕРДАЯ ФАРМАЦЕВТИЧЕСКАЯ ФОРМА ПРОГРАММИРУЕМОГО ВЫДЕЛЕНИЯ ДЛЯ ПЕРОРАЛЬНОГО ВВЕДЕНИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1991 |
|
RU2012330C1 |
| RU 20011377 С1, 30.04.1994 | |||
| DE 4239244 А, 26.05.1994 | |||
| Пожарный двухцилиндровый насос | 0 |
|
SU90A1 |
Авторы
Даты
2005-04-27—Публикация
2000-06-06—Подача